Журнал «Медицина неотложных состояний» 3 (58) 2014
Вернуться к номеру
Пути повышения эффективности интенсивной терапии у пациентов с острым панкреатитом
Авторы: Кравец О.В. - ГУ «Днепропетровская медицинская академия МЗ Украины»
Рубрики: Медицина неотложных состояний, Хирургия
Разделы: Клинические исследования
Версия для печати
С целью оценки эффективности препарата этилметилгидроксипиридина сукцинат в объеме интенсивной терапии острого панкреатита обследовано 12 больных. В зависимости от вида терапии больные были разделены на 2 группы. В основной группе применялся этилметилгидроксипиридина сукцинат на протяжении 7 суток лечения. Больные были обследованы клинически, инструментально и лабораторно. В исследовании доказано, что использование этилметилгидроксипиридина сукцината в составе интенсивной терапии острого панкреатита обеспечивает сокращение длительности панкреатогенной токсемии на 2 суток, эффективную регидратацию в течение первых 2 суток терапии; быстро стабилизирует цитолиз и ограничивает деструктивные процессы поджелудочной железы, что уменьшает проявления органной дисфункции.
З метою оцінки ефективності препарату етилметилгідроксипіридину сукцинат в об’ємі інтенсивної терапії гострого панкреатиту було обстежено 12 хворих. Залежно від складу терапії хворі були розділені на 2 групи. В основній групі було застосовано етилметилгідроксипіридину сукцинат упродовж 7 діб лікування. Хворі були обстежені клінічно, інструментально та лабораторно. У дослідженні було доведено, що використання етилметилгідроксипіридину сукцинату у складі інтенсивної терапії гострого панкреатиту забезпечує скорочення тривалості панкреатогенної токсемії на 2 доби, ефективну регідратацію у перші 2 доби терапії; швидко стабілізує цитоліз і обмежує деструктивні процеси у підшлунковій залозі, що зменшує прояви органної дисфункції.
To assess the effectiveness of ethylmethylhydroxypyridine succinate preparation in the amount of intensive care for acute pancreatitis we examined 12 patients. Depending on the type of therapy, the patients were divided into 2 groups. In the study group we used ethylmethylhydroxypyridine succinate for 7 days of treatment. The patients were examined clinically, instrumentally and laboratory. The study proved that the use of ethylmethylhydroxypyridine succinate as a part of intensive care for acute pancreatitis reduces the duration of pancreatogenic toxemia by 2 days, provides effective rehydration during the first 2 days of therapy; quickly stabilizes cytolysis and limits the destructive processes of the pancreas that reduces the appearance of organ dysfunction.
острый панкреатит, интенсивная терапия, профилактика синдрома полиорганной недостаточности, этилметилгидроксипиридина сукцинат.
гострий панкреатит, інтенсивна терапія, профілактика синдрому поліорганної недостатності, етилметилгідроксипіридину сукцинат.
acute pancreatitis, intensive care, prevention of multiple organ dysfunction syndrome, ethylmethylhydroxypyridine succinate.
Статья опубликована на с. 136-140
Введение
Острый панкреатит (ОП) — острое хирургическое заболевание, в основе которого лежит первичный асептический некроз ткани поджелудочной железы, вызывающий при деструктивных формах тяжелый эндотоксикоз, местную и системную ответную воспалительную реакцию, полиорганную дисфункцию с возможным развитием инфицированного панкреонекроза. В Украине заболеваемость ОП составляет 10,2 на 100 000 населения, а уровень летальности достигает 11,2 % [1, 5, 7]. Занимая второе место в структуре ургентной хирургической патологии, ОП сопровождается увеличением тяжелых и осложненных форм с исходом в панкреонекроз. При этом уровень инвалидизации и летальности составляет 80 и 90 % соответственно, не имея тенденции к принципиальному снижению [1, 3, 5, 7]. Это объясняется развитием синдрома системного воспалительного ответа (ССВО), переходящего в синдром полиорганной недостаточности (СПОН), как при стерильном, так и при инфицированном некрозе. ССВО и/или органная недостаточность могут возникать в ранней фазе ОП, с последующими локальными осложнениями в поздней фазе ОП [6, 8–10, 12]. Органная недостаточность является наиболее важным критерием тяжести ОП. СПОН, сохраняющийся более 48 часов, ассоциирован со смертностью свыше 50 %, а его разрешение значительно снижает уровень летальности [11]. Поэтому актуальным является раннее и интенсивное вмешательство с целью предотвращения перехода дисфункции в органную недостаточность [2, 4]. В исследованиях полионного раствора сукцината у больных с некротической формой острого панкреатита была описана возможность коррекции «метаболической гипоксии», что позволило нам считать это способом повышения эффективности проводимой терапии ОП [2, 4].
Целью исследования являлась оценка эффективности применения этилметилгидроксипиридина сукцината в комплексе интенсивной терапии (ИТ) ОП.
Материалы и методы
Обследовано 12 больных с острым панкреатитом. Среди обследованных было 8 мужчин и 4 женщины. Средний возраст составлял 42,6 ± 2,3 года. Предварительный диагноз острого панкреатита был установлен на основании анамнестических и клинических данных, верифицирован лабораторными (повышение амилазы сыворотки крови в 2–3 раза выше нормы) и инструментальными методами (ультразвуковое исследование, компьютерная томография (КТ)) в течение 48 часов от момента поступления. Степень тяжести острого панкреатита оценивалась по шкале АPACHE II с использованием критериев степени тяжести (Атланта, 1992) [11]. Выраженность ССВО определялась по уровню С-реактивного белка в сыворотке крови [11]. Оценка органной дисфункции и эффективности терапии осуществлялась на основании шкалы MODS [11].
Максимальная стандартизация ИТ проводилась согласно «Удосконаленим алгоритмам діагностики та лікування гострого панкреатиту» (Киев, 2012) [5]. В зависимости от проводимой ИТ больные были разделены на 2 группы. Группы были репрезентативны по полу и сопутствующей патологии. В 1-ю группу (основную, n = 7) вошли пациенты, получавшие на фоне стандартной ИТ этилметилгидроксипиридина сукцинат с момента госпитализации и на протяжении 7 суток. В течение первых 5 суток этилметилгидроксипиридина сукцинат вводили в дозе 200 мг внутривенно капельно (в 200 мл изотонического раствора натрия хлорида) 3 раза в сутки, последующие 2 суток препарат применяли внутримышечно. Пациентам 2-й группы (контрольной, n = 5) проводилась стандартная интенсивная терапия ОП.
Больные были обследованы на момент госпитализации, к концу 1, 3, 4, 5-х суток ИТ. Клинически мы определяли частоту сердечных сокращений (ЧСС), уровень артериального давления (АД), сатурацию кислорода, частоту дыхания (ЧД). Болевой синдром оценивался по данным визуальной аналоговой шкалы (ВАШ). В объеме неинвазивных инструментальных методик мы осуществляли электрокардиограмму, анализировали данные рентгенографии органов грудной клетки, КТ и ультрасонографии брюшной полости. Величина внутрибрюшного давления (ВБД) определялась стандартной методикой. Лабораторно мы изучали данные общего клинического анализа крови и мочи, глюкозы крови, биохимического анализа крови, показателей коагулограммы, электролитов и газового состава смешанной венозной крови, амилазы крови и диастазы мочи.
Исследование проводилось в соответствии с требованиями этического комитета. Статистическую обработку полученных результатов осуществлялась с помощью пакета программ Microsoft Excel 2007. Статистически достоверными считали значения p < 0,05. Критериями исключения из исследования являлись: повышенная индивидуальная чувствительность к препарату, острая печеночная или почечная недостаточность, панкреонекроз, шок.
Результаты исследования и их обсуждение
Диагноз ОП был установлен у всех пациентов в течение 48 часов от момента поступления. Наиболее частыми причинами острого панкреатита являлись прием алкоголя и погрешность в питании (70 %), заболевания внепеченочных желчных путей (30 %). При поступлении больные жаловались на выраженный болевой синдром. У пациентов 1-й группы показатель ВАШ составлял 9,4 ± 0,4 балла, во 2-й группе — 10,0 ± 0,5 балла. Диспептические явления (тошнота, нарушение стула) и/или вздутие живота наблюдались у 90 % пациентов обеих групп. Умеренное повышение ВБД до 13,1 ± 0,5 см рт.ст. отмечалось у пациентов 1-й группы, до 15,0 ± 0,6 см рт.ст. — 2-й группы исследования.
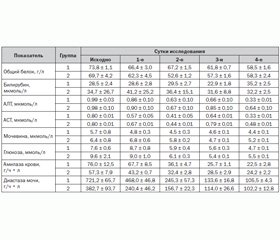
Исходная степень тяжести ОП в обеих группах наблюдения проявлялась умеренным тахипноэ (ЧД — 21,2 ± 1,1 в 1 мин), тахикардией (ЧСС в 1-й группе 91,5 ± 2,4 уд/мин, во 2-й группе — 102,7 ± 11,5 уд/мин (р > 0,05)) и относительной гипердинамией (систолическое АД 140,2 ± 5,6 мм рт.ст. в 1-й группе и 143,3 ± 7,6 мм рт.ст. — во 2-й группе (р > 0,05)). Диагноз ОП и клинические признаки его тяжести подтверждались повышенным уровнем амилазы крови и диастазы мочи (табл. 1).
Так, у пациентов 1-й группы уровень амилазы крови составлял 76,0 ± 12,5 г/ч • л, диастазы мочи — 721,2 ± 65,7 г/ч • л, во 2-й группе больных — 57,3 ± 7,9 г/ч • л и 382,7 ± 93,7 г/ч • л соответственно.
ОП сопровождался признаками выраженной дегидратации у больных обеих групп наблюдения. Так, при поступлении нами отмечалось повышение уровня Na+ у пациентов как 1-й группы (до 148,5 ± 0,7 ммоль/л), так и 2-й группы (до 151,3 ± 0,4 ммоль/л). Показатели К+ и Cl– плазмы крови достоверно не отличались от значений нормы. При этом в обеих группах нами отмечался компенсированный метаболический ацидоз. Так, у пациентов 1-й группы уровень pH составлял 7,33 ± 0,01, ВЕ — –4,8 ± 0,3. Во 2-й группе больных уровень рН соответствовал 7,33 ± 0,01, ВЕ — –5,2 ± 0,3. У всех пациентов наблюдалось снижение уровня НCO3–. Так, значения HCO3– у больных 1-й группы соответствовали 18,2 ± 0,6 мэкв/л, 2-й группы — 16,5 ± 0,3 мэкв/л.
При поступлении у больных показатели общего белка не отличались от физиологической нормы (табл. 1). Значения билирубина крови превышали норму, однако различия были недостоверными внутри каждой группы (р = 0,154). Рост креатинина сыворотки крови отмечался как в 1-й группе больных (139,3 ± 17,2 мкмоль/л), так и во 2-й группе (140,0 ± 24,3 мкмоль/л) (р = 0,981). Клинические и биохимические признаки органной дисфункции при поступлении подтверждались количеством баллов по шкале MODS — 3,0 ± 0,1 балла в 1-й группе и 2,9 ± 0,2 балла — во 2-й группе (р > 0,05). Это объяснялось наличием ССВО (определялся лейкоцитоз: 12,4 ± 0,5 • 109/л в 1-й группе, 9,0 ± 0,3 • 109/л — во 2-й группе; нейтрофилез: 13,8 ± 5,9 % в 1-й группе, 8,7 ± 1,7 % — во 2-й группе; лимфопения: 6,3 ± 1,2 % в 1-й группе, 11,1 ± 2,3 % — во 2-й группе), несмотря на проведение стартовой антибактериальной терапии. Это характеризовало течение ОП как тяжелое и подтверждалось балльной оценкой по шкале APACHE II — 7,6 ± 0,9 балла в 1-й группе, 7,5 ± 0,3 балла — во 2-й группе.
Проведение ИТ уменьшало выраженность болевого синдрома уже к концу первых суток в обеих группах наблюдения (р = 0,001 по отношению к исходному уровню), показатель по ВАШ составлял 3,7 ± 0,5 балла в 1-й группе, 6,7 ± 0,4 балла — во 2-й группе (межгрупповые отличия достоверны (р = 0,024)). Достоверное снижение выраженности болевого синдрома по ВАШ до 1,7 ± 0,2 балла в 1-й группе и 2,7 ± 0,4 балла — во 2-й группе (межгрупповые отличия (р = 0,094)) отмечалось на 3-и сутки проводимой терапии, при отсутствии жалоб на боль у пациентов на 5-е сутки после госпитализации. Это совпадало с купированием диспептических расстройств и вздутия живота на 3-и сутки интенсивной терапии ОП и могло свидетельствовать об эффективности интенсивной терапии ОП. При этом со 2-х суток наблюдения значения ВБД у пациентов 1-й группы составляли 10,5 ± 0,6 см рт.ст. (р = 0,009 по отношению к исходному уровню) и достоверно (межгрупповые отличия р = 0,021) отличались от показателей внутрибрюшной гипертензии 1-й степени во 2-й группе (ВБД 14,7 ± 1,1 см рт.ст.). Показатели ВБД у пациентов 2-й группы снижались до 10,0 ± 0,1 см рт.ст. только к 4-м суткам интенсивной терапии (р = 0,004 по отношению к исходному уровню).
Таким образом, проведение интенсивной терапии ОП ликвидировало болевой и диспептический синдромы в обеих группах пациентов. Однако использование этилметилгидроксипиридина сукцината в составе ИТ позволяло достичь безболевого периода и нормализации внутрибрюшного давления на 2 суток быстрее.
Уровень секреторной активности поджелудочной железы мы оценивали по динамике амилолитической активности. Поскольку при поступлении уровень амилазы крови и диастазы мочи у пациентов 1-й группы был в 1,5 раза выше по сравнению с контрольной, то анализ полученных данных мы проводили, оценивая процентные соотношения с исходными (табл. 1). Так, в 1-е сутки уровень амилазы снижался на 12 и 25 % соответственно группам, а на 2-е сутки проводимой ИТ — на 52,5 и 45,6 % от исходного уровня. Через 3 дня лечения уровень амилазы крови у пациентов 1-й и 2-й группы достигал значений нормы — 25,7 ± 1,1 г/ч • л и 28,5 ± 2,9 г/ч • л соответственно (межгрупповые отличия р = 0,345). Уровень диастазы мочи в течение первых суток также понижался на 35,1 и 37,2 % соответственно группам, на 2-е сутки — на 66 и 59,2 % от исходного уровня. И хотя на 3-и сутки ИТ уровень диастазы мочи соответствовал 133,6 ± 16,8 мккат/л в 1-й группе и 114,0 ± 26,6 мккат/л во 2-й группе, однако динамика его значений по отношению к исходным (р = 0,026 и р = 0,041 соответственно) была более выраженной у пациентов основной группы. После 4 суток проведения ИТ показатели диастазы мочи достоверно не отличались в группах (р = 0,992) и составляли 105,5 ± 4,3 г/ч · л и 102,2 ± 12,8 г/ч • л соответственно. Полученные данные позволили предположить, что применение этилметилгидроксипиридина сукцината в комплексе интенсивной терапии позволяет достаточно эффективно воздействовать на панкреатогенную токсемию у больных острым панкреатитом.
Анализ уровня глюкозы крови выявил его снижение в течение первых суток интенсивной терапии до 5,9 ± 0,4 ммоль/л в 1-й группе (р = 0,241), до 6,1 ± 0,3 ммоль/л — во 2-й группе (р = 0,127) (межгрупповые отличия недостоверны (р = 0,908)) (табл. 1). С 3-х суток значения глюкозы крови соответствовали верхней границе нормы в обеих группах и составляли 5,6 ± 0,3 ммоль/л и 5,4 ± 0,1 ммоль/л соответственно. Дальнейшее наблюдение динамики глюкозы показало более стойкое снижение уровня сахара крови (в пределах 4,4 ± 0,2 ммоль/л на 6-е сутки) в основной группе, что опосредованно может указывать на корригирующее влияние этилметилгидроксипиридина сукцината на углеводный обмен при ОП.
Течение ОП сопровождалось изменениями белкового обмена в обеих группах (табл. 1). Анализ выявил тенденцию к снижению уровня общего белка уже с первых суток заболевания. Значения общего белка составляли 66,4 ± 3,0 г/л (р = 0,183) в 1-й группе и 62,3 ± 4,5 г/л (р = 0,263) — во 2-й группе. В контрольной группе это усугублялось ко 2-м суткам ИТ, когда уровень общего белка составлял 52,6 ± 1,2 г/л, межгрупповые отличия достоверны (р = 0,001). У пациентов основной группы незначительная гипопротеинемия отмечалась с 3-х суток и нарастала к 4-м суткам ИТ, когда значения общего белка составляли 58,5 ± 1,6 г/л (р = 0,004 к исходному уровню). Таким образом, в сравнении со 2-й группой у больных 1-й группы нарушения белкового обмена носили отсроченный и менее выраженный характер, что косвенно указывает на органопротективное действие этилметилгидроксипиридина сукцината при ОП.
Уровень билирубина крови у больных 1-й и 2-й группы превышал верхнюю границу нормы в течение 5 суток ИТ (табл. 1) и характеризовался недостоверными значениями, что объяснялось различной этиологией острого панкреатита.
При оценке влияния ИТ на степень цитолиза нами отмечалось достоверное отличие в группах. Так, повышение уровня трансаминаз крови с первых суток наблюдалось на протяжении всего периода у всех исследуемых пациентов. В 1-е сутки значения АЛТ составляли 0,99 ± 0,03 мкмоль/л в 1-й и 0,98 ± 0,10 мкмоль/л — во 2-й группе (табл. 1). Уровень АСТ не отличался в обеих группах и соответствовал 0,80 ± 0,01 мкмоль/л. После 4 суток лечения у больных определялась тенденция к нормализации среднего уровня АСТ до 0,33 ± 0,01 мкмоль/л и 0,48 ± 0,01 мкмоль/л соответственно группам (межгрупповые отличия недостоверны, р = 0,765) и АЛТ до 0,33 ± 0,01 мкмоль/л и 0,64 ± 0,10 мкмоль/л соответственно группам (межгрупповые отличия недостоверны, р = 0,765). Однако явления цитолиза у больных 1-й группы были менее выражены в сравнении со 2-й группой, что может свидетельствовать об органопротективном действии этилметилгидроксипиридина сукцината при лечении ОП.
Анализ динамики уровня фибриногена показал, что, несмотря на проведение регидратации, реологической терапии и профилактики тромбоэмболических осложнений низкомолекулярными гепаринами с момента госпитализации, значения фибриногена увеличивались на 3-и сутки заболевания. Так, у пациентов 1-й группы уровень фибриногена составлял 5,3 ± 0,4 г/л, 2-й группы — 4,5 ± 0,9 г/л, что свидетельствовало о сохранении признаков ССВО в обеих группах больных и указывало на необходимость проведения профилактики тромбоэмболических осложнений до момента регресса ССВО.
При этом превышающие норму в первые сутки показатели С-реактивного белка (45,1 ± 13,9 мг/л в 1-й группе, 46,0 ± 15,8 мг/л — во 2-й группе) возвращались к нормальным на 2-е сутки ИТ (р = 0,508). Во 2-й группе больных в эти сроки наблюдалось недостоверное повышение уровня изучаемого показателя (р = 0,182). Достоверное снижение уровня С-реактивного белка до 24,7 ± 7,4 мг/л у пациентов 1-й группы и до 26,4 ± 17,4 мг/л — 2-й группы определялось на 4-е сутки проведения ИТ.
Проведение регидратации позволяло откорригировать исходную гипернатриемию у больных с ОП. С первых суток лечения нами отмечалась тенденция к нормализации Na+ плазмы до 142,8 ± 1,3 ммоль/л у пациентов 1-й группы и 146,2 ± 0,8 ммоль/л — 2-й группы, при последующей нормализации значений уже на 2-е сутки ИТ. Уровень Cl– плазмы пациентов 1-й группы сохранялся в пределах нормы весь период наблюдения и составлял 100,2 ± 2,2 ммоль/л. Во 2-й группе больных снижение уровня Cl– плазмы до 94,0 ± 1,7 ммоль/л в первые сутки сохранялось до 3 суток наблюдения. Анализ динамики уровня К+ сыворотки крови на фоне интенсивной терапии показал сохранение значений нормы на протяжении всего периода наблюдения. При этом показатели кислотно-щелочного состояния соответствовали нормальным со 2-х суток ИТ и достоверно не изменялись на протяжении дальнейшего периода, что могло свидетельствовало об эффективности проводимой инфузионной терапии. Это подтверждалось достижением нормоосмолярности плазмы крови на 3-и сутки наблюдения в обеих группах пациентов.
Проведение ИТ больным с тяжелым ОП позволяло снизить активность проявлений ССВО, что подтверждалось снижением в 2 раза количества баллов согласно шкале MODS уже на 2-е сутки лечения. Так, в 1-й группе больных количество баллов по MODS составляло 1,00 ± 0,05, во 2-й группе — 1,7 ± 0,5 балла. Это коррелировало со снижением степени тяжести согласно APACHE II при отсутствии признаков ССВО на 5-е сутки лечения.
Таким образом, применение этилметилгидроксипиридина сукцината в объеме интенсивной терапии ОП позволяло на 2 суток быстрее достигнуть безболевого периода и снизить признаки интраабдоминальной гипертензии в сравнении со стандартной ИТ, эффективно воздействовать на панкреатогенную токсемию у больных острым панкреатитом, корригировать нарушения углеводного обмена, оказать органопротективные и цитостатические эффекты, что уменьшает проявления ССВО и/или СПОН.
Выводы
1. Оценка выраженности болевого синдрома, уровня амилазы крови, визуализация поджелудочной железы методом сонографии или компьютерной томографии позволяет быстро (в течение 48 часов) и точно верифицировать острый панкреатит.
2. Стратификация степени тяжести острого панкреатита на основании клинических проявлений, уровня С-реактивного белка, признаков СПОН и балльной оценки по шкале APACHE II улучшает результаты лечения при остром панкреатите за счет своевременной и эффективной реализации современных протоколов интенсивной терапии.
3. Манифестация острого панкреатита тяжелой степени характеризуется выраженным болевым синдромом и степенью дегидратации на фоне компенсированного метаболического ацидоза, клиническими и лабораторными признаками органной дисфункции в сочетании с умеренной интраабдоминальной гипертензией.
4. Применение стандартной ИТ острого панкреатита эффективно корригирует углеводный обмен; снижает уровень панкреатогенной токсемии и оказывает органопротекторный эффект на 4-е сутки лечения; купирует болевой синдром, снижает активность проявлений ССВО и тяжести СПОН на 5-е сутки терапии.
5. Использование этилметилгидроксипиридина сукцината в составе ИТ острого панкреатита обеспечивает сокращение длительности панкреатогенной токсемии на 2 суток, эффективную регидратацию в течение первых 2 суток терапии; быстро стабилизирует цитолиз, что ограничивает деструктивные процессы поджелудочной железы и уменьшает проявления органной дисфункции.
1. Десятилетний опыт профилактики и лечения синдрома полиорганной недостаточности при тяжелом остром панкреатите: анализ 223 случаев / Дацюк А.И., Шлапак М.П., Титаренко Н.В., Дацюк Л.В. // Вестник интенсивной терапии. — 2013. — № 2. — С. 19-26.
2. Комплексный эффект полиионного раствора сукцината при его включении в состав интенсивной терапии у больных с острым некротическим панкреатитом / Никонов В.В., Хижняк А.А., Курсов С.В., Михневич К.Г., Битчук Н.Д., Скороплет С.Н., Иевлев В.И., Белашко С.А., Митясов А.Н., Пивненко М.А. // Медицина неотложных состояний. — 2012. — № 5(44). — С. 60-65.
3. Иоффе И.В. Сравнительная оценка эффективности применения ингибиторов протеаз, цитостатиков и октрестатина в профилактике острого послеоперационного панкреатита у больных, перенесших операцию на желудке и двенадцатиперстной кишке // Український медичний альманах. — 2006. — Т. 9, № 7. — С. 99-106.
4. Малыгина Н.В. Применение мексидола в комбинированном лечении острого панкреатита / Н.В. Малыгина // Хирургия. — 2006. — № 10. — С. 42-50.
5. Удосконалені алгоритми діагностики та лікування гострого панкреатиту: методичні рекомендації / Під ред. П.Д. Фоміна, Я.С. Березницького. — К., 2012. — 80 с.
6. Ермолов А.С., Иванов П.А., Благовестнов Д.А. и др. Диагностика и лечение острого панкреатита. — М.: ВИДР, 2013. — 382 с.
7. Савельев В.С., Филимонов М.И., Бурневич С.З. Острый панкреатит // Национальное руководство по хирургии. — 2009. — Т. 2. — С. 196-229.
8. Савельев В.С., Филимонов М.И., Бурневич С.З. Панкреонекрозы. — М.: МИА, 2008. — 259 с.
9. Савельев В.С., Гельфанд Б.Р., Филимонов М.И. и др. Деструктивный панкреатит. Доказательные методы диагностики и лечения. Методические рекомендации. — М., 2008.
10. Дибиров М.Д., Юанов А.А. Панкреонекроз. Протокол диагностики и лечения. Учебно-методическое пособие. — М., 2012. — 366 с.
11. American College of Gastroenterology Guideline: Management of Acute Pancreatitis // Am. J. Gastroenterol. — 2013. — Аdvance online publication, 30 July 2013; doi: 10.1038/ajg.2013.218.
12. Кондратенко П.Г. Острый панкреатит: концептуальные вопросы диагностики и тактики лечения / П.Г. Кондратенко, М.Г. Конькова // Украинский журнал хирургии. — 2009. — № 1. — С. 68-76.

/138/138.jpg)