Журнал «Медицина неотложных состояний» 5 (60) 2014
Вернуться к номеру
Фазові зсуви електрорушійної сили серця у хворих на гострий інфаркт міокарда
Авторы: Бєлая І.Є. - Державний заклад «Луганський державний медичний університет»
Рубрики: Медицина неотложных состояний
Разделы: Клинические исследования
Версия для печати
У роботі виявлено особливості електрорушійної сили серця у хворих на гострий інфаркт міокарда із зубцем Q задньобічної локалізації, які векторкардіографічно характеризуються зсувом петель QRS уперед, угору та вправо з розташуванням у другій проекції в IV квадранті їх початкової частини та праворуч вертикальної координати — основної частини, зменшенням площі петель QRS, появою вектора ушкодження ST, спрямованого униз і вліво, залученням у патологічний процес відділів серця, які локалізуються поза межами ішемізованого міокарда, що оточують зону некрозу: передньої стінки лівого шлуночка, верхівки, базальних відділів обох шлуночків та передсердь. При цьому порушення провідності та процесів реполяризації спостерігаються в усьому міокарді, але різного ступеня вираженості. Ехокардіографічне дослідження дозволило виявити збільшення порожнини лівих камер серця за зниженням скорочувальної функції лівого шлуночка, його податливості та збільшенням тиску наповнення.
В работе выявлены особенности электродвижущей силы сердца у больных с острым инфарктом миокарда с зубцом Q заднебоковой локализации, которые векторкардиографически характеризуются сдвигом петель QRS вперед, вверх и вправо с расположением во второй проекции в IV квадранте их начальной части и справа от вертикальной координаты — основной части, уменьшением площади петель QRS, появлением вектора повреждения ST, направленного вниз и влево, вовлечением в патологический процесс отделов сердца, расположенных за границей ишемизированного миокарда, окружающего зону некроза: передней стенки левого желудочка, верхушки, базальных отделов обоих желудочков и предсердий. При этом нарушения проводимости и процессов реполяризации наблюдаются во всем миокарде, но характеризуются разной степенью выраженности. Эхокардиографическое исследование позволило выявить увеличение полости левых камер сердца при снижении сократительной функции левого желудочка, его податливости и увеличении давления наполнения.
In this paper, the peculiarities of the electromotive force of the heart were revealed in patients with acute myocardial infarction with Q wave of posterolateral localization, which are characterized vectorcardiographically by a shift of QRS loops forward, up and to the right with the location of the second projection in IV quadrant of the initial part and the right of the vertical coordinate — the main part, decreasing the area of QRS loops, the appearance of ST damage vector, directed down and to the left, involvement in the pathological process of compartments of heart, located outside ischemic myocardium, surrounding the zone of necrosis: the anterior wall of the left ventricle, apex, basal parts of both ventricles the atria. In this, disorders of conduction and repolarization are being observed throughout the myocardium, but are characterized by varying degrees of severity. Echocardiography revealed an increase in the cavity of the left chambers of the heart with a decrease in left ventricular contractility, its pliability and increasing filling pressures.
гострий період інфаркту міокарда, векторкардіографія, електрокардіографія, ехокардіографія.
острый период инфаркта миокарда, векторкардиография, электрокардиография, эхокардиография.
acute period of yocardial infarction, vectorcardiography, electrocardiography, echocardiography.
Статья опубликована на с. 107-112
Значне поширення кардіоваскулярної патології серед населення України та щорічний ріст захворюваності та смертності від інфаркту міокарда (ІМ) свідчать про необхідність удосконалення діагностики цієї нозології [6]. При цьому акцент треба робити на засоби, які можна використовувати біля ліжка хворого та які потребують найменшого часу для інтерпретації даних і прогнозування перебігу хвороби [4]. Цим умовам відповідає спосіб векторкардіографічної (ВКГ) діагностики за методом Акулінічева на новому розробленому поліграфі. Він дозволяє в масштабі реального часу проводити моніторинг змін електрорушійної сили (ЕРС) серця й отримувати збільшення траси петель до 3000 разів. Це підвищує якість отриманої інформації, що дає змогу доповнювати електрокардіографічну (ЕКГ) картину за гострої коронарної патології [2].
Мета роботи — дослідити векторкардіографічні ознаки гострого інфаркту міокарда із зубцем Q задньобічної стінки лівого шлуночка (ЛШ).
Матеріали та методи
В умовах інфарктного відділення Луганської міської клінічної багатопрофільної лікарні № 1 обстежено 147 хворих із гострим ІМ лівого шлуночка. Для реалізації мети у роботу включені 10 хворих із первинним ІМ задньобічної локалізації віком від 56 до 81 року. Середній вік становив 69 ± 3 роки. Чоловіків і жінок було порівну. Хворі госпіталізовані в перші 24 години від початку захворювання. У дослідження не включено хворих із повторним ІМ та ІМ без зубця Q, із повною блокадою лівої ніжки пучка Гіса, із більш пізніми строками надходження до стаціонару, з органічними ураженнями клапанів та гострою лівошлуночковою недостатністю III–IV класу за Killip — Kimbal. Діагноз ІМ ЛШ був установлений відповідно до рекомендацій Європейського товариства кардіологів [8], за клінічним даними, результатами ЕКГ у динаміці та результатами оцінки біохімічних маркерів некрозу.
Інструментальне дослідження включало: ЕКГ, ВКГ та ехокардіографію (ЕхоКГ).
Під час ЕКГ–дослідження реєстрували стандартні, посилені однополюсні та грудні відведення, а також V7–9, V3R і за Небом.
Результати ВКГ проаналізовані з урахуванням зміни розташування петель Р, QRS і Т у системі координат у п’яти проекціях (ВА1–5), обертання петель за годинниковою стрілкою, напрямків головного вектора, види траси, величини максимального вектора, площі, швидкості поширення імпульсу трасою петель Р, QRS і Т, кутової розбіжності петель QRS-Т і QRS-Р, наявності розмикання петель QRS і Т, а також напрямку вектора ST. Дослідження ЕРС серця проводилося на кардіодіагностичному багатофункціональному комплексі МТМ-СКМ Сєверодонецького науково-виробничого підприємства «Мікротерм» (свідоцтво про державну реєстрацію № 2375/2003, реєстраційний № 19081403 від 26 грудня 2003 р.).
Для оцінки основних параметрів внутрішньосерцевої гемодинаміки проводили ехокардіографічне дослідження за допомогою ультразвукової діагностичної системи DC-–6 (Shenzhen Mindray Bio-Medical Electronics Co.LTD, Китай). Визначалися такі параметри: кінцево-діастолічний розмір лівого (КДР ЛШ) і правого шлуночків (КДР ПШ), діаметр лівого передсердя (ЛП), аорти, товщину стінок ЛШ у діастолу, задньої стінки (ЗСЛШ) і міжшлуночкової перегородки (МШП). Фракцію викиду (ФВ) ЛШ визначали згідно з рекомендаціями Американського товариства ехокардіографії за модифікованою методикою Simpson. Для оцінювання параметрів діастолічної функції ЛШ усім хворим проводили допплерівське дослідження з визначенням таких показників трансмітрального кровотоку, як пікова швидкість раннього (Ve) і пізнього (Va) діастолічного наповнення ЛШ, співвідношення Ve/Va, IVRT — час ізоволюмічного розслаблення ЛШ, DT — час сповільнення раннього діастолічного наповнення ЛШ. Для диференціації нормального та псевдонормального типів трансмітрального кровотоку на 14–18-й день проводили пробу Вальсальви, що полягає в зниженні тиску в лівому передсерді внаслідок зменшення венозного повернення крові до серця при натужуванні, що сприяє переходу псевдонормального діастолічного потоку в спектр із порушеним розслабленням [7]. Таким чином, якщо при проведенні проби відношення Ve/Va знижувалося, ми розглядали тип трансмітрального кровотоку як псевдонормальний.
Із метою оцінки у хворих величин ВКГ та ЕхоКГ ми порівнювали їх із такими референтної групи, яку становили 15 фактично здорових чоловіків та 5 жінок [2, 3].
Статистичну обробку результатів дослідження робили за допомогою комп’ютерної програми Statistica 6.1. Для аналізу результатів використано: перевірку нормальності розподілу випадкової величини за допомогою критерію Шапіро — Уїлка, параметричний t-критерій і непараметричний U-критерій Манна — Уїтні для порівняння двох незалежних вибірок, критерій Стьюдента для визначення можливих меж помилок (у вигляді M ± m, де M — середнє значення показника, m — стандартна помилка середнього показника).
Результати та обговорення
У клінічній картині захворювання у 8 пацієнтів (80 % випадків) відзначався типовий інтенсивний ангінозний біль тривалістю не менше 30 хвилин. У двох хворих був дискомфорт у ділянці серця. Іррадіація болю в ліве плече й ліву руку спостерігалась у половині випадків, в обидві верхні кінцівки — у трьох хворих, безбольова форма інфаркту міокарда — у двох хворих.
Гостра лівошлуночкова недостатність IІ класу за Killip — Kimbal була у 4 хворих. Гіпертонічна хвороба I стадії була виявлена у 4 хворих, II стадії — у 3.
У 50 % досліджених було визначено сироватковий рівень серцевого тропоніну I, який становив 6,061 ± 1,505 нг/мл (за норми 0–0,5 нг/мл), що підтверджувало наявність некрозу міокарда.
При ЕКГ-дослідженні у всіх хворих реєстрували елевацію сегмента ST в II, III, avF, V5(6), V7–9 відведеннях та в Dorsalis за Небом понад 1 мм. У трьох хворих такі зміни були й у I, avL та Inferior за Небом. У V5,6 глибокі зубці S спостерігалися у двох випадках, зменшення амплітуди зубця R — у 7 хворих (70 %). Виражена зазубреність комплексу QRS у II, III, avF, V5(6) відзначалась у трьох хворих. Крім цього, у 70 % випадків (7 хворих) виявлялись реципрокні зміни по передній стінці ЛШ у вигляді депресії сегмента ST та високого позитивного зубця Т в V1–2(3) та V3R. Також у V1,2 збільшилась висота зубця R і зменшилась амплітуда зубця S у трьох хворих. Порушення деполяризації шлуночків у всіх хворих проявлялося патологічним зубцем Q у III, avF, V5(6). При цьому у 4 пацієнтів зубець Q сформувався на 2-гу добу. У 3 хворих визначалися ознаки гіпертрофії міокарда ЛШ (рис. 1).
За даними ВКГ головний вектор у системі координат у всіх пацієнтів був спрямований униз і назад, а також у 6 хворих — уліво й у 4 пацієнтів — управо.
У 60 % хворих спостерігалася картина локальної внутрішньошлуночкової блокади в першій проекції. Вона виявлялася в тому, що початкова частина петлі QRS з II квадранта переходила в IV, де була розташована основна частина, і закінчувалася в III квадранті. У 4 хворих петля QRS була звужена. При цьому записувалася петля за годинниковою стрілкою, що підтверджувало задній ІМ.
Крім того, у всіх обстежених у проекції ВА2 основна частина петлі QRS була розташована праворуч (просторово попереду) вертикальної координати, що свідчить про ослаблення електричних сил у ділянці задньої стінки ЛШ. У другій і третій проекціях реєструвався виражений зсув вектора початкового відхилення петлі QRS уперед, угору і вправо у вигляді додаткового полюса за записом петлі у звичайному напрямку у всіх пацієнтів. Ці зміни виражають втрату ЕРС, у нормі спрямованих назад, униз і вліво. У всіх хворих початкова частина петель QRS була розташована у IV квадранті, що підтверджує залучення в патологічний процес бічних відділів ЛШ. У 40 % випадків напрямок траси петель QRS різко псувався в другій, третій, четвертій та п’ятій проекціях, унаслідок чого петлі набувають вигляду вісімки, де точка перетину позначається як «справжній вузол». Це відображає асинхронність збудження міокарда задньобічної стінки ЛШ, ділянці верхівки й базальних відділів шлуночків [1].
Крім того, відбувалось пригнічення електричної активності міокарда в зоні некробіотичних змін, на що вказує зменшення сумарної площі петель QRS за рахунок другої та третьої проекцій в 1,8 раза (р < 0,001). Максимальний вектор петель QRS був зменшений у ВА1,4,5 (р < 0,01), напевно, у зв’язку з їх деформацією (табл. 1).
Згущення позначок часу по трасі петель QRS реєструвалося в кінцевій частині петель у четвертій (р < 0,001) та п’ятій (р < 0,01) проекціях та в початковій частині петель у ВА5 (р < 0,01) як відбиття вповільнення внутрішньошлуночкової провідності в ділянці верхівки та базальних відділів шлуночків (табл. 2).
Розрядження позначок часу відзначалося в ділянці вектора кінцевого відхилення в ВА1,2,5 (р < 0,01) і в ділянці вектора початкового відхилення в п’ятій проекції (р < 0,001). Зміни швидкісних показників свідчать про збільшення швидкості поширення збудження міокардом. Це пов’язано з підвищенням навантаження на відділи серця, які розташовані за межами ішемізованого міокарда, що оточують зону некрозу, а саме у високих відділах передньої, задньобічної стінки ЛШ та базальних відділах шлуночків.
У всіх випадках реєструвалося розмикання петель QRS-Т: у ВА1 — 0,49 ± 0,02 мм, у ВА2 — 1,32 ± 0,25 мм, у ВА3 — 1,36 ± 0,21 мм, у ВА4 — 1,24 ± 0,25 мм і у ВА5 — 1,54 ± 0,24 мм. При цьому вектор ушкодження ST, що є еквівалентом зсуву інтервалу ST на ЕКГ, вказував на локалізацію вогнища ураження — униз і вліво. Дезорганізацію фази реполяризації віддзеркалює як поява вектора ST на тлі розмикання петель QRS і Т, так і зміна параметрів петлі Т. Петлі Т були розташовані поза петлями QRS у всіх хворих. У першій проекцій петлі Т відхилялися вгору. У ВА2 петля Т мала клиноподібну форму та була спрямована уперед, уліво й угору. Її розщеплена основа була повернута назад, управо й униз. Отже, така особлива спрямованість петель Т характерна для задньобічної локалізації ІМ [1, 5]. У першій, четвертій та п’ятій проекціях ВКГ петля Т «округлилася» за рахунок зменшення максимального вектора. Площа петель Т збільшилася в 3–3,6 раза в другій та третій проекціях (р < 0,001). У 2 випадках виявлені перехрести петель Т у ВА1. Збільшення кутової розбіжності петель QRS-Т відзначалося в усіх проекціях: у ВА1,2,4,5 (р < 0,001) та у ВА3 (р < 0,01) (табл. 1). Швидкість поширення імпульсу петлями Т (табл. 3) була уповільнена у ВА1–5 (р < 0,001). Отже, порушення процесів пізньої реполяризації спостерігалось не тільки в зоні некробіозу, а також в передній стінці ЛШ, верхівці та базальних відділах обох шлуночків.
Площа передсердних петель Р суттєво збільшилась у ВА1–3 (р < 0,001) і у ВА4 (р < 0,05) за збільшення максимального вектора петлі Р у п’ятій проекції (р < 0,001) (табл. 1). Це вказує на гемодинамічне перевантаження передсердь. Різноспрямовані зміни швидкісних показників (р < 0,001), очевидно, пов’язані із різною мірою деполяризації кардіоміоцитів на тлі ішемічних проявів (табл. 4). Порушення процесів реполяризації у задньобічній стінці лівого та задній стінці правого передсердь підтверджувалось зменшенням кутової розбіжності петель QRS-Р у ВА3 (p < 0,01) і збільшенням — у ВА4,5 (p < 0,001) (табл. 1).
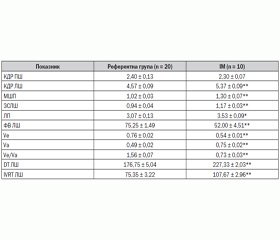
Ехокардіографічне дослідження зроблене у 3 хворих через летальний кінець інших 7 хворих упродовж 10 діб. Аналіз результатів двовимірної ЕхоКГ у хворих на ІМ порівняно з контрольною групою виявив вірогідне збільшення порожнини ЛШ (р < 0,01), лівого передсердя (р < 0,05) і зниження систолічної функції ЛШ (ФВ, р < 0,01). Відбувалося помірне потовщення МШП та ЗСЛШ (р < 0,01). У всіх хворих визначався помірний гіпокінез задньобічної стінки ЛШ, у двох — помірний гіперкінез МШП. За результатами допплерівського дослідження трансмітрального кровотоку у порівнянні з нормою у хворих реєструвалося зниження співвідношення швидкостей раннього та пізнього наповнення ЛШ Ve/Va за рахунок зменшення швидкості раннього діастолічного руху Ve і збільшення відносного внеску в наповнення ЛШ систоли ЛП Va (р < 0,01) за подовження інтервалу DT та часу ізоволюмічного розслаблення ЛШ (р < 0,01) (табл. 5).
У всіх хворих на ІМ визначено потовщення стінок аорти. Помірний фіброз стулок мітрального й аортального клапанів визначено у одного хворого. Ще у одного пацієнта реєструвалася легка регургітація на аортальному клапані через кальциноз стулок.
Таким чином, зміни ЕРС серця у хворих на гострий ІМ задньобічної локалізації векторкардіографічно характеризуються зсувом петель QRS уперед, угору та вправо з розташуванням у другій проекції в IV квадранті їх початкової частини та праворуч вертикальної координати — основної частини, зменшенням площі петель QRS, появою вектора ушкодження ST, спрямованого униз і вліво, залученням у патологічний процес відділів серця, які локалізуються поза межами ішемізованого міокарда, що оточують зону некрозу. При цьому порушення провідності та процесів реполяризації спостерігаються в усьому міокарді, але різного ступеня вираженості. Ехокардіографічне дослідження дозволило виявити збільшення порожнини лівих камер серця за зниженням скорочувальної функції ЛШ і зниженням його податливості та збільшенням тиску наповнення.
Висновки
1. Гострий інфаркт міокарда задньобічної локалізації в зоні некрозу векторкардіографічно проявляється в другій та третій проекціях зсувом петель QRS уперед, угору та вправо зменшенням їх площі в 1,8 раза (p < 0,001), порушенням провідності у вигляді перехреста петель і процесів реполяризації та розташуванням у другій проекції основної частини петель QRS праворуч від вертикальної координати, а її початкової частини — у IV квадранті.
2. У ділянці некротичних змін порушення процесів реполяризації виявляються незамкнутістю петель QRS і Т із появою вектора ушкодження ST, спрямованого униз і вліво, розташуванням петель Т поза петлями QRS, відхиленням петель Т у першій проекції угору, у другій — уперед, уліво та вгору; у другій та третій проекціях — збільшенням площі петель Т у 3–3,6 раза (p < 0,001), порушенням швидкості поширення імпульсу петлями Т та збільшенням кутової розбіжності петель QRS-Т.
3. При гострому інфаркті міокарді задньобічної стінки лівого шлуночка поза зоною некрозу в четвертій та п’ятій проекціях векторкардіограми реєструються вповільнення внутрішньошлуночкової провідності в ділянці верхівки та базальних відділах шлуночків. Прискорення швидкості поширення збудження в їх високих відділах та в передній стінці лівого шлуночка з порушенням у цих ділянках процесів реполяризації у вигляді збільшення кутової розбіжності петель QRS-Т, порушення проведення імпульсу петлями Т за зменшення максимального вектора петлі Т відповідають змінам у першій, четвертій та п’ятій проекціях.
4. Залучення передсердь у патологічний процес виражається в збільшенні площі петель Р у 2,2–4 раза (p < 0,05–0,001) у перших чотирьох проекціях векторкардіограми та максимального вектора петель Р — у п’ятій проекції, різноспрямованими змінами швидкісних показників у всіх проекціях та кутової розбіжності петель QRS-Р — у п’ятій проекції.
5. Структурно-функціональні зміни серця при гострому інфаркті міокарда задньобічної локалізації проявляються збільшенням порожнини лівих камер серця та порушенням параметрів трансмітрального діастолічного кровотоку у вигляді зниження передсердно-шлуночкового градієнта тиску за зменшенням фракції викиду (p < 0,01).
1. Акулиничев И.Т. Практические вопросы векторкардиоскопии. — М.: Медгиз, 1960. — 214 с.
2. Бєлая І.Є. Векторкардіографічні ознаки гострого інфаркту міокарда із зубцем Q задньо-нижньої локалізації в перші 24 години захворювання // Серце і судини. — 2012. — № 3. — С. 62–71.
3. Бєлая І.Є. Структурно-функціональні зміни серця у хворих на гострий інфаркт міокарда на тлі неалкогольної жирової хвороби печінки // Медицина неотложных состояний. — 2013. — № 1 (48). — С. 94–98.
4. Пархоменко О.М., Шумаков О.В., Гур’єва О.С., Корнацький Ю.В., Кожухов С.М. Неінвазивні електрофізіологічні маркери несприятливого перебігу інфаркту міокарда у хворих зі збереженою систолічною функцією серця та проявами гострої серцевої недостатності: Матеріали XIV Національного конгресу кардіологів України, м. Київ, 18–20 вересня 2013 р. // Укр. кардіол. журн. — 2013. — Додаток 4. — С. 150–159.
5. Тартаковский М.Б. Основы клинической векторкардиографии. — Л.: Медицина, 1964. — 435 с.
6. Устінов О.В. Проблеми надання медичної допомоги хворим на гострий інфаркт міокарда в Україні // Укр. мед. часопис. — 2013. — № 2 (94), III/IV. — Режим доступу до журн.: http://www.umj.com.ua/article/55726/problemi-nadannya-medichnoi-dopomogi-xvorim-na-gostrij-infarkt-miokarda-v-ukraini
7. Recommendations for chamber quantification: А report from the American Society of Echocardiography’s guidelines and Standards Committee and the Chamber Quantification Writing Group, Developed in Conjunction with the European Association of Echocardiography, а Branch of the European Society of Cardiology // J. Amеr. Soc. Echocardiography. — 2005. — Vol. 18. — P. 1440–1463.
8. Van de Werf F., Bax J., Betriu A. et al. The Task Force on the management of ST-segment elevation acute myocardial infarction of the European Society of Cardiology // Eur. Heart. J. — 2008. — Vol. 29, Issue 23. — P. 2909–2945. doi: 10.1093/eurheartj/ehn416.

/109/109_2.jpg)
/109/109.jpg)
/110/110.jpg)
/111/111.jpg)
/111/111_2.jpg)