Газета «Новости медицины и фармации» Кардиология (512) 2014 (тематический номер)
Вернуться к номеру
Ревматоїдний артрит Адаптована клінічна настанова, заснована на доказах 2014 (скорочено)
Рубрики: Кардиология
Разделы: Официальная информация
Версия для печати
Статья опубликована на с. 29-76
Рекомендовано
Наказ Міністерства охорони здоров’я України
від 11.04.2014 року № 263
Вступ
Ревматичні хвороби розглядаються у всьому світі як одна з найбільш поширених патологій та як одна з найбільш значимих медичних та соціально–економічних проблем сучасного суспільства.
За даними МОЗ України в 2010 р. поширеність ревматоїдного артриту (РА) в абсолютних показниках становила 116 492 хворих (серед яких понад 52 000 — особи працездатного віку), а захворюваність — 6190. Це зумовлено тим, що недостатніми є профілактичні заходи, спрямовані на раннє виявлення захворювання, дуже повільно впроваджуються сучасні методи діагностики та лікування РА, недостатня кількість медикаментів та обладнання.
Втрата працездатності і зростання інвалідності є найважливішим соціально–економічним наслідком РА. Вона може початися вже на ранній стадії розвитку хвороби і стає пожиттєвою проблемою у 27 % хворих на РА протягом перших трьох років після початку хвороби, а через 8–11 років виникає приблизно у 85 % пацієнтів, які потребують постійного сучасного медикаментозного лікування, проведення реабілітаційних заходів, обов’язкової госпіталізації при загостренні хвороби, нерідко складних ортопедичних оперативних втручань. Рівень смертності у хворих на РА вищий принаймні у два рази, ніж у загальній популяції. Цей показник погіршується з кожним роком.
Лікування хворих з РА потребує великих коштів, які суттєво перевищують витрати на лікування більшості хронічних захворювань. Наприклад, загальні витрати в системі охорони здоров’я Великобританії, пов’язані з РА, були оцінені в 1,3 млрд фунтів стерлінгів, а в Швеції ці витрати становили більше 3 млрд шведських крон (близько 423 млн доларів США), що приблизно дорівнює витратам на лікування онкологічних хворих.
Синтез настанови
Пошук інформації обмежувався керівництвами або систематичними оглядами з використанням основних інтернет–сайтів з медицини, включаючи бази даних GIN, Embase, Healthstar і Pascal. Пошук додаткової інформації, проведений з використанням вищезазначених баз даних, був спрямований на інформацію з діагностики та лікування хворих на РА в рамках надання первинної та вторинної медичної допомоги. Пошук основної інформації доповнено матеріалами, зібраними робочою групою з розробки клінічної настанови. Усі відібрані матеріали оцінювалися з застосуванням стандартної методології, перш ніж отримані висновки були використані як докази.
Дана клінічна настанова є адаптованою для системи охорони здоров’я України версією клінічних настанов.
1. NICE Rheumatoid arthritis: national clinical guideline for management and treatment in adults. London: Royal College of Physicians, 2009.
2. EULAR recommendations for the management of rheumatoid arthritis with synthetic and biological disease–modifying antirheumatic drug, 2010.
Ці настанови були обрані робочою групою з адаптації як ключові прототипи найкращої практики надання медичної допомоги пацієнтам з РА, що грунтуються на даних доказової медицини стосовно ефективності та безпеки медичних втручань, фармакотерапії та організаційних принципів її надання. Клінічні настанови були обрані на основі об’єктивних критеріїв їх оцінки, а саме за допомогою Опитувальника AGREE.
Дану адаптовану клінічну настанову пропонується розглядати як інформаційне джерело з вибору діагностичної та лікувальної тактики при лімфомах у дорослих. Певні відхилення можливі, але вони мають бути обґрунтовані відповідним чином — консиліумом спеціалістів на чолі з керівником відділення.
Загальний коментар робочої групи щодо рекомендацій NICE
Представлені NICE рекомендації повною мірою відображають стан та значимість проблеми РА, є досить доступними і включають всі аспекти ведення хворого — від встановлення діагнозу, призначення максимально ефективних та безпечних схем фармакотерапії до схем реабілітації пацієнта.
Значимість рекомендацій підтверджується глибоким статистичним аналізом, наявністю метааналізів, чітким визначенням значимих для аналізу показників.
Важливість створення мультидисциплінарної команди (МДК) з ключовою фігурою — медичною сестрою — координатором (спеціаліст з РА) — є незаперечною (див. Коментар робочої групи в тексті).
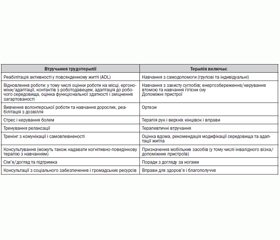
Також вважаємо необхідним вдосконалення етапу реабілітації хворих на РА, який детально висвітлений в Рекомендаціях, в тому числі більш широке застосування механічних приладів — ортезів, коригуючих устілок тощо.
— Різниця між країнами в структурі служб, які надають допомогу хворому на РА, та недостатній розвиток страхової медицини не дозволяють повною мірою адаптувати протокол до реалій нашої країни. Те ж саме стосується методологій економіки здоров’я, що наведені в Рекомендаціях.
— На наш погляд, затримка в наданні медичної допомоги, на відміну від Великої Британії, визначається в Україні не тим, що сімейний/дільничний лікар не направляє своєчасно хворого до ревматолога, а пізнім звертанням хворого до лікаря первинної ланки, зволіканням з направленням до фахівця–ревматолога та застосуванням глюкокортикоїдів при невстановленому діагнозі.
— Деякі БА, які включені в настанову, не зареєстровані в Україні.
— Залишається невизначеним питання про те, який БА має бути першим при призначенні хворим на РА.
— За умов створення міждисциплінарної групи доцільним є створення протоколу з чітким розподілом функцій між членами групи.
Пропозиції:
— Необхідно створення Реєстру хворих на РА, а також об’єднання останніх в Асоціацію за типом PARE EULAR (див. Коментарі в тексті).
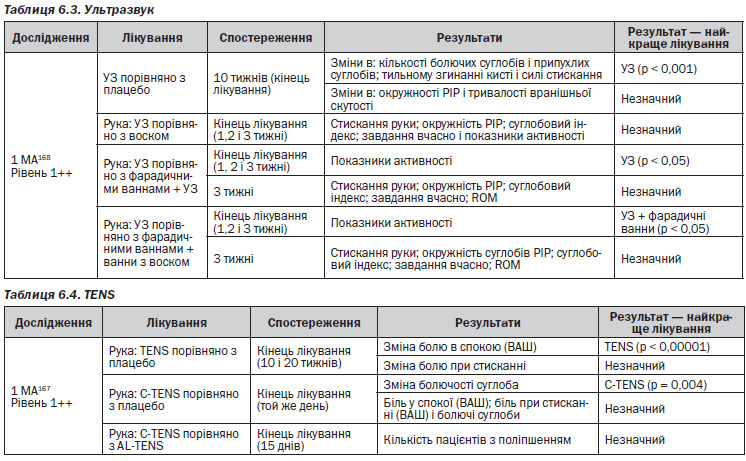
— Враховуючи доступність та високу інформативність УЗД для хворих з РА, слід запровадити навчання лікарів–ревматологів методикам ультразвукового дослідження суглобів в рамках підвищення кваліфікації.
Скорочення
АКН — адаптована клінічна настанова
АнтиЦЦП — антитіла до циклічного цитрулінованого пептиду
ВАШ — візуальна аналогова шкала (Visual analogue scale — VAS)
ГК — глюкокортикоїд
ГРН — група розробки постанови
ДІ — довірчий інтервал (95%, якщо не вказано інше)
ІНФ — інфліксимаб
MA — метааналіз
МДК — мультидисциплінарна команда
МТ — метотрексат
СРБ — С–реактивний білок
ССЗ — сульфасалазин
НП — несприятливі події (Adverse events — AEs)
НППЗ — нестероїдні протизапальні і протиревматичні засоби
РКД — рандомізоване контрольоване дослідження
РА — ревматоїдний артрит
ФНП–-а — фактор некрозу пухлин а
ЦОГ–2 — циклооксигеназа 2
ШОЕ — швидкість осідання еритроцитів
ABA — Abatacept — Абатацепт
ACR — American College of Rheumatology — Американська колегія ревматології
ACR20, 50, 70 — ACR criteria 20, 50, 70 — критерії ACR 20, 50, 70
ADA — Adalimumab — адалімумаб
ADL — Activities of daily living — активність щоденного життя
AIMS — Arthritis Impact Measurement Scale — Шкала вимірювання впливу артриту
AL–TENS — Acupuncture–like transcutaneous electrical nerve stimulation — черезшкірна електрична стимуляція нервів, подібна до голковколювання
ARA — American Rheumatism Association (now ACR) — Американська асоціація ревматизму (зараз — Американська колегія ревматологів)
ARMA — Arthritis and Musculoskeletal Alliance — Артрити та кістково–м’язовий альянс
AUC — Area under the curve — площа під кривою
ARC — Arthritis Research Campaign — Компанія дослідження артритів
BMI — Body mass index — індекс маси тіла
BSR — British Society of Rheumatology — БТР — Британське товариство з ревматології
CBT — Cognitive behavioral therapy — когнітивна поведінкова терапія
CsA — Cyclosporin A — циклоспорин А
CTX — Cyclophosphamide — циклофосфамід
DAS — Disease Activity Score — індекс активності хвороби (DAS28, DAS32)
DMARD — Disease modifying antirheumatic drug —хворобомодифікуючі антиревматичні препарати
EA — Electroacupuncture — електроакупунктура
EQ–5D — EuroQol 5–dimensional outcomes questionnaire — опитувальник EuroQol
EOW — Every other week — раз на два тижні
ETN — Etanercept — етанерцепт
EULAR — The European League against Rheumatism — Європейська ліга проти ревматизму
EW — Every week — щотижня
HAQ — Health Assessment Questionnaire — анкета оцінки стану здоров’я
HCQ — Hydroxychloroquine — гідроксихлорохін
ICER — Incremental cost–effectiveness ratio — диференційований коефіцієнт рентабельності
IRGL — Impact of Rheumatic Diseases on General Health and Lifestyle Questionnaire — Опитувальник впливу ревматичних захворювань на загальний стан здоров’я і спосіб життя
ITT — Intention to treat analysis — аналіз залежно від призначеного лікування
JSN — Joint space narrowing — звуження суглобової щілини
MACTAR — McMaster Toronto Arthritis Patient Preference Disability Questionnaire —– опитувальник переваг інвалідності у хворих артритом (McMaster Toronto)
MCP — Metacarpophalangeal joint — п’ясно–фалангові суглоби
MD — Mean difference — середня різниця
MTP — Metatarsophalangeal joint — плесно–фалангові суглоби
MHRA — Medicines and Healthcare products Regulatory Agency — Агентство з регулювання лікарських засобів і медичних виробів
NCC–CC — National Collaborating Centre for Chronic Conditions — Національний центр співробітництва з хронічних захворювань
NHS — National Health Service — Державна служба охорони здоров’я
NICE — National Institute for Health and Clinical Excellence — Національний інститут здоров’я та якості медичної допомоги
NS — not significant — незначний (при 5% рівні, якщо не встановлене інше)
NRAS — National Rheumatoid Arthritis Society — Національне товариство ревматоїдного артриту
OMERACT — Outcome Measures in Rheumatoid Arthritis Clinical Trials — оцінка результатів клінічних досліджень ревматоїдного артриту
OR — Odds ratio — співвідношення шансів
OT — Occupational therapy or therapis — трудотерапія або трудотерапевт
PIP — Proximal interphalangeal joint — проксимальні міжфалангові суглоби
PPI — Proton pump inhibitor — інгібітори протонної помпи
PPV — Positive predictive value — позитивна прогностична цінність
QALY — Quality–adjusted life–year — рік життя з урахуванням його якості
QoL — Quality of Life — якість життя
RAI — Ritchie Articular Index — суглобовий індекс Рітчі
TJR — Total joint replacement — тотальна заміна суглоба
TSS — Total Sharp Score — загальний індекс Шарпа
WMD — Weighted mean differences — зважена різниця середніх
Глосарій
Біологічний препарат/біопрепарат — тип DMARD (хворобомодифікуючий протиревматичний препарат), дія якого спрямована на прозапальні цитокіни, які залучені до руйнування суглобів (зокрема ФНП–альфа та ІЛ–1).
Клінічно значуще покращення — в деяких дослідженнях дихотомічний результат клінічно значущого полегшення болю визначається як такий, що досягається при перевищенні специфічного порогу за шкалою болю, наприклад рівень болю за ВАШ. Проте будь–який стандартний поріг відсутній, і кожне дослідження повинно розглядатися індивідуально.
Когортне дослідження — ретроспективне або проспективне дослідження протягом тривалого часу. Групи осіб, за якими ведеться подальше спостереження, визначаються на підставі наявності або відсутності дії на них потенційного чинника ризику або втручання. Когортне дослідження може бути порівняльним, при якому відбираються дві або більша кількість груп на підставі відмінностей за дією на них певного чинника.
Довірчий інтервал (ДІ) — діапазон значень, який містить істинне значення для популяції зі встановленою вірогідністю (традиційно 95 %). Цей інтервал розраховується на підставі даних вибірки і зазвичай включає оцінку вибірки. 95% довірчий інтервал означає, що якщо дослідження і метод, використаний для розрахунку цього інтервалу, повторюються багато разів, то 95 % розрахованих інтервалів насправді міститимуть істинне значення для усієї цієї популяції.
Кокранівський огляд — Кокранівська бібліотека складається з регулярно оновлюваної колекції баз даних доказової медицини, включаючи Кокранівську базу даних систематичних оглядів (огляди рандомізованих контрольованих досліджень, що підготовлені Кокранівською спілкою).
Аналіз наслідків витрат — тип економічної оцінки, при якій для кожного втручання на додаток до витрат повідомляються різні ефекти лікування, проте відсутня оцінка загального показника здоров’я населення.
Аналіз ефективності витрат — дизайн економічного дослідження, в якому наслідки різних втручань вимірюються за даними єдиного результату, зазвичай в природних одиницях (наприклад, збережені роки якісного життя, кількість попереджених смертей, кількість попереджених серцевих нападів, виявлені випадки), після чого альтернативні втручання порівнюють за показниками витрат на одиницю ефективності.
Аналіз корисності витрат — форма аналізу ефективності витрат, в якій одиницями ефективності є кількість збережених років якісного життя (QALY).
Хворобомодифікуючий протиревматичний препарат (DMARD) — лікування, яке може зменшити або запобігти ушкодженню суглобів.
Розгорнута стадія РА — ревматоїдний артрит, тривалість якого перевищує два роки.
Приріст витрат — вартість одного альтернативного препарату мінус вартість іншого.
Коефіцієнт ефективності приросту витрат (ICER) — відношення різниці вартості двох альтернативних препаратів до різниці ефективності даних альтернативних препаратів.
Індекс Ларсена — рентгенологічний метод оцінки ушкодження суглобів, що спричинене РА.
Мануальна терапія — спеціальні фізіотерапевтичні техніки, при проведенні яких виконуються маніпуляції з ураженим суглобом (переважно кульшовий) і його мобілізація поза межами амплітуди рухів, які може здійснювати хворий з остеоартрозом.
Метааналіз — статистичний метод комбінування (об’єднання) результатів низки досліджень, які присвячені певній проблемі і в яких отримано одні й ті самі результати, для отримання узагальнювального результату.
Методологічні обмеження — особливості дизайну або звітності про результати клінічного дослідження, про які відомо, що вони пов’язані з ризиком систематичної помилки або відсутністю валідності. У разі, якщо в цій настанові згадується дослідження, що має значні методологічні обмеження, то безпосередньо воно не стає підставою для будь–якої рекомендації.
Багатоваріантний — одночасний аналіз більше однієї змінної. Приймається до уваги вплив усіх змінних на певну відповідь.
Обсерваційне дослідження — ретроспективне або проспективне дослідження, при проведенні якого дослідник спостерігає за природним перебігом подій з контрольною групою або без неї, наприклад, когортні дослідження або дослідження «випадок–контроль».
Відношення шансів — ступінь ефективності лікування: шанс того, що певна подія станеться в групі, яка зазнає медичного впливу, розділений на шанс того, що вона станеться в контрольній групі. «Шанси» — це відношення відсутності події до події.
Значення р — вірогідність того, що спостережувана відмінність могла статися випадково. Значення р менше ніж 0,05 традиційно вважається «статистично значущим».
Якість життя (QоL) — відноситься до рівня комфорту, задоволеності якістю життя і здатності здійснювати повсякденну діяльність.
Роки життя з поправкою на їх якість (QALY) — ступінь ефективності лікування за наслідками щодо стану здоров’я, згідно з якою кожному періоду часу надаються бали в діапазоні від 0 до 1, що відповідають якості життя, пов’язаній зі здоров’ям протягом цього періоду, де бал 1 відповідає оптимальному здоров’ю, а бал 0 відповідає стану здоров’я, який вважається еквівалентним смерті; потім вони об’єднуються за часовими періодами.
Рандомізоване контрольоване дослідження (РКД) — дослідження, в якому особи розподіляються випадковим чином на дві (чи більше) групи: одна (експериментальна група) отримує лікування, яке тестується, а інша (група порівняння або контрольна група) отримує альтернативне лікування, плацебо (лікування «неактивною» речовиною) або зовсім не отримує лікування. Потім за обома групами проводиться спостереження для проведення порівняння відмінностей за результатами, щоб побачити, наскільки ефективним було експериментальне лікування. Така схема дослідження допомагає мінімізувати експериментальну систематичну помилку.
Ранній РА — ревматоїдний артрит, тривалість якого складає менше двох років. В межах раннього РА категорії підозрюваного стійкого синовіту або підозрюваного РА відносяться до хворих, у яких діагноз все ще не з’ясований, але які потребують направлення до спеціаліста або додаткового обстеження.
Резервна терапія — у цій настанові він це є результат, що зареєстрований у деяких дослідженнях. Частота застосування засобів резервної терапії — це частота, з якою учасники повинні застосовувати активніший препарат (зазвичай для знеболення).
Самоконтроль — термін, який використовується щодо аспектів самостійного лікування РА хворими згідно з рекомендаціями групи первинного лікування, наприклад сімейного лікаря, медсестри, фізіотерапевта, лікаря трудової терапії та інформаційних листів.
Аналіз чутливості — ступінь величини, до якої невеликі зміни в параметрах і змінних впливають на результати, що розраховані на їх основі. У цій настанові аналіз чутливості використовується для моделювання економіки здоров’я.
Зацікавлена сторона — будь–яка національна організація, включаючи хворих і групи надання медичної допомоги, медичних працівників і комерційні компанії, що зацікавлені в настанові, що розробляється.
Статистична значущість — результат вважається статистично значущим, якщо вірогідність результату, що відбувається випадково, складає менше ніж 1 з 20 (р < 0,05).
Систематичний огляд — дослідження, яке узагальнює результати досліджень чітко сформульованого питання відповідно до заздалегідь визначеного протоколу, з використанням систематичних і явних методів для ідентифікації, вибору і оцінки відповідних досліджень, та для отримання, впорядковування і опису їх результатів. Він може використовувати або не використовувати статистичний метааналіз.
Технологічна оцінка — формальне встановлення і огляд доказів в області медичної технології, що обмежені в цьому документі оцінкою, що проведена NICE.
Одноваріантний — аналіз, який окремо досліджує кожну змінну в наборі даних.
Корисність — число від 0 до 1, яке може надаватися певному стану здоров’я, оцінюючи цілісний вплив на якість життя, і дає можливість розташувати стани у порядку (в середньому) переваги хворим.
1. Передмова
1.1. Загальна інформація
Ревматоїдний артрит (РА) є запальним захворюванням, яке справляє величезний вплив на ті суглоби тіла, які вкрито синовіальною оболонкою, що є спеціалізованою тканиною, яка відповідає за підтримку живлення і зволоження суглоба. Розподіл щодо уражених суглобів (синовіальні суглоби) є характерним для РА. Він типово уражає дрібні суглоби кистей і стоп, і зазвичай двобічно з симетричним розподілом, хоча може уражатися будь–який синовіальний суглоб. У хворих з розгорнутою стадією і агресивним перебігом захворювання з часом уражаються більшість суглобів.
Початковий пусковий механізм розвитку РА є невідомим. Існують факти, що припускають наявність відхилень у компонентах імунної системи, які призводять до того, що в організмі розвиваються аномальні імунні і запальні відповіді, особливо в суглобах. Ці зміни можуть передувати симптоматичному РА протягом багатьох років. Те, що призводить до патології руху, спричиняє значне збільшення кровотоку в суглобах (підвищуючи температуру і іноді сприяючи почервонінню), проліферацію синовіальної оболонки із збільшенням кількості синовіальної рідини (набряк) і біль (у зв’язку з розтягуванням больових рецепторів у навколишніх м’яких тканинах і кістках по обох боках суглоба). Ці ознаки призводять до швидкої втрати м’язів навколо ураженого суглоба і, таким чином, разом з болем і набряком спричиняють втрату функції суглоба. Якщо запалення синовіальної оболонки не буде пригнічене, воно призведе до посилення ушкодження суглоба через виділення протеолітичних ферментів із запальних та інших клітин і до перетворення частини синовіальної оболонки на запалену тканину, що має назву «панус», яка може проникати в кістку і хрящ по краях суглоба. Ступінь прогресування ушкодження пов’язаний з інтенсивністю і тривалістю запалення. Ушкодження суглобів призводить до прогресуючої деформації, непрацездатності та інвалідності. Інші структури також мають синовіальну оболонку (піхви сухожилків), і їх запалення може спричинювати розрив зв’язок. Тому пригнічення запалення на ранніх стадіях захворювання може сприяти значному поліпшенню за довгостроковими результатами для суглобів та інших компонентів скелетно–м’язової системи.
Проблемою цього широко поширеного запального артриту є той факт, що РА уражає не лише суглоби, а є системним захворюванням. В усіх хворих виділення великих концентрацій білків, які спричинюють запальний процес (такі як фактор некрозу пухлини а (ФНП–а)), призводить до симптомів вираженої втоми з відчуттям постійних грипоподібних симптомів і навіть лихоманки, потіння й втрати ваги. Крім того, інші системи органів можуть уражатися запальним процесом, із сухістю очей і рота (синдром Шегрена) і вузликами (тверді утворення, особливо на розгинальних поверхнях, як на зворотному боці ліктів), уражаючи до третини хворих.
Більш значні запальні прояви можуть призводити до серйозної патології, такої як фіброз у легенях, запалення серозних оболонок серця і легень (плевральний і перикардіальний випіт) або васкуліт. Васкуліт спричиняє запалення внутрішньої оболонки кровоносних судин і може призводити до потенційно руйнівних ефектів в тому органі, який кровопостачається ураженими кровоносними судинами. Прикладами васкуліту є склерит очей, що є болючим і потенційно загрозливим для зору васкулітом, і периферична нейропатія, при якій нерви незворотно ушкоджуються, призводячи до слабкості або сенсорних порушень. Запалення суглобів також може бути життєво небезпечним, коли воно уражає шию, викликаючи потенційно нестабільні з’єднання між кістками і запальний панус. Така комбінація деформації кісток і набряку запальної тканини може стискати спинний мозок, призводячи до ішемії і розповсюджених неврологічних наслідків із ураженням усіх чотирьох кінцівок, функції кишківника і сечового міхура, або дихальні м’язи і центри в стовбурі головного мозку, які контролюють дихання, потенційно призводячи до летального кінця.
Коментар робочої групи
Для РА характерне прискорення процесів атерогенезу, яке призводить до раннього розвитку атеросклерозу та його ускладнень — інфарктів та інсультів, що набуває особливого значення для вітчизняної системи охорони здоров’я, враховуючи високий рівень захворюваності та смертності від серцево–судинних захворювань в українській популяції (Гайдаєв Ю.О., Корнацький В.М. Проблеми здоров’я та напрямки його покращання в сучасних умовах // Український кардіологічний журнал. — 2007. — № 5. — С. 12–16).
Слід зазначити, що результати останніх досліджень геномних асоціацій підтверджують генетичну детермінованість РА. Встановлено ряд генетичних локусів, які зазвичай асоціюються з РА: HLA локус, R620W (rs2476601) поліморфізм в гені PTPN22 та асоціація з локусом 6q23/TNFAIP3 (Gisela Orozco, Steve Eyre, Anne Hinks et al. Clinical and epidemiological research Extended report: Study of the common genetic background for rheumatoid arthritis and systemic lupus erythematosus. — Ann. Rheum. Dis. — 2011. — Vol. 70. — P. 3463–3468).
На щастя, ці загрозливі життю запальні прояви захворювання є нечастими і, можливо, стають все рідкіснішими. Проте дедалі стає більш очевидно, що тривале запалення і втрата рухової функції можуть мати інші непередбачувані наслідки для хворих з РА. Було показано, що серцеві захворювання, такі як ішемічна хвороба серця і серцева недостатність, є частішими при РА і призводять до передчасної смерті багатьох хворих. Атеросклероз (коли внутрішня оболонка артерій прогресивно потовщується і порушує кровотік до органу, який вона кровопостачає) частково викликається тривалим запаленням, тому хворі з високою активністю РА мають найбільший ризик розвитку серцевих захворювань. Остеопороз також є характерним захворюванням у зв’язку з обмеженою функцією руху, запаленням та інколи з прийомом ліків (особливо глюкокортикоїдів). Хворі з РА більш схильні до інфекцій, ніж інша частина населення, ймовірно, через порушення в імунній системі і іноді у зв’язку з прийомом ліків (імунодепресивна дія глюкокортикоїдів).
Зрозуміло, що РА потенційно може спричиняти не лише розповсюджене ушкодження суглобів і м’яких тканин, запальні процеси також можуть безпосередньо або опосередковано впливати на більшість систем органів в організмі і призводити до передчасної смерті. Тому потрібне відповідне лікування, направлене не лише на суглоби, але також на весь організм хворого, що страждає цим захворюванням, його сім’ю і осіб, що надають медичну допомогу і при необхідності їх роботодавців.
1.2. Визначення
Класифікаційні критерії РА, що найчастіше використовуються, були описані в 1987 р. комітетом Американської колегії ревматології2 і опубліковані в «Переглянутих в 1987 р. класифікаційних критеріях ревматоїдного артриту Американської асоціації ревматологів» (див. таблицю 1.1).

Важливо відзначити, що це класифікаційні, а не діагностичні критерії. Іншими словами, вони були призначені для полегшення спілкування між дослідниками і для забезпечення проведення більш надійних досліджень шляхом точного визначення випадків, таким чином, незалежно від того, де проводиться дослідження, кожен мав на увазі одне і те саме під терміном «РА». Вони не є діагностичними критеріями (хоча часто необґрунтовано називаються такими), оскільки немає діагностичних тестів для РА, які диференціюють його від нормального стану або від інших типів артриту. Тому діагноз є значною мірою клінічним, покладаючись, зокрема, на ранніх стадіях на історію хвороби і клінічне обстеження хворого, з допомогою тестів (аналіз крові або методи візуалізації), які інколи допомагають підтвердити найбільш вірогідний діагноз.
Критерії ACR 1987 не були призначені для клінічної практики, хоча вони наштовхують клініцистів на думку про РА і з’являються в національних клінічних рекомендаціях. Проте вони не прийнятні для розподілу між РА і самовиліковним захворюванням з раннім синовітом, який може, врешті–решт, трансформуватися в захворювання, яке відповідає критеріям РА. Вони також виключають деяких осіб з поліартритом, які повністю не відповідають критеріям, проте хвороба яких дуже нагадує РА і має схожий перебіг і відповідь на лікування.
В межах створення цієї настанови група з розробки настанови (ГРН) прийняла, що клінічна діагностика РА є важливішою порівняно з класифікаційними критеріями 1987 для РА2, оскільки ранній стійкий синовіт, коли інші патології були виключені, має лікуватись як РА, щоб запобігти ушкодженню суглобів. Ідентифікація стійкого синовіту і відповідне раннє лікування є важливішим за те, чи задовольняє захворювання критеріям класифікації3. Тому ГРН схиляється до того, щоб використовувати прагматичний підхід і брати до уваги усіх хворих з ранньою або розгорнутою стадією запального артриту, а інші основні патології виключити.
1.3. Частота захворювання і захворюваність
Перше дослідження, присвячене частоті поширеності РА у Великобританії, було опубліковане в 1961 р., коли Лоренс оцінив, що 1,1 % населення Лея і Уенслідейлу мали РА4. Застосовуючи критерії ACR2, Сіммонс з колегами прийшов до схожої цифри (0,8 %) в дослідженні населення Норфолка5. Зрештою, у Великобританії налічується приблизно до 400 000 осіб з цим захворюванням.
Розповсюдженість цього захворювання досить низька, що було продемонстровано при проведенні другого дослідження в Норфолку, яке показало розповсюдженість захворюваності на рівні 1,5 особи на 10 000 населення на рік для чоловіків і 3,6 особи для жінок6. Це складає близько 12 000 осіб, яким щороку вперше встановлюється діагноз РА у Великобританії. Ці цифри також демонструють іншу особливість РА, яка пов’язана з тим, що загальна частота виникнення РА в 2–4 рази вище у жінок, ніж у чоловіків. Піковий вік захворюваності РА у Великобританії для представників обох статей складає близько 70 років, проте довгий «хвіст» по обох боках розподілу показує, що це захворювання може розвиватися в будь–якому віці.
ГРН поділяє РА на дві категорії за тривалістю захворювання: «рання стадія» (тривалість захворювання ≤ 2 років) і «розгорнута стадія» (тривалість захворювання > 2 років). Британське ревматологічне товариство також прийняло цей підхід при розробці своєї настанови7. В межах раннього РА категорії підозрюваного стійкого синовіту або РА, або раннього запального артриту відносяться до хворих, діагноз яких все ще не з’ясований, проте які потребують направлення на огляд до спеціаліста або додаткові обстеження. Вперше діагностований РА відноситься до хворих, у яких діагноз тільки що було встановлено, і зазвичай ними є хворі з раннім РА.
1.4. Принципи терапії
Медикаментозна терапія РА може розглядатися в двох напрямках. Перший — це покращення симптомів, серед яких основним пріоритетом для хворих є полегшення болю. Другий — це модифікація процесу захворювання, спрямована на уповільнення або зупинку рентгенологічного прогресування, яка тісно корелює з прогресуванням функціональних порушень.
Кінцевою метою терапії для хворого є досягнення ремісії захворювання. Ремісія захворювання визначається по–різному, включаючи бали нижче визначених рівнів за індексами активності захворювання (наприклад, DAS28 < 2,6). Кожне визначення включає елементи відсутності ознак і симптомів активності захворювання та інші докази того, що прогресування захворювання було зупинено. Якщо ремісія не може бути досягнута, то метою терапії є мінімізувати активність захворювання для оптимізації шансів запобігання прогресивному ушкодженню суглобів з подальшою непрацездатністю. Чим довший період ремісії або чим менша активність захворювання, яка може бути досягнута, тим кращий довгостроковий прогноз. Якщо в цій настанові згадується тривалий контроль захворювання, то це передбачає як мінімум шість місяців ремісії або мінімальної активності захворювання.
Анальгетики і нестероїдні протизапальні засоби (НППЗ), якщо вони не протипоказані, можуть допомогти в полегшенні болю. В межах класу НППЗ є група препаратів, які спочатку розроблялися з урахуванням безпечнішого шлунково–кишкового профілю. До них відносяться інгібітори ЦОГ–2 (циклооксигенази–2). До ГРН звернулися з проханням оновити існуючу технологічну оцінку цих препаратів, однак, оскільки група була повідомлена про те, що в нещодавно опублікованій настанові NICE, присвяченій терапії остеоартрозу (ОА)7, 8, це питання було розглянуто, група вважає, що рекомендації, згадані в нещодавно опублікованій настанові з ОА, можуть також відноситися і до терапії РА.
Традиційні хворобомодифікуючі протиревматичні препарати (DMARD) включають метотрексат, сульфасалазин, гідроксихлорокін, лефлуномід та ін’єкції золота. Ці препарати можуть сприяти уповільненню руйнівного компонента процесу захворювання; проте їх точні механізми дії все ще є об’єктом досліджень.
Коментар робочої групи
Незважаючи на доведену ефективність, препарати золота на сьогодні практично не застосовуються в реальній клінічній практиці через високу частоту побічних ефектів (J.S. Smolen «EULAR RA management recommendations 2013: what is new?» — доповідь на конгресі EULAR 2013). Станом на 01.11.2013 р. препарати золота не зареєстровані в Україні.
Оптимальна послідовність застосування DMARD залишається предметом суперечок, і також дискутується питання про те, чи слід хворим розпочинати лікування з комбінації різних терапій або з одного DMARD. ГРН вважає, що це є значним полем для детального аналізу економіки охорони здоров’я в спробі намагатися визначити, яка стратегія застосування DMARD є найбільш ефективною за витратами.
Була розроблена група препаратів під назвою «біологічні», оскільки вони складаються з моноклональних антитіл і розчинних рецепторів, які специфічно модифікують процес захворювання шляхом блокування молекул ключових білкових месенджерів (таких як цитокіни) або клітин (таких як В–лімфоцити). Розробка біологічних препаратів ґрунтується на дедалі значніших успіхах у розумінні патології захворювання. Ключові драйвери РА включають цитокіни, такі як фактор некрозу пухлини а (ФНП–а), інтерлейкін–1 (ІЛ–1) та інтерлейкін–6 (ІЛ–6). Антагоніст рецептора ІЛ–1 під назвою «анакінр» був оцінений NICE, проте він був відхилений для застосування Національною системою охорони здоров’я, оскільки не є рентабельним9. В процесі розробки цієї настанови до ГРН звернулися з проханням оновити цю технологічну оцінку (див. розділ 7 цієї настанови — «Фармакологічна терапія»).
Крім того, ГРН була повідомлена про те, що при розробці цієї настанови з РА проводилися інші одноразові і численні технологічні оцінки NICE, що стосуються біологічної терапії РА. Цими оцінками NICE є такі:
— Повторна оцінка застосування інгібіторів ФНП–-а при РА (оновлення «Настанови із застосування етанерцепту і інфліксимабу для лікування ревматоїдного артриту»)1. Його було опубліковано в жовтні 2007 р., і з ним можна ознайомитися на сайті www.nice.org.uk/TA 130.
— Застосування ритуксимабу (зниження рівня В–лімфоцитів) для лікування ревматоїдного артриту*7, 10.
— Застосування абатацепту (костимулюючий інгібітор, що попереджає активацію Т–лімфоцитів) для лікування ревматоїдного артриту*7, 11.
— Технологічна оцінка, спрямована на послідовне застосування адалімумабу, етанерцепту та інфліксимабу, застосування цертолізумаб–пеголю і тоцилізумабу для лікування ревматоїдного артриту. Ці результати не були опубліковані під час розробки цієї настанови.
*Див. розділ 10 з приводу формулювання цих рекомендацій.
Коментар робочої групи
Станом на 01.11.2013 р. лікарські засоби Абатацепт та Цертолізумаб в Україні не зареєстровані.
Анакінра — торгова назва лікарського засобу з міжнародною непатентованою назвою Кінерет, який станом на 01.11.2013 р. в Україні не зареєстровано.
1.5. Навантаження на здоров’я й ресурси
Ревматоїдний артрит може призводити до значного ряду ускладнень, що виникають у окремих хворих, осіб, що надають лікарську допомогу, Національної системи охорони здоров’я і суспільства в цілому. Економічний вплив цього захворювання включає:
— безпосередні витрати Національної системи охорони здоров’я і асоційованих служб підтримки охорони здоров’я;
— опосередковані витрати економіки, включаючи ефекти настання ранньої смертності і втрати працездатності;
— персональний вплив РА і наступних ускладнень на хворих та їх сім’ї.
Хоча перебіг РА є неоднорідним і змінним, протягом двох років після встановлення діагнозу хворі починають відчувати помірну непрацездатність, а через 10 років 30 % стають значно непрацездатними. Тривалість життя хворих з РА також скорочується. Наприклад, очікується, що 50–річна жінка з РА помре на чотири роки раніше, ніж 50–річна жінка без РА.
Приблизно одна третина хворих через це захворювання припиняє роботу через два роки після його появи, і ця кількість надалі зростає. Загальні витрати на РА у Великобританії, включаючи опосередковані витрати і витрати на непрацездатність, оцінюються на рівні 3,8–4,75 млрд фунтів стерлінгів на рік12. Дослідження, проведене Національним товариством ревматоїдного артриту, показало, що коли хворий припиняє роботу через РА, то середня втрата продуктивності складає в еквіваленті 287 544 фунтів стерлінгів7, 13. Зрозуміло, що захворювання спричиняє величезні витрати для економіки Великобританії і гігантські витрати для самого хворого.
Коментар робочої групи
Відсутність даних про пов’язані з РА витрати для економіки України та неможливість оцінити економічну ефективність діагностично–лікувальних процедур в умовах вітчизняної системи охорони здоров’я потребують проведення досліджень фінансово–економічної ефективності окремих діагностичних та лікувальних заходів у хворих на РА.
1.6. Життя з РА
ГРН обговорила вплив РА на хворих з пацієнтами — представниками ГРН. Зрозуміло, що РА справляє вплив на більшість сфер життя людини. Сама оголошення діагнозу часто є шоком, а уражені артритом люди занепокоєні якістю життя при зростанні непрацездатності.
Якщо хворого з РА попросити назвати лише один симптом, який викликає найбільшу проблему, то це біль. І не завжди ці страждання можуть викликати співчуття з боку інших людей, особливо на ранніх стадіях захворювання, коли зовнішні прояви можуть бути мінімальними, що може призводити до появи у хворих відчуття ізоляції і депресії. Також складно може виявитися для хворих змиритися з наявністю у них РА і прийняти те, що їх плани на майбутнє, які до встановлення цього діагнозу вважалися їм непорушними, можуть бути значно змінені.
РА потенційно змінює стосунки з іншими людьми, впливаючи на здатність залишатися на роботі, що, таким чином, позначається на фінансовому стані й незалежності хворого та його сім’ї. Обнадійливим є усвідомлення того, що якщо діагноз був поставлений рано, а хворобу лікують із застосуванням ефективної терапії, то вірогідність виникнення непрацездатності є набагато меншою.
4. Направлення, діагностика і обстеження
4.1. Направлення до лікаря–спеціаліста
4.1.1. Клінічний вступ
Ключовий момент ранньої діагностики раннього РА — виявлення синовіту. Це запалення синовіальної оболонки, яка вкриває внутрішню поверхню синовіальних суглобів (більшість суглобів організму). Запалення проявляється безпосередньо болем, набряком, підвищенням температури і втратою функції ураженого суглоба. Суглоби також будуть скутими, неначе рухи у них відбуваються через опір, особливо уранці, але іноді також і ввечері. Інколи суглоби можуть також червоніти, але це не характерно для РА, і один червоний гарячий набряклий суглоб треба завжди лікувати як інфікований, поки не буде доведено протилежне. Розповсюджений синовіт може також викликати системні симптоми запалення, з нездужанням, лихоманкою, пітливістю, втомою і втратою маси тіла. Усі ці симптоми і ознаки можуть бути присутніми меншою або більшою мірою у хворого з раннім РА.
Початковий тригерний механізм для ревматоїдного артриту невідомий. Незалежно від того, що ініціює запалення, це призводить до різкого збільшення кровотоку до суглоба з підвищенням температури в результаті (і інколи почервонінням). Згодом кількість кровоносних судин у синовії помітно збільшується, закріплюючи підвищення температури суглоба. Внутрішня оболонка суглоба складається з клітин, так званих синовіоцитів, і зазвичай їх тільки два–три шари. Половина цих клітин виробляє зволожуючу і поживну синовіальну рідину, яка формує тонкий в’язкий шар у нормальному суглобі. При запаленні збільшення розміру і кількості синовіоцитів, а також синтез синовіальної рідини помітно збільшуються. Така комбінація збільшення кількості синовіальної рідини і проліферації синовіальної оболонки призводить до набряку суглоба, при пальпації відчувається його м’якість. У м’яких тканинах і кістці навколо суглоба є багато рецепторів болю, і їх подразнення набряком та іншими подразниками призводить до болю. Біль та набряк призводить до втрати функції суглоба.
Головне завдання для неспеціалістів — якнайшвидше розпізнати синовіт. Це означає виявлення підвищення температури суглоба, набряку, болю, втрати функції, ранкової скутості та системних особливостей запалення. У контексті ревматоїдного артриту якщо деякі з цих ознак і симптомів наявні в малих суглобах, то поріг виявлення для того, щоб припускати РА, значно знижується. Деякі автори вважають: стискання п’ястково–фалангових або плесне–фалангових суглобів, що спричиняє біль, є достатнім, щоб викликати занепокоєння7, 14.
Колеги з первинної медичної допомоги стикаються з багатьма труднощами у виявленні раннього РА, особливо коли він може спочатку бути представлений значною кількістю варіантів. У багатьох пацієнтів спостерігаються скелетно–м’язові болі і больові відчуття, і навіть докази синовіту, але тільки мала частина прогресуватиме до ревматоїдного артриту. При рівні захворюваності ідіопатичним запальним артритом, що становить приблизно 2 на 10 000 в популяції5, 7, терапевт зі списком хворих 2000 пацієнтів бачитиме один новий випадок РА приблизно кожні 2 роки. Інші проблеми для терапевтів включають:
— необхідність ідентифікувати відносно рідкісний стійкий синовіт у пацієнтів, які потребують невідкладних втручань, з усіх інших дуже частих причин скелетно–м’язового болю;
— нестачу чутливих і специфічних діагностичних аналізів. Якщо у пацієнта дуже швидко розвивається поліартрит, встановлюється клінічний діагноз і розвиваються патологічні результати, а також біль і інвалідність, це зазвичай закінчиться швидким направленням до лікаря–спеціаліста вторинної меддопомоги. Цей тип початку мало поширений, у більшості пацієнтів набагато більш характерний безсимптомний початок або рецидивуючий початок, коли хвороба може наставати і зменшуватися в нападах, перш ніж стати сталою. Тому більшість пацієнтів представляють собою діагностичну дилему на ранніх стадіях хвороби.
Коментар робочої групи
Для ранньої верифікації синовіту (основної ранньої ознаки РА) слід надати можливість лікарям–ревматологам використовувати в клінічній практиці високочутливий та досить простий в технічному виконанні ультразвуковий метод дослідження уражених суглобів (M. Dougados, V. Devauchelle–Pensec, J.F. Ferlet. The ability of synovitis to predict structural damage in rheumatoid arthritis: a comparative study between clinical examination and ultrasound. — Ann. Rheum. Dis. — 2013. — Vol. 72. — P. 5665–5671).
— Лабораторні результати і рентгенологічні дані можуть бути в нормі на ранніх стадіях, навіть у хворих з вірогідним РА, особливо якщо він уражає тільки дрібні суглоби. В більшості випадків ключові навички для ідентифікації — це клінічні можливості виявлення синовіту, що не завжди є достовірним, навіть для спеціалістів.
— Деякі пацієнти зі стійким раннім синовітом можуть отримати користь від НППЗ або анальгезуючих засобів, але це може спонукати як пацієнта, так і терапевта до помилкового почуття безпеки відносно впливу, який ліки справляють на хворобу.
Ще однією проблемою у пацієнтів з раннім синовітом, що отримують лікування, є затримка людини з симптомами, яка представляє їх терапевтові вперше. Останні дослідження припустили, що це складає велику частину затримок у хворих з РА, які бачать спеціаліста вперше, при порівнянні з затримками до огляду людини терапевтом15. Люди з синовітом можуть накопичувати порушення в суглобах до огляду будь–яким представником медичної професії, і тому інформаційна кампанія охорони здоров’я зобов’язана звернути на це увагу. Проте терапевти можуть все ще затримати направлення до лікаря–спеціаліста, тому що симптоми можуть бути невизначеними, або ознаки синовіту важко ідентифікувати, або позитивні реакції на анальгезуючі засоби і НППЗ призводять до помилкового почуття безпеки. В іншому місці в цій настанові буде зроблено посилання на потребу ініціювати DMARD в 3–місячному вікні можливостей, яке забезпечить величезну різницю в довготривалих результатах (див. розділ 7.3.13). Це висуває на перший план потребу в:
— ознайомленні широкого загалу із симптомами і ознаками синовіту так, щоб вони могли відвідати свого терапевта раніше, і
— продовженні спроби закріпити у терапевтів (та інших лікарів, які можуть зустріти ранній РА, таких як травматологи) необхідність у швидкому направленні до лікаря–спеціаліста.
Ці проблеми обумовлюють такі запитання:
— Чи існують будь–які клінічні особливості симптомів або ознак запального артриту, де повинні реєструватися прогностичні проблеми, і пацієнт буде швидко направлений для надання вторинного медобслуговування?
— Якщо такі ознаки і симптоми очевидні, чи існують будь–які дані, щоб запропонувати часові межі для такого направлення до лікаря–спеціаліста?
4.1.2. Клінічний методологічний вступ
Ми проводили пошук досліджень, в яких досліджувалися клінічні симптоми, які повинен розпізнати неспеціаліст, щоб звернутися за медобслуговуванням до спеціаліста, і те, як швидко направлення до лікаря–спеціаліста має відбутися з огляду впливу на симптоми, порушення суглобів, функцію і якість життя в пацієнтів із раннім недиференційованим запальним артритом. Були вибрані усі типи дослідження з популяцією, відповідною британській.
Були знайдені тринадцять досліджень15–27, які відповідали критеріям. Усі дослідження були перевірені методологічно. Деякі з досліджень були діагностичними дослідженнями, і в них був елемент прогностичного дизайну; вони оцінювали, на підставі яких клінічних симптомів можна було визначити пацієнтів, у яких продовжував розвиватися РА (і відповідали критеріям Американської колегії ревматологів (ACR)), по завершенні принаймні одного року після того, як аналіз був виконаний.
Клінічні симптоми
Були знайдені одне когортне дослідження16 і 12 досліджень серії випадків (проспективних)17–25, 28, 29, які відповідали критеріям, за клінічними симптомами яких неспеціаліст повинен розпізнати направлення до вузького спеціаліста. Усі дослідження були перевірені методологічно.
Когортне дослідження16 розглядало на предмет клінічних симптомів пацієнтів (N = 474) з артритичними симптомами, які відвідували клініку раннього артриту порівняно із звичайною клінікою, і спостереження за цими пацієнтами здійснювалося протягом 1 року.
12 досліджень серії випадків розглядали на предмет клінічних симптомів пацієнтів з раннім запальним артритом, і в деяких дослідженнях спостереження за цими пацієнтами здійснювалося для контролю особливостей тих із них, у кого продовжував розвиватися РА. Дослідження відрізнялися відносно:
— об’єму вибірки (діапазон: від N = 41 до N = 903)
— тривалості дослідження (діапазон: час не вказаний, 1–8 років).
Вибір часу направлення до лікаря–спеціаліста
Було знайдено три ретроспективні дослідження серії випадків15, 26, 27, які розглядали оптимальний вибір часу направлення до лікаря–спеціаліста у пацієнтів з РА. Перше дослідження серії випадків26 розглянуло вплив раннього порівняно із пізнім направленням до лікаря–спеціаліста у пацієнтів (N = 200). Друге дослідження серії випадків27 розглянуло вплив затримки направлення до лікаря–спеціаліста і запуску терапії DMARD у пацієнтів (N = 198). Третє дослідження серії випадків15 розглянуло затримку за часом направлення до лікаря–спеціаліста і причини затримки пацієнтів (N = 169).
4.1.3. Методологічний вступ для економічних показників лікування
Досліджень з економічними показниками лікування знайдено не було.
4.1.4. Оцінка клінічних даних
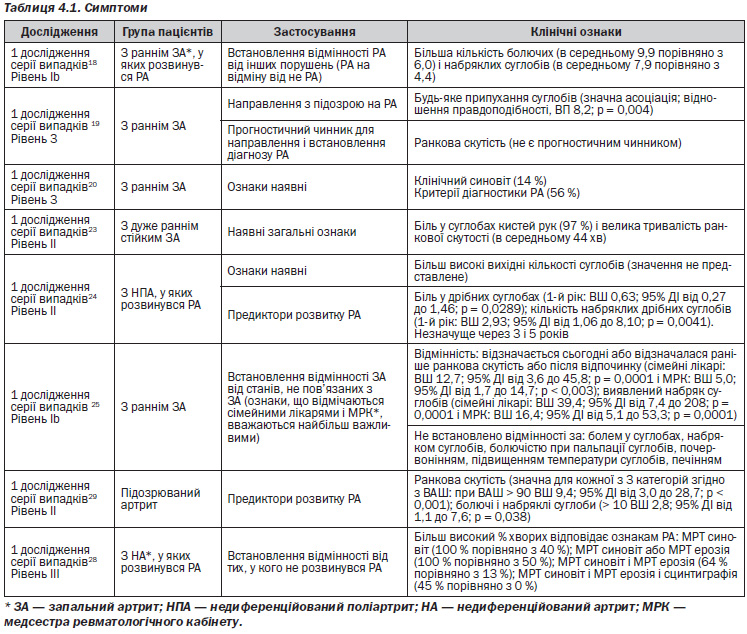
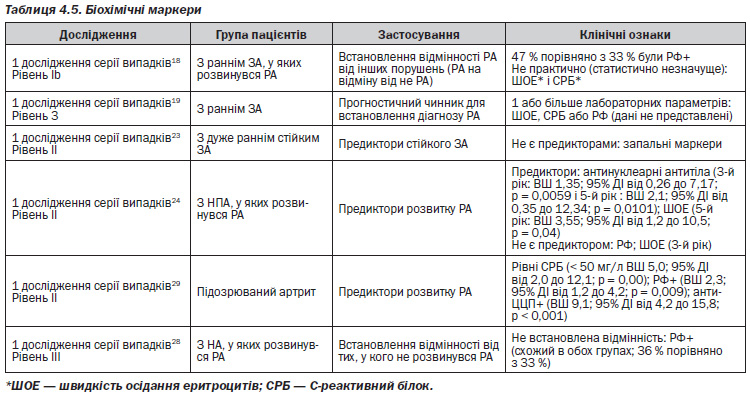
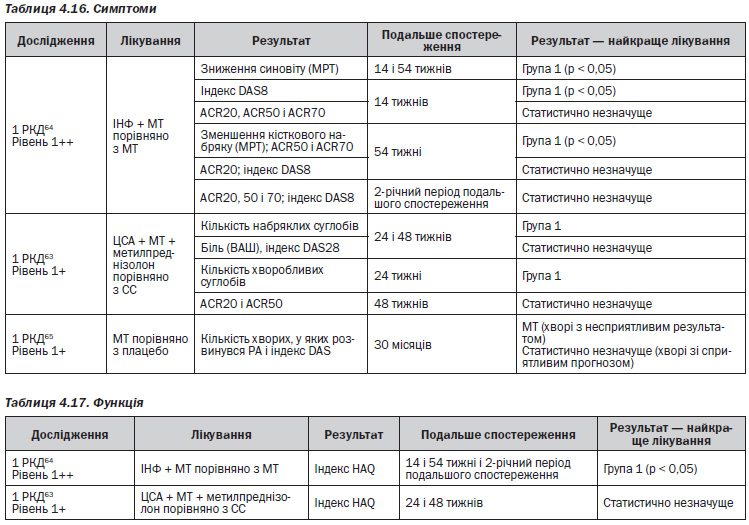
Клінічні ознаки (табл. 4.1)
В одному дослідженні серії випадків15 було виявлено, що чинники, які залежать від пацієнта (такі як затримка часу від появи симптомів до оцінки при проведенні первинної медичної допомоги), призводять до пізнього звернення до лікаря, який надає первинну медичну допомогу, і є основною причиною затримки проведення обстеження хворих з РА ревматологами.
Коментар робочої групи
Робоча група вважає, що найбільш частою причиною затримки надання адекватної мед. допомоги хворим на РА в Україні є пізнє звертання хворого до лікаря первинної ланки, зволікання з направленням до фахівця–ревматолога та застосування глюкокортикоїдів при невстановленому діагнозі.
4.1.5. Резюме оцінки даних
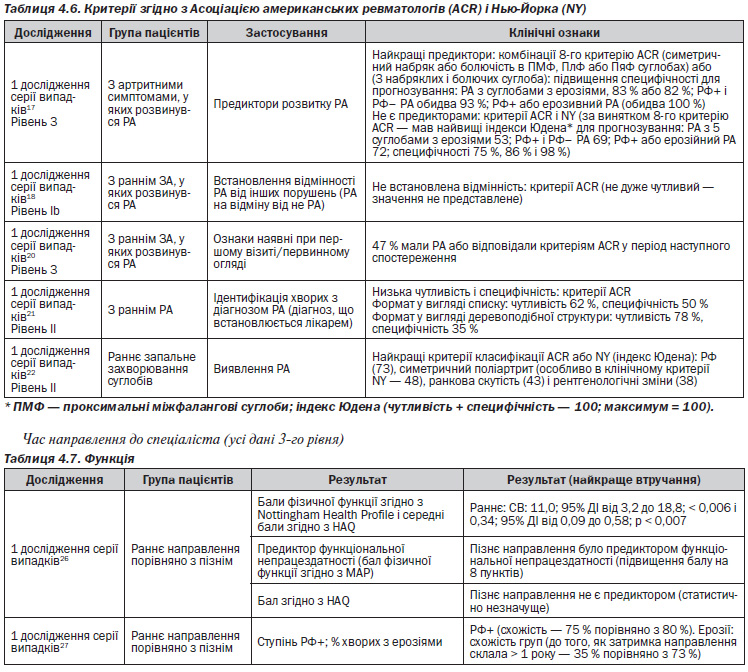
— Критерії ACR ідентифікують хворих, у яких, ймовірно, є стійкий синовіт, і хворих з несприятливим прогнозом, проте вони не ефективні як діагностичні критерії при ранньому РА17, 18, 20–22.
— Ключові клінічні ознаки, які полегшують ідентифікацію хворих, у яких, ймовірно, є стійкий синовіт, і хворих з несприятливим прогнозом, включають:
– кількість уражених суглобів (чим більше таких суглобів, тим гірше прогноз)18, 22;
– наявність одночасно припухання і болючості в уражених суглобах (особливо в дрібних суглобах)18, 19;
– позитивний результат тесту на стискування ПяФ суглобів23;
– ураження ПМФ і ПяФ суглобів23 і симетричність ураження суглобів.
— Нездатність стискати руку в кулак або згинати пальці була пов’язана з можливістю розпізнати РА і відрізнити його від інших діагнозів в одному дослідженні19. Постійне відчуття тривалої ранкової скутості є більш практичною ознакою, ніж наявність ранкової скутості в поточний час для діагностики раннього РА23.
— Ревматоїдний фактор виявляється менше ніж у половини хворих з РА на момент первинного огляду18.
— Гострофазові показники у хворих із запальним артритом, який розвивається в РА, не відрізняються від тих, які відзначаються при запальному артриті, який розвивається в інше захворювання (не РА)23.
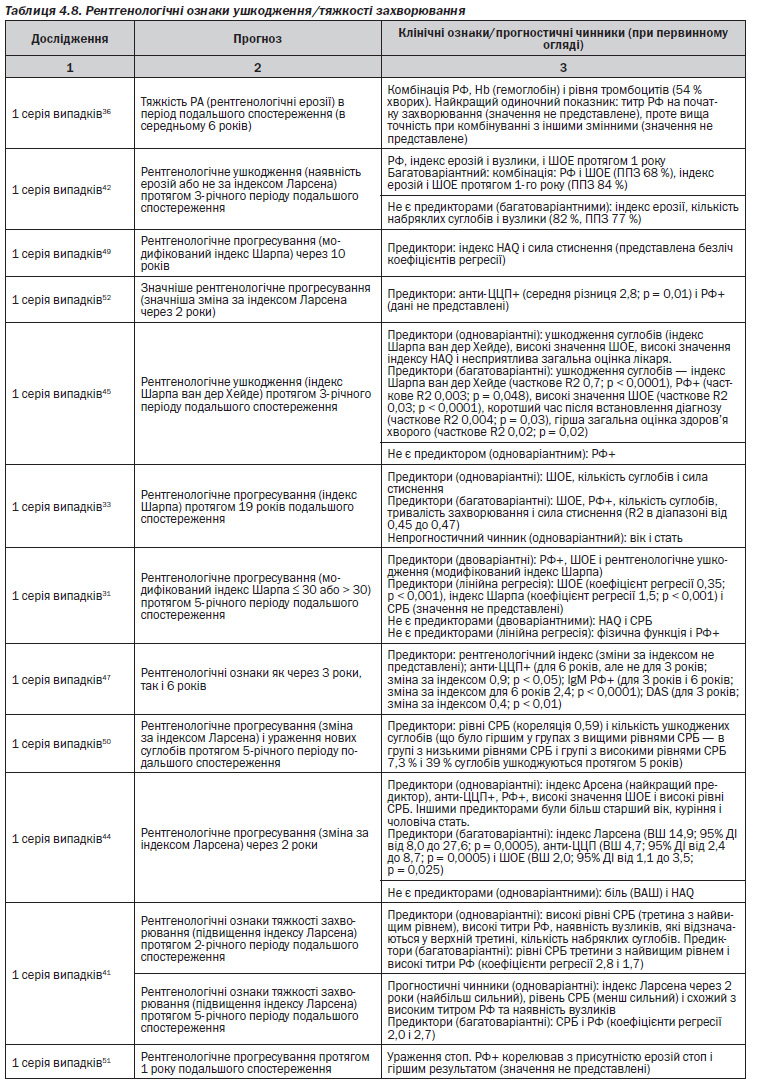
— Затримки при направленні пов’язані з гіршою функцією при первинному огляді28, а якщо затримка складає 1 рік, то спостерігається збільшення ерозивних змін на рентгенограмі27.
— Найбільш значним чинником затримки початку прийому DMARD була затримка із зверненням до ревматолога27.
— Факти свідчать, що найбільша затримка у хворих, що звертаються за лікарською допомогою до спеціалістів, відзначається скоріше у хворих, які спочатку відвідують свого сімейного лікаря з симптомами, порівняно із затримкою у хворих, які направляються сімейним лікарем до спеціаліста15.
4.1.6. Від доказів до рекомендацій
Група з розробки цієї настанови вважає, що діагностика РА повинна ґрунтуватися на клінічних даних, таких як історія і обстеження, причому корисними іноді є й дослідження. Діагностика не повинна обмежуватися критеріями класифікації ACR, які є непотрібними при ранньому захворюванні. Вважається, що критерії ACR є більше прогностичними, ніж діагностичними, для раннього запального артриту. Іншими словами, якщо хворий приходить із захворюванням дрібних суглобів, то це є несприятливим прогнозом, і його слід негайно направити на огляд до спеціаліста. Те саме стосується кількості уражених суглобів, коли дані свідчать, що чим більша їх кількість, тим гірший прогноз, і, отже, існує більш висока необхідність в ранній ідентифікації і в ранньому направленні до спеціаліста. Найбільш значною ознакою раннього РА є клінічне виявлення синовіту. Це є клінічною навичкою, а при ранньому РА усі аналізи крові можуть бути в нормі, не дивлячись на сильно інвалідизуюче захворювання. Таким чином, вважається важливим, щоб на цей сигнал було звернено увагу, і що навіть при нормальних результатах обстеження сімейним лікарям слід негайно направляти хворих на отримання вторинної медичної допомоги. Було визнано, що існують факти, які свідчать про те, що основна затримка, пов’язана з направленням за медичною допомогою до спеціаліста, часто перебуває за межами контролю сімейного лікаря, і це пов’язано з тим, що хворий сам не звертається негайно за медичною допомогою, коли симптоми тільки починають з’являтися. Враховуючи той факт, що ця затримка підвищує ризик ушкодження суглобів і затримує початок прийому DMARD, хворі, які звертаються до свого сімейного лікаря з розгорнутою стадією захворювання, повин–ні негайно направлятися за медичною допомогою до спеціаліста, щоб спробувати мінімізувати будь–яке подальше ушкодження суглобів, особливо якщо симптоми вже були наявні протягом більше трьох місяців.
Рекомендації
R1 Направляйте на огляд до спеціаліста будь–якого хворого з підозрою на стійкий синовіт невизначеної етіології. Також направляйте до спеціаліста, якщо спостерігається будь–яка ознака з перелічених нижче:
— уражені дрібні суглоби кистей і стоп;
— уражено більше одного суглоба;
— затримка 3 місяці або довше між настанням симптомів і зверненням за медичною допомогою.
R2 Не сумнівайтеся з негайним направленням будь–якого хворого з підозрою на стійкий синовіт невизначеної етіології, результати аналізу крові якого показують нормальну відповідь гострої фази або негативний ревматоїдний фактор.
4.2. Наявні симптоми і ознаки
4.2.1. Вступ до клініки
Термін РА відноситься до дуже широкого спектра захворювань. У разі раннього РА у деяких хворих відбувається швидке настання хвороби і її швидкий розвиток до поліартриту. У інших відбувається прихований розвиток і може минути декілька місяців до того, як моно– або олігоартрит поступово розвинеться в симетричну периферичну картину. У хворих з раннім РА і з розгорнутою стадією захворювання можуть спостерігатися позасуглобові ознаки, які впливають на важкість захворювання і пов’язану з ним непрацездатність, наприклад інтерстиційне захворювання легень і васкуліт. У інших можуть бути відсутніми очевидні позасуглобові прояви, або вони можуть бути відносно легкими, проте дратуючими, наприклад сухість очей. Доцільно ідентифікувати хворих з вірогідним несприятливим прогнозом на ранніх стадіях перебігу захворювання. За цими хворими потім слід ретельніше спостерігати, щоб мати нижчий поріг інтенсивного втручання для зміни перебігу їх агресивного захворювання. Навпаки, у хворих, у яких відсутні маркери несприятливого прогнозу або у яких наявні маркери сприятливого прогнозу, може застосовуватися менш інтенсивна стратегія подальшого спостереження і лікування. Чи існують маркери, які могли б допомогти зробити терапію більш цільовою, залежно від прогнозу перебігу захворювання?
4.2.2. Вступ до клінічної методології
Ми провели пошук досліджень, що стосуються того, які клінічні ознаки хворих з РА (рання і розгорнута стадії захворювання) можуть застосовуватися для ідентифікації цих хворих із сприятливим або несприятливим прогнозом. Через великий обсяг даних про прогностичні чинники відбиралися ті дослідження, які охоплювали британське населення; якщо в популяції був змішаний артрит, то в ній має бути > 75 % РА, або проводився аналіз підгрупи з РА, при цьому розмір вибірки N > 200. Ми також провели пошук досліджень, в яких оцінювали, яке лікування є найкращим для хворих з несприятливим прогнозом; жодні обмеження не встановлювалися для відбору критеріїв, за винятком того, що популяція має бути британською.
Була отримана інформація про 33 дослідження серії випадків, які відповідали критеріям включення. Усі дослідження були методологічно правильними і оцінювали клінічні ознаки хворих з РА, які мали або сприятливі або несприятливі прогностичні наслідки (або за пацієнтами спостерігали проспективно, або дані збиралися ретроспективно).
Ранній РА
Була отримана інформація про 23 дослідження серії випадків30–52, які відповідали критеріям. Вони відрізнялися:
— розміром вибірки (діапазон: від N = 211 до N = 1387);
— тривалістю дослідження (діапазон: від 1 року до 43 років).
Розгорнута стадія РА
Була отримана інформація про 10 досліджень серій випадків53–62, які відповідали критеріям. Вони відрізнялися:
— розміром вибірки (діапазон: від N = 263 до N = 2448);
— тривалістю дослідження (діапазон: від 6 місяців до 50 років).
Лікування хворих з несприятливим прогнозом
Була отримана інформація про 3 рандомізовані контрольовані дослідження (РКД)63–65 і 1 когортне дослідження66, 67, які відповідали критеріям, за якими обиралося найкраще лікування для пацієнтів з РА з несприятливим прогнозом. Усі дослідження проводилися на хворих з НА або з раннім РА. Когортне дослідження66, 67 було опубліковано у вигляді двох окремих робіт з різним часом подальшого спостереження, і тому воно вважалося одним дослідженням. Проте ми представили результати обох робіт, і на них дано посилання.
Три РКД63–65 були дослідженнями в паралельних групах. В перших двох РКД63, 64 проводилося дослідження лікування із застосуванням DMARD (окремо порівняно з комбінацією) у хворих з раннім РА з несприятливим прогнозом (N = 82 і N = 20 відповідно). У першому РКД63 проводилося порівняння двох різних груп лікування: сульфасалазин (СС) 500 мг/день проти циклоспорину А (ЦСА) 1,5 мг/кг/день + Метотрексат (МТ) 7,5 мг/тиждень + глюкокортикоїд (ГК) метилпреднізолон протягом 48–тижневої фази лікування. У другому РКД64 проводилося порівняння двох різних груп лікування: МТ 7,5 мг/тиждень + плацебо проти МТ 7,5 мг/тиждень + інфліксимаб (ІНФ) 3 мг/кг/день протягом фази лікування упродовж 1 року з періодом наступного спостереження упродовж 1 року після лікування. У третьому РКД65 проводилося дослідження лікування із застосуванням DMARD в групі, що складається з 110 хворих з НА, з яких у 51 людини розвинувся РА. У цьому дослідженні проводилося порівняння двох різних груп лікування: МТ проти плацебо протягом 30–місячної фази лікування, а також виконувався підгруповий аналіз результату у пацієнтів у кожній групі, у яких був несприятливий прогноз (анти–ЦЦП+ або РФ+). Методологічними обмеженнями РКД були: ті, що були класифіковані як 1+, були або відкритими односторонніми сліпими, або в них не проводився аналіз ITT (бажання лікуватися). Дослідження, класифіковане як 1++, було подвійним сліпим, і автори провели аналіз ITT.
У когортному дослідженні66, 67 вівся пошук найкращого способу лікування серед N = 206 хворих з раннім РА з несприятливим прогнозом. У цьому дослідженні проводилося порівняння двох різних груп лікування: раннє лікування (DMARD + НППЗ) порівняно з відстроченим лікуванням (НППЗ, а потім DMARD) протягом 4–річної фази лікування.
4.2.3. Вступ до методології економіки здоров’я
Було сформульовано два питання, оскільки терміни пошуку були дуже схожими. Було знайдено 144 тези, серед яких 142 не відносилися конкретно до ревматоїдного артриту. Дві інші були замовлені у вигляді повних робіт, проте згодом виявилось, що вони не відповідають критеріям включення (вони не були економічною оцінкою). Одна робота68 була опублікована в режимі онлайн вже після проведення пошуку і була знайдена членом групи з розробка настанови. Вона відповідала критеріям включення і тому була розглянута.
4.2.4. Оцінка клінічних даних
Ранній РА (усі дослідження 3–го рівня)
4.2.5. Оцінка даних щодо медичної економіки
Не було знайдено економічної оцінки в британській популяції. Konnopka et al.68 в одному голландському дослідженні оцінювали застосування тестування на антитіла до ЦЦП порівняно з діагностикою РА з використанням критеріїв ACR. Проте ця модель містить дані, які були отримані не шляхом застосування будь–якого формального огляду фактів, а з використанням моделі Маркова, і загалом погано пояснені. Припущення про вплив пізнього встановлення діагнозу на прогресування HAQ викликає сумніви, а при варіюванні від 0,01 до 0,15 призводить до варіювання за показником ICER від переважання до більше ніж 153 євро на 1 QALY. Початкові результати оцінюють ICER на рівні 930 євро на 1 QALY, хоча відмінності за вартістю між стратегією аЦЦП і стратегією ACR (15 010 євро і 14 995 відповідно) і відмінність по QALY між стратегією аЦЦП і стратегією ACR (7 1237 QALY і 7 1073 QALY) є відносно невеликими.
4.2.6 Резюме даних доказової медицини
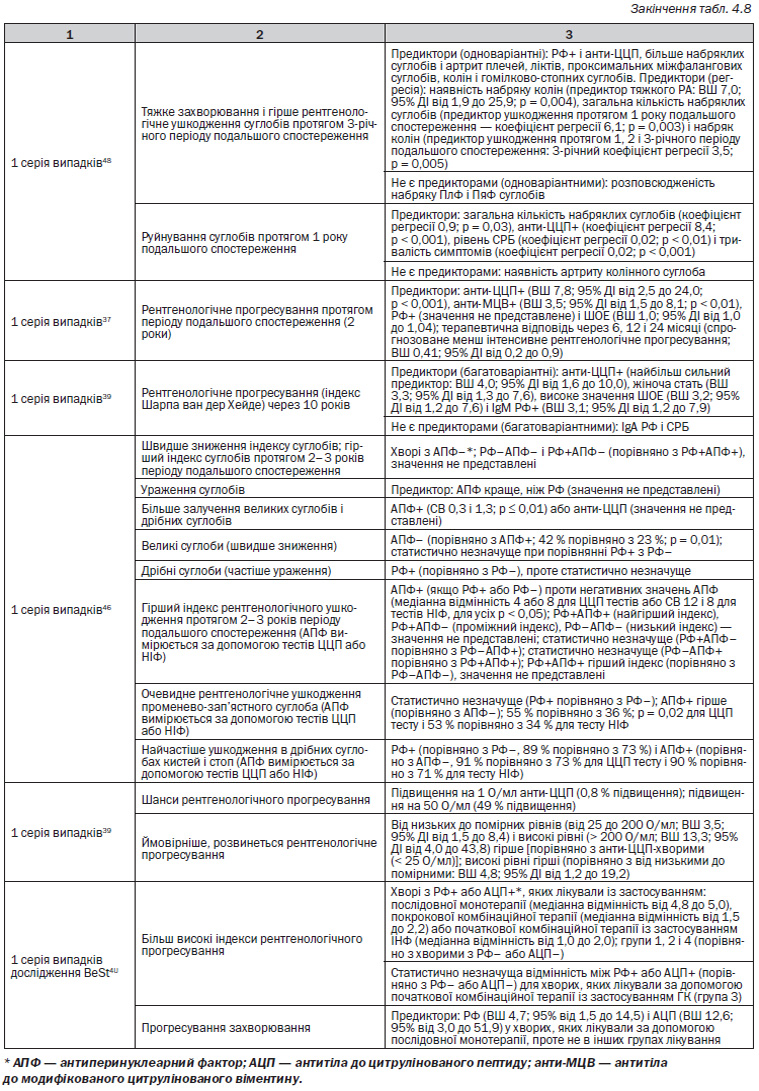
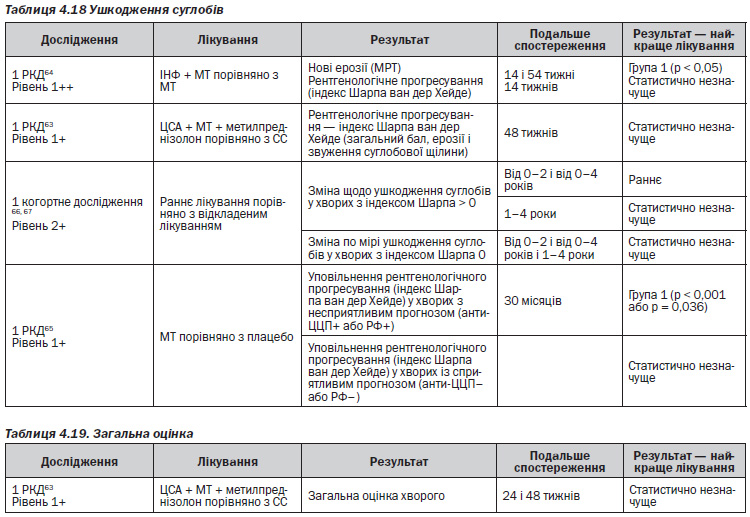
Більшість досліджень раннього захворювання спрямовані на рентгенологічні результати впродовж варіабельних періодів подальшого спостереження. Розглядаються такі теми:
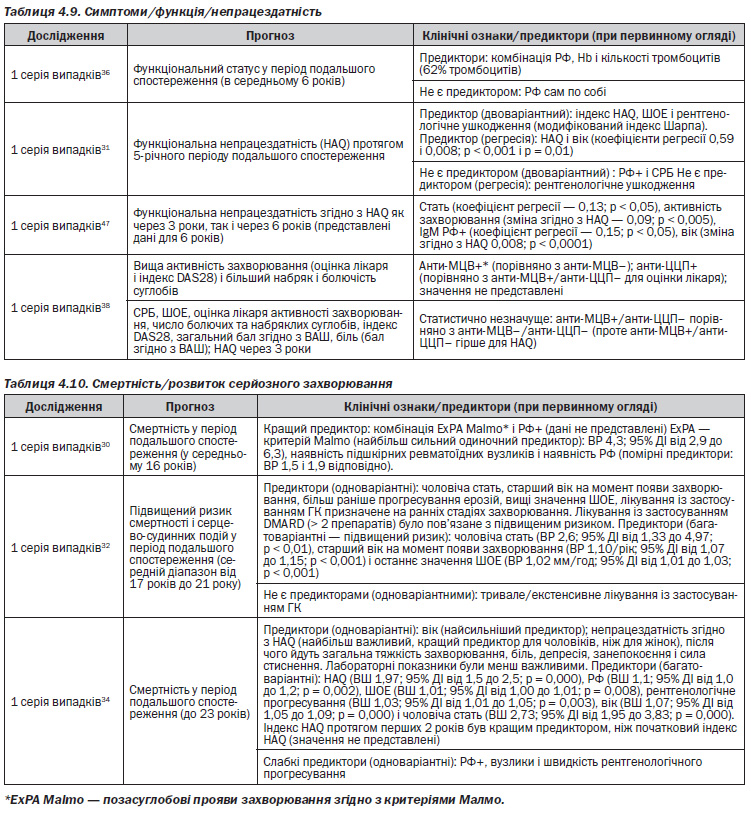
— Титр РФ визначається постійно як вірогідний предиктор прогнозу (для рентгенологічних і функціональних показників) у більшості досліджень31, 33, 36, 41–44, 47, 48, 51, 52.
— Позитивність за антитілами до ЦЦП є предиктором прогнозу44, 48, 52.
Доведено їх взаємодії з РФ, таким чином, для пацієнтів, позитивних за РФ та антитілами до ЦЦП, прогноз найгірший, в той час як найкращий прогноз визначається для пацієнтів, негативних за обома антитілами; проміжний прогноз — для пацієнтів, позитивних тільки за одним типом антитіл46. Інші змінні показники, які, як виявилося, використовують для прогнозування в більш ніж одному дослідженні, включають:
— вихідний рентгенологічний індекс31, 42, 44, 45, 47;
— вузлики42;
— гострофазові показники31, 33, 41, 42, 45, 48, 50;
— показник HAQ43, 45, 49 (HAQ — опитувальник оцінки стану здоров’я);
— сила стиснення33, 49;
— кількість набряклих суглобів33, 41, 48.
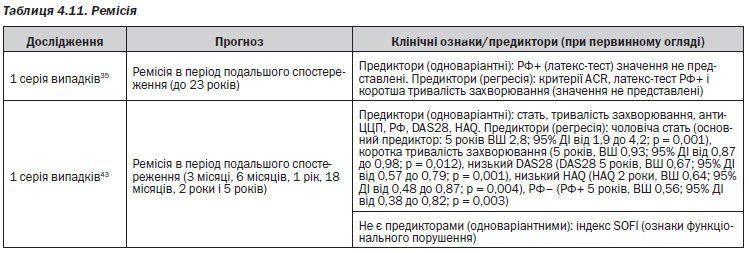
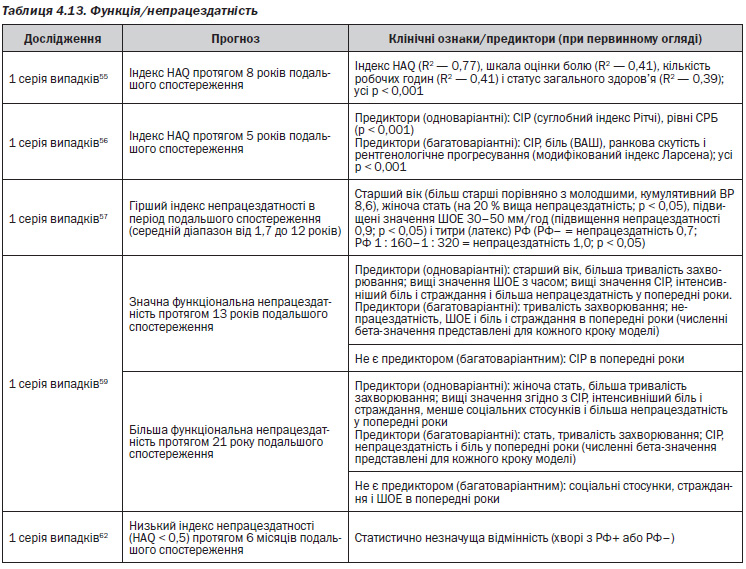
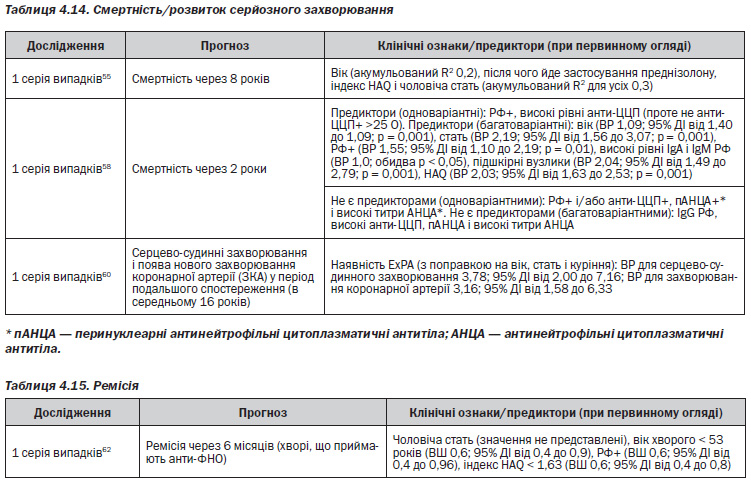
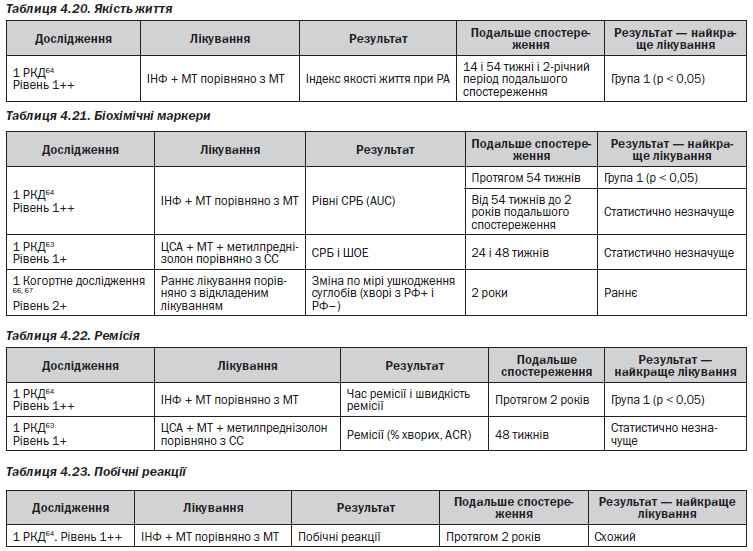
У дослідженнях розгорнутої стадії хвороби вивчали сукупність функціональних і рентгенологічних наслідків. Основні теми такі:
— Недієздатність або інвалідність прогнозується:
– за вихідним показником недієздатності55, 57, 61;
– похилим віком57–59;
– більшою тривалістю захворювання57–59, 61;
— У жінок, як правило, спостерігаються гірші результати, ніж у чоловіків57, 58.
— Жодне з досліджень не вивчало, чи слід лікувати пацієнтів із поганим прогнозом іншим чином.
4.2.7. Від доказів до рекомендацій
ГРН (група з розробки настанови) відмітила, що в даний час не існує універсального тесту для визначення антитіл до ЦЦП. Дані доказової медицини свідчать, що антитіла до ЦЦП доповнюють інформацію до визначеного попередньо ревматоїдного фактору, коли мова йде про прогноз, причому комбінація позитивного ревматоїдного фактору та антитіл до ЦЦП пов’язана з особливо поганим прогнозом. Однак доки не існує доказів, що для групи з поганим прогнозом, яка була ідентифікована таким чином, може знадобитися інша тактика лікування, доти це не буде підтверджувати рекомендацію стандартного використання визначення антитіл до ЦЦП у позитивних за ревматоїдним фактором пацієнтів. Також відмічалося, що визначення антитіл до ЦЦП може використовуватися у хворих, позитивних за ревматоїдним фактором, але клінічна картина яких не нагадує ревматоїдний артрит. За таких обставин позитивний тест на антитіла до ЦЦП може вказувати на те, що індивідуум має ризик розвитку РА в майбутньому і, таким чином, заслуговує на ретельне подальше спостереження. Однак на даний час існують лише обмежені дані щодо цієї групи хворих, і ГРН погоджується, що рекомендації були б передчасними.
ГРН погоджується з тим, що дані доказової медицини вказують на те, що визначення антитіл до ЦЦП може бути дуже ефективним для хворих, які серонегативні за ревматоїдним фактором і у яких первинним лікуванням має бути інтенсивна комбінована терапія (див. рекомендацію 16). У такої групи хворих, які можуть відмовитись від початку інтенсивної терапії під час виникнення стійкого синовіту без додаткових специфічних тестів для діагностики та прогнозу, позитивність на антитілами до ЦЦП може використовуватися для отримання їх рішення щодо прийому рекомендованої терапії. ГРН зробила висновок, що для даної групи пацієнтів доцільною буде специфічна консенсусна рекомендація, однак для введення розповсюдженого визначення антитіл до ЦЦП в інших групах буде необхідна наявність переконливого доказу економічної ефективності, що має сформувати основу для розробки рекомендацій.
Рекомендації
R3 Розглянути виявлення антитіл до циклічного цитрулінового пептиду (ЦЦП) у хворих із передбачуваним ревматоїдним артритом (РА), якщо:
— вони є негативними за ревматоїдним фактором, і
— існує необхідність прийняття обґрунтованих рішень про початок комбінованої терапії (див. рекомендацію 16).
4.3. Дослідження
4.3.1. Клінічне введення
Ідентифікація стійкого синовіту є головним чином вмінням та навичкою клініциста. Однак існують такі дослідження, які можуть допомогти довести, що є порушення, які вимагають втручання. Деякі з них можуть бути неспецифічні, такі як ознаки запалення, що триває (наприклад, підвищений рівень С–реактивного білка (СРБ), анемія хронічного захворювання), в той час як інші можуть бути більш корисними для підтвердження діагнозу (наприклад, високі титри ревматоїдного фактора, ерозивні зміни на рентгенівських знімках). Деякі дослідження допомагають виключити інші причини поліартриту або поліартралгії, такі як тести на функцію щитоподібної залози. Інші дослідження корисні у визначенні первинного статусу хворого, який допомагає визначити тактику та підхід до лікування, наприклад, тести на функцію нирок і печінки до початку прийому нестероїдних протизапальних засобів (НППЗ) або базисних препаратів для лікування ревматоїдного артриту (DMARDs). У цьому розділі особлива увага приділяється тим тестам, які допомагають розпізнати захворювання на ранній стадії, але потрібно мати на увазі, що вони не замінюють необхідність ретельного вивчення історії хвороби та обстеження, і навіть якщо результати всіх тестів нормальні, це не повинно перешкоджати відповідному втручанню у дослідження пацієнтів зі стійким синовітом. Антитіла до циклічного цитрулінованого пептиду (анти–ЦЦП) виявилися в останні роки такими ж чутливими, але більш специфічними, ніж ревматоїдний фактор в діагностиці РА. Вони розглядаються в розділі 4.3 (наявні ознаки та симптоми). Існують підстави вважати, що ультразвукове дослідження та магнітно–резонансна томографія (МРТ) перевершують клінічне обстеження щодо виявлення синовіту і що вони більш чутливі до наявних ерозій та інших ранніх ознак запалення та уражень, ніж звичайні рентгенівські знімки69, 70. Однак тривала значущість отриманих результатів дослідження, а також обмежена доступність для багатьох лікарів обмежує їх використання, залишаючи виявлення синовіту для клінічного обстеження в якості золотого стандарту.
4.3.2. Клінічне методологічне введення
Ми шукали дослідження, які оцінюють можливість процедур дослідження виявляти пацієнтів з недиференційованим запальним артритом, який би в подальшому трансформувався в ревматоїдний артрит (РА). У зв’язку з великим обсягом доказів були відібрані дослідження відповідної групи населення Великобританії, пацієнти мали пре–РА(pre–RА)/недиференційований артрит, якщо в популяції був змішаний артрит, то в ній мало бути > 75 % РА, або проводився аналіз підгрупи з РА, при цьому розмір вибірки N > 50 (за винятком МРТ або УЗД досліджень). Відібрані дослідження були діагностичними дослідженнями, але з елементом прогностичного дизайну; вони оцінювали здатність дослідницьких тестів виявити пацієнтів, у яких продовжував розвиватися ревматоїдний артрит (відповідно до критеріїв ACR) принаймні через 1 рік після проведеного дослідження.
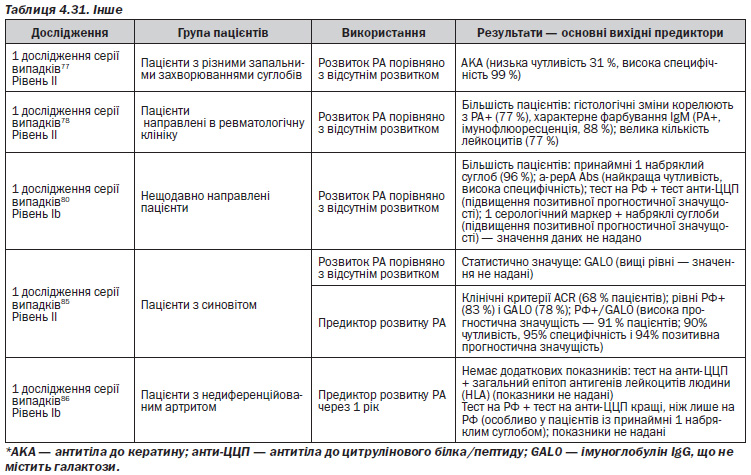
Було знайдено два метааналізи (МА)71, 72, 3 дослідження типу «випадок–контроль»73–76 і 12 досліджень серії випадків29, 35, 77–86, що відповідали критеріям. Одне з досліджень типу «випадок–контроль» було опубліковано у вигляді двох окремих наукових статей74, 75, в яких наводились різні результати, і тому дослідження враховувалось лише один раз. Однак тут наводяться результати обох наукових статей і даються посилання на них. Не було знайдено ніяких досліджень з використанням УЗД. Дослідження серії випадків і дослідження типу «випадок–контроль» були включені в додаток до метааналізу, оскільки ці дослідження не з’явилися в метааналізі або були опубліковані після дати закінчення терміну пошуку МА. Три з них з’явилися в метааналізі та були включені, оскільки вони містили результати, які не були включені в МА.
Метааналізи
Перший метааналіз71 концентрував увагу на всіх дослідженнях, у яких визначали антитіла до ЦЦП для діагностики ревматоїдного артриту (РА), і включав 68 досліджень з даними. З них 14 досліджень розглядали процедури дослідження, які прогнозують розвиток РА (11 включали пацієнтів із недиференційованим артритом і 3 включали пацієнтів з РА, які здали кров до розвитку РА). Сам метааналіз проводився належним чином, однак не проводилося жодного тесту на гетерогенність. Всі дослідження, що були включені в аналіз, використовували однаковий метод виявлення антитіл до ЦЦП (ELISA); однак вони відрізнялися щодо:
— типу дослідницького тесту, який використовувався (5 досліджень використовували антитіла до ЦЦП1, 10 досліджень використовували антитіла до ЦЦП2);
— діапазону для антитіл до ЦЦП (діапазон для антитіл до ЦЦП1 складав від 21,4 МО до 1000 МО, діапазон для антитіл до ЦЦП2 складав від 3,8 МО до 50 МО);
— масштабу дослідження (1327 пацієнтів із недиференційованим артритом для виявлення антитіл до ЦЦП; 2017 пацієнтів із недиференційованим артритом для виявлення антитіл до ЦЦП2; 79 пацієнтів із ревматоїдним артритом, які здали кров до розвитку РА для виявлення антитіл до ЦЦП1 і 142 — для виявлення антитіл до ЦЦП2);
— тривалості дослідження — тривалості подальшого лікарського спостереження (пацієнти з недиференційованим артритом: діапазон 5–36 місяців; пацієнти з РА, які здали кров до розвитку РА, — діапазон від < 1,5 року до 9 років).
Другий метааналіз72 розглядав діагностичну точність виявлення антитіл до ЦЦП і виявлення ревматоїдного фактору (РФ) у пацієнтів із раннім РА (тривалість < 1 року), і включав 87 досліджень. З них 37 досліджень розглядали виявлення антитіл до ЦЦП і 50 — виявлення ревматоїдного фактору. Дослідження відрізнялися щодо:
— масштабу дослідження (діапазон не вказаний);
— дизайну дослідження (проспективне в 18/37 для антитіл до ЦЦП та 25/50 для ревматоїдного фактору);
— якості дослідження — максимальний бал 5 (1 — дуже гарна якість, 22 — 30% прийнятна якість, 9 — 10 % погана якість);
— тривалості дослідження — тривалості подальшого лікарського спостереження (діапазон не вказаний);
— груп порівняння (головним чином пацієнти з недиференційованим артритом; здорові пацієнти; пацієнти з іншими хворобами; інші ревматичні захворювання);
— втручання — типу виявлення антитіл до ЦЦП (антитіла до ЦЦП1 — 8; антитіла до ЦЦП2 — 29);
— втручання — типу тесту на ревматоїдний фактор (IgM, IgA, IgG).
Дослідження типу «випадок–контроль»
3 дослідження типу «випадок–контроль»73–76 розглядали дослідницькі тести, які можуть бути використані для прогнозування розвитку РА у пацієнтів із недиференційованим артритом. Перші два дослідження типу «випадок–контроль»73–75 розглядали дослідницькі тести (антитіла до ревматоїдного фактору та антитіла до філагрину (AFA), антитіла до ЦЦП, РФ і колагену відповідно) у хворих, які знаходилися під ризиком розвитку РА (в обох N = 19,072). У дослідженнях порівнювалися випадки (ті, у кого продовжував розвиватися РА) з аналогічною контрольною групою (ті, у кого не розвивався РА), подальше лікарське спостереження проводилося протягом 22 років або від 12 до 16 років відповідно. У третьому дослідженні «випадок–контроль»76 розглядалися дослідницькі тести (РФ і AFA) у 330 пацієнтів із недиференційованим артритом. У дослідженні порівнювалися випадки (ті, у кого продовжував розвиватися РА) з аналогічною контрольною групою (пацієнти, які вже були хворі на РА), подальше лікарське спостереження проводилося протягом 1 року.
Дослідження серії випадків
12 досліджень серії випадків29, 35, 77–86 розглядали дослідницькі тести та процедури, які можуть бути використані для прогнозування розвитку РА у пацієнтів із преревматоїдним артритом/недиференційованим артритом. Дослідження відрізнялися щодо:
— об’єму вибірки (діапазон: від N = 30 до N = 1003);
— тривалості дослідження (діапазон: в середньому від 1 року до 6,9 року);
— процедури дослідження/використовуваний тест (РФ, антитіла до ЦЦП, ACPA (антитіла до цитрулінового білка/пептиду), СРБ (С–реактивний білок), APF (антиперинуклеарний фактор), ШОЕ (швидкість осідання еритроцитів), МРТ, симптоми, рентгенограми, гістопатологія, критерії ACR (Американської колегії ревматології) та інше).
4.3.3. Медичне економічне методологічне введення
Не виявлено медико–економічних наукових статей.
4.3.4. Ствердження доказів
Ревматоїдний артрит
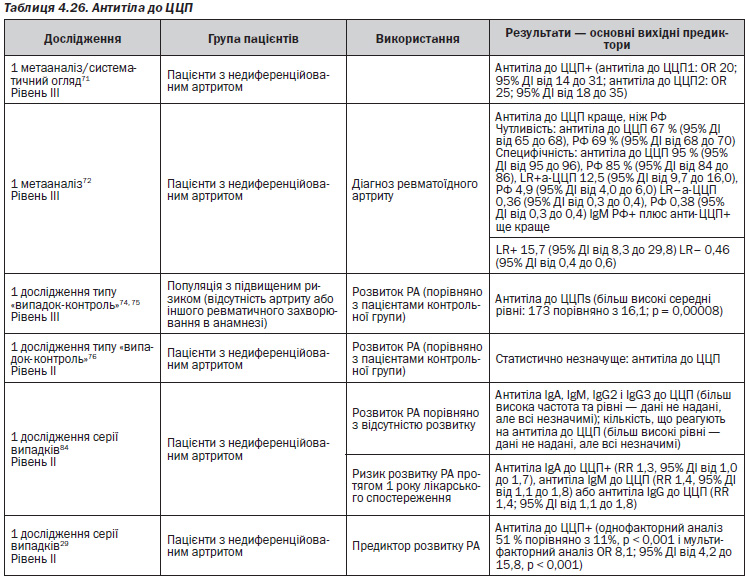
В одному метааналізі/систематичному огляді71 повідомляється про три дослідження, в яких розглядалися пацієнти з ревматоїдним артритом, які здали зразки крові перед розвитком РА. Рівень III
— Одне дослідження показало, що антитіла до ЦЦП2 прогнозували розвиток РА у пацієнтів із низькою чутливістю (4 %, 25 % і 52 % через 9 років, > 1,5 років і < 1,5 років до появи симптомів) і високою специфічністю (98 %). OR 28 (95% СІ від 8 до 95).
— В одному дослідженні був проведений аналіз тих самих пацієнтів, і було виявлено, що антитіла до ЦЦП2 мали вищу прогностичну цінність порівняно з РФ; OR 15,9 для антитіл до ЦЦП2 і 6,8 — для РФ.
— Одне дослідження показало, що за 5 років до появи симптомів пацієнти з антитілами до ЦЦП1 мали низьку чутливість і високу специфічність щодо прогнозування РА (29 % і 99,5 % відповідно, OR 64,5 (95% СІ від 8,5 до 48,9)).
4.3.5. Стислий огляд ствердження доказів
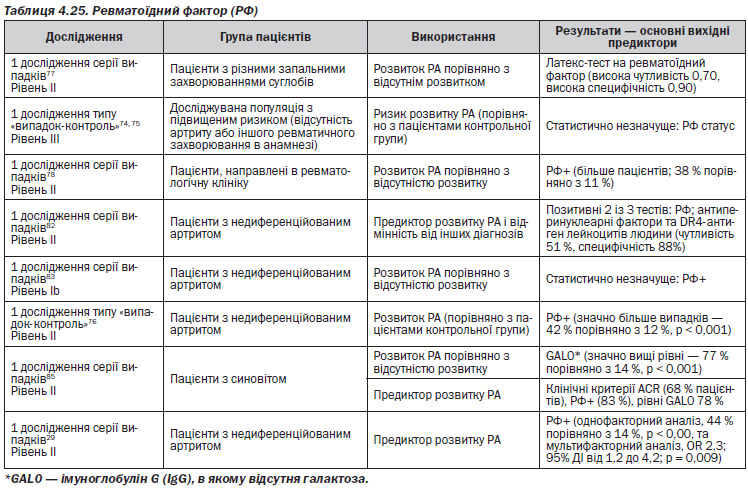
Ревматоїдний фактор (РФ) в більшості досліджень є корисним предиктором розвитку ревматоїдного артриту (РА)29, 76–78, 82, 85.
— Позитивність за антитілами до ЦЦП є корисним предиктором розвитку РА29, 71, 74, 75, 84 і порівняно з позитивністю за РФ має вищу специфічність, але подібну чутливість71, 72.
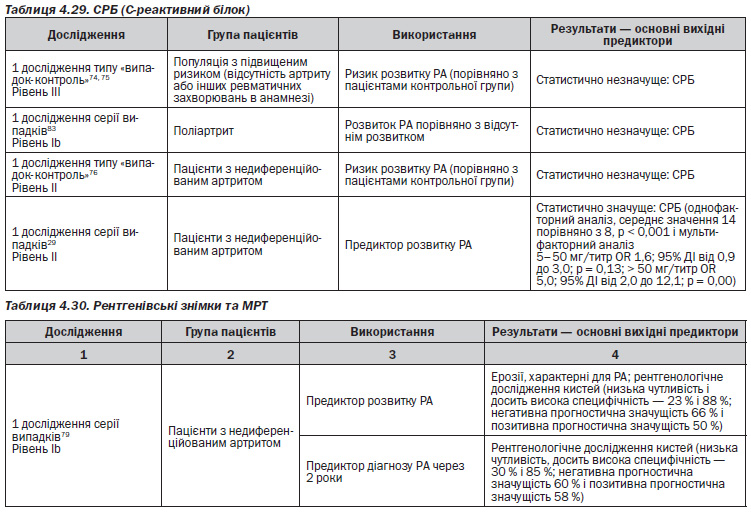
— Вихідний С–реактивний білок (СРБ) є поганим предиктором можливості розвитку РА74–76, 83.
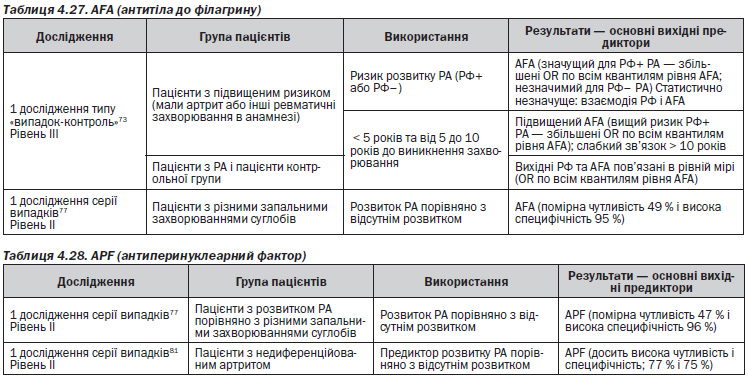
— AFA мали помірну чутливість і специфічність щодо розвитку РА і були кращими в прогнозуванні розвитку РФ+ РА, ніж РФ– РА73, 77, 78, 82.
— АPF мав помірну чутливість і специфічність для розвитку РА77, 78, 81, 82.
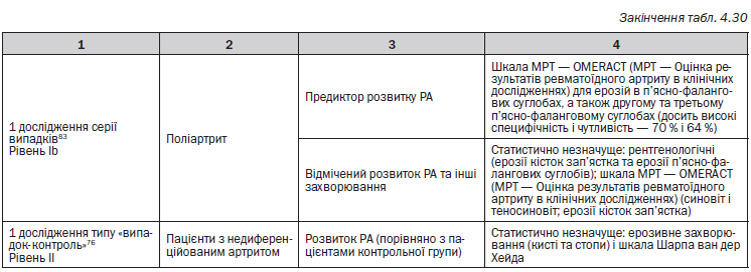
— Наявність ерозій на рентгенограмах кистей демонструє високу специфічність, але низьку чутливість щодо розвитку РА79.
— Ерозії п’ясно–фалангових суглобів, визначені за допомогою МРТ, мають достатньо високу чутливість та специфічність щодо розвитку РА83.
4.3.6. Від доказів до рекомендацій
Хоча антитіла до ЦЦП більш специфічні, ніж ревматоїдний фактор, ця різниця невелика, а чутливість зіставна. Рекомендації по антитілам до ЦЦП також мають бути підтверджені медичним економічним аналізом, щоб визначити, чи є додаткові витрати і вища специфічність цього тесту економічно ефективними (див. розділи 4.2.7 і 4.2.8) як щодо всіх ранніх запальних артритів, так і за підгрупами (наприклад, підозра на РА, але ревматоїдний фактор негативний). Тест на ревматоїдний фактор залишається відносно дешевим і корисним у пацієнтів із недиференційованим синовітом і може використовуватись як з діагностичною, так і з прогностичною метою.
Після багатьох обговорень було вирішено, що рентгенівські знімки кистей і стоп при вперше діагностованому синовіті доцільні, оскільки, хоча це і є грубим інструментом для виявлення запалення суглобів, бувають випадки, коли виявляють ерозивне ураження в той час, коли результати всіх інших тестів нормальні; рентгенографія кистей також є легкодоступним способом визначення базового рівня ураження для визначення в майбутньому швидкості прогресування захворювання. Оскільки УЗД і МРТ дрібних суглобів стають все більш доступними, довгострокове значення деяких ранніх запальних та ерозивних змін, які були описані за допомогою цих методів діагностики, має стати очевидним, і з часом вони можуть замінити рентгенологічне дослідження.
Рекомендації
R4 Пропонується проводити аналіз крові на ревматоїдний фактор у хворих з підозрою на ревматоїдний артрит (РА), у яких виявлено синовіт при клінічному обстеженні.
R5 Робити рентгенівські знімки рук кистей і стоп на ранніх стадіях захворювання у хворих зі стійким синовітом.
Коментар робочої групи
Метою проведення рентгенографії кистей та стоп на ранніх стадіях РА є створення можливості для наступного регулярного моніторингу рентгенологічних змін.
5. Просвітницька та навчальна робота
5.1. Уявлення та переконання хворих
5.1.1. Клінічне введення
Настанови розробляються для блага пацієнтів і цілком логічно, що ця настанова включає в себе розділ, присвячений переконанням і уявленням пацієнтів про їх захворювання. Патерналістичний підхід, при якому медики володіють інформацією, а пацієнт є пасивним отримувачем допомоги, має стати далеким спогадом. Багато пацієнтів бажають усвідомлено брати активну участь у своєму лікуванні і пов’язаному з ним процесі прийняття рішень. Проте навіть тоді, коли лікарі прагнуть залучити пацієнта до лікування їх хвороби, ще є можливості для роз’єднання між пацієнтами, особами, які за ними доглядають, і їх лікарями. Це стосується і сприйняття хвороби та терапевтичних втручань, а також пріоритетів щодо їх потреб в медичній допомозі.
Деякі попередні уявлення про РА у пацієнтів з щойно діагностованим захворюванням повинні бути розглянуті на початку захворювання. Пацієнти, які йдуть на перший призначений візит до клініки, вже можуть знати діагноз хвороби від лікаря загальної практики, і це може призвести до виникнення багатьох міфів і чуток про хворобу. Про захворювання можуть надати інформацію погано обізнані друзі і родичі, а іноді, на жаль, і медичні працівники. Деякі попередні уявлення про хворобу можуть бути отримані раніше формування відповідного розуміння і переконання.
Хворим із встановленим діагнозом РА важливо зрозуміти, що їх сприйняття РА та їх пріоритети в лікуванні можуть відрізнятися від розуміння і сприйняття мультидисциплінарною командою (МДК), яка їх лікує.
Хоча це достатньо широке коло питань, необхідно розглянути два ключові моменти:
— Який досвід, уявлення і переконання пацієнта позитивно впливають на симптоми, ураження суглобів, функцію і якість життя, і які з них можуть бути виявлені і посилені самим пацієнтом і тими, хто хоче йому допомогти?
— Навпаки, який досвід, уявлення і переконання пацієнта чинять негативний вплив, і які необхідно мінімізувати або уникнути їх?
5.1.2. Клінічне методологічне введення
Ми шукали дослідження, які вивчали досвід пацієнтів з РА і його лікування. Через великий обсяг даних доказової медицини дослідження включалися лише за умови публікації в останні 10 років (з 1997 року); неякісні дослідження повинні були мати розмір вибірки з N > 100 відповідної популяції Великобританії, і популяція зі змішаним артритом мала включати > 75 % РА або містити аналіз підгруп з РА.
Ранній РА
Було знайдено вісім досліджень31, 87–93, які відповідали критеріям. Дослідження відрізнялися щодо:
— розміру вибірки (від N = 68 до N = 573);
— тривалості дослідження — спостереження (від короткого до п’яти років);
— дизайну дослідження (6 обсерваційно–кореляційних досліджень; 1 обсерваційно–поздовжнє дослідження, 1 перехресне дослідження, 1 ретроспективне дослідження).
Розгорнута стадія РА
Було знайдено 25 досліджень94–117, які відповідали критеріям. Два документи94, 95, 98–102, 104, 107–109, 111, 113–115, 117–120 повідомляли про одне й те ж саме дослідження, але містили різні результати. Результати обох робіт представлені, але це дослідження враховане один раз. Дослідження відрізнялися стосовно:
— розміру вибірки (від N = 6 до N = 7702);
— тривалості дослідження — спостереження (від короткого до п’яти років):
— дизайну дослідження (13 обсерваційно–кореляційних досліджень, 7 якісних досліджень, 4 перехресних досліджень, 1 дослідження «випадок–контроль», 1 обсерваційне дослідження).
Недиференційована тривалість хвороби (нещодавній початок і РА з хронічним перебігом) або тривалість не вказано
Було знайдено п’ять досліджень119, 121–124, які відповідали критеріям. Дослідження відрізнялися стосовно:
— розміру вибірки (від N = 10 до N = 190);
— тривалості дослідження — спостереження (4 випробування безпосередні, 1 дослідження — 1 рік);
— дизайну дослідження (2 обсерваційно–кореляційні дослідження, 2 якісні дослідження, 1 перехресне дослідження).
5.1.3. Методологічне введення з економіки в охороні здоров’я
Жодних робіт з економіки охорони здоров’я з цього питання не було знайдено.
5.1.4. Заяви про клінічні докази
Всі дослідження мали доказовість 3–го ступеня, за винятком якісних досліджень — 3+.
Ранній РА
Виявлено кілька основних тем.
Сфери життя, які найбільше постраждали, і те, яким чином хвороба вплинула на пацієнтів (чотири дослідження)87, 88, 90, 119.
Обсерваційні дослідження засвідчили, що біль, відсутність контролю над болем і незадоволення дієздатністю впливали на психологічне благополуччя, самоповагу та адаптацію до хвороби. Високі рівні тривоги і депресії були пов’язані з втомою, болем і низьким рівнем сприйняття. Крім того, пацієнти, які відчувають більшу втому, мають більший ризик болю, більшу недієздатність, депресію, нижчу самооцінку, менш задоволені наданою їм підтримкою, демонструють зменшення активності в дозвіллі, відчувають себе менш незалежними і пристосованими і оцінюють своє здоров’я як значно гірше.
Надання медичної допомоги — це сфера, яку пацієнти вважають важливою і яку необхідно вдосконалювати, а також забезпечувати інформацією (одне дослідження)119.
Обсерваційне дослідження засвідчило, що обізнаність пацієнта і потреба в інформації були однаковими у пацієнтів з недавнім початком захворювання і у пацієнтів з пізнім РА.
Кореляція між демографією, характеристиками захворювання та оцінкою хвороби (чотири дослідження)31, 89, 91, 92
Експериментальні дослідження продемонстрували, що:
— жінки мали вірогідно гірші показники симптомів, функцію і якість життя, крім болю, зміни на рентгенівських знімках кистей або рівень С–реактивного білка;
— якість життя слабо асоціювалася з клінічними і лабораторними показниками, а загальна оцінка пацієнтів асоціювалася з болем, депресією, інвалідністю і болючістю суглобів.
— результати стану фізичного здоров’я прогнозувалися базовими показниками HAQ, AIMS фізичного, вікового і AIMS психологічного стану здоров’я. Базові показники HAQ і AIMS фізичного стану асоціювалися з фізичною непрацездатністю. Психологічний стан здоров’я прогнозувався показниками психологічного здоров’я AIMS.
— старші, менш стурбовані пацієнти (STAI–SF), зі значно більшою ймовірністю припинять приймати свої початкові DMARDs протягом першого року. Продовження прийому DMARDs асоціювалося з HAQ, відносинами з лікарями лікарні, переконаннями щодо анкети лікування та іншими важливими шкалами.
Ставлення до лікування (в тому числі переваги та ефективність); одне дослідження BeSt93
— Не виявлено суттєвої різниці між чотирма групами лікування щодо «значного» та «дуже значного» поліпшення загального стану здоров’я від початку лікування або поточного стану здоров’я від ліків, які вони повин–ні приймати (однак група 3 була менш задоволена).
Групи 1 і 2 мали значно повільніше полегшення симптомів, ніж групи 3 або 4, але мали незначну різницю між собою.
— Перевага пацієнтів щодо розподілу до певної групи до початку дослідження: не було переваг (44 %), лише 3–я група мала вплив на розподіл груп — 22 % пацієнтів, які насправді отримали це лікування, сподівалися не бути віднесеними до групи 3, в той час як цей показник був набагато вищим (> 40 %) і в інших групах.
— Якщо РА діагностували сьогодні, пацієнти віддали б перевагу такому лікуванню: лікуванню одним відомим протиревматичним препаратом (21 %), комбінації без преднізолону (19 %); комбінації з преднізоном (12 %); комбінації з новим в/в препаратом (в даному випадку інфліксимаб) — 44 %.
— Відчуття пацієнтів, що приймали преднізолон: 50 % пацієнтів у групі 3 не подобалося приймати преднізолон (15 %, 20 % і 9 % в групах 1, 2 і 4 відповідно).
— Відчуття пацієнтів, що отримували в/в лікування в лікарні: 8 % пацієнтів групи 4 не хотіли госпіталізуватись до лікарні для в/в лікування (2 %, 3 % і 2 % в групах 1, 2 і 3 відповідно).
РА з хронічним перебігом
Виявлено кілька основних тем.
Сфери життя, які пацієнти найбільш хотіли б поліпшити (2 дослідження)97, 115
Обсерваційні та якісні дослідження засвідчили, що пацієнти найбільше хотіли б поліпшення щодо болю, функції (кисті і пальців), а також ходьби і згинання. Пацієнти, які бажали полегшення болю, мали нижчу самоефективність в самодопомозі, більшу втому, гірший загальний стан здоров’я і застосовували більше анальгетиків. Літні люди найбільше бажали поліпшення функції, в той час як пріоритетами молодших пацієнтів були біль, працездатність і психічний стан. Коли обговорювалося питання взуття, жінки хотіли більше інформації щодо його вибору, вони хотіли б висловити свою думку і переконатися, що їх слухають, а також підтвердження з боку лікаря, що вони достатньо розуміють свою хворобу. Почуття довіри до практикуючого лікаря розглядається як важливий фактор під час консультації. Чоловіки не зазначали будь–які аспекти їх досвіду, які необхідно поліпшити.
Найбільш уражені сфери життя і як хвороба впливає на пацієнтів (10 досліджень)94, 95, 98, 100, 104, 107–109, 111, 114, 115, 118
Обсерваційні, якісні і дослідження «випадок–конт–роль» виявили, що:
— Найбільш проблемними сферами для хворих були: їх особистість (приватна та публічна сфери), фізична активність у повсякденному житті (ADLS), якість життя (QOL), біль, фізична та розумова втома, знижена активність, депресія, втрата довіри і мотивації, фрустрація, самосвідомість або збентеження при деформації, вплив на стосунки і сімейне життя.
— Пацієнти були стурбовані щодо: майбутнього (посилення болю і втрата працездатності); неефективності лікування, нездатності (виконувати ADLS, бути сексуально активними, працювати з відповідними фінансовими наслідками роботи, звільнення з роботи через біль).
— Пацієнти виражали такі емоції: скорботу і гнів у зв’язку з втратою здатності до звичайної роботи (до внесення необхідних змін у спосіб життя), мужність, щоб протистояти болю і щоденним очевидним втратам, страх перед майбутнім і побічними ефектами, розчарування і депресію.
— Багато пацієнтів виявили потребу у переконанні себе та інших щодо наявності у них РА (хвороба «невидима» на ранніх стадіях, і люди не розуміють хворобу). Через негативну реакцію деякі пацієнти симулюють гарне самопочуття, в той час як це не відповідає дійсності. Пацієнти хотіли б відчувати, що їх цінує суспільство (їх труднощі цінують і розуміють). Вони також вважають основною формою підтримки розуміння з боку родини. Сім’я/друзі часто переоцінюють тяжкість та особливості болю і недооцінюють негативні наслідки РА щодо життя пацієнта в цілому. Лікарі, навпаки, як правило, недооцінюють силу болю і його характеристики. Для подружжя важливо зрозуміти відчуття своїх партнерів щодо контролю їх РА і його циклічності, мати оптимістичні погляди і об’єктивно оцінювати наслідки РА.
— Пацієнти мають керувати новим «способом життя» (знайти методи лікування хвороби, адаптуватися до змін, розвивати нові навички та здібності, щоб звикнути до втрачених можливостей). Широко використовується адаптація для виконання повсякденної діяльності. Серед них обмеження і збільшення витрат часу для активних дій, допомога і пристрої.
— Хворі описували біль як: мінливий (80 %), непередбачуваний (68 %), такий, що викликає серйозні перешкоди у роботі або виконанні домашніх обов’язків (67 %); виявлені недооцінка болю дружиною (чоловіком) (23 % пацієнтів) і лікарем (14 % хворих), іншими членами родини або друзями (38 %).
— Жінки мали гірші результати оцінки якості життя, ніж чоловіки. Якість життя знижувалася з віком. Вплив РА на психічне здоров’я був нижчим у пацієнтів < 50 років порівняно з іншими віковими групами.
— Жінки висловили стурбованість з приводу зовнішнього вигляду своїх ніг і взуття, в той час як жоден чоловік не говорив про зовнішній вигляд ніг. Чоловіки ставилися позитивно до взуття і відчували, що воно допомагає їх рухливості і зменшенню болю.
— РА впливав на особистість пацієнта, соціальну роль і самооцінку, і значна кількість пацієнтів зазнала змін зовнішності, щоб пристосуватися до обмежень або щоб приховати фізичні вади.
— Важливість наслідків захворювання змінюється з часом і залежить від обставин (наприклад, на різних стадіях захворювання і в період загострення).
Надання медичної допомоги — сфера, яку пацієнти вважають важливою, сферою, що вимагає поліпшення, в тому числі надання інформації (10 досліджень)94, 95, 98, 99, 101, 102, 113, 115, 117, 119, 120
Обсерваційні та якісні дослідження продемонстрували, що:
— Аспекти надання медичної допомоги, які важливі для пацієнтів, такі: обізнаність з РА (ніякої різниці між раннім і пізнім РА), інформація про методи супутньої терапії і про ефективність препаратів і їх побічні ефекти, комунікація (чітка та ефективна і позитивні відносини з практикуючими лікарями), доступ до інших практикуючих лікарів між запланованими призначеннями, доступ до інших відділень, знайомство з персоналом.
— Аспекти надання допомоги, які вважалися неадекватними: допомога МДК (відсутність пристосованих туалетів у лікарнях, вибір лікаря, інформація про РА, перебіг симптомів, пристрої і домашні пристосування, хороша координації допомоги і готовність відповісти на питання), обмежені контакти з постачальниками послуг, відсутність надання медичної допомоги в громаді; соціальна підтримка (нещасні від того, що повин–ні покладатися на партнерів або членів сім’ї); активніша участь у прийнятті рішень щодо лікування (хоча деякі хотіли, щоб лікар взяв під свій контроль лікування при погіршенні стану).
— Пацієнти хотіли мати більше інформації (особливо жінки, без різниці між раннім і пізнім РА), а зміст повинен стосуватися: діагностики, патогенезу і ліків, вправ, повсякденної діяльності, погіршення хвороби, цілей лабораторних тестів; інших способів лікування. Значна кількість хворих відчували відсутність чіткої і однозначної інформації під час лікування та відсутність загальних рекомендацій щодо наявних послуг і фінансової вигоди. Вони хотіли як усної, так і письмової інформації.
— Задоволеність наданням медичної допомоги: деякою мірою задоволені або дуже задоволені — 68 %, відчули незадоволення медичних потреб (зокрема, фізичних симптомів, наслідків хвороби — структури тіла і функції, якості медичної допомоги та медичних послуг) — 27 %. Незадоволення потреб асоціювалося з погіршенням здоров’я, збільшенням кількості супутніх захворювань і незадоволеністю, була стурбованість щодо комунікації (з працівниками охорони здоров’я). Жінки довіряють кваліфікації лікаря щодо взуття, але не задоволені тим, як з ними поводилися експерти, які часто відхиляли їх інтереси і потреби. Чоловіки відчували по–іншому, вони мали деякі товариські стосунки і довіряли кваліфікації лікарів.
— Рішення щодо ефективності лікування асоціювались зі зменшенням симптомів, змогою пацієнта «забути», що він є хворим на РА, зміною пріоритетів щодо результатів з плином часу, величиною поліпшення/зміни, та відрізнялись залежно від тривалості захворювання.
— Пацієнти хотіли б відчувати контроль їх стану і, як правило, відмовлялись від втручань як способу конт–ролю, вони відчували надію, коли медичний персонал шукав нові методи лікування. Лікування давало їм поліпшення симптомів, допомогло їм повернутися до норми і дозволило їм краще спати. Біологічні препарати надали позитивний фізичний і емоційний ефект. Задоволеність препаратами була вищою серед пацієнтів, які приймали біопрепарат, ніж серед тих, хто не отримував ці препарати.
— Більшість пацієнтів не хотіли змінювати своє лікування (в тому числі на біопрепарати), допоки їх стан не погіршиться. Значна кількість хворих відчувала, що їх лікар думав, що їм не потрібна зміна препарату або немає кращих ліків, ніж ті, які вони приймають в даний час, а деякі не бажали отримувати препарати внутрішньовенно.
— Додаткові методи лікування: багато хто спробував один або кілька методів для полегшення болю, в тому числі голковколювання і масаж. Один пацієнт зазначив, що він «не може обійтися без... голковколювання і масажу... і тепло дійсно допомагає». Значна кількість хворих говорили, що їм нічого не залишалося, крім того як приймати токсичні препарати, щоб уповільнити прогресування або полегшити симптоми, і були стурбовані побічними ефектами. Майже всі пацієнти сподівались, що нове дослідження знайде необхідні ліки.
— Значна кількість хворих хотіли б кращого зворотного зв’язку з вторинною медичною допомогою. Первинна медична допомога була описана як безкоштовний і критичний шлях (затримка у встановленні діагнозу і початку лікування).
— Значна кількість хворих намагалася догодити співробітниками тим, що обіцяли не бути «надокучливими». Вони були більш впевненими з медсестрами, ніж з лікарями, і тільки половина з них отримувала лікування від інших членів MДК. Наявність студентів–медиків або тих, хто здійснює догляд, а для пацієнток також побачити лікаря чоловічої статі ставило хворих в незручне становище, особливо коли мова йде про особисті питання (гінекологічні/емоційні).
Кореляція між демографією, характеристиками захворювання та засобами оцінки хвороби (12 досліджень)96, 100–103, 106, 110, 112, 116, 117, 119
Обсерваційні дослідження засвідчили, що:
— Прогностичними показниками гірших результатів (у тому числі непрацездатності, болю і QOL) були: біль, втома, тривалість активного захворювання, депресія, радіологічне підтвердження ураження, жіноча стать, літній вік, гірший соціально–економічний статус, рідша наявність оплачуваної роботи і подружнього життя, вища активність, більша кількість соматичних/ психологічних супутніх захворювань, більша кількість видів діяльності, на які вплинув РА.
— Низький рівень участі у прийнятті рішень асоціювалася з: молодим віком, більшим задоволенням від допомоги, наявністю партнера, продовженням праці, тривалим часом перебування у формальній освіті, меншою кількістю супутніх захворювань, зниженням активності захворювання, зниження втоми і меншим болем. Високий рівень участі у прийнятті рішень асоціювався з: молодим віком, високим рівнем формальної освіти, високим рівнем отриманої інформації і високим рівнем задоволення пацієнта.
— Потреба в інформації асоціювалася з: віком, освітою (у жінок), втомою, кількістю DMARDs, які приймав пацієнт, та з побічними ефектами (у чоловіків). Переваги щодо прийняття рішення асоціювалися з: віком, освітою, кількістю DMARDs, які приймав пацієнт, та поінформованістю щодо РА (у жінок та чоловіків).
— Гірша функціональна здатність, більша кількість порушень й інвалідності при оцінці активності асоціювалися з нижчою задоволеністю фізичними можливостями, які, в свою чергу, асоціювалися з більш виразною депресією.
— Високий рівень тривоги і депресії був обумовлений сильнішим болем, втомою і нижчою прихильністю до лікування.
— Пасивне подолання хвороби було психологічним прогностичним показником як болю, так і депресії, і медіатором впливу інвалідності як на біль, так і на депресію.
— Пацієнти з РА мали значно нижчу активність порівняно з активністю 1 і 10 років тому, але позитивно оцінювали свою активність у майбутньому.
— Виконання багатьох видів діяльності асоціювалося з хорошим станом психічного здоров’я або психологічного благополуччя, а виконання небагатьох видів діяльності мало протилежний ефект.
— Роль фізичної діяльності за SF–36 корелювала з кількістю видів діяльності, які пацієнт здійснював у минулому (1 рік, але не 10 років тому), в даний час і кількістю, яка планується в майбутньому.
— Фізична функція за SF–36, проте, корелювала лише з кількістю видів діяльності, запланованою на майбутнє.
— Непрацездатність пацієнта була стрес–фактором для пацієнтів, але не для партнерів. Стрес–факторами для партнерів, але не для пацієнтів, були негативні вчинки і якість шлюбу, інвалідність пацієнта асоціювалися з тягарем для партнера. Вплив якості шлюбу на пацієнта залежить від навантаження на партнера.
— Багато пацієнтів з поганими показниками HAQ або PAS (тобто незадовільною функцією або незадовільним рівнем активності через захворювання) були задоволені своїм контролем РА, в той час як інші пацієнти з «хорошими» балами були незадоволені.
— Мета в житті асоціювалася з (багатофакторний аналіз): молодим віком, участю у дозвіллі/громадській діяльності, кращим психічним здоров’ям і оптимізмом у подоланні.
Недиференційована тривалість хвороби (нещодавній початок і РА з хронічним перебігом) або тривалість не вказано
Сфери життя, які найбільше постраждали, і як хвороба впливає на пацієнтів (2 дослідження)122, 123
Обсерваційні і якісні дослідження засвідчили, що:
— Пацієнти розглядали РА як виклик життєздатності і активно намагалися контролювати хворобу або пристосувалися до неї і відчували, що це є «щось таке, до чого треба звикнути» і «зробити все, що від них залежить, щоб вийти з поганої ситуації».
— Працюючі пацієнти мали значно нижчий рівень депресії, ніж непрацюючі.
Лікування — переваги і прийняття рішень (2 дослідження)121, 124
Обсерваційні та якісні дослідження продемонстрували, що:
— Думки пацієнтів щодо того, хто повинен вибирати ліки (пацієнти, які не застосовували інгібітори ФНП–-а): ревматологи (41 %), вирішують самі (33 %), невпевнені (18 %), спільне рішення (7 %).
— Чоловіки значно частіше віддавали право вибору ревматологу, без вікової різниці. Деякі пацієнти не відчували себе впевненими, коли приймали рішення без подальшої підтримки і обговорення з медичними працівниками, а один пацієнт вважав, що в Інтернеті дуже багато інформації про смерть.
— Думки пацієнтів щодо того, хто повинен вибирати ліки (пацієнти, які застосовували анти–ФНП): всі пацієнти хотіли брати участь у прийнятті рішення, і ті, хто був залучений до спільного прийняття рішення, вважали це позитивним і корисним.
— Чотири шляхи прийняття рішення:
1. Відмова від прийняття рішення — залишити це в руках лікаря, оскільки «лікар знає краще»;
2. Примусовий/усвідомлений вибір — лікар міг мати більше успіху при застосуванні конкретного препарату, таким чином він «віддає йому перевагу... в той час, як інший препарат може бути таким, який ти дійсно хочеш приймати».
3. Колективне рішення «дозволяє звернутися за наступною консультацією... піти геть і дещо обдумати. Ви повинні бути впевнені, що це те, чого ви хочете».
4. Вибір пацієнта: пацієнти вибирають самі, «інформація має бути представлена таким чином, щоб не примушувати до вибору».
— Більшість пацієнтів, які використовують шини з приводу РА кисті/зап’ястя, повідомили, що використання ними шин залежало від тяжкості симптомів. Вони застосовували їх з метою полегшення симптомів і підтримки та іммобілізації зап’ястя. Вони знімали шину, коли повинні були знизити функціональні можливості, і при виконанні брудної роботи або роботи у вологому середовищі.
Кореляція між демографією, характеристиками захворювання та оцінкою хвороби (два дослідження)119, 123
Обсерваційні дослідження продемонстрували, що:
— Обізнаність щодо РА і потреба в інформації незначно відрізнялася між пацієнтами з довготривалим (> 10 років) і короткотривалим (< 1 року) захворюванням.
— Високий рівень втоми, болю, підвищення функціональної недієздатності і низький рівень прийняття були показниками прогнозу щодо високої тривожності і депресії і нижчої задоволеності життям. Психологічне благополуччя корелювало з оптимізмом, песимізмом і передбачуваним стресом, але не з медичною соціальною підтримкою, активною когнітивною і поведінковою ефективністю, тривалістю захворювання, запаленням, застосуванням антидепресантів та наявністю супутніх захворювань. Загальна соціальна підтримки значно корелювала з більш низьким рівнем депресії і більшою задоволеністю життям.
— Серед пацієнтів з нижчим рівнем стресу спостерігався незначний ефект впливу активного поведінкового подолання депресії і задоволеності життям. Проте серед хворих з вищим рівнем стресу заняття з активного поведінкового подолання асоціювалося з нижчим рівнем депресії і вищим задоволенням життям.
5.1.5. Резюме даних доказової медицини
Обсерваційні та якісні дослідження продемонстрували наступні результати щодо пацієнтів з РА:
— Вони часто відчували брак інформації (особливо про побічні ефекти лікарських препаратів, інші варіанти лікування, пристрої і прилади, а також домашні пристосування)94, 95, 98, 99, 101, 102, 113, 115, 117, 119, 120; хотіли б брати більшу участь у прийнятті рішень щодо лікування101, 102.
— У багатьох випадках у пацієнтів були незадоволені потреби з боку охорони здоров’я і вони хотіли б поліпшення в кожному сегменті мультидисциплінарної команди97–99, 101, 115. Найбільш уражені сфери життя, у яких пацієнти хотіли б поліпшення, — це біль, функція, ADL та хобі94, 95, 97–102, 113, 115, 117, 119, 120.
— Показники якості життя та стану хвороби часто гірші у жінок, ніж у чоловіків89, 97, 115.
— Пріоритетом для молодих пацієнтів були біль, робота (див. «Трудотерпія» в розділі 6), а також тривога і депресія97, 115.
— Пріоритетом для літніх пацієнтів була функція97, 115.
— Біль, втома, депресія, втрата функції, втрата активності, втручання в ADL і нездатність працювати були проблемами для багатьох пацієнтів з РА87, 88, 90, 94–103, 106, 110, 112, 113, 115–117, 119, 120.
— Поганий психологічний стан часто асоціювався з гіршими результатами симптомів, функції і QOL31, 87–92, 96, 100–103, 106, 110, 112, 116, 117, 119.
5.1.6. Від доказів до рекомендацій
ГРН зазначила, що дані доказової медицини виявили низку проблем, з якими стикаються хворі на РА, які часто залишаються невизнаними працівниками охорони здоров’я. До них відносяться біль і втома, депресія, мобільність, неможливість працювати або проводити дозвілля і громадську діяльність і вплив на сексуальні стосунки. Багато з цих аспектів та ускладнення хвороби було б найкраще обговорити з відповідними членами МДК (див. розділ 6.1), а також під час щорічного огляду (див. розділ 8.2). Проте ГРН вважає, що прагматично було б мати конкретні рекомендації для пацієнтів щодо забезпечення періодичної оцінки їх хвороби, які б містили ці важливі аспекти, і це повинно бути частиною рекомендації, пов’язаної з мультидисциплінарною командою (див. розділ 6 з МДК).
ГРН також відзначила наявність доказів потреби хворих у збільшенні їх участі в лікуванні хвороби. Через довготривалий характер ревматоїдного артриту і (з точки зору пацієнта) змін пріоритетів впродовж тривалого часу ГРН вважає доцільним регулярне обговорення з пацієнтом усіх аспектів лікування (в тому числі переваги та недоліки різних терапевтичних методів). Цю точку зору найбільш активно підтримали представники пацієнтів, які також підкреслили нагальну необхідність наявності достатнього часу для дискусій з медичними працівниками легко зрозумілою мовою і визнання важливості самостійного прийняття рішення пацієнтом.
Рекомендація
R6 Поясніть пацієнтам ризики і користь лікування РА таким чином, щоб вони могли їх легко зрозуміти. Впродовж перебігу хвороби слід надавати пацієнтам можливість поговорити про неї і узгодити всі аспекти лікування, а також поважати рішення, які вони приймають.
5.2. Навчання пацієнтів
5.2.1. Клінічне введення
При наданні допомоги хворим на РА пацієнти повною мірою повинні брати участь у прийнятті рішень щодо лікування; необхідно надавати інформацію та навчати хворих з питань хвороби, її лікування і того, як людина може допомогти сама собі в лікуванні цього захворювання. Надання якісної інформації є обов’язковим для всіх працівників охорони здоров’я, як частина їх кодексу поведінки, що має сприяти розумінню хворими свого стану і прийняттю рішення щодо лікування. Інформація, як правило, надається неофіційно «віч–на–віч» в клініці, з використанням навчальних матеріалів (наприклад, листівки, книги, DVD, веб–сайти з артриту). Освіта пацієнта виходить за рамки підвищення рівня знань і є «спланованим організованим навчанням, спрямованим на сприяння добровільному прийняттю поведінки та/або переконань, які сприяють здоров’ю»125. Додатково формується здатність ефективно самостійно надавати собі допомогу, тобто «контролювати свій стан і впливати на когнітивні, поведінкові і емоційні відповіді, необхідні для підтримання задовільної якості життя»126 за рахунок використання освітніх, мотиваційних та поведінкових засобів. Це може бути забезпечено шляхом проведення бесід, через самонавчання чи втручання з використанням комп’ютера або в офіційно організованих групових сеансах на чолі з ревматологом або підготовленим представником від пацієнтів з артритом або іншими хронічними захворюваннями. Можуть бути використані різні формати: освітні лекції/сеанси обговорення щодо підвищення обізнаності, задоволеності і зменшення проблем; або поведінкові, які також називаються психіатричним підходом, в тому числі регулярні практичні заняття з навичок та використання домашніх програм, що сприяють зміні поведінки.
Програми надання інформації та навчання пацієнтів можуть потребувати багато часу, але важливо розглянути користь таких заходів. Баланс між зусиллями хворих на РА і медичних працівників і отриманою користю має бути добрим. Які ж докази того, що освіта впливає на симптоми, прогресування хвороби, функцію і якість життя? Зокрема:
— Після отримання інформації, чи пам’ятають її хворі на РА і чи знаходять її корисною?
— Чи веде опанування пацієнтом освітньої програми (віч–на–віч або в групі) до стійкої користі або лише до короткотривалого поліпшення?
— Чи є стадії хвороби, на яких різні освітні втручання, швидше за все, будуть успішними? Чи навчання пацієнтів більш імовірно буде корисним, якщо воно буде проводитись на початку хвороби?
— Чи існують методи освіти для пацієнтів, які є більш успішними, ніж інші?
Було вирішено виключити формальну когнітивно–поведінкову терапію, оскільки вона виходить за рамки цього питання, але освітні програми з використанням поведінкового підходу розглядаються. Будь ласка, зверніть увагу, що NICE надав оцінку технології «Комп’ютеризованої когнітивно–поведінкової терапії депресії і тривоги»127.
5.2.2. Клінічне методологічне введення
Робоча група шукала дослідження, які вивчали користь і шкоду різної інформації для пацієнта та/або методів навчання та/або різних освітніх програм для пацієнтів або самолікування щодо симптомів, ураження суглобів, функції та якості життя хворих з раннім РА або у пацієнтів із розгорнутою клінікою РА. У зв’язку з великим об’ємом доказів були відібрані тільки РКД з 1997 року з N ≥ 50, які мали відповідні Великобританії групи населення і, якщо це був змішаний артрит, мали питому вагу РА > 75 % або підгрупу аналізу РА. Також відбиралися дослідження, в яких порівнювалося наступне:
а) освіта/самолікування проти інших освітніх методів/самолікування;
б) освіта/самолікування проти звичайного лікування.
Примітка. Через критерії включення/виключення, встановлені для цього огляду, деякі корисні дані було виключено, а саме довгострокові програми Великобританії з самолікування артриту128, 129.
Змішана популяція (ранній РА і РА з хронічним перебігом)
Було вирішено, що в зв’язку з великою кількістю доказів щодо програм освіти і самолікування було б корисно включити опублікований метааналіз130, хоча він не розподіляє популяцію з раннім РА і з встановленим захворюванням.
Було знайдено один Кокранівський систематичний огляд131, який відповідав критеріям і базувався на РКД, які порівнювали втручання освіти пацієнта (яке включало навчальний компонент) проти відсутності втручання в контрольній групі пацієнтів з раннім та пізнім РА. Контрольна група «без втручання» отримала деяке втручання, оскільки пацієнти зверталися до лікарів для оцінки своєї хвороби. МА був добре проведеним, проте 31 РКД, які він включав, були різної якості і відрізнялися щодо:
— засліплення (7 РКД подвійні сліпі, 20 — РКД сліпі, 23 РКД — без засліплення);
— величини дослідження (від N = 18 до N = 1140);
— якості дослідження — максимальна кількість балів 8 (21 дослідження гарної якості (1+ і 1++), 29 низької якості (Г));
— тривалості дослідження — тривалість втручання (від 7 годин до 15 місяців);
— тривалості дослідження — тривалість спостереження (від 8 днів до 18 місяців).
Примітка. Оскільки Кокранівский МА об’єднав роботи, які включали пацієнтів як з раннім, так і з пізнім РА, було вирішено, що дублікати робіт (тобто документи, отримані в нашому пошуку, які вже були включені в МА) включаються в якості доказів в цей розділ з раннім або з пізнім РА для того, щоб виявити будь–які впливи на ці підгрупи. Результати, представлені в МА, були отримані з 17 РКД лише високої якості (дані з досліджень низької якості були виключені).
Ранній РА
Було знайдено чотири РКД132, 136, які відповідали критеріям. Одне з цих РКД було опубліковано у вигляді двох окремих робіт134, 135, які містили різні результати, тому дослідження було враховано тільки один раз, хоча результати обох робіт і посилання представлені. Методологічні обмеженнями РКД були наступні: ті, які мали ступінь 1+ (3 РКД), були сліпими, а аналіз ІТТ не проводився. РКД з рівнем 1++ було сліпим, і аналіз ІТТ був проведений.
Всі чотири РКД були сліпими дослідженнями в паралельних групах, але вони відрізнялися щодо:
— розміру вибірки (від N = 64 до N = 326);
— тривалості дослідження (від 3 місяців до 4 років після втручання);
— лікування (1 РКД132 освітньої програми + DMARDs проти освітніх листівок + DMARDs; 1 РКД133 стандартної освітньої програми проти когнітивно–поведінкової освітньої програми, 1 РКД134, 135 стандартної освітньої програми проти освітньої програми з захисту суглобів, 1 РКД136 програма з самолікування трудотерапією проти звичайного лікування).
РА з хронічним перебігом
Було знайдено дев’ять РКД137, 145, які відповідали критеріям. Три з цих РКД137, 140, 142 були виключені через методологічні обмеження (несліпі і ІТТ аналіз не проводився). Методологічні обмеження інших включених РКД були наступними:
1+ — сліпі (3 РКД) та/або ІТТ аналіз не проводився (2 РКД). Решта РКД оцінювалися як 1++, оскільки були сліпими і ІТТ аналіз був виконаний.
6 включених РКД138, 139, 141, 143–145 були дослідженнями в паралельних групах, але вони відрізнялися щодо:
— розміру вибірки (від N = 59 до N = 363);
— засліплення (4 РКД сліпі, 2 РКД несліпі/засліплення не згадується);
— тривалості дослідження (від 4 тижнів до 1 року втручання; спостереження варіювало від негайного до 9 місяців після втручання);
— лікування (1 РКД включало стандартні програми навчання проти стандартного лікування; 1 РКД138 освітньої програми + листівки проти стандартної терапії + листівки, 1 РКД140 — групове навчання зі значним іншим проти тільки групове навчання пацієнтів порівняно з контролем самолікування; 1 РКД142 програма самолікування з залученням дружини/чолові–ка + звичайне лікування проти тільки освітньої програми + звичайне лікування, 1 РКД143 листівки з РА ACR + асоціативна карта проти листівок з РА ACR і 1 РКД145 — освітня програма + інформаційний листок проти звичайного лікування + інформаційний листок).
5.2.3. Методологічне введення з економіки охорони здоров’я
Жодні економічні дослідження в охороні здоров’я не оцінювалися.
5.2.4. Заяви про докази (табл. 5.1)
Ранній РА
Освіта/самолікування порівняно зі звичайним лікуванням
Одне РКД виявило, що ефективність лікування в групі «програма з самолікування/трудотерапії» значно краще, ніж у контрольній (без втручання) групі щодо: використання деяких методів самолікування (зокрема, вправ для рук та передпліччя, захисту суглоба і спокою); отримання робочої шини і шини для спокою, придбання та використання допоміжних пристроїв. Проте не було різниці щодо: показників DAS28, HAQ, AIMS2 та балів самоефективності (ASES). Рівень 1++ (табл. 5.2)
Освітня програма порівняно з освітніми листівками
Було знайдено одне РКД132, в якому була незначна різниця між освітньою програмою + DMARD та освітні листівки + DMARD для оцінки DAS, оцінки –М–HAQ та діапазону рухів плечей, ліктів і колін, шкала AIMS, СРБ, відповідність активності і захисту суглоба (але освіта значно краще щодо відповідності зі збереженням енергії). Рівень 1+
РА з хронічним перебігом (табл. 5.3)
Одне РКД146 виявило, що 75 % пацієнтів вважали освітню програму дуже корисною і лише 8 % не вважали її корисною взагалі щодо повсякденної активності.
Освітня програма порівняно з освітніми листівками
Одне РКД141 встановило, що значної різниці між освітніми програмами для пацієнтів + інших значних осіб і освітніх листівок щодо показників DAS28, вимірів самоефективності, всіх вимірів поведінкового здоров’я не було; застосування активного самолікування; ступінь, до якої люди застосовують стратегії здатності активно справлятися з хворобою — Dutch Coping with Rheumatoid Stressors. Проте освітня програма з освітою іншої значущої особи була значно гіршою щодо втоми. Рівень 1++
Буклет ARC + карта пам’яті порівняно з буклетом ACR
Одне РКД144 встановило, що не існує значної різниці між буклетом ACR + карта пам’яті порівняно з буклетом ACR щодо розширення знань.
Те ж саме РКД141 встановило, що погана здатність до читання призводить до поганих знань, що асоціюється з більшою стурбованістю і депресією. Рівень 1+
5.2.5. Резюме даних доказової медицини
Кокранівський метааналіз131 показав, що навчання пацієнтів мало невеликий, короткотривалий вплив на непрацездатність, показники суглобів, глобальну оцінку пацієнта, психологічний стан і депресію. Не було жодних доказів довготривалої користі.
Групи, що навчаються, як правило, не показують переваги порівняно з контрольною групою. Одне РКД не показало різниці між освітньою програмою і освітніми листівками щодо різних результатів132. Інше РКД показало, що навчальна програма віч–на–віч порівняно тільки зі стандартним лікуванням призвела лише до підвищення знань пацієнта і прихильності до лікування, але ніякої різниці щодо інших результатів немає138, 139. Були деякі докази короткотривалої користі щодо болю в руці, кількості загострень захворювання і загальних оцінок, поведінки щодо суглобової протекції та довготривалого (4 роки) зменшення ранкової скутості і зменшення відвідувань лікаря загальної практики, хоча не було ніяких змін у використанні загальноприйнятих ліків134, 135. Ті ж дослідження показали менший розвиток деяких деформацій руки, і, хоча не було ніякого поліпшення функції руки134, 135, можна було спостерігати деякі коротко– і довготривалі покращення повсякденної активності133–135. Одне РКД136 виявило, що програма самолікування/трудотерапії була значно кращою, ніж у контрольних групах (без втручання), щодо використання деяких методів самолікування, отримання і використання шин та інших допоміжних пристроїв.
Когнітивно–поведінкові підходи мали короткотривалу користь щодо настрою і зменшення відчуття безпорадності133, а інші дослідження не показали поліпшення134, 135. Відвідування програми з особою, яка здійснює догляд, чи з «іншою значущою особою» в цілому не покращує результатів141, 143.
5.2.6. Від доказів до рекомендацій
ГРН зазначила, що існує величезна кількість інформації, з якої важко вибрати саме те, що є ефективним. ГРН зазначила, що було багато факторів потенційного втручання. Не було жодних сумнівів, що пацієнти хочуть отримати чіткі пояснення в ході своєї хвороби і що вони хочуть отримати її як у письмовій, так і в усній формі. Хоча існують певні докази того, що при установленій хворобі письмова інформація може поліпшити деякі результати, не було знайдено ніяких досліджень, які б оцінювали письмову інформацію щодо хвороби, яка почалася недавно. Було дуже мало оцінок структурованих віч–на–віч освітніх програм, і ГРН відмітила, що це одна із сфер, що потребує подальших досліджень. Проте у зв’язку з бажанням пацієнтів отримати як письмову, так і усну інформацію про їх стан ГРН вважала, що було б доцільно створити рекомендації щодо такого впливу.
Ознакою багатьох досліджень була демонстрація короткотривалої, а не довготривалої користі. ГРН вважає, що це сфера, в якій було б доцільним зробити рекомендації щодо курсів підвищення кваліфікації, які можуть вирішити цю проблему; це також дозволить пацієнтам, які не хочуть отримувати інформацію на ранній стадії, мати можливість отримати її в більш пізньому терміні.
ГРН зазначила, що забезпечення пацієнтів програмами, які заохочують здійснювати самоконтроль, в даний час вважається одним з основних аспектів надання медичної допомоги при всіх довготривалих станах і що є докази того, що групові навчання під керівництвом медичних професіоналів з застосуванням поведінкового підходу виявилися ефективними у хворих з ревматоїдним артритом. Більшість досліджень групових програм під керівництвом навченого представника від пацієнтів, які використовують поведінковий підхід, такий як Arthritis Self Management Programme and Chronic Disease Self Management Programme, проводилися волонтерами від громади з різними ревматичними захворюваннями. ГРН вважала, що в даний час існує недостатньо доказів, щоб виправдати ці програми спеціально для РА (хоча відповідні рекомендації щодо досліджень були внесені), але загальна концепція програм самолікування під керівництвом представника від громади була підтримана.
Таким чином, ГРН відзначила недостатність чітких доказів у багатьох сферах, необхідність подальших досліджень, а також бажання пацієнтів мати доступ до широкого спектра освітніх заходів.
Тому було б доречно зробити загальні рекомендації з підтримки низки заходів, які вже можуть бути доступні, поки подальші дослідження (в тому числі дані економічної ефективності) визначать найбільш придатні методи навчання.
Рекомендації
R7 Надавайте усну і письмову інформацію людям з РА:
— покращуйте розуміння ними їхнього стану і його лікування, а також
— враховуйте будь–які помилки, які вони можуть мати.
R8 Пацієнтам з РА, які хочуть знати більше про свою хворобу і її лікування, необхідно давати можливість брати участь у існуючій освітній діяльності, у тому числі в програмах з самоконтролем.
6. Мультидисциплінарна команда
6.1. Мультидисциплінарна команда
6.1.1. Клінічне введення
Підхід з включенням мультидисциплінарної команди (медичні професіонали різних спеціальностей, такі як медсестри, фізіотерапевти, спеціалісти з трудотерапії і ортопеди, які спеціалізуються на захворюваннях стопи) часто використовується у веденні пацієнтів з ревматоїдним артритом. Склад команди в кожному центрі буде різним, але акцент повинен бути на завданнях, які відповідають індивідуальним потребам пацієнта, з метою зведення до мінімуму наслідків цього захворювання. Цей комбінований підхід поєднує навички та знання всіх членів команди щодо оцінки та лікування хвороби, але потребує високого рівня взаємодії та співпраці. Пацієнт часто може бути активним членом команди з метою вивчення і керування всіма аспектами медичної допомоги.
Цей розділ настанови оцінює докази ефективності всіх втручань, які традиційно здійснюються окремими членами мультидисциплінарної команди. Деталі відповідних втручань, які здійснюють фізіотерапевти, спеціалісти з трудотерапії і ортопеди, які спеціалізуються на захворюваннях стопи, наведені у відповідних розділах. Роль медсестри–спеціаліста з ревматології коротко наведена нижче.
Медсестра–спеціаліст з ревматології
Медсестра–спеціаліст з ревматології є невід’ємною частиною мультидисциплінарної команди, яка надає медичну допомогу пацієнтам з ревматоїдним артритом. Хоча її роль може змінюватись залежно від потреб служби, більшість медсестер будуть здійснювати клінічну, освітню та консультаційну допомогу. Медсестра–спеціаліст з ревматології може також брати участь у дослідженнях, веденні пацієнтів та стратегічних розробках. Проте головною особливістю цієї посади є забезпечення фізичного, емоційного і соціального благополуччя хворих з ревматоїдним артритом з використанням підходу, орієнтованого на пацієнта.
Клінічні аспекти
Більшість медсестер–спеціалістів з ревматології повинні обслуговувати відділення, очолювані медсестрою, де вони оцінюють і лікують пацієнтів, які працюють в тісній співпраці з консультантом–ревматологом. Це, як правило, включає обстеження суглобів, оцінку загального стану хворого, моніторинг результатів аналізу крові хворих, що отримують імуносупресивне лікування і призначення аналізів та перегляд досліджень. Деякі медсестри–спеціалісти з ревматології виконують ін’єкції в суглоби, призначають і змінюють лікування та проводять інші методи лікування, такі як інфузії. Медсестра–спеціаліст з ревматології зазвичай є професіоналом, який є головним координатором медичної допомоги в мультидисциплінарній команді, звертається до членів команди та інших установ, якщо це необхідно.
Освіта, підтримка та консультації
Діагноз ревматоїдного артриту може бути спустошливим, але разом з членами команди медсестра–спеціаліст з ревматології може надавати підтримку і пораду, щоб допомогти зменшити страх і занепокоєння, які може викликати такий діагноз. Детальне пояснення діагнозу, медикаментозної терапії та інших стратегій і методів лікування може надавати медсестра–спеціаліст з ревматології на початку захворювання і впродовж хвороби. У зв’язку з впливом патологічного процесу і заклопотаністю з приводу початку лікування, головним елементом ролі медсестри–спеціаліста з ревматології є надання легко доступної точки контакту для пацієнтів і осіб, які здійснюють за ними догляд. Більшість медсестер–спеціалістів з ревматології надають цю послугу по телефону довіри. У співпраці з мультидисциплінарною командою багато медсестер–спеціалістів з ревматології надають допомогу групам пацієнтів з самолікування з метою розширення можливостей пацієнтів і допомогти їм впоратися зі своїм захворюванням.
Освіта є важливим елементом, і більшість медсестер–спеціалістів з ревматології виступають в якості допоміжної ланки для колег і широкої медичної громадськості. Деякі з них беруть участь у розробці і реалізації освітніх програм з ревматології для медичних професіоналів. Це може бути від днів навчання до формального диплома, курсів у співпраці з університетом з метою підвищення знань і досвіду в догляді за пацієнтами з ревматоїдним артритом.
Хоча ГРН (особливо представники пацієнтів) визнала важливу роль медсестри–спеціаліста з ревматоїдного артриту, як описано вище, було визнано недоречним шукати докази з ролі тільки цієї спеціальності, отже, роль мультидисциплінарних команд вивчалася в повному обсязі.
6.1.2. Клінічне методологічне введення
Ми шукали дослідження, які вивчали користь і шкоду мультидисциплінарних команд щодо пацієнтів з ревматоїдним артритом з недавнім початком та зі встановленим діагнозом захворювання. Окремі дослідження були проведені в популяції Великобританії, і якщо це була популяція зі змішаним артритом, то в ній повинно було бути > 75 % хворих на РА або проводився аналіз в підгрупі з РА.
Було знайдено п’ять РКД147, 152 і три серії випадків153, 155, які відповідали критеріям включення. Одне з РКД було опубліковано у вигляді двох окремих документів148, 149, які повідомляли про різний час спостереження, тому дане РКД було враховано лише один раз. Проте тут є посилання на результати обох робіт. Два РКД151, 152 були виключені як докази в зв’язку з методологічними обмеженнями (вони були не сліпі, і ІТТ аналіз не проводився). Методологічні обмеження інших включених РКД були наступні: всі вони були оцінені як 1+, оскільки вони були або сліпими або ІТТ аналіз не проводився.
Ранній РА
Дві роботи серії випадків154, 155: N = 110 і N = 70 пацієнтів відповідно, оцінювали вплив програми медичної допомоги мультидисциплінарною командою на пацієнтів з недавнім початком РА. Prier et al.154 проводили 3–місячний курс лікування, в той час як Nordmark et al.155 проводили 2–річний курс лікування.
РА з хронічним перебігом
Були виявлені три РКД147, 150 і одна серія випадків153 щодо пацієнтів із встановленим РА.
Три РКД порівнювали лікування МДК з лікуванням без команди (N = 59) (Ahlmen)147, рутинним амбулаторним лікуванням (N = 68) (Vliet Vlieland,Vlijeland)148, 149 або контрольним списком очікування (N = 68) (Scholten)150. Усі мали курс лікування впродовж 1 року з подальшим контролем на 2 році (Vlijeland) і 5 році (Scholten). Серія випадків153 вивчала вплив програми допомоги МДК на N = 92 пацієнтах, які мали 3–тижневий курс лікування з контролем на 3 місяці.
6.1.3. Методологічне введення з економіки в охороні здоров’я
Було виявлено і оцінено одне дослідження. Van den Hout et al.156 — це голландське дослідження корисності витрат, яке порівнювало надання медичної допомоги клінічною медсестрою–спеціалістом, стаціонарну медичну допомогу мультидисциплінарної команди і медичну допомогу МДК пацієнтам денного стаціонару. Дві роботи157, 158 були виключені, оскільки не стосувалися МДК.
6.1.4. Заяви про клінічні докази
Ранній РА
Симптоми, функції і якість життя
— В одній серії випадків154 виявлено, що програма надання медичної допомоги МДК призвела до незначних змін якості життя (AIMS) на 3 місяці спостереження. Рівень 3
— В одній серії випадків155 виявили, що після 2 років лікування МДК всі пацієнти відчували значне полегшення болю (середня зміна ВАШ: від –16 до –24, усі р < 0,05), за винятком тих, хто покинув роботу і отримував допомогу по хворобі. Рівень 3
Знання і задоволеність
В одній серії випадків154 виявили, що в пацієнтів, які брали участь в програмі допомоги МДК, було значне розширення знань з РА на 3 місяці спостереження (середнє збільшення балів тесту 6,2, р < 0,0001). Рівень 3
Застосування лікування РА
В одній серії випадків155 виявлено, що в пацієнтів, які брали участь в програмі допомоги МДК, не було ніяких змін щодо кількості пацієнтів, які отримували DMARDs, а кількість пацієнтів, які отримували метотрексат або комбіновану терапію з метотрексатом, збільшилася з 8 % до 41 % на 2 році спостереження (кінець програми лікування МДК), а також тих, хто отримував глюкокортикоїди (збільшення з 11 % до 15 %). Рівень 3
РА з хронічним перебігом
Симптоми
— Два РКД147–149 встановили, що була незначна різниця щодо суглобового індексу Рітчі на 12 тижні147, 52 і 104 тижнях148, 149. Також незначна різниця була виявлена в самооцінці фізичного дискомфорту (шкала симптомів, BSS) і LAI (індекс суглобів Ленсбері — болючість суглобів при натисканні або при русі) на 12 тижні147 і болю (ВАШ), кількості набряклих суглобів, втоми і сили стискування на 12, 52 і 104 тижнях148, 149; ACR20 на 104 тижні148, 149. Рівень 1+
— Одне РКД148, 149 виявило, що лікування в стаціонарі МДК була значно краще, ніж звичайне амбулаторне лікування: ранкова скутість на 12 тижні (MD 2,62, р < 0,05) і на ACR20 на 12 тижні (MD 10,0, р < 0,05) і 52 тижні (MD 18, р < 0,05). Рівень 1+
— Одна серія випадків153 виявила, що у пацієнтів, які брали участь в програмі допомоги МДК, було значне поліпшення: в DAS (середня зміна — 0,59, 95% ДІ від — 0,8 до — 0,38, р < 0,001), біль, ВАШ (середня зміна –12, 95% ДІ від –17 до –7, р < 0,05), набряк суглобів (середня зміна –3,3, 95% ДІ від –5,2 до –1,4, р < 0,05) і суглобовий індекс Рітчі (середня зміна –1,6, 95% ДІ від –2,5 до –0,7, р < 0,05) на 3 місяці спостереження, і 26 % і 52 % пацієнтів відповідали критеріям відповіді ACR20 і EULAR. Рівень 3
Функція
— Одне РКД148, 149 встановило, що не було значної різниці між лікуванням в стаціонарі МДК і рутинним амбулаторним лікуванням щодо оцінки HAQ на 12, 52 і 104 тижнях. Рівень 1+
— Проте інше РКД150 виявило, що програма лікування MДК значно покращила показники з непрацездатності HAQ (шкала 0–5) на 52 тижні (середня зміна –0,4, р < 0,001) і на 5 році (середня зміна 0,9, р < 0,0001). Рівень 1+
— Одна серія випадків153 виявила, що у пацієнтів, які брали участь в програмі допомоги MDT, було значне поліпшення в HAQ (середня зміна — 0,16, 95% ДІ від –0,24 до –0,08, р < 0,05) і SOFI (середня зміна — 2,6, 95% ДІ від –3,5 до –1,7, р < 0,05) через 3 місяці, і 26 % і 52 % пацієнтів відповідали критеріям відповіді ACR20 і EULAR відповідно. Рівень 3
Загальна оцінка
— Одне РКД148, 149 виявило, що стаціонарне лікування MДК було значно краще щодо загальної оцінки активності захворювання пацієнта (ВАШ) впродовж 4 тижнів (MD 3,9, р < 0,05), 12 тижнів (MD 3,3, р < 0,05) і 52 тижнів (MD 2,8, р < 0,05) впродовж 4, 12 і 52 тижнів, проте була незначна різниця на 104 тижні. Рівень 1+
— Одна серія випадків153 виявила, що пацієнти, які брали участь у програмі медичної допомоги мультидисциплінарною командою, мали значне поліпшення: загальна оцінка пацієнтом і лікарем активності захворювання (ВАШ середня зміна –13, 95% ДІ від –18 до –8, р < 0,05) на 3 місяці спостереження. Рівень 3
Якість життя
— Одне РКД147 виявило, що медична допомога МДК мала значно кращий вплив: загальний стан здоров’я (профіль впливу хвороби — SIP; MD 3,5, р < 0,05), але незначний щодо показників MACL (настрій) на 12 тижні. Рівень 1+
— Одне РКД148, 149 виявило, що стаціонарне лікування MДК було значно краще, ніж звичайне амбулаторне лікування щодо: тривоги (шкала 0–10) на 12 тижні (MD 3,3, р < 0,05), але незначне на 52 і 104 тижні; депресії (шкала 0–10) на 12 тижнів (MD 2,4, р < 0,05), але незначне на 52 і 104 тижні. Рівень 1+
— Одне РКД150 встановило, що на 52 тижні стаціонарне лікування MДК значно покращило здатність пацієнта справлятися з хворобою (шкала FQCI від 5 до 25) (середня зміна –1,9, р < 0,01) і показників депресії Бека (шкала 0–63) (середня зміна 2,5, р < 0,001). Рівень 1+
Біохімічні маркери
— Два РКД147–149 встановили, що була незначна різниця між двома групами щодо СРБ на 12 тижні147 і ШОЕ і СРБ на 12, 52 і 104 тижнях148, 149. Рівень 1+
— Одна серія випадків153 виявила, що пацієнти, які брали участь в програмі медичної допомоги МДК, мали значне поліпшення в ШОЕ (середня зміна –6, 95% ДІ від –10 до — 3, р < 0,05) на 3 місяці спостереження. Рівень 3
Використання ліків/лікування
— Одне РКД встановило, що була незначна різниця між двома групами: використання препаратів (DMARDs, НППЗ і глюкокортикоїдів) на 12 тижні. Рівень 1+
— Одне РКД150 виявило, що програма медичної допомоги МДК на 52 тижні покращила використання пристроїв для захисту суглобів (середня зміна 68,5 %, р < 0,001), регулярного виконання релаксаційних вправ (середня зміна 60,5 %, р < 0,001) і регулярної лікувальної фізкультури (середня зміна 26,3, р < 0,001). Рівень 1+
6.1.5. Резюме заяв про докази
При ранньому РА роль МДК включає:
— визнання важливості і ефективності праці та соціальної ролі і забезпечення того, щоб пацієнт міг це виконувати155;
— відповідальність за навчання пацієнта154;
— забезпечення того, щоб пацієнти мали доступ до широкого кола спеціалістів різного профілю і кваліфікації154;
— моніторинг захворювань і відповідні зміни DMARD терапії для того, щоб підтримувати належний контроль155.
При РА з хронічним перебігом МДК може:
— бути корисною у моніторингу та забезпеченні належного контролю захворювання148, 149, 153, а також у наданні допомоги щодо поліпшення настрою пацієнта і можливості справлятися з цим захворюванням впродовж короткого періоду147–150. Проте не вистачає доказів, щоб показати, чи є користь впродовж тривалого періоду148, 149.
— впливати на функції пацієнта150, 153, проте слід зазначити, що докази суперечливі148, 149.
6.1.6. Від доказів до рекомендацій
Незважаючи на відсутність продемонстрованої користі, загальна думка ГРН визнає важливість МДК, яка може надати широкий спектр послуг пацієнтам з РА, використовуючи знання та кваліфікацію спеціалістів, які доповнюють знання і досвід ревматолога, вирішуючи інші проблеми, крім суто медичних, як при недавньому початку РА, так і при встановленому РА. Було також відзначено, що можливість для пацієнтів підняти будь–які питання, що стосуються їхньої хвороби (необхідність визначена у розділі «Сприйняття пацієнтом і переконання» — див. розділ 6.3), може найбільш доцільно вирішуватись шляхом забезпечення постійного доступу до МДК.
Незважаючи на брак доказів, ГРН визнала, що з точки зору перспективи пацієнта такі спеціалісти МДК, як медсестра–спеціаліст, проводять більше часу з пацієнтами в оцінці активності захворювання та моніторингу впливу препаратів в лікуванні їх захворювання. Партнерство в МДК є ключовим елементом у наданні належної медичної допомоги пацієнтам, що було відзначено у доповіді Quality for All Darzi report в червні 2008 року. Існує стурбованість тим, що за відсутності комплексного підходу МДК люди можуть працювати в ізоляції, лікування може бути фрагментованим або дублюватися, і це, в свою чергу, може впливати на якість отриманої пацієнтом медичної допомоги. Тому точка зору ГРН полягає в тому, що дуже важливо, щоб один з призначуваних членів МДК був відповідальним за координацію лікування своїх пацієнтів.
Рекомендації
R9 Пацієнти з РА повинні мати постійний доступ до мультидисциплінарної команди. Це повинно забезпечувати можливість періодичної оцінки (див. рекомендації 36 і 37) впливу хвороби на їхнє життя (наприклад, біль, втому, повсякденну діяльність, мобільність, здатність працювати або брати участь у соціальній діяльності або дозвіллі, якість життя, настрій, сексуальні стосунки) і допомагати керувати станом.
R10 Пацієнти з РА повинні мати доступ до члена мультидисциплінарної команди (наприклад, до медсестри–спеціаліста), який відповідає за координацію їхнього лікування.
Коментар робочої групи
В Україні створення МДК є бажаним у спеціалізованих ревматологічних відділеннях, оскільки збалансує навантаження на членів медичного колективу та зменшить навантаження на лікуючого лікаря стосовно проведення бесід з хворим щодо деталей хвороби та особливостей лікування, що співпадає з принципами «treat–to–target».
6.2. Фізіотерапія
6.2.1. Клінічне введення
Незважаючи на фармакологічні досягнення у лікуванні РА, багато пацієнтів дотепер вперше звертаються до лікаря з функціональними проблемами, які може вирішити фізіотерапія.
Фізіотерапія може зменшити біль і скутість, попередити деформацію і максимізувати функцію, незалежність та якість життя. На це націлені різні втручання, які можуть бути зручно згруповані за активними і пасивними назвами. У першій — освіта і вправи є ключовими компонентами, і до недавнього часу страх прискорення ураження суглобів обмежує активність до руху та ізометричних вправ. Проте за останні кілька десятиліть спостерігається зміна парадигми в напрямку аеродинамічних вправ, частково підтверджених дослідженнями, які показують, що пацієнти з РА є неактивними159 і мають більший ризик серцево–судинних захворювань і переломів, ніж хворі без РА160.
За даними Всесвітньої конфедерації фізіотерапевтів, фізіотерапія «спрямована на виявлення і максимізацію потенціалу руху у напрямку зміцнення здоров’я, профілактики, лікування і реабілітації в партнерстві зі своїми клієнтами»161. Компоненти фізіотерапевтичних втручань включають:
— Лікувальна фізкультура — на землі і у воді (гідротерапія/водна фізіотерапія), включає аеробну активність, гнучкість і вправи на зміцнення м’язів, основні вправи на стабільність, відновлення рівноваги, сприяння розвитку фізично активного способу життя.
— Навчання пацієнтів і самоконтроль — стратегії захисту суглобів, збереження енергії/управління втомою, навчання гігієні сну, управління спалахами хвороби, стратегії з полегшення болю, навчання релаксації, фізичним вправам і рекомендації з фізичної активності.
— Термотерапія — гарячі/холодні пакети, парафінові/воскові ванни та інфрачервоні процедури.
— Електротерапія — черезшкірна електрична стимуляція нервів (TENS), ультразвук.
— Імпульсна електромагнітна енергія (РЕМЕ), інтерференційна терапія (IFT) і лазер.
— Забезпечення та навчання використанню допоміжних пристроїв — милиць, шин, ортезів, устілок.
— Мануальна терапія — включає мобілізацію, маніпуляції, міофасціальне полегшення, терапія тригерних точок, голковколювання і масаж.
Повідомляється про втричі підвищений ризик переломів стегна при ревматоїдному артриті в центральній Фінляндії162. Частково на це можуть впливати пацієнти з РА, які мають обмежені фізичні можливості з самого початку захворювання163. Інтуїтивно здається, що стратегії вправ, спрямованих на поліпшення і підтримку здоров’я, можуть підвищити біомеханічну ефективність. Користь від фізичної активності та стратегії фізичних вправ може бути очевидною тільки тоді, коли є достатній стимул, коли вони виконуються регулярно і стабільно, тому питання згоди може бути настільки ж важливим, як і сама активність.
Пасивне лікування, успіх якого залежить не стільки від згоди пацієнта, включає методи мануальної терапії та застосування електрофізичних засобів. Вони використовуються обмежено при певних клінічних порушеннях і спрямовані на розширення можливостей щодо виконання фізичних вправ або збільшення фізичної активності. Мануальна терапія — це «клінічний підхід, при якому використовуються певні методи руками», який включає мобілізацію і маніпуляції на суглобах і м’яких тканинах164. Електрофізичні засоби представляють як термотерапію (поверхневе тепло/холод), так і електротерапію (див. приклади вище) і використовуються, щоб зменшити біль і поліпшити функцію.
Фізіотерапія РА застосовує мультимодальний або комплексний підхід, який полягає в поєднанні навчання, фізичних вправ і застосування знеболюючих засобів залежно від клінічних потреб і цілей, узгоджених між лікарем і пацієнтом. Заохочення в застосуванні стратегій самодопомоги і самоефективності щодо регулярної фізичної активності є загальною стратегією і потребує підтримки і зміцнення навчальних заходів щодо зміцнення здоров’я.
При розгляді ефективності фізіотерапії необхідно провести оцінку доказів фізіотерапії в мінімізації впливу захворювання на симптоми, ураження суглобів, функцію і якість життя впродовж життя з РА. Зокрема:
1. Які стратегії фізичних вправ, якщо такі є, найбільш корисні щодо симптомів, уражень суглобів, функції та якості життя?
2. Які зі стратегій мануальної терапії найкраще і найтриваліше можуть забезпечити полегшення симптомів і покращити функцію?
3. Які електрофізичні засоби можуть запропонувати найбільші терапевтичні ефекти з точки зору симптоматичного полегшення і покращення функції і тривалості?
6.2.2. Клінічне методологічне введення
Ми шукали дослідження, які вивчали ефективність різних аспектів фізіотерапії щодо симптомів, ураження суглобів, функції і якості життя у пацієнтів з РА (ранній РА і встановлене захворювання). У зв’язку з великим обсягом доказів були відібрані тільки метааналізи і РКД, які стосувалися відповідної групи населення Великобританії і певного втручання, якщо популяція включала змішаний артрит, то повинно було бути > 75 % РА або аналізу підгруп РА, а також випробувань, які досліджували TENS і вправи, вибірка повинна бути N ≥ 50 (і зміцнюючих вправ, N > 70).
Було знайдено п’ять системних оглядів/MA165–169 і 17 РКД170–191, які відповідали критеріям включення. Три з цих РКД були опубліковані у вигляді статей, які повідомляли про різні результати або точки часу, і тому ці випробування були враховані один раз, проте повідомлялися результати з усіх робіт з посиланнями на них у цій роботі. Три РКД172, 185–188, 192, 193 були виключені через методологічні обмеження (несліпі і ITT аналіз не проводився). Методологічні обмеження решти РКД були наступні: всі вони були оцінені 1+ через те, що були сліпими і ITT аналіз не проводився (6 РКД), або несліпі і ITT аналіз виконувався (1 РКД), або сліпе і ITT аналіз був виконаний, але мали високі показники відсіву (2 РКД). Одне з РКД190 з вправ було включено, хоча воно мало невелику вибірку < 70, тому що це було єдине випробування з вправ, яке розглядало пацієнтів з активним РА.
Всі випробування, за винятком одного191 (пацієнти з нещодавно виявленим РА), проводилися стосовно пацієнтів з встановленим РА, МА використовували випробування зі змішаною популяцією (недавній початок і РА з хронічним перебігом).
Змішана популяція (ранній і РА з хронічним перебігом)
Було виявлено п’ять систематичних оглядів/MA165–169, які відповідали критеріям. Всі МА були добре проведені, проте РКД, включені в аналіз, були різної якості. Перший систематичний огляд/MA165 розглядав терапію теплом і холодом і включав 7 РКД в аналіз, всі були від поганої до помірної якості. Проте РКД відрізнявся щодо:
— пацієнтів (N = 4 стаціонарні, N = 7 амбулаторні);
— тривалості захворювання (від 5 років або менше до 14 років);
— втручання (1 РКД кожен на лікуванні льодом, парафінових ваннах плюс вправи, трьох різних методах термотерапії (парафінові ванни, фарадичні ванни і ультразвук), різних температурах нагріву, 2 РКД тепла);
— групи порівняння (контроль, фізичні вправи, кріо–терапія);
— розміру дослідження (від N = 14 до N = 90).
Другий систематичний огляд/MA166 розглядав лазерну терапію і включав в аналіз 6 РКД, які відрізнялися щодо:
— втручання — довжина хвилі (1 РКД 633 нм, 1 РКД 850 нм, 1 РКД 820 нм, 1 РКД 830 нм, 1 РКД 820 нм і 1 РКД 632,5 нм);
— втручання — вихідна потужність (1 РКД 10 мВт, 1 РКД 940 мВт, 1 РКД 40 мВт, 1 РКД 21 мВт, 1 РКД 15 мВт і 1 РКД 1 мВт);
— порівняння (5 РКД з плацебо і 1 РКД контралатерального суглоба);
— розміру дослідження (від N = 17 до N = 72);
— засліплення (4 РКД подвійні сліпі, 1 РКД потрійне сліпе, 1 РКД частково сліпе).
Третій систематичний огляд/MA167 розглядав лікування TENS і включав 3 РКД (всі належної якості) в аналіз, які відрізнялися щодо:
— втручання (1 РКД 15 хвилин 70 Гц, 1 РКД 20 хвилин 100 Гц, 1 РКД 5 хвилин 70 Гц);
— групи порівняння (2 РКД з плацебо, 1 РКД –AL–TENS);
— розміру дослідження (від N = 19 до N = 33);
— засліплення (1 РКД подвійне сліпе, 1 РКД сліпе, 1 РКД несліпе);
— спостереження (1 РКД — 15 днів, 2 РКД — не вказано).
Четвертий систематичний огляд/МА168 розглядав ультразвукову терапію і включав 2 РКД (які були від поганої до помірної якості) в аналіз і мав 3–тижневу фазу лікування. Проте РКД відрізнялися щодо:
— втручання (1 РКД — ультразвук поєднувався з вправами або з електричним струмом, парафіновими ваннами або електричним струмом і вправами; 1 РКД — лише ультразвук);
— групи порівняння (плацебо ультразвук);
— розміру дослідження (1 РКД N = 30 і 1 РКД N = 50);
— засліплення (1 РКД подвійне сліпе, 1 РКД несліпе).
П’ятий систематичний огляд/МА169 розглядав вправи тай–чи і включав в аналіз 4 РКД, які були поганої якості і не сліпі, проте відрізнялися щодо:
— втручання (1 РКД — навчання щодо здоров’я + діапазон руху (ROM) — танці та релаксація); 1 РКД — пероральні китайські трави + навчання + вправи + масаж + гарячий компрес, 2 РКД — вправи тай–чи);
— групи порівняння (2 РКД — пероральні китайські трави + відсутність вправ);
— розміру дослідження (від N = 28 і N = 100);
— тривалості дослідження — тривалість втручання (від 8 до 10 тижнів).
Ранній РА
Включене РКД191 було методологічно відповідним рандомізованим дослідженням паралельних груп з N = 228 пацієнтів. Випробування порівнювало дві різні групи лікування: вправи (здорова фізична активність) порівняно зі звичайною терапією впродовж 1–річної фази лікування.
РА з хронічним перебігом
13 включених РКД відрізнялися щодо наступного:
— розміру вибірки (від N = 57 до N = 310);
— засліплення (12 РКД сліпі, 1 РКД несліпі);
— тривалості дослідження (від 3 тижнів до 2 років, спостереження 1 РКД 6 місяців);
— лікування (2 РКД — загальна РТ, 11 РКД — вправи).
6.2.3. Методологічне введення з економіки в охороні здоров’я
Було виявлено і оцінено одне дослідження. Van den Hout et al.194 — це голландський аналіз корисності витрат, який порівнює довготривалу програму вправ високої інтенсивності (програма РАРІТ) зі звичайною індивідуальною фізичною терапією.
6.2.4. Заяви про клінічні докази
Змішана популяція (ранній РА і РА з хронічним перебігом) (табл. 6.1, 6.2)
Той же самий MA166 також виявив, що не було ні–яких істотних відмінностей між лазером і плацебо щодо: методологічної якості; тривалості лікування (болю); суглобів порівняно з додаванням нервів (біль) і довжиною хвилі (біль). Проте була значна різниця на користь дози: низькі дози лазерної терапії (≤ 3 Дж/см2) порівняно з плацебо, але не високі дози лазерної терапії порівняно з плацебо (щодо зміни болю (ВАШ), але незначний ефект щодо сили стискання). Рівень 1++ (табл. 6.3–6.5)
Ранній РА
Фізичні вправи порівняно з контрольною групою (звичайне лікування)
Одне РКД191 виявило, що програма фізичних вправ була значно кращою, ніж у контрольній групі (звичайне лікування) на 1 році: EuroQol EQ–5D (ВАШ), тест на своєчасне вставання і сили стискання (обидва р < 0,01). Проте, була незначна різниця: ROM; болю (ВАШ); HAQ–DI; DAS28; відсоток пацієнтів, які отримували різні види лікування та відсоток пацієнтів, які досягли здорової фізичної активності. Рівень 1++
РА з хронічним перебігом (табл. 6.6)
6.2.5. Заяви про докази з економіки в охороні здоров’я
Середньорічна вартість медичної допомоги пацієнту за програмою РАPIT складала 2115 євро порівняно з 1683 євро для звичайного лікування. Група РАPIT не показала суттєвої різниці у QALY за SF–6D і EQ–5D і ВАШ програми звичайного лікування показали вищий показник QALY. Дослідження повідомляє ICER щодо загальних соціальних витрат (але не прямих витрат на медичне обслуговування), підсумувавши, що використання EQ–5D і ВАШ, UC має більшу корисність витрат, а використання SF–6D ICER — це 67 000 євро за QALY, але без суттєвої різниці щодо чистої користі. Тому цей документ не показує переконливих доказів економічної ефективності на підтримку програми вправ високої інтенсивності194.
6.2.6. Резюме заяв про докази
Загалом фізичні вправи викликають позитивну відповідь з точки зору фізичної та психологічної користі149, 169, 171, 177, 181–183. Програми аеробних (динамічних) вправ поліпшують компоненти пов’язаного зі здоров’ям фітнесу, поліпшують психологічний стан, зменшують біль і втому і позитивно впливають на функціональні можливості без загострення захворювання або прискорення ураження суглобів180–183. Спеціальні вправи, спрямовані на зміцнення діапазону рухів (гнучкість суглобів) або сили м’язів (силові тренування) призводять до деякого поліпшення171, 181. Більшість доказів отримано у пацієнтів з хронічним стабільним РА функціональних класів I/III181, 183. Вправи у воді приносять аналогічну фізичну користь, як і вправи на землі, але можуть мати додаткові і важливі психологічні ефекти (які позитивно впливають на згоду)171, 177. Прийняття стратегій регулярної фізичної активності та вправ буде більше успішним, якщо є особистий контакт з медичними професіоналами, коли обговорюються користь і перепони до вправ і є можливість групового контакту.
Існує ряд доказів, що комплексна медична допомога, яка надається в громаді і вирішує конкретні потреби пацієнта через навчання, фізичні вправи і умови полегшення болю, приносить довготривалу користь щодо власної ефективності, знань з лікування хвороби і деяких вимірів активності захворювання і функції173, 174.
Даних щодо очевидної користі електрофізичних засобів у лікуванні РА недостатньо. Наявні дані вказують на суперечливі результати, в основному, дослідження поганої якості, в яких втручання і результати сплутують синтез, тому особливої довіри до результатів немає. Проте деякі засоби, наприклад TENS, воскові ванни, показують, що може відбуватися короткотривале полегшення симптомів165, 167.
Терапевтичний ефект мануальної терапії не може бути визначений для РА в зв’язку з браком літератури в цій галузі.
6.2.7. Від доказів до рекомендацій
Фізичні вправи на суші або в воді корисні для більшості хворих з ревматоїдним артритом.
ГРН вважає, що необхідно, щоб усі пацієнти з ревматоїдним артритом мали доступ до періодичного огляду, консультацій з фізіотерапії щодо включення належним чином підготовлених вправ, направлених на покращення як загального здоров’я, пов’язаного з фітнесом, так і конкретних проблем опорно–рухового апарату і рівноваги в їхньому житті.
Узгодженість щодо вправ була підкреслена як особлива проблема. Консенсус ГРН полягав у тому, що дуже важливо, щоб всі члени МДК надавали людям з ревматоїдним артритом послідовну підтверджуючу інформацію про їх користь.
ГРН зазначила, що електрофізичні засоби, такі як ванни з воском і TENS, були аналогічними щодо знеболення, хоча немає жодних доказів довготривалого впливу на прогресування захворювання, багато пацієнтів вважають, що вони надають короткотривале полегшення симптомів. Консенсус ГРН полягав у тому, що передчасним є відмовлятися від цих процедур, які можуть надавати пацієнтам паліативний ефект.
При розгляді доказів з комплексної фізіотерапії ГРН зазначила, що результати перспективні і буде отримана користь від додаткових досліджень.
Рекомендації
R11 Пацієнти з РА повинні мати доступ до фізіотерапевта щодо періодичного огляду (див. Рекомендації 36 і 37), щоб:
— поліпшити загальну фізичну форму і заохотити до регулярного виконання фізичних вправ;
— вивчити вправи для зміцнення гнучкості суглобів, сили м’язів і керування іншими функціональними порушеннями;
— навчитися полегшувати біль на короткий термін такими методами, як черезшкірна електрична стимулятори нервів [TENS] і ванни з воском.
6.3. Трудотерапія
6.3.1. Клінічне введення
Трудотерапія має на меті поліпшення здатності людини виконувати повсякденну діяльність, брати участь у важливій для життя роботі, відігравати важливу роль на роботі, вдома, на відпочинку та у соціальному житті, сприяти успішній адаптації до життя, а також запобігати або зменшувати функціональні і психологічні проблеми. Комплексні програми трудотерапії можуть включати широкий спектр заходів (див. таблицю 6.11 нижче). Здатність до самодопомоги з використанням таких стратегій, як захист суглобів і керування втомою, є центральною частиною лікування. Підвищення узгодженості необхідне, і трудотерапія часто пропонує когнітивно–поведінкові підходи. Приділяється особлива увага трудотерапії на підтримку функції руки при РА. «Ми користуємося руками у виконанні усієї роботи, тому зберегти їх дуже важливо для мене». Трудова реабілітація надається тим, хто ще працює з ризиком втрати роботи, а також безробітним. «Робота допомогла мені підвищити самооцінку. Я щиро вірю, що якщо б я не працював, мій РА прогресував би швидше, і мені було б гірше, ніж зараз». «Візит [оцінка трудотерапевта роботи] став поворотним моментом в моєму житті... з пристосуванням до стану, я зміг продовжувати підтримувати свою сім’ю... і досягти успіху на робочому місці» (Національне товариство з ревматоїдного артриту, NРАS буклет: «Я хочу працювати: керівництво з самодопомоги людям з РА» (2007))13 (табл. 6.11).
Трудотерапія має подвійне навчання щодо відновлення фізичного і психічного здоров’я. Багато хворих з РА обговорюють «розчарування», спричинене численними функціональними труднощами, болем, втомою, а іноді відчуття напруги або поганий настрій. Таким чином, психологічне втручання часто використовують, щоб допомогти людям в адаптації до життя зі своєю хворобою.
Дані показують195–199, що на ранньому етапі близько 60 % хворих мають проблеми, при яких можливо отримати користь від трудотерапії з приводу захворювання руки (захист суглобів, вправи для рук, ортези) і навчання з діяльності у повсякденному житті (ADL). Більше третини хворих, які страждають на РА, можуть отримати користь від повернення до роботи. На пізніших стадіях захворювання цей показник може бути вищим. Які є докази того, що трудотерапія впливає на симптоми, прогресування захворювання, функції та якість життя при початковому або встановленому РА? Зокрема:
— Чи допомагає трудотерапія підтримувати функціональну здатність та/або сповільнити її погіршення?
— Чи терапія руки (тобто захист суглобів, вправи для рук, шини) має вплив на підтримання функції руки?
— Чи трудотерапія допомагає підтримувати або поліпшувати участь у соціальному житті, зокрема в роботі?
— Чи трудотерапія має вплив на психологічний стан?
6.3.2. Клінічне методологічне введення
Ми шукали дослідження, які вивчали ефективність різних аспектів трудотерапії щодо симптомів, ураження суглобів, функції і якості життя у пацієнтів з РА (недавній початок і встановлене захворювання). Через велику кількість доказів відбиралися тільки МА і РКД, які стосувалися населення Великобританії; якщо популяція включала змішаний артрит, то повинно було бути > 75 % РА, аналіз підгруп РА і випробування, які розглядають шини, ортези або когнітивно–поведінкову терапію повинні включати ≥ 30 осіб.
Було знайдено два MA200, 201 і вісім РКД136, 202–209, які відповідали критеріям включення. Одне РКД207, 208 було опубліковано у вигляді двох окремих документів і повідомляло про результати 18–місячного і 5–річного спостереження РКД, вже включеного в МА з психологічних втручань200. Було знайдено два РКД136, 207, які вивчали пацієнтів з недавнім початком РА, всі інші були РКД, які проводилися за участю пацієнтів із встановленим РА, і два МА використовували випробування, які мали змішані популяції (недавній початок і РА з хронічним перебігом). Методологічні обмеження РКД були наступними: ті, які мали 1+, були однобічно сліпими, і аналіз ITT не виконувався (три РКД), або не сліпі, і ITT аналіз проводився (два РКД). Випробування, оцінене 1++, було однобічно засліпленим, і автори провели аналіз ITT.
Примітка: дослідження про захист суглобів були описані в розділі навчання.
Змішані популяції (недавній початок і РА з хронічним перебігом)
Було знайдено два MA200, 201 і РКД, у яких порівнювали психологічні втручання200 або шини і ортези201. Обидва МА були добре проведені, проте РКД, включені в аналіз, були різної якості.
Перший систематичний огляд/MA200 включав 25 РКД в аналіз, які відрізнялися стосовно:
— розміру дослідження (від N = 8 до N = 141);
— якості дослідження — максимально 10 балів (деякі поганої, деякі належної якості);
— тривалості дослідження — тривалість втручання (від 3 днів до 9 місяців з наступним діапазоном від 2–18 місяців);
— порівняльних груп (плацебо; звичайне лікування; список очікування);
— втручання (N = 13 — мультимодальні когнітивно–поведінкові втручання, N = 5 — включений біологічний зворотний зв’язок, N = 5 — більш традиційні психотерапевтичні втручання, N = 2 — втручання включали пацієнтів, які виражали емоції важко або мали стресові ситуації).
Другий систематичний огляд/MA201 включав 7 РКД в аналіз, всі розглядали робочі шини на зап’ясті (РКД ортезів були охоплені в питанні подіатрії). Проте РКД відрізнялися щодо:
— групи порівняння (3 РКД без шин, 2 РКД — інші шини);
— розміру дослідження (від N = 10 до N = 110 щодо шин на зап’ястя);
— якості дослідження — максимально 5 балів (деякі поганої і деякі належної якості щодо шин на зап’ястя);
— тривалості дослідження — тривалість втручання (від 1 тижня до 6 місяців для шин на зап’ястя).
Ранній РА
Два включені РКД136, 207 порівнювали трудотерапію зі звичайним лікуванням і мали розмір вибірки N = 326 і N = 53 відповідно. Одне РКД136 мало фазу лікування від 6 до 8 тижнів з 6–місячним спостереженням, а інше РКД207 було 18–місячним спостереженням, включеним в МА200 з психологічних втручань.
РА з хронічним перебігом
7 включених РКД136, 202–206 відрізнялися щодо наступного:
— розміру вибірки (від N = 47 до N = 144);
— засліплення (1 РКД подвійне сліпе, 4 РКД однобічно засліплені, 2 РКД несліпі);
— тривалості випробування (від 4 тижнів до 6 місяців, спостереження від 6 місяців до 5 років);
— лікування (4 РКД — когнітивно–поведінкова терапія порівняно зі стандартною терапією або плацебо; 1 РКД — комерційні шини порівняно з двома комерційними шинами; 1 РКД — трудотерапія порівняно з відсутністю лікування; 1 РКД — когнітивно–поведінкова терапія болю проти терапії регулювання емоцій проти конт–рольної групи навчання).
6.3.3. Методологія клініко–економічного обґрунтування
Було знайдено та проаналізовано два дослідження. Дослідження Li et al.158 є аналізом співвідношення витрати — ефективність у Канаді, в якому порівнювали 2 моделі: лікування за участю вузькопрофільного спеціа–ліста (ПТМ) та спеціаліста широкого профілю (ТТМ). Дослідження Van den Hout et al.194 є порівняльним аналізом співвідношення витрати — ефективність мультидисциплінарної програми робочої реабілітації хворих та звичайного догляду за пацієнтами, які можуть втратити роботу.
6.3.4. Клінічні дані
Рання стадія РА
В одному РКД136 було продемонстровано, що використання методів реабілітації було достовірно ефективнішим, ніж контроль (відсутність втручання), за наступними показниками: деякі методи самообслуговування (особливо вправи для рук, захист суглобів, відпочинок), отримання лангет для відпочинку та роботи, отримання та використання допоміжних пристроїв. Однак, різниця була недостовірною для наступних показників: HAQ, DAS28, AIMS , шкала самооцінки. Рівень 1++
6.3.5. Методологія клініко–економічного обґрунтування
В дослідженні Li et al.158 не було продемонстровано статистично достовірної різниці між результатами анкетування за шкалою якості життя та іншими соціальними тестами, однак було показано, що модель, в якій допомогу надає вузькопрофільний спеціаліст, є оптимальною за співвідношенням витрати — ефективність порівняно з традиційною реабілітацією та фізіотерапією. Тривалість дослідження становила лише 6 місяців, тому бажано провести тривалий аналіз співвідношення вартості та ефективності. В дослідженні van den Hout et al.194 не було показано достовірної різниці у витратах чи якості життя по QALY. Широкий діапазон витрат в даному дослідженні пояснюється нечіткими даними по програмі робочої реабілітації; відсутність достовірної різниці у витратах та якості життя по QALY не дозволяє зробити висновки щодо співвідношення витрати — ефективність. Можливість використання даних голландської програми для закладів Великобританії є обмеженою.
6.3.6. Висновки
— Програма повної реабілітації (див. опис в таблиці 6.11) дозволяла тимчасово покращити функціонування пацієнтів з розгорнутою стадією РА202. У пацієнтів з ранньою стадією РА реабілітація дозволяла досягти значного покращення в тому, що стосувалося використання різних методів самообслуговування136, але не впливала на симптоми чи функціональні можливості (у більшості пацієнтів симптоми РА добре контролювалися за допомогою DMARDs).
— Терапія руки може мати вплив на її функцію. У деяких дослідженнях (огляд наведений у розділі 5.2), в яких приймали участь пацієнти з ранньою стадією РА, проводили оцінку тренінгів із технік захисту суглобів та збереження енергії з використанням групового когнітивно–поведінкового підходу. В одному дослідженні134, 135 було продемонстровано, що в групі, в якій використовувався захист суглобів, через 1 рік (ранкова скутість та біль в руці) та 4 роки (ранкова скутість) значно полегшувалися деякі симптоми порівняно з контролем.
— В іншому РКД у пацієнтів з розгорнутою стадією РА, які приймали терапію 146 інгібіторами ФНП–-а, було з’ясовано, що захист суглобів, збереження енергії та вправи для рук значно зменшували відчуття болю, фізичні симптоми та покращували функцію кінцівки порівняно з контролем протягом 8–місячного періоду спостереження. В більшості досліджень ортезів зап’ястя для роботи201 були проведені лише порівняння дизайнів лангети, а термін спостереження був коротким. В них була виявлена незначна різниця між лангетами з різним дизайном та зазначалося, що у виборі лангети пацієнти керувалися своїми побажаннями. В коротких (1–2 тижні) та тривалих дослідженнях (у метааналіз було включене лише одне дослідження з більшою тривалістю — 6 тижнів)210 не було знайдено різниці між групою, у якій пацієнти використовували лангету, та контрольною. Однак у групі, яка використовувала лангету, відмічали суттєве полегшення больових відчуттів, покращення сили стискання порівняно з контрольною, і пацієнти надавали перевагу використанню лангети210.
— Вправи для рук передбачені як у реабілітаційній програмі, так і в фізіотерапії. Існують дані, що комбінація фізичних вправ, спрямованих на розвиток діапазону руху, а також вправ на опір, значно покращують мобільність, силу стискання та загальну функцію кінцівки (згідно зі свідченнями самих пацієнтів)176, 178. Таке поєднання є більш ефективним, ніж виконання лише вправ на підвищення діапазону руху.
— Кількість даних, які б підтверджували ефективність робочої реабілітації пацієнтів з РА, які працюють та мають ризик втратити роботу, є недостатньою.
— У системному огляді200 було продемонстровано, що психологічні втручання, які застосовують реабілітологи (розслаблення, уявлення, протистояння стресу тощо), дозволяють досягти значного зменшення болю, покращити функціональний та психологічний стан в кінці лікування та під час спостереження. Однак ефективність залежала від типу втручання та була меншою в дослідженнях, де об’єктом виступали групи, в яких виконувалася освітня програма, програма на увагу та у контрольній групі. Техніки, спрямовані проти стресу, та КПТ мали достовірний позитивний вплив на психологічний статус (сприйняття проблеми, психологічний дистрес)205, 206. В одному дослідженні207 були також продемонстровані зміни в функціональному статусі. Не було зафіксовано змін у відчутті болю. Результати могли залежати від природи та тривалості терапії.
6.3.7. Від доказів до рекомендацій
Група з розробки настанов (ГРН) відмітила, що програми реабілітації сприяють покращенню функціональних можливостей пацієнтів з розгорнутою стадією РА та підвищують ступінь самообслуговування у пацієнтів з ранньою стадією РА. Склалося враження, що для всіх хворих на РА було важливим мати можливість періодично приймати участь у програмах реабілітації. ГРН зробила висновок, що тренінги з захисту суглобів та вправи для рук (сила та гнучкість) є ефективними у пацієнтів з порушеною функцією кінцівок. Причому ефективними вважалися лише ті тренінги, які надавалися підготовленими спеціалістами з використанням відповідних технік. ГРН відмітила недостатню кількість доказів впливу лангетів, що підтримують руку у відпочиваючому положенні, на симптоми захворювання, однак визнала, що пацієнти схилялися до їх використання під час періоду гострого болю та запалення. Не дивлячись на відсутність доказів тривалої користі від використання таких лангет, ГРН відмітила, що забезпечення ними має таке ж значення, як забезпечення анальгетиками, оскільки багато пацієнтів вважають їх корисними для симптоматичної допомоги.
ГРН була розчарована недостатністю інформації щодо впливу робочої реабілітації на зменшення вираженості симптомів хвороби, ушкодження суглобів, покращення якості життя, оскільки працюючі хворі на РА свідчать про особливу користь роботи для полегшення їх стану.
ГРН відмітила достатню кількість свідчень про позитивний вплив психологічних технік (релаксація, стресотерапія та когнітивні практики) на зменшення больових відчуттів та покращення якості життя хворих на РА ранньої та розгорнутої стадії, а також що антистресові техніки та когнітивно–поведінкова терапія покращують психологічний статус пацієнта. Не дивлячись на те, що лікування депресії не входило в завдання даного керівництва, ГРН вважає за потрібне запропонувати згадані психологічні втручання для лікування пацієнтів, яким необхідна допомога у боротьбі з наслідками захворювання. Ця допомога може надаватися реабілітологом, або іншим учасником мультидисциплінарного колективу, або іншим спеціалістом за рекомендацією лікаря.
З огляду на недостатню кількість досліджень багатьох специфічних реабілітаційних технік ГРН рекомендує провести додаткові дослідження для оцінки ефективності загальних та специфічних реабілітаційних методик.
Рекомендації
R12 Хворі на РА повинні мати можливість отримувати кваліфіковану реабілітацію та періодичні ревізії (див. рекомендації 36 та 37), якщо вони мають:
— труднощі зі щоденними справами чи
— проблеми з функцією руки
R13 Запропонувати психологічну допомогу (релаксація, антистресова терапія, когнітивні практики), щоб полегшити пристосування до життя зі хворобою.
6.4. Подіатрія
6.4.1. Вступ
Ноги є частиною опорно–рухового апарату, яку більшість сприймає як належне, але для хворих на ревматоїдний артрит усі ці кістки та хрящі означають джерело серйозного болю, і, як правило, на обох кінцівках. Для багатьох це буде їх першою скаргою, хоча проблеми з ногами частіше пов’язані з тривалим перебігом хвороб212. Навіть якщо незначною мірою хвороба поширюється на ноги, це суттєво погіршує мобільність та інші функціональні можливості213. У 3/4 хворих на РА ноги є однією з причин ускладнень при ходьбі, і головною, чи навіть єдиною, причиною у 1/4214. Ураження ніг при РА не обмежується пошкодженням суглобів та структурними змінами, а може включати погіршення кровопостачання, неврологічний дефіцит, патологію м’яких тканин, погіршення життєздатності тканин та проблеми, які походять від неможливості здійснювати звичайний догляд за ногами через проксимальні та системні ефекти РА. Незважаючи на те, що проблеми зі стопами є типовими для хворих на РА, цією областю ортопедичної допомоги часто нехтують, і забезпечення подіатричних послуг часто є недостатнім215. Оскільки стопи є складною та життєво важливою структурою, потрібні спеціалісти, які б надавали допомогу хворим на РА з ускладненнями в області стоп. У Великобританії послуги, пов’язані з лікуванням стоп, може надавати низка професіоналів, хоча професією, основним завданням якої є діагностика та лікування захворювань стоп, вважається подіатрія/хіроподія. Спеціалісти–хіроподи, які працюють в NHS (системі медичного обслуговування Великобританії), повинні бути зареєстровані в HPC та пройти до реєстрації тренінг з наданням відповідного ступеня.
Основний догляд за стопами пацієнтів з РА може бути наданий усіма зареєстрованими в HPC подіатрами, які працюють у поліклініках та спеціалізованих ревматологічних пунктах. Деякі пацієнти з більш складними потребами (надання складного ортезу, догляд через високий ризик, ін’єкції в суглоб, хірургічні втручання) можуть потребувати більш кваліфікованої діагностики та лікування подіатром, який має спеціалізовану підготовку чи досвід в області ревматології, а також взаємодії з іншими членами мультидисциплінарної ревматологічної команди.
6.4.2. Клінічні методи
Ми шукали дослідження, в яких вивчалася ефективність різних технік подіатрії залежно від симптомів, пошкодження суглобів, функціонування та якості життя пацієнтів з РА (рання та розгорнута стадії). Були –обрані дослідження, в яких була представлена адекватна вибірка пацієнтів з Великобританії, якщо така вибірка була змішаною (різні типи артриту), доля пацієнтів з РА повинна була становити не менше 75 %.
Один метааналіз201, 3 РКД216–219 та одне дослідження серії випадків220 відповідали критеріям включення. Одне РКД було опубліковано у вигляді двох окремих протоколів17, 219, в яких доповідалися різні результати, тому це дослідження враховували лише один раз. Однак тут наведені результати обох протоколів. Одне з РКД218 було виключене через обмежену методичну базу (висока кількість відмов та відсутність ІТТ аналізу). Усі інші дослідження були методично адекватними (сліпими, включали ІТТ аналіз). В жодному з досліджень не обстежували пацієнтів з ранньою стадією РА.
Змішана вибірка (рання та розгорнута стадії)
В базі Кокрана був знайдений один системний огляд/метааналіз201, в якому порівнювалися всі типи ортезів та плацебо, а також активне втручання та постійне лікування. В даному звіті приведені лише результати досліджень ортезів ніг. Метааналіз був виконаний на належному рівні, однак три РКД, які входили до його складу, мали різну якість. Дослідження, включені до аналізу, відрізнялися у наступному:
— втручання (підтримуючі устілки, взуття збільшеної глибини, а також устілки у спеціальному взутті);
— група порівняння (звичайне взуття, взуття з підвищеною глибиною, устілки плацебо);
— величина дослідження (N від 28 до 102 для ортезів ніг);
— якість дослідження — максимальне значення по шкалі — 5 (усі дослідження мали якість від задовільної до доброї в тому, що стосувалося ортезів ніг);
— тривалість дослідження — тривалість втручання (від 2 місяців до 3 років для ортезів ніг).
Розгорнута стадія РА
Були знайдені два РКД216, 217, 219 і одне дослідження серії випадків220, в яких досліджували участь подіатрії в лікуванні пацієнтів з розгорнутою стадією РА.
Два РКД216, 217, 219 були односторонніми сліпими дослідженнями в паралельних групах. Перше РКД216 стосувалося лікування кісткового мозолю у 38 пацієнтів, в ньому порівнювалися два різні шляхи лікування, нормальне та фіктивне, та включало 5–тижневий період спостереження. В другому РКД217, 219 досліджували ортези ніг у 101 пацієнта та порівнювали дві гілки лікування: жорсткі ортези порівняно з контролем (відсутність ортезу) протягом 30–місячної фази лікування.
В дослідженні серії випадків220 досліджували ефект носіння термоформованого взуття у 25 пацієнтів з РА (тривалість захворювання не вказана) протягом 3–місячного періоду лікування.
6.4.3. Вступ до методології медичної економіки
Були знайдені три роботи, і дві з них не відповідали критеріям включення221, 222. В третій роботі, Clark et al.223, був проведений огляд ортезів стоп у хворих на РА. В двох роботах217, 224 розглядалася вартість ортезів, однак в жодній не проводилося порівняння вартості та ефективності.
6.4.4. Результати клінічних досліджень
Змішана вибірка (рання та розгорнута стадії РА)
Взуття збільшеної глибини порівняно зі звичайним (2 місяці)
В одному метааналізі201 було продемонстровано, що відповідно до результатів 2–місячного спостереження, взуття зі збільшеною глибиною є достовірно кращим за звичайне: HAQ (1 РКД, N = 30; WMD (зважена різниця середніх) величини ефекту –0,20, 95% ДІ від –0,35 до –0,05; р = 0,01); біль при ходьбі (1 РКД, N = 30; WMD величини ефекту — 18,7, 95% ДІ від –28,5 до –8,9; р = 0,0002); біль при підйомі по сходах (1 РКД, N = 30; WMD величини ефекту — 27,0, 95% ДІ від –37,8 до –16,2; р < 0,00001); тривалість ходьби без болю (1 РКД, N = 30; WMD величини ефекту — 18,2, 95% ДІ від 8,2 до 28,2; р = 0,0004). Для показників втоми та суб’єктивного гарного самопочуття різниця була недостовірною. Рівень 1++
Напівжорсткі устілки порівняно з взуттям збільшеної глибини (12 тижнів)
В одному метааналізі201 було продемонстровано, що напівжорсткі устілки були достовірно кращими за взуття збільшеної глибини після 12 тижнів використання за наступними показниками: біль, візуальна аналогова шкала (1 РКД, N = 48; WMD величини ефекту — 1,9, 95% ДІ від –3,3 до –0,51; р = 0,007). Різниця була недостовірною для: ходьби, підйому сходами, стояння, активності щоденного життя (в тому, що стосувалося ходьби, підйому сходами), кількості суглобів нижніх кінцівок, кількості суглобів МТР (кількість суглобів, які болять). Рівень 1++
М’які устілки порівняно з взуттям збільшеної глибини (12 тижнів)
В одному метааналізі201 була продемонстрована відсутність суттєвої різниці між м’якими устілками та взуттям збільшеної глибини після 12 тижнів використання за наступними показниками: біль (візуальна аналогова шкала), ходьба, підйом сходами, стояння, активність щоденного життя (в тому, що стосувалося ходьби, підйому сходами), час, за який проходиться відстань 15 м, кількість суглобів нижніх кінцівок та кількість суглобів МТР (кількість суглобів, які болять). Рівень 1++
Напівжорсткі устілки порівняно з плацебо (12 тижнів)
В одному метааналізі201 було продемонстровано, що підтримуючі устілки (ортези стопи Rohadar) були суттєво кращими за устілки плацебо протягом 3–річного дослідження: кут відхилення великого пальця залишався < 21° (1 РКД, N = 98; WMD величина ефекту — 3,6, 95% ДІ від 2,2 до 5,9; р < 0,00001). Різниця була недостовірною для: кількості суглобів з відчуттям болі, індексу функції стоп та болі в стопах. Рівень 1++
Розгорнута стадія РА
Видалення кісткової мозолі та симуляція
В одному РКД216 не було знайдено достовірної різниці між нормальним видаленням кісткової мозолі та його симуляцією для наступних показників: біль в передній частині стопи (візуальна аналогова шкала), заходи проти тиску на підошву та для виправлення ходи через 4 тижні після втручання. Рівень 1++
Термоформоване взуття (рівень 3)
В дослідженні серії випадків220 було продемонстровано, що у випадку використання термоформованого взуття:
— 80 % пацієнтів носили взуття весь час і 20 % — іноді;
— 72% носили у взутті виготовлені на замовлення напівжорсткі ортези, решта (28 %) — ні;
— 20 % носили модифіковане взуття для контролю варусу задньої частини стопи;
— 50 % пацієнтів з тих, що носили ортези стопи, відмітили, що завжди носили вкладиші у взутті;
— 80 % підтвердили, що в термоформованому взутті ходити легше;
— достовірно більше пацієнтів свідчить про те, що в термоформованому взутті ходити легше, ніж у звичайному;
— пацієнти відмічали, що термоформоване взуття є кращим та більш зручним, ніж звичайне.
Ортези, виготовлені на замовлення, порівняно з конт–ролем (відсутність ортезів)
В одному РКД217, 219 було продемонстровано, що ортези стопи були достовірно кращими за їх відсутність у контрольній групі за наступними показниками: індекс функціонування стопи (загальний, біль, недієздатність — усі р < 0,05), діапазон дорсифлексії/згинання підошви, рух всередину/назовні, комплексне обертання гомілковостопного суглоба назовні та всередину та внутрішнє обертання через 30 тижнів (усі р < 0,01). Через 30 тижнів не було виявлено достовірної різниці між використанням виготовлених на замовлення ортезів та контрольною групою за наступними показниками: індекс функціонування стопи (функціональні обмеження), загальний біль, шкала DAS, шкали HAQ та Larsen (руки та стопи). Рівень 1++
6.4.2. Висновки
Наступні види втручання мають доведену ефективність: взуття збільшеної глибини порівняно зі звичайним201, напівжорсткі устілки порівняно з взуттям збільшеної глибини (біль і деформація пальців)201, термоформоване взуття (відповідно до відгуків користувачів)220, ортези, виготовлені на замовлення порівняно з їх відсутністю (функція, біль, недієздатність)217, 219. Необхідність видалення кісткової мозолі підтверджена не була216. Також не було виявлено різниці між використанням м’яких устілок та взуття збільшеної глибини201.
Більшість досліджень мали порівняно невелику тривалість (від 5 до 30 тижнів)201, 216, 217, 219 з одним виключенням (3 роки дослідження підтримуючих устілок порівняно з плацебо)201.
6.4.3. Від доказів до рекомендацій
Існують факти, які підтверджують позитивний вплив устілок та спеціалізованого взуття на симптоми, функціонування та якість життя хворих на РА. На перше місце за доведеною ефективністю можна поставити взуття, виготовлене на замовлення відповідно до форми ноги кожного окремого пацієнта, а на останнє — м’які устілки.
ГРН вважає за потрібне рекомендувати можливість обстеження пацієнтів подіатром. Основний огляд та процедури можуть бути проведені усіма подіатрами, зареєстрованими в HPC; повинна гарантуватися оцінка потреб пацієнта, пов’язаних зі здоров’ям ніг, та надання відповідної допомоги. ГРН також погоджується, що в окремих, більш складних випадках може знадобитися допомога більш кваліфікованих подіатрів. Просте втручання, таке як устілки фабричного виробництва, не має достатньої кількості доказів своєї ефективності, тоді як щодо використання устілок та взуття на замовлення, навпаки, є багато свідчень, що підтверджують їх ефективність. ГРН вважає, що прості устілки підходять для загального використання через їх низьку ціну, тоді як надання більш складних устілок та взуття потребує консультації спеціаліста–подіатра.
Рекомендації
R14 Усі хворі на РА, які мають проблеми в області стоп, повинні мати можливість звернутися до подіатра для оцінки та періодичного огляду стоп (дивись рекомендації 36 та 37).
R15 При необхідності усі пацієнти з РА повинні бути забезпечені функціональними устілками та терапевтичним взуттям.
Коментар робочої групи
Відповідно до клінічного протоколу санаторно–курортного лікування сироваткопозитивного ревматоїдного артриту хворі на РА з І та ІІ ступенем активності хвороби можуть бути направленні на санаторно–курортне лікування (Наказ № 56 від 06.02.2008 «Про затвердження клінічних протоколів санаторно–курортного лікування в санаторно–курортних закладах (крім туберкульозного профілю) для дорослого населення», Ю.Л. Шевченко, І.Н. Денисов, В.І. Кулаков, Р.М. Хаитов. Клинические рекомендации для практикующих врачей, основанные на доказательной медицине. — 2–е изд. — М.: ГЭОТАР–МЕД, 2003. — 1248 с.).
Загалом реабілітація хворих на РА проводиться з урахуванням періоду хвороби. У гострому періоді захворювання лікування базується на принципі збереження спокою для ураженого суглоба. Проводиться лікування положенням, застосовується магнітне та лазерне випромінювання до зменшення хворобливості в уражених суглобах. У підгострій стадії рекомендовано комплексну фізичну реабілітацію: лікування положенням, лікувальний масаж, заняття лікувальною гімнастикою разом із фізіотерапевтичними процедурами. У хронічній стадії використовують лікувальний масаж, заняття лікувальної гімнастикою, бальнеолікування (сірководневі, радонові ванни), грязелікування у поєднанні з санаторно–курортним лікуванням.
Система фізичної реабілітації складається з 3 етапів: в стаціонарі; в умовах санаторію чи поліклініки; в домашніх умовах за участі фахівців із фізичної реабілітації. Основні завдання фізичної реабілітації:
— вплив на уражені суглоби з метою підвищення їх рухливості і профілактики подальшого порушення функції;
— зміцнення м’язової системи та підвищення праце–здатності хворого;
— поліпшення кровообігу в суглобах, боротьба з атрофією м’язів;
— протидія негативному впливу ліжкового режиму (стимуляція функцій кровообігу, дихання, підвищення обміну речовин);
— зменшення больових відчуттів шляхом пристосування уражених суглобів до дозованого фізичного навантаження.
Реабілітація хворих з РА відбувається за участі лікаря–ревматолога, методиста ЛФК та лікаря загальної практики — сімейної медицини.
Для своєчасної корекції функціональних вад та їх попередження хворого з РА слід направляти для обстеження до ортопеда одразу після встановлення діагнозу.
Далі буде