Газета «Новости медицины и фармации» 18 (514) 2014
Вернуться к номеру
Мочекаменная болезнь
Авторы: C. Türk (chair), T. Knoll (vice-chair), A. Petrik, K. Sarica, A. Skolarikos, M. Straub, C. Seitz
Разделы: Медицинское образование
Версия для печати
Статья опубликована на с. 22-28 (Укр.)
Руководство Европейской ассоциации урологов по уролитиазу (EAU, 2013)
(сокращенное изложение)
Guidelines on Urolithiasis
European Association of Urology 2013
1. Введение
Группа по составлению рекомендаций Европейской ассоциации урологов по мочекаменной болезни (МКБ) разработала данные рекомендации, чтобы помочь урологам в ведении больных с конкрементами, основываясь на данных доказательной медицины, а также способствовать внедрению указанных рекомендаций в клиническую практику. Документ полно и всесторонне раскрывает большинство аспектов этого заболевания. Несмотря на научные и технические достижения, большое число людей продолжает страдать от МКБ. Рабочая группа принимала во внимание разную степень доступности медицинского обеспечения в регионах.
2. Классификация камней
Конкременты можно классифицировать по следующим критериям: размер, локализация, рентгенологические характеристики, этиология, минералогический состав и степень риска повторного камнеобразования.
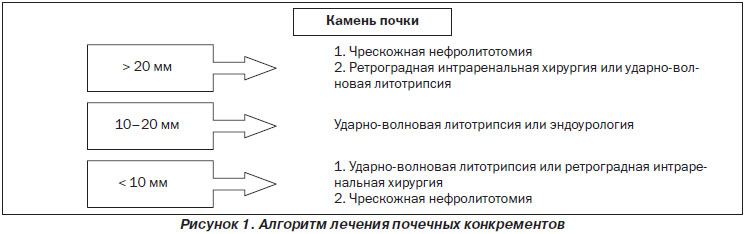
2.1. Размер камней
Как правило, размер конкремента обозначается в миллиметрах, с указанием 1 или 2 измерений. Также конкременты можно подразделить на группы размером < 5, 5–10, 10–20 и > 20 мм.
2.2. Локализация конкремента
Конкременты можно классифицировать согласно анатомической локализации: в верхней, средней или нижней чашечке; в почечной лоханке; в верхнем, среднем или дистальном отделе мочеточника и мочевом пузыре.
2.3. Рентгенологические характеристики
Камни можно классифицировать в соответствии с их изображением на обзорном снимке органов мочевой системы (табл. 3), которое зависит от их минерального состава. При проведении компьютерной томографии (КТ) без контрастирования для классификации можно использовать шкалу единиц Хаунсфилда, поскольку КТ представляет информацию о плотности конкремента и его структуре, что непосредственно влияет на выбор тактики лечения.
2.4. Этиология формирования камней
Конкременты можно подразделить на те, которые образовались вследствие инфекции (инфекционные), и те, которые не были вызваны инфекцией (неинфекционные), а также конкременты, возникшие вследствие генетических нарушений, и конкременты, образовавшиеся как побочное явление при приеме лекарств (лекарственные).
Классификация конкрементов на основе их этиологии
Неинфекционные конкременты:
— оксалат кальция;
— фосфат кальция (включая брушит и апатит);
— мочевая кислота.
Инфекционные конкременты:
— фосфат магния аммония;
— апатит;
— урат аммония.
Генетические причины:
— цистин;
— ксантин;
— 2,8-дигидроксиаденин.
Лекарственные конкременты.
2.5. Минералогический состав камней
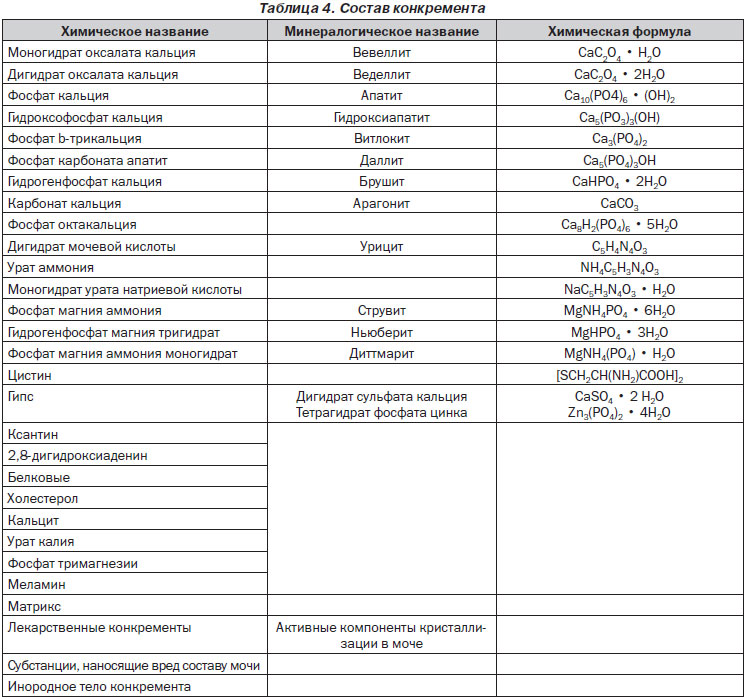
Важным фактором образования конкрементов является обмен веществ, поэтому для исключения каких-либо нарушений необходимо провести оценку метаболизма. Кроме того, правильный анализ конкремента в отношении каких-либо нарушений обмена веществ служит основой для принятия дальнейших решений по диагностике и лечению. Зачастую конкременты состоят из различных веществ. Клинически наиболее значимые вещества и их минеральные составляющие перечислены в табл. 4.
2.6. Группы риска камнеобразования
Степень риска камнеобразования представляет особый интерес, поскольку определяет не только вероятность рецидива или роста конкрементов, но и необходимость медикаментозного лечения.
Примерно у 50 % больных с рецидивирующим течением МКБ на протяжении всей жизни наблюдается лишь 1 рецидив камнеобразования. Большое количество рецидивов отмечается в немногим более 10 % всех случаев МКБ. Степень риска повторного камнеобразования определяется видом конкремента и тяжестью заболевания.
Высокий риск камнеобразования
Общие факторы:
— развитие МКБ в раннем возрасте (особенно у детей и подростков);
— семейный анамнез МКБ;
— брушит в составе конкрементов (СаНРО4 • 2Н2О);
— мочевая кислота и урат в составе конкрементов;
— инфекционные конкременты;
— единственная почка (сама по себе единственная почка не обладает повышенным риском повторного камнеобразования, однако профилактика возможного рецидива при этом имеет большое значение).
Заболевания, связанные с развитием МКБ:
— гиперпаратиреоидизм;
— нефрокальциноз (НК);
— гастроинтестинальные заболевания (еюноилеальный обходной анастомоз, резекция кишечника, болезнь Крона, мальабсорбция, кишечная гипероксалурия после отведения мочи);
— саркоидоз.
Генетические причины МКБ:
— цистинурия (тип А, В и АВ);
— первичная гипероксалурия (ПГ);
— почечный тубулярный ацидоз (ПТА) тип І;
— 2,8-дигидроксиаденин;
— ксантинурия;
— синдром Леша — Нихена;
— муковисцидоз.
Лекарственные препараты, способствующие камнеобразованию.
Анатомические отклонения, способствующие камнеобразованию:
— медуллярная губчатая почка (тубулярная эктазия);
— обструкция лоханочно-мочеточникового сегмента;
— дивертикул чашечки, киста чашечки;
— стриктура мочеточника;
— пузырно-мочеточниково-почечный рефлюкс;
— подковообразная почка;
— уретероцеле.
3. Диагностика
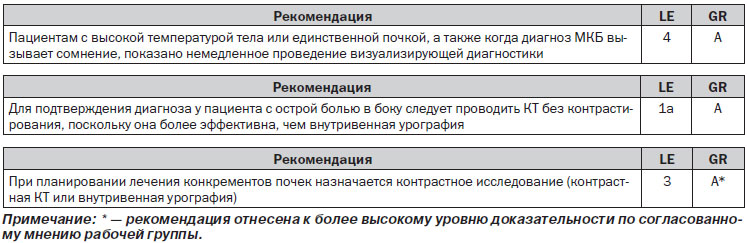
3.1. Диагностическая визуализация
У пациентов с конкрементами в почках обычно присутствуют боль в пояснице, рвота, иногда лихорадка, но течение заболевания может быть и бессимптомным. Стандартное обследование включает подробное изучение истории болезни и врачебный осмотр.
В качестве первичной процедуры следует назначать ультразвуковое исследование (УЗИ), так как оно безопасно (не используется радиоактивное излучение), воспроизводимо и является недорогим методом обнаружения конкрементов. УЗИ позволяет выявить конкременты в чашечках, лоханке, лоханочно-мочеточниковом и пузырно-мочеточниковом сегментах, а также диагностировать расширение верхних мочевыводящих путей. При диагностике почечных конкрементов размером > 5 мм чувствительность УЗИ составляет 96 %, а специфичность — почти 100 %. При диагностике всех конкрементов (любой локализации) чувствительность и специфичность УЗИ оказываются ниже — 78 и 31 % соответственно.
Чувствительность и специфичность обзорного снимка органов мочевой системы составляют 44–77 и 80–88 % соответственно. Не следует назначать обзорный снимок, если планируется проведение КТ без контрастирования. Тем не менее обзорный снимок может быть полезен для дифференциации рентгеннегативных и рентгенконтрастных конкрементов и для их сопоставления во время последующего наблюдения.
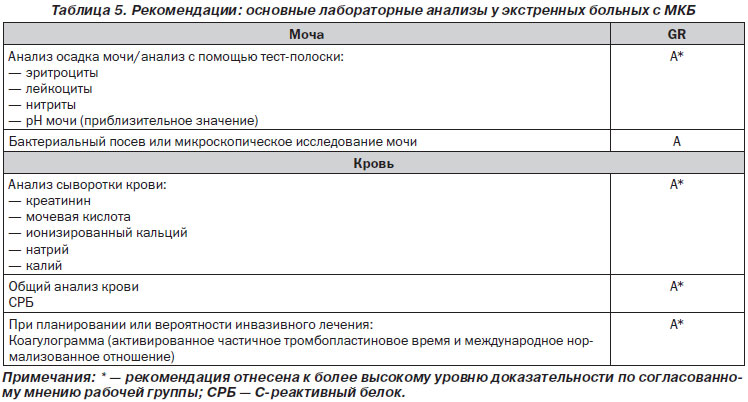
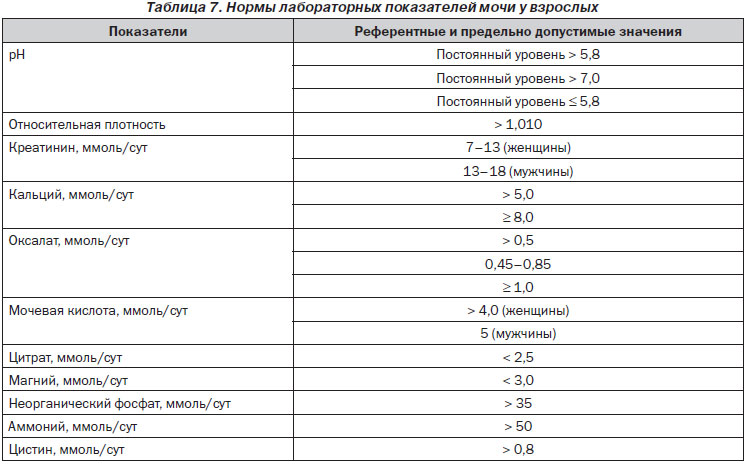
3.2. Лабораторная диагностика
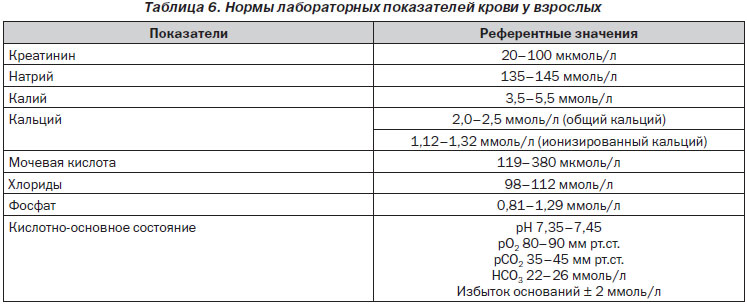
Всем пациентам с неотложными проявлениями МКБ наряду с методиками визуализации необходимо назначать сокращенное биохимическое исследование мочи и крови. На данном этапе рекомендации одинаковые для пациентов группы как низкого, так и высокого риска.
3.2.1. Основные плановые анализы у неэкстренных больных с МКБ
Биохимические исследования назначаются всем пациентам с МКБ практически в одинаковом объеме. Однако неэкстренным пациентам можно не проводить исследование на натрий, калий, СРБ и коагулограмму. Более тщательному обследованию следует подвергать только пациентов с высоким риском повторного камнеобразования. Специфическая оценка метаболизма с учетом состава конкрементов рассматривается в разд. 11.
Самым простым способом поставить правильный диагноз считается анализ отошедшего конкремента с помощью достоверного аналитического метода (разд. 2.5). На основании его минералогического состава можно определить возможные нарушения обмена веществ. К достоверным аналитическим методам относятся инфракрасная спектроскопия и дифракция рентгеновских лучей.
4. Лечение пациента с почечной коликой
4.1. Почечная колика
4.1.1. Купирование боли
Первый этап лечения при почечной колике — купирование боли.
Клинические исследования однозначно продемонстрировали, что нестероидные противовоспалительные препараты (НПВП) (например, диклофенак) эффективно купируют боль у пациентов с почечной коликой. Эти препараты при почечной колике значительно эффективнее опиатов, и у пациентов, принимающих НПВП, достигается большее снижение боли и реже требуется дальнейшая анальгезия в кратчайшие сроки.
Если все же назначается опиат, рекомендуется не останавливать выбор на петидине в связи с тем, что опиаты, и особенно петидин, чаще вызывают рвоту по сравнению с НПВП и чаще требуют продолжения анальгезии.
4.1.3. Рекомендации по обезболиванию при почечной колике
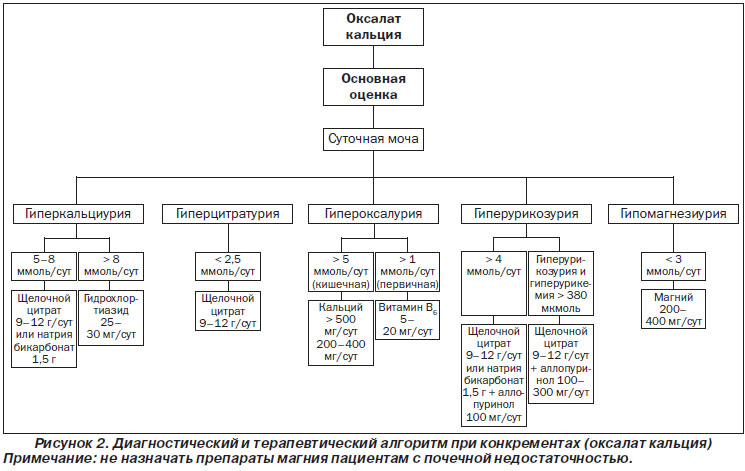
11. Метаболическая оценка и предотвращение рецидива
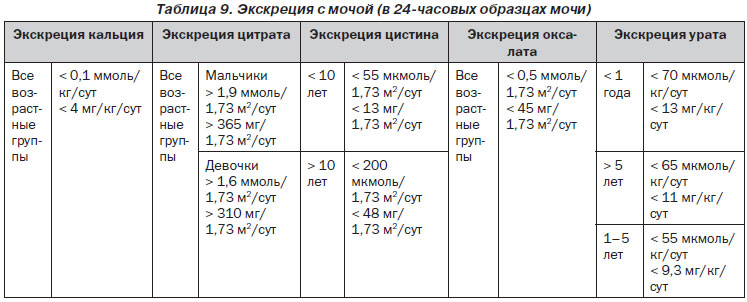
Таблица 9. Экскреция с мочой (в 24-часовых образцах мочи)
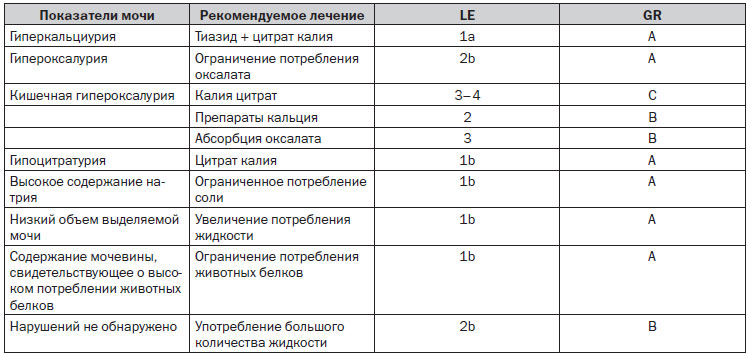
11.4.4. Рекомендации по медикаментозному лечению пациентов со специфическими нарушениями состава мочи
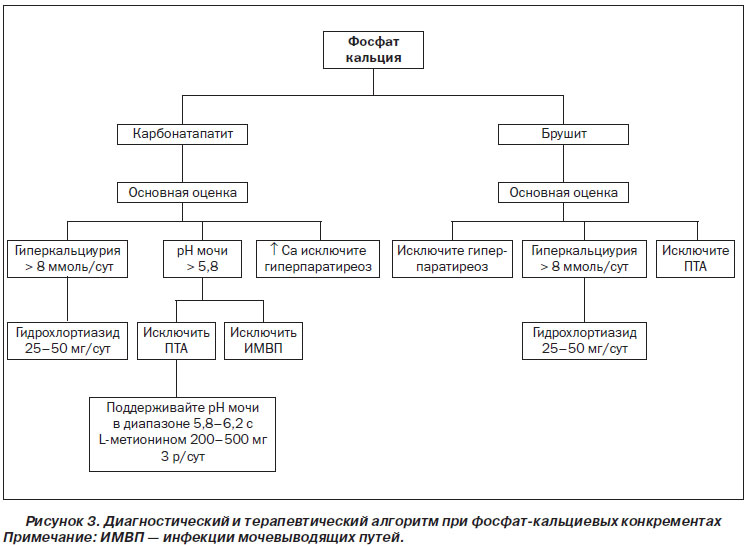
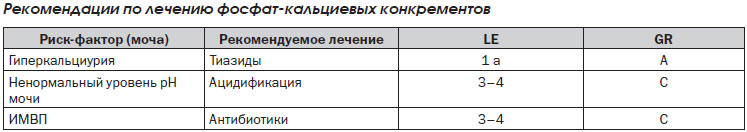
Рекомендации по лечению фосфат-кальциевых конкрементов
11.6.3. Первичная гипероксалурия
Пациентов с ПГ следует направлять в специализированные клиники, так как для успешного лечения требуются междисциплинарный подход и большой опыт. Главная цель терапии заключается в снижении эндогенного образования оксалата, которое у пациентов с ПГ чрезвычайно повышено. Примерно у трети пациентов с ПГ 1-го типа можно достичь нормализации или значительного снижения выведения оксалата с мочой с помощью пиридоксина. Нормальное разведение мочи достигается при повышении потребления жидкости до 3,5–4,0 л в день для взрослых (для детей — 1,5 л/м2 поверхности тела) и равномерном потреблении жидкости в течение дня.
К медикаментозным способам предотвращения кристаллизации оксалата кальция относятся диуретики, щелочные цитраты и магний. Тем не менее при терминальной стадии почечной недостаточности для лечения ПГ необходима одновременная трансплантация печени и почки.
Схемы лечения включают:
— пиридоксин при ПГ 1-го типа: 5–20 мг/кг/сут в зависимости от выведения оксалата с мочой и переносимости лечения пациентом;
— щелочной цитрат: 9–12 г/сут для взрослых, 0,1–1,5 мЭкв/кг/сут для детей;
— магний 200–400 мг/сут (терапия магнием противопоказана при почечной недостаточности).
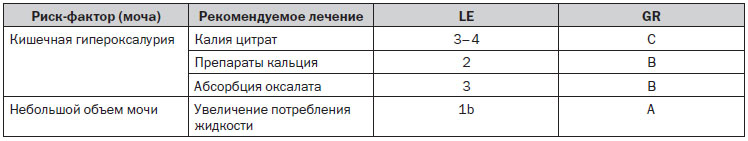
11.6.4. Кишечная гипероксалурия
Кишечная гипероксалурия — характерное заболевание у пациентов с нарушением всасывания жиров в кишечнике. Это заболевание, связанное с высоким риском камнеобразования, может развиваться после резекции кишечника, наложения еюноилеального обходного анастомоза для лечения ожирения, при болезни Крона и недостаточности поджелудочной железы. Снижение всасывания жирных кислот приводит к потере кальция. Вследствие этого нарушается обычное связывание оксалата с кальцием и резко увеличивается всасывание оксалата. Наряду с гипероксалурией у таких пациентов в результате потери щелочей развивается гипоцитратурия. При этом, как правило, отмечаются низкие показатели рН мочи, снижение содержания кальция в моче и объема мочи. Все перечисленные нарушения способствуют значительному повышению концентрации оксалата кальция, развитию кристаллурии и камнеобразованию.
К специфическим профилактическим мерам относятся:
— ограничение потребления пищи, богатой оксалатами;
— ограничение потребления жиров;
— прием препаратов кальция во время еды, чтобы обеспечить связывание оксалата с кальцием в кишечнике;
— достаточное потребление жидкости для компенсации ее потери вследствие диареи;
— терапия щелочными цитратами для повышения рН мочи и содержания цитратов.
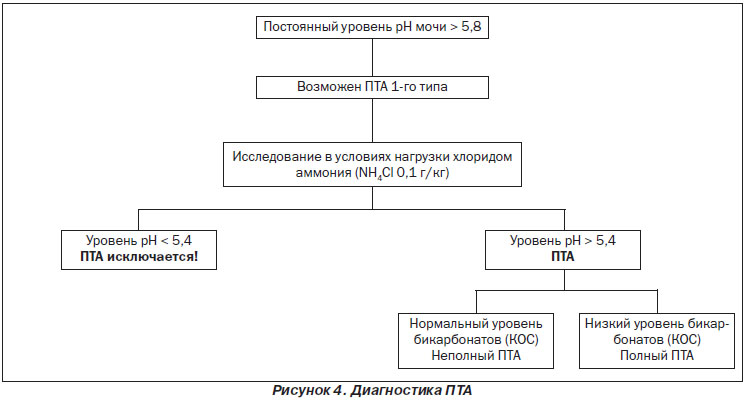
11.6.5. Почечный тубулярный ацидоз
ПТА развивается вследствие нарушения секреции протонов или реабсорбции бикарбонатов в нефронах. Наибольшая вероятность формирования конкрементов в почках отмечается при дистальном ПТА 1-го типа. На рис. 4 представлена схема диагностики ПТА.
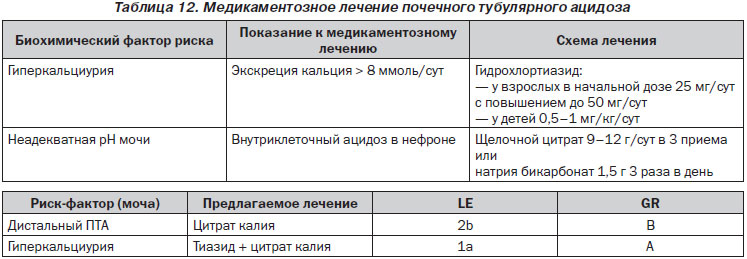
Главная терапевтическая задача заключается в восстановлении кислотно-щелочного равновесия. Несмотря на высокий уровень рН мочи при ПТА, подщелачивание с помощью щелочных цитратов или бикарбоната натрия представляется основным способом нормализации метаболических процессов (внутриклеточного ацидоза), связанных с камнеобразованием. Щелочная нагрузка снижает канальцевую реабсорбцию цитрата, что, в свою очередь, приводит к нормализации выведения цитрата и в то же время к снижению обмена кальция. В случае полного ПТА эффективность лечения можно контролировать с помощью определения газов венозной крови (избыток оснований ± 2,0 ммоль/л). Если после восстановления кислотно-щелочного равновесия выведение кальция остается повышенным (> 8 ммоль/сут), снижения выведения кальция с мочой можно добиться назначением тиазидов.
11.6.6. Нефрокальциноз
Термином «нефрокальциноз» обозначается повышенное отложение кристаллов в корковом и мозговом слое почек. Это заболевание может развиваться самостоятельно или сопровождаться образованием конкрементов в почках. НК может вызываться различными нарушениями обмена веществ. К основным факторам риска относятся: гиперпаратиреоз, первичная гипероксалурия, ПТА, нарушения обмена витамина D, идиопатическая гиперкальциурия и гипоцитратурия, а также генетические нарушения, включая болезнь Дента, синдром Барттера и медуллярную губчатую почку.
Поскольку этиология НК может быть различной, не существует единого стандартного способа лечения этого заболевания. Лечение должно быть направлено на коррекцию метаболических и генетических нарушений, лежащих в его основе, и одновременно на минимизацию биохимических факторов риска развития НК.
11.6.6.1. Диагностика
Для постановки диагноза необходимо провести анализ крови на паратгормон (в случае повышенного содержания кальция), витамин D и метаболиты, витамин А, натрий, калий, магний, хлорид, и КОС. Анализ мочи должен включать измерение рН (не менее 4 раз в день), суточного объема, удельного веса, содержания кальция, оксалата, фосфата, мочевой кислоты, магния и цитрата.
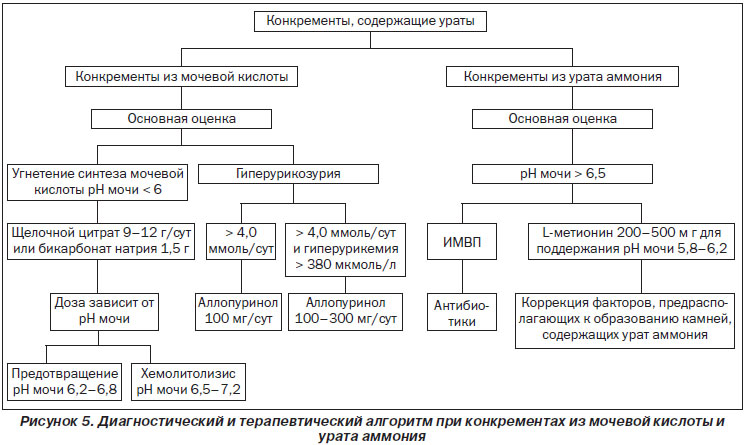
11.7. Конкременты из мочевой кислоты и урата аммония
11.9. Цистиновые конкременты
Рекомендации по лечению цистиновых конкрементов
Перевод О.В. Антонова,С.В. Кушниренко,
научное редактирование Н.А. Григорьева