Газета «Новости медицины и фармации» Гастроэнтерология (521) 2014 (тематический номер)
Вернуться к номеру
Хронічний панкреатит Адаптована клінічна настанова, заснована на доказах 2014
Рубрики: Гастроэнтерология
Разделы: Официальная информация
Версия для печати
Статья опубликована на с. 48-71
Робоча група з адаптації клінічної настанови
|
Харченко Наталія В’ячеславівна |
Завідувач кафедри гастроентерології, дієтології і ендоскопії Національної академії післядипломної освіти імені П.Л. Шупика, член-кор. Національної академії медичних наук України, професор, доктор медичних наук, головний позаштатний спеціаліст МОЗ України зі спеціальності «Гастроентерологія» |
|
Ліщишина Олена Михайлівна |
Директор Департаменту стандартизації медичних послуг ДП «Державний експертний центр МОЗ України» |
|
Бабак Олег Якович |
Завідувач відділу ДУ «Інституту терапії імені Л.Т. Малої НАМН України», професор, доктор медичних наук, віце-президент Української гастроентерологічної асоціації |
|
Губергріц Наталія Борисівна |
Завідувач кафедри внутрішньої медицини ім. проф. О.Я. Губергріца Донецького національного медичного університету імені М. Горького, професор, доктор медичних наук |
|
Драгомирецька Наталія Володимирівна |
Головний науковий співробітник, керівник відділу відновного лікування хворих гастроентерологічного профілю ДП «Український науково-дослідний інститут медичної реабілітації та курортології» МОЗ України, професор кафедри загальної практики та медичної реабілітації Одеського національного медичного університету, доктор медичних наук |
|
Захараш Михайло Петрович |
Завідувач кафедри хірургії № 1 Національного медичного університету імені О.О. Богомольця, член-кор. Національної академії медичних наук України, професор, доктор медичних наук, головний позаштатний спеціаліст МОЗ України зі спеціальності «Проктологія» |
|
Копчак Володимир Михайлович |
Завідувач відділу хірургії підшлункової залози та реконструктивної хірургії жовчовивідних проток ДУ «Національний інститут хірургії та трансплантології імені О.О. Шалімова» НАМН України, професор, доктор медичних наук |
|
Корендович Володимир Степанович |
Головний позаштатний спеціаліст зі спеціальності «Гастроентерологія» Управління охорони здоров’я Житомирської обласної державної адміністрації, завідувач гастроентерологічного відділення Житомирської обласної клінічної лікарні ім. О.Ф. Горбачевського |
|
Коруля Ірина Анатоліївна |
Доцент кафедри гастроентерології, дієтології і ендоскопії Національної медичної академії післядипломної освіти імені П.Л. Шупика, кандидат медичних наук |
|
Матюха Лариса Федорівна |
Завідувач кафедри сімейної медицини Національної медичної академії післядипломної освіти імені П.Л. Шупика, професор, доктор медичних наук, головний позаштатний спеціаліст МОЗ України зі спеціальності «Загальна практика — сімейна медицина» |
|
Нікішаєв Володимир Іванович |
Завідувач відділення ендоскопічної діагностики та малоінвазивної хірургії Київської міської клінічної лікарні швидкої медичної допомоги, доктор медичних наук |
|
Свінціцький Анатолій Станіславович |
Завідувач кафедри внутрішньої медицини № 3 Національного медичного університету імені О.О. Богомольця, професор, доктор медичних наук |
|
Скрипнік Ігор Миколайович |
Завідувач кафедри післядипломної освіти лікарів–терапевтів Вищого державного навчального закладу України «Українська медична стоматологічна академія», професор, доктор медичних наук |
|
Степанов Юрій Миронович |
Директор ДУ «Інститут гастроентерології НАМН України», віце-президент Української гастроентерологічної асоціації, професор, доктор медичних наук |
|
Ткач Сергій Михайлович |
Професор кафедри внутрішньої медицини № 1 Національного медичного університету імені О.О. Богомольця, професор, доктор медичних наук |
|
Філіппова Олександра Юріївна |
Доцент кафедри госпітальної терапії № 1 та профпатології Державного закладу «Дніпропетровська медична академія», кандидат медичних наук |
|
Фомін Петро Дмитрович |
Завідувач кафедри факультетської хірургії № 2 Національного медичного університету імені О.О. Богомольця, академік Національної академії медичних наук України, професор, доктор медичних наук, головний позаштатний спеціаліст МОЗ України зі спеціальності «Хірургія» |
|
Червак Ігор Миколайович |
головний позаштатний спеціаліст зі спеціальності «Гастроентерологія» Головного управління охорони здоров’я Київської міської державної адміністрації, завідувач гастроентерологічного відділення Київської міської клінічної лікарні № 8 |
Методичний супровід та інформаційне забезпечення
|
Горох Євген Леонідович |
Начальник відділу якості медичної допомоги та інформаційних технологій ДП «Державний експертний центр МОЗ України» |
|
Шилкіна Олена Олександрівна |
Начальник відділу методичного забезпечення новітніх технологій у сфері охорони здоров’я ДП «Державний експертний центр МОЗ України» |
Державний експертний центр Міністерства охорони здоров’я України є членом
Guidelines International Network (Міжнародна мережа настанов)
ADAPTE (Франція) (Міжнародний проект з адаптації клінічних настанов)
Рецензенти
|
Вдовиченко Валерій Іванович |
Професор кафедри терапії № 1 та медичної діагностики ФПДО Львівського національного медичного університету імені Данила Галицького, професор, доктор медичних наук |
|
Стаднюк Леонід Антонович |
Завідувач кафедри терапії і геріатрії Національної медичної академії післядипломної освіти імені П.Л. Шупика професор, доктор медичних наук |
Дата наступного перегляду: 2017 рік.
Зміст
Список скорочень
Шкала рівнів доведеності і градації рекомендацій
Передмова мультидисциплінарної робочої групи з адаптації клінічної настанови. Синтез даних
1. Хронічний панкреатит (PRODIGY, грудень 2010):
1.1. Вступ
1.2. Визначення хронічного панкреатиту
1.3. Патофізіологія хронічного запалення підшлункової залози
1.4. Чинники хронічного запалення підшлункової залози
1.5. Прогноз при хронічному панкреатиті
1.6. Ускладнення хронічного панкреатиту
1.7. Діагностика та лікування хронічного панкреатиту
1.8. Інформація для пацієнтів
2. Рекомендації Іспанського клубу панкреатологів з діагностики та лікування хронічного панкреатиту (лютий, 2013):
2.1. Як визначається і діагностується екзокринна недостатність підшлункової залози?
2.2. Як визначається і діагностується ендокринна недостатність підшлункової залози?
2.3. Коли необхідно виконувати генетичне дослідження при ХП і як інтерпретувати його результати?
2.4. Які неендоскопічні методи візуалізації дозволяють діагностувати хронічний панкреатит?
2.5. Яка оптимальна фармакотерапія болю при хронічному панкреатиті?
2.6. Яке ендоскопічне лікування доступне для полегшення болю, пов’язаного з ХП? Яка роль екстракорпоральної ударно–хвильової літотрипсії в лікуванні пацієнтів з ХП?
2.7. Які хірургічні методи лікування болю при ХП?
2.8. Які є інші інтервенційні методи лікування болю, пов’язаного з хронічним панкреатитом?
2.9. Варіанти лікування псевдокіст підшлункової залози та їх ускладнень
2.10. Як лікувати екзокринну недостатність підшлункової залози і як контролювати лікування
2.11. Харчова підтримка при хронічному панкреатиті: як виявити, попередити та лікувати дефіцит поживних речовин
2.12. Які клінічні та лабораторні показники повинні використовуватися для подальшого спостереження за пацієнтами з хронічним панкреатитом?
2.13. У яких пацієнтів з ХП слід проводити скринінг на рак підшлункової залози?
3. Італійські керівні принципи консенсусу щодо хронічного панкреатиту (листопад 2010):
3.1. Чи доцільна ендоскопічна терапія у безсимптомних пацієнтів з хронічним панкреатитом і розширенням головної протоки підшлункової залози?
3.2. Які показання до операції у хворих з хронічним панкреатитом без екстрапанкреатичних ускладнень?
Список літератури
Додаток
Список скорочень
АТПО — аутологічна трансплантація панкреатичних острівців
ГПН — рівень глюкози в плазмі натще
ДУХЛ — дистанційна ударно-хвильова літотрипсія
ЕДТ — ендоскопічна декомпресійна терапія
ЕНПЗ — екзокринна недостатність підшлункової залози
ЕРХПГ — ендоскопічна ретроградна холангіопанкреатографія
ЖКХ — жовчнокам’яна хвороба
КТ — комп’ютерна томографія
МРХПГ — магнітно-резонансна холангіопанкреатографія
МРТ — магнітно-резонансна томографія
ПЗ — підшлункова залоза
ПЗПДР — пілорозберігаюча панкреатодуоденальна резекція
СЛТ — середньоланцюгові тригліцериди
УЗД — ультразвукове дослідження
ХП — хронічний панкреатит
ЦД-ХП — цукровий діабет, вторинний до хронічного панкреатиту
КАЖ — коефіцієнт абсорбції жиру
CFTR — ген трансмембранного регулятора кістозного фіброзу
HbA1c — глікозильований гемоглобін
SPINK 1 — ген інгібітора протеази Kazal типу 1
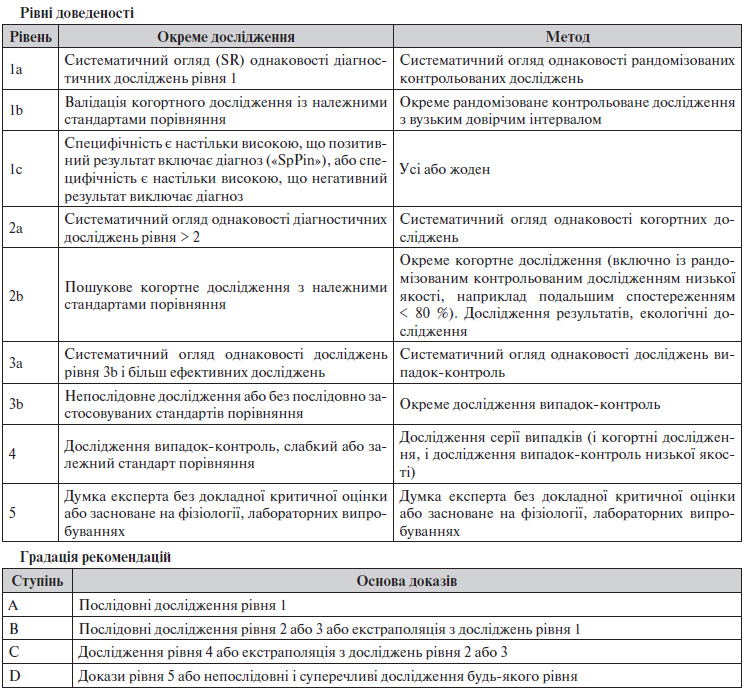
Шкала рівнів доведеності і градації рекомендацій
Italian consensus guidelines for chronic pancreatitis. November 2010
The Spanish Pancreatic Club recommendations for the diagnosis and treatment of chronic pancreatitis. February 2013
Рівні доведеності
Передмова мультидисциплінарної робочої групи з адаптації клінічної настанови. Синтез даних
Дана адаптована клінічна настанова для системи охорони здоров’я України є синтезом клінічних настанов:
— PRODIGY. Pancreatitis — chronic. December 2010, розроблена мережею Clinical Knowledge Summaries (CKS), Великобританія, для сімейних лікарів з метою забезпечення клінічних рекомендацій у сфері первинної медичної допомоги у Великобританії.
Положення настанови щодо надання вторинної (спеціалізованої) медичної допомоги адаптовані з наступних інформаційних джерел:
— Italian consensus guidelines for chronic pancreatitis. November 2010;
— The Spanish Pancreatic Club recommendations for the diagnosis and treatment of chronic pancreatitis: Part 1 (diagnosis). February 2013;
— The Spanish Pancreatic Club recommendations for the diagnosis and treatment of chronic pancreatitis: Part 2 (treatment). February 2013.
Дану адаптовану клінічну настанову пропонується розглядати як інформаційне джерело щодо вибору методів діагностичної та лікувальної тактики при хронічному панкреатиті (ХП). Дана клінічна настанова не повинна розглядатися та використовуватися в якості стандарту лікування. Стандарти лікування визначаються на основі всіх клінічних даних, доступних для кожного окремого випадку, і можуть піддаватися змінам у міру вдосконалення наукових знань і технологій, а також розробки моделей лікування.
Остаточне рішення щодо вибору певних клінічних процедур та плану лікування повинне бути ухвалене відповідним (-и) працівником (-ами) охорони здоров’я з урахуванням клінічних даних, отриманих у конкретного пацієнта, результатів діагностики і прийнятих методів лікування. Певні відхилення можливі, але вони повинні бути обґрунтовані відповідним чином — консиліумом фахівців на чолі з керівником підрозділу.
PRODIGY. Pancreatitis — chronic. December 2010
Вступ
Клінічна тема
Вік пацієнтів — від 18 років і старше.
Тема клінічної настанови «PRODIGY. Pancreatitis — chronic» висвітлює лікування хронічного запалення підшлункової залозі в умовах первинної допомоги.
Вона не стосується лікування гострого запалення підшлункової залози або специфічного лікування хронічного запалення підшлункової залози.
Цільовою аудиторією даної настанови є професійні працівники в галузі охорони здоров’я, зокрема Національної системи охорони здоров’я Англії, що надають первинну допомогу. Інформація для пацієнтів з NHS Choices призначена для роздрукування та надання пацієнтам за допомогою даного ресурсу або самостійно.
Коментар робочої групи
В Україні дана адаптована клінічна настанова призначена для використання лікарями загальної практики — сімейної медицини, лікарями терапевтами дільничними, гастроентерологами та іншими фахівцями, які надають медичну допомогу пацієнтам з хронічним панкреатитом, також з нею можуть ознайомитись пацієнти та інші зацікавлені особи в Реєстрі медико-технологічних документів за посиланням.
Мета створення настанови
Підтримка лікарів первинної допомоги щодо:
— встановлення первинного діагнозу хронічного запалення підшлункової залози за допомогою збору історії хвороби та огляду;
— направлення особи з підозрою на хронічне запалення підшлункової залози на відповідні дослідження та лікування;
— відповідного догляду та лікування підтвердженого хронічного запалення підшлункової залози.
Визначення хронічного панкреатиту
Хронічне запалення ПЗ є хронічним, незворотним, запальним та/або фіброзним захворюванням ПЗ, що часто характеризується сильним болем, інтенсивність якого посилюються при зміні положення тіла, та розвитком ендокринної та екзокринної недостатності.
Коментар робочої групи
Вважаємо, що термін «іммобілізуючий» є дещо невдалим. Скоріше за все, мається на увазі те, що біль знижує якість життя та перешкоджає повсякденній активності хворого.
Екзокринна панкреатична недостатність є результатом пошкодження ациноцитів з недостатнім виробленням ензимів травлення та виникає при знищенні 90 % функціональної екзокринної тканини ПЗ.
Ендокринна панкреатична недостатність є результатом пошкодження ендокринної тканини ПЗ (острівці Лангерганса) з недостатнім виробленням інсуліну, що спричиняє непереносимість глюкози та цукровий діабет [Mergener and Baillie, 1997; Bornman and Beckingham, 2001; Whitcomb, 2006; Nair et al., 2007; National Clinical Guideline Centre for Acute and Chronic Conditions, 2010].
Патофізіологія хронічного запалення ПЗ
Хронічне запалення ПЗ часто починається як повторний прояв гострого запалення ПЗ, однак у деяких пацієнтів гострий панкреатит відсутній в історії хвороби. Не у всіх пацієнтів навіть після повторного гострого панкреатиту розвивається ХП.
Гострий панкреатит є гострим запальним процесом ПЗ із різним ураженням місцевих тканин або більш віддалених систем організму.
Повторне запалення ПЗ характеризується чіткими проявами з періодами відновлення між епізодами.
Зараз прийнято етіологічну модель, за якою ХП виникає у людей, які мають неадекватну імунну відповідь при гострому запаленні ПЗ [Mergener and Baillie, 1997; Forsmark, 2006; Steinberg, 2006; Nair et al., 2007].
Чинники хронічного запалення ПЗ
Загальними чинниками хронічного запалення ПЗ є:
— Алкоголь.
— Ідіопатія (невизначені чинники).
Рідкісні причини хронічного запалення ПЗ:
— Аутоімунні захворювання.
— Генетичні порушення.
— Медичні препарати.
— Розлади метаболізму.
— Обструктивні процеси.
— Постнекротичне хронічне запалення ПЗ.
— Радіотерапія.
— Куріння.
— Травма.
— Тропічні умови.
Коментар робочої групи
У Західній Європі та США вважають, що біліарний панкреатит може бути тільки гострим. Це пов’язано з тим, що при першому ж епізоді біліарного панкреатиту на тлі жовчнокам’яної хвороби проводять оперативне лікування, тому цей панкреатит, як правило, не розвивається в хронічний. В Україні та країнах СНД часто хворі не оперуються впродовж тривалого часу, внаслідок чого розвивається ХП. В Україні хронічний біліарний панкреатит зустрічається часто. Жовчнокам’яна хвороба є причиною більш ніж половини випадків ХП в Україні. Розвиток хронічного біліарного панкреатиту можна попередити або зменшити ризик його розвитку при виконанні своєчасної холецистектомії. Формування хронічного біліарного панкреатиту можливе при хронічному безкам’яному холециститі, особливо за наявності біліарного сладжу, а також при біліарних дисфункціях.
Термін «тропічні умови» означає, що причиною розвитку панкреатиту є особливості харчування у країнах з тропічним кліматом.
Алкоголь
Алкоголь є причиною 70–90 % випадків хронічного запалення ПЗ, однак достеменний механізм невідомий. Найчастіше вражає чоловіків віком 40–50 років. При зловживанні алкоголем ризик розвитку хронічного запалення ПЗ зростає з кількістю та тривалістю споживання алкоголю.
ХП розвивається лише у 5–10 % осіб, які зловживають алкоголем, ймовірно, через важливість супутніх факторів, як, наприклад, генетичні зміни, харчування з високим вмістом жирів та білків або низькою кількістю антиоксидантів, куріння.
Біль при алкогольному хронічному запаленні ПЗ, ймовірно, полегшується через абстинентний стан, хвороба може прогресувати в тяжкості, незважаючи на припинення споживання алкоголю.
Супутній цироз печінки відносно рідко зустрічається у хворих з ХП [Mergener and Baillie, 1997; Bornman and Beckingham, 2001; Forsmark, 2006].
Ідіопатичний чинник
Хронічне запалення ПЗ класифікується як ідіопатичне, якщо всі інші можливі причини виключено. Ідіопатичне хронічне запалення ПЗ складає 10–20 % всіх випадків цього захворювання. Ранній ідіопатичний ХП діагностують у віці 10–20 років, пізній — у віці 50–60 років. Кількість вражених чоловіків та жінок однакова. В деяких випадках ідіопатичний ХП може бути діагностований невірно через такі причини:
— приховане вживання алкоголю або гіперчутливість до малої кількості алкоголю;
— попередня травма;
— генетичні причини [Mergener and Baillie, 1997].
Аутоімунні захворювання
Аутоімунні панкреатити складають до 5–6 % всіх випадків хронічного запалення ПЗ. Вони спричинені аутоімунною запальною відповіддю ПЗ. Частіше зустрічаються у чоловіків, а найчастіше спостерігаються у людей, старших за 50 років, однак захворювання має широку варіативність щодо віку.
Аутоімунний панкреатит є системним захворюванням, при якому часто розвиваються позапанкреатичні ушкодження, вражаються інші органи, такі як жовчний міхур, жовчні протоки, нирки, легені та слинні залози. Аутоімунні панкреатити пов’язані з іншими аутоімунними станами, такими як ревматоїдний артрит, синдром Сьоргена (Sjögren’s syndrome), первинний біліарний цироз, первинний склерозуючий холангіт, запальні захворювання кишківника [Finkelberg et al., 2006; Nair et al., 2007].
Генетичні чинники
Спадкове запалення ПЗ вражає невелику кількість родин, його успадковують як аутосомне домінантне захворювання, яке проявляється приблизно у 80 % випадків. Більшість випадків спричинена мутацією гену катіонного трипсогену (PRSS1), але деякі випадки викликані спонтанними мутаціями. Мутації пошкоджують інактивацію трипсину, дозволяючи активному трипсину самоперетравлювати власну ПЗ. У більш ніж 80 % клінічні ознаки захворювання проявляються до 20 років. У пацієнтів зі спадковим хронічним запаленням ПЗ ризик розвитку раку ПЗ складає 40 %.
Інші мутації, що в багатьох випадках спостерігалися при алкогольному, ідіопатичному або тропічному запаленні ПЗ, зокрема, такі:
— мутація гена інгібітора протеази Kazal типу 1 (SPINK 1);
— мутація гена трансмембранного регулятора кістозного фіброзу (CFTR).
Недостатність a1-антитрипсину також може спричинити ХП [Mergener and Baillie, 1997; Whitcomb, 2006].
Лікарські препарати
Запалення ПЗ, спричинене ліками, зазвичай проявляється як гострий панкреатит або повторні гострі панкреатити. Препарати, що найчастіше спричиняють хронічне запалення ПЗ:
— інгібітори ангіотензин-перетворюючого ензиму;
— статини;
— диданозин;
— азатіоприн;
— фуросемід;
— циметидин;
— кортикостероїди;
— ламівудин;
— гідрохлортіазид;
— вальпроєва кислота;
— оральні контрацептиви;
— інтерферон [Nair et al., 2007].
Порушення метаболізму
Обмінні порушення, що спричиняють хронічне запалення ПЗ:
— Гіпертригліцеридемія [Forsmark, 2006].
— Ниркова недостатність [Forsmark, 2006].
— Гіперкальціємія [Callery and Freedman, 2008].
— Хронічне запалення ПЗ розвивається у близько 10–15 % хворих на гіперпаратероїдизм [Mergener and Baillie, 1997].
Обструктивні чинники
Пошкодження тканин ПЗ, що можуть передувати обструкції протоків ПЗ:
— Стриктура протоків.
— Каміння в жовчному міхурі.
— Пухлина.
— Кіста стінки дванадцятипалої кишки.
— Дисфункція сфінктера Одді або стеноз.
Обструкція також може бути наслідком вроджених анатомічних вад:
— Розділена ПЗ (pancreas divisum).
— Кільцеподібна ПЗ (pancreas annulare).
Пошкодження може прогресувати, незважаючи на полегшення обструкції [Mergener and Baillie, 1997].
Постнекротичне хронічне запалення ПЗ
ХП може розвинутися після некротизуючого гострого запалення ПЗ, найчастіше після хірургічного видалення некротизованих тканин [Forsmark, 2006].
Променева терапія
Зрідка хронічне запалення ПЗ може виникнути через кілька років після абдомінальної радіотерапії [Forsmark, 2006].
Куріння
Зазвичай у людей, які страждають від алкогольного панкреатиту, збільшується ризик кальцифікації ПЗ (через обструкцію протоків ПЗ та попереднє пошкодження тканин ПЗ). Є незалежним фактором ризику запалення ПЗ. Пов’язане з підвищеним рівнем загальної смертності серед хворих на хронічне запалення ПЗ (це може бути спричинене фактом ураження курінням інших органів) [Forsmark, 2006].
Травма
Тупе або проникаюче поранення абдомінальної області може призвести до ураження ПЗ [Mergener and Baillie, 1997].
Тропічний панкреатит
Тропічне запалення ПЗ є найчастішою причиною ХП в тропічній Африці та на більшій території Азії. Може бути спричинене порушеннями травлення та споживанням великої кількості маніоки, але наразі ймовірніше це пов’язано з генетичними мутаціями [Mergener and Baillie, 1997; Bornman and Beckingham, 2001].
Поширеність
Дослідження у Франції, Японії та Китаї звітують, що частота проявів хронічного запалення ПЗ складає 6–9 випадків на 100 000 людей, а розповсюдженість — 14–33 на 100 000 людей [Bornman and Beckingham, 2001; Otsuki, 2003; Kocher, 2008; Wang et al., 2009]. PRODIGY не знайшов точних даних щодо частоти проявів та розповсюдженості ХП у Великобританії.
Коментар робочої групи
В Україні епідеміологічні показники захворюваності на ХП в 3–4 рази гірші, ніж у Європі, причому захворюваність і розповсюдженість продовжують зростати. В Україні рівень захворюваності на патологію ПЗ у 2002 р. склав 149,8, а поширеність — 2400–2760 на 100 тис. дорослих і підлітків. З 1997 р. показники зросли відповідно на 49,9 і 71,3 %. Первинна інвалідизація досягає 15 %. Хворі на ХП складають 25 % всіх, які звертаються в гастроентерологічні кабінети поліклінік України, а в спеціалізованих гастроентерологічних стаціонарах нашої країни ці хворі займають 9–12 % ліжок. Серед хворих на ХП у 30 % випадків розвиваються ранні ускладнення (гнійно-септичні, кровотечі з виразок гастродуоденальної зони, тромбоз у системі портальної вени, стеноз холедоха або дванадцятипалої кишки та ін.), летальність складає 5,1 %. З подальшим розвитком ХП, особливо при неефективному лікуванні, прогресує функціональна недостатність ПЗ, розвивається абдомінальний ішемічний синдром. Захворювання ПЗ в 10,9 % випадків є причиною інвалідизації хворих з патологією органів травлення [Н.В. Харченко, 2011].
Прогноз
Хронічний біль виникає часто, і його може бути важко позбутися. Він може тимчасово зникати, може бути постійним або з несподіваними спалахами. Біль може залишатися постійно однаковим, посилюватися або слабшати з часом.
Екзокринна та ендокринна недостатність формується у 40–50 % пацієнтів з хронічним алкогольним запаленням ПЗ за 8–20 років після виявлення хвороби.
Зазвичай тривалість життя скорочується до 10–20 років.
Причиною смерті часто є не сам панкреатит, а інші захворювання та ускладнення, пов’язані з наступним:
— продовження зловживання алкоголем;
— куріння (наприклад, емфізема, коронарна судинна недостатність, інсульт та злоякісні новоутворення поза ПЗ);
— рак ПЗ;
— післяопераційні ускладнення.
Псевдокісти та їх ускладнення спричиняють 5–10 % всіх летальних випадків при хронічному запаленні ПЗ. Пацієнти з алкогольним ХП, які продовжують вживати алкоголь, мають вищі показники смертності [Mergener and Baillie, 1997; Forsmark, 2006; Callery and Freedman, 2008; Lieb and Forsmark, 2009].
Ускладнення
Найбільш значущими ускладненнями хронічного запалення ПЗ є такі:
— Порушення травлення та мальабсорбція.
— Цукровий діабет.
— Формування псевдокіст.
— Обструкція вихідних відділів шлунка або дванадцятипалої кишки.
— Обструкція протоків жовчного міхура.
Рідше зустрічаються такі ускладнення:
— Фістули.
— Рак ПЗ.
— Псевдоаневризма.
— Тромбоз селезінкової або портальної вени.
Екзокринна недостатність розвивається майже у 40 % хворих на ХП та може спричиняти мальабсорбцію вітаміну B12 та недостатність жиророзчинних вітамінів, таких як вітамін D [Mergener and Baillie, 1997; Levy et al., 2006].
Цукровий діабет
Цукровий діабет розвивається у 50 % хворих на хронічне запалення ПЗ. Ризик збільшується за наявності кальцифікації ПЗ або хірургічного втручання щодо ПЗ. Очевидний цукровий діабет зазвичай виявляється пізно (часто за 20 років після виявлення захворювання) і важко піддається лікуванню:
— вражаються альфа-клітини ПЗ, які продукують глюкагон, а також інсулоцити, що продукують інсулін;
— сукупність недостатності глюкагону, порушень травлення та вживання алкоголю підвищує ризик гіпоглікемії: спонтанної або спричиненої вживаними ліками;
— гіпоглікемічна кома є частою причиною летальних випадків у тих, хто вживає алкоголь або переніс видалення ПЗ.
Діабетичний кетоацидоз, нейропатія та ретинопатія виникають рідко, але у курців може розвинутися ангіопатія. Діабет, спричинений аутоімунним хронічним запаленням ПЗ, можна вилікувати із застосуванням глюкокортикоїдів [Mergener and Baillie, 1997; Bornman and Beckingham, 2001; Levy et al., 2006; Ito et al., 2007].
Формування псевдокіст
Псевдокісти ПЗ є локалізованими відокремленими скопиченнями рідини всередині або поряд із ПЗ, спричиненими руйнуванням протоків ПЗ. Розвиваються у 25 % пацієнтів із ХП. У 25–30 % хворих із псевдокістами розвиваються такі ускладнення:
— місцеві механічні впливи, такі як біль, біліарна обструкція, ерозії кровоносних судин, що спричиняють кровотечу або інфекцію;
— розрив крізь плевроперитоніальні структури спричиняє плевральний випіт;
— розрив кісти до черевної порожнини призводить до тяжких асцитів.
Псевдокісти є причиною 5–10 % летальних випадків серед хворих на ХП [Mergener and Baillie, 1997; Bornman and Beckingham, 2001].
Обструкція вихідного відділу шлунка та дванадцятипалої кишки
Обструкція вихідного відділу шлунка або дванадцятипалої кишки спричиняє біль після прийому їжі, передчасне насичення їжею, нудоту та блювання. Псевдокісти в голівці ПЗ можуть спричиняти обструкцію вихідного відділу шлунка через надлишковий тиск на оточуючі тканини, який усувається після декомпресії псевдокісти [Mergener and Baillie, 1997; Bornman and Beckingham, 2001].
Обструкція протоків жовчного міхура
Стеноз або звуження протоків жовчного міхура може спричиняти біль, порушення рівня ензимів печінки та, можливо, жовтяницю та зазвичай є вторинним, тобто розвивається внаслідок фіброзу ПЗ. Також може виникати внаслідок набряку голівки ПЗ, і в такому разі жовтяниця та підвищення рівня ензимів печінки носять нестійкий характер або усуваються. Псевдокісти в голівці ПЗ можуть спричиняти біліарні обструкції через надлишковий тиск на оточуючі тканини, який усувається після декомпресії псевдокісти [Mergener and Baillie, 1997; Bornman and Beckingham, 2001].
Фістули
Формування фістули між протоком ПЗ та черевною або грудною порожниною може стати причиною розвитку абдомінального асциту або плеврального чи абдомінального випоту [Mergener and Baillie, 1997].
Рак ПЗ
Хронічне запалення ПЗ, пов’язане з алкоголем, підвищує ризик розвитку раку ПЗ в 15 разів, а куріння підвищує цей показник ще більше.
Ризик розвитку раку ПЗ протягом життя складає:
— 4 % усіх чинників хронічного запалення ПЗ;
— 40 % спадкового хронічного запалення ПЗ [Forsmark, 2006].
Псевдоаневризма
Це рідкісне ускладнення вражає артерії, найближчі до ПЗ, такі як селезінкова (найчастіше вражається), печінкова гастродуоденальна та панкреатодуоденальна [Nair et al., 2007].
Тромбоз селезінкової або воротної вени
Тромбоз селезінкової вени спричиняється запаленням селезінкової вени, оскільки вона проходить вздовж поверхні задньої стінки ПЗ, та може призводити до варикозного розширення вен стравоходу, шлунка, дванадцятипалої кишки та товстого кишківника з кровотечею. Лікується видаленням селезінки [Mergener and Baillie, 1997].
Коментар робочої групи
До ускладнень, які виникають, слід віднести також бактеріальні ускладнення, білково-енергетичну недостатність. Бактеріальні ускладнення виникають частіше при хронічному біліарному панкреатиті. Можуть розвиватися холангіти, абсцеси ПЗ та печінки, інфікування панкреонекрозу, сепсис [А.Н. Казюлин, 2005].
Діагностика та лікування
Діагностика: охоплює клінічні ознаки підозрюваного запалення ПЗ, диференційну діагностику, рекомендовані дослідження та направлення до відповідного спеціаліста. Лікування: охоплює лікування хронічного запалення ПЗ та надання спеціалізованої вторинної допомоги при звернені особи з визначеним ХП.
Діагностика хронічного запалення ПЗ
Рання діагностика ХП зазвичай складна і потребує участі спеціаліста вторинної допомоги. Наявні симптоми та ознаки схожі на хронічне запалення ПЗ за всіма чинниками, але найчастіше вони спричинені надмірним вживанням алкоголю.
Зберіть докладну історію хвороби та запитайте пацієнта про таке.
Споживання алкоголю. Для інформації щодо оцінки заподіяної шкоди, шкідливого впливу споживання алкоголю та алкогольної залежності зверніться до теми PRODIGY «Алкоголь — проблемне споживання».
Абдомінальні болі. Можливо, пацієнт має хронічний біль або в історії хвороби присутні записи щодо рецидивуючих епізодів болю, однак біль відсутній у 10 % пацієнтів із хронічним алкогольним панкреатитом. Якщо біль наявний:
— чи є біль в епігастральній області глибоким, сильним, тупим. Він може проходити наскрізь до спини або бути локалізованим у правому або лівому квадранті;
— він може бути періодичним, бути постійним або з сильними спалахами;
— може з’являтись, коли пацієнт сидить прямо або нахиляється вперед;
— часто з’являється після прийому їжі.;
— може супроводжуватись нудотою та блюванням.
Інші симптоми хронічного запалення ПЗ:
— здуття, кольки в животі;
— втрата ваги;
— стеаторея (рідкі, жирні випорожнення з сильним відразливим запахом, які важко змити, може спричиняти нетримання калу).
Коментар робочої групи
«Оперізуючий» біль при ХП має характерну іррадіацію вліво та доверху, за типом «повного поясу», «лівого або правого «напівпоясу». Біль може бути періодичним. У 20 % хворих на ХП біль може бути відсутній. Нудота та блювання при ХП не приносять полегшення. Крім того, біль може з’явитися на ранніх стадіях ХП, коли функціональні і структурні порушення ПЗ, які можна виявити, ще не розвинулися [The Spanish Pancreatic Club recommendations for the diagnosis and treatment of chronic pancreatitis: Part 1 (diagnosis). February 2013].
У разі розвитку цукрового діабету з’являється спрага, сухість у роті, збільшення об’єму сечі.
Під час об’єктивного обстеження клінічні ознаки можуть не співпадати за тяжкістю із вираженістю скарг. До типових ознак хронічного запалення ПЗ можуть відноситися:
— ознаки хронічного захворювання печінки (ймовірно при хронічному вживанні алкоголю);
— больові відчуття в епігастральній області;
— потовщення кінцевих фаланг пальців (внаслідок стеатореї);
— жовтяниця, спричинена наступним: супутнім захворюванням печінки; механічною обструкцією жовчних протоків ззовні печінки масою голівки ПЗ або псевдокістою. Псевдокіста визначається пальпацією;
— теплова еритема, що характеризується невиразним знебарвленням в епігастральній області або нижньому відділі хребта, що може говорити про застосування пацієнтом теплових джерел для полегшення болю впродовж тривалого часу;
— тверді вузли в шкірі через дисемінований некроз жирової тканини (проявляється рідко).
Коментар робочої групи
Крім цих ознак під час об’єктивного обстеження виявляється пальпаторна болісність у проекції ПЗ. Виявляються підшкірні геморагії, малі ангіоми, особливо на передній черевній стінці.
Обґрунтування рекомендацій
Інформація щодо клінічних ознак хронічного запалення ПЗ ґрунтується на думці експертів з наведених статей [Mergener and Baillie, 1997; Bornman and Beckingham, 2001; Callery and Freedman, 2008; Lieb and Forsmark, 2009], медичного підручника [Forsmark, 2006] та повного медичного керівництва «Порушення при вживанні алкоголю: Діагностика та клінічне лікування фізичних ускладнень, пов’язаних з вживанням алкоголю», опублікованого Національним центром клінічних методів при гострих та хронічних захворюваннях для Національного інституту охорони здоров’я та удосконалення медичної допомоги [NICE] [National Clinical Guideline Centre for Acute and Chronic Conditions, 2010].
Інші чинники
Захворювання та стани, які можуть супроводжуватися болем в абдомінальній області, наведені нижче.
Кишково-шлункові чинники:
— Гострий холецистит.
— Обструкція протоків жовчного міхура/каміння.
— Гострий панкреатит.
— Гострий апендицит.
— Дивертикулярний абсцес.
— Парез шлунка.
— Обструкція кишківника.
— Синдром подразненого кишківника.
— Мальабсорбція іншої етіології.
— Хвороба Крона.
— Пептична виразка.
— Пухлини ПЗ.
Судинні чинники:
— Гостра ішемія або інфаркт тонкого кишківника.
— Запалення аневризми черевної аорти.
Гінекологічні чинники:
— Гострий сальпінгіт (запалення маткових труб).
— Позаматкова вагітність.
— Ендометріоз.
— Кіста яєчника.
— Рак яєчника.
Неврологічні чинники:
— Грудна радикулопатія.
Коментар робочої групи
До інших чинників болю в абдомінальній області, які мають бути диференційовані з хронічним запаленням ПЗ, також відносяться хронічний холецистит, неспецифічний виразковий коліт, сечокам’яна хвороба, синдром хронічної абдомінальної ішемії, оперізуючий лишай.
Обґрунтування рекомендацій
Інформація щодо диференційної діагностики хронічного абдомінального болю ґрунтується на експертній оцінці, викладеній у двох статтях [Mergener and Baillie, 1997; Nair et al., 2007], а також на оцінці експертів-оглядачів PRODIGY.
Підтвердження діагнозу хронічного запалення ПЗ
Діагноз хронічного запалення ПЗ вимагає направлення для досліджень до вторинної спеціалізованої медичної допомоги. Однак дослідження при наданні первинної допомоги можуть бути корисними для попереднього діагнозу та виключення інших хвороб за нечіткої клінічної картини.
Звичайні лабораторні дослідження не рекомендовані при наданні первинної допомоги і не повинні затримувати перенаправлення пацієнта.
— За відсутності інфекції рівень лейкоцитів зазвичай залишається нормальним.
— Тести функцій печінки можуть мати відхилення за наявності інших захворювань печінки або через компресію жовчних протоків ПЗ (наприклад, через псевдокісту або фіброз в області голівки ПЗ).
— Рівень амілази в сироватці зазвичай не підвищується, не є діагностичним показником при хронічному запаленні ПЗ, і тому даний тест не слід проводити.
Слід прийняти до уваги абдомінальну ультрасонографію при нечіткому діагнозі з метою виключення інших захворювань, таких як жовчнокам’яна хвороба, та з’ясування ознак хронічного запалення ПЗ, таких як її кальцифікація.
Направлення до вторинної спеціалізованої допомоги необхідне для подальших досліджень, включаючи комп’ютерну томографію, для остаточного встановлення діагнозу при наявності за скаргами, анамнезом, об’єктивними даними підозри щодо ХП.
Обґрунтування рекомендацій
Лабораторні дослідження. Рекомендація щодо відсутності необхідності звичайних лабораторних досліджень під час первинної допомоги для підтвердження клінічного діагнозу хронічного запалення ПЗ ґрунтується на експертній оцінці, викладеній в двох статтях огляду [Mergener and Baillie, 1997; Callery and Freedman, 2008], медичному підручнику [Forsmark, 2006], а також на оцінці експертів PRODIGY.
Візуалізація. Абдомінальна ультрасонографія не рекомендована як метод візуалізації при первинній допомозі за наявності підозри на ХП, пов’язаній з вживанням алкоголю, через недостатню чутливість і специфіку в діагностиці хронічного запалення ПЗ та низької діагностичної цінності [National Clinical Guideline Centre for Acute and Chronic Conditions, 2010]. Однак, на думку експертів-оглядачів PRODIGY, абдомінальна ультрасонографія є більш точним методом візуалізації, ніж КТ, наприклад, для діагностики каменів та корисна при первинній допомозі за умов нечіткого діагнозу.
Порядок лікування та перенаправлення пацієнта з підозрою на хронічне запалення ПЗ:
— всіх пацієнтів слід направляти до гастроентеролога або спеціаліста в галузі захворювань ПЗ для підтвердження діагнозу;
— слід вживати невідкладну госпіталізацію, якщо пацієнт звертається з ускладненнями можливого хронічного запалення ПЗ.
Завжди, як тільки можливо, підтверджене хронічне запалення ПЗ має лікуватися командою спеціалістів вторинної допомоги. У будь-якому випадку, якщо пацієнт страждає від підтвердженого ХП і звертається до установи первинної допомоги, його слід відповідно направити.
Обґрунтування рекомендацій
Рекомендації щодо направлення по вторинну спеціалізовану допомогу для подальших досліджень ґрунтуються на медичному керівництві «Порушення при вживанні алкоголю: Діагностика та клінічне лікування фізичних ускладнень, пов’язаних з вживанням алкоголю», опублікованому Національним інститутом охорони здоров’я та удосконалення медичної допомоги [NICE, 2010].
Діагноз хронічного запалення ПЗ підтверджується на основі симптомів, наявних у пацієнта, результатів візуалізації з метою визначення структури ПЗ (УЗД, комп’ютерна томографія) та тестів екзокринної та ендокринної функції.
Направлення:
До дієтолога для зміни дієти, що включає низьку кількість жирів, багата на протеїни, висококалорійна та включає жиророзчинні вітамінні добавки.
До діабетолога невідкладно, якщо у пацієнта розвивається цукровий діабет — діабет, спричинений хронічним запаленням ПЗ дуже важко піддається лікуванню.
До гастроентеролога, хірурга, який займається оперативним лікуванням хвороб ПЗ та жовчних протоків, центру захворювань ПЗ або клініки болю, якщо біль у пацієнта не піддається контролю.
До гастроентеролога, хірурга, який займається оперативним лікуванням хвороб ПЗ та жовчних протоків або центру захворювань ПЗ, якщо пацієнт має повторні напади гострого запалення ПЗ.
Невідкладно (протягом 2 тижнів) до гастроентеролога або спеціаліста з ПЗ, якщо пацієнт із незрозумілих причин швидко втрачає вагу.
Госпіталізувати пацієнта у випадку тяжких гострих ускладнень панкреатиту або при гострому запаленні ПЗ.
Коментар робочої групи
Робочою групою до даної адаптованої клінічної настанови включені окремі розділи рекомендацій Іспанського панкреатичного клубу 2013 року та Італійського консенсусу з керівних принципів лікування хронічного панкреатиту 2010 року, в яких представлено методи діагностики і лікування пацієнтів з ХП на етапі надання спеціалізованої (вторинної) медичної допомоги.
The Spanish Pancreatic Club recommendations for the diagnosis and treatment of chronic pancreatitis. February 2013
Як визначається і діагностується екзокринна недостатність підшлункової залози?
На основі поняття про недостатність як нездатність органу виконувати свої фізіологічні функції і з урахуванням відомого функціонального резерву підшлункової залози екзокринна недостатність підшлункової залози (EНПЗ) має відноситися тільки до ситуації, в якій порушення функції підшлункової залози пов’язане з нездатністю підшлункової залози полегшувати нормальне травлення.
В даний час золотим стандартом для діагностики ЕНПЗ є визначення коефіцієнта абсорбції жиру (КАЖ) шляхом вимірювання екскреції жиру в калі, зібраному протягом 72 годин поспіль. Проте цей метод має низку недоліків: він клопіткий як для пацієнтів, так і для співробітників лабораторії, він не є широко доступним, і перевірка цим методом застаріла [31, 32]. При ХП секреція підшлункової залози нижче 10 % від нижньої межі норми, за вимірами тесту секретинхолецистокініну корелює з наявністю стеатореї [33]. Таким чином, він може використовуватися в якості тесту для діагностики ЕНПЗ. Проте цей тест не рекомендується через інвазивність, складність, вартість і відсутність протоколів. Був описаний варіант цього тесту, який використовує ендоскоп для отримання аспірату дванадцятипалої кишки [34], але в жодному дослідженні немає кореляції ендоскопічних тестів функції підшлункової залози з КАЖ. Класично вважається, що концентрація еластази в калі нижче 50 мкг/г узгоджується з наявністю EНПЗ. Проте немає жодних повідомлень щодо кореляції між фекальною еластазою і КАЖ у пацієнтів з ХП, а також у пацієнтів з муковісцидозом, ця кореляція погана з чутливістю тільки 40 % і специфічністю 81 % для діагностики EНПЗ [35]. Серед субстратів, використовуваних для дихального тесту із застосуванням змішаного тригліцериду 13C, який є єдиним, що порівнювався з відповідним КАЖ, демонструє високу кореляцію, чутливість 91 % і специфічність 91 % щодо діагнозу ЕНПЗ [36]. На жаль, цей тест не є широко доступним. Рівень наповнення дванадцятипалої кишки під час МРХПГ зі стимуляцією секретином має чутливість 69 % і специфічність 90 % у діагностиці ЕНПЗ за виміром КАЖ [37].
Рекомендація
Екзокринна недостатність підшлункової залози повинна характеризуватися тільки як ситуація, при якій порушення функції підшлункової залози пов’язане з неможливістю підшлункової залози здійснювати нормальне травлення (рівень доказовості 5, ступінь рекомендації D).
Хоча тест не є широкодоступним, КАЖ слід визначати за допомогою кількісної екскреції жиру з фекаліями, зібраними протягом 72 послідовних годин, що вважається золотим стандартом для цього діагнозу (рівень доказовості 5, ступінь рекомендації D). Значне зменшення фекальної еластази є підставою підозрювати наявність ЕНПЗ (рівень доказовості 5, ступінь рекомендації D). Дихальний тест з застосуванням змішаного тригліцериду 13C може бути підходящою альтернативою КАЖ для діагностики ЕНПЗ в контексті ХП (рівень доказовості 1b, ступінь рекомендації А). Зниження заповнення дванадцятипалої кишки після введення секретину при МРХПГ може бути індикатором екзокринної недостатності підшлункової залози, хоча нормальне заповнення дванадцятипалої кишки не виключає її наявності (рівень доказовості 1b, ступінь рекомендації А).
Коментар робочої групи
В України більш доцільним є використання тесту з визначенням фекальної еластази, оскільки збір калу протягом 72 годин потребує спеціальних умов, а тест з використанням 13С-змішаних тригліцеридів має високу вартість і може виконуватись тільки в окремих спеціалізованих гастроентерологічних центрах.
Як визначається і діагностується ендокринна недостатність підшлункової залози?
Цукровий діабет, вторинний до ХП (ЦД-ХП), який також класифікується як діабет типу 3с, включено до складу «інших специфічних форм» діабету в етіологічній класифікації ЦД Американської діабетичної асоціації і визначається як група метаболічних захворювань, що характеризуються гіперглікемією внаслідок недостатності секреції інсуліну і/або дії, вторинної до процесів, які дифузно впливають на підшлункову залозу [38].
Для діагностики ЦД-ХП рекомендується визначення глюкози в плазмі натще (ГПН ) та/або глікозильованого гемоглобіну (HbA1c). ГПН ≥ 126 мг/дл і/або HbA1c ≥ 6,5 % підтвердить діагноз ЦД; за відсутності однозначної гіперглікемії результат повинен бути підтверджений повторним тестом [38]. У випадках сумніву або граничних значень тест необхідно повторити або виміряти глюкозу в плазмі через 120 хв із навантаженням глюкози (75 г), оскільки послідовні зміни рівня глюкози в крові, сумісні з ЦД, можна спостерігати в тесті пероральної толерантності глюкози у 22 % пацієнтів з нормальним базовим рівнем глюкози [39]. У цьому випадку ГПН ≥ 200 мг/дл підтверджує діагноз.
Рекомендація
ЦД-ХП визначається як група метаболічних захворювань, що характеризуються гіперглікемією внаслідок дефектів секреції інсуліну та/або дії, вторинної до процесів, які дифузно впливають на підшлункову залозу (рівень доказовості 5, ступінь рекомендації D). Критеріями для діагнозу ЦД вторинно до ХП є ГПН ≥ 126 мг/дл і/або HbA1c ≥ 6,5 % (рівень доказовості 1a, ступінь рекомендації В).
Коли необхідно виконувати генетичне дослідження при ХП і як інтерпретувати його результати?
Спадковий ХП — це аутосомне домінантне спадкове захворювання з пенетрантністю гена 80 %. У 70 % пацієнтів зі спадковим ХП були зареєстровані мутації протеази, серину, 1 (трипсину 1) гена PRSS1 [53, 54]. Варіанти гена інгібітора протеази серину Kazal типу 1 (SPINK1) також асоціювалися з ХП; SPINK1 блокує активність внутрішньопанкреатичного трипсину, щоб попередити додаткову активацію трипсиногену і обмежити подальше ушкодження тканин [55]. Ген, який відповідає за синтез хімотрипсину C (CTRC), має низьку пенетрантність. Мутації в CTRC асоціювалися з ХП [56, 57]. Інший ген, мутації якого можуть бути пов’язані з ХП, це регулятор трансмембранної провідності (CFTR), який відповідає за муковісцидоз [58–62]. Повідомлялося про пацієнтів з мутаціями в кількох генах сприйнятливості, наприклад, пацієнти з мутаціями CFTR і SPINK1 мають дуже високий ризик панкреатиту [63]. Вважається, що мутації PRRS1 викликають спадковий ХП, а мутації в SPINK1, CFTR і CTRC призводять до алкогольного, ідіопатичного і тропічного панкреатиту.
У даний час пропонується, щоб пацієнти з рецидивуючим панкреатитом, із сімейним анамнезом панкреатиту і діти з незрозумілими епізодами цього захворювання перевірялися на мутації PRSS1 [64].
Діагностика спадкового панкреатиту важлива не тільки щодо ризику ХП, але і щодо високого ризику (близько 40 %) раку підшлункової залози [65]. Рекомендується, щоб ідентифікація інших генів, пов’язаних з панкреатитом, виконувалася тільки в межах дослідницьких протоколів [66]. Проте ця позиція повинна переглядатися відповідно до нових даних, які з’являються у цій галузі, і можливості того, що усунення супутніх факторів, таких як вживання тютюну чи алкоголю, змінить природну історію. Пацієнтам з виявленими мутаціями PRSS1 слід рекомендувати змінити спосіб життя, наприклад припинити вживання алкоголю (через його токсичність на підшлункову залозу) і тютюну (фактора ризику розвитку раку підшлункової залози). Також необхідно оцінити всіх прямих родичів і забезпечити генетичне консультування.
Рекомендація
Пацієнти з хронічним панкреатитом невідомої причини із сімейним анамнезом або діти з незрозумілими епізодами цього стану повинні бути перевірені на наявність мутацій у PRSS1, CFTR, і SPINK1 CTRC (рівень доказовості 5, ступінь рекомендації D).
Коментар робочої групи
На момент розробки даної адаптованої клінічної настанови в Україні дослідження на наявність мутацій в PRSS1, CFTR, і SPINK1 CTRC виконуються обмежено через високу вартість дослідження і недостатню кількість лабораторій, які можуть його проводити.
Які неендоскопічні методи візуалізації дозволяють діагностувати хронічний панкреатит?
ХП діагностується методами візуалізації на основі морфологічних змін залози, які можуть бути дуже помітними на його пізній стадії, але важко виявляються на ранніх стадіях [16, 17].
На простій рентгенографії черевної порожнини наявність кальцифікатів підшлункової залози з відповідними клінічними проявами може бути діагнозом ХП.
Трансабдомінальне УЗД виявляє ХП тільки пізньої стадії [18]. Комп’ютерна томографія (КТ) є кращим неендоскопічним методом візуалізації для діагностики та виявлення локалізації кальцифікації підшлункової залози. Як і УЗД, КТ корисна тільки для діагностики ХП у пізніх стадіях. Розширення протоки підшлункової залози і її вторинних гілок добре корелює з ендоскопічною ретроградною холангіопанкреатографією (ЕРХПГ). Вона також виявляє атрофію паренхіми й осередки уражень.
МРТ є більш чутливим методом у виявленні ранніх стадій ХП, спостерігають зміни сигналу перед появою морфологічних змін. Ці зміни включають втрату нормального високоінтенсивного сигналу в T1-зважених послідовностях. В артеріальній фазі після введення гадолінію сила сигналу зменшується, даючи гетерогенний зовнішній вигляд підшлункової залози; поглинання поступово збільшується в пізніх стадіях [19]. Магнітно-резонансна холангіопанкреатографія (MРХПГ) дає відмінну візуалізацію жовчних протоків та протоків підшлункової залози. Аномалії протоки підшлункової залози включають нерівномірне розширення та вигляд намистинок, часто містять внутрішньопротокові камені. Бокові гілки також розширені на пізній стадії [20]. MРХПГ після введення секретину може забезпечити кращу візуалізацію протоків підшлункової залози та її гілок і одночасно дозволити оцінити екзокринну функцію підшлункової залози на основі кількісного визначення заповнення дванадцятипалої кишки та коефіцієнта дифузії [21].
Рекомендація
Діагностика ХП методами візуалізації — рентген, УЗД черевної порожнини, КТ та МРТ/MРХПГ — відносно легка на пізніх стадіях захворювання. МРТ/MРХПГ і MРХПГ із секретином є неендоскопічними методами, які можуть виявити початкові стадії захворювання з більшою надійністю (рівень доказовості 2с, ступінь рекомендації В).
Коментар робочої групи
На момент розробки даної адаптованої клінічної настанови в Україні МРХПГ із введенням секретину не виконується, оскільки станом на 01.02.2014 р. секретин в Україні не зареєстрований.
PRODIGY. Pancreatitis — chronic. December 2010
Лікування хронічного запалення ПЗ
Лікування ХП зазвичай проводиться спеціалістами вторинної допомоги, але спеціалісти первинної допомоги можуть вжити наступних заходів.
Забезпечення адекватного полегшення болю:
— Призначити прості анальгетичні препарати при больових відчуттях від слабких до помірних, пов’язаних з хронічним запаленням ПЗ.
— Парацетамол або нестероїдні протизапальні препарати (ібупрофен) є відповідною терапією першої лінії.
— Переконатися у відсутності протипоказань щодо застосування нестероїдних протизапальних засобів та призначити інгібітор протонної помпи для захисту шлунка за необхідності.
— Розглянути питання призначення слабких опіатів, якщо прості анальгетики діють неадекватно.
Коментар робочої групи
Лікування болю повинно здійснюватися відповідно до медико-технологічних документів зі стандартизації медичної допомоги при хронічному больовому синдромі.
Якщо просте знеболення не діє адекватно, слід направити пацієнта до спеціалістів центру міждисциплінарної оцінки. До можливостей вторинної допомоги відносяться:
— Ендоскопічна терапія для усунення обструкції камінням протоків ПЗ або розширення стриктур.
— Хірургічні або інші втручання (наприклад, ендоскопічна ретроградна холангіопанкреатографія [ЕРХПГ] та стентування) для полегшення болю при хронічному запаленні ПЗ, пов’язаному з вживанням алкоголю, з обструкцією великих протоків або інших ускладнень, таких як псевдокіста ПЗ або обструкція вихідного отвору шлунка.
— Ад’ювантні препарати, такі як амітриптилін, габапентин або прегабалін.
— Блокада нервів на рівні черевних хребців, спланхнектомія (видалення черевного нерва) або хірургічне втручання, якщо біль у пацієнта контролюється слабко при хронічному запаленні ПЗ без обструкціі протоків.
Коментар робочої групи
Нестероїдні протизапальні препарати є основними засобами для полегшення болю при ХП, але більшій частині пацієнтів з резистентним до лікування болем потрібні опіоїдні препарати. Трамадол більш ефективний, ніж морфін, оскільки він менше впливає на функціональний стан шлунково-кишкового тракту. Опіоїдні засоби в різних формах мають таку ж ефективність [J.E. Dominguez-Munoz, 2005].
При вираженому загостренні ХП клінічна картина може наближатися до гострого панкреатиту. В таких випадках необхідно проводити дезінтоксикаційну інфузійну терапію [M. Buchler et al., 2002, 2004]. У деяких випадках виникає необхідність в антибактеріальній терапії. Це необхідно при розвитку бактеріальних ускладнень ХП або при підвищеному ризику таких ускладнень: при підозрі на панкреонекроз, при обструктивній жовтяниці, при підозрі на розрив панкреатичної протоки, в період формування псевдокісти. У цих ситуаціях призначають антибіотики, які добре проникають в паренхіму ПЗ і створюють в ній бактерицидну концентрацію: карбапенеми, цефалоспорини ІІІ–IV поколінь, фторхінолони, уреїдопеніциліни, похідні 5-нітроімідазолу в комбінації з цефалоспоринами [M. Buchler et al., 2002, 2004].
Перевірка на цукровий діабет
Щорічно має проводитись перевірка метаболізму глюкози разом із діабетологом при хронічному запаленні ПЗ.
Підтримка погоджених рішень
Лікування, розпочате при первинній та яке продовжується при вторинній допомозі, включає наступне:
— Призначення ензимів ПЗ при стеатореї та недостатності травлення або для полегшення болю.
— Кортикостероїди для лікування аутоімунного хронічного запалення ПЗ.
— Лікування гіпертригліцеридемії або гіперкаліємії.
— Лікування вторинного діабету при ХП призначається ендокринологом.
— Консультація спеціаліста, якщо пацієнт не відвідуватиме лікарню і потребуватиме рекомендації лікаря.
Забезпечення загальних порад щодо способу життя та психологічної підтримки. Зокрема, повна відмова від алкоголю та куріння.
Перенаправлення та госпіталізація до закладів вторинної допомоги прийнятні у випадках розвитку в пацієнта ускладнень, пов’язаних з хронічним запаленням ПЗ.
Обґрунтування рекомендацій
Дані рекомендацій ґрунтуються на сучасній практиці, думці експертів, викладеній у наведених статтях [Mergener and Baillie, 1997; Bornman and Beckingham, 2001; Finkelberg et al., 2006], медичному керівництві «Порушення при вживанні алкоголю: Діагностика та клінічне лікування фізичних ускладнень, пов’язаних з вживанням алкоголю», опублікованому Національним інститутом охорони здоров’я та удосконалення медичної допомоги [NICE, 2010], та думці експертів-оглядачів PRODIGY.
Знеболення. Хронічне запалення ПЗ часто характеризується нестерпним болем. Для багатьох пацієнтів просте знеболення, надане при первинній допомозі, може бути неадекватним. Тим не менше, хірургія та лікарські засоби вторинної допомоги мають можливості для полегшення прогресуючого або стійкого болю. Ця інформація ґрунтується на керівництві [National Clinical Guideline Centre for Acute and Chronic Conditions, 2010] та думці експертів-оглядачів PRODIGY.
Перевірка наявності цукрового діабету. Експерти-оглядачі PRODIGY вважають, що щорічна перевірка щодо цукрового діабету ґрунтується на значному співвідношенні пацієнтів, хворих на хронічне запалення ПЗ, у яких розвинувся цукровий діабет [Ito et al., 2007]. Думка щодо вибору методу перевірки розходяться: від випадкового аналізу крові на глюкозу та проби Боренгіра-Мангейма (ВМ-проба на рівень цукру в крові) до щорічного тесту на сприйняття глюкози у співпраці з діабетологом.
Додавання ензимів ПЗ. Призначення ензимів ПЗ рекомендоване NICE пацієнтам із хронічним запаленням ПЗ, пов’язаним із вживанням алкоголю, стеатореєю або недостатністю травлення. Терапевтичні заходи із застосування ензимів ПЗ мають починатися в установах вторинної допомоги [Winstead and Wilcox, 2009].
Кортикостероїди. Лікування із застосуванням кортикостероїдів є оптимальним для хворих на аутоімунне запалення ПЗ [Finkelberg et al., 2006].
Відмова від алкоголю та куріння. Надзвичайно важливо запровадити відмову від тютюну та алкоголю, бо вони є значущими чинниками хронічного запалення ПЗ, а продовження їх вживання пов’язане з негативними прогнозами.
Коментар робочої групи
З метою раннього виявлення цукрового діабету у хворих на ХП доцільно застосовувати методи діагностики відповідно до медико–технологічних документів зі стандартизації медичної допомоги при цукровому діабеті І типу.
У клінічній практиці діагностування екзокринної панкреатичної недостатності зазвичай ґрунтується на оцінці клінічного стану пацієнта, його випорожнень, інформації про втрату ваги у дорослих і відставання в розвитку в дітей.
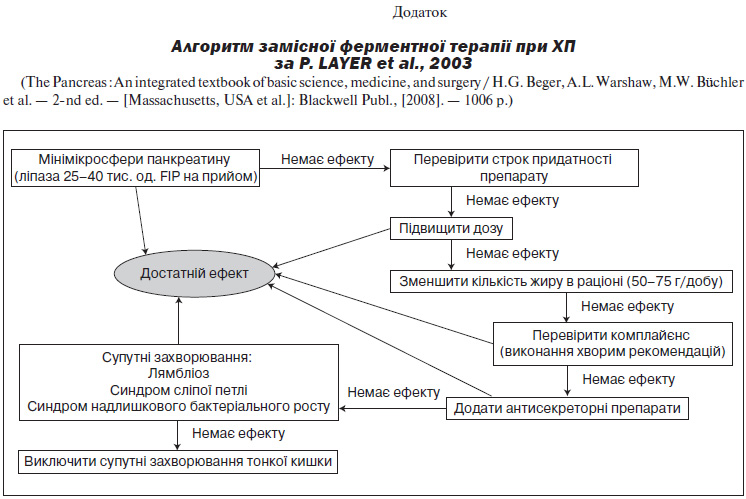
Згідно з даними клінічних досліджень та міжнародних керівництв із панкреатології, при ХП з ознаками зовнішньосекреторної недостатності ПЗ необхідне призначення ферментної замісної терапії.
Алгоритм призначення замісної ферментної терапії представлено в Додатку.
The Spanish Pancreatic Club recommendations for the diagnosis and treatment of chronic pancreatitis: Part 2 (treatment). February 2013
Яка оптимальна фармакотерапія болю при хронічному панкреатиті?
Перш ніж почати лікування болю, пов’язаного з ХП, треба виключити інші можливі супутні причини, такі як наявність псевдокіст, новоутворень шлунка або підшлункової залози, виразкової хвороби або утворення каменів жовчного міхура. Бажано також усунути причини ХП, такі як алкоголь або тютюнопаління, та обструкцію протоків або провести лікування аутоімунного панкреатиту. Є кілька високоякісних досліджень з лікування болю, пов’язаного з ХП. Болезаспокійливі препарати слід вводити в ефективних дозах з відповідними інтервалами з моніторингом ниркової, дихальної та печінкової функції. При медикаментозному лікуванні слід враховувати характер болю (безперервний або епізодичний) і лікувальний заклад (стаціонарний або амбулаторний). Клініцисти мають сприяти адекватному дотриманню лікування. Метод ВООЗ з полегшення болю може забезпечити основу для медикаментозного лікування болю при ХП [2].
Першим запропонованим кроком у фармакотерапії болю є парацетамол (який має безпечний профіль) при гострому або хронічному болю і нестероїдні протизапальні засоби (НПЗЗ), в тому числі метамізол, при гострому болю. Парацетамол є безпечним у пацієнтів із хронічним надмірним вживанням алкоголю [3–5]. Метамізол доступний не в усіх країнах з міркувань безпеки, проте реальна частота агранулоцитозу дуже низька [6–8]. При хронічному болю застосування НПЗЗ і метамізолу слід уникати у зв’язку з небажаними довгостроковими побічними ефектами. Було показано, що прегабалін помірно зменшує біль при ХП [9]. Прегабалін можна призначати при хронічному болю в комбінації з парацетамолом.
Якщо вищевказані процедури не контролюють біль, другим кроком рекомендується трамадол. Цей препарат ефективний у контролі болю і має менше побічних ефектів, ніж сильні опіати, особливо в плані моторики кишечнику [10]. Якщо прегабалін раніше не застосовувався, його можна вводити в комбінації з трамадолом.
Третім кроком буде застосування сильних опіоїдів, переважно з контрольованим вивільненням, щоб уникнути піків у плазмі і повільного досягнення центральної нервової системи (таким чином запобігаючи ефекту ейфорії) [11]. Доза повинна бути скоригована залежно від болю пацієнта. У клінічних випробуваннях порівняння трансдермального фентанілу з морфіном у препаратах з контрольованим вивільненням група фентанілу потребувала більш високих доз рятувального морфіну негайного звільнення і частіше мала місцеві шкірні реакції [12]. Інвазивне лікування слід розглядати, якщо лікування сильними опіоїдами повинно поширюватися більш ніж на три місяці, у разі побічних ефектів або відсутності реальної користі. Його слід розглядати у пацієнтів з помірним до сильного болем, щоб перейти безпосередньо до другого або третього кроку відповідно.
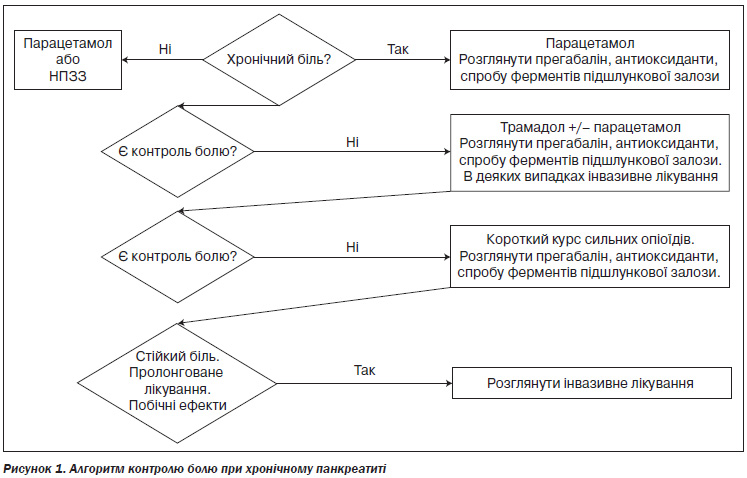
Деякі пацієнти можуть отримати користь від більш раннього інвазивного лікування, наприклад, при обструктивному хронічному панкреатиті. Використання ферментів підшлункової залози при болю, пов’язаному з ХП, залишається спірним. Проведені дослідження мають методологічні недоліки та недоліки дизайну [13], і результати були неоднорідними. Деякі дослідження не продемонстрували значного полегшення болю [14–16], але інші показали полегшення болю [17–19]. Більшість досліджень з позитивними результатами застосовували ферменти підшлункової залози без оболонки [17, 18], які доступні не в усіх країнах. В останніх систематичних оглядах застосовування ферментів підшлункової залози не показало чіткого впливу на болі [13, 20]. Проте, враховуючи низький профіль токсичності ферментів підшлункової залози і вищезазначені методологічні недоліки опублікованих досліджень, можна спробувати їх застосування [13]. У цьому випадку ми рекомендуємо 2-місячне застосування. Антиоксиданти показали довготривале легке зменшення болю у двох плацебо-контрольованих подвійних сліпих випробуваннях [21, 22]. У дослідженні кращого дизайну і з більшою кількістю включених пацієнтів застосовували коктейлі з антиоксидантів, які містять щоденні дози органічного селену, аскорбінової кислоти, бета-каротину, альфа-токоферолу і метіоніну [22]. Рекомендовані кроки для лікування болю підсумовані на рис. 1.
Рекомендація
Коли пацієнт звертається з болем, пов’язаним з ХП, лікар повинен спробувати усунути етіологію захворювання і виключити ускладнення та інші захворювання. Рекомендується знеболювальна терапія парацетамолом (гострого або хронічного болю) або НПЗЗ/метамізолом (гострого болю) (рівень доказовості 5, ступінь рекомендації D). Комбіноване лікування прегабаліном є варіантом (рівень доказовості 1b, ступінь рекомендації А).
На другому етапі рекомендується трамадол (з прегабаліном або без нього) (рівень доказовості 5, ступінь рекомендації D). У випадках постійного болю можна спробувати короткий курс сильних опіатів (рівень доказовості 2b, ступінь рекомендації B). Доцільно переглянути застосування сильних опіоїдів, якщо лікування продовжується понад три місяці, у випадку побічних ефектів або відсутності реальної користі (рівень доказовості 5, ступінь рекомендації D).
Антиоксиданти показали довготривале полегшення болю (рівень доказовості 1b, ступінь рекомендації А).
При цьому ефективність лікування ферментами підшлункової залози не була переконливо продемонстрована (рівень доказовості 1а, ступінь рекомендації А). Деякі пацієнти мають користь від двомісячного терміну застосування (рівень доказовості 5, ступінь рекомендації D).
Коментар робочої групи
В частині випадків за наявності дисфункції сфінктера Одді, наприклад, у хворих, яким виконано холецистектомію, ефективним засобом усунення болю є призначення селективних спазмолітиків, що діють прицільно на сфінктер Одді, зокрема доцільне призначення мебеверину [Dominguez-Munoz, 2005].
Яке ендоскопічне лікування доступне для полегшення болю, пов’язаного з ХП? Яка роль екстракорпоральної ударно-хвильової літотрипсії в лікуванні пацієнтів із ХП?
Інвазивне лікування болю у пацієнтів із ХП показане, коли медикаментозне лікування не допомагає або коли доводиться довго застосовувати опіоїди. Ендоскопічна декомпресійна терапія (EДT) є варіантом лікування болю у пацієнтів із розширеною головною протокою підшлункової залози (збільшений тиск протоки) і в пацієнтів з каменями, що спричиняють обструкцію або стеноз системи протоків [23, 24]. Рекомендуючи EДT для полегшення болю, лікар повинен враховувати низку обмежень: 1) Рандомізовані клінічні випробування, які порівнюють EДT і хірургічне лікування з приводу болю при ХП, показали кращі результати хірургічного лікування [25, 26]. Рандомізовані випробування порівняння ендоскопічного або хірургічного лікування з медикаментозною терапією не проводилися. 2) Важко визначити ефективність EДT у знеболюванні в довготривалому дослідженні без контрольної групи з урахуванням тенденції зникнення її ефекту з плином часу [27]. 3) EДT з приводу ХП є технічно складною і тому залежить від оператора.
EДT з використанням ендоскопічної ретроградної холангіопанкреатографії (ЕРХПГ) складається з дилатації, розміщення стента в області стенозу і екстракції каменів з головної протоки. З таким підходом у 70–94 % пацієнтів відзначається короткотривале, а у 52–82 % пацієнтів — довготривале полегшення болю [28–33]. Камені, стеноз або комбінація обох можуть викликати обструкцію протоків підшлункової залози; EДT дає аналогічні результати у пацієнтів з усіма трьома типами обструкції [29]. EДT зменшує кількість випадків госпіталізації з приводу болю і необхідність знеболювальної терапії [34, 35]. Проте EДT не змінює якості життя пацієнтів [26, 36, 37]. Розширення стенозу протоки підшлункової залози не є корисним лікуванням, якщо воно не супроводжується розміщенням одного або декількох стентів для підтримання отвору. Крім того, стенти повинні залишатися в місці протягом довгого часу (від одного до двох років) і вимагають заміни у випадках обструкції і рецидиву симптомів [38]. Кілька стентів можуть поліпшити результат EДT [39]. У третини пацієнтів після видалення стента виникає рецидив болю [28, 30, 31]; такий біль часто полегшується, коли встановлюється новий стент. Екстракорпоральна ударно-хвильова літотрипсія (ЕУХЛ) була доведено корисною у лікуванні болю, пов’язаного з ХП, у метааналізі серії різних випадків [40] і в рандомізованому дослідженні, яке порівнювало монотерапію ЕУХЛ з ЕУХЛ у комбінації з ендоскопією [41]. У цьому клінічному випробуванні не було ніяких доказів того, що комбінація ендоскопії і ЕУХЛ була краще, ніж монотерапія ЕУХЛ, для профілактики болю.
Блокада/невроліз сонячного сплетення під спостереженням EУЗ шляхом застосування кортикостероїдів та/або спирту є одним з варіантів для полегшення болю і поліпшення якості життя пацієнтів з ХП, і це може бути використано у пацієнтів з нерозширеною головною протокою підшлункової залози [42]. Невроліз під спостереженням EУЗ асоціюється з кращими результатами і є більш економічно ефективним, ніж невроліз під спостереженням КТ, і має низьку частоту побічних ефектів [43, 44]. Проте ефективність такої терапії залишається неясною. Немає рандомізованих досліджень з порівняння корисності блокади сонячного сплетіння/невролізу під контролем ЕУЗ з плацебо у пацієнтів з ХП і мало результатів досліджень щодо тривалих спостережень [45]. Загалом 55–70 % пацієнтів відчули короткотривале полегшення болю [44–49] і менше 10 % пацієнтів відчули тривале полегшення болю (більше 24 тижнів) [44].
Рекомендація
Ендоскопічне декомпресійне лікування менш ефективне і має короткотривалі ефекти порівняно з хірургією (рівень доказовості 1b, ступінь рекомендації B).
Було показано, що ендоскопічне лікування болю у пацієнтів з ХП було ефективним у пацієнтів із розширеною головною протокою підшлункової залози, особливо коли поєднуються різні ендоскопічні методи (рівень доказовості 3b, ступінь рекомендації B).
Стенти підшлункової залози є ефективними для лікування короткотривалого болю у пацієнтів зі стенозом протоки підшлункової залози, але це вимагає кілька ЕРХПГ протягом періоду спостереження (рівень доказовості 4, ступінь рекомендації С). Стенти підшлункової залози повинні стояти не менше 12 місяців (рівень доказовості 3b, ступінь рекомендації B).
ЕУХЛ є ефективною для видалення внутрішньопротокових каменів і полегшує біль (рівень доказовості 2a, ступінь рекомендації B).
Блокада сонячного сплетення під спостереженням EУЗ може бути варіантом для лікування болю, пов’язаного з ХП, у деяких пацієнтів, які не відповідають на інші варіанти лікування (рівень доказовості 4, ступінь рекомендації С).
Коментар робочої групи
На момент розробки даної адаптованої клінічної настанови в Україні ударно-хвильова літотрипсія та блокада черевного сплетіння при захворюваннях ПЗ не виконуються.
Які хірургічні методи лікування болю при ХП?
Операції у пацієнтів з ХП показані в трьох випадках: нестерпний біль, рак підшлункової залози і при деяких ускладненнях ХП.
Немає підтвердженого порогу для призначення операції з приводу контролю болю [50]. В даний час немає ніяких доступних рандомізованих контрольованих випробувань з порівняння хірургії з консервативним лікуванням або різного часу операції. Як було зазначено, ми рекомендуємо інвазивне лікування пацієнтів з болем, які отримують сильні опіоїди більш ніж три місяці, у випадках побічних ефектів або відсутності реальної користі.
Якщо коротко, то поточні варіанти операції з приводу болю діляться на три категорії: декомпресія (з упором на гіпертензію протоки [51]), резекція (з упором на запальні пухлинні маси [52–54] і голівку підшлункової залози, де виникає біль [55, 56]) і змішані методи.
1. Методи декомпресії. Методи декомпресії повинні застосовуватися у пацієнтів з дилатацією головної протоки підшлункової залози (> 7–8 мм) [57] і відсутністю запальних мас. Найчастіше виконувана методика декомпресії — це методика, яку випустили Partington і Rochelle в 1966 році [58]. Ця методика досягає полегшення болю у 66–91 % пацієнтів із низькою захворюваністю та смертністю (20 і 2 % відповідно) [26, 59–61]. Проте довготривалі результати показують, що майже у 50 % пацієнтів настає рецидив болю і зберігається у 15–30 % пацієнтів [61–63]. Проспективне рандомізоване випробування порівнювало техніку панкреатоєюностомії з ендоскопічним трансампулярним дренуванням [26]. У кінці дослідження (на 24 місяці) повне або часткове полегшення було досягнуте у 32 % пацієнтів з ендоскопічним дренуванням і у 75 % пацієнтів з хірургічним дренажем.
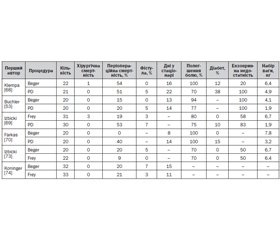
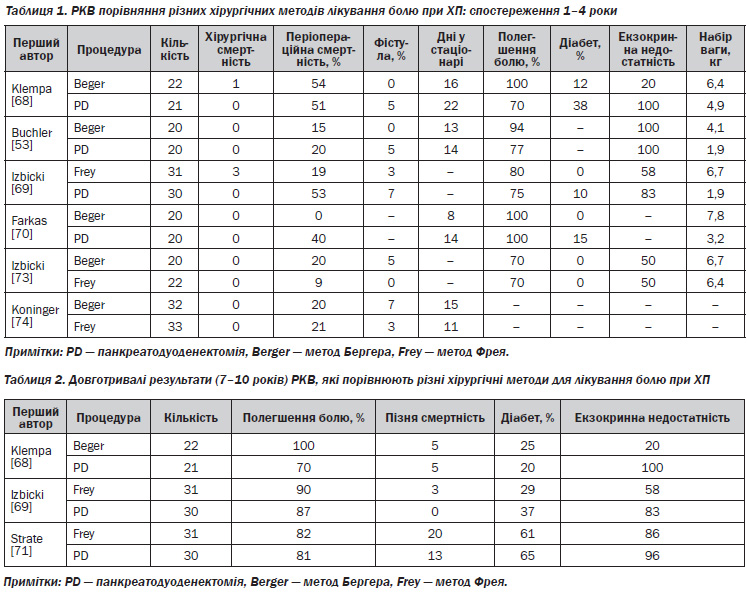
2. Методи резекції показані у пацієнтів із запальними масами голівки підшлункової залози, особливо якщо є підозра на рак підшлункової залози. Резекція дистальної частини підшлункової залози показана при запальних пухлинних масах або постобструктивному ХП, що впливають на тіло або хвіст підшлункової залози [64]. Деякі автори вважають голівку підшлункової залози тригером болю підшлункової залози при ХП [55, 56], тому вони виступають за резекцію. У трьох основних хірургічних серіях панкреатодуоденектомія продемонструвала полегшення болю на 4 і 6 роках у 71 і 89 % пацієнтів відповідно [65–67]. Рандомізовані контрольовані випробування показали короткотривале полегшення болю у 70–100 % пацієнтів (табл. 1) і довготривале у 70–87 % (табл. 2) [53, 68–71]. Проте захворюваність, пов’язана з панкреатодуоденектомією [68–70], на користь більш консервативних змішаних методів (табл. 1 і 2).
3. Змішані методи. Існують також змішані резекції і дренажні методи. В основі цих методів є видалення запальної маси в голівці підшлункової залози і дренування обструкції підшлункової області (тіла і хвоста). В даний час найбільш широко використовуються два методи: 1) часткова резекція голівки підшлункової залози зі збереженням дванадцятипалої кишки, або метод Бегера [56], і 2) видалення серцевини голівки підшлункової залози, пов’язане з технікою поздовжньої панкреатоєюностомії, або техніка Фрея [72]. У рандомізованих контрольованих випробуваннях змішані втручання показали короткотривале полегшення болю у 70–100 % пацієнтів (табл. 1) і довготривале полегшення болю у 82–100 % (табл. 2) [53, 68–71, 73, 74 ].
Була описана хірургічна процедура, яка може бути корисною при легкому захворюванні протоки без запальної маси: поздовжнє видалення вентральної частини підшлункової залози у формі V у поєднанні з поздовжньою панкреатоєюностомією [75].
У таблиці 1 представлені рандомізовані контрольовані проспективні дослідження, які порівнюють два або більше втручань [53, 68–70, 73, 74]. Таблиця 2 включає рандомізовані контрольовані випробування з довготривалим спостереженням [68, 69, 71].
Рекомендація
Резекція, декомпресія або змішана техніка досягають полегшення болю, яке підтримується протягом довгого часу приблизно у 80 % хворих (рівень доказовості 1а, ступінь рекомендації А).
Які є інші інтервенційні методи лікування болю, пов’язаного з хронічним панкреатитом?
У цілому пацієнти з розширеною протокою є кандидатами на ендоскопічну або хірургічну декомпресію, які розглядалися раніше в цьому консенсусі. Проте інтервенційні методи, які показані пацієнтам без розширення протоків, обговорюються в цьому розділі. Блокада сонячного сплетіння обговорювалася раніше. Ці інтервенційні методи також можуть бути використані, коли декомпресійне лікування невдале. Докази їх використання незначні. Опубліковані дослідження не мають контрольної групи.
Двостороння торакоскопічна абляція великих вісцеральних нервів вивчалась проспективно у пацієнтів з ХП [76] і показала довготривале полегшення болю на 28 %. У систематичному огляді був зроблений висновок, що цей метод зменшує біль і асоціюється з поліпшенням якості життя [77]. Він описує черезшкірну радіочастотну вісцеральну абляцію [78].
Інтратекальна терапія безперервним інфузійним насосом морфіну була описана в серії випадків [79] з хорошим знеболюючим результатом. У всіх випадках процедури виконувались у пацієнтів, у яких інші стандартні методи зазнали невдачі. Опубліковані серії випадків повідомили, що у пацієнтів з ХП і стійким болем досягнуто поліпшення після імплантації стимулятора задніх зв’язок [80].
Променева терапія вивчалася для лікування болю при ХП [81, 82]. У нещодавно опублікованому дослідженні призначали одноразову дозу 8 Гр пацієнтам з повторними гострими нападами загострення ХП або хронічного болю, що призвело до повної відсутності симптомів у 13 з 15 пацієнтів [82].
Рекомендація
Абляція вісцеральних нервів може полегшити болі, пов’язані з ХП (рівень доказовості 4, ступінь рекомендації C).
Коментар робочої групи
На думку Dominguez-Munoz (2005), абляція нервів не завжди є ефективною, але супроводжується високим ризиком побічних ефектів.
Варіанти лікування псевдокіст підшлункової залози та їх ускладнень
Псевдокіста підшлункової залози — це накопичення рідини з високою концентрацією амілази, оточено фіброзною тканиною. Більшість досліджень не роблять різниці між псевдокістами при гострому і хронічному панкреатиті і включають мало пацієнтів, що ускладнює прийняття рішень. Більшість псевдокіст невеликі і безсимптомні [83]. Псевдокісти, пов’язані з ХП, мають менше шансів самостійно зникнути, ніж кісти, які пов’язані з іншими розладами.
Тридцять дев’ять відсотків псевдокіст при ХП розвиваються таким чином, що спонтанно зникають [84]. Тривалість і розмір псевдокіст неточно прогнозують ймовірність спонтанної ремісії або розвиток ускладнень, проте більші (> 4 см ) та/або більш тривалі (> 6 тижнів) псевдокісти, як правило, є кістами, які вимагають активного лікування [85].
Інвазивні процедури з приводу псевдокіст включають черезшкірне або ендоскопічне дренування та хірургію. Показаннями до інвазивного лікування є: компресія судин, симптоматична компресія шлунка або дванадцятипалої кишки, стеноз жовчних протоків, інфекція, кровотеча, панкреатоплевральний свищ і синдром панкреатит-панікуліт-поліартрит, іншими словами, це залежить від наявності симптомів, пов’язаних із псевдокістами. Псевдокісти можуть рости поступово, в таких випадках інвазивне лікування може бути необхідним навіть у безсимптомних пацієнтів, щоб уникнути розриву псевдокісти. Черезшкірний дренаж рідко показаний, тільки при наявності інфекції [86], коли ендоскопічні і хірургічні методи не доступні. Це лікування слід розглядати, якщо клінічна ситуація пацієнта змушує провести швидкий дренаж, а хірургічні ризики дуже високі. Черезшкірний дренаж слід використовувати з обережністю, оскільки наявність проксимальної обструкції буде викликати свищі підшлункової залози [87].
Якщо існує комунікація, більшість псевдокіст можна дренувати ендоскопічно через сосочок шляхом розміщення стента в головній протоці підшлункової залози або трансмурального дренажа. Дренаж через EУЗ є високоефективним і має низьку частоту побічних ефектів і смертність [88]. При множинних псевдокістах із некротичними залишками хірургічному дренажу зазвичай надають перевагу [89].
Операція показана при великих кістах, множинних кістах і таких, які супроводжуються стенозом, каменями або порушенням протоків. Хірургічні методи, що використовуються для лікування псевдокіст, включають створення комунікації з шлунково-кишковим трактом (шлунком, дванадцятипалою кишкою або порожньою кишкою) і резекцію псевдокіст (іноді в поєднанні з резекцією підшлункової залози). У деяких випадках може бути необхідним дренаж головної протоки підшлункової залози. Операція є високоефективною методикою [90]. Показники успіху, ускладнень і рецидивів хірургічного лікування аналогічні ЕУЗ дренажу, проте EУЗ дренаж пропонує більш коротке перебування в лікарні і нижчу вартість [91].
Найнебезпечнішим ускладненням псевдокіст є розрив псевдоаневризми будь-якої з перипанкреатичних артерій, який може бути пов’язаний з масивною внутрішньою кровотечею і високим ризиком смерті. Ангіоемболізація є методом вибору при лікуванні псевдоаневризми при ХП. Операцію слід зарезервувати в якості другої лінії лікування, якщо емболізація не припиняє кровотечі [92–94]. Рецидив кровотечі та захворюваність більш поширені після операції, ніж після ангіоемболізації [95].
Рекомендація
Спонтанне зникнення псевдокісти при хронічному панкреатиті буває рідко (рівень доказовості 4, ступінь рекомендації С).
Активне лікування має бути зарезервоване для симптоматичних або складних псевдокіст (рівень доказовості 4, ступінь рекомендації С).
Ендоскопічне внутрішнє дренування має переваги над хірургічним дренуванням (рівень доказовості 2с, ступінь рекомендації B).
Бажано лікувати розрив псевдоаневризми ангіографічними методами, які використовують переваги діагностичної ангіографії; операції повинні бути зарезервовані для ситуацій, в яких ангіографія була неефективною (рівень доказовості 4, ступінь рекомендації С).
Italian consensus guidelines for chronic pancreatitis. November 2010
Е.1: Чи доцільна ендоскопічна терапія у безсимптомних пацієнтів з хронічним панкреатитом і розширенням головної протоки підшлункової залози?
Заява (EL 5 — RGD): Немає показань до ендоскопічного лікування безсимптомних пацієнтів із розширенням головної протоки підшлункової залози.
Консенсусні рівні погодженості:
А+ 84,6 %; A 7,7 %; А– 2,6 %; D– 2,6 %; D 2,6 %; D+ 0 %
Доцільність ендоскопічного дренування у пацієнтів із безсимптомним розширенням головної протоки підшлункової залози полягає у відновленні відтоку панкреатичного соку і запобіганні розвитку екзокринної та ендокринної недостатності підшлункової залози, щоб затримати процес атрофії залози. У хірургічній літературі обмежені дослідження показали поліпшення функції підшлункової залози після панкреоєюностомії [169]. Проте не існує жодного ендоскопічного дослідження, яке б оцінювало ендоскопічне лікування щодо результатів ендокринної та екзокринної функції підшлункової залози у цих пацієнтів.
S.1: Які показання до операції у хворих з хронічним панкреатитом без екстрапанкреатичних ускладнень?
Заява (EL 4 — RGC): Основним показанням до операції є недієздатність і сильний біль.
Заява (EL 4 — RGC): Іншим показанням до операціє є підозра на рак підшлункової залози.
Консенсусні рівні погодженості:
А+ 76 %; A 11,6 %; А– 11,6 %; D– 0 %; D 0 %; D+ 0 %
Біль є найбільш частим симптомом при хронічному панкреатиті, хоча різної частоти і тяжкості [227]. Хоча ніякі проспективні рандомізовані дослідження ще не порівнювали консервативне та хірургічне лікування, є докази, що операція ефективна при болю. Операція, з урахуванням передбачуваного болю, забезпечує його тривале полегшення.
На сьогодні було проведено вісім рандомізованих досліджень з порівняння різних методів лікування [36, 174, 228–233]. Одне з них не включало полегшення болю як кінцеву точку [233]. Решта сім досліджень включали хірургічне лікування 302 пацієнтів і отримали істотне полегшення болю у більшості пацієнтів, які перенесли деривативну і резективну операції. Більш того, два рандомізованих дослідження показали більшу користь від операції, ніж від ендоскопічного лікування, для контролю болю при хронічному панкреатиті з обструкцією протоків підшлункової залози [36, 174].
Підозра на рак. Необхідно розглядати три аспекти: 1) асоціацію між хронічним панкреатитом і раком підшлункової залози [57, 60]; 2) необхідність розрізняти центральні внутрішньопротокові папілярні муцинозні новоутворення і хронічний панкреатит, щоб уникнути неправильного консервативного лікування; 3) необхідність діагностики аутоімунного панкреатиту, щоб уникнути непотрібної резекції. Поліпшення передопераційних діагностичних інструментів (EУЗ, КТ, МРТ, ПЕТ, гістології, лабораторних аналізів) дозволяє поставити правильний діагноз у більшості випадків підозри на злоякісність. Проте якщо підозру на рак не можна виключити, пацієнт повинен пройти резективну операцію, а не деривативну, щоб отримати відповідний матеріал для гістологічного діагнозу. Затримка в лікуванні раку підшлункової залози через неправильний діагноз часто є фатальною [234, 235].
Коментар робочої групи
Показаннями для хірургічного втручання вважають також: кальциноз ПЗ і камені проток з вираженим больовим синдромом; обструктивний ХП — при неможливості ендоскопічної декомпресії; обтураційну жовтяницю за рахунок стиснення холедоха; дуоденостеноз; підпечінкову портальну гіпертензію; кісти більше 6 см в діаметрі або свищ ПЗ, що не виліковуються консервативно протягом 3 місяців; вторинний ХП, пов’язаний з ЖКХ, виразкою, що пенетрує, дуоденостазом, абдомінальним ішемічним синдромом; парафатеральні дивертикули [The Pancreas, 2008; Шалімов, 2000].
The Spanish Pancreatic Club recommendations for the diagnosis and treatment of chronic pancreatitis. February 2013
Як лікувати екзокринну недостатність підшлункової залози і як контролювати лікування
Лікування екзокринної недостатності підшлункової залози (EНПЗ) засноване на заміщенні пероральних ферментів підшлункової залози для оптимізації процесу перетравлення та засвоєння поживних речовин. Хоча може бути погане перетравлення жирів, вуглеводів і білків при EНПЗ, більшість авторів в першу чергу вивчали стеаторею, оскільки вона виникає рано і часто при ХП [136, 137]. Спочатку терапію пероральними ферментами слід рекомендувати пацієнтам зі стеатореєю (> 15 г/день) [138] або порушенням всмоктування ліпідів (13С-тригліцеридний дихальний тест (13С-ТДТ)) [139] або пацієнтам з діареєю, втратою маси тіла або іншими клінічними або лабораторними ознаками харчової недостатності [138, 139]. Користь лікування пацієнтів з легкою стеатореєю (7–15 г/день) спірна.
Серед доступних препаратів ферментів тільки мінімікросфери або мікросфери з ентеророзчинним покриттям показали достатню терапевтичну ефективність при EНПЗ, пов’язаній із ХП [139], в рандомізованих подвійних сліпих дослідженнях [140, 141]. Замісна ензимотерапія покращує травлення і засвоєння поживних речовин і пов’язана зі значним поліпшенням якості життя пацієнтів з ХП [19]. Доза ферментів повинна бути достатньою для заміщення екзокринної функції підшлункової залози. В цілому, хоча немає ніяких рандомізованих випробувань, які порівнюють різні дози ферментів, дослідження показали, що клінічна ефективність досягається з введенням мінімальної дози 40 000–50 000 Ph.Eur.U (одиниць європейської фармакопеї) ліпази під час кожного основного прийому їжі і половини цієї дози (20 000–250 000 Ph.Eur.U.) під час їжі вранці та вдень [139–142]. Ферменти мають бути розподілені впродовж їжі або прийняті наприкінці їжі [143].
Незважаючи на застосування препаратів ферментів у ентеророзчинній оболонці мінімікросфер і застосування відповідних доз з оптимальними режимами дозування, замісна ензимотерапія не показала нормалізацію травлення жиру приблизно в 40 % випадків EНПЗ, вторинної до ХП [139, 144]. Недостатнє дотримання пацієнтом лікування, кислотна рН в кишечнику, наявна у більшості пацієнтів з EНПЗ, та наявність кишкового росту бактерій є основними факторами неефективності лікування. Пригнічення секреції кислоти інгібіторами протонної помпи значно підвищує ефективність ензимотерапії ферментами у формі мінімікросфер з ентеророзчинним покриттям у пацієнтів з EНПЗ, вторинною до ХП, які мали недостатню відповідь на монотерапію ферментами [144]. Симптоматична відповідь на замісну ензимотерапію (тобто полегшення або зникнення симптомів і таких ознак, як пронос, здуття живота або втрата маси тіла) не гарантує нормалізацію травлення та живлення у хворих з EНПЗ, вторинною до ХП [139–142]. Таким чином, моніторинг відповіді на лікування повинен також засновуватися на об’єктивних параметрах, тобто нормалізації травлення, вимірюваної КАЖ або дихальним тестом, або стандартизацією статусу харчування пацієнта. Через обмежену доступність згаданих діагностичних тестів достатньо нормалізації параметрів живлення і поліпшення симптомів, щоб визначити ефективність замісної ензимотерапії в більшості випадків.
Рекомендація
Пероральна ензимотерапія показана пацієнтам з явною стеатореєю, або порушенням всмоктування ліпідів, або з діареєю, втратою маси тіла, або іншими клінічними та лабораторними ознаками недостатності поживних речовин (рівень доказовості 2b, ступінь рекомендації B).
Мінімікросфери або мікросфери з ентеророзчинним покриттям продемонстрували ефективність при лікуванні екзокринної недостатності підшлункової залози, вторинної до ХП. Мінімальна доза ліпази від 40 000 до 50 000 Ph.Eur.U рекомендується з кожним основним прийомом їжі, і половина дози — з їжею вранці та вдень (рівень доказовості 5, ступінь рекомендації D). Її необхідно приймати в середині або в кінці їжі (рівень доказовості 1b, ступінь рекомендації А).
Пригнічення секреції кислоти інгібіторами протонної помпи покращує ефективність ензимотерапії ентеророзчинними мінімікросферами у пацієнтів, які недостатньо відповіли на монотерапію ферментами (рівень доказовості 1b, рівень рекомендації А). Інші причини поганої відповіді включають погане дотримання лікування та надлишковий ріст бактерій. Щоб оцінити ефективність замісної ензимотерапії, в більшості випадків достатньо перевірити нормалізацію харчових параметрів і поліпшення симптомів (рівень доказовості 2b, ступінь рекомендації B).
Коментар робочої групи
Інгібітори протонної помпи сприяють зниженню стимуляції зовнішньосекреторної функції ПЗ і тому в частині випадків зменшують вираженість абдомінального болю [The Pancreas, 2008].
У разі резистентного болю при вираженому загостренні ХП, недостатній ефективності інгібіторів протонної помпи призначають октреотид [J.E. Dominguez-Munoz, 2005].
Харчова підтримка при хронічному панкреатиті: як виявити, попередити та лікувати дефіцит поживних речовин
Найважливішим механізмом, який лежить в основі харчової недостатності, є EНПЗ; інші фактори включають збільшення витрати енергії, супутній біль у животі, діабет і зловживання алкоголем [145]. Таким чином, часто виявляється дефіцит жиророзчинних вітамінів [146–150], кальцію, цинку [151, 152] й іноді вітаміну В12 [153].
Через такий високий ризик недостатності поживних речовин вкрай важливо провести ретельну оцінку статусу поживних речовин, що включає вимірювання маси тіла, симптомів, які перешкоджають живленню, вживання алкоголю, оцінку харчової цінності продуктів (шляхом обчислення енергії), відсотку мікроелементів і кількість споживаних поживних мікроелементів, антропометричні дані, оцінку маси м’язів і жирової маси та наявності асциту або набряку, а також аналіз крові, який включає визначення рівня альбуміну, жиророзчинних вітамінів і вуглеводного та кісткового метаболізму [154].
Перед початком конкретного лікувального харчування важливо контролювати біль у животі і припинити споживання алкоголю. Дієта, яка забезпечує 35 ккал/кг/день, 1–1,5 г/кг/день білка і 30 % жиру, є багатою на складні вуглеводи і має низький вміст клітковини, як правило, є достатньою для підтримки харчового статусу [154]. Рекомендується щоденний прийом полівітамінів з мінералами і нормально калорійна дієта, щоб запобігти дефіциту поживних речовин при надмірній масі тіла [155, 156].
Класично клініцисти рекомендують зменшити споживання харчових жирів до < 20 г/добу у пацієнтів зі стеатореєю, хоча немає ніяких доказів на підтримку цієї рекомендації [157]. У цьому контексті ензимозамісна терапія EНПЗ повинна бути оптимізована.
Нерозчинну клітковину необхідно вживати помірно, щоб запобігти можливим перешкодам у дії добавок ферментів [136]. У випадках втрати маси тіла, незважаючи на оптимальне лікування EНПЗ, необхідно ввести пероральні харчові добавки з полімерними нормальними/гіперкалорійними формулами у міру необхідності. Формули інтактного білка, як правило, добре переносяться, проте якщо це не так, можна доповнити формули частково перевареного пептиду. Добавки середньоланцюгових тригліцеридів (СЛТ) не продемонстрували послідовної користі. Рандомізоване контрольоване випробування показало, що комерційний препарат, збагачений СЛТ, не показав ніякої переваги над домашнім збалансованим харчуванням для поліпшення харчового статусу пацієнтів з ХП [158]. Крім того, дотримання прийому добавок СЛТ низьке через їх смак і високу вартість [155, 159].
Ентеральне харчування показане у таких випадках: 1) втрата маси тіла, незважаючи на вищевказані заходи, 2) низький рівень споживання через болі в животі, 3) гострі ускладнення, при яких показане штучне харчування, і 4) перед плановою операцією у випадках від помірної до важкої харчової недостатності. Ентеральне харчування з доступом через порожню кишку (назо-порожньокишкова трубка) повинно включати дієти з частково гідролізованими пептидами і середньоланцюговими тригліцеридами (CЛT), хоча немає жодних довгострокових досліджень, що демонструють ефективність. Якщо ця ситуація триває довше восьми тижнів, слід розглядати еюностомію або хірургічну черезшкірну ендоскопічну/радіологічну гастростомію [155, 157, 160]. Парентеральне харчування показане у пацієнтів з наступними проблемами: 1) стеноз дванадцятипалої кишки, 2) свищі підшлункової залози і 3) важка харчова недостатність до операції, коли ентеральне харчування неможливе. Клінічний дефіцит тіаміну і так званий синдром відновлення живлення може розвиватися у виснажених хворих, які не отримують належної підтримки поживних речовин, особливо в перші дні парентерального харчування [159].
Якщо є нестача вітамінів, це необхідно виправити. Був описаний дефіцит жиророзчинних вітамінів (А, D, Е і К), кальцію, магнію, цинку, міді, тіаміну, вітаміну В12 і фолієвої кислоти. Хоча цей дефіцит часто не помічають клінічно, він може викликати порушення обміну речовин кісток і втому. Цей дефіцит, якщо спостерігається, повинен поповнюватися тільки перорально, і парентеральне введення слід використовувати, якщо пероральне застосування не нормалізує дефіцит вітамінів. Якщо є дефіцит вітаміну D, добавка кальцифедіолу краща через її високу полярність. Рівні кальцію повинні контролюватися у хворих, які отримують кальцифедіол через підвищений ризик гіперкальціємії [155, 157].
Рекомендація
Висока поширеність харчової недостатності при хронічному панкреатиті вимагає виявляти осіб, які потребують харчової підтримки (рівень доказовості 2с, ступінь рекомендації B).
Підтримка адекватного раціону, виправлення дефіциту поживних мікроелементів, застосування ферментів підшлункової залози і лікування болю показали позитивний вплив на стан харчування хворих з хронічним панкреатитом (рівень доказовості 2с, ступінь рекомендації B).
Коментар робочої групи
Станом на 01.02.2014 р. лікарський засіб кальцифедіол в Україні не зареєстровано.
При відсутності парентеральних форм лікарських препаратів, які містять жиророзчинні вітаміни, можливе призначення цих вітамінів перорально [J.E. Dominguez-Munoz, 2005].
Які клінічні та лабораторні показники повинні використовуватися для подальшого спостереження за пацієнтами з хронічним панкреатитом?
Метою моніторингу ХП є раннє виявлення ендокринної і екзокринної недостатності та ускладнень, які можуть виникнути на будь-якій стадії захворювання. Цими ускладненнями є псевдокісти, обструкції жовчних шляхів, дванадцятипалої кишки, надмірний зріст бактерій, асцит, пов’язаний з підшлунковою залозою, внутрішньопротокові або заочеревинні інтракістозні крововиливи, тромбоз селезінки і/або брижі і рак підшлункової залози. Для моніторингу ХП не встановлено, як часто необхідно проводити спостереження і які параметри необхідно контролювати. Доцільним у пацієнтів зі стабільним ХП є проведення клінічного та лабораторного спостереження кожні 6 місяців. У пацієнтів з ускладненнями подальше спостереження повинно проводитися за необхідності у кожному випадку.
Перебіг болю у животі може бути непередбачуваним, але має тенденцію полегшуватися з плином часу, і навпаки, ЕНПЗ і ЦД-ХП, як правило, погіршують. Важливо встановити диференційний діагноз з іншими процесами, які можуть спричиняти епізоди черевного болю з аналогічними характеристиками. Жовтяниця виникає внаслідок обструкції інтрапанкреатичної загальної жовчної протоки через запалення і фіброз підшлункової залози, а в деяких випадках — через компресію псевдокісти.
Обструкція дванадцятипалої кишки через ХП може бути пов’язана з запаленням голівки підшлункової залози або з псевдокістами. Асцит, пов’язаний з підшлунковою залозою, виникає в результаті розриву передньої протоки підшлункової залози або, частіше, через псевдокісти. Пацієнти зі змінним типом болю, втратою маси тіла і/або жовтяницею повинні бути обстежені на рак підшлункової залози.
Щодо лабораторних аналізів, необхідних пацієнтам з ХП, немає ніяких даних, заснованих на доказах, щоб встановити, які параметри повинні бути проаналізовані і як часто. Таким чином, рекомендація повинна включати аналіз показників крові, який дозволить контролювати наслідки хвороби і включатиме загальний аналіз з параметрами поживних речовин та печінки, підшлункової залози і глікемічного профілю.
Щоб виявити виникнення EНПЗ, необхідно виконати функціональні тести. Хоча, як зазначалося вище, золотим стандартом є КАЖ, який є трудомістким, незручним і широко не застосовуваним тестом, який часто замінюють іншим, більш доступним (хоча і менш точним), наприклад, тестом фекальної еластази [89] або дихальним тестом мічених тригліцеридів [36]. У пацієнтів з EНПЗ бажано час від часу виконувати денситометрію кісток у зв’язку з підвищеним ризиком розвитку остеопенії та остеопорозу [90]. Оцінка ендокринної функції підшлункової залози рекомендується у всіх пацієнтів з ХП шляхом щорічного визначення рівня глюкози в плазмі натще і HbA1c [38].
Рекомендація
У пацієнтів зі стабільним ХП клінічне та лабораторне спостереження рекомендується кожні 6 місяців. У пацієнтів з ускладненнями спостереження повинно проводитися за необхідності у кожному випадку (рівень доказів 5, ступінь рекомендації D). Наявність ендокринної і екзокринної недостатності підшлункової залози необхідно оцінювати щорічно впродовж періоду спостереження (рівень доказовості 5, ступінь рекомендації D). При появі болю або якщо є зміни типу болю, важливо встановити диференціальний діагноз з іншим процесами, які можуть викликати епізоди черевного болю з аналогічними характеристиками (рівень доказовості 2b, ступінь рекомендації С).
Коментар робочої групи
Санаторно-курортне лікування хворих на ХП є ефективним етапом відновлювального лікування даної категорії хворих у фазі стійкої ремісії, оскільки природні та преформовані фізичні чинники здатні справляти суттєвий протизапальний ефект щодо тканини ПЗ, володіють спазмолітичною та десенсибілізуючою дією, поліпшують зовнішньо- та внутрішньосекреторну функції залози (стимулюють виділення панкреатичного соку, збільшують вміст бікарбонатів, відновлюють вміст ферментів у секреті ПЗ), поліпшують кровопостачання органу, відновлюють функціональний стан органів травлення.
Проведення реабілітаційних заходів пацієнтам, у яких захворювання знаходиться у стадії ремісії, також представляється важливою медичною та соціальною задачею, оскільки природні та преформовані фізичні чинники володіють саногенетичною та превентивною спрямованістю впливу, що дає змогу збільшувати періоди ремісії захворювання, поліпшувати якість життя [J.E. Dominguez-Munoz, 2005; Н.Б. Губергріц із співавт., 2007].
У яких пацієнтів з ХП слід проводити скринінг на рак підшлункової залози?
Зв’язок між ХП і раком підшлункової залози був підтверджений у кількох епідеміологічних і когортних дослідженнях. Проте ці дослідження отримали різні висновки щодо кількісного визначення ризику залежно від методів і типу ХП. Не повинно бути часового збігу між діагнозом ХП і раком підшлункової залози. Тому, щоб розглядати справжній випадок раку в пацієнта з ХП, повинно пройти не менше 2 років прогресування від встановлення діагнозу ХП. Недавно був опублікований метааналіз, щоб з’ясувати, які типи ХП піддаються ризику розвитку раку підшлункової залози [91]; був зроблений висновок, що у 5 % пацієнтів із ХП буде розвиватися рак підшлункової залози впродовж 20 років після встановлення діагнозу панкреатиту. Проте спадковий панкреатит має набагато вищий ризик розвитку раку підшлункової залози. Пацієнти з ХП мають ризик раку підшлункової залози в 5–10 разів вищий, ніж решта населення, і ще вищий ризик мають пацієнти зі спадковим панкреатитом [92, 93]. Зокрема, відповідно до Міжнародного дослідження спадкового панкреатиту, ризик раку підшлункової залози в 50 разів вищий у пацієнтів зі спадковим панкреатитом, ніж у населення в цілому [94], і, відповідно до Європейського реєстру спадкового панкреатиту і раку підшлункової залози, ці пацієнти мають більш високий ризик розвитку раку підшлункової залози після 50 років, незалежно від генотипу [65].
Експерти на IV Міжнародному симпозіумі спадкових захворювань підшлункової залози рекомендують програми скринінгу для пацієнтів зі спадковим панкреатитом [92].
Немає чіткого консенсусу щодо того, як проводити скринінг на рак підшлункової залози. Багато центрів рекомендують використовувати EУЗ, виходячи з його здатності визначати патологічні ділянки розміром менше 1 см [95, 96] і можливість проведення тонкоголкової аспірації. Проте ця можливість зменшується, коли є запалення підшлункової залози, як і у випадку спадкового панкреатиту [97]. КТ і МРХПГ також представляють труднощі, оскільки вони мають обмежену чутливість для виявлення невеликих уражень, які потенційно виліковні.
Правильний час, коли необхідно починати проводити скринінг, також є спірним і засновується на рекомендаціях експертів [92]. Було встановлено, що скринінг повинен починатися у віці 45 років. Якщо є сімейна історія спадкового панкреатиту, скринінг повинен починатися за 15 років до наймолодшого віку, в якому випадок раку підшлункової залози з’явився в цій родині. У курців скринінг повинен починатися ще раніше [98]. Також немає ніякої узгодженості щодо частоти моніторингу; рекомендується в діапазоні від щорічно до кожні 3 роки [92].
Рекомендація
Спадковий панкреатит є єдиною формою панкреатиту, при якій рекомендується скринінг для виявлення раку підшлункової залози в ранній стадії (рівень доказовості 2b, ступінь рекомендації В).
Рекомендується метод EУЗ кожні 1–3 роки, але цей метод має обмеження (рівень доказовості 5, клас рекомендації D). Скринінг повинен початися у віці 45 років або за 15 років до наймолодшого віку, в якому випадок раку підшлункової залози зафіксовано в цій родині (рівень доказів 5, ступінь рекомендації D).
PRODIGY. Pancreatitis — chronic. December 2010
Коментар робочої групи
В міжнародній практиці прийнято видавати окремі версії настанов для пацієнтів, що містять короткі відомості щодо захворювання чи стану, які розглядаються в повній версії клінічної настанови, методів профілактики, лікування, реабілітації тощо. В документі PRODIGY. Pancreatitis — chronic. December 2010 така інформація представлена, і робоча група вважає доцільним включити її в дану адаптовану клінічну настанову.
Інформація для пацієнтів
Вступ
Панкреатит є запаленням підшлункової залози (ПЗ). Основний симптом — біль в абдомінальній області, який часто буває сильним.
ПЗ є невеликим за розміром і за формою схожим на листок органом, розташованим поза шлунком і нижче грудної клітини.
ПЗ виконує дві важливі функції:
— виробляє травні соки для перетравлення їжі;
— виробляє потужні «речовини-кур’єри», які називаються гормонами, що можуть мати важливий вплив на всі клітини тіла.
Інсулін є найважливішим гормоном, що продукується ПЗ, оскільки він регулює рівень цукру (глюкози) в крові.
Існує два види запалення ПЗ:
— гострий панкреатит, при якому ПЗ запалена невеликий проміжок часу, що минає за кілька днів;
— хронічний панкреатит, при якому запалення ПЗ триває роками з усе більшим пошкодженням, що розвивається після попередніх повторюваних епізодів гострого панкреатиту.
Наскільки часто трапляється хронічне запалення ПЗ? Хронічне запалення ПЗ не є рідким захворюванням. 45 зі 100 000 чоловіків та 12 зі 100 000 жінок страждають від хронічного запалення ПЗ. ХП в основному вражає чоловіків. Найчастіше він виявляється у віці 40–50 років.
Тривале зловживання алкоголем є найзначущим фактором ризику розвитку хронічного запалення ПЗ. Вважається, що тривале зловживання (протягом років) призводить до 70 % випадків ХП.
Коментар робочої групи
В Україні на ХП частіше хворіють жінки у віці 40–60 років. Жовчнокам’яна хвороба значно підвищує ризик виникнення ХП [Н Б. Губергріц із співавт., 2007].
Перспектива. Перспектива хронічного запалення ПЗ залежить від кількох факторів:
— Вік пацієнта, в якому діагностовано захворювання.
— Звичка споживання алкоголю.
— Ступінь ураження ПЗ, за якого припиняється вироблення інсуліну (що призводить до симптомів, пов’язаних з діабетом).
Наприклад, у чоловіка 20 років без звички до споживання алкоголю з діагностованим ХП хороші перспективи. Це не матиме значного впливу на його тривалість життя.
Тривалість життя 50-річного чоловіка з хронічним запаленням ПЗ, тривалою звичкою до зловживання алкоголем може скоротитися на 10–20 років через те, що невідповідне функціонування ПЗ додає навантаження на весь організм.
Близько 70 % пацієнтів з хронічним запаленням ПЗ виживають щонайменше протягом 10 років після встановлення діагнозу. Близько 45 % пацієнтів з хронічним запаленням ПЗ виживають щонайменше протягом 20 років після встановлення діагнозу.
Однак ліків від хронічного запалення ПЗ немає, лікарські засоби можуть лише контролювати симптоми болю. В тяжких випадках може знадобитися хірургічне втручання. Найефективнішим способом попередження ХП є уникнення споживання алкоголю або принаймні помірне споживання.
Симптоми. Більшість пацієнтів відчуває нерегулярні напади больових відчуттів.
Біль. При ХП біль локалізований у верхній частині черева та дає відчуття тягнучого болю, часто сильного. Біль може переміщатися від черева вздовж спини. Часто біль стає сильнішим після їжі. До певної міри нахил вперед або згинання можуть допомогти полегшити біль. Також під час нападів болю Ви можете відчувати нудоту або блювати. З розвитком хронічного запалення ПЗ напади болю можуть траплятись частіше та з сильнішим відчуттям. Дехто відчуває постійний біль у череві.
Тривалий ХП. Коли ПЗ втрачає здатність виробляти інсулін та травні соки (що приймають участь у перетравленні їжі в травній системі), можуть з’являтися нові симптоми.
Зазвичай ПЗ втрачає ці функції через багато років після появи перших симптомів. Недостатність інсуліну означає розвиток панкреатогенного діабету (діабет типу 1) в майбутньому. Симптоми цього діабету такі:
— посилення спраги;
— часте сечовипускання;
— почуття сильного голоду;
— втрата ваги;
— стомлюваність;
— розмитість зору.
Панкреатогенний діабет (діабет типу 1) контролюється регулярними ін’єкціями інсуліну. Недостатність травних соків, що виробляються ПЗ, означає ускладнення перетравлення жирів та певних білків. Це може призвести до того, що випорожнення стають більш жирними та набувають більш неприємного запаху. Часто фекалії важко змити в туалеті.
У Вас також можуть бути такі симптоми:
— здуття;
— кольки в череві;
— надмірний метеоризм.
Чинники. Хронічне запалення ПЗ зазвичай розвивається після повторюваних нападів гострого панкреатиту, що призводять до постійного ураження ПЗ.
Гострий панкреатит. Гостре запалення ПЗ порушує утворення трипсину. Трипсин є ензимом, що виробляється ПЗ. Він потрібен для полегшення розщеплення білків в їжі для допомоги травленню. Коли трипсин виробляється ПЗ, він залишається в неактивному стані та не має травних властивостей. Так відбувається, поки трипсин не вивільняється з ПЗ до кишківника і не стає активним та здатним до розщеплення білків. У випадку гострого запалення ПЗ трипсин активується ще в ПЗ та починає руйнувати її клітини, що призводить до подразнення та запалення.
Алкоголь є найголовнішим фактором ризику розвитку гострого панкреатиту, його вживання може призводити до активації трипсину у ПЗ, але чому це відбувається, неясно. Вважається, що молекули етанолу порушують нормальну роботу клітин ПЗ, і вони передчасно активують трипсин.
Алкогольне хронічне запалення ПЗ. Як і при гострому панкреатиті, зловживання алкоголем є найбільшим фактором ризику розвитку хронічного запалення ПЗ (70 % випадків). Особи, які вживають велику кількість алкоголю, мають збільшений ризик повторюваних нападів гострого запалення ПЗ. З часом це призводить до хронічного запалення ПЗ. ХП, спричинений зловживанням алкоголю, відомий як алкогольний ХП. Алкогольний ХП зазвичай розвивається у людей, які споживають більше 10 одиниць алкоголю на добу протягом 10–15 років. Більше 4 пінт пива або більше 5 бокалів вина складають більше 10 одиниць алкоголю на день.
Алкогольний ХП порівняно нечасто розвивається у людей з тривалою звичкою зловживання алкоголем. Захворювання вражає 5–10 % людей із тривалою звичкою зловживання алкоголем. Існує думка, що люди, вражені алкогольним хронічним запаленням ПЗ, мають певні «змінені гени» (генетичні мутації), які роблять їх більш вразливими до впливу алкоголю.
Ідіопатичне хронічне запалення ПЗ. У 30 % випадків хронічного запалення ПЗ чинник розвитку хвороби невідомий або його неможливо пояснити. ХП, що виник з невідомих причин, називають ідіопатичним запаленням ПЗ. Ідіопатичні ХП зазвичай розвиваються у дітей та молодих люди в віці від 10 до 20 років і у дорослих віком старше 50 років. Зрідка ідіопатичний ХП вражає й інші вікові категорії.
Є припущення, що генетичні мутації можуть бути причиною ідіопатичного хронічного запалення ПЗ. У половини хворих на ідіопатичний ХП було визначено два окремих змінених гени — ген SPINK-1 та ген CFTR. Можливо, мутація цих двох генів порушує нормальну роботу ПЗ.
Рідкісні чинники. Близько 1 % всіх випадків ХП складають:
— аутоімунний ХП — рідкісне захворювання, при якому імунна система починає атакувати ПЗ;
— спадковий панкреатит — рідкісне генетичне захворювання, при якому люди народжуються з порушеннями ПЗ;
— фіброзно-кістозна дегенерація ПЗ — генетичне захворювання, при якому певні органи, включаючи ПЗ, можуть бути пошкоджені.
Діагностика. На відміну від гострого запалення ПЗ, відповідних аналізів крові для визначення ХП немає. Захворювання зазвичай діагностується лише за тестами, що оцінюють ПЗ. Якщо за результатами оцінки Ваших симптомів та історії хвороби Ваш лікар підозрює у вас наявність хронічного запалення ПЗ, Вас буде направлено для подальших обстежень. Ці обстеження можуть бути наступними:
— рентген;
— ультразвукове дослідження;
— сканування за допомогою комп’ютерного томографа (КТ);
— магнітно-резонансна томографія (МРТ);
— ендоскопічна ретроградна холангіопанкреатографія (ЕРХПГ).
Лікування
Зміни способу життя. Якщо у Вас діагностовано хронічне запалення ПЗ, можливо, буде необхідним дещо змінити в способі життя. Найважливішою є відмова від вживаня алкоголю. Це допоможе захистити Вашу ПЗ від пошкодження та, можливо, допоможе зменшити больові симптоми.
Ви маєте повідомити свого лікаря, якщо підозрюєте виникнення проблем з припиненням вживання алкоголю. Він може направити Вас до спеціальних служб, створених задля допомоги в припиненні споживання алкоголю.
Відмова від куріння. Якщо Ви курите, Ви також маєте відмовитись від вживання тютюну. При тому, що куріння не спричиняє хронічного запалення ПЗ, воно може пришвидшити його прогрес, що, ймовірно, може призвести до втрати функцій ПЗ. Ваш лікар зможе направити Вас до служб, які допомагають кинути курити.
Зміни харчування. Можливо, Вам знадобиться змінити харчування. Для більшості хворих на хронічне запалення ПЗ рекомендована дієта з низьким вмістом жирів та споживання їжі шістьма невеликими прийомами на день замість трьох великих. Ваш лікар надасть відповідні рекомендації щодо харчування або направить до дієтолога, який складе для Вас відповідну схему харчування.
Можливо, Вам призначать лікарські засоби, які містять штучні ензими ПЗ, з метою поліпшення ефективності роботи травної системи, полегшення симптомів здуття та кольок у животі, а також зменшення жирності та відразливого запаху випорожнень.
Полегшення болю. Полегшення болю є важливою частиною лікування хронічного запалення ПЗ, оскільки хронічний біль може спричиняти психологічний вплив, такий як депресія.
Рекомендується поступове зменшення болю під контролем Вашого лікуючого лікаря. Безрецептурні знеболювальні (OTC) можуть бути ефективними при болю від слабкого до помірного. Сильніший біль може вимагати призначення знеболювальних на основі опіатів. Існує ризик розвитку залежності від більш сильних знеболювальних на основі опіатів. Для зменшення ризику використовуйте знеболювальні тільки відповідно інструкції та призначень лікаря.
Інсулін. Якщо ПЗ пошкоджена настільки, що не виробляє інсулін в достатній кількості, розвивається панкреатогенний діабет. Це означає, що Вам необхідно буде регулярне застосування інсуліну впродовж всього життя для утримання рівня цукру в крові в нормі. Інсулін призначається у формі ін’єкцій. Інсулін в таблетках зазвичай не рекомендується через можливу нездатність травної системи розщеплювати таблетки та вивільняти інсулін.
Хірургія. Якщо у Вас сильний хронічний біль, що не відповідає на знеболювальні, може знадобитися хірургічне втручання. Ймовірно, сильний хронічний біль може виникати з двох причин:
— протоки ПЗ можуть заблокуватись в результаті накопичення кальцію в пошкоджених тканинах, що спричиняє накопичення травного соку, призводить до збільшення тиску в протоках і болю;
— основна частина ПЗ, яка називається голівкою, може бути запаленою, що призводить до подразнення головного нервового закінчення.
Ендоскопічна хірургія. При хронічному запаленні ПЗ, коли протоки заблоковані, може бути можливим зменшити тиск на протоки за допомогою їх дилатації чи стентування. Цю процедуру виконують за допомогою ендоскопа, який вводиться до травної системи під рентгенологічним контролем.
Хірургічне лікування ХП. При запаленні голівки ПЗ, ймовірно, відбувається подразнення нервових закінчень, і голівка ПЗ може бути видалена хірургічним шляхом — резекцією ПЗ. Видалення голівки ПЗ також може знизити тиск на протоки. Видалення ПЗ застосовують у випадку неефективності ендоскопічного втручання. Перевагою видалення лише голівки ПЗ є те, що решта залози часто зберігає свої функції вироблення інсуліну та травних соків.
Існує кілька різних технік для проведення резекції ПЗ. Найбільш широко виконуються такі:
— Операція Beger — застосовується для лікування запалення голівки ПЗ. Запалена тканина видаляється, а решта ПЗ приєднується до кишківника.
— Операція Frey — застосовується, коли виявлено блокування протоків та запалення ПЗ. Запалену частину голівки видаляють, а протоки приєднують прямо до кишківника.
— Пілорозберігаюча панкреатодуоденальна резекція (ПЗПДР) — застосовується для лікування найтяжчих випадків хронічного болю. Під час ПЗПДР голівка ПЗ видаляється разом з жовчним міхуром та жовчними протоками, решта ПЗ приєднується до шлунка.
Результати резекції ПЗ. Кожний тип хірургічного втручання має свої переваги та недоліки. ПЗПДР є найбільш ефективною технікою відносно зменшення болю та зберігання функцій ПЗ, але має вищий ризик ускладнень, таких як інфекція та внутрішня кровотеча.
Операції Beger та Frey несуть менший ризик ускладнень та потребують менше часу на відновлення, при цьому вони не такі ефективні щодо довготривалого полегшення болю та зберігання функцій ПЗ.
Перед прийняттям рішення щодо хірургічного втручання Вам слід обговорити всі «за» та «проти» кожної техніки з Вашим лікарем.
Загальна панкреатектомія. У самих тяжких випадках ХП, коли ПЗ значно ушкоджена, може стати необхідним видалення всієї ПЗ, повна панкреатектомія. Вона може бути дуже ефективною при лікуванні симптомів болю, але веде до неможливості ПЗ виробляти інсулін. Аутологічна трансплантація панкреатичних острівців (АТПО) є порівнювано новою технікою в спробах подолати цей недолік.
Ускладнення. Будь-яке хронічне порушення стану здоров’я, що повторюється чи завдає постійного болю, таке як ХП, може мати небажаний вплив на Ваш емоційний та психологічний стан.
Спілкуйтеся зі своїм лікарем, якщо у Вас виникають психологічні або емоційні труднощі. Існують ефективні засоби для полегшення симптомів стресу, страху або депресії. Також може допомогти приєднання до групи хворих на ХП, оскільки спілкування з людьми, які мають таке ж захворювання, часто допомагає зменшити відчуття ізольованості та стресу.
Псевдокіста. Псевдокіста є зібранням рідини, що формується всередині або навколо ПЗ. Зазвичай вона розвивається внаслідок протікання травного соку через пошкоджені протоки ПЗ. У 70 % випадків псевдокісти не спричиняють симптомів та не потребують лікування. У решті 30 % випадків псевдокіста може інфікуватися, може розірватися, що призводить до внутрішньої кровотечі, блокування частини кишківника. Якщо ускладнення дійсно розвивається, може знадобитися хірургічне втручання для дренування кісти.
Рак ПЗ. Хронічне запалення ПЗ підвищує ризик розвитку раку ПЗ. Однак підвищення ризику порівняно невелике. Наприклад, встановлено, що на кожних 500 хворих на ХП тільки в одного розвивається рак ПЗ.
Попередження
Алкоголь. Якщо раніше у Вас були напади гострого запалення ПЗ, спричинені зловживанням алкоголю, слід повністю відмовитись від вживання алкоголю. Це зменшить ризик наступних випадків гострого панкреатиту та розвитку хронічного запалення ПЗ. Важливо обмежити вживання алкоголю навіть при відсутності гострого запалення ПЗ, оскільки це допомагає захистити ПЗ від ураження та знизити ймовірність розвитку інших серйозних захворювань, таких як рак печінки.
Чоловік не повинен споживати більше 3–4 порцій алкоголю на день, а жінка не повинна споживати більше 2–3 порцій алкоголю на день. Порція алкоголю еквівалента половині пінти світлого пива нормальної міцності, маленькому бокалу вина або 25 мл спирту.
Коментар робочої групи
Одна пінта пива складає 0,57 л.
При хронічному панкреатиті обов’язковою є відмова від вживання алкоголю.
Список джерел
1. PRODIGY. Pancreatitis — chronic. December 2010.
2. The Spanish Pancreatic Club recommendations for the diagnosis and treatment of chronic pancreatitis: Part 1 (diagnosis). February 2013.
3. The Spanish Pancreatic Club recommendations for the diagnosis and treatment of chronic pancreatitis: Part 2 (treatment). February 2013.
4. Italian consensus guidelines for chronic pancreatitis. November 2010.
1. Clinical Pancreatology for practicing gastroenterologists and surgeons / Ed. J.E. Dominguez-Munoz. — A Blackwell Publishing Company, 2005. — 535 р.
2. Гастроентерологія / Під редакцією Харченко Н.В., Бабак О.Я. — К., 2007. — 720 с.
3. Хронический билиарнозависимый панкреатит: Учебн.-метод. пособие / Авт.: А.Н. Казюлин, Ю.А. Кучерявый / Под ред. И.В. Маева / МЗ РФ. — М.: ГОУ ВУНМЦ МЗиСР РФ, 2005. — 72 с.
4. Губергриц Н.Б. Клиническая панкреатология / Н.Б. Губергриц, Т.Н. Христич. — Донецк: Лебедь, 2000. — 416 с.
5. Губергриц Н.Б. Метаболическая панкреатология / Н.Б. Губергриц, А.Н. Казюлин. — Донецк: Лебедь, 2011. — 464 с.
6. Губергріц Н.Б. Практична панкреатологія / Н.Б. Губергріц, С.В. Скопиченко. — Донецьк: Лебідь, 2007. — 244 с.
7. Современные подходы к диетическому питанию больных хроническим панкреатитом / Н.В. Харченко, Г.А. Анохина, И.А. Коруля, В.В. Харченко // Здоров’я України. — 2011. — Листоп. 4. — С. 17–18.
8. Chronic pancreatitis: novel concepts in biology therapy / Eds.: M.W. Buchler, H. Friess, W. Uhl, P. Malfertheiner. — Oxford [et al.]: Blackwell Science, 2002. — 614 p.
9. Diseases of the pancreas / M.W. Buchler, W. Uhl, P. Malfertheiner, M.G. Sarr. — Basel: Karger A.G., 2004. — 212 p.
10. Layer P. Lipase supplementation therapy: standards, alternatives, and perspectives / P. Layer, J. Keller // Pancreas. — 2003. — Vol. 26, № 1. — P. 1–7.
11. Löhr J.-M. Exocrine pancreatic insufficiency / J.-M. Löhr. — Bremen: UNI-MED, 2010. — 91 p.
12. Treatment for painful calcified chronic pancreatitis: extracorporeal shock wave lithotripsy versus endoscopic treatment: a randomised controlled trial / J.M. Dumonceau, G. Costamagna, A. Tringali [et al.] // Gut. — 2007. — Vol. 56. — P. 545–552.
13. The Pancreas: An integrated textbook of basic science, medicine, and surgery / H.G. Beger, A.L. Warshaw, M.W. Büchler [et al.]. — 2-nd ed. — [Massachusetts, USA et al.]: Blackwell Publ., [2008]. — 1006 p.).