Газета «Новости медицины и фармации» Гастроэнтерология (521) 2014 (тематический номер)
Вернуться к номеру
Вірусний гепатит С Aдаптована клінічна настанова, заснована на доказах
Рубрики: Гастроэнтерология
Разделы: Официальная информация
Версия для печати
Статья опубликована на с. 93-123
ДОДАТОК
до наказу Міністерства охорони здоров’я України
02.04.2014 № 233
Cклад робочої групи з опрацювання клінічної настанови
Голубовська Ольга Анатоліївна — завідувач кафедри інфекційних хвороб НМУ імені О.О. Богомольця, д.мед.н., професор, головний позаштатний спеціаліст МОЗ України зі спеціальності «Інфекційні хвороби»;
Ліщишина Олена Михайлівна — директор Департаменту стандартизації медичних послуг ДП «Державний експертний центр МОЗ України», к.мед.н.;
Андрейчин Михайло Антонович — завідувач кафедри інфекційних хвороб з епідеміологією, шкірними та венеричними хворобами Тернопільського державного медичного університету імені І.Я. Горбачевського, президент асоціації інфекціоністів України;
Боднарук Наталія Миколаївна — заступник начальника управління спеціалізованої медичної допомоги — начальник відділу спеціалізованої медичної допомоги Департаменту реформ та розвитку медичної допомоги МОЗ України;
Бреднева Лариса Юріївна — лікар-інфекціоніст Комунальної установи «Центральна міська лікарня № 1» м. Житомира, обласний позаштатний інфекціоніст Департаменту охорони здоров’я Житомирської ОДА (за згодою);
Гаврилова Ольга Валеріївна — представник пацієнтської організації ВГО «Зупинимо гепатит» (за згодою);
Герасун Борис Абрамович — професор кафедри інфекційних хвороб та епідеміології Львівського державного медичного університету імені Данила Галицького, д.мед.н.;
Дубинська Галина Михайлівна — завідувач кафедри інфекційних хвороб з епідеміологією ВДНЗ України «Українська медична стоматологічна академія»;
Козько Володимир Миколайович — завідувач кафедри інфекційних хвороб Харківського національного медичного університету;
Коваль Дмитро Михайлович — представник пацієнтської організації ВГО «Зупинимо гепатит» (за згодою);
Курпіта Володимир Іванович — виконавчий директор ВБО «Всеукраїнська мережа ЛЖВ» (за згодою);
Лєженцев Костянтин Юрійович — представник пацієнтської організації, член БФ «Дорадча рада спільнот з питань доступу до лікування в Україні»;
Матюха Лариса Федорівна — завідувач кафедри сімейної медицини НМАПО імені П.Л. Шупика, д.мед.н., головний позаштатний спеціаліст МОЗ України зі спеціальності «Загальна практика — сімейна медицина»;
Мороз Лариса Василівна — завідувач кафедри інфекційних хвороб Вінницького Національного медичного університету імені М.І. Пирогова, д.мед.н., професор;
Мостовенко Раїса Василівна — завідувач дитячого інфекційного відділення Національної дитячої спеціалізованої лікарні «ОХМАТДИТ», головний позаштатний спеціаліст МОЗ України зі спеціальності «Педіатрія»;
Нетяженко Василь Захарович — завідувач кафедри пропедевтики внутрішньої медицини № 1 НМУ імені О.О. Богомольця, д.мед.н., професор, головний позаштатний спеціаліст МОЗ України зі спеціальності «Терапія»;
Пришляк Олександра Ярославівна — професор кафедри інфекційних хвороб та епідеміології Івано-Франківського національного медичного університету, д.мед.н.;
Рябоконь Олена В’ячеславівна — завідувач кафедри інфекційних хвороб з епідеміологією Запорізького державного медичного університету;
Сергеєва Тетяна Анатоліївна — провідний науковий співробітник лабораторії епідеміології, парентеральних вірусних гепатитів та ВІЛ-інфекції ДУ «Інститут епідеміології та інфекційних хвороб імені Л.В. Громашевського», д.мед.н.;
Федорченко Сергій Валерійович — завідувач відділу ВІЛ-інфекції та вірусних гепатитів ДУ «Інститут епідеміології та інфекційних хвороб імені Л.В. Громашевського» (за згодою);
Хаджинова Наталія Афанасіївна — начальник відділу санаторно-курортного лікування Управління охорони материнства, дитинства та санаторного забезпечення Департаменту реформ та розвитку медичної допомоги МОЗ України;
Харченко Наталія В’ячеславівна — завідувач кафедри гастроентерології і дієтології, декан терапевтичного факультету НМАПО імені П.Л. Шупика, член-кореспондент НАМН України, д.мед.н., професор, головний позаштатний спеціаліст МОЗ України зі спеціальності «Гастроентерологія»;
Шкурба Андрій Вікторович — професор кафедри інфекційних хвороб Національного медичного університету імені О.О. Богомольця;
Бацюра Ганна Володимирівна — асистент кафедри сімейної медицини та амбулаторно-поліклінічної допомоги імені П.Л. Шупика;
Бойко Валентина Олександрівна — асистент кафедри інфекційних хвороб НМАПО імені П.Л. Шупика;
Савенко Оксана Юріївна — менеджер програми лікування, МБФ «Міжнародний альянс з ВІЛ/СНІД в Україні»;
Демчишина Ірина Вікторівна — зав. лабораторією вірусології та СНІД, референс-лабораторії МОЗ із діагностики грипу та ГРВІ Центральної СЕС МОЗ України;
Стефанишина Ольга Анатоліївна — благодійний фонд «Дорадча рада спільнот із питань доступу до лікування в Україні»;
Кулєш Олена Валеріївна — асистент кафедри інфекційних хвороб Національного медичного університету імені О.О. Богомольця;
Метелюк Анна Сергіївна — фахівець програм лікування МБФ «Міжнародний Альянс з ВІЛ/СНІД в Україні».
Методичний супровід та інформаційне забезпечення
Горох Є.Л. — начальник відділу якості медичної допомоги та інформаційних технологій Державного підприємства «Державний експертний центр Міністерства охорони здоров’я України», к.т.н.;
Мельник Є.О. — начальник відділу доказової медицини Державного підприємства «Державний експертний центр Міністерства охорони здоров’я України»;
Шилкіна О.О. — начальник відділу методичного забезпечення новітніх технологій у сфері здоров’я Державного підприємства «Державний експертний центр Міністерства охорони здоров’я України»;
Мігель О.В. — завідувач сектору економічної оцінки Департаменту стандартизації медичних послуг Державного підприємства «Державний експертний центр Міністерства охорони здоров’я України».
Державний експертний центр МОЗ України є членом
Guidelines International Network
(Міжнародна мережа настанов)
ADAPTE (Франція)
(Міжнародний проект з адаптації клінічних настанов)
Рецензенти адаптованої клінічної настанови, заснованої на доказах, «Вірусний гепатит С»
Зайцев Ігор Анатолійович — завідувач кафедри інфекційних хвороб та епідеміології Донецького національного медичного університету імені М. Горького, д.мед.н., професор;
Дикий Богдан Миколайович — професор кафедри інфекційних хвороб із курсом епідеміології Івано-Франківського національного медичного університету, д.мед.н., заслужений діяч науки і техніки України.
Шкала доказів і градація рекомендацій
Рівні доведеності первинних даних
|
1++ |
Високоякісні метааналізи, систематичні огляди рандомізованих контрольованих досліджень (РКД) або РКД із дуже низьким ризиком систематичної помилки |
|
1+ |
Належним чином проведені метааналізи, систематичні огляди РКД або РКД з низьким ризиком систематичної помилки |
|
1– |
Метааналізи, систематичні огляди РКД або РКД з високим ризиком систематичної помилки |
|
2++ |
Високоякісні систематичні огляди досліджень «випадок-контроль» або когортних досліджень |
|
|
Високоякісні дослідження «випадок-контроль» або когортні дослідження з дуже низьким ризиком похибки, систематичних помилок або відхилень і високою вірогідністю причинного зв’язку |
|
2+ |
Належним чином проведені дослідження «випадок–контроль» або когортні дослідження з низьким ризиком похибки, систематичних помилок або відхилень і помірною вірогідністю причинного зв’язку |
|
2– |
Дослідження «випадок-контроль» або когортні дослідження з високим ризиком похибки, систематичних помилок або відхилень і значним ризиком того, що цей зв’язок не є причинним |
|
3 |
Неаналітичні дослідження, наприклад повідомлення про випадки, серії випадків |
|
4 |
Думка експерта |
Градація рекомендацій
Примітка. Рівні доказів рекомендацій пов’язані з силою доказів, на яких вони засновані. Вони не відображають клінічне значення рекомендацій.
|
А |
Принаймні один метааналіз, систематичний огляд або РКД, оцінені як 1++ і безпосередньо застосовні до цільової популяції, або |
|
В |
Сукупність доказів, що складаються в основному з досліджень, оцінених як 1+ і безпосередньо застосовних до цільової популяції, які мають узгоджувані результати Сукупність доказів, включаючи дослідження 2++, безпосередньо застосовні до цільової популяції, мають узгоджувані результати Екстрапольовані докази з досліджень 1++ або 1+ |
|
С |
Сукупності доказів, включаючи дослідження, застосовні до цільової популяції, які мають узгоджувані результати Екстрапольовані докази з досліджень, які оцінюються як 2++ |
|
D |
Докази рівня 3, або 4, або Екстрапольовані докази з досліджень 2+ |
Положення належної практики
- Рекомендована належна практика, заснована на клінічному досвіді групи з розробки настанови
Коментар робочої групи:
Актуальність для України
Вірусні гепатити з парентеральним механізмом передачі збудників, одним з яких є гепатит С, є важливою проблемою сучасної медичної науки і практичної охорони здоров`я усіх країн світу. Це обумовлено широким розповсюдженням, високим рівнем захворюваності, вираженим поліморфізмом клінічних проявів, численністю шляхів та факторів передачі збудника, а також надзвичайно несприятливими наслідками, до яких може призвести гепатит, — формуванням усього спектра хронічних уражень печінки, в тому числі цирозу і гепатоцелюлярної карциноми. В останні роки помітна тенденція до збільшення випадків хронічних форм захворювання. За оцінками експертів ВООЗ, від хронічного гепатиту С страждає біля 150 млн осіб, а 350 тис. щорічно помирає внаслідок ураження печінки вірусом гепатиту С. Захворюваність та летальність внаслідок гепатиту С прогресивно збільшується на планеті та, за даними експертів, подвоїться до 2015–2020 рр. Вже зараз загальна кількість хворих на гепатити у світі в 14–15 разів перевищує кількість ВІЛ-інфікованих. Вірусні гепатити у 50–100 разів є більш заразними, ніж ВІЛ.
За оціночними даними ВООЗ, 57 % випадків цирозу печінки і 78 % випадків первинного раку печінки зумовлено впливом вірусів гепатиту В або С. Окрім цього, гепатит С має багато позапечінкових проявів, що ускладнює їх діагностику та може перешкоджати призначенню відповідного лікування.
За ступенем негативного впливу на здоров’я населення та масштабами захворюваності вірусні гепатити в Україні займають домінуюче місце в структурі інфекційної патології разом із грипом та гострими інфекційними захворюваннями верхніх дихальних шляхів.
Україна належить до країн із середнім рівнем поширення вірусного гепатиту С — інфіковано приблизно 3 % громадян, що складає ~ 1 170 000 осіб. Однак, за результатами вибіркового моніторингу груп ризику, рівень інфікування вірусом гепатиту С серед деяких з них значно перевищує середньосвітові показники і сягає 40–60 %.
Разом з цим слід зазначити, що на теперішній час досягнуто значний прогрес у лікуванні гепатиту С, зараз його можна вважати виліковним захворюванням. Окрім цього, наукові дослідження в цьому напрямку продовжуються та нові препарати здатні значно підвищити ефективність лікування. Велике значення у досягненні основної мети терапії — стійкої вірусологічної відповіді — має своєчасне виявлення хвороби, визначення її стадії та призначення оптимальної схеми лікування. Оскільки вірусний гепатит С є мультидисциплінарною проблемою, дуже важливо адаптувати найкращі клінічні настанови, що використовуються в світі, до реальної медичної практики України задля підвищення якості надання допомоги таким хворим.
Синтез настанови
За прототип Адаптованої клінічної настанови «Вірусний гепатит С» взято Клінічну настанову «SIGN 133 — Management of hepatitis C. A national clinical guideline» (2013) — http://www.sign.ac.uk/pdf/sign133.pdf
Додаткові докази включені з джерел:
1. An Update on Treatment of Genotype 1 Chronic Hepatitis C Virus Infection: 2011 Practice Guideline by the American Association for the Study of Liver Diseases (AASLD).
2. AASLD Practice Guideline. Management of Hepatocellular Carcinoma: An Update (2011).
3. An update on the management of chronic hepatitis C: Consensus guidelines from the Canadian Association for the Study of the Liver (2012).
4. EASL Clinical Practice Guidelines: Management of hepatitis C virus infection (2011).
І. Вступ
1.1. Необхідність розробки клінічної настанови
Вірус гепатиту C (ВГС) було вперше виявлено у 19891 році, а ВГС інфекція стала значною проблемою у всьому світі. Вважається, що приблизно 0,8 % населення Шотландії мають хронічну інфекцію ВГС (близько 37 500 осіб). Поширеність інфекції варіюється між групами населення і може досягати від 50 % серед споживачів ін’єкційних наркотиків (СІН) до менше ніж 0,04 % серед нових донорів крові.1
До 80 % пацієнтів, які інфіковані ВГС, стають хронічно хворими, і в більшості з таких пацієнтів проявляються ознаки хронічного гепатиту.2
Гепатит C зазвичай прогресує дуже повільно. Цей процес займає багато років. Серед 5–15 % пацієнтів із хронічним гепатитом може розвинутися цироз печінки через 20 років.3 Серед 4–9 % пацієнтів із цирозом розвивається печінкова недостатність, а серед 2–5 % пацієнтів із цирозом розвивається первинна гепатоцелюлярна карцинома.
Двома основними шляхами передачі ВГС у Сполученому Королівстві є спільне використання засобів для ін’єкцій серед СІН та переливання інфікованої крові або продуктів крові. Обробка продуктів крові для інактивації вірусу почалася у 1987 році, а з 1991 року проводиться скринінг крові на гепатит С, що виключає продукти крові з переліку джерела інфікування ВГС.
Коментар робочої групи:
Підходи стосовно адаптації надання медичної допомоги хворим на вірусний гепатит С потребують приведення у відповідність до доказів найкращої практики.
ВГС можна ефективно лікувати, використовуючи терапію комбінованими препаратами (пегільованим а-інтерфероном та рибавірином) зі стійкими показниками вірусологічної відповіді у 50–80 % пацієнтів. І хоча існують клінічні настанови щодо відбору пацієнтів до лікування,4–7 досі не існує національних клінічних настанов щодо скринінгу, тестування, діагностування, конфігурування послуг, надання допомоги протягом лікування чи контролю після лікування для дітей та дорослих. На даний час по всій Шотландії існують різноманітні розбіжності у наданні послуг особам, які інфіковані ВГС.
Коментар робочої групи:
В Україні адаптована клінічна настанова «Вірусний гепатит С», заснована на доказах, є першим документом, в якому наведені докази щодо необхідного обсягу діагностичних обстежень та строків їх виконання; лікарських засобів, що зарекомендували свою ефективність у лікуванні ВГС, та схеми їхнього призначення; очікуваних побічних дій противірусного лікування та поради щодо їхньої корекції.
1.1.1. Оновлення доказів
Ця настанова оновлює настанову SIGN 92 «Лікування гепатиту С», аби відобразити останні дані з лікування інгібіторами протеази в якості доповнення до поточної стандартної подвійної терапії.
Це оновлення було обмежене за своїми масштабами і стосується лікування хронічного гепатиту С (ХГС), надання інформації для пацієнтів і доглядачів і декілька інших незначних оновлень (див. розділ 1.2.3 і Додаток 1). У розділах неоновлений текст і рекомендації дослівно повторюють настанову SIGN 92. Оригінальні підтверджуючі докази не були повторно оцінені поточною групою в індивідуальному порядку.
1.2. Сфера компетенції клінічної настанови
1.2.1. Загальні цілі
Клінічна настанова надає рекомендації на основі доказів, що охоплюють усі етапи надання допомоги пацієнту; скринінгу, тестування, діагностування, направлення, лікування, надання допомоги та контроль для немовлят, дітей та дорослих, які інфіковані або піддаються впливу інфекції ВГС. Сфера компетенції включає запобігання вторинної трансмісії вірусу, але при цьому виключає первинне запобігання інфікуванню на ВГС. Первинне запобігання інфекції гепатиту С є важливим питанням громадського здоров’я, але складною темою для того, щоб охопити її в рамках доказової КН. Принципи і докази запобігання розповсюдженню вірусів, що передаються через кров, нічим особливим не виділяються, а перегляд всіх доказів виходить за межі роботи будь-якої групи з розробки КН; водночас розгляд доказів лише по ВГС міг би справити порушене бачення цього питання.
1.2.2. Цільові користувачі настанови
Дана КН зацікавить професіоналів сфери охорони здоров’я первинної та вторинної ланки надання допомоги, що залучаються до ведення пацієнтів, які інфіковані вірусом гепатиту С.
1.2.3. Резюме оновлень настанови по розділах
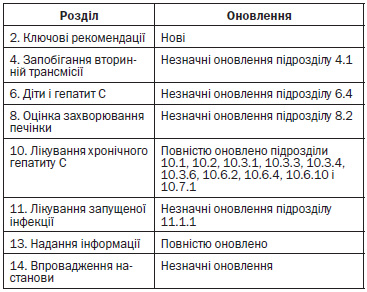
1.3. Заява про наміри
Даний посібник не призначений для сприйняття в якості стандарту лікування. Стандарти надання допомоги визначаються на основі всіх клінічних даних, доступних для конкретного випадку, і можуть бути змінені відповідно до наукових знань, технологічних досягнень та розвитку моделей надання допомоги. Дотримання настанов не забезпечить успішний результат у кожному випадку; не треба сприймати їх такими, що включають всі належні методи надання допомоги або виключають інші прийнятні методи лікування, що спрямовані на ті ж результати. Остаточне рішення має бути прийняте відповідним лікарем, який відповідає за клінічні рішення щодо конкретної клінічної процедури або плану лікування. Це рішення має бути прийняте тільки після відповідного обговорення варіантів з пацієнтом, що включає можливість вибору методів діагностики та лікування. Водночас радимо, щоб істотні посилання у національних чи будь-яких місцевих КН на основі даного документу були повністю задокументовані у історії пацієнта перед прийняттям адекватного рішення.
1.3.1. Призначення ліцензованих ліків за межами їх реєстраційного свідоцтва
Рекомендації даної настанови засновані на кращих клінічних доказах. Деякі рекомендації можуть стосуватися ліків за рецептами за межами їх реєстраційного свідоцтва, також відомого як ліцензія на продукт. Це відомо як використання за «незареєстрованими показаннями».
Лікарські засоби можуть бути призначені за «незареєстрованими показаннями» в наступних випадках:
— за показаннями, не зазначеними у торговій ліцензії;
— для введення іншим шляхом;
— для введення інших доз;
— для інших пацієнтів.
Неліцензовані препарати — це препарати, які не мають реєстраційного свідоцтва для медичного застосування в людей.
Загалом використання ліків за «незареєстрованими показаннями» стає необхідним, якщо клінічна потреба не може бути задоволена ліцензованими лікарськими препаратами відповідно до реєстраційного свідоцтва. Таке використання повинно бути підтверджене відповідними доказами та досвідом.8
«Призначення препаратів поза умовами їх дозволу на продаж змінює (і, ймовірно, збільшує) професійну відповідальність тих, хто їх призначає».8
Генеральна медична рада (GMC) рекомендує, що при призначенні препаратів не за прямим показанням лікарі повинні:
— бути впевненими, що таке використання краще послужить потребам пацієнта, ніж офіційно затверджені альтернативи (якщо такі існують);
— бути впевненими, що є достатньо доказів/досвіду використання ліків, що свідчать про їх безпеку та ефективність, при пошуку необхідної інформації з відповідних джерел;
— записати в медичних картках пацієнта призначені препарати і, якщо лікар не слідує загальноприйнятій практиці, причини такого вибору;
— взяти на себе відповідальність за призначення препаратів та догляд за пацієнтом, у тому числі моніторинг наслідків препаратів.
Немедичні консультанти повинні переконатися, що вони знайомі із законодавчою базою і своїми професійними нормативними стандартами.
Перед будь-яким призначенням необхідно перевірити статус ліцензування ліків у поточній версії Британського національного формуляра (BNF).8 Особа, яка призначає препарат, повинна бути компетентною, діяти в рамках професійної етики і практики призначення свого роботодавця.9
1.3.2. Додаткові поради для NHS Шотландії від Healthcare Improvement Scotland і Шотландського консорціуму лікарських засобів
Healthcare Improvement Scotland здійснює багатофункціональні оцінки технологій для NHSScotland, які були підготовлені Національним інститутом досконалості медичної допомоги (NICE) в Англії та Уельсі.
Шотландський консорціум лікарських засобів (ШКЛЗ) консультує NHS та його комітети з лікарських засобів та терапії про статус всіх нових зареєстрованих препаратів і будь-які серйозні зміни у показаннях для вже зареєстрованих препаратів.
Рекомендації ШКЛЗ щодо даної настанови наводяться у розділі 14.
Коментар робочої групи:
В Україні застосування лікарських засобів регламентоване ст. 7 Закону України «Про лікарські засоби», ст. 4 Закону України «Про захист прав споживачів», наказом МОЗ України № 651 від 26.07.2013 р. Відповідно до законодавчої бази лікарський засіб слід застосовувати відповідно до інструкції.
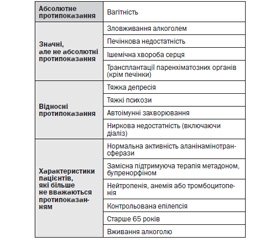
ІІ. Ключові рекомендації
Наступні рекомендації були виділені групою з розробки настанови в якості ключових клінічних рекомендацій, які повинні бути пріоритетними для реалізації. Градація рекомендацій відноситься до сили доказів, на яких рекомендація заснована. Вона не відображає клінічної важливості рекомендації.
2.1. Лікування хронічного гепатиту С
|
A |
Усіх нелікованих пацієнтів, інфікованих ВГС генотипу 1, необхідно розглядати як кандидатів на отримання лікування пегільованим ІФН і рибавірином з урахуванням маси з додаванням інгібітора протеази в якості потрійної терапії. |
|
A |
Усіх раніше лікованих пацієнтів, інфікованих ВГС генотипу 1, необхідно розглядати як кандидатів на лікування пегільованим ІФН і рибавірином з урахуванням маси з додаванням інгібітору протеази в якості потрійний терапії. |
|
В |
Неліковані пацієнти з ко-інфекцією ВІЛ і ВГС генотипу 1, яким не підходить лікування за схемою, яка включає інгібітори протеази ВГС, повинні бути розглянуті як кандидати на лікування пегільованим ІФН і рибавірином з урахуванням маси впродовж 48–72 тижнів залежно від вірусологічної відповіді. |
Коментар робочої групи:
У даній настанові словосполучення «з урахуванням маси тіла» стосується виключно рибавірину.
Можливість використовувати інгібітори протеази з пегільованим ІФН і рибавірином у потрійній терапії, що з’явилася нещодавно, значно поліпшила СВВ у пацієнтів з ВГС генотипу 1 з перспективою зниження загальної тривалості лікування залежно від відповіді на терапію. Пацієнти, інфіковані ВГС генотипу 2 і 3, продовжують досягати високої СВВ з подвійною терапією пегільованим ІФН і рибавірином. Це комбіноване лікування повинно бути обговорене й запропоноване в якості стандарту лікування для всіх відповідних пацієнтів із ВГС.
An update on the management of chronic hepatitis C: Consensus guidelines from the Canadian Association for the Study of the Liver (2012)
Рекомендації:
Всіх пацієнтів із хронічним вірусним гепатитом С слід розглядати для противірусної терапії, особливо пацієнтів з ознаками фіброзу печінки (клас 1, рівень А).
Пацієнти з позапечінковими проявами інфекції ВГС повинні бути розглянуті для противірусної терапії (клас 1, рівень В).
Постійно нормальний рівень активності АЛТ не виключає ні значного захворювання печінки, ні необхідності противірусної терапії (клас 1, рівень А).
EASL Clinical Practice Guidelines: Management of hepatitis C virus infection (2011)
Все не получавшие лечения пациенты с компенсированным заболеванием печени вследствие ВГС подлежат терапии (A2).
Лечение следует начинать немедленно при тяжелом фиброзе (F3-F4 по шкале METAVIR). Настоятельно рекомендуется назначение лечения у пациентов с умеренным фиброзом (F2 по шкале METAVIR) (B2).
У пациентов с менее тяжелым поражением печени показания к терапии являются индивидуальными (C2).
2.2. Діти і гепатит С
|
А |
Дітей, інфікованих всіма генотипами вірусу гепатиту С з ознаками помірного або важкого захворювання печінки, слід розглядати для лікування пегільованим ІФН і рибавірином. |
|
В |
Дітей, інфікованих генотипом 2 і 3 ВГС, слід розглядати для лікування пегільованим ІФН і рибавірином незалежно від стадії захворювання. |
|
С |
У дітей з легкою формою захворювання та інфекцією інших генотипів переваги лікування повинні бути збалансовані з ризиками побічних ефектів. |
У дітей результат лікування пегільованим ІФН і рибавірином рівнозначний тому, що спостерігається у дорослих.10 Побічні ефекти лікування спостерігаються з однаковою частотою, а щотижневі ін’єкції спричиняють незручності. Переваги досягнення СВВ у ранньому віці, усуваючи ризик подальшої передачі (особливо до досягнення дівчатами віку дітонародження) і до настання хронічного захворювання печінки, переважать ці недоліки в багатьох дітей, інфікованих сприятливими генотипами. Тим не менше, для тих, хто має менш сприятливі генотипи і не має ознак хронічного захворювання печінки, доцільно почекати, поки більш ефективне і прийнятне лікування не стане доступним.
2.3. Тестування
|
D |
Тестування методом сухої краплі крові слід розглядати як зручний і економічно ефективний спосіб доступу до деяких цільових груп населення. |
|
D |
Необхідно приділяти увагу методам підвищення обізнаності та виділення важливої інформації щодо гепатиту С серед груп ризику та широкої громадськості. Рекомендується направлення пропаганди на конкретну аудиторію. Співробітники повинні мати доступ до відповідної підготовки. |
|
D |
Кожному, хто має негативний тест, але залишається з ризиком зараження, мають бути запропоновані подальші тестування на щорічній основі. |
|
D |
Тестування на ВГС має бути запропоноване мігрантам з країн із середнім або високим рівнем поширеності ВГС. |
Настанова NICE «Hepatitis B and C: Ways to promote and offer testing to people at increased risk of infection»11 містить ряд ключових рекомендацій з тестування. Хоча вона призначена для служб NHS в Англії та Уельсі, вона має пряме застосування до тестування на ВГС в Шотландії.
ІІІ. Тестування
3.1. Клінічні та економічно ефективні тестування на ВГС
|
Національні та міжнародні КН рекомендують особам, які мають підвищений ризик інфікування і можуть отримати вигоду від знання ВГС статусу, запропонувати тестування на ВГС. Така рекомендація базується в основному на необхідності діагностування прихованої інфекції, що дозволяє розпочати швидке противірусне лікування, якщо це необхідно.15 Оскільки лікування не може бути запропоноване до встановлення діагнозу хронічного ВГС, інформування населення з ризиком інфікування ВГС щодо необхідності тестування має клінічні переваги. |
4 |
Подальші переваги у діагностуванні осіб, які інфіковані ВГС, включають можливість інформування з метою зниження швидкості прогресування ВГС (напр., поради щодо небезпеки надмірного споживання алкоголю) та зниження шансів передачі інфекції іншим особам. Надійних і переконливих доказів, що вказують на ефективність таких втручань, виявлено не було.
|
Керівні документи Сполученого Королівства наполегливо рекомендують особам, які можуть мати ризик передачі ВГС пацієнтам у закладах охорони здоров’я, проходити тестування на ВГС.5, 12–14 Було зареєстровано кілька випадків передачі ВГС від медпрацівника до пацієнта і від донора крові/органа до реципієнта.16, 17 |
4 |
|
Контрольовані дослідження або когортні дослідження для оцінки економічної ефективності ВГС тестування в різних групах населення не проводилися. Обмежені дані з робіт економічного моделювання вказують, що пропонування тестів на ВГС колишнім СІН на лікуванні та, можливо, у інших закладах матиме економічно ефективні клінічні переваги.18 Рівень поширеності ВГС та прихильності до лікування вище серед колишніх СІН порівняно з дійсними СІН. Моделі кращих практик для виявлення й тестування колишніх СІН не розроблялися і не оцінювалися. Експертна думка зазначає, що загальні практики, а особливо ті, що застосовуються при високих рівнях поширеності споживання наркотиків, можуть складати умови, де сфокусовані, добре підтримані ініціативи з тестування можуть мати успіх. Тюрми також можуть мати такі можливості.19 Проводилися цільові та генералізовані кампанії з інформування/тестування, але не проводилася оцінка їх успішності з підтримки людей (включаючи колишніх СІН), що мають високий ризик ВГС, для надання їм допомоги. |
4 |
|
|
|
|
Серед населення, яке має низький рівень поширеності ВГС (напр., відвідувачі гінекологічних, урологічних та венерологічних клінік), економічне моделювання вказує, що універсальне тестування не несе в собі економічно ефективної користі.18 |
4 |
|
На ВГС необхідно тестувати наступні групи населення: — донори крові/тканин; — пацієнти на гемодіалізі; — медичні працівники, які планують працювати у сфері, яка передбачає проведення процедур, що становлять ризик інфікування. |
|
|
|
Наступним групам населення необхідно пропонувати тестування на ВГС: — пацієнти з нез’ясованим постійно підвищеним рівнем активності АЛТ; — особи, які мають в анамнезі споживання ін’єкційних наркотиків; — особи, які є ВІЛ-позитивними; — реципієнти фактора згортання крові до 1987 року; — реципієнти крові та її компонентів до вересня 1991 року та трансплантованих органів/тканин у Сполученому Королівстві до 1992 року; — діти, мати яких інфікована ВГС; — медичні працівники, які мають контакт через шкіру або слизові мембрани із кров’ю, що є або може бути інфікована ВГС; — особи, які отримали медичну чи стоматологічну допомогу в країнах, де ВГС є поширеним явищем, а інфекційний контроль є низьким; — особи, у яких є татуювання або пірсинг на тілі, що були зроблені в умовах, де інфекційний контроль є або може бути недостатнім; — особи, які мали статевого партнера/побутові контакти з особою, яка інфікована ВГС; — особи, які народилися в період з 1945 по 1965 роки. |
|
|
|
Настанова NICE «Hepatitis B and C: Ways to promote and offer testing to people at increased risk of infection»11 містить ряд ключових рекомендацій з тестування. Хоча вона призначена для служб NHS в Англії та Уельсі, вона має пряме застосування до тестування на ВГС в Шотландії. |
4 |
|
|
D |
Тестування цільної крові слід розглядати як зручний і економічно ефективний спосіб доступу до деяких цільових груп населення. |
|
|
D |
Необхідно приділяти увагу методам підвищення обізнаності і виділення важливої інформації щодо гепатиту С серед груп ризику та широкої громадськості. Рекомендується направлення пропаганди на конкретну аудиторію. Співробітники повинні мати доступ до відповідної підготовки. |
|
|
D |
Кожному, хто має негативний тест, але залишається з ризиком зараження, мають бути запропоновані подальші тестування на щорічній основі. |
|
|
D |
Тестування на ВГС має бути запропоноване мігрантам із країн із середнім або високим рівнем поширеності ВГС. |
|
Коментар робочої групи:
В Україні при визначенні груп ризику доцільно не враховувати часові періоди, встановлені для Сполученого Королівства.
3.2. Діагностичне тестування на ВГС
3.2.1. Принципи тестування
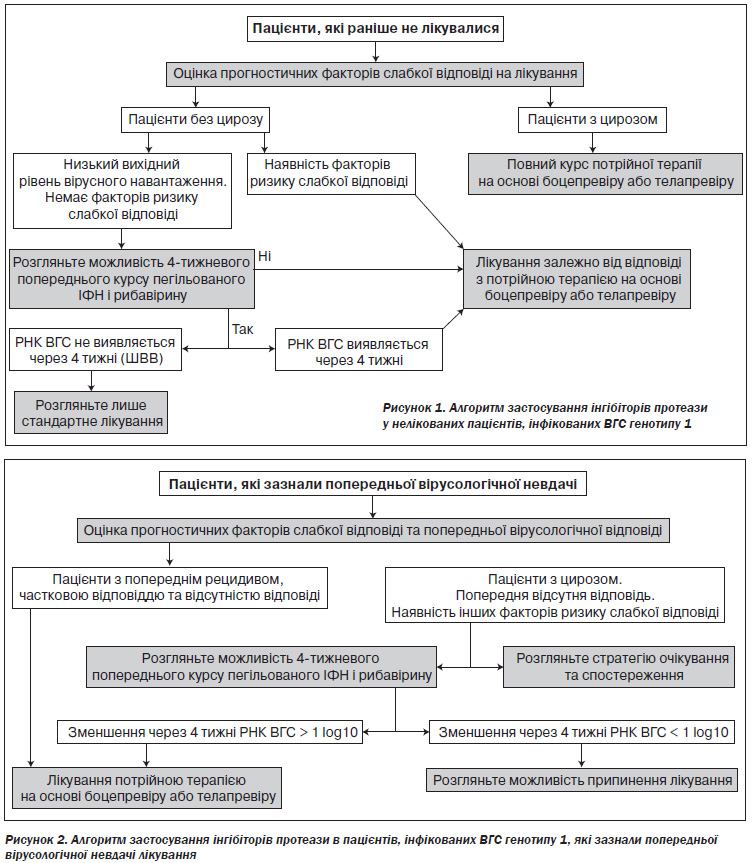
Виявлення вірусної РНК за допомогою тесту ампліфікації нуклеїновими кислотами (ТАНК), зазвичай за використання зворотньотранскрипційної полімеразної ланцюгової реакції (ЗТ ПЛР) вказує перенесену або наявну інфекцію. Алгоритм тестування наведено на рис. 1. Він базується на наступних ключових принципах:
|
— діагностичні аналізи є найбільш надійними, коли використовується плазма чи сироватка крові;20 |
2++ |
|
— аналізи на антитіла в слині є дуже чутливими за умови використання оптимальних засобів відбору слини та використання модифікованих твердофазних імуноферментних аналізів (ELISA), але ТАНК для вірусної РНК є ненадійним;20–22 |
2++ |
|
— для виявлення наявної інфекції необхідно проводити тестування нуклеїновими кислотами, що є достатньо чутливими для виявлення 50–100 МО/мл вірусу.23 |
2+ |
EASL Clinical Practice Guidelines: Management of hepatitis C virus infection (2011)
Недавні розробки ґрунтуються на полімеразній ланцюговій реакції (ПЛР) в режимі реального часу. Завдяки цьому стало можливим визначення кількості HCV-РНК за хвилину (до 10 МО/мл) і точне визначення рівня HCV-РНК приблизно до 107 МО/мл. Динамічний режим підрахунку відповідає клінічним потребам діагностики та моніторингу.
Визначення та кількісний підрахунок HCV-РНК слід проводити, використовуючи чутливі методики (нижня межа визначення — 50 МО/мл чи нижче). Ідеальним варіантом є ПЛР в режимі реального часу. Рівень HCV-РНК слід визначати в міжнародних одиницях на 1 мл (C1).
An update on the management of chronic hepatitis C: Consensus guidelines from the Canadian Association for the Study of the Liver (2012)
Виявлення HCV-РНК слід проводити з використанням чутливого кількісного аналізу (нижча межа виявлення від 10 МО/мл до 15 МО/мл або менше) з широким динамічним діапазоном. Результати повинні бути стандартизовані та виражені в МО/мл; строк виконання обстеження не повинен перевищувати 7 днів (клас 1, рівень С).
Коментар робочої групи:
ВООЗ стандартизувало кількісну ПЛР, порадивши використовувати виключно МО/мл. В Україні ще продовжують використовувати копії в мл, що не відповідає міжнародному стандарту.
|
— Вірусна РНК може бути виявлена вже в перший-другий тижні після інфікування, в той час як антитіла можуть бути виявлені на сьомому-восьмому тижні після інфікування;24 |
4 |
|
— антитіла до інфекції можуть не вироблятися, особливо коли імунітет такої особи пригнічений;25 |
4 |
|
— після гострого перебігу інфекції РНК ВГС може коливатися між позитивними та негативним значеннями кілька місяців. Результати зразків, що відібрані у даний час, можуть бути оманливими.24 В особи, яка позитивна на антитіла до ВГС, але негативна на РНК ВГС, необхідно провести аналіз другого зразка для підтвердження початкового діагнозу, особливо коли в більшості випадків дата інфікування невідома; |
4 |
|
— особи з позитивним результатом тесту на антитіла до ВГС і повторно негативним РНК не потребують подальшого активного ведення гепатиту С;25 |
4 |
|
— оскільки гепатит С є серйозним інфекційним захворюванням, після початкового лабораторного діагностування у пацієнта необхідно взяти другий зразок для підтвердження правильності результатів першого зразка;26 |
4 |
|
— необхідним є проведення генотипування вірусу в осіб з підтвердженою ВГС інфекцією для визначення ймовірної відповіді на лікування. Особи з інфекцією вірусу генотипу 1 потребують лікування довшої тривалості, ніж особи з інфекцією генотипу 2 і 3 (див. розділ 10.2.1);27 |
1++ |
|
— експертні вказівки передбачають, що медичним працівникам, які мають або можуть мати тривалий професійний контакт з ВГС, необхідно пропонувати проведення РНК тестування на 6, 12 та 24-й тиждень з тестуванням на антитіла до ВГС на 12-й та 24-й тиждень.28 |
4 |
|
B |
Діагностичне тестування на ВГС має проводитися на сироватці або плазмі крові, коли це можливо. |
|
D |
Генотипування ВГС має проводитися у випадку, коли розглядається питання призначення противірусної терапії. |
|
D |
Після черезшкірної експозиції з інфікованою кров’ю або потенційно інфікованою кров’ю медичним працівникам необхідно запропонувати проведення тестування РНК ВГС на 6, 12 та 24-му тижнях з тестуванням на антитіла до ВГС на 12-му та 24-му тижнях. |
EASL Clinical Practice Guidelines: Management of hepatitis C virus infection (2011)
Особам, які зазнали травмування голкою, що була контамінована HCV, необхідно провести аналіз на HCV-РНК протягом 4 тижнів.
Аналізи на активність АЛТ та антитіла до вірусу гепатиту С слід проводити через 12 і 24 тижні (B2).
Працівники закладів охорони здоров’я повинні здавати аналізи на антитіла до HCV. Медичні працівники з позитивним ПЛР на РНК вірусу гепатиту С повинні уникати діяльності, що пов’язана з підвищеним ризиком випадкового проколу чи травмування шкіри чи слизових оболонок (C2).
ІV. Запобігання вторинній трансмісії
Поняття вторинної трансмісії визначається як подальша передача інфекції від осіб, про яких відомо, що вони інфіковані ВГС.
4.1. Трансмісія через статевий або побутовий контакт
|
Спостережні дослідження вказують, що існує дуже низький ризик передачі інфекції від осіб, які інфіковані ВГС, до членів їх сімей, близьких або статевих партнерів. Когортні дослідження дискордантних пар по ВГС вказують на захворюваність ВГС у 0–2 на 1000 років статевих контактів.29–31 Особи, які мають коінфекцію з ВІЛ, особливо чоловіки, які мають статеві стосунки з чоловіками, можуть мати більшу вірогідність передачі свого ВГС захворювання своїм статевим партнерам.32, 33 З’ясовані факти передбачають, що передача відбувається через контакт з кров’ю, наприклад внаслідок спільного користування лезами для гоління та зубними щітками (тобто ті види діяльності, що призводять до черезшкірного контакту та контакту слизових мембран з інфікованою кров’ю), а також через незахищений статевий акт. |
2+ 1– |
|
Не проводилося жодних досліджень для підтвердження ефективності таких інтервенцій, як освітні ініціативи, включаючи пропаганду використання презервативів, що націлені на осіб, у яких діагностовано ВГС, у зниженні частоти ризикованої поведінки та/або запобігання асоційованій вторинній трансмісії ВГС. Експертна думка наголошує, що особи, які інфіковані ВГС, мають отримувати консультації щодо використання презервативів та уникнення видів діяльності, що можуть призвести до черезшкірного контакту та контакту слизової тканини з інфікованою кров’ю. Це дозволить, хоча і невеликою мірою, зменшити ризик трансмісії вірусу до інших осіб.14, 34 |
4 |
|
- |
Після консультації про низький ризик передачі ВГС статевим шляхом особам, які інфіковані ВГС, необхідно рекомендувати розглянути питання використання презервативів впродовж статевого контакту, якщо це чоловік, який має статеві контакти з чоловіком, або один із партнерів інфікований ВІЛ. |
|
D |
Особам, які мають ко-інфекцію ВГС/ВІЛ, необхідно рекомендувати завжди практикувати тільки безпечний статевий контакт і використовувати презервативи. |
|
D |
Особам, які інфіковані ВГС, необхідно рекомендувати уникати дій, що можуть призвести до контакту з їх інфікованою кров’ю через шкіру чи через слизові мембрани, як то спільне використання лез для гоління та зубних щіток. |
4.2. Трансмісія через споживання ін’єкційних наркотиків
|
Спільне використання ін’єкційних засобів споживачами наркотиків є головним способом передачі інфекції у розвинутих країнах.14, 34 Спостережні дослідження демонструють, що такі інтервенції, як обмін голок та шприців, а також підтримуюча терапія метадоном, мають велику вірогідність знизити, хоча і неконтрольовано, трансмісію ВГС серед СІН у багатьох країнах, включаючи Шотландію.35 Дослідження інтервенцій, що направлені конкретно на запобігання поширенню інфекції від інфікованих СІН до інших осіб через спільне використання ін’єкційного приладдя, не виявлені. |
2+ |
|
Жодних надійних переконливих доказів впливу знання свого ВГС статусу серед СІН на їх ризиковану ін’єкційну поведінку не виявлено. Експертна думка пропонує рекомендувати активним СІН з хронічним ВГС як запобігти трансмісії інфекції іншим СІН, наприклад, завдяки впровадженню безпечних ін’єкційних практик. Така інтервенція може бути ефективною.14, 34 |
4 |
|
D |
СІН, які знають, що вони інфіковані ВГС, мають отримати рекомендації щодо того, як вони можуть запобігти трансмісії інфекції іншим споживачам ін’єкційних наркотиків. |
4.3. Трансмісія між медичними працівниками та пацієнтами
4.3.1. Ризик інфікування медичних працівників
|
За експертною думкою, заходи інфекційного контролю мають бути стандартизованими та універсальними, а не визначатися знанням про статус пацієнта та вірус, що передається через кров.36 |
4 |
|
Оцінки ризику трансмісії після уколу голкою різняться. Було проведено одне оглядове дослідження із залученням 4403 медичних працівників, які мали контакти з такими пацієнтами. Дослідження виявило, що загальний рівень трансмісії становить 0,31 %, в той же час як оцінка 25 менших досліджень дали комбінований результат з рівнем у 1,9 % при залученні 2357 осіб.16, 37 |
2+ 4 |
|
Відносний ризик вище, коли поранення глибокі, а в голці була кров. Ризик від поверхневого контакту або контакту слизової ймовірно значно вищий, але його важче обрахувати, в той час як трансмісія через тверді голки є дуже низькою.37 Трансмісія відбувається лише від РНК-позитивних джерел. |
|
|
- |
Стандартні заходи інфекційного контролю проти трансмісії вірусних захворювань, що передаються через кров, мають проводитися всіма медичними працівниками незалежно від знання пацієнта свого статусу або підозри на інфекцію. |
|
- |
Медичні працівники, які отримали травми від голки з інфікованого ВГС джерела, мають знати: — загальний ризик трансмісії ймовірно нижче 2 %, а може бути і набагато нижче; — ризик вище при нанесенні глибоких ран та при пораненні голками, що наповнені кров’ю; — ймовірність трансмісії через безпорожнинні голки є низькою. |
4.3.2. Ризик інфікування пацієнтів
|
Існують документи, що посвідчують передачу ВГС від медичних працівників до пацієнтів.17 Більшість з них відбулися в результаті контакту після проведення процедур, зазвичай після порожнинних хірургічних втручань. Оцінка значення трансмісії до пацієнтів у двох ретроспективних аналізах за участі кардіохірургів склала 2,3 і 0,36 %, в той час як ризик трансмісії від інфікованого гінеколога склав лише 0,04 %.38–40 Управління охорони здоров’я Сполученого Королівства рекомендує, щоб медичні працівники, які є ВГС РНК-позитивними, не проводили небезпечних процедур з пацієнтами.17, 41 |
3 4 |
|
D |
Медичні працівники, які знають, що вони є ВГС РНК-позитивними, не повинні проводити небезпечних процедур із пацієнтами. |
V. Направлення
Необхідно розглядати можливість направлення на надання спеціалізованої допомоги для всіх пацієнтів з активною ВГС інфекцією (ВГС РНК-позитивні), а не обмежуватися лише потенційними кандидатами на противірусну терапію. Спеціалізовані клініки часто є джерелом інформації для пацієнтів та їх родичів, включаючи пропаганду охорони здоров’я та методів уникнення вторинної трансмісії вірусу.
|
Нещодавні моделювання вказують, що 90 % осіб із ВГС в Шотландії є активними або колишніми СІН.1 Фактори, що асоціюються зі споживанням ін’єкційних наркотиків (напр., бідність, безладний спосіб життя, супутні захворювання, включаючи алкогольну залежність), можуть стати перешкодою для осіб, які перебувають в процесі дослідження, направлення та лікування.15,19 Експерти дійшли консенсусу, що надання послуг може бути вдосконалено шляхом інтегрованої мультидисциплінарної |
4 |
|
допомоги, що також допомагає особам, які мають проблеми з алкоголем та наркотиками, одночасно з наданням їм допомоги спеціалістами з ВГС.15 |
|
Не було виявлено жодних доказів на підтримку превалюючої думки, що дослідження та лікування активних СІН із ВГС інфекцією не повинно пропагандуватися, оскільки вони навряд чи мають хоча би помірний гепатит або навряд чи будуть дотримуватися такого лікування.
|
Два спостережні дослідження та одне контрольне п’ятирічне дослідження не виявили різниці в дотримуванні протоколів лікування та показали, що СІН, які описані як «активні» на момент реєстрації та проходження лікування наркозалежності, дотримувалися противірусного лікування в такій же мірі як ті, хто ніколи не вживав ін’єкційних наркотиків.42–44 Дані дослідження були маломасштабними і не містили деталей про ін’єкційну поведінку учасників дослідження. |
2 |
|
Всі пацієнти з гострим ВГС мають негайно направлятися на надання спеціалізованої допомоги, оскільки лікування впродовж гострої фази має більшу ймовірність бути успішним (див. розділ 7.3).45 |
1++ |
За ідеальних умов спеціалізована клініка повинна бути інтегрована з іншими службами, що мають можливість забезпечити безперешкодне пересування пацієнтів, особливо тих, яким важко отримати медичну допомогу. Така інтеграція має заохочувати служби, такі як служба з наркотичних проблем та медичні тюремні служби, до позитивного та безперервного реагування на питання ВГС інфекції.
|
D |
Особи, включаючи СІН, у яких діагностовано хронічний ВГС, повинні отримувати інтегровану мультидисциплінарну допомогу, що може максимізувати початок лікування та утримування пацієнта на лікуванні. |
|
A |
Пацієнти з гострою ВГС інфекцією мають негайно направлятися на надання спеціалізованої допомоги. |
|
- |
Активні СІН, які інфіковані ВГС, не повинні виключатися з розгляду можливості клінічного ведення ВГС, включаючи противірусну терапію, на основі їх ін’єкційного статусу. |
|
- |
Всі пацієнти мають направлятися до медичного закладу, щоб періодично проводити оцінку стану інфекції та прогресування хвороби печінки, для визначення необхідності подальших заходів або терапії. |
VІ. Діти і вірусний гепатит С
6.1. Трансмісія від матері до дитини
|
Вагітні жінки, які є ВГС РНК-негативними, не складають ризику трансмісії для своєї дитини.46,47 |
2+ |
|
Ризик серед жінок, які інфіковані ВГС і є РНК-позитивними, у передачі інфекції дитині внутрішньоутробно або протягом пологів складає приблизно 5 %, а для тих, хто мають ко-інфекцію з ВІЛ, ризик є вдвічі вищим.48 Ризик дитини в інфікуванні ВГС від матері не залежить від методу народження чи грудного годування.48 Одне перспективне дослідження вказує: моніторинг шкіряного покрову голови плода може підвищити ризик передачі інфекції від матері до дитини.49 Велике ретроспективне дослідження не продемонструвало жодного підвищеного ризику.48 Вагінальні пологи можуть підвищити ризик трансмісії ВГС, якщо мати дитини має ко-інфекцію з ВІЛ з очевидним вірусним навантаженням.48 |
2++ |
|
B |
ВГС РНК-позитивний статус вагітної жінки не повинен впливати на акушерське ведення вагітності або на стандартні поради щодо грудного вигодовування. |
Коментар робочої групи:
Українська нормативна база з акушерсько–гінекологічної допомоги відповідає положенням даної настанови.
6.2. Тестування дітей та немовлят на вірусний гепатит С
Метою тестування немовлят, які народилися у жінок із гепатитом С, є не стільки виявлення всіх дітей, яким передалося захворювання, а виявлення тих, хто має ризик хронічної інфекції та довготривалих наслідків цього.
|
Немовлята, які народилися у жінок з позитивним результатом на антитіла до ВГС, матимуть позитивні результат на антитіла до ВГС після народження.50 Немовлята, які не є інфікованими, стають негативними на антитіла до ВГС в період з 6-го по 20-й місяць від народження. Близько 80 % будуть негативні до 12 місяців від народження.46, 51 Позитивні результати на вірусну РНК за ТАНК-тестом можуть бути отримані в перші місяці життя дітей, які пізніше стануть негативними і втратять антитіла до ВГС.51–54 Деякі інфіковані немовлята можуть не бути ВГС РНК-позитивними до 12 місяців від народження або після цього періоду.54 Нещодавнє дослідження вказує, що чутливість позитивних результатів ЗТ ПЛР, які отримані з двох досліджень (у період з 2 до 6 місяців життя), для прогнозування інфекції складає 81 % (95% довірчий інтервал; ДІ 58–97 %).55 |
2+ |
|
У випадку ко-інфекції з ВІЛ немовлята, які є стабільно позитивні за РНК, можуть мати негативні результати тесту на антитіла до ВГС між 12-м та 18-м місяцями життя.53 |
3 |
|
B |
Немовлята, які народилися у жінок з позитивним результатом на антитіла до ВГС і негативним до ВГС РНК, не потребують тестування. |
|
B |
У дітей, які народилися у жінок з ВГС, тест на антитіла до ВГС має проводитися на 12-му місяці життя або пізніше для виявлення меншості дітей, які є інфікованими. |
|
B |
Діти, матері яких мають ко-інфекцію з ВІЛ, та немовлята, у яких виявлено позитивні результати тесту на антитіла до ВГС після 12 місяців, мають пройти тест на РНК ВГС. А коли це можливо — підтвердити результати за допомогою другого зразка. |
|
B |
Якщо інформація про ризик інфікування ВГС окремої дитини необхідна раніше ніж на 12-й місяць життя, тест на РНК ВГС та повторний аналіз може бути проведено після 2 місяців від народження. Для отримання остаточного діагнозу необхідне подальше тестування. |
6.3. Перебіг вірусного гепатиту С у дітей
|
Перехресні дослідження вказують, що у 20–40 % дітей, які мають позитивний результат на антитіла до HCV після 18 місяців, не виявляється РНК-HCV, що свідчить про спонтанний кліренс.57, 58 Серед хронічно інфікованих, які залишаються позитивні на РНК-HCV, подальша ймовірність спонтанного кліренсу є низькою (3,5 %).59 |
3 |
|
Рівні активності трансаміназ (АЛТ) вдвічі вище від верхньої межі норми спостерігаються у 50 % інфікованих дітей.59 |
3 |
|
D |
Діти, які інфіковані ВГС, повинні проходити моніторинг для виявлення меншості, що має ризик прогресуючого фіброзу в дитинстві, і які можуть бути кандидатами на лікування. |
|
- |
Діти, які інфіковані ВГС, повинні проходити клінічну оцінку кожні 6–12 місяців, здавати кров на аналіз та проводити тест на функціональність печінки. За наявності клінічних або УЗ порушень або у випадку підвищення РТ в сироватці крові вдвічі вище від верхньої межі норми необхідно розглянути питання проведення біопсії печінки. |
6.4. Лікування дітей з вірусним гепатитом С
|
Рівні відповіді на лікування у дітей мають подібні значення, вказують на той же самий вплив генотипу, як і у дорослих (див. розділ 10).60 Комбіноване лікування інтерферонами та рибавірином дає загальну СВВ на рівні 50–60 %.60–63 Існує потенційна загроза впливу на функції щитовидної залози та спричинення проблем росту. 62, 63 |
3 |
|
Комбінована терапія пегільованим ІФН і рибавірином краща, ніж лише пегільованим інтерфероном, і призводить до результатів, подібних до результатів у дослідженнях дорослих (див. розділ 10).10 |
1+ |
|
Комбіноване лікування інтерфероном і рибавірином забезпечує СВВ на рівні 80–93 % у дітей з інфекцією генотипу 3, але тільки 47–59 % у дітей з генотипом 1, що схоже на дані у дослідженнях дорослих. 10, 64, 65 |
2+ |
|
А |
Дітей, інфікованих всіма генотипами вірусу гепатиту С з ознаками помірного або важкого захворювання печінки, слід розглядати для лікування пегільованим ІФН і рибавірином. |
|
В |
Дітей, інфікованих генотипом 2 і 3 ВГС, слід розглядати для лікування пегільованим ІФН і рибавірином незалежно від стадії захворювання. |
|
С |
У дітей з легкою формою захворювання та інфекцією інших генотипів переваги лікування повинні бути збалансовані з ризиками побічних ефектів. |
|
- |
Лікування дітей з генотипом 1 ВГС з використанням інгібіторів протеази слід розглядати тільки як частину клінічних досліджень. |
|
- |
Випадки захворювання дітей на ВГС необхідно вести у консультаціях з педіатричною службою зі спеціалістом з питань гепатиту С. |
VІІ. Гострий гепатит C
7.1. Перебіг хвороби
|
Захворюваність на гострий гепатит С є невідомою, але її можна оцінити на основі поширеності хронічного гепатиту C (ХГС).66 Гострий гепатит С зазвичай є асимптоматичним.67 Повний клінічний спектр симптомів гострого гепатиту С проявляється дуже рідко (< 15 % пацієнтів).68 Рівень смертності від гострого гепатиту С є дуже низьким (0,1 % або менше), а найбільш поширеним результатом захворювання є хронічна інфекція.67–69 |
3 |
|
Лабораторне діагностування має починатися з аналізу на антитіла до ВГС, але у ранніх випадках ВГС РНК може бути єдиним маркером інфекції (див. розділ 3.2).70 |
2+ |
|
Спонтанне одужання спостерігається у 30–50 % пацієнтів з симптомами інфекції впродовж, як правило, 3 місяців після діагностування. Найбільше це поширено серед жінок із жовтяничною формою хвороби.66, 67, 71, 72 |
3 |
|
D |
Пацієнти з гострим гепатитом С потребують клінічного та лабораторного моніторингу (нагляд за спонтанним кліренсом вірусу) протягом 3 перших місяців після діагностування, оскільки у таких пацієнтів часто відбувається самообмеження хвороби. |
7.2. Профілактика після контакту
|
Не існує досліджень, що виявили б ефективність імуноглобуліну, терапії інтерферонами або противірусними препаратами у запобіганні трансмісії при прийомі одразу після ризикованого контакту. Дві оцінки розглядали старі дослідження щодо імуноглобуліну і не встановили ніякої його ефективності, та прийшли до висновку, що імуноглобулін та терапія інтерферонами не рекомендовані після контакту з ВГС.28, 73 |
4 |
7.3. Лікування пацієнтів з гострим гепатитом С
7.3.1. Час лікування
|
У більшості пацієнтів, у яких спостерігається спонтанний кліренс вірусу гепатиту С, це відбувається у період 12 тижнів після діагностування.66, 72 Немає даних, що вказували б на те, що відкладене лікування від трьох до шести місяців після діагностування знижує відповідь на лікування, хоча дозволяє спонтанний кліренс.45 Відкладення лікування на один рік після виявлення знижує стійку вірусологічну відповідь.45 |
3 1++ |
|
D |
Лікування має починатися у період від 3 до 6 місяців після діагностування гострого гепатиту С, якщо інфекція не зникла самостійно. |
7.3.2. Вибір та тривалість лікування
|
Два систематичні огляди розглянули ефективність застосування непегільованих інтерферонів для лікування пацієнтів з гострим гепатитом С.74,75 В одному з досліджень учасники груп лікування мали вищий рівень стійкої вірусологічної відповіді (62 %), ніж учасники груп без лікування (12 %).74 Оцінка Кокрейна продемонструвала, що збільшення дози непегільованих інтерферонів протягом початкової фази лікування асоціювалося із вищим рівнем стійкої вірусологічної відповіді.75 Немає даних про залежність відповіді на лікування гострого гепатиту С від генотипу HCV. |
1++ |
|
Не було виявлено РКД пегільованих інтерферонів проти звичайних інтерферонів для пацієнтів із гострим гепатитом С. У серії випадків 16 пацієнтів, які не мали сероконверсії за три місяці, проходили лікування лише пегільованими інтерферонами протягом 24 тижнів. Повідомлялося, що стійка вірусологічна відповідь склала 94 %.66 |
3 |
|
A |
Пацієнти з гострим гепатитом С мають лікуватися інтерферонами, якщо інфекція не зникла самостійно. |
|
D |
Пацієнтів можна лікувати пегільованими або непегільованими інтерферонами. |
|
D |
Пацієнти з гострим ВГС повинні проходити лікування інтерферонами протягом 24 тижнів незалежно від генотипу захворювання. |
VІІІ. Оцінка стану печінки
8.1. Клінічна оцінка
|
Клінічна оцінка тяжкості захворювання печінки пацієнтів із хронічним гепатитом С є неточною і недооцінює тяжкість змін, як це показує біопсія печінки. |
3 |
8.2. Маркери фіброзу
|
Дослідження неінвазивних методів виявлення важкості хвороби печінки із використанням |
2++ |
|
комбінації клінічних та біохімічних показників виявили, що може бути можливим розрізняти пацієнтів з цирозом від тих, у кого легкий перебіг захворювання. Проміжні етапи не розрізняються.77 |
|
|
Систематична оцінка продемонструвала, що сурогатні маркери фіброзу, які відображають порушення функції печінки (активність АЛТ, тромбоцити) або метаболізм фіброзу (напр., тканинний інгібітор матричних металопротеїназ 1, гіалуронова кислота), не можуть використовуватися окремо для прогнозування фіброзу. У окремих пацієнтів такі маркери, використані самі по собі, не можуть надійно диференціювати стадії фіброзу. Якщо маркери використовуються в панелях, вони можуть визначати, чи особа має високий або низький рівень фіброзу. 14 досліджень у систематизованій оцінці застосовували 10 різних панелей маркерів, жоден із яких не був кращий за інші з точки зору статистичного порівняння. Тест порівнювали із золотим стандартом біопсії печінки як частину процесу їх валідації, хоча і біопсія печінки потенційно може бути неточною через похибку вибірки. Порівняння сурогатних маркерів та біопсії печінки з клінічними результатами може бути більш релевантним.78 |
2++ |
|
B |
Біохімічні маркери не треба використовувати у якості альтернативи біопсії печінки для визначення проміжних стадій фіброзу. |
|
B |
Біохімічні тести можуть використовуватися як альтернатива біопсії печінки для діагностування цирозу або прямого скринінгу ускладнень фіброзу. |
|
- |
Вимірювання щільності печінки може бути корисним в якості неінвазивної оцінки фіброзу печінки |
Коментар робочої групи:
Останніми роками виявлено недоліки біопсії, результатом цього стала поява неінвазивних методів оцінки фіброзу у пацієнтів з хронічним ВГС, що включають всебічний аналіз. Вони включають біохімічні маркери та транзитну еластографію.
8.3. Біопсія печінки
|
Біопсія печінки має бути принаймні 25 мм завдовжки для того, щоб визначити ступінь фіброзу з точністю у 75 %.79 Смертність в результаті біопсії печінки складає 0,13–0,33 %, а ступінь значної захворюваності складає близько 5,9 %.80 |
3 |
8.3.1. Коли проводити біопсію
|
Біопсія печінки для пацієнтів з ХГС може забезпечити додатковий діагноз, такий як алкогольна хвороба печінки або стеатоз (10 % пацієнтів), і може вплинути на прийняття рішення щодо ведення випадку захворювання у 5 % |
3 |
|
пацієнтів.81 Повторна біопсія печінки може бути корисна для ідентифікації осіб для лікування; третина пацієнтів з легкою формою ХГС мають один ступінь прогресування фіброзу за шкалою Іцхака (0–6) в середньому за 30 місяців.82 Частота і час проведення біопсії печінки мають відповідати потребам індивідуального пацієнта, оскільки прогресування фіброзу не є лінійним. |
|
|
Виражений фіброз або цироз за результатами біопсії печінки порівняно з легкою формою захворювання прогнозує помірне зниження СВВ після противірусної терапції.83 |
1++ |
|
Біопсія печінки до та після успішної противірусної терапії (середній інтервал 20 місяців) показала як покращення з точки зору фіброзу (277 з 1094 пацієнтів), так і в зниженні ступеня цирозу (75 з 153 пацієнтів).84 |
1+ |
|
D |
Біопсія печінки має проводитися тоді, коли є підозра щодо додаткових причин захворювання печінки. |
|
D |
Повторна біопсія печінки має розглядатися для пацієнтів з легким перебігом захворювання, які залишаються без лікування, якщо прогресування фіброзу печінки може вплинути на рішення щодо вибору противірусної терапії. |
|
- |
У пацієнтів з вродженими порушеннями згортання крові біопсія печінки має проводитися після консультації з фахівцем з питань гемофілії. |
8.3.2. Біопсія та генотипи
|
Показник стійкої вірусологічної відповіді після терапії пегільованими інтерферонами та рибавірином для пацієнтів з генотипом 2 і 3 складає 76–82 %, 41–51 % — для пацієнтів з генотипом 1.7 Центр оцінки технологій охорони здоров’я Сполученого Королівства рекомендує не вимагати проведення біопсії печінки перед початком лікування пацієнтів з генотипом 2 і 3.7 |
4 |
|
D |
Біопсія печінки не повинна розглядатися як суттєвий тест перед початком противірусної терапії, особливо для пацієнтів з інфекцією генотипу 2 і 3. |
ІХ. Прогресування нелікованої хвороби
|
Хронічний гепатит С асоціюється зі значним ризиком розвитку цирозу і гепатоцелюлярної карциноми (ГЦК).3, 85 Розрахувати величину ризику розвитку цирозу і ГЦК з часом важко, оскільки результати сильно залежать від дизайну дослідження та характеристик досліджуваної популяції.3, 85 |
2++ |
|
Систематичний огляд 57 досліджень (всі перехресні та вивчені в різні моменти часу), які включали пацієнтів клінік захворювань печінки, |
|
|
пацієнтів після трансфузій, донорів та пацієнтів широкої громадськості, оцінили ризик прогресування цирозу через 20 років: — клініки захворювань печінки: 22 % (95% ДІ від 18 до 26 %); — пацієнти після трансфузій: 24 % (95% ДІ від 11 до 37 %); — донори: 4 % (95% ДІ від 1 до 7 %); — пацієнти широкої громадськості: 7 % (95% ДІ від 4 до 10 %). |
2++ |
|
Через систематичні похибки вибірки, притаманні перехресним клінічним даним щодо захворювань печінки, когортні дослідження для популяції можуть найбільш достовірно представляти прогресування захворювання на рівні популяції. Когорти на основі популяції вказують, що в осіб, які були інфіковані ВГС у молодому віці, лише у 10 % через 20 років розвинеться цироз. Старший вік інфікування ВГС, чоловіча стать і сильне зловживання алкоголем асоціюються з більш швидким прогресуванням хвороби.3 |
2++ |
|
Середній період часу від інфікування ВГС до розвитку ГЦК також показує значні варіації між дослідженнями, коливаючись від 9 до 31 року в одній систематизованій оцінці.85 Фактично жодного випадку ГЦК не розвивається у першу декаду після інфікування ВГС, більшість виявляються вже після 20 років від моменту інфікування.85 |
2++ |
|
Ризик розвитку ГЦК для пацієнтів з встановленим цирозом, що викликаний ВГС, складає 7 % впродовж контролю через 5 років.86, 87 |
2+ |
|
Пацієнти з встановленим цирозом, асоційованим з ВГС, схильні до ризику ускладнень, таких як асцит, шлунково–кишкові кровотечі і печінкова енцефалопатія.86, 87 Кумулятивна ймовірність всіх форм декомпенсації пацієнтів з цирозом, у яких немає пухлин, складала 18 % на 5 років у одному дослідженні із загальним п’ятирічним рівнем виживання у 91 %.87 |
2+ |
9.1. Вік, стать, етнічне походження
|
Збільшення віку впродовж розвитку ВГС інфекції пов’язано з більш швидким прогресуванням фіброзу печінки і скороченням часу від інфікування до розвитку цирозу.87-89 Вік більше 40 років на момент зараження особливо пов’язаний з більш швидкою прогресією.89, 90 |
3 |
|
Три когортні дослідження звітують, що чоловіки, які інфіковані ВГС, мають більшу вірогідність до прогресування хвороби до прогресуючих стадій фіброзу печінки, ніж жінки.89, 91, 92 |
3 |
|
Відмінності в прогресуванні захворювання спостерігаються у пацієнтів різних рас. Два когортні дослідження продемонстрували, що захворювання прогресувало дещо не так швидко серед пацієнтів афроамериканців порівняно з пацієнтами, які не є афроамериканцями.93, 94 |
2+ |
|
Вірогідна швидкість прогресування у цих пацієнтів має розглядатися впродовж прийняття рішення про необхідність продовження противірусної терапії. |
|
|
D |
Оцінюючи ймовірну швидкість прогресування хвороби печінки, необхідно брати до уваги вік, стать та етнічне походження пацієнта. |
9.2. Маса тіла
Дослідження виявили, що індекс маси тіла (ІМТ) > 25 асоціюється зі стеатозом печінки (див. розділ 12.1.3).
9.3. Тютюнопаління
|
Тютюнопаління є незалежним чинником ризику прогресування запалення печінки і фіброзу у хворих із ХГС.95, 96 Даних про вплив припинення паління виявлено не було. |
3 |
|
D |
Пацієнти з ХГС мають бути поінформовані, що тютюнопаління може прискорити прогресування хвороби печінки. |
9.4. Алкоголь
|
Сильне зловживання алкоголем у пацієнтів, інфікованих ХГС, асоціюється з більш важким захворюванням печінки, включаючи цироз печінки, термінальні стадії захворювання печінки і гепатоцелюлярний рак.97, 98 Середнє споживання алкоголю більше шести одиниць в Сполученому Королівстві в день асоціюється з більш швидким прогресуванням фіброзу печінки.88, 89, 92 |
2+ 2++ |
|
Коментар робочої групи: В країнах Європи одиниця алкоголю дорівнює 10 мл чистого етанолу. |
|
|
Навіть помірна (визначена Шотландськими директивами) кількість алкоголю асоціюється з підвищеним ризиком розвитку фіброзу печінки у порівнянні з тими, хто утримується від споживання алкоголю.89, 99 |
|
|
Пацієнти, які знають свій ВГС статус, мають вищу вірогідність прислухатися до поради припинити споживати алкоголь, аніж ті, хто вважає себе неінфікованим.100 |
2++ |
|
B |
Пацієнти з ХГС повинні бути поінформовані, що вживання алкоголю (навіть помірне) може прискорити прогресування хвороби печінки. |
9.5. Аланінамінотрансфераза
|
Приблизно 25 % (діапазон 10–40 %) пацієнтів з ХГС мають стабільно нормальний показник активності аланінамінотрансферази сироватки крові (НАЛТ). Такі пацієнти, більш імовірно, є жінками з легким перебігом хвороби.101 Хоча є суттєва кореляція між пацієнтами з НАЛТ і пацієнтами з легкою формою захворювання печінки, ці терміни не є синонімічними, а групи розглядаються окремо в лікувальних цілях (див. розділи 10.3.1 і 10.3.3). Визначення «стабільно |
1— 2— |
|
нормальний» відрізняється в довідковій літературі з показниками вимірювання активності АЛТ кожні 2–3 місяці за період часу від 6 до 18 місяців.101 Тим не менш, загострення активності АЛТ може відбуватися у 21,5 % пацієнтів після того, як воно було нормальним протягом 12 місяців.102 У даному випадку немає асоціації з гепатитом С, генотипом або вірусним навантаженням.101 |
|
|
Прогресування фіброзу печінки відбувається повільніше у пацієнтів із НАЛТ, ніж у пацієнтів з підвищеним рівнем активності АЛТ.103 У пацієнтів, які не лікувалися, з легким перебігом захворювання, прогресування до помірного або важкого захворювання за час спостереження (5,6 року) складає 5 % для пацієнтів з НАЛТ і 24 % для пацієнтів із підвищеним рівнем активності АЛТ. |
2++ |
An update on the management of chronic hepatitis C: Consensus guidelines from the Canadian Association for the Study of the Liver (2012)
Нормальний рівень активності АЛТ не є протипоказанням до лікування. Ці пацієнти, які становлять приблизно одну третину хронічно інфікованих осіб, також реагують на терапію, як і пацієнти з підвищеним рівнем АЛТ. Більше того, приблизно одна четверта частина пацієнтів з постійно нормальним рівнем активності АЛТ мають хворобу печінки від помірної до важкої за даними біопсії.
|
Вважається, що рутинна біопсія печінки є непотрібною, якщо немає потреби у конкретній інформації щодо вибраних пацієнтів.101 |
1+ |
|
D |
Виявивши НАЛТ, необхідно проводити вимірювання активності АЛТ кожні 2–3 місяці, щоб упевнитися, що зростання активності АЛТ не були пропущені. |
|
- |
Тривалість контролю для визначення НАЛТ має складати 12 місяців. |
|
- |
Проведення біопсії печінки має розглядатися лише за умови клінічного занепокоєння або інших проблем з окремим пацієнтом. |
9.6. Ко-інфекція з ВІЛ
|
Існує підвищений рівень розвитку термінальної стадії захворювання печінки у пацієнтів з ко-інфекцією ВІЛ і ВГС порівняно з тими, хто має тільки ВГС (відносний ризик, ВР = 6,14, 95% ДІ від 2,86 до 13,2).104 Середній період часу до цирозу печінки у хворих з ко-інфекцією складає 26 років, у порівнянні з 38 роками у пацієнтів з моноінфекцією ВГС.104 Пацієнти з ВГС з помірною імуносупресією в результаті ВІЛ також мають більш серйозні захворювання печінки, ніж ті, хто хворіє тільки на ВГС.105 Існує помітне збільшення смертності внаслідок захворювання печінки у пацієнтів з ко-інфекцією ХГС і ВІЛ (ВР = 17,5).106 |
1+ 2+ |
|
Ефективна терапія проти ВІЛ і пов’язане з цим відновлення імунітету може обмежити прогресування захворювання печінки на ВГС.107 |
2++ |
|
B |
Прискорення швидкості розвитку декомпенсованого захворювання печінки у пацієнтів з ко-інфекцією ВГС та ВІЛ повинно спонукати до якнайшвидшого призначення противірусної терапії. |
9.7. Ко-інфекція з вірусом гепатиту А або гепатиту В
|
Особам з ВГС рекомендована вакцинація проти гепатиту А і гепатиту В.108 Спільний звіт про лікування гепатиту рекомендує вакцинацію проти гепатиту В, але не проти гепатиту A.109 Одне дослідження випадку пацієнта з ВГС, який заразився гепатитом А, підтвердив високий рівень загрози фулмінантного гепатиту.110 |
4 |
|
Відповідь антитіл на вакцинацію проти гепатиту В у пацієнтів з хронічним ВГС знижена.111 |
3 |
|
D |
Необхідно розглянути можливість вакцинації пацієнтів з гепатитом С проти гепатиту А і В. |
|
Пацієнти з ВГС, які мають серологічні докази наявної чи перенесеної інфекції гепатиту В (ВГВ), мають більшу вірогідність отримати важке захворювання печінки.91, 112, 113 |
3 |
|
D |
Розраховуючи вірогідність прогресування хвороби печінки в результаті гепатиту С, необхідно зважати на наявну або перенесену хворобу ВГВ. |
|
- |
Пацієнти з ВГС мають проходити тести на наявне або перенесене захворювання гепатиту В. |
9.8. Визначення рівня заліза
|
Пацієнти з ХГС можуть мати підвищені показники заліза (ППЗ), але немає єдиної думки з приводу того, чи це має вплив на захворювання. Показники феритину сироватки і сатурації трансферину збільшені в 20–60 % пацієнтів і корелюють з активністю АЛТ, допускаючи, що вони є маркерами запалення. Існує слабка кореляція з концентрацією заліза в печінці (КЗП).113 ППЗ рідко значно підвищений у пацієнтів із передцирозним станом. Від 20 до 50 % пацієнтів із цирозом печінки матимуть підвищені значення показників заліза, але це також часто зустрічається у пацієнтів з цирозом через гепатит В та алкогольну хворобу печінки.113 |
4 |
|
Невідомо, чи підвищений показник заліза як єдиний фактор має вплив на відповідь на лікування лише інтерферонами.113 |
4 |
|
Не було знайдено доказів того, що виснаження запасів заліза (через кровопускання) має будь-який вплив на вірус чи перебіг захворювання печінки.114 Існують попередні докази від 4 невеликих РКД, що кровопускання окремим пацієнтам з маркерами підвищення показників заліза до початку монотерапії інтерферонами може покращити СВВ.114, 115 |
4 1– |
|
D |
Помірне навантаження заліза не виправдовує конкретних заходів перед початком противірусної терапії, оскільки навряд чи має клінічну важливість. |
|
D |
Пацієнти із суттєвим рівнем збереження заліза потребують подальшого дослідження додаткових умов, які ведуть до перевантаження залізом. |
9.9. Генотип вірусного гепатиту С
|
Стійкого зв’язку між генотипом ВГС та прогресуванням хвороби у кількох когортних дослідженнях виявлено не булo.88, 91, 92, 116, 117 |
2+ |
9.10. Кріоглобулінемія
|
Метааналіз низької якості щодо впливу кріоглобулінемії припускає, що цироз частіше діагностується у пацієнтів із кріоглобулінемією.118 |
1– |
Х. Лікування хронічного гепатиту С
10.1. Противірусна терапія
|
Кілька метааналізів і систематичних оглядів підтверджують, що комбінація пегільованого ІФН з рибавірином ефективна при лікуванні пацієнтів з ХГС, що призводить до високого рівня СВВ.7, 119–121 Всі пацієнти повинні розглядатися як кандидати на лікування. |
1+ |
|
A |
Всі пацієнти з хронічною ВГС-інфекцією повинні розглядатися на противірусну терапію. |
Коментар робочої групи
В окремих клінічних ситуаціях лікування пегільованими інтерферонами може бути протипоказане: алергічні реакції на рекомбінантні інтерферони, поява антитіл до рекомбінантного інтерферону, гематологічні зміни (нейтропенія, тромбоцитопенія як наслідок лікування вірусного гепатиту С), онкогематологічна патологія, вагітність, перші роки життя дитини. Тоді доцільно розглянути використання непегільованого інтерферону альфа.
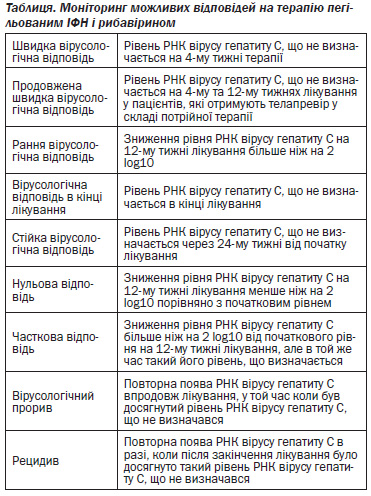
10.1.1. Стійка вірусологічна відповідь
Стійка вірусологічна відповідь стала прийнятою ціллю програм лікування ХГС і в даний час досягнута у 41–51 % пацієнтів з генотипом 1 і у 73–82 % пацієнтів з генотипом 2 і 3, які отримали курс комбінованої терапії пегільованим ІФН і рибавірином.122, 123 Є певні дані, але їх небагато, щодо довготривалих результатів після СВВ, якості та тривалості спостереження:
|
— вірусологічний рецидив рідко трапляється після СВВ (у 1–13 % пацієнтів);124–126 |
1+ |
|
— знижений рівень смертності після СВВ;127 |
2+ |
|
— пацієнти з СВВ мають знижений ризик розвитку цирозу та первинної гепатоклітинної карциноми.124, 128 |
2++ |
|
— латентний гепатит С може зберігатися в макрофагах, лімфоцитах або гепатоцитах у деяких пацієнтів, які досягли СВВ. При цьому може бути невеликий ризик рецидиву у майбутньому у наведених вище випадках.129, 130 |
3 |
|
В |
Стійка вірусологічна відповідь повинна використовуватися у якості маркера для кліренсу вірусу. |
|
СВВ 80 % досягається у пацієнтів, які приймають 80 % дози пегільованого ІФН та рибавірину впродовж понад 80 % часу, що можна зіставити з 33 % у пацієнтів, які менше дотримуються лікування.131 |
2+ |
An update on the management of chronic hepatitis C: Consensus guidelines from the Canadian Association for the Study of the Liver (2012)
10.2. Варіанти лікування за генотипами
10.2.1. Генотип 1 і тривалість лікування
|
Систематичний огляд оцінив додаткову терапію інгібіторами протеази боцепревіром і телапревіром у пацієнтів з гепатитом С генотипу 1. Як у раніше нелікованих, так і у лікованих пацієнтів стійка вірусологічна відповідь частіше досягалася при застосуванні інгібіторів протеази боцепревіру або телапревіру в складі потрійної терапії пегільованим ІФН і рибавірином з урахуванням маси тіла порівняно лише з пегільованим ІФН і рибавірином з урахуванням маси тіла. Обидва препарати добре переносилися, причому анемія була найбільш обмежуючим лікування побічним ефектом.132 Рис. 1 і 2 показують алгоритми лікування пацієнтів з ВГС генотипу 1. |
1+ |
|
Три РКД, які розглядалися у двох систематичних оглядах, виявили, що застосування тела– |
|
|
превіру впродовж принаймні 12 і максимум 48 тижнів у комбінації з пегільованим ІФН і рибавірином з урахуванням маси в якості потрійної терапії було ефективним в лікуванні раніше нелікованих або лікованих дорослих з хронічним гепатитом С генотипу 1. Випробування включало раніше лікованих дорослих, які відповіли, частково відповіли і мали рецидив після лікування пегільованим ІФН і рибавірином з урахуванням маси. Стійка вірусологічна відповідь (СВВ) була значно кращою, ніж з подвійною |
1+ |
|
терапією пегільованим ІФН і рибавірином з урахуванням маси.133, 134 |
|
|
Два систематичних огляди виявили, що боцепревір упродовж 24–44 тижнів в якості потрійної терапії в поєднанні з пегільованим ІФН і рибавірином на основі маси впродовж 48 тижнів був ефективним у лікуванні раніше нелікованих або лікованих дорослих з хронічним гепатитом C генотипу 1. Ці дослідження включали раніше лікованих дорослих, які частково відповіли або мали рецидив після лікування |
1+ |
|
пегільованим ІФН і рибавірином з урахуванням маси, але не включали пацієнтів, які раніше не відповіли на лікування. Стійка вірусологічна відповідь була значно кращою, ніж з подвійною терапією пегільованим ІФН і рибавірином з урахуванням маси; 66 % з потрійною терапією фіксованої тривалості порівняно з 63 % з потрійною терапією залежно від відповіді порівняно з 38 % у контрольній групі, яка отримувала стандартну подвійну терапію.134, 135 |
|
Схема, яка включає боцепревір, потребує чотиритижневого підготовчого лікування пегільованим ІФН і рибавірином з урахуванням маси, в той час як телапревір цього не потребує. Підготовче лікування боцепревіром, проте, не знижує СВВ. Відповідь на підготовче лікування може вказувати на ймовірність СВВ при лікуванні як раніше нелікованих, так і лікованих пацієнтів.
Коментар робочої групи:
Станом на 20.10.2013 року телапревір не зареєстрований в Україні.
|
A |
Всіх нелікованих пацієнтів, інфікованих ВГС генотипу 1, необхідно розглядати на отримання лікування пегільованим ІФН і рибавірином з урахуванням маси тіла з додаванням інгібітору протеази в якості потрійної терапії. |
|
A |
Всіх раніше лікованих пацієнтів, інфікованих ВГС генотипу 1, необхідно розглядати на лікування пегільованим ІФН і рибавірином з урахуванням маси тіла з додаванням інгібітору протеази в якості потрійної терапії. |
|
- |
У раніше лікованих пацієнтів з низькою ймовірністю СВВ користь від лікування необхідно зважувати проти потенційних ризиків і побічних ефектів. |
|
A |
Терапія залежно від відповіді може використовуватися тільки в нелікованих пацієнтів і пацієнтів із рецидивом, які не мають цирозу, після попереднього лікування. |
Немає прямих порівняльних досліджень боцепревіру і телапревіру, тому жоден препарат не може бути рекомендований більше, ніж інший.
Немає жодних доказів, що припускають, що певний пегільований ІФН слід використовувати у комбінації з певним інгібітором протеази.
10.2.2. Генотип 1 і тривалість лікування пацієнтів, які не підходять для лікування інгібіторами протеази
|
Оптимальна тривалість лікування пацієнтів з гепатитом С генотипу 1 становить 48 тижнів.7, 119, 120 |
1+ |
|
Пацієнти з інфекцією генотипу 1, які не змогли досягти ранньої вірусологічної відповіді (РВВ) через 12 тижнів, мають менше 5 % шансів досягнення РВВ.136 З пацієнтів з інфекцією генотипу 1, які не змогли досягти РВВ, але продовжували лікування і залишалися позитивними на ВГС РНК впродовж 24 тижнів, жоден не мав РВВ.137 Після ретельної клінічної оцінки деяких пацієнтів, інфікованих ВГС генотипу 1, можна вважати непридатними для лікування за схемою, яка включає інгібітор протеази. До них |
1+ |
|
належать пацієнти з потенційно небезпечними взаємодіями призначених або недозволених засобів і пацієнти із супутніми захворюваннями, які гірше дотримуються лікування, що може знизити ефективність потрійної терапії і збільшити ризик розвитку медикаментозної резистентності.134 |
|
|
Дослідження для реєстрації телапревіру і боцепревіру в post hoc аналізі продемонстрували, що пацієнти з низьким вірусним навантаженням, ліковані пегільованим ІФН і рибавірином з урахуванням маси, які досягли швидкої вірусологічної відповіді (ШВВ), мають однакову частоту СВВ, як і пацієнти, які отримували лікування з додаванням інгібітору протеази.138 Метааналіз розглядав скорочення строку лікування пацієнтів, які отримували пегільований ІФН і рибавірин з урахуванням маси. Загалом серед усіх пацієнтів частота рецидивів була значно вищою серед пацієнтів з ШВВ генотипу 1, якщо тривалість лікування була скорочена до 24 тижнів із загальним зниженням СВВ на –13,6 % (95% ДІ від –22,8 до –4,4 %, р = 0,004). Якщо вірусне навантаження було менш 400 000 МО/мл, не було статистично значущого зниження СВВ при 24-тижневому лікуванні з середньою різницею в –3,1 % (96% ДІ від –8,6 до 2,4 %).138 |
1+ |
|
A |
— Пацієнтів з інфекцією генотипу 1 необхідно перевірити на РВВ на 12-му тижні. — У пацієнтів з інфекцією генотипу 1, які не досягли РВВ на 12-му тижні, необхідно розглянути припинення лікування. — Пацієнти з інфекцією генотипу 1 з РВВ на 12-му тижні повинні продовжувати лікування впродовж 48 тижнів. Пацієнти, позитивні на ВГС РНК впродовж 24 тижнів, повинні припинити лікування. |
|
В |
Після поінформованого обговорення неліковані пацієнти з інфекцією генотипу 1 та: — з мінімальним або нульовим фіброзом; — з низьким вірусним навантаженням (менше 400 000 МО/мл); — ті, хто досяг ШВВ після попереднього лікування пегільованим ІФН і рибавірином з урахуванням маси впродовж чотирьох тижнів, можуть розглядатися на 24-тижневе лікування без додавання інгібітору протеази. |
An Update on Treatment of Genotype 1 Chronic Hepatitis C Virus Infection: 2011 Practice Guideline by the American Association for the Study of Liver Diseases (AASLD)
Рекомендації:
1. Оптимальна терапія для генотипу 1 хронічного гепатиту С включає використання боцепревіру або телапревіру в комбінації з пегінтерфероном альфа і рибавірином (клас 1, рівень А).
2. Боцепревір та телапревір не повинні використовуватися без пегінтерферону альфа і рибавірину (клас 1, рівень А).
10.2.3. Генотип 2 і 3 і тривалість лікування
|
Оптимальним лікуванням пацієнтів з інфекцією генотипу 2 і 3 є пегільований ІФН і рибавірин з урахуванням маси.7, 119, 120 В якості первинного результату один метааналіз порівнював показники СВВ у пацієнтів з інфекцією генотипу 2 або 3. Через 24 тижні терапії показники СВВ склали 74 і 69 % відповідно, з СШ 1,49 (95% ДІ від 1,23 до 1,80), проте відсоткова різниця не була значущою (р = 0,90). У пацієнтів з вищим вірусним навантаженням показники ШВВ з інфекцією генотипу 2 (75 %) відрізнялися від показників генотипу 3 (58 %) з СШ 2,36 (95% ДІ 1,80 до 3,09). Різниця у відсотках в 24,9 % (95% ДІ від 12,8 до 37,0, р = 0,07) не була значущою. У пацієнтів з низьким вірусним навантаженням відповідні показники були 79 і 75 % з СШ 1,50 (95% ДІ від 1,08 до 2,09), знову ж таки, з незначною різницею (р = 0,84). В якості вторинного результату аналізували скорочений строк терапії у пацієнтів з ШВВ, які отримували лікування впродовж 12–16 або 24 тижнів. ШВВ у пацієнтів з інфекцією генотипу 2 була 83 і 84 % відповідно, а у пацієнтів з інфекцією генотипу 3 склала 84 і 86 %. У пацієнтів без ШВВ, які отримували лікування впродовж 24 тижнів, ШВВ була вище у пацієнтів з інфекцією генотипу 2, з 17,8% зваженою різницею (95% ДІ: від 8,7 до 27,0) та загальним СШ 2,06 (95% ДІ від 1,40 до 3,02). Автори дійшли висновку, що лікування впродовж 24 тижнів повинно залишатися стандартним строком для пацієнтів з інфекціями генотипу 2 або 3. Проте серед пацієнтів, які досягають ШВВ, пацієнти з ВГС генотипу 3 відповіли на скорочене лікування, а також пацієнти з генотипом 2 незалежно від початкової віремії.139 |
1+ |
|
Метою другого метааналізу було визначення оптимальної тривалості лікування у хворих з генотипами 2 і 3. Результати цих двох генотипів об’єднували. Об’єднані дані СВВ були вищими при стандартному лікуванні в РКД, які рандомізовані на початку дослідження з СШ 0,88 (95% ДІ від 0,76 до 1,01) на користь стандартної терапії порівняно зі скороченою терапією. Об’єднана пропорція показників СВВ РКД, рандомізованих при ШВВ, була аналогічною в групі скороченого лікування (82 %) і в групі стандартного лікування (83 %) із загальним ефектом із ВР 1,00 (95% ДІ від 0,92 до 1,09). До висновків авторів слід ставитися з обережністю, враховуючи відсутність деталей методології та високий рівень гетерогенності включених досліджень. Автори роблять висновок, що на основі вихідних характеристик усі пацієнти повинні отримувати подвійну терапію впродовж 24 тижнів. Проте в пацієнтів, які досягнуть ШВВ через чотири тижні їх лікування, може бути скорочено до 12–16 тижнів подвійної терапії пегільованим ІФН і рибавірином з урахуванням маси. Вони не виявили жодної різниці між лікуванням 12 або 16 тижнів, |
1+ |
|
але кількість була невеликою. Кількість пацієнтів з цирозом була надто невеликою, щоб можна було зробити будь-який висновок щодо цієї групи. Рибавірин з урахуванням маси досяг вищих показників СВВ, ніж рибавірин у низьких фіксованих дозах.140 |
|
|
Дані з двох досліджень показують, що у пацієнтів з інфекцією генотипу 2 або 3, які досягли швидкої вірусологічної відповіді (ВГС РНК-негативна) через чотири тижні, можуть отримувати пегільований ІФН і рибавірин з урахуванням маси впродовж 12 або 16 тижнів з аналогічними результатами, що і лікування впродовж 24 тижнів.141, 142 |
1+ |
|
A |
У пацієнтів з генотипом 2 або 3 стандартним лікуванням має бути пегільований ІФН і рибавірин з урахуванням маси впродовж 24 тижнів. |
|
В |
Пацієнти без цирозу печінки з генотипом 2 або 3, які досягли ШВВ через 4 тижні терапії, можуть бути розглянуті на скорочену терапію від 12 до 16 тижнів. |
An update on the management of chronic hepatitis C: Consensus guidelines from the Canadian Association for the Study of the Liver (2012)
Скорочення строків лікування не слід розглядати у пацієнтів з ко-факторами, що знижують ймовірність успіху лікування (наприклад, виражений фіброз, негроїдна раса, ожиріння, метаболічний синдром/інсулінорезистентність), навіть якщо ШВВ досягнута. Якщо у пацієнта після скороченого курсу лікування виник рецидив, слід розглянути можливість повторного 24-тижневого курсу лікування (клас 1, рівень А).
У пацієнтів, які інфіковані генотипом 3, які не досягли ШВВ, але досягли РВВ, лікування повинно бути продовжено до 36–48 тижнів, особливо в умовах ко-факторів, які знижують ймовірність успішності лікування (клас 2а, рівень С).
10.2.4. Генотип 4, 5, 6 і тривалість лікування
|
Оптимальна тривалість лікування пацієнтів з генотипом 4 гепатиту С становить 48 тижнів.7, 119, 120 |
1++ |
|
Мета-аналіз двох великих РКД третьої/четвертої фаз, проведених у Бельгії у пацієнтів з хронічним гепатитом С (n = 1073), порівнює відповіді на противірусну терапію пацієнтів з вірусом генотипу 5, з відповіддю у пацієнтів з іншими генотипами ВГС. Дослідження показало, що інфекція генотипу 5 відповідає на терапію аналогічно генотипу 1, проте популяція з генотипом 5 старша за віком, більш імовірно, має набуту інфекцію при переливанні крові і частіше має цироз печінки. У мета-аналізі рекомендували лікування пацієнтів з інфекцією генотипу 5 впродовж 48 тижнів подвійною терапією.143 |
1+ |
|
Систематичний огляд знайшов дуже мало досліджень із лікування хворих з інфекцією генотипу 6. Лікування пегільованим ІФН і рибавірином з урахуванням маси є ефективним з показниками |
|
|
СВВ близько 70 % після 48 тижнів терапії. Показники СВВ аналогічні в пацієнтів з інфекцією генотипу 6, які отримують пегільований ІФН і рибавірин з урахуванням маси 24 тижні, хоча необхідні додаткові дослідження, перш ніж рекомендувати 24 тижні як оптимальну тривалість лікування цих пацієнтів.144 |
1+ |
|
А |
Для пацієнтів з інфекцією генотипу 4, 5 або 6 стандартне лікування повинно тривати 48 тижнів пегільованим ІФН і рибавірином з урахуванням маси. |
10.3. Підгрупи пацієнтів
10.3.1. Пацієнти з легкою формою хронічного гепатиту
|
У пацієнтів з легкою формою ХГС ефективність і безпека комбінованої терапії непегільованим інтерфероном і рибавірином аналогічна ефективності й безпеці в інших пацієнтів з гепатитом С. Таким чином, біопсія печінки, щоб виключити пацієнтів із легкою формою захворювання, не потрібна перед розглядом питання про противірусне лікування.145 |
1++ |
|
А |
Пацієнти з легкою формою ХГС повинні розглядатися на отримання лікування. |
10.3.2. Пацієнти з цирозом
Див. Розділ 11.1.1 щодо інформації про пацієнтів з цирозом.
10.3.3. Пацієнти з нормальною активністю АЛТ
|
Ефективність та безпека комбінованої терапії пегільованими інтерферонами та рибавірином у пацієнтів із ХГС із нормальними рівнями активності АЛТ аналогічна ефективності й безпеці у пацієнтів із підвищеним рівнем активності АЛТ. (див. розділ 9.5)146 |
1+ |
|
А |
Пацієнти з хронічним гепатитом С і нормальним рівнем активності АЛТ повинні розглядатися на лікування. |
10.3.4. Пацієнти з ко-інфекцією ВІЛ
|
Пегільований ІФН і рибавірин впродовж 48 тижнів ефективні в лікуванні пацієнтів із ВГС і супутньою ВІЛ-інфекцією. Їх застосування призвело до стійкої вірусологічної відповіді у 60 % пацієнтів з генотипом 2 і 3 та у 14–29 % пацієнтів із генотипом 1. У пацієнтів з генотипом 1 і низьким вірусним навантаженням (< 800 000 МО/мл) показник стійкої вірусологічної відповіді становив близько 60 %.147–149 |
1+ |
|
98 % пацієнтів з супутніми ВІЛ/ВГС, які не мали РВВ на 12-му тижні, не досягли СВВ на 48–му тижні.149 |
1+ |
|
Пацієнти з ко-інфекцією ВІЛ і ВГС генотипу 2 і 3, у яких не визначається РНК ВГС на 4-му тижні, не отримають користі від терапії тривалістю понад 24 тижні.150 |
1+ |
|
Пегільований ІФН плюс рибавірин з урахуванням маси для лікування ВГС був більш ефектив |
|
|
ним, ніж стандартний ІФН плюс рибавірин з урахуванням маси в досягненні стійкої вірусологічної відповіді в пацієнтів з ко-інфекцією ВІЛ: 55 % проти 26 % у цілому, 46 % проти 18 % при генотипі 1 і 4, і 71 % проти 43 % при генотипі 2 і 3. Різниця між когортами залежала від генотипу ВГС у перші 12 тижнів терапії пегільованим ІФН, незалежно від статусу ВІЛ. Серед пацієнтів із генотипом вірусу 2 або 3 дослідження показало значно більш різке зменшення рівня РНК ВГС у пацієнтів з моноінфекцією ВГС порівняно з ВГС ВІЛ-інфікованими пацієнтами тільки на 4-му тижні, в той час як значні відмінності серед пацієнтів з ВГС генотипу 1 спостерігалися тільки після 12 тижнів лікування. В цілому більш тривале лікування (48–72 тижні) показало кращі відповіді на лікування незалежно від генотипу, ніж більш коротка тривалість лікування (24–48 тижнів).150–152 |
1+ |
|
Думка експертів групи з розробки настанови полягала в тому, що можливо зробити рекомендації стосовно лікування хворих із ко-інфекцією ВІЛ і ВГС генотипу 1 шляхом екстраполяції схем лікування пацієнтів з моноінфекцією ВГС генотипу 1, які включають інгібітори протеази. |
|
|
А |
Усі пацієнти з ко-інфекцією ВІЛ і ВГС повинні бути розглянуті на лікування гепатиту. |
|
А |
У пацієнтів з 1-м генотипом ВГС і ВІЛ-інфекцією, які не досягають РВВ, лікування необхідно припинити. |
|
А |
— Пацієнтам з ко-інфекцією не 1-го генотипу, які вважаються придатними для лікування, пропонується лікування пегільованим ІФН і рибавірином з урахуванням маси впродовж 48 тижнів. — Пацієнти з ко-інфекцією генотипу 2 або 3, які досягли ШВВ, можуть розглядатися на лікування впродовж 24 тижнів. |
|
С |
Усі пацієнти з ко-інфекцією ВІЛ і ВГС генотипу 1 повинні бути розглянуті на лікування за схемою, яка включає інгібітори протеази ВГС. |
|
В |
Неліковані пацієнти з ко-інфекцією ВІЛ і ВГС генотипу 1, яким не підходить лікування за схемою, яка включає інгібітори протеази ВГС, повинні бути розглянуті на лікування пегільованим ІФН і рибавірином з урахуванням маси впродовж 48–72 тижнів залежно від вірусологічної відповіді. |
|
- |
Пацієнти з ко-інфекцією генотипу 1, не вилікувані від гепатиту, повинні контролюватися щодо прогресування захворювання. |
10.3.5. Пацієнти з ко-інфекцією гепатиту В
|
Результати лікування комбінацією непегільованого ІФН і рибавірину в пацієнтів з ко-інфекцією хронічним гепатитом В і С аналогічні результатам, досягнутим у пацієнтів з моноінфекцією ВГС.153, 154 Жодного дослідження не було знайдено, яке б вивчило взаємодію пегільованого інтерферону і рибавірину у пацієнтів з ко-інфекцією хронічним гепатитом В і С. |
2++ |
Не знайдено ніяких доказів, щоб зробити рекомендації з лікування інгібіторами протеази пацієнтів з генотипом 1 і з ко-інфекцією гепатиту В, оскільки ці пацієнти були виключені з клінічних досліджень.
|
С |
Пацієнти з ко-інфекцією хронічного гепатиту В та С повинні розглядатися на отримання комбінованої терапії пегільованим інтерфероном і рибавірином з урахуванням маси. |
|
- |
Пацієнти з хронічним гепатитом В і ко-інфекцією С генотипу 1 можуть бути розглянуті на комбіноване лікування пегільованим ІФН і рибавірином з урахуванням маси з додаванням інгібітору протеази на індивідуальній основі в центрах, які мають досвід в лікуванні гепатиту В. |
10.3.6. Пацієнти в програмах лікування наркозалежності
|
У пацієнтів з ХГС, які беруть участь в стабільній програмі лікування наркозалежності, лікування комбінацією пегільованого ІФН і рибавірину є ефективним і призводить до високого рівня СВВ. У той же час показник відмов від лікування вищий, ніж в інших когортах, відмови трапляються раніше, зазвичай протягом перших восьми тижнів. Після восьми тижнів прийому препаратів дотримання лікування аналогічне дотриманню лікування в інших групах.44, 155 |
2++ |
|
Останні дослідження показали, що пацієнти, які активно вживають наркотики, мають аналогічні результати лікування, як і ті, хто не вживає наркотиків. 156–158 |
2+1+ |
|
С |
Пацієнти із ХГС, які беруть участь в програмі лікування наркозалежності, можуть розглядатися для лікування. |
|
- |
Активні споживачі наркотиків мають залучатися до заходів із забезпечення медичної допомоги та зниження шкоди здоров’ю. |
|
- |
Активні споживачі наркотиків повинні мати комплексну оцінку їх психологічних потреб та ймовірність дотримання противірусного лікування. |
An update on the management of chronic hepatitis C: Consensus guidelines from the Canadian Association for the Study of the Liver (2012)
Рішення лікувати споживачів ін’єкційних наркотиків, які хворі на ВГС, з недавнім або активним вживанням наркотиків має прийматися в індивідуальному порядку досвідченими докторами, в ідеалі — в умовах міждисциплінарного консенсусу. Навчання застосуванню на практиці стратегій зменшення шкоди є незамінним компонентом світової практики лікування цих пацієнтів (клас 1, рівень С).
10.4. Фактори, що впливають на ефективність
10.4.1. Вік, стать, етнічна приналежність
|
Противірусна терапія менш ефективна у пацієнтів віком понад 40 років; чоловіки рідше, ніж жінки, досягають СВВ.7 ,119, 120 У пацієнтів різних |
|
|
рас спостерігалися певні розбіжності у відповіді на противірусну терапію. Мета-аналіз різних етнічних груп показав, що пацієнти афроамериканського чи латиноамериканського походження мали нижчий показник СВВ порівняно з білими або азіатськими групами (16 і 24 % проти 32 і 59 % з генотипом 1 досягли СВВ).159 |
1+ |
|
А |
Пацієнти мають знати, що старший вік на початку лікування знижує ймовірність СВВ. |
|
В |
Пацієнти мають знати про ймовірність СВВ відповідно до їх етнічної групи. |
10.4.2. Маса тіла
|
Три систематичні огляди повідомляють, що у пацієнтів з ХГС, вага яких понад 75 кг, лікування комбінацією пегільованого ІФН і рибавірину призводить до нижчої СВВ, ніж у пацієнтів з масою тіла до 75 кг.7, 119, 120 Дозування пегільованих ІФН і рибавірину в цих дослідженнях було визначено для маси 75 кг і не пов’язувалося зі справжньою вагою, тому слід проявляти обережність при екстраполяції результатів. Питання маси та дієти обговорюються в розділі 12. |
1+ |
10.4.3. Алкоголь
|
Дослідження з лікування пацієнтів, які продовжують вживати алкоголь, обмежені. Два когортних дослідження показали, що відповідь на стандартне лікування інтерферонами була обернено пропорційна кількості вжитого алкоголю.160, 161 Утримання від алкоголю протягом 6 місяців не змінило показники від колишнього вживання алкоголю.162 |
2+ |
|
- |
Пацієнти мають знати, що вживання алкоголю (навіть помірне) може знизити відповідь на лікування пегільованим інтерфероном і рибавірином. |
10.5. Протипоказання
10.5.1. Вагітність та ризик вагітності
Немає досліджень про вплив противірусної терапії на вагітність жінки. Дослідження на тваринах показали, що рибавірин у набагато нижчій від рекомендованої дози порівняно з людиною викликає вади розвитку плода. Частота і важкість тератогенного ефекту збільшується з підвищенням дози рибавірину. Виживання плоду і потомства знижується.163 Подальші дослідження на тваринах показали відхилення в спермі.163
Даних про застосування пегільованого інтерферону у вагітних жінок немає, і невідомо, чи пегільований ІФН або рибавірин виводяться з організму через жіноче молоко.
|
- |
Пегільований ІФН і рибавірин не повинні призначатися вагітним жінкам. |
|
- |
Лікування пегільованим ІФН і рибавірином не повинно починатися до моменту виключення ймовірності наявної вагітності. |
|
- |
Пари, в яких один з партнерів отримує пегільований ІФН і рибавірин, повинні використовувати дві форми контрацепції впродовж лікування і ще 6 місяців після завершення терапії. |
10.5.2. Пацієнти з нирковою недостатністю
|
Рибавірин викликає залежну від дози гемолітичну анемію, а ступінь гемолізу залежить від важкості ниркової недостатності.164 Може розглядатися лікування пегільованим ІФН у якості монотерапії в дозі 135 мкг підшкірно на тиждень у пацієнтів, які перебувають на гемодіалізі, але такі пацієнти потребують ретельного спостереження.165 |
1+ 3 |
|
D |
Пацієнти з ХГС та нирковою недостатністю можуть отримувати лікування ІФН в якості монотерапії з ретельним моніторингом. |
10.5.3. Пацієнти з психічними розладами
|
Пацієнти з проблемами психічного здоров’я мають хорошу відповідь на терапію ІФН і рибавірином, але необхідно ретельно спостерігати за їх психічними симптомами, особливо у перші чотири тижні лікування.166, 167 |
2+ 3 |
|
В |
У пацієнтів зі стійкими психічними проблемами не повинно виключатися лікування ХГС. |
|
В |
У пацієнтів з психічними розладами необхідно забезпечити моніторинг їх психічних симптомів до початку і під час лікування ІФН. |
|
- |
При необхідності слід розглядати проведення офіційної психіатричної оцінки. |
10.5.4. Пацієнти, які приймають інші ліки
|
Інгібітори протеази телапревір і боцепревір є як інгібіторами, так і субстратами метаболізуючого ферменту цитохрому Р450 (CYP) 3А4. Одночасне введення телапревіру або боцепревіру з ліками, які метаболізуються цим ферментом, може призвести до клінічно значущих і, можливо, небезпечних для життя лікарських взаємодій. У зв’язку з потенційною можливістю токсичності та/або субоптимального лікування особливу увагу слід приділяти вивченню повної історії застосування ліків у всіх пацієнтів (включаючи призначені ліки, засоби, що відпускаються без рецепта, трав’яні і/або заборонені препарати).134, 168 Необхідно здійснити оцінку, щоб гарантувати, що одночасне введення не призведе до будь-яких клінічно значущих змін у метаболізмі ліків. В якості основних джерел інформації слід звертатися до довідкових матеріалів, таких як короткі характеристики препарату і веб-сайт Університету гепатиту С Ліверпуля щодо взаємодії препаратів.169 Проте всі можливі джерела достовірної інформації повинні бути використані для запобігання проблемам з лікарських взаємодій. У пацієнтів зі складними схемами лікування слід розглянути направлення до спеціаліста фармацевта, щоб врахувати всі складні взаємодії адекватно. Провайдери первинної медичної допомоги повинні бути попереджені про можливість взаємодії, повідомляючи результати оглядів лікарських засобів. У пацієнтів, у яких призначені і заборонені препарати протипоказані одночасно |
4 |
|
з інгібіторами протеази, лікування з застосуванням пегільованого ІФН і рибавірину повинно проводитися тільки після консультації з місцевою мультидисциплінарною командою.134 |
|
Слід дотримуватися обережності при одночасному призначенні інгібіторів протеази з препаратами, які пролонгують інтервал QT. Інформація з призначення окремих препаратів забезпечує інструкцію з моніторингу ЕКГ. Можуть бути залучені інші механізми метаболізму ліків, але ще не визначені і консультантам слід бути пильними. При одночасному призначенні інших ліків необхідно дотримуватися обережності і здійснювати ретельний моніторинг.
|
D |
У пацієнтів слід взяти повну історію застосування лікарських засобів, в тому числі призначених, тих, що відпускаються без рецепта, і заборонених препаратів. |
|
D |
Одночасне введення будь-яких ліків повинно бути оцінене для забезпечення відсутності неприйнятної потенційної токсичності або субоптимальної ефективності кожного засобу. |
|
- |
Пацієнти зі складною поліпрагмазією можуть отримати користь від консультації зі спеціалістом-фармацевтом. |
|
- |
Пацієнти повинні бути поінформовані про потенційно небезпечні взаємодії між ліками, які відпускаються без рецепта, забороненими препаратами і лікуванням гепатиту С, навіть якщо невідомо, що вони вживають заборонені препарати. |
An update on the management of chronic hepatitis C: Consensus guidelines from the Canadian Association for the Study of the Liver (2012)
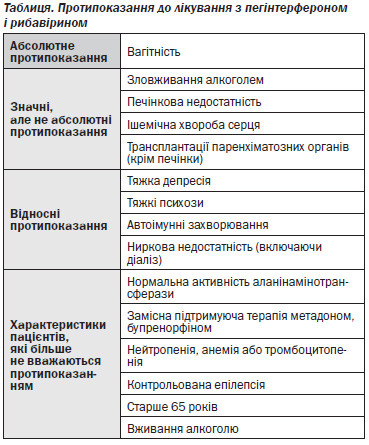
10.6. Ведення побічних ефектів
10.6.1. Грипоподібні симптоми
|
Практично всі пацієнти, які приймають пегільований ІФН і рибавірин, мають грипоподібні симптоми, такі як лихоманка, м’язові болі, озноб, біль у суглобах і головний біль. Ці симптоми, як правило, полегшуються після першого місяця лікування.170 Прості втручання, такі як застосування парацетамолу, більше споживання рідини та відпочинок можуть мінімізувати ці ефекти.170, 171 |
4 |
|
D |
Пацієнти, у яких спостерігаються грипоподібні побічні ефекти внаслідок прийому пегільованого ІФН і рибавірину, можуть приймати парацетамол відповідно до інструкцій виробника. |
|
D |
Пацієнтам необхідно рекомендувати підтримувати відповідний рівень споживання рідини впродовж лікування пегільованим ІФН і рибавірином. |
|
D |
Пацієнтам необхідно рекомендувати узгодити свої ін’єкції пегільованого ІФН і рибавірину з періодами зниженої активності, наприклад, вихідні або свята. |
10.6.2. Анемія та нейтропенія
|
У клінічних випробуваннях застосування ЕП у пацієнтів, у яких розвинулася анемія (рівень гемоглобіну < 120 г/л) впродовж прийому пегільованого ІФН і рибавірину, поліпшили показники анемії і зменшили необхідність зниження дози рибавірину. Крім того, поліпшилася якість життя.172, 173 Немає прямих доказів того, що це призводить до збільшення СВВ. Жоден з ЕП на даний час не ліцензований для такого призначення. |
1+ |
|
Рівень гемоглобіну повинен підтримуватися на рівні, який не допускає необхідності зниження дози або припинення застосування пегільованого ІФН і рибавірину, оскільки це може призвести до зниження СВВ.174 Майже у третини пацієнтів, які отримували комбіновану терапію, розвивається анемія, і в 13 % зниження гемоглобіну менш ніж до 100 г/л. З додаванням інгібіторів протеази до лікування пегільованим ІФН і рибавірином анемія може бути частіше і серйозніше, що спостерігається в перші кілька тижнів лікування.174 РКД порівнювало застосування ЕП в якості терапії першої лінії для підтримки гемоглобіну, зі зниженням дози рибавірину у пацієнтів, які отримують боцепревір. Воно показало, що зниження дози рибавірину підтримувало рівень гемоглобіну і забезпечувало аналогічну СВВ (71 %) у пацієнтів, лікування яких було доповнено ЕП. Цей висновок був підтверджений у пацієнтів з цирозом175 і в третій фазі випробування з застосуванням телапревіру в схемах потрійної терапії.176 |
2+ 1+ |
|
Гранулоцитарний колонієстимулюючий фактор (Г-КСФ) може полегшити медикаментозну |
|
|
нейтропенію у пацієнтів, які отримували пегілований інтерферон і рибавірин. Найчастіше він необхідний пацієнтам, які отримують противірусну терапію після трансплантації печінки.177 |
3 |
|
В |
Необхідно розглядати можливість призначення ЕП у пацієнтів з ХГС, які приймають пегільований ІФН і рибавірин і в яких розвинулася анемія, щоб запобігти відміні або зниженню дози рибавірину. |
|
В |
У пацієнтів, які отримували інгібітор протеази в поєднанні з пегільованим ІФН і рибавірином, слід розглянути зниження дози рибавірину в якості альтернативи до додавання EП для контролю анемії. |
|
D |
Гранулоцитарний колонієстимулюючий фактор (Г-КСФ) має розглядатися окремо у кожного пацієнта, у якого розвинулася значна нейтропенія впродовж лікування ХГС пегільованим ІФН та рибавірином, щоб запобігти відміні або зниженню дози пегільованого ІФН |
10.6.3. Депресія
|
Депресія є частим побічним ефектом пегільованого ІФН і рибавірину як у пацієнтів з попередньою депресією, так і в пацієнтів без такої.178 Антидепресанти можуть успішно застосовуватися при депресії, пов’язаній з лікуванням, як превентивний захід перед початком противірусного лікування.166, 179 |
1++ 1+ 3 |
|
В |
Всі пацієнти, які отримують пегільований інтерферон та рибавірин, мають проходити моніторинг на ознаки депресії перед, впродовж та одразу після курсу лікування. |
|
В |
Пацієнти, які отримували лікування пегільованим інтерфероном і рибавірином, з депресією в анамнезі повинні розглядатися на лікування антидепресантами та направлятися до спеціаліста, якщо в цьому є потреба. |
|
- |
Для моніторингу стану депресії слід використовувати затверджений інструмент оцінки (наприклад, шкала госпітальної депресії та неспокою). |
10.6.4. Шкірні реакції
|
Важкі шкірні реакції впродовж прийому пегільованого ІФН або рибавірину зустрічаються рідко, але сухість шкіри, свербіж і дифузні екзематозні ураження зустрічаються приблизно у 20 % пацієнтів.170 Може також посилюватися псоріаз. Реакції в місці ін’єкції виникають більш ніж у 50 % пролікованих пацієнтів.171 Ураження шкіри з’являються найчастіше на кінцівках і області голови та шиї, що свідчить про попереднє сонячне опромінення відкритих сонцю частин тіла.180 Пацієнти добре відповідають на антигістамінні препарати, пом’якшуючі препарати та стероїди місцевої дії, що дозволяє продовжити лікування.180 Показник припинення лікування через дерматологічні побічні ефекти складає приблизно 34 %.181 |
4 3 |
|
Три РКД повідомили про потенційно смертельний висип, один з головних побічних ефектів лікування телапревіром. Він призводить до припинення прийому телапревіру у 5–7 % пацієнтів. Як тільки ліки припиняються, висип зникає (хоча це може зайняти кілька тижнів). Висип переважно екзематозний і сверблячий. У п’ятдесяти відсотків пацієнтів розвивається висип впродовж перших чотирьох тижнів лікування, хоча він може виникнути в будь-який час. Раннє втручання з застосуванням стероїдів місцевої дії зменшує вираженість висипів. Рідко телапревір асоціювався з реакцією на препарати з еозинофілією і системними симптомами (DRESS) або синдромом важких шкірних побічних реакцій на препарати (SCAR), які включають синдром Стівенса — Джонсона і токсичний епідермальний некроліз, які повинні виявлятися, і якщо вони виявлені, терапію слід припинити.182–184 |
1+ 1++ |
|
D |
Всі пацієнти, які отримують пегільований інтерферон і рибавірин, мають отримати рекомендації щодо відповідної гігієни шкіри та її зволоження. |
|
D |
Пацієнтам необхідно рекомендувати утримуватися від перебування на сонці. |
|
D |
Пацієнтам необхідно рекомендувати чергувати місця ін’єкцій препаратів. |
|
D |
Використання пом’якшуючих засобів та відповідних кортикостероїдів може розглядатися як варіант при неспецифічних висипаннях. |
|
А |
Пацієнти, які приймають телапревір, повинні ретельно стежити за висипами, і лікувальні центри повинні мати план ведення висипів. |
|
- |
Застосування антигістамінних препаратів можна розглядати при свербежу. |
|
- |
Пацієнти з важкими дерматологічними реакціями і ті, хто не відповів на лікування першої лінії, повинні направлятися до спеціаліста для дерматологічної оцінки. |
|
- |
Пацієнти, які приймають телапревір, повинні негайно оцінюватися на тяжкість відповідно до відсотка ураженої площі поверхні тіла і наявності системних симптомів. |
|
- |
Пацієнтів з висипами або з проблемами шкіри в анамнезі слід розглядати на лікування боцепревіром, а не телапревіром. |
10.6.5. Дисфункція щитовидної залози
|
У шести відсотків пацієнтів впродовж лікування ІФН розвиваються дисфункції щитовидної залози (як гіпотиреоз, так і гіпертиреоз).150 Жінки мають вищий ризик, особливо ті, хто має аутоантитіла перед початком лікування.185 ІФН-терапія пов’язана з індукцією та підвищенням автоімунних процесів у щитоподібній залозі.186, 187 Аутоантитіла перед початком лікування не є універсальним прогнозом дисфункції щитовидної залози впродовж лікування.170 |
4 1– 2+ |
|
D |
Базовий моніторинг функції щитовидної залози має проводитися перед початком терапії інтерфероном, на 12-му тижні лікування та у будь-який момент, коли виникає підозра дисфункції щитовидної залози. |
|
- |
Пацієнтів, у яких розвивається дисфункція щитовидної залози, слід направляти на консультацію до ендокринолога |
10.6.6. Втрата маси
|
Хронічний гепатит С призводить до прискорення основного метаболізму у пацієнтів без цирозу.188 Втрата маси зазвичай спостерігається у пацієнтів на противірусному лікуванні.170, 171, 189 Дієтотерапія у пацієнтів з ВГС обговорюється в розділі 12.1. |
2– 4 |
10.6.7. Диспное
|
Диспное рідко спостерігається як побічний ефект лікування пегільованим інтерфероном і рибавірином. Диспное може статися в результаті лікування анемії, але також може бути викликано більш серйозними серцево-судинними і респіраторними захворюваннями.170, 171, 190 |
2– 4 |
|
D |
Пацієнти, які лікуються пегільованими інтерферонами та рибавірином, у яких спостерігається диспное, не пов’язане з анемією, мають негайно пройти медичне обстеження на виявлення серцево-легеневих захворювань. |
10.6.8. Ретинопатія
|
Ретинопатія в період лікування ІФН є поширеним явищем, але, як правило, проходить у м’якій формі і швидко минає. Зникає спонтанно після припинення лікування ІФН, рідко потребує лікування. Довгострокові наслідки невідомі.191 Пацієнти з гіпертонією або діабетом схильні до більшого ризику розвитку ретинопатії.171 Інші наслідки з офтальмологічної сторони є рідкістю. |
1+ 4 |
|
D |
Пацієнти з ХГС і гіпертонією або діабетом повинні пройти офтальмологічне обстеження до початку лікування, звертаючи особливу увагу на схожі на вату плями і крововилив у сітківку. |
|
D |
Будь-який пацієнт, який скаржиться на порушення зору впродовж лікування, має бути оглянутий офтальмологом. |
|
D |
Прийом ІФН необхідно припинити, поки у пацієнта з порушенням зору не зникнуть ці порушення або поки офтальмолог не підтвердить відсутність ураження сітківки |
10.6.9. Алопеція
|
Алопеція — це доволі поширене побічне явище впродовж прийому ІФН та рибавірину. Після припинення лікування волосся відростає знову.170, 171 |
4 |
|
D |
Пацієнтам необхідно повідомити, що після припинення лікування волосся відросте знову. |
10.6.10. Інші побічні ефекти
Інші побічні ефекти включають безсоння, зниження концентрації, захворювання порожнини рота, анальний/ректальний дискомфорт, шлунково-кишкові проблеми, зміни смаку, нудоту, симптоми абстиненції після лікування. Не виявлено доказів щодо ефективного їх усунення.
|
Втома є одним з найбільш частих побічних ефектів лікування ІФН або рибавірином і може бути багатофакторною у зв’язку з анемією, гіпотиреозом, порушенням сну і депресією, які впливають на неї.170, 171 |
4 |
10.7. Рецидив чи невдале лікування
10.7.1. Інтерферон та рибавірин
|
Повторне лікування комбінацією пегільованого інтерферону і рибавірину ефективне у пацієнтів з ХГС, у яких було невдалим лікування непегільованим інтерфероном з або без рибавірину, і призводить до стійкої вірусологічної відповіді у певної частини пацієнтів. СВВ є найвищою у пацієнтів, які раніше отримували монотерапію непегільованим ІФН, у інфікованих генотипами 2 або 3, у пацієнтів з рецидивами, а не в пацієнтів з відсутністю відповіді на попереднє лікування і в пацієнтів без цирозу впродовж повторного лікування.192 |
3 |
|
Два випробування, які досліджували повторне лікування пацієнтів з генотипом 1 ВГС, у яких лікування було раніше невдалим, показали, що існує значна користь від повторного лікування пегільованим ІФН і рибавірином з додаванням інгібітору протеази.134 При потрійній терапії з телапревіром загальна СВВ була 64 % (без підготовки), 66 % (з чотиритижневою підготовкою) і 17 % у контрольній групі подвійної терапії, різниця в 47 % (95% ДІ від 37 до 57, р < 0,001) і 50 % (95% ДІ від 40 до 60, р < 0,001) між потрійною терапією та контрольною групою була значущою.193 Для потрійної терапії боцепревіром загальна СВВ була 59 % (32 тижні потрійної терапії), 66 % (44 тижні потрійної терапії ) і 21 % у контрольній групі. Різниця на 38 % (95% ДІ від 25,7 до 49,1, р < 0,001) і 45 % (95% ДІ від 33,7 до 56,8, р = 0,001) між потрійною терапією та контрольною групою була значущою.194 |
1+ |
|
D |
Пацієнти з ХГС, у кого було неуспішне лікування непегільованим ІФН та рибавірином, мають розглядатися на повторне лікування пегільованим ІФН та рибавірином. |
|
А |
Пацієнти з ХГС генотипу 1, у яких було невдале будь-яке лікування, повинні розглядатися на застосування основної схеми інгібітору протеази. |
|
- |
Пацієнти з генотипом 2 або 3 ХГС, які потримали субоптимальну терапію, можуть розглядатися на повторне лікування пегільованим IФН і рибавірином впродовж 48 тижнів. |
An Update on Treatment of Genotype 1 Chronic Hepatitis C Virus Infection: 2011 Practice Guideline by the American Association for the Study of Liver Diseases (AASLD)
Для раніше лікованих хворих:
1. Повторне лікування боцепревіром або телапревіром разом із пегінтерфероном альфа і рибавірином на основі маси може бути рекомендоване для хворих з вірусологічним рецидивом або частковою відповіддю після попереднього курсу лікування зі стандартним інтерфероном альфа чи пегінтерфероном альфа і/або рибавірином (клас 1, рівень А).
2. Повторне лікування телапревіром разом з пег-інтерфероном альфа і рибавірином на основі маси може розглядатися для пацієнтів з відсутньою відповіддю на курс стандартного інтерферону альфа чи пег-інтерферону альфа та/або рибавірину на основі маси (клас 2b, рівень В)
3. Терапія на основі відповіді раніше лікованих пацієнтів із використанням режимів на основі боцепревіру або телапревіру може розглядатися для пацієнтів з рецидивом (клас 2a, рівень B для боцепревіру; клас 2b, рівень С для телапревіру), може розглядатися для пацієнтів з частковою відповідю (клас 2b, рівень B для боцепревіру клас 3, рівень С для телапревіру), але не може бути рекомендована для пацієнтів без відповіді на лікування (клас 3, рівень С).
4. Пацієнти, у яких після повторного лікування боцепревіром плюс пегінтерфероном альфа і рибавірином продовжує утримуватися РНК ВГС > 100 МО на 12-му тижні, повинні припинити лікування через високу імовірність розвитку стійкості до противірусних препаратів (клас 1, рівень В).
5. Пацієнти, у яких після повторного лікування телапревіром плюс пегінтерфероном альфа і рибавірином продовжує утримуватися РНК ВГС > 1000 МО на 4 або 12 тижні, повинні припинити лікування через високу ймовірність розвитку стійкості до противірусних препаратів (клас 1, рівень В).
10.8. Моніторинг за пацієнтами, які не отримують лікування
10.8.1. Клінічний огляд
Жодних доказів не було виявлено щодо ефективної практики моніторингу та консультування пацієнтів, які не є кандидатами на лікування або які пройшли неуспішне лікування.
|
- |
Необхідно заохочувати пацієнтів продовжувати спостереження в клініках з метою моніторингу стану здоров’я, обговорення нових схем лікування, якщо вони з’являються. |
|
- |
Пацієнтам необхідно мати доступ до консультування та послуг спеціалізованої медсестри для надання підтримки з питань, що стосуються життя з гепатитом С. |
10.8.2. Роль біопсії печінки
|
Рутинна біопсія печінки протягом або після противірусного лікування не призначається, якщо не потрібна певна конкретна інформація щодо окремих пацієнтів.101 |
1– |
ХІ. Лікування інфекції, що прогресує
11.1. Противірусна терапія
11.1.1. Пацієнти з цирозом
Пацієнти з цирозом поділяються на пацієнтів із компенсованим та декомпенсованим цирозом. Пацієнти з декомпенсацією мають погіршення з розвитком одного або більше ускладнень: жовтяниця, асцит, варикозні кровотечі або енцефалопатія.
|
Є кілька великих добре проведених РКД з інтерферону і рибавірину, пегільованих ІФН з рибавірином, монотерапії пегільованим інтерфероном у пацієнтів з ХГС, які мають високу ймовірність прогресування до термінальної стадії хвороби печінки.122, 123, 195, 196 Підгрупи в рамках цих досліджень мали цироз або запущений фіброз. Рандомізація розподілила їх рівномірно між інтервенціями, так що аналіз підгруп був можливий. Виявилося, що терапія не була більш токсичною для пацієнтів з цирозом печінки порівняно з пацієнтами без цирозу печінки, але була менш ефективною. СВВ були досягнуті у 50–70 % для генотипу 2 і 3 і у 20–30 % для генотипу 1. Подальший систематичний огляд пацієнтів з цирозом підтвердив зниження ризику гепатоцелюлярної карциноми у тих, хто досягнув СВВ (ВР 0,25, 95% ДІ від 0,14 до 0,46, р = 0,00001).97 |
1+ |
|
Хоча і покращені порівняно з попереднім лікуванням, показники СВВ скоріше за все залишаться низькими в пацієнтів із цирозом печінки, які раніше не відповіли, особливо в контексті поганої відповіді на початкове лікування пегільованим ІФН і рибавірином. Лікування цих пацієнтів з інгібіторами протеази, ймовірно, також збільшить розвиток медикаментозно резистентних мутантів, що потенційно ставить під загрозу майбутнє використання противірусних препаратів прямої дії. Таким чином, необхідно приділити серйозну увагу найкращому варіанту лікування для цієї групи. У хворих із вираженим фіброзом або цирозом є незначні тенденції до поліпшення показників СВВ з терапією фіксованої тривалості, але в даний час недостатньо доказів для використання терапії в залежності від відповіді у пацієнтів з цирозом.134 Подальші дослідження ефективності інгібіторів протеази у хворих з цирозом принесли б користь, оскільки основні випробування телапревіру виключають пацієнтів з кількістю тромбоцитів < 90000/мм3.133 |
1+ |
Прямих порівняльних досліджень різних пегільованих ІФН виявлено не було. Довготривала терапія для пацієнтів з цирозом в даний момент досліджується, але наразі результати не опубліковано.
|
A |
Пацієнти з компенсованим цирозом мають розглядатися в якості кандидатів на терапію, якщо не мають протипоказань. |
|
Лікування щотижневими низькими дозами пегільованого ІФН у пацієнтів з цирозом печінки |
|
|
не показало суттєвої різниці в уповільненні прогресування захворювання або зменшенні клінічних результатів у порівнянні з пацієнтами, які не отримували лікування. Не було ніяких відмінностей у розвитку ГЦК, декомпенсації або трансплантації.198, 199 |
1++ |
|
Одне РКД показало, що 48 тижнів ескалації монотерапії пегільованим ІФН у переважно лікованих раніше пацієнтів з цирозом печінки показало зниження загальної смертності і неонкологічної захворюваності; проте це дослідження було недостатньо підтримане і поки що не відтворюється іншими дослідниками.200 Проспективний заданий субаналіз в іншому РКД пацієнтів з портальною гіпертензією показав, що пегільований ІФН затримує суттєві випадки портальної гіпертензії, такі як варикозна кровотеча.201 |
1– 1+ |
|
A |
Пацієнти з компенсованим цирозом ВГС можуть отримати перевагу від лікування ІФН в зниженні ризику розвитку ХГС. Тривалість терапії для досягнення такого ефекту не визначена. |
Для надання рекомендацій з лікування пацієнтів з ВГС та декомпенсованим цирозом недостатньо доказового матеріалу.
11.1.2. Пацієнти, які направляються на трансплантацію печінки
|
Кілька досліджень вже окреслювали переваги противірусної терапії в період до або після ортотопічної трансплантації печінки.177, 202–205 У період перед трансплантацією багатьох пацієнтів знімають з лікування через протипоказання. Показники СВВ низькі. Існує мало доказів для лікування в перитрансплантаційному періоді (період безпосередньо до, впродовж і після трансплантації). Після трансплантації терапія переноситься погано, що обумовлено анемією і лейкопенією, але здається безпечною з точки зору відторгнення трансплантата. У тих пацієнтів, які можуть витримати повну дозу терапії, досягається високий показник СВВ. |
3 1+ |
|
D |
Пацієнти, яким планується трансплантація, не повинні отримувати противірусну терапію у передтрансплантаційний або перитрансплантаційний періоди, окрім випадків клінічних випробувань. |
|
D |
Для досягнення кліренсу ВГС у випадках повторного захворювання печінки, що пов’язане з ВГС, необхідно розглядати призначення пацієнтам противірусної терапії у посттрансплантаційному періоді. |
11.2. Трансплантація печінки
|
У ранніх дослідженнях серед пацієнтів, яким було трансплантовано печінку через ВГС цироз, 5- і 10-річний показник виживання був еквівалентний пацієнтам, які перенесли ортотопічну трансплантацію печінки через причини, не пов’язані з ВГС (68 і 60 %).205 У нещодавньому |
2+ |
|
аналізі Об’єднаної мережі з обміну органами було проведено дослідження баз даних по ВГС-позитивним (n = 5640, 43 %) і ВГС-негативним реципієнтам (n = 7386, 56,7 %). У ВГС-негативних і ВГС-позитивних реципієнтів п’ятирічні показники виживання пацієнтів склали 83,5 % проти 74,6 % (p < 0,00001), а п’ятирічні показники життєздатності трансплантата — 80,6 % проти 69,9 % (р < 0,00001) відповідно. ВГС інфекція знижує результати після трансплантації, але цей ефект не є достатнім, щоб відмовити окремому пацієнту в трансплантації.206 |
|
|
Пацієнти з ВГС та гепатоцелюлярною карциномою, що дозволяє трансплантацію (один осередок < 5 см або менше трьох осередків < 3 см на поперечному перерізі зображення), не мають зниження виживаності до 48 місяців після ортотопічної трансплантації печінки порівняно з пацієнтами, які мають лише ВГС.205, 207 |
2+ |
|
Якість життя пацієнтів після ортотопічної трансплантації печінки для ВГС є еквівалентною до пацієнтів, які не мають ВГС на етапі 3 років.208 |
3 |
|
C |
Пацієнтам з гепатитом С та одночасною операбельною гепатоцелюлярною карциномою мають запропонувати трансплантацію печінки. |
|
C |
Пацієнтам з ВГС-асоційованою хворобою печінки необхідно пропонувати трансплантацію печінки |
Досліджень щодо ефективності ретрансплантації у пацієнтів із відторгненням через повторне виникнення ВГС не виявлено.
11.3. Скринінг на гепатоцелюлярну карциному
|
Результати досліджень з оцінки чутливості і специфічності сироватки фетопротеїну для виявлення ГЦК у пацієнтів з ВГС показують, що інтерпретація окремо взятого цього маркеру має обмежену інформаційну цінність. |
1+ |
|
Щорічне ультразвукове дослідження пацієнтів з цирозом і ВГС не виявляє пухлини на тій стадії, яка дозволяє вірогідний лікувальний ефект.210 Сканування раз на шість місяців може допомогти у виявленні пухлин на тій стадії, яка дозволяє отримати лікувальний ефект від терапії.211 |
2+ |
|
Інші методи скринінгу та нагляду, окрім фетопротеїну та ультразвукового дослідження, залишаються експериментальними. |
|
|
Показник розвитку ГЦК у пацієнтів з ВГС, які не мають цирозу, є дуже низьким (7,6 проти 92,4 %).212 |
2+ |
|
A |
Вимірювання α-фетопротеїну має проводитися ізольовано для скринінгу або нагляду за розвитком ГЦК у пацієнтів з гепатитом С. |
|
D |
Нагляд з використання УЗД має проводитися з інтервалами у 6 місяців. |
|
C |
Нагляд має охоплювати пацієнтів з цирозом. |
AASLD Practice Guideline. Management of Hepatocellular Carcinoma: An Update (2011)
Роль АФП у діагностиці
Альфа-фетопротеїн вже давно використовується для діагностики ГЦК. Крім того, він був частиною алгоритмів спостереження. Однак, як описано вище, АФП недостатньо чутливий або специфічний для використання в якості спостережного аналізу. Останні дані також показують, що його використання в якості діагностичного тесту менш специфічне, ніж колись вважалось. АФП може бути підвищений при внутрішньопечінковій холангіокарциномі (ВХК) і при деяких метастазах раку товстої кишки.167, 168
Таким чином, наявність вогнищевого утворення в печінці у пацієнтів з підвищеним АФП не свідчить про ГЦК. ВХК також більш поширена при цирозі печінки, ніж у пацієнтів без цирозу.
Хоча поширеність ВХК значно нижча, ніж ГЦК, той факт, що обидві злоякісні пухлини є більш поширеними при цирозі, означає, що необхідно з обережністю розрізняти їх, аби врахувати відмінності в лікуванні та результати. Оскільки АФП може бути підвищений при обох станах, рекомендується, щоб він більше не використовувався. Таким чином, діагноз ГЦК має спиратися на радіологічні ознаки та гістологію.
ХІІ. Харчування, підтримуюча терапія і додаткові методи лікування
12.1. Заходи щодо харчування
12.1.1. Дієта
|
Недостатня кількість білка є поширеним явищем у всіх пацієнтів з хронічними захворюваннями печінки, і може призвести до втрати маси. ХГС підвищує базовий метаболізм у пацієнтів з нецирозними захворюваннями.188 Невідповідне харчування (мала або надлишкова маса тіла) негативно впливає на нутритивний статус, якість життя і виживання. Оцінка харчування для виявлення пацієнтів з ризиком і забезпечення харчової підтримки (ентерально і парентерально) для поліпшення клінічних результатів повинні відігравати важливу роль у догляді за пацієнтами.213 |
2– 4 |
|
У пацієнтів впродовж отримання противірусної терапії зазвичай спостерігається втрата маси.170, 171, 189 Ймовірно, це є наслідком інших побічних наслідків, таких як втома і депресія, що можуть мати негативний вплив на апетит.170, 171 |
2– 3 |
|
D |
Лікувальне харчування осіб, які інфіковані гепатитом С, має включати пропаганду оптимального харчування та запобігання неправильному харчуванню або нестачі конкретних поживних речовин або лікування. Пацієнти мають проходити тест на дефіцит поживних речовин, а за необхідності — нутритивну оцінку з відповідними рекомендаціями дієтолога. |
|
D |
Пацієнтам із розвиненою хворобою печінки слід приділяти увагу харчуванню, щоб уникнути випадків недостатнього харчування. |
|
- |
Противірусна терапія представляє високу загрозу для втрати маси, а тому необхідно ретельно проводити моніторинг серед пацієнтів і надавати їм нутритивну підтримку, коли необхідно, протягом лікування. |
|
Систематичний огляд 11 РКД не виявив переконливих доказів на підтримку будь-якої переваги від амінокислот із розгалуженим ланцюгом (BCCA) у пацієнтів із цирозом печінки і печінковою енцефалопатією.214 Було неясно, як багато пацієнтів, включених у дослідження, були ВГС-позитивними. Амінокислоти з розгалуженими боковими ланцюгами поліпшують рівні сироваткового альбуміну в компенсованій стадії цирозу печінки у пацієнтів з розгалуженим співвідношенням тирозину < 4 і рівнем альбуміну в сироватці 35–39 г/л. 215, 216 Методологія, яка використовувалася в цих дослідженнях, мало уваги приділяла недостовірним змінним. |
1++ 1– |
|
Кава може мати захисний ефект проти розвитку гепатоцелюлярної карциноми у пацієнтів із захворюваннями печінки при споживанні в кількості трьох і більше чашок на день. Неясно, які саме складові у каві викликають такий ефект.217, 218 |
2+ |
12.1.2. Вітаміни та мінерали
Існує мало доказів того, що прийом пацієнтами вітамінів та мінералів може вплинути на перебіг хвороби ХГС.
|
Додаткове вживання цинку в дозуванні 34 мг/день може мати позитивний ефект на СВВ у пацієнтів, які перебувають на терапії ІФН; з генотипом 1b; з вірусним навантаженням нижче 5 x 105 копій/мл.219 |
2– |
|
Вітамін K2 може мати позитивний вплив у запобіганні розвитку ГЦК у пацієнтів із гепатитом С.220 |
2– |
|
Вітамін E не мав позитивного ефекту на пацієнтів, які приймали інтерферон та рибавірин. Не схоже, що він допомагає у запобіганні гемолізу рибавірину або підвищує вірусологічний кліренс.221 |
1– |
|
Прийом заліза, що обмежений до < 7 мг/день, у поєднанні з контрольованою кількістю спожитих калорій у 30 Ккал/кг, споживанням білків 1,1–1,2 г/кг та жирів у 15 % від дієтологічного прийому знижує рівні амінотрансферази.222 |
4 |
|
Вітамін C у дозі 600 мг/день не має позитивного ефекту в запобіганні ретинопатії, що асоційована з терапією інтерфероном.191 |
1– |
|
- |
Пацієнтів з хронічним гепатитом С необхідно заохочувати до досягнення рекомендованих Сполученим Королівством рівнів споживання поживних речовин, вітамінів та мінералів.223 Необхідно мати на увазі, що не існує ніяких виявлених доказів на підтвердження кращої дії вказаних речовин у вищих дозах. |
|
- |
Пацієнтам зі стабільно високими показниками феритину в сироватці необхідно рекомендувати знизити рівень споживання продуктів, що містять залізо. |
12.1.3. Надмірна вага
|
Дослідження виявили, що ІМТ > 25, пов’язаний зі стеатозом печінки, призводить до більш важкої форми фіброзу.89, 224 Фіброз печінки, стеатоз і зниження рівнів активності АЛТ з контрольованою втратою маси тіла пацієнтом у 3 дієтологічних програмах та завдяки регулярним фізичним вправам, що направлені на зниження маси на 0,5 кг щотижнево.225 |
2+ 3 |
|
C |
Пацієнтам, які мають надлишкову вагу, слід рекомендувати схуднення у реалістичних рамках втрати маси, оскільки це може мати позитивний вплив на ступінь пошкодження печінки, що пов’язане з гепатитом С. |
|
- |
Втрату маси слід розглядати тільки тоді, коли пацієнт є стабільним із точки зору ведення захворювання на гепатит С. Заходи, що спрямовані на зниження маси впродовж противірусного лікування, не рекомендуються, так як побічні ефекти можуть призвести до надмірної незапланованої втрати маси. |
|
- |
Пацієнти, які перебувають в програмах схуднення, мають регулярно отримувати підтримку та проходити контроль. |
An update on the management of chronic hepatitis C: Consensus guidelines from the Canadian Association for the Study of the Liver (2012)
Деякі, але не всі дослідження також показують, що підвищена маса тіла має негативний вплив на ймовірність СВВ на подвійну терапію з пег–ІФН і рибавірином. При комбінованій терапії, включаючи телапревір або боцепревір, ожиріння не впливає суттєво на відповідь на лікування. У світлі цих висновків не можна зробити конкретних рекомендацій щодо втрати маси перед PI-терапією з метою покращення рівня СВВ (як вже було повідомлено щодо подвійної терапії).
12.2. Спеціалізований санітарний догляд
|
Спеціальна підтримка і догляд є ключем для підтримання прихильності до лікування пацієнтів з нейропсихіатричними захворюваннями.226 Спеціальний гепатологічний догляд має визначну роль у допомозі пацієнтам в досягненні та підтримуванні СВВ.227 |
2– |
|
- |
Клінічні спеціалісти із санітарного догляду за пацієнтами мають бути невід’ємною частиною клінічної команди, яка піклується про пацієнтів з ХГС. |
12.3. Психосоціальні заходи
|
Два дослідження щодо психологічних впливів на пацієнтів з гепатитом С не показали можливої користі від цього. Одне невелике нерандомізоване дослідження показало деяку користь, |
2– 1+ |
|
але інше РКД, що перевіряло індивідуально результати кожного заходу, не показало жодної різниці в результатах порівняно зі стандартним доглядом.228, 229 |
|
12.4. Фізичні вправи
|
Пацієнтам, які отримують лікування від гепатиту, рекомендовано легкі та помірні фізичні вправи.170 Невелике когортне дослідження показало, що пацієнти на противірусній терапії мають знижену переносимість до фізичних вправ.230 |
4 2– |
|
D |
Пацієнтів з гепатитом С необхідно закликати до легких та помірних фізичних вправ. Пацієнтам, які перебувають на противірусній терапії, слід знати, що їх можливості до виконання фізичних вправ будуть знижені. |
12.5. Додаткові методи лікування
|
Два метааналізи дійшли висновку, що немає ніяких доказів, що підтримують використання додаткових або альтернативних лікарських засобів у лікуванні хворих з гепатитом C.231, 232 |
1++ |
Ні в одному з досліджень не було виявлено (через обмеженість часу проведення досліджень) безпечність або шкоду від довготривалого прийому рослинних лікарських засобів.
|
- |
Пацієнти повинні знати, що існують певні загрози, пов’язані з деякими додатковими препаратами. |
12.6. Паліативний догляд
Жодних доказів щодо надання паліативного догляду за пацієнтами з ВГС виявлено не було.
ХІІІ. Надання інформації
Аби дізнатися про основні інформаційні потреби пацієнтів, були проведені інтерв’ю та фокус-групи, впроваджено анкети для людей з гепатитом С по всій Великобританії через мережу центрів підтримки з питань гепатиту С в Шотландії та завдяки ресурсному центру Сполученого Королівства. Результати були переформатовані на запитання із запропонованими відповідями (див. розділ 13.2), що можуть бути використані для заохочення дискусій між пацієнтами та медичними працівниками. Деякі з організацій, наведених у розділі 13.1, розробляють якісні інструкції для пацієнтів.
13.1. Джерела подальшої інформації
Коментар робочої групи:
Більш докладну інформацію про джерела подальшої інформації можна знайти за посиланням http://www.sign.ac.uk/pdf/sign133.pdf.
13.2. Інформація про гепатит с для пацієнтів та медперсоналу
Що таке гепатит С?
Гепатит С — це захворювання, що викликається вірусом, який може передаватися через кров від однієї людини до іншої. Захворювання в основному вражає печінку.
Коли ваша печінка вражається вірусом, вона може пошкоджуватися, і зрештою виникнуть труднощі з виконанням своїх різноманітних і життєво важливих функцій. Протягом тривалого періоду часу це може прогресувати до серйозного пошкодження печінки (наприклад, фіброзу і цирозу) або, в деяких випадках, до раку печінки (гепатоцелюлярної карциноми).
Як хвороба впливає на людей?
Потенційно це захворювання загрожує життю людини і може вплинути на Вас фізично й емоційно. Захворювання може погіршити якість Вашого життя. У багатьох випадках за умови відповідного лікування гепатит С можна вилікувати.
Які симптоми захворювання на гепатит С?
Деякі люди не мають жодних симптомів захворювання протягом багатьох років, у той час як інші можуть відчувати підвищену стомлюваність, пітливість (особливо вночі), ломоту та болі, втрату апетиту і концентрації уваги. Симптоми можуть з’являтися і зникати. На більш пізніх стадіях захворювання, коли печінка пошкоджена більш серйозно, можуть бути такі симптоми, як жовтяниця, свербіж, внутрішня кровотеча і закреп.
Мені це загрожує?
Фактори ризику, коли кров інфікованої гепатитом С особи може потрапити в кровотік іншої особи, включають наступні:
— переливання крові, хірургічне втручання за кордоном або у Сполученому Королівстві до 1991 року, продукти крові у Сполученому Королівстві до 1987 року (переливання та продукти крові у Сполученому Королівстві зараз безпечні з точки зору ВГС); та
— отримання медичної або стоматологічної допомоги в країнах, де гепатит є поширеним захворюванням, а інфекційний контроль є неякісним;
— спільне використанням будь-якого обладнання при споживанні ін’єкційних наркотиків або інгаляційних наркотиків;
— спільне використання таких речей, як леза для гоління, зубні щітки або речі, що можуть подряпати шкіру;
— пірсинг, татуювання або косметичні ін’єкційні процедури (наприклад, ботокс), якщо обладнання для цього використовується повторно;
— статеві відносини; хоча ризик дуже низький, якщо немає загрози кровотечі;
— контакт з кров’ю на роботі, наприклад, поранення голкою, порізи, прибирання крові, робота на місці жорстоких подій з присутністю крові;
— передача від матері до дитини в момент народження.
Мені треба здати аналізи?
Якщо Ви вважаєте, що знаходитеся у групі ризику, необхідно пройти попередню консультацію з лікарем. Чим раніше почати лікування, тим більша вірогідність вилікування інфекції. Якщо ви знаєте, що маєте позитивний результат тесту на інфекцію, Ви можете уникнути зараження інших.
Що мається на увазі під «позитивний» чи «негативний»?
Є три типи тестів. Перший тип тесту (тест на антитіла до ВГС) визначає, чи Ви коли-небудь мали вірус. Деякі люди позбавляються вірусу природнім шляхом, без медичної допомоги. Другий тип (ПЛР) вказує, чи вірус наявний у даний момент у Вашому організмі (тобто чи інфіковані Ви гепатитом С). Якщо тест ПЛР позитивний, додаткове тестування покаже генотип (штам) вірусу. Генотип визначає лікування, яке Ви отримуватимете.
Як щодо конфіденційності?
Конфіденційне тестування доступне в сімейних лікарів та інших місцях. Результати цього тесту є конфіденційними і не будуть передані третім особам без вашого дозволу. Сімейні лікарі лише передадуть інформацію про позитивні тести страховій компанії, якщо ви подали заяву на страхування і дали свою згоду на передачу медичної інформації. Негативні результати не будуть розголошуватися.
Ви можете знайти інформацію про служби гепатиту по всій Шотландії, відвідавши сайт Hepatitis Scotland (див. розділ 13.1)
Це загрожує моїй родині та друзям? Мені треба їм розповісти?
Підтримка родини і друзів має вирішальне значення, тому варто сказати їм про Ваш діагноз і те, якими можуть бути результати і побічні ефекти лікування. Ви не можете заразити членів Вашої сім’ї і друзів через повсякденну діяльність, таку як спільне використання посуду, обійми та поцілунки.
Аби не заразити інших,
— не використовуйте спільно такі предмети побуту, як зубні щітки або бритви;
— очищуйте будь-які плями крові слабким розчином хлорки;
— не використовуйте спільно будь-яке приладдя для вживання ліків (наприклад, трубки, голки та шприци, воду або посуд тощо).
Ризик передачі інфекції статевим шляхом є дуже низьким за відсутності інших ускладнюючих чинників, таких як:
— кров від менструації або анального сексу;
— виразки на геніталіях, тобто від інфекцій, що передаються статевим шляхом, таких як гонорея, герпес або генітальні бородавки.
Як це вплине на мою роботу і кар’єрні перспективи?
Багато людей з гепатитом С почуваються досить добре, щоб працювати, але Вам, можливо, доведеться внести деякі корективи у Вашу повсякденність, якщо у Вас є надмірна втомлюваність або інші симптоми.
Як правило, Ви не зобов’язані повідомляти своєму роботодавцю, що у Вас ВГС (якщо Ви не медичний працівник, який бере участь у процедурах, що можуть включати контакт з кров’ю, наприклад деякі операції). Проте побічні ефекти від лікування можуть означати, що Ви відчуваєте себе погано і не в змозі працювати протягом певного періоду часу. Може бути корисно розказати, що Ви перебуваєте на лікуванні. Наприклад, Вас можуть підтримати, змінивши робочі години або фізичну діяльність, що пов’язана з Вашою роботою впродовж періоду лікування.
Як позитивний діагноз вплине на моє страхування життя?
Як і будь-яке серйозне захворювання, діагноз гепатиту С буде мати вплив на страхування життя. Є багато видів страхування життя, так що варто перевірити будь-які поліси, які у вас є, оскільки, можливо, Вам доведеться сказати страховику, якщо є зміни у стані Вашого здоров’я. Важливо пам’ятати, що будь-яка інформація, яку Ви надаєте вашим страховикам, є складовою частиною правового договору. Якщо інформація є неточною або невірною, угода може бути недійсною.
Якщо Ви подаєте заяву на страхування та згоду на передачу медичної інформації, людина, яка проводила тестування, зобов’язана передати інформацію про позитивний результат тесту, якщо страхова компанія звернеться з таким проханням.
Ви повинні прочитати дрібний шрифт на поточних або нових договорах страхування, перш ніж підписувати.
Як вплине на моє страхування життя негативний діагноз?
Лікарі не повинні надавати страховикам жодної інформації про негативний діагноз. Страховики можуть тільки запитувати інформацію, чи має хтось позитивний результат або проходить курс лікування.
Що відбувається впродовж тестування?
Перед тестуванням лікар повинен з Вами обговорити, що відбувається. Це допоможе Вам зрозуміти процес тестування, результати тестування та конфіденційність.
Зразки крові будуть відправлені на лабораторне дослідження. Якщо Ваш контакт з вірусом відбувся в останні шість місяців, Вас можуть попросити повернутися для повторного тесту. Це відбувається через те, що існує «вікно» після контакту, поки тест не стає позитивним.
Якщо тест негативний, команда лікарів дасть Вам поради про те, як не піддавати себе ризику в майбутньому. Якщо тест позитивний, вони будуть пояснювати, що це означає, і направлять Вас у спеціалізовану клініку для оцінки.
Що відбувається далі?
Оцінка буде включати в себе аналізи крові, такі як тест на печінкові проби, тест на генотип (штам вірусу гепатиту С), клінічне обстеження, дискусії про спосіб життя, інші захворювання та ліки, що Ви приймаєте, УЗД, еластографію і, в окремих випадках, біопсію печінки. Біопсія печінки означає забір невеликого шматка печінки для лабораторного аналізу. Це робиться під місцевою анестезією, але не обов’язково до початку лікування.
По завершенню оцінки Ваш лікар буде говорити з Вами про лікування. Лікування дуже ефективне, і побічних ефектів можна уникнути при гарному догляді та підтримці. Ваша клініка повинна допомогти Вам знайти підтримку, що є частиною Вашого лікування. Лікування не підходить для всіх і залежить від інших захворювань або ускладнень, які Ви можете мати.
У той час, як Ви або Ваш партнер знаходитесь на лікуванні, і протягом від 6 до 12 місяців після цього, Ви повинні використовувати контрацепцію, щоб уникнути вагітності, оскільки ці препарати можуть бути шкідливі для майбутньої дитини.
Життя з гепатитом С?
Є багато речей, що стосуються стилю життя, які можуть полегшити життя з гепатитом С.
— Не вживайте алкоголь. Алкоголь і гепатит С можуть призвести до пошкодження печінки, а їх поєднання робить цей процес набагато швидшим. Існує спеціальна професійна підтримка, щоб допомогти вам зменшити або припинити споживання алкоголю.
— Збалансована дієта є життєво важливою. Зменшіть споживання надмірно жирних та солодких продуктів. Втрата надмірної маси допоможе знизити навантаження на печінку. Проте втрата ваги може бути побічним ефектом лікування, тому можуть бути необхідні харчові добавки. Професійна допомога в плануванні здорової збалансованої дієти стане вам у нагоді.
— Якщо у вас поганий апетит, намагайтеся їсти малими порціями, але частіше.
— Регулярні помірні фізичні вправи зменшують стрес або депресію, тонізують, допомагають зміцнити імунну систему.
— Якщо у вас гепатит С, припиніть палити. Відмова від куріння знижує ризик захворіти на рак. Для припинення паління можна звернутися за допомогою.
Коментар робочої групи:
Вживання тютюну — основна причина передчасних смертей та хвороб в усьому світі, яким людство здатне запобігти. Куріння викликає широкий спектр хвороб і станів, що можуть призвести до передчасної смерті. За офіційною статистикою, в Україні щороку від хвороб, пов’язаних з курінням, помирає 120 тисяч чоловік.
Допомогти припинити палити Вам допоможе сімейний лікар відповідно до «Стандартів первинної медичної допомоги при припиненні вживання тютюнових виробів». http://www.dec.gov.ua/mtd/_pvtv.html
— Поговоріть з вашим лікарем з приводу щеплень проти гепатиту А і В. Інші типи інфекції печінки, особливо якщо у вас вже є гепатит С, спричиняють набагато більше навантаження на печінку і можуть уповільнити або зупинити відновлення для всіх типів гепатиту. Ви також повинні переконатися, що Ви отримуєте сезонне щеплення проти грипу в якості додаткової міри обережності, коли імунна система може бути ослаблена.
Існує дуже мало доказів користі застосування додаткових лікарських засобів, але багато пацієнтів вважають їх корисними у вирішенні багатьох різних симптомів, пов’язаних з цим захворюванням. Перш ніж почати їх вживання, необхідно отримати професійну консультацію.
Яку підтримку я можу отримати?
Існують різні спеціалізовані служби підтримки для людей з гепатитом С, такі як консультування, підтримка осіб з подібним діагнозом, адвокації для допомоги у прийнятті рішень.
Гепатит С може змусити людей відчувати себе ізольованими, а тому емоційна підтримка є дуже важливою. Пацієнти повинні сподіватися на:
— підтримку багатопрофільних служб, що забезпечують добру комунікацію з пацієнтом;
— якісні інформаційні послуги;
— залучення пацієнта на всіх стадіях допомоги та лікування;
— плавний перехід до паліативної допомоги, якщо це необхідно; та
— регулярну оцінку потреб.
ХІV. Впровадження настанови
14.1. Стратегія впровадження
Впровадження національних настанов є обов’язком кожної Ради NHS і є невід’ємною частиною клінічного управління. Повинні існувати механізми, що дозволяють переглядати медичну допомогу, що надається відповідно до рекомендацій настанови. Причини відмінності повинні розглядатися і там, де необхідно, переглядатися. Повинні бути здійснені місцеві механізми для впровадження національної настанови в окремих лікарнях, відділеннях тощо.
14.2. Ресурси для впровадження ключових положень клінічної настанови
Не було виявлено жодного положення КН, що потребувало б значної бюджетної підтримки.
14.3. Аудит поточної практики
Існують два механізми для аудиту практики щодо тестування, лікування, догляду та підтримки, які надаються службами з гепатиту С в Шотландії. Першим є індикатори якості з гепатиту С Healthcare Improvement Scotland, які самостійно підраховуються радами з питань охорони здоров’я. Іншим є індикатори діяльності, які містяться в «Blood Borne Virus and Sexual Health framework» і які підраховуються національним шотландським урядом.
14.4. Додаткові поради
Додаткові поради для NHS Scotland від Quality Improvement Scotland та шотландського консорціуму лікарських засобів:
У вересні 2011 року ШКЛЗ повідомив, що боцепревір був прийнятий для використання в межах NHSScotland для лікування ХГС генотипу 1 у поєднанні з пегільованим ІФН і рибавірином у дорослих пацієнтів з компенсованим захворюванням печінки, які зазнали невдачі попередньої терапії або які раніше не отримували лікування.
У вересні 2011 року ШКЛЗ повідомив, що телапревір у поєднанні з пегільованим ІФН і рибавірином показаний для лікування ХГС генотипу 1 у дорослих пацієнтів з компенсованим захворюванням печінки (у тому числі цирозом печінки), які раніше лікувалися а-інтерфероном (пегільованим або непегільованим) окремо або в комбінації з рибавірином, включаючи пацієнтів з рецидивом, частковою відповіддю і відсутньою відповіддю, або пацієнтів, які раніше не отримували лікування.
ХV. Доказова база
15.1. Систематична оцінка літератури
Доказова база для даної КН була створена відповідно до методології мережі SIGN. Систематичний огляд літератури проводили з використанням чіткої стратегії пошуку, що була розроблена працівником мережі з питань інформації у співпраці з членами групи розробки КН. Пошуки літератури проводилися в бібліотеках Medline, Embase, Cinahl, PsycINFO та Cochrane. Пошук охоплював період 2006–2012 рр. Пошук в Інтернеті проводився на різних сайтах, у тому числі на сайті координаційного центру настанов США. Основні пошуки були доповнені матеріалами, визначеними окремими членами групи з розробки. Кожен з обраних документів оцінювався одним членом групи і одним співробітником SIGN з використанням стандартних листів оцінки SIGN, перш ніж висновки були розглянуті в якості доказів.
15.1.1. Пошук літератури щодо питань, пов’язаних із пацієнтами
На початку процесу розробки настанови спеціалісти з пошуку доказів та інформації SIGN провели пошук літератури для якісних і кількісних досліджень, які охоплювали питання, пов’язані з пацієнтами, які мають відношення до раннього лікування пацієнтів з гепатитом С. Пошуки літератури проводилися в бібліотеках Medline, Embase, Cinahl і PsycINFO, і результати були узагальнені й представлені групі з розробки настанови.
15.2. Рекомендації для дослідження
Група з розробки настанови не змогла визначити достатньо доказів, щоб відповісти на всі ключові питання в цій настанові (див. Додаток 1). Були визначені наступні області для подальшого дослідження:
— лікування гепатиту С у дітей;
— лікування активних споживачів наркотиків;
— маршрути пацієнтів для лікування гепатиту С (пацієнти похилого віку, ув’язнені, пацієнти після трансплантації, хворі на декомпенсований цироз);
— тестування і скринінг.
15.3. Перегляд та оновлення
Ця настанова була опублікована в 2013 році і буде розглядатися на предмет перегляду через 3 роки. Будь-які оновлення даної настанови в перехідний період будуть відзначені на сайті SIGN: www.sign.ac.uk.
ХVІ. Розробка клінічної настанови
16.1. Вступ
SIGN — це спільна мережа лікарів, інших медичних працівників і організацій пацієнтів, що є частиною Національної служби з вдосконалення якості охорони здоров’я Шотландії. Настанови SIGN розробляються міждисциплінарними групами практикуючих лікарів з використанням стандартної методології, заснованої на систематичній оцінці доказів. Більш детальну інформацію про мережу і методологію розробки настанови Ви можете знайти у довіднику «SIGN 50: Настанова для розробників настанов» на сайті www.sign.ac.uk
Коментар робочої групи:
Більш докладну інформацію про склад групи з розробки настанови та рецензентів можна знайти за посиланням http://www.sign.ac.uk/pdf/sign133.pdf.
Скорочення
|
GUM |
Гінекологія, урологія, венерологія |
|
NHS |
Національна система охорони здоров’я |
|
NICE |
Національний інститут досконалості медичної допомоги |
|
SIGN |
Шотландська міжуніверситетська мережа настанов |
|
UNOS |
Об’єднана мережа розподілу органів |
|
АЛТ |
Аланінамінотрансфераза |
|
АРЛ |
Амінокислоти з розгалуженими ланцюгами |
|
ВГВ |
Вірус гепатиту В |
|
ВГС |
Вірус гепатиту С |
|
ВІЛ |
Вірус імунодефіциту людини |
|
ВР |
Відносний ризик |
|
Г–КСФ |
Гранулоцитарний колонієстимулюючий фактор |
|
ГЦК |
Гепатоцелюлярна карцинома |
|
ДІ |
Довірчий інтервал |
|
ЕП |
Еритропоетин |
|
ЗТ ПЛР |
Полімеразна ланцюгова реакція зі зворотною транскрипцією |
|
ІМТ |
Індекс маси тіла |
|
ІФА |
Імуноферментний аналіз |
|
ІФН |
Інтерферон |
|
НПП |
Небезпечні процедури з пацієнтом |
|
ПКЗ |
Печінкова концентрація заліза |
|
РВВ |
Рання вірусологічна відповідь |
|
РКД |
Рандомізоване контрольоване дослідження |
|
РНК |
Рибонуклеїнова кислота |
|
СВВ |
Стійка вірусологічна відповідь |
|
СІН |
Споживачі ін’єкційних наркотиків |
|
СШ |
Співвідношення шансів |
|
ТАНК |
Тест ампліфікації нуклеїнових кислот |
|
ХГС |
Хронічний гепатит С |
|
ШВВ |
Швидка вірусологічна відповідь |
|
ШКЛЗ |
Шотландський консорціум лікарських засобів |
Список літератури, що була використана при розробці прототипу клінічної настанови та в процесі її адаптації, знаходиться в редакції.