Газета «Новости медицины и фармации» 20 (522) 2014
Вернуться к номеру
Сучасні можливості лікування й профілактики доброякісної гіперплазії передміхурової залози (за матеріалами 10-го Південно-східного європейського мітингу SEEM Європейської асоціації урологів)
Авторы: Тетяна Чистик
Разделы: Медицинские форумы
Версия для печати
Статья опубликована на с. 8-9 (Мир)
24–26 жовтня в м. Бєлграді (Сербія) відбувся 10-й Південно-східний мітинг SEEM Європейської асоціації урологів (ЄАУ), у рамках якого проводився симпозіум, присвячений новим аспектам лікування й профілактики доброякісної гіперплазії передміхурової залози (ДГПЗ).
Симпозіум відкрив президент регіонального відділення ЄАУ, професор кафедр урології Нью-Йоркського й Віденського медичних університетів Bob Djavan, який запропонував увазі слухачів доповідь «Які причини доброякісної гіперплазії передміхурової залози, її прогресування й ризики для пацієнтів?».
Охарактеризувавши основні фактори ризику прогресування ДГПЗ, він докладно зупинився на даних нових досліджень, що доповнюють сучасні погляди на патогенез захворювання. Особлива увага в презентації приділялася запаленню як новій терапевтичної мішені в лікуванні ДГПЗ. Так, відповідно до результатів гістопатологічних досліджень біоптатів, отриманих D. Sieveriо від 3942 пацієнтів, було підтверджено, що в 43,1 % випадків ДГПЗ супроводжується запаленням. При цьому була встановлена виражена кореляція між розміром простати й хронічним запаленням. Також відзначений більш високий ризик розвитку цієї патології в чоловіків, які мають в анамнезі простатит. У дослідженні J.L.St. Sauver і співавт. (2008) було показано, що середній час від установлення діагнозу простатиту до встановлення діагнозу ДГПЗ становить 8,1 року, а від установлення діагнозу простатиту до лікування — 9,8 року.
Доведено, що в пацієнтів із ДГПЗ і супутнім запаленням більш високий ризик ускладнень (прогресування, гостра затримка сечі), що обумовлює необхідність хірургічного втручання (Roehborn MTOPS Study Group, AUA 2005). Причому інфільтрація тканини простати лімфоцитами відзначається раніше, ніж її ріст. Так, за даними Fujikawa et al. (2005), які досліджували японських чоловіків, маркери запалення наявні в 60 % пацієнтів після 40 років, у той час як гіперплазія виявляється, як правило, після 50 років.
Bob Djavan відзначив, що запалення не тільки призводить до розвитку симптомів захворювання, але й є важливим пусковим фактором лімфокінообумовлених механізмів, до яких належать фактори росту, що впливають на прогресування й результат захворювання. Вони регулюють співвідношення між проліферацією й апоптозом, і його зниження є одним із ключових факторів розвитку пухлини. У той же час вивільнення мембранних фосфоліпідів підсилює обмінні процеси в каскаді арахідонової кислоти та збільшує синтез медіаторів запалення, простагландинів і лейкотрієнів. Крім того, тканини, ушкоджені запальним процесом, вивільняють андрогенозалежний фактор ангіогенезу — VEGE, що відіграє важливу роль у проліферації судин при раку простати.
З огляду на те, що в розвитку прогресування ДГПЗ доведена роль гормонів і різних факторів росту, визначене ключове значення таких процесів, як апоптоз, проліферація, запалення й ангіогенез, стає очевидною логічність багатовекторності дії лікарських препаратів, які можуть бути рекомендовані для лікування й зниження ризику прогресування даного захворювання.
У цей час найбільш вивченим фітотерапевтичним агентом у лікуванні ДГПЗ є екстракт плодів північноамериканської пальми повзучої Serenoa repens, що має мультимодальну дію й здатний впливати на основні механізми патогенезу даного захворювання, що забезпечує:
- блокування обох ізомерів (1-го й 2-го типу) 5a-редуктази й інгібування зв’язування дигідротестостерону з рецепторами простати;
- інгібування циклооксигенази й 5-ліпоксигенази та продукції медіаторів запалення або цитокинів (протизапальний ефект);
- супресію проліферації клітин/проапоптотичний ефект і вплив на простатичні фактори росту;
- протинабрякову дію;
- блокування взаємодії пролактину зі специфічними рецепторами в простаті й порушення процесів передачі сигналу;
- інгібуючий вплив на α1-адренорецептор у простаті й розслаблюючий вплив на гладку мускулатуру.
Особливий інтерес викликали дані власних досліджень B. Djavan, що підтверджують прямий вплив S. repens на шляхи патогенезу ДГПЗ та обумовлюють значне зниження рівня клінічного прогресування захворювання в чоловіків із симптомами нижніх сечових шляхів через 24 місяці лікування (B. Djavan et al., 2005). Із метою вивчення впливу S. repens на клінічне прогресування обструкції сечового міхура автором було обстежено 189 пацієнтів із різних європейських клінік із визначенням показника за міжнародною шкалою простатичних синдромів (IPSS), якості життя (QoL), максимальної швидкості потоку сечі (Qmax), простатичного специфічного антигену (PSA) та об’єму простати. До речі, на тлі лікування в меншого числа пацієнтів (на 33 %) легкий ступінь захворювання змінився на середній/тяж–кий. Було показано, що S. repens за 2 роки може значно відстрочити прогресування ДГПЗ.
На завершення Bob Djavan ще раз підкреслив, що запалення є важливим чинником, який впливає на прогресування й результат ДГПЗ, і потенційною терапевтичною мішенню. Тому очевидна доцільність застосування S. repens як препарату багатовекторної дії, що має протизапальні властивості.
У доповіді професора А.З. Вінарова (Росія) «Як запобігти загостренню доброякісної гіперплазії передміхурової залози» був зроблений акцент на недостатній ефективності медикаментозної терапії в зниженні ризику виникнення й прогресування даної патології.
Такий стан речей, на думку доповідача, пояснюється неможливістю проведення тривалого курсу терапії через виникнення небажаних ефектів або симптоматичною дією препаратів, тому головна роль у вирішенні цієї проблеми відводиться лікарським засобам із групи рослинних екстрактів.
Екстракт Serenoa repens уже відомий як один із варіантів керування симптомами ДГПЗ. Це пов’язане з його протизапальними, антипроліферативними, антиапоптотичними й антиандрогенними властивостями, що, у свою чергу, забезпечують позитивні клінічні ефекти. Крім того, препарат має максимальний рівень безпеки й гарну переносимість і може призначатися протягом тривалого періоду, що дуже важливо для пацієнтів, які потребують лікування протягом багатьох місяців і навіть років.
Доповідач розповів про результати трирічного російського мультицентрового дослідження, у якому вивчалися ефективність і безпека Простамолу® уно в лікуванні пацієнтів з аденомою передміхурової залози на ранніх стадіях і високим ризиком прогресування. У дослідженні взяли участь 100 пацієнтів, рандомізованих на 2 групи: пацієнти основної групи (n = 50) протягом 36 місяців приймали препарат Простамол® уно в добовій дозі 320 мг, пацієнти контрольної (n = 50) не одержували специфічного лікування, але проходили ретельне обстеження, у них оцінювали ключові параметри протягом усього періоду дослідження.
Через 36 місяців після початку дослідження в пацієнтів основної групи відзначалося зниження симптоматики за шкалою IPSS на 37 % і поліпшення показника якості життя на 52 %, тоді як у контрольній групі вираженість симптомів збільшилася на 36 %, а якість життя погіршилася на 17 %.
Статистично вірогідне збільшення максимальної (на 21,5 %) і середньої (на 57 %) швидкості потоку сечі зафіксовано в групі препарату Простамол® уно, у групі спостереження відзначене зниження за даними показниками на 16 і 22 % відповідно. Обсяг залишкової сечі знизився в групі контролю на 42 % і майже у 2 рази збільшився в групі спостереження. За три роки прийому препарату в пацієнтів у групі Простамолу® уно відбулося зменшення об’єму простати (у середньому на 13,2 %) при незмінному рівні простатичного специфічного антигену, тоді як у контрольній групі об’єм простати виріс на 22 %.
При цьому лікування не супроводжувалося небажаними явищами, за весь період у жодного пацієнта основної групи не було відзначено прогресування симптоматики за жодним критерієм спостереження.
Далі професор А.З. Вінаров навів результати 10-літнього дослідження ефективності й безпеки застосування екстракту Serenoa repens (Простамол® уно) в 39 пацієнтів із легким і помірним ступенем ДГПЗ і ризиком її прогресування (рис. 1).
Результати клінічного дослідження продемонстрували ефективність про-філактичного призначення 320 мг Простамолу® уно 1 раз на день протягом 10 років. Було відзначене зменшення вираженості суб’єктивної симптоматики за шкалами IPSS, QoL і поліпшення об’єктивних параметрів, що свідчать про відсутність прогресування захворювання: збільшення максимальної й середньої швидкості потоку сечі на 24 і 9 % відповідно й зменшення об’єму простати на 7,2 %.
При цьому було відзначено поліпшення еректильної функції за шкалою «Міжнародний індекс еректильної функції» (ІIEF) і відсутність небажаних реакцій, пов’язаних із безпосереднім прийомом досліджуваного препарату.
Таким чином, на думку професора А.З. Вінарова, ці результати є вагомим аргументом на користь застосування Простамолу® уно з метою запобігання прогресуванню аденоми передміхурової залози. Тривале лікування цим препаратом забезпечує вдосконалення суб’єктивних та об’єктивних параметрів при ДГПЗ, що підвищує прихильність пацієнтів до терапії й гарантує її успіх.
На завершення симпозіуму професор F. Giuliano (Франція) виступив із доповіддю «Чи може зберігатися сексуальна функція в пацієнтів із легким і помірним ступенем доброякісної гіперплазії передміхурової залози?».
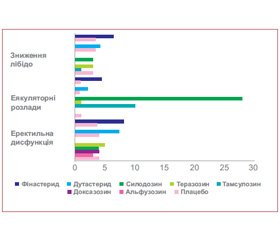
Згідно з даними численних досліджень, відзначив лектор, медикаментозні препарати, призначувані при ДГПЗ/симптомах нижніх сечових шляхів, нерідко викликають сексуальну дисфункцію. У порівняльному дослідженні V. Mirone et al. (2011) із вивчення впливу α1-адреноблокаторів та інгібіторів 5a-редуктази на сексуальну сферу пацієнтів було виявлено, що застосування фінастериду призводить до зниження лібідо, еякуляційного об’єму й еректильної дисфункції, силодозин негативно впливає на сім’явилиття й викликає неприємні суб’єктивні відчуття при оргазмі. При цьому частота розвитку еякуляторних розладів при прийманні силодозину в багато разів перевищує таку при призначенні тамсулозину й інших aадреноблокаторів (рис. 2).
Недоліком силодозину є висока вибірковість щодо α1α-адренорецепторів, що веде до високої частоти розвитку еякуляторних розладів, і трохи менша спорідненість до a1d-адренорецепторів, хоча на ефективності лікування це не позначається й не визначає клінічні переваги силодозину. Так, систематичний огляд і метааналіз рандомізованих контрольованих досліджень, що оцінюють силодозин у лікуванні ненейрогенних симптомів нижніх сечових шляхів при ДГПЗ, показав, що силодозин був більш ефективний, ніж плацебо й тамсулозин у дозі 0,2 мг, і так само ефективний, як тамсулозин у дозі 0,4 мг. Що стосується побічних ефектів, то порушень еякуляції було більше при застосуванні силодозину. В іншому дослідженні, проведеному в 9 медичних центрах за участю 209 пацієнтів, які приймали 4 мг силодозину 2 рази на день і 0,2 мг тамсулозину на день протягом 12 тижнів, показано, що прийом 4 мг силодозину 2 рази на день не гірший, ніж 0,2 мг тамсулозину на день для пацієнтів із симптомами ДГПЗ. Більш масштабне мультицентрове подвійне сліпе плацебо-контрольоване дослідження за участю 1228 пацієнтів із 72 міст у 11 європейських країнах показало, що загальна ефективність силодозину не нижча й не вища за таку тамсулозину [7]. Таким чином, із патогенетичної точки зору найбільш доцільним засобом для лікування симптомів нижніх сечових шляхів при ДГПЗ варто визнати тамсулозин.
Рекомендації ЄАУ 2014 року констатують, що всі α1-блокатори мають подібну ефективність у порівнянних дозах. Разом із тим тільки в тамсулозину відзначений достатній профіль безпеки: він практично не викликає судинних ускладнень (характерних для теразозину, доксазозину й альфузозину) й еякуляторних розладів (характерних для силодозину), що робить його кращим засобом для лікування симптомів нижніх сечових шляхів при ДГПЗ.
У дослідницькій роботі Сorona et. al. (2012), пов’язаній із вивченням побічних ефектів інгібіторів 5a-редуктази, також були зафіксовані небажані явища в сексуальній сфері пацієнтів, що проявляються зниженням статевого потягу, еректильною дисфункцією й зниженням числа нічних ерекцій.
Професор F. Giuliano помітив, що подібна реакція може відзначатися не тільки в пацієнтів із ДГПЗ/симптомами нижніх сечових шляхів, а й у тих хворих, які приймають фінастерид при алопеції. Так, Michael S. Irwig et al. (центр андрології й відділення ендокринології, Університет Джорджа Вашингтона) проспективно оцінювали 54 молодих пацієнтів, які при первинному обстеженні відзначали сексуальну дисфункцію, що зберігається не менше ніж 3 місяці після завершення прийому фінастериду. У всіх хворих була відсутня супутня патологія, початково не було сексуальної дисфункції, психіатричних захворювань, вони не приймали пероральні препарати до застосування фінастериду. При повторному обстеженні через 9–16 місяців (у середньому через 14 місяців) після першого візиту в 96 % чоловіків зберігалася сексуальна дисфункція, незважаючи на припинення прийому фінастериду.
На підставі цих результатів, відзначив доповідач, необхідно з обережністю підходити до призначення цього препарату, оскільки небажані побічні ефекти фінастериду були отримані й у ряді подвійних сліпих рандомізованих досліджень, і в постмаркетингових дослідженнях на здорових добровольцях.
У цьому аспекті, зазначив професор F. Giuliano, особливу цінність становлять дані порівняльних досліджень, що довели відсутність негативного впливу S. repens на сексуальну сферу пацієнтів. Так, у дослідженні SLOVAK, проведеному в 30 центрах урології в Словаччині (Breza J. et al., 2006) за участю 600 пацієнтів із ДГПЗ, було показано, що призначення Простамолу® уно протягом 12 місяців є не тільки ефективним, а й безпечним лікуванням. Результати дослідження продемонстрували позитивну динаміку IPSS при тяжкому й середньому ступені тяжкості ДГПЗ; покращання якості життя й максимальної швидкості сечовипускання; зниження залишкового об’єму сечі при тяжкому ступені захворювання; поліпшення симптоматики; покращання показників уродинаміки; незначну зміну рівня PSA і об’єму простати. При цьому Простамол® уно не змінював індекс еректильної функції навіть через 12 місяців щоденного прийому.
Довгострокова ефективність S. repens у 120 пацієнтів із легкими й помірними симптомами нижніх сечових шляхів, викликаними аденомою передміхурової залози, була показана в дослідженні I. Sinescu (2010). Через 24 місяці від початку лікування було досягнуте поліпшення якості життя на 5,5 бала, зменшення залишкової кількості сечі на 35 % і зниження об’єму простати на 10 %. При цьому індекс еректильної функції за IIEF збільшився на 6,4 бала.
Підбиваючи підсумки, професор F. Giuliano відзначив, що проблема впливу препаратів на сексуальну функцію особливо значима для молодих пацієнтів і стає все більш актуальною для урологів. Як показали дослідження Perry et al. (2012), крім позбавлення від симптомів захворювання, основними критеріями вибору препаратів S. repens для урологів виявилися відсутність ризику сексуальної дисфункції (61 %), прийнятність для пацієнтів (53 %), відсутність ризику еякуляційних розладів (47 %), поінформованість про препарат (47 %) і зниження запалення (38 %).
Таким чином, вибір правильних препаратів для правильних пацієнтів повинен виправдати зростаючі очікування пацієнтів відносно лікування, що підходить їх стилю життя, позбавляє від симптомів, що турбують, із мінімумом побічних ефектів. Простамол® уно повністю відповідає цим критеріям, оскільки має мультимодальну дію, гальмує прогресування захворювання й має профіль безпеки, порівнянний із таким у плацебо.

/9_m/9_m.jpg)
/9_m/9_m2.jpg)