Журнал «Медицина неотложных состояний» 7 (62) 2014
Вернуться к номеру
Лечение эндотелиальных нарушений у новорожденных, перенесших тяжелую асфиксию при рождении
Авторы: Овчаренко С.С., Межирова Н.М., Кравцова Г.Д., Данилова В.В. - Харьковский национальный медицинский университет, кафедра детской хирургии и детской анестезиологии
Рубрики: Медицина неотложных состояний
Разделы: Клинические исследования
Версия для печати
В данной статье представлены результаты лечения новорожденных с системным воспалительным ответом вследствие перенесенной тяжелой асфиксии при рождении. Изучалось влияние препарата на эндотелиальное звено патогенеза системного воспаления. У 16 новорожденных, находящихся в крайне тяжелом состоянии за счет кардиореспираторной и церебральной недостаточности, в комплексе интенсивной терапии применялся депротеинизированный гемодиализат из крови молочных телят. Исследование показателей тромбоцитов, производных оксида азота и молекул средней массы позволило определить, что депротеинизированный гемодиализат из крови молочных телят положительно влияет на течение патологического процесса за счет снижения активности эндотелия и отсутствия эндогенной интоксикации.
У даній статті наведені результати лікування новонароджених із системною запальною відповіддю внаслідок перенесеної тяжкої асфіксії при народженні. Вивчався вплив препарату на ендотеліальну ланку патогенезу системного запалення. У 16 новонароджених, які знаходяться у вкрай тяжкому стані за рахунок кардіореспіраторної та церебральної недостатності, у комплексі інтенсивної терапії застосовувався депротеїнізований гемодіалізат із крові молочних телят. Дослідження тромбоцитів, показників похідних оксиду азоту і молекул середньої маси дозволило визначити, що депротеїнізований гемодіалізат із крові молочних телят позитивно впливає на перебіг патологічного процесу за рахунок зниження активності ендотелію та відсутності ендогенної інтоксикації.
This article presents the results of treatment of infants with systemic inflammatory response to severe birth asphyxia. We studied the preparation’s effect on the endothelial link in the pathogenesis of systemic inflammation. In 16 critically ill infants with cardio-respiratory and cerebral insufficiency, deproteinised hemodialysate of vealers blood was used in a complex of intensive therapy. The study of the parameters of thrombocytes, nitric oxide derivatives and average weight molecules made it possible to determine that the deproteinised hemodialysate of vealers blood has a positive effect on the pathologic process due to reduction of the endothelium activity and endogenous intoxication.
новорожденные, асфиксия, эндотелий, депротеинизированный гемодиализат из крови молочных телят.
новонароджені, асфіксія, ендотелій, депротеїнізований гемодіалізат із крові молочних телят.
newborns, asphyxia, deproteinised hemodialysate of vealers blood.
Статья опубликована на с. 125-130
Введение
Проблема терапии системного воспалительного ответа (СВО) является актуальной в современной медицине. В настоящее время не разработано единого подхода к ее решению. Патогенез СВО включает в себя три основных звена: воздействие эндотоксина, увеличение выработки цитокинов и активацию эндотелия. С учетом звеньев патогенеза терапия СВО имеет три направления. Первое — антимикробная терапия, при проведении которой предпочтительней использование антибактериальных препаратов цитостатического действия [1, 2]. Второе — управление цитокиновым балансом — рассматривается в настоящее время в качестве новой мишени воздействия на СВО, однако практическая реализация и правильный выбор стратегии цитокинокорригирующей терапии затруднены из-за нерешенности принципиальных вопросов: сложност определения цитокинов и их дозировки. [3, 4]. Третьим направлением лечения СВО является влияние на состояние эндотелия [5, 6]. Депротеинизированный гемодиализат из крови молочных телят является ангиопротектором и представляет собой совокупность ряда физиологически активных ингредиентов, которые стимулируют утилизацию кислорода тканями в условиях гипоксии, обеспечивают усиление транспорта глюкозы через биологические мембраны, повышают синтез внутриклеточного аденозинтрифосфата и увеличивают долю аэробного гликолиза. Стимуляция утилизации кислорода при гипоксии приводит к тому, что в эндотелии сосудов нормализуется анаэробный метаболизм, происходит высвобождение простациклина и оксида азота (NO), обладающих вазодилатирующим эффектом. Вышеперечисленными механизмами действия данного препарата обосновано изучение его применения у новорожденных, перенесших тяжелую асфиксию при рождении.
Цель исследования: определение влияния депротеинизированного гемодиализата на активность эндотелия у новорожденных, перенесших тяжелую асфиксию при рождении.
Материалы и методы
Исследование проводилось на базе отделения анестезиологии и интенсивной терапии новорожденных в коммунальном учреждении охраны здоровья «Областная детская клиническая больница № 1» г. Харькова, куда новорожденные переводились из районных роддомов Харьковской области. В исследование включены 50 доношенных новорожденных с массой тела 3000,0 ± 350,0 г, перенесших асфиксию тяжелой степени при рождении, без видимых клинических симптомов и лабораторных проявлений очагов воспаления. Все наблюдаемые больные находились в крайне тяжелом состоянии за счет кардиореспираторной и церебральной недостаточности. Искусственная вентиляция легких (ИВЛ) проводилась с первых суток жизни современными дыхательными аппаратами. Проведенные лабораторные исследования свидетельствовали о наличии биохимической картины системного воспалительного ответа.
Больные поделены на группы: основную и контрольную. Основную группу составили 16 новорожденных, в стандартную терапию которых введен депротеинизированный гемодиализат из крови молочных телят в дозе 0,5 мл/кг в сутки. В контрольную группу вошли 34 новорожденных, получавших стандартную терапию, соответствующую протоколам лечения тяжелой асфиксии и гипоксически-ишемического поражения центральной нервной системы (ЦНС).
Объектом биохимического исследования являлась венозная кровь. Исследование включало в себя определение показателей функциональной активности эндотелия — количества тромбоцитов, производных оксида азота и количественного показателя эндогенной интоксикации — молекул средней массы (МСМ) на третьи, пятые и седьмые сутки заболевания.
Одним из свойств сосудистого эндотелия является выработка эндогенного антикоагулянта тромбомодулина. Его недостача приводит к нарушению тромборезистентности сосудистой стенки, вследствие чего развивается тромбоцитопения. Подсчет тромбоцитов осуществлялся в камере Горяева путем определения в одном литре с учетом разведения крови и объема большого квадрата счетной сетки Горяева с применением фазово-контрастного микроскопа.
Оксид азота — показатель активности эндотелия. Определение его количества в биологических субстратах невозможно, потому что он быстро окисляется до стабильных соединений в виде нитритов (NO3) и нитратов. Производные оксида азота определяли по методам L.C. Green и соавт. в модификации В.О. Метельской и Н.Г. Гумановой.
Сыворотку крови разводили 96% этиловым спиртом в соотношении 1 : 2, тщательно перемешивали и центрифугировали 15 минут при 2000 об/мин. К 0,5 мл центрифугата добавляли 0,5 мл 0,025% раствора реактива Грисса в 15% уксусной кислоте и 0,5 мл 0,8% раствора хлористого ванадия. Пробы инкубировали 30 минут при 37 °С и измеряли оптическую плотность на спектрофотометре СФ-46 при длине волны 540 нм против дистиллированной воды. Количество суммарных метаболитов оксида азота рассчитывали по калибровочному графику, который строили параллельно с пробами, используя раствор NaNO2. Содержание суммарных метаболитов определяли в микромолях в миллилитре сыворотки (мкмоль/мл).
Среднемолекулярные пептиды являются продуктами нарушения белкового обмена, а их накопление усугубляет течение патологического процесса, дистанционно влияя на все органы и системы, а количественное значение МСМ определяет выраженность эндогенной интоксикации.
Содержание среднемолекулярных пептидов в сыворотке крови больных определяли методом А. Badd и В. Seribner (1975) с использованием трихлоруксусной кислоты (ТХУ). К 1 мл сыворотки добавляли 0,5 мл 10% раствора ТХУ, тщательно перемешивали и оставляли на 5 минут при комнатной температуре. Далее пробы центрифугировали 15 минут при 3000 об/мин. К 0,5 мл центрифугата добавляли 4,5 мл дистиллированной воды. Оптическую плотность измеряли на спектрофотометре СФ-46 при длине волны 254 нм против дистиллированной воды. Содержание МСМ обозначали в единицах (ед.). Норма — не более 3,5 усл.ед. [7].
Результаты всех исследований были обработаны с использованием пакета программ статистики общего предназначения Statistica for Windows версии 6.0: из дискриптивных (описательных) статистик для показателей, измеряемых в количественных шкалах, нами использованы медиана и среднее значение, распределение всех проанализированных количественных показателей проводилось по критерию Колмогорова — Смирнова, для определения расхождения между группами использовался непараметрический критерий Манна — Уитни.
Результаты исследования и их обсуждение
Показатели, отражающие функциональную активность эндотелия и уровень эндогенной интоксикации, исследуемые нами в первые сутки заболевания, свидетельствуют об отсутствии достоверных различий между группами (табл. 1).
Полученные данные позволяют сделать вывод о том, что обе группы исходно однородны.
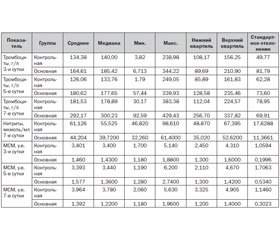
Для изучения влияния применяемого в терапии депротеинизированного гемодиализата из крови молочных телят нами проведен анализ результатов динамического исследования вышеперечисленных параметров на третьи, пятые и седьмые сутки заболевания (табл. 2).
Для оценки состояния эндотелия мы использовали значения нитритов, поскольку наши данные свидетельствуют об отсутствии каких бы то ни было изменений со стороны нитратов.
Как видно из табл. 2, содержание тромбоцитов в основной группе больных достоверно выше и на третьи, и на пятые, и на седьмые сутки заболевания, чем у больных контрольной группы. Кроме того, следует отметить, что у детей основной группы на седьмые сутки уровень тромбоцитов находится в диапазоне нормальных значений, в то время как у детей другой группы едва достигает нижней границы нормы.
Динамическое исследование показателей нитритов свидетельствует об их одинаковом уровне на третьи и пятые сутки заболевания в обеих группах новорожденных. На седьмые сутки заболевания у детей основной группы уровень нитритов оставался прежним, а у детей контрольной группы он достоверно повышался, что свидетельствовало о сохраняющейся активности функции эндотелия.
Характерна динамика МСМ у наблюдаемых больных: у детей контрольной группы уровень МСМ на протяжении всего периода наблюдения превышал нормальные значения, что свидетельствовало о сохранении эндогенной интоксикации, а у больных основной группы в это же время уровни МСМ находились в пределах нормальных значений, более того, были в 2 раза ниже, чем у больных контрольной группы.
Динамика клинического состояния больных включала оценку дыхательной функции и неврологического статуса.
Протезирование функции внешнего дыхания предусматривало поддержание насыщения крови кислородом (SatO2) в пределах 90–91 %, РО2 30–45 мм рт.ст., РСО2 45–50 мм рт.ст., pH 7,25–7,3, дыхательным объемом 6–8 мл/кг путем коррекции PIP (positive inspiratory pressure), PEEP (positive expiratory pressure), FiO2 (концентрация кислорода), Ti (time inspiratory), ЧД (общая и аппаратная частота дыханий). Данные параметров ИВЛ (аппарат Leoni-2 в режиме Synchronized Intermittent Pressure Positive Ventilation (SIPPV)) представлены в табл. 3.
Из данных табл. 3 видно, что в первые сутки заболевания параметры искусственной вентиляции в обеих группах одинаково жесткие: высокое давление на вдохе и выдохе, высокая концентрация кислорода во вдыхаемой смеси, короткое время вдоха, отсутствие попыток дыхания. На третьи сутки в основной группе больных отмечалось снижение PIP, PEEP, FiO2, при этом у больных появились регулярные попытки дыхания, что позволило уменьшить аппаратную ЧД. В контрольной группе изменение (смягчения) параметров PIP, PEEP, FiO2 менее значительное, а попытки самостоятельного дыхания единичные, аппаратная ЧД существенно не изменилась. На пятые сутки заболевания в основной группе больных имело место еще более значительное изменение параметров ИВЛ: уменьшение PIP, PEEP, FiO2, увеличение инспираторного времени, учащение попыток дыхания, что позволило уменьшить частоту аппаратного дыхания с 40 до 32 в 1 минуту без ущерба насыщения крови кислородом и с сохранением необходимого дыхательного объема, то время как в контрольной группе параметры ИВЛ к 5-м суткам снижаются незначительно, а частоту дыхания удалось снизить с 45 до 40. На седьмые сутки в основной группе больных параметры ИВЛ стали значительно мягче: низкое давление на вдохе и выдохе, концентрация кислорода во вдыхаемой смеси составляла 21 %, насыщение крови кислородом в пределах 90–91 %, дыхательным объемом 6–8 мл/кг, что позволило перейти на вспомогательный режим вентиляции СРАР (constant positive airway pressure). В контрольной группе больных к седьмым суткам заболевания параметры ИВЛ улучшились незначительно и возможности перехода на вспомогательный режим вентиляции СРАР не было.
В неврологическом статусе у всех детей отмечался синдром церебрального угнетения: глубокий ступор или кома, резкое угнетение спонтанной двигательной активности, плавающие движения глазных яблок или неподвижность взора с центрированным положением глаз, генерализованное снижение мышечного тонуса в виде позы «лягушки», гиподинамия, симметричное угнетение периостальных и сухожильных рефлексов, рефлексов периода новорожденности церебрального и спинального уровней, преобладание парасимпатического тонуса с наличием миоза, артериальной гипотензии, брадикардии, брадипноэ или периодических апноэ, усиление бронхиальной и слюнной секреции, в ряде случаев — усиление перистальтики кишечника.
В ряде случаев отмечалось сочетание синдрома угнетения с гипертензионно-гидроцефальным, судорожным синдромом. Периодически синдром угнетения сменялся признаками синдрома повышенной рефлекторной возбудимости. Такая смена состояний характеризовалась периодическим возбуждением, периодически возникающим тремором, беспокойством появлением горизонтального нистагма, преимущественно сходящимся страбизмом. При сочетании тремора с протрузией глазных яблок, появлением симптома Грефе, «заходящего солнца», выбуханием родничка и расхождением черепных швов состояние расценивалось как гипертензионно-гидроцефальный синдром.
Судорожный синдром при гипоксически-ишемическом поражении ЦНС характеризовался преимущественно тоническими припадками, которые проявлялись приступами, похожими на децеребрацию, длящимися обычно менее одной минуты и заключающимися в ретракции шейных мышц и экстензии рук и ног, приступообразном нарушении дыхания, напоминающем затянувшийся вдох. Чаще всего они встречались в первые сутки жизни у детей с перенесенной гипоксией.
В ряде случаев нами фиксировались клонические и генерализованные клонические судороги, которые представляли собой ритмическое подергивание какой-либо из частей тела, обычно с частотой 3 в 1 секунду, немедленно купировавшиеся введением раствора сибазона 0,5% из расчета 15 мг/кг болюсно.
При нейросонографическом исследовании определялась эхографическая картина отека мозга, которая характеризовалась повышением общей эхогенности паренхимы мозга, отсутствием четкой дифференциации анатомических структур, в том числе и борозд коры головного мозга, компрессии желудочковой системы, снижением пульсации мозговых сосудов, что клинически соответствовало синдрому угнетения ЦНС.
В результате проведенного лечения у всех больных к пятым суткам жизни ступор сменился вялостью, сонливостью, появились слабые рефлексы периода новорожденности сначала церебрального уровня, затем спинального, было отмечено оживление сухожильных и периостальных рефлексов, нарастание мышечного тонуса, а у больных контрольной группы отмечалась мышечная дистония. В основной группе больных отсутствие судорог отмечалось с 5-х суток жизни, а у больных контрольной группы синдром угнетения трансформировался у 8 больных в гипертензионно-гидроцефальный (увеличение окружности головы, дилатация боковых желудочков и судорожная готовность), а у 12 новорожденных отмечался синдром повышенной нервно-рефлекторной возбудимости, сопровождающийся кратковременными клонико-тоническими судорогами до седьмых суток жизни.
У больных основной группы усиление пульсации мозговых сосудов на фоне четкой визуализации анатомических структур мозга отмечалось на двое суток раньше, чем в контрольной группе. Следует отметить, что нейросонографические исследования за время пребывания детей в отделении анестезиологии и реанимации не выявили кровоизлияний в структуры мозга в основной группе детей, в то время как в контрольной группе у 5 детей на 2-е — 3-и сутки возникали кровоизлияния преимущественно в зоне сосудистых сплетений, что могло приводить к усилению тяжести состояния.
Кроме того, период пребывания в отделении реанимации детей основной группы сократился на 2 койко-дня в сравнении с контрольной.
Таким образом, результаты проведенного исследования свидетельствуют, что у новорожденных детей, перенесших тяжелую асфиксию при рождении, с третьих суток жизни имело место нарушение функциональной активности эндотелия в виде снижения тромборезистентности сосудистой стенки и усиления тромбообразования. Аналогичные результаты получены исследователями Ростовского НИИ акушерства и педиатрии [8], Омской государственной медицинской академией, НИИ общей реаниматологии РАМН [9] и др. Многие исследования свидетельствуют о том, что под действием используемого нами препарата в эндотелии сосудов происходит увеличение высвобождения оксида азота [10, 11], но, по нашим данным, такого не произошло. Напротив, у больных контрольной группы уровень нитритов на седьмые сутки достоверно выше, что, согласно данным ряда авторов [12, 13], объясняет и более медленное восстановление функции внешнего дыхания. Снижение активности эндотелия за счет восстановления нормального количества тромбоцитов и нормализации уровня нитритов у детей, получавших препарат, способствовало более раннему восстановлению функции внешнего дыхания. Аналогичные данные получены Т. Kuninaka, Y. Senga [14, 15], и объясняют они это тем, что в условиях оксидантного стресса компоненты данного препарата осуществляют блокаду перекисного окисления липидов и предотвращают синтез оксида азота, благодаря чему достигается антиоксидантное действие, что является не менее весомым вкладом в лечение последствий гипоксии.
Применение данного препарата в комплексе интенсивной терапии сопровождалось отсутствием развития эндогенной интоксикации, опасность которой заключается в реализации биологических эффектов эндотоксинов и усугублении полиорганной патологии [16], а также положительной клинической динамикой неврологической картины, что соответствует данным исследований сотрудников Санкт-Петербургской академии последипломного образования В.М. Шайтор и А.Б. Бичуну детей с перинатальными поражениями ЦНС.
Мы далеки от мысли, что использование депротеинизированного гемодиализата из крови молочных телят является панацеей при данной патологии, но наличие очевидного положительного эффекта в клинической и биохимической картине позволяет рекомендовать его к применению в комплексе интенсивной терапии у новорожденных, перенесших тяжелую асфиксию при рождении.
Выводы
1. Применение депротеинизированного гемодиализата из крови молочных телят в комплексе интенсивной терапии новорожденных, перенесших тяжелую асфиксию при рождении, положительно влияет на течение патологического процесса за счет снижения активности эндотелия и предотвращения развития эндогенной интоксикации.
2. Применение депротеинизированного гемодиализата из крови молочных телят в комплексе интенсивной терапии новорожденных, перенесших тяжелую асфиксию при рождении, положительно влияет на клиническую картину заболевания в виде улучшения дыхательной функции легких, сокращения длительности проведения искусственной вентиляции, положительной неврологической динамики, что сопровождается уменьшением времени пребывания больных в отделении анестезиологии и интенсивной терапии новорожденных.
1. Хубутия М.Ш. Селективная сорбция эндотоксина в комплексном лечении больных тяжелым сепсисом / М.Ш. Хубутия, М.М. Абакумов, И.В. Александрова, С.И. Рей, М.Е. Ильинский, В.Б. Хватов, Н.В. Боровкова, А.С. Перцев, В.Ю. Зинкин // Анестезиология и реаниматология. — 2010. — № 5. — С. 65-68.
2. Бондарь М.В. Молекулярные аспекты патогенеза грамположительного и грамотрицательного септического шока / М.В. Бондарь, И.П. Шлапак, О.М. Строгуш, В.И. Максименко, С.С. Боганова // Біль, знеболювання і інтенсивна терапія. — 2001. — № 2. — С. 73-75.
3. Останин А.А. Цитокинопосредованные механизмы развития системной иммуносупрессии у больных с гнойно-хирургической патологией / А.А. Останин, О.Ю. Леплина, М.А. Тихонова, Е.Я. Шевела, Е.В. Курганова, Е.И. Стрельцова, Е.Р. Черных // Цитокины и воспаление. — 2002. — № 1.
4. Ашиткова Н.В. Эффективность препарата рекомбинантного интерлейкина-2 человека в терапии неонатального сепсиса и тяжелых неонатальных инфекций / Н.В. Ашиткова, Н.Н. Володин, М.В. Дегтярева, И.Г. Солдатова, И.Д. Беляева, Т.Н. Эверстова, М.В. Кыштымов, Н.В. Давыдова, А.П. Продеус, А.Ю. Котов, А.С. Симбирцев // Педиатрия. — 2009. — Т. 87, № 3. — С. 80-85.
5. Березенко В.С. Функціональний стан ендотелію та системи L-аргінін NO у дітей з хронічними гепатитами / В.С. Березенко, Б.А. Тарасюк, О.Б. Динник, Н.І. Гончаренко // Перинатология и педиатрия. — 2006. — № 3(27). — С. 102-105.
6. Козлов И.А. Метиленовый синий как ингибитор гиперпродукции эндогенного оксида азота при коррекции постперфузионной сосудистой недостаточности / И.А. Козлов, В.Н. Попцов, А.В. Алферов // Вестник интенсивной терапии. — 2002. — № 4. — С. 7-11.
7. Габриэлян Н.И. Опыт использования показателя средних молекул в крови для диагностики нефрологических заболеваний у детей / Н.И. Габриэлян, В.И. Липатова // Лаб. дело. — 1984. — № 3. — С. 138-140.
8. Бережанская С.Б. Роль оксилипинов в формировании эндотелиальной дисфункции и нарушений гемостаза при перинатальной патологии / С.Б. Бережанская, А.С. Тодорова, Е.А. Лукьянова // Педиатрия. — 2011. — Т. 90, № 1. — С. 137-140.
9. Долгих В.Т. Нарушения коагуляционных свойств крови в раннем постреанимационном периоде и их профилактика / В.Т. Долгих, Ф.И. Разгонов, Л.Г. Шикунова // Анестезиология и реаниматология. — 2004. — № 6. — С. 35-40.
10. Kuninaka Т. Nature of enhanced mitochondrial oxidative metabolism by a calf blood extract / Т. Kuninaka, Y. Senga, H. Senga, M.J. Weiner // Cell Physiol. — 1991. — Vol. 146, № 1. — P. 148-155.
11. Ryuu H. Effect of solcoseryl on experimental cerebral injury: morphological studies of cerebral mitochondria. Kihon to Rinsho / H. Ryuu et al. // Clin. Report. — 1983. — Vol. 17, № 2. — P. 465-471.
12. Кузменко Г.Н. Клиническое значение нарушений регуляции функции эндотелия в развитии респираторного дистресс-синдрома у недоношенных новорожденных / Г.Н. Кузменко, В.В. Чемоданов, С.Б. Назаров // Педиатрия. — 2008. — Т. 87, № 1. — С. 22-27.
13. Шуматова Т.А. Роль оксида азота и цитокинов в развитии синдрома острого повреждения легких / Т.А. Шуматова, В.Б. Шуматов, Е.В. Маркелова, Л.Г. Сухотеплая // Вестник интенсивной терапии. — 2001. — № 1. — С. 15-19.
14. Hamazaki T. Blood viscosity and disease / T. Hamazaki et al. // Ther. Res. — 1985. — Vol. 2, № 1. — P. 64-70.
15. Kobayashi S. The effect of SS-094 on RBC fitrability / S. Kobayashi et al. // Cytoprot Biol. — 1983. — № 1. — P. 125-129.
16. Афанасьева А.Н. Синдромы эндогенной интоксикации и системного воспалительного ответа: общность и различия / А.Н. Афанасьева, И.Н. Одинцова, В.В. Удут // Анестезиология и реаниматология. — 2007. — № 4. — С. 67-71.

/126/126.jpg)
/127/127.jpg)
/128/128.jpg)