Газета «Новости медицины и фармации» Гастроэнтерология (537) 2015 (тематический номер)
Вернуться к номеру
Огляд: езомепразол у лікуванні гастроезофагеальної рефлюксної хвороби
Авторы: Kalaitzakis Evangelos, Björnsson Einar — Відділ внутрішньої медицини, підрозділ гастроентерології та гепатології, госпіталь університету Салгренска, Гетеборг, Швеція
Рубрики: Гастроэнтерология
Разделы: Справочник специалиста
Версия для печати
Статья опубликована на с. 7-16
Вступ
Гастроезофагеальний рефлюкс (ГЕРХ) — повернення шлункового вмісту в стравохід, що спричиняє виникнення симптомів рефлюксу, які негативно впливають на якість життя пацієнта, пов’язану зі здоров’ям, та/або зумовлюють ускладнення (Vakil та ін., 2006). Популяційні дослідження свідчать про те, що печія є надзвичайно поширеним симптомом у загальній популяції (10–20 % у західних країнах), проте далеко не всі дослідження є інформативними. Незважаючи на це, в Азії поширеність ГЕРХ-подібних симптомів більш низька і, згідно з повідомленнями, становить менше ніж 5 % (Dent та ін., 2005; Moayyedi і Talley, 2006). За результатами стандартної ендоскопії ГЕРХ розподіляється на рефлюксний езофагіт (ерозивна ГЕРХ) та ендоскопічно негативну рефлюксну хворобу (неерозивна рефлюксна хвороба, НЕРХ) (Moayyedi і Talley, 2006; Vakil та ін., 2006). У близько 50 % пацієнтів із даним захворюванням спостерігаються нормальні результати ендоскопічних досліджень, проведених у спеціалізованих клініках (Johansson та ін., 1986; Johnsson та ін., 1987), при цьому частота виявлення езофагіту в центрах первинної допомоги є більш низькою (Vakil та ін., 2006). Ерозивна ГЕРХ асоціюється з такими ускладненнями, як стравохідні стриктури та стравохід Барретта (Vakil та ін., 2006).
Інгібітори протонної помпи (ІПП) — це заміщені бензімідазоли, які приймають у вигляді кишковорозчинних таблеток або капсул, що проходять через шлунок та абсорбуються у дванадцятипалій кишці. Вони впливають на молекулу протонної помпи, розміщену на інтралюмінальній поверхні парієтальних клітин шлунка, здійснюючи інгібуючий вплив на секрецію кислоти (Hatlebakk, 2003). Езомепразол являє собою останній ІПП, що був синтезований у вигляді S-ізомеру омепразолу, який має досконаліші фармакокінетичні властивості (Hatlebakk, 2003; Kendall, 2003). ІПП є препаратами вибору для лікування ГЕРХ (Moayyedi і Talley, 2006).
Вважається, що езомепразол є дещо більш сильним інгібітором виділення кислоти порівняно з іншими ІПП (Hatlebakk, 2003; Kendall, 2003; Hellstrom і Vitols, 2004). Однак попередні доповіді свідчать про різні результати при порівнянні ефективності в усуненні ерозивної ГЕРХ, у підтримуючій терапії загоєної ерозивної ГЕРХ, а також у лікуванні НЕРХ з іншими ІПП. Було опубліковано деякі системні огляди та метааналізи, присвячені ефективності езомепразолу в лікуванні ерозивної ГЕРХ (Klok та ін., 2003; Vakil і Fennerty, 2003; Edwards та ін., 2006; Gralnek та ін., 2006). Метою цього системного огляду було надання нових даних про ефективність езомепразолу в пригніченні виділення соляної кислоти при короткотривалій та підтримуючій терапії ерозивної ГЕРХ та НЕРХ, а також у покращенні якості життя з точки зору здоров’я при ГЕРХ. У даному контексті також було застосовано порівняння з іншими ІПП.
Відбір даних
Нами було здійснено структурований електронний пошук у PuBMed з метою ідентифікації викладених англійською мовою рандомізованих клінічних випробувань за період із 2000 по 2006 рік, у яких проводилось порівняння езомепразолу з альтернативними ІПП у лікуванні ГЕРХ. Пошук джерел літератури — системних оглядів та метааналізів, у яких проводилося порівняння ефективності езомепразолу з іншими ІПП при ГЕРХ, здійснювався вручну для джерел, не знайдених за допомогою вищевказаної стратегії. Резюме з презентацій на конференціях, досліджень на тваринах, а також дані від виробників із неопублікованим повним текстом включені не були. Огляд літератури щодо езомепразолу та стравоходу Барретта або позастравохідних проявів ГЕРХ не належав до тематики даної статті.
Пригнічення секреції соляної кислоти
Незважаючи на те, що дослідники погоджуються з причинно-наслідковим зв’язком між ГЕРХ та порушенням моторики, наслідками порушення рівноваги між нормальними захисними факторами, такими як стравохідний кліренс, знижений тонус стравохідного сфінктера, а також агресивними факторами, до яких належать соляна кислота та пепсин, стає все більш зрозуміло, що ключем до контролю симптомів та вилікування езофагіту є зниження тривалості впливу поверненого кислотного вмісту (Hunt, 1999). Було продемонстровано, що вплив рефлюксату з рН 4,0 або нижче корелює з пошкодженням слизової оболонки та погіршує її здатність до проліферації та загоєння (Bell та ін., 1992; Hunt, 1999). Контроль симптомів ГЕРХ та загоєння ерозивної ГЕРХ може бути найкращим чином здійснено за рахунок підвищення рН шлункового соку до 4,0 та вище на якомога триваліший проміжок часу (Bell та ін., 1992; Hunt, 1999). Окрім цього, існують дані про те, що пацієнти з більш тяжким ступенем езофагіту мають аномально високі рівні впливу соляної кислоти вночі (Bell та ін., 1992). Виразковий езофагіт, стравохідні стриктури, а також стравохід Барретта характеризуються високим відсотком тривалості нічного рефлюксу кислого вмісту в період пригнічення (Frazzoni та ін., 2003), що вказує на необхідність контролю нічної секреції кислоти.
ІПП знижують секрецію шлункової кислоти за рахунок пригнічення активності шлункової H+/К+-АТФази. У кислому середовищі шлунка вони приєднують протони, перетворюючись в активні форми, що необоротно зв’язуються з H+/К+-АТФазою та інактивують її (Hunt, 1999; Hatlebakk, 2003; Hellstrom і Vitols, 2004). Всі ІПП блокують останній етап ланцюга секреції шлункового соку і є ефективними як в період базальної, так і стимульованої секреції соляної кислоти (Hunt, 1999; Hellstrom і Vitols, 2004).
Вплив езомепразолу на кислотність шлункового соку
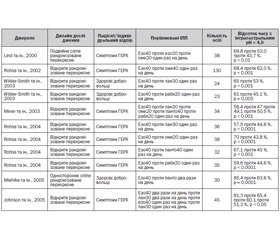
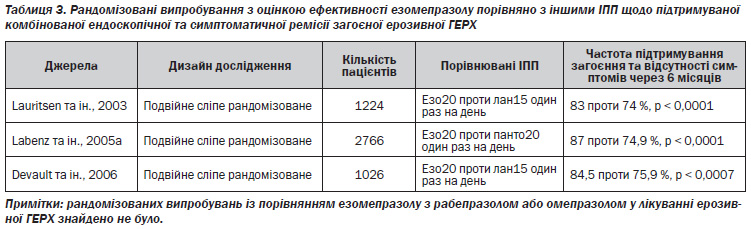
Нещодавно в кількох перехресних дослідженнях було проведено порівняння регуляції виділення соляної кислоти езомепразолом з іншими ІПП у пацієнтів із ГЕРХ або здорових осіб. Як показано в табл. 1, усі дослідження продемонстрували вищу ефективність езомепразолу в дозуванні 40 мг один раз на день у підтриманні інтрагастрального рН на рівні 4,0 або нижче порівняно з іншими ІПП, отримуваними в стандартних дозах. Ті самі дослідження підтвердили перевагу езомепразолу 40 мг один раз на день над усіма іншими ІПП в стандартних дозах з точки зору досягнення вищого 24-годинного медіанного показника інтрагастрального рН, а також за кількістю пацієнтів, у яких було досягнуто рівень інтрагастрального рН > 4,0 протягом не менше як 12 годин на день. Нічний рівень рН встановлювали в одному з цих досліджень, у яких езомепразол 40 мг порівнювали з пантопразолом 40 мг два рази на день (Miehlke та ін., 2005). Вночі відсоток тривалості інтрагастрального рН > 4,0 становив 85,4 % для езомепразолу та 63,6 % для пантопразолу (р = 0,0001). Нічний кислотний «прорив», визначений як рівень інтрагастрального рН < 4,0 протягом щонайменше однієї послідовної години в межах інтервалу з 10-ї години вечора до 6-ї години ранку, спостерігався у 26,7 % суб’єктів, які отримували езомепразол, та у 73,3 % таких, які отримували пантопразол (р = 0,009) (Miehlke та ін., 2005). Даних про вплив езомепразолу на нічний рівень рН порівняно з іншими ІПП значно бракує.
У певних ситуаціях доцільно використовувати вищі за рекомендовані дози ІПП, що часто розподіляють на два прийоми. Останні включають діагностичне випробування при болях за грудиною некардіального генезу, випробування з емпіричним лікуванням при надстравохідних симптомах ГЕРХ, випадки часткової відповіді на стандартні дози терапії, випадки з симптомами кислотного прориву, пацієнтів із ГЕРХ із порушенням моторики стравоходу тяжкого ступеня, а також стравоходом Барретта (DeVAult і Castell, 2005).
У нещодавно проведеному подвійному сліпому рандомізованому перехресному дослідженні проводилась оцінка 24-годинного профілю інтрагастрального рН під впливом езомепразолу 40 мг два рази на день проти 20 мг два рази на день проти 40 мг один раз на день у 25 здорових добровольців (Katz та ін., 2004). Під впливом езомепразолу 40 мг два рази на день вдалося досягнути інтрагастрального рН > 4,0 середньою тривалістю 19,2 години (80,1 % 24-годинного інтервалу, 95% довірчий інтервал (ДІ) 74,5–85,7 %) проти 14,2 години з 40 мг один раз на день (59,2 %, 95% ДІ 53,7–64,7 %) та 17,5 години з 20 мг два рази на день (73,0 %, 95% ДІ 67,4–78,5 %). Відсоток часу в межах 24-годинного періоду, протягом якого рівень рН залишався більше ніж 4,0, був значно вищим на фоні прийому езомепразолу два рази на день порівняно з режимом 40 мг один раз на день у період пригнічення (сну) моніторингу (83,7 % (95% ДІ 74,9–92,4 %) для езомепразолу 40 мг два рази на день проти 79,2 % (95% ДІ 70,5–87,9 %) для езомепразолу 20 мг два рази на день проти 57,9 % (95% ДІ 49,0–66,9 %) для езомепразолу 40 мг один раз на день (Katz та ін., 2004). Езомепразол 40 мг два рази на день також продемонстрував перевагу над пантопразолом 40 мг два рази на день та лансопразолом 30 мг два рази на день у підтриманні інтрагастрального рН на рівні 4,0 та нижче (табл. 1). Ці дані свідчать, що доза омепразолу, розподілена на два прийоми, викликає значно більш виражене пригнічення виділення кислоти порівняно з одноразовим прийомом і, таким чином, може бути доцільною альтернативою для пацієнтів, які потребують більш суттєвого зниження кислотності при ГЕРХ.
Вплив езомепразолу на кислотність стравохідного середовища
У двох дослідженнях будо проведено оцінку впливу езомепразолу на профіль внутрішньостравохідного рН порівняно з іншими ІПП. У подвійному сліпому рандомізованому перехресному дослідженні за участю 35 пацієнтів із симптомами ГЕРХ езомепразол 40 мг один раз на день порівнювали з пантопразолом 40 мг один раз на день з оцінкою впливу препаратів на рівень внутрішньостравохідного рН (Simon та ін., 2003). На вихідному рівні медіана процентного відношення всієї тривалості з рН < 4,0 становила 20,1 % у групі езомепразолу та 21,3 % у групі пантопразолу. Через 7 днів повторного прийому відбулося скорочення даного проміжку часу до 0,9 та 2,6 % відповідно, при цьому середня різниця для окремого учасника між середніми 24-годинними показниками рН, а саме між показниками до та після лікування, становила 19,2 та 18,7 % відповідно. Оцінка середньої різниці за Ходжесом — Леманом для окремого учасника між середніми 24-годинними показниками рН, а саме між показниками до та після лікування для двох ІПП, становила 2,86 %, і відповідний 90% довірчий інтервал знаходився в межах діапазону еквівалентності, встановленого на рівні ± 10 % (90% ДІ 2,27–7,07) (Simon та ін., 2003). В іншому відкритому рандомізованому дослідженні здійснювалось порівняння езомепразолу 40 мг з лансопразолом 30 мг один раз на день у 30 пацієнтів з ускладненою ГЕРХ (Frazzoni та ін., 2006). Нормалізація загальної експозиції стравохідного середовища під впливом кислоти, а також експозиції в період нічного пригнічення, була досягнута у 75 проти 28 % (р = 0,026) та 93 проти 50 % (р = 0,012) пацієнтів у групі езомепразолу та в групі лансопразолу відповідно (Frazzoni та ін., 2006).
Ерозивна ГЕРХ
Було здійснено огляд рандомізованих випробувань впливу езомепразолу на загоєння ерозивної ГЕРХ або як підтримуючої терапії при усуненні ерозивної ГЕРХ.
Загоєння ерозивної ГЕРХ
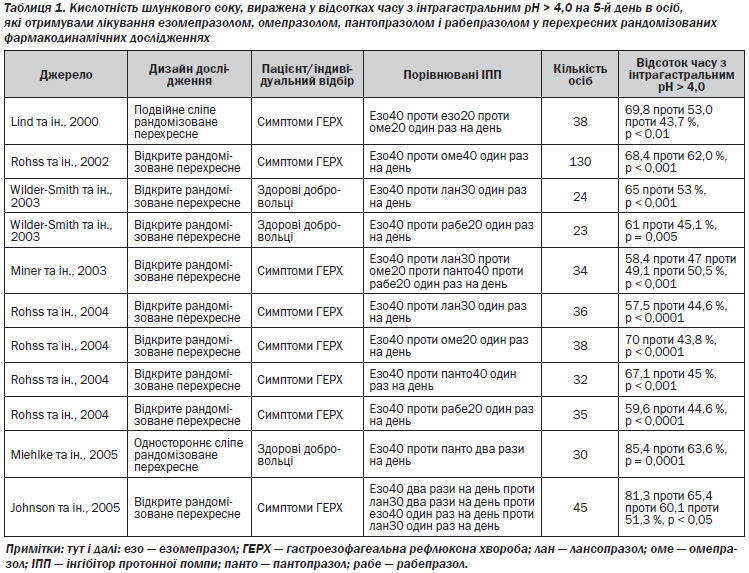
У декількох клінічних випробуваннях було проведено порівняння езомепразолу з іншими ІПП з точки зору загоєння ерозивної ГЕРХ (табл. 2). Наведені в табл. 2 дослідження мають подібний дизайн подвійних сліпих рандомізованих досліджень; останні включали аналіз в когорті пацієнтів з призначеним лікуванням (intention-to-treat) частоти загоєння і як вторинну кінцеву точку оцінку терапевтичного впливу на симптоматику ГЕРХ. Таким чином, усі дослідження включали пацієнтів із підтвердженою при ендоскопії ерозивною ГЕРХ на початковому рівні. Контрольна ендоскопія проводилась на 4-му та 8-му тижнях за винятком одного дослідження, у якому пацієнти проходили першу контрольну ендоскопію на 4-му або 6-му тижні, а другу контрольну ендоскопію — на 8-му або 10-му тижні (Gillessen та ін., 2004). Незважаючи на те, що було ідентифіковано як мінімум два рандомізованих дослідження з порівнянням езомепразолу з кожним з інших ІПП, порівняльних досліджень езомепразолу та рабепразолу при ерозивній ГЕРХ знайдено не було.
П’ять із 8 досліджень продемонстрували, що на фоні прийому езомепразолу 40 мг один раз на день удалося досягнути більш високої частоти загоєння ерозивного езофагіту після 4 та 8 тижнів лікування порівняно з омепразолом 20 мг, лансопразолом 30 мг або пантопразолом 40 мг один раз на день (табл. 2). Загальна кількість пацієнтів, які брали участь у даних випробуваннях, становила 13 797 осіб. Вища за омепразол, лансопразол або пантопразол ефективність езомепразолу була однозначно підтверджена при коригуванні її за ступенями тяжкості езофагіту на вихідному рівні відповідно до Лос-Анджелеської класифікації. Окрім цього, всі дані дослідження продемонстрували вищу ефективність езомепразолу 40 мг один раз на день порівняно з омепразолом 20 мг, лансопразолом 30 мг або пантопразолом 40 мг один раз на день у досягненні усунення ГЕРХ-асоційованих симптомів (Kahrilas та ін., 2000; Richter та ін., 2001; Castell та ін., 2002; Fennerty та ін., 2005; Labenz та ін., 2005b). Цікаво, що всі ці дослідження були проведені за підтримки виробника езомепразолу.
Незважаючи на це, 3 з 8 порівняльних досліджень за участю всього 1659 пацієнтів засвідчили відсутність вірогідної різниці в частоті загоєння на 4-му або 8-му тижнях між езомепразолом 40 мг один раз на день та омепразолом 20 мг, лансопразолом 30 мг або пантопразолом 40 мг один раз на день. Одне з цих досліджень продемонструвало значно вищу частоту загоєння на фоні прийому езомепразолу порівняно з омепразолом на 4-му тижні (60,8 проти 47,9 %, р = 0,02) та 8-му тижні (88,4 проти 77,5 %, р = 0,007) у пацієнтів з ерозивним езофагітом середнього та тяжкого ступенів (ступінь C або D за Лос-Анджелеською класифікацією) на вихідному рівні, при цьому не показавши вірогідної різниці в пацієнтів з ерозивним езофагітом легкого ступеня (ступінь A або В за Лос-Анджелеською класифікацією) (Schmitt та ін., 2006). У даних дослідженнях повідомлялось про подібну ефективність езомепразолу порівняно з омепразолом, лансопразолом або пантопразолом за наявності ГЕРХ-асоційованих симптомів (Howden та ін., 2002; Gillessen та ін., 2004; Schmitt та ін., 2006). Одне з трьох даних досліджень проводилось за підтримки виробника езомепразолу та продемонструвало деякі переваги езомепразолу в пацієнтів з езофагітом більш тяжкого ступеня (Schmitt та ін., 2006). Інші два дослідження були підтримані виробниками лансопразолу й підтвердили відсутність різниці між лансопразолом та езомепразолом (Howden та ін., 2002), а також виробником пантопразолу і підтвердили відсутність різниці між пантопразолом та езомепразолом (Gillessen та ін., 2004). Еквівалентність езомепразолу 40 мг та пантопразолу 40 мг один раз на день у лікуванні ГЕРХ-асоційованих симптомів у пацієнтів з ерозивною ГЕРХ була також підтверджена результатами подвійного сліпого рандомізованого дослідження, у якому брали участь 217 пацієнтів з езофагітом (Scholten та ін., 2003). У даному випробуванні контрольні ендоскопічні дослідження не проводились, що унеможливило підрахунок даних про частоту загоєння (Scholten та ін., 2003).
Було продемонстровано, що інфекція Helicobacter pylori підвищує рівень інтрагастрального рН, досягнутого завдяки ІПП (Verdu та ін., 1995; Labenz та ін., 1996). У дослідженні з пантопразолом було висловлено припущення, що підвищена ефективність ІПП у пацієнтів з інфекцією Helicobacter pylori може бути пов’язана з покращеним контролюванням симптомів, а також більш швидким загоєнням езофагіту (Holtmann та ін., 1999).
Більше того, також повідомлялось, що ерадикація H.pylori є предиктором невдалого лікування ГЕРХ омепразолом 20 мг один раз на день (Wu та ін., 2004), однак даний результат не був відтворений в іншому дослідженні (Kuipers та ін., 2004). У результаті останнього перегляду з даної тематики були зроблені висновки про те, що питання про необхідність ерадикації H.pylori в пацієнтів із ГЕРХ залишається невизначеним (Delaney та McColl, 2005). В усіх розглянутих дослідженнях у включених пацієнтів проводилось визначення статусу H.pylori. Значний вплив інфекції H.pylori було підтверджено в одному з досліджень із порівнянням омепразолу 40 мг з пантопразолом 40 мг один раз на день за участі H.pylori-негативних пацієнтів із більш низькою частотою загоєння порівняно з H.pylori-позитивними пацієнтами (Labenz та ін., 2005b). Різниці між H.pylori-негативними та H.pylori-позитивними пацієнтами з ГЕРХ в ефективності езомепразолу в дослідженнях, у яких проводилась дана оцінка, встановлено не було (Kahrilas та ін., 2000; Richter та ін., 2011; Castell та ін., 2002; Gillessen та ін., 2004; Fennery та ін., 2005; Labenz та ін., 2005b; Schmitt та ін., 2006). Однак слід взяти до уваги, що вплив статусу H.pylori на вилікування езофагіту слугував лише вторинною кінцевою точкою даних досліджень.
Було виділено п’ять метааналізів ефектів різноманітних ІПП (Edwards та ін., 2001, 2006; Klok та ін., 2003; Vakil та Fennerty, 2003; Gralnek та ін., 2006), три з яких були сфокусовані на оцінці ефективності різноманітних ІПП (включаючи езомепразол) у загоєнні ерозивного езофагіту (Edwards та ін., 2001, 2006; Gralnek та ін., 2006). У нещодавно проведеному метааналізі, присвяченому порівнянню ефективності ІПП при короткотривалому використанні (Klok та ін., 2003), було розглянуто два дослідження з оцінкою ефективності частоти загоєння на фоні прийому езомепразолу 40 мг проти омепразолу 20 мг один раз на день (Kahrilas та ін., 2000; Richter та ін., 2001). Автори дійшли висновку про перевагу езомепразолу над омепразолом (відносний ризик 1,18; 95% ДІ 1,14–1,23) (Klok та ін., 2003). Інший метааналіз, у якому порівнювалась ефективність ІПП у веденні ГЕРХ та пептичної виразкової хвороби (Vakil та Fennerty, 2003), включав три дослідження з порівнянням езомепразолу 40 мг один раз на день з омепразолом 20 мг один раз на день (Kahrilas та ін., 2000; Richter та ін., 2001) або з лансопразолом 30 мг один раз на день (Castell та ін., 2002). Автори дійшли висновку, що езомепразол мав перевагу над обома іншими ІПП, з якими він порівнювався, у загоєнні ерозивного езофагіту, а також стосовно швидкості усунення симптомів (Vakil та Fennerty, 2003). У метааналіз ефективності ІПП при короткотривалому лікуванні рефлюксного езофагіту (Edwards та ін., 2001) було включено три дослідження з порівнянням езомепразолу 40 мг з омепразолом 20 мг один раз на день. Два з останніх були також проаналізовані в даному огляді (Kahrilas та ін., 2000; Richter та ін., 2001), однак Edwards та ін. (2001) також використовували дані досьє езомепразолу від виробника. Вони дійшли висновків про те, що езомепразол продемонстрував більшу частоту загоєння, аніж омепразол, на 4-му тижні (відносний ризик 1,14; 95% ДІ 1,10–1,18) та 8-му тижні (відносний ризик 1,08; 95% ДІ 1,05–1,10) (Edwards та ін., 2001). В іншому метааналізі, проведеному тими самими дослідниками, з порівнянням езомепразолу з іншими ІПП у загоєнні ерозивного езофагіту (Edwards та ін., 2006) включали всі рандомізовані дослідження, коротко викладені в табл. 2. Автори дійшли висновку, що езомепразол продемонстрував більш високу частоту вилікування порівняно зі стандартними дозами ІПП на 4-му тижні (відносний ризик 0,92; 95% ДІ 0,90–0,94; p < 0,00001) та на 8-му тижні (відносний ризик 0,95; 95% ДІ 0,94–0,97; р < 0,00001) (Edwards та ін., 2006). Нарешті, метааналіз рандомізованих клінічних випробувань із порівнянням езомепразолу з іншими блокаторами ІПП щодо загоєння ерозивного езофагіту (Gralnek та ін., 2006) включав 7 із 8 рандомізованих досліджень, коротко викладених в табл. 2 (Kahrilas та ін., 2000; Richter та ін., 2001; Catell та ін., 2002; Howden та ін., 2002; Gillessen та ін., 2004; Fennerty та ін., 2005; Labenz та ін., 2005b), дані від виробника езомепразолу, внесені до інформації про продукт (езомепразол проти омепразолу 20 мг один раз на день), а також дослідження, опубліковане у вигляді резюме (езомепразол 40 мг один раз на день проти омепразолу 40 мг один раз на день). Останні два вищенаведені дослідження опубліковані не були і тому можуть бути потенційним джерелом статистичної похибки в даному контексті. При порівнянні частоти загоєння ерозивного езофагіту на 4-му та 8-му тижнях авторами було визначено 10% (відносний ризик 1,10; 95% ДІ 1,05–1,15) та 5% (відносний ризик 1,05; 95% ДІ 1,02–1,08) відносне підвищення ймовірності загоєння відповідно для езомепразолу порівняно з альтернативними ІПП. Таким чином, автори встановили, що езомепразол зумовив 8% (відносний ризик 1,08; 95% ДІ 1,05–1,11) відносне підвищення ймовірності усунення симптоматики ГЕРХ на 4-му тижні (Gralnek та ін., 2006). У даному метааналізі підрахована чисельність популяції з необхідністю лікування за Лос-Анджелеською шкалою ерозивного гастриту (ступені A-D) становила 50, 33, 14 та 8 (Gralnek та ін., 2006). Це свідчить про те, що переваги езомепразолу можуть відігравати важливу роль саме стосовно більш тяжкого ступеня ерозивного захворювання, на що вказує зниження чисельності популяції з необхідністю лікування з високим ступенем тяжкості за Лос-Анджелеською шкалою (Gralnek та ін., 2006). На даний момент залишається не до кінця вирішеним питання про те, чи є дана статистично значуща різниця клінічно значущою.
Підтримуюча терапія загоєної ГЕРХ
Рецидив ГЕРХ, як правило, має місце при відміні медикаментозної терапії, при цьому у 80 % пацієнтів із ГЕРХ рецидив настає після 6–12 місяців (DeVault і Castell, 2005; Moayyedi і Talley, 2006). Відповідно до цього багато пацієнтів із ГЕРХ потребують тривалої терапії ІПП, можливо, впродовж усього життя (Moayyedi і Talley, 2006). Незважаючи на це, нещодавно проведене дослідження щодо відміни терапії ІПП у пацієнтів із довготривалим лікуванням свідчить про те, що 20 % пацієнтів із ГЕРХ мали змогу завершити прийом ІПП без розвитку симптоматики (Bjornsson та ін., 2006).
Два подвійні сліпі рандомізовані дослідження продемонстрували перевагу езомепразолу 40, 20 або 10 мг один раз на день порівняно з плацебо як підтримуючої терапії загоєної ерозивної ГЕРХ (Johnson та ін., 2001; Vakil та ін., 2001). Первинною кінцевою точкою обох досліджень було підтверджене ендоскопією підтримуване загоєння через 6 місяців після залучення в дослідження. В одному з них 375 пацієнтів з ендоскопічно діагностованим загоєним езофагітом були рандомізовані для отримання езомепразолу 40, 20, 10 мг або плацебо один раз на день (Vakil та ін.). Через 6 місяців у вірогідно (р < 0,001) більшої кількості пацієнтів при ендоскопії було виявлено підтримуване загоєння на фоні лікування езомепразолом 40 мг (87,9 %), 20 мг (78,7 %) або 10 мг (54,2 %) порівняно з групою плацебо (29,1 %) (Vakil та ін., 2001). В іншому плацебо-контрольованому дослідженні 318 пацієнтів з ендоскопічно підтвердженим загоєнням ерозивної ГЕРХ були рандомізовані для отримання езомепразолу 40, 20, 10 мг або плацебо один раз на день (Johnson та ін., 2001). Через 6 місяців загоєння зберігалося у 93,6 % пацієнтів, які отримували лікування езомепразолом 40 мг, у 93,2 % — езомепразолом 20 мг, у 57,1 % — езомепразолом 10 мг; р < 0,001, проти 29,1 % пацієнтів, які отримували плацебо (Johnson та ін., 2001). В обох дослідженнях повідомлялось про те, що пацієнти групи езомепразолу мали менш виражені прояви печії порівняно з групою плацебо. Незважаючи на це, дані цих досліджень стосовно підтримуваного загоєння слід інтерпретувати з обережністю, оскільки продовжували відвідувати лікаря протягом 6-місячного періоду дослідження лише ті пацієнти, у яких загоєння підтримувалося під час попереднього візиту (Johnson та ін., 2001; Vakil та ін., 2001).
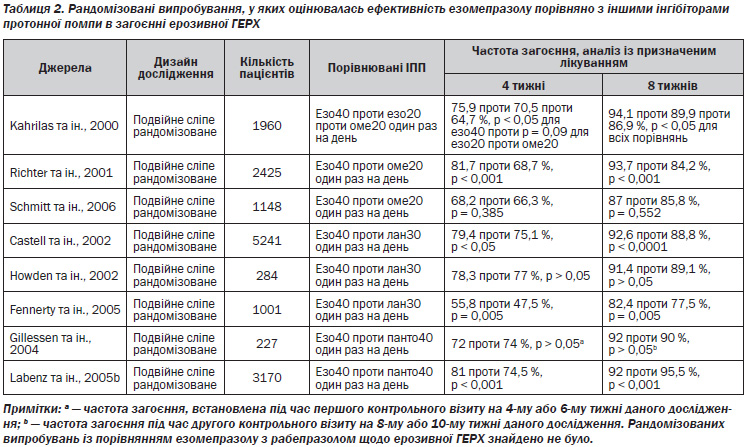
У трьох клінічних випробуваннях здійснювалось порівняння езомепразолу з іншими ІПП як підтримуючою терапією в пацієнтів із ГЕРХ та загоєним ерозивним езофагітом (табл. 3). Вказані в табл. 3 дослідження мали подібний подвійний сліпий рандомізований дизайн і включали аналізи частоти підтримуваного загоєння за даними ендоскопії та відсутності симптомів у групах із призначеним лікуванням. Таким чином, всі три дослідження включали пацієнтів із підтвердженим при ендоскопії загоєнням у них ерозивної ГЕРХ на вихідному рівні, при цьому контрольна ендоскопія проводилась на 3-му та 6-му місяцях. Первинною кінцевою точкою було підтверджене ендоскопічно підтримуване загоєння та відсутність симптомів на 6-му місяці. Вторинними кінцевими точками були окремо частота підтвердженого ендоскопічно підтримуваного загоєння та частота відсутності симптомів на 6-му місяці (Leuritsen та ін., 2003; Labenz та ін., 2005а; Devault та ін., 2006). Порівняльних досліджень езомепразолу проти омепразолу або рабепразолу в підтримуючій терапії загоєної ерозивної ГЕРХ знайдено не було.
Всі три дослідження продемонстрували перевагу езомепразолу 20 мг порівняно з лансопразолом 15 мг або пантопразолом 20 мг один раз на день порівняно з первинною кінцевою точкою (табл. 3).
Більше того, дані дослідження засвідчили перевагу езомепразолу 20 мг над лансопразолом 15 мг (частота підтримуваного ендоскопічного загоєння: 84 проти 76 %; р < 0,0002 (Lauritsen та ін., 2003); 84,5 проти 75,9 %, р < 0,0001) (Devault та ін., 2006) або пантопразолом 20 мг (88,1 проти 76,6 %, р < 0,0001) (Labenz та ін., 2005а) один раз на день у підтриманні ендоскопічної ремісії на 6-му місяці. З точки зору підтримання лише симптоматичної ремісії в одному з цих досліджень повідомлялось про те, що езомепразол 20 мг був більш ефективним, аніж лансопразол 15 мг один раз на день (частота підтримання симптоматичної ремісії: 78 проти 71 %, р < 0,001) (Lauritsen та ін., 2003), а в іншому — що езомепразол 20 мг був більш ефективним за пантопразол 20 мг один раз на день (94,5 проти 90,5 %, р < 0,0001) (Labenz та ін., 2005а). Незважаючи на це, третє дослідження не продемонструвало статистично вірогідної різниці між езомепразолом та лансопразолом 15 мг один раз на день у підтриманні симптоматичної ремісії (76,4 проти 73 %, р > 0,05) (Devault та ін., 2006). І нарешті, дослідження з порівнянням езомепразолу з лансопразолом підтвердили те, що для езомепразолу характерна значно вища частота підтримання ремісії за умови стратифікації пацієнтів згідно з вихідним ступенем тяжкості ерозивної ГЕРХ (Lauritsen та ін., 2003; Devault та ін., 2006). Однак у дослідженні з порівнянням езомепразолу 20 мг з пантопразолом 20 мг один раз на день повідомлялось про те, що, незважаючи на вищу частоту підтримання ремісії на фоні лікування езомепразолом у пацієнтів з ерозивною ГЕРХ ступенів А–С за Лос-Анджелеською класифікацією, різниця в пацієнтів зі ступенем D Лос-Анджелеської класифікації статистично вірогідною не була (Labenz та ін., 2005а).
Незважаючи на те, що ці дані вказують на перевагу езомепразолу порівняно з лансопразолом або пантопразолом у підтримуючій терапії загоєної ерозивної ГЕРХ, для більш чітких висновків необхідне проведення нових клінічних випробувань із порівнянням езомепразолу з омепразолом та рабепразолом.
Неерозивна ГЕРХ
Пацієнти з НЕРХ можуть мати той самий ступінь тяжкості симптомів, що і пацієнти з ерозивною ГЕРХ, однак половина з них може продемонструвати нормальні результати стравохідного рН-моніторингу з рН у межах норми для здорових суб’єктів (Martinez та ін., 2003). Незважаючи на підтверджену досвідом ефективність ІПП у пацієнтів із НЕРХ (Lind та ін., 1997), покращення симптоматики в них досягалося більш повільно порівняно з пацієнтами з ерозивною ГЕРХ (Martinez та ін., 2003).
Було ідентифіковано три документи клінічних випробувань, у яких проводилось порівняння постійного прийому езомепразолу з іншими ІПП як терапії пацієнтів з НЕРХ. Усі вони характеризувались подібним подвійним сліпим рандомізованим дизайном, при цьому пацієнти мали нормальні результати ендоскопії на вихідному рівні; було проведено аналіз даних групи з призначеним лікуванням, а тривалість дослідження становила 4 тижні (Armstrong та ін., 2004; Fock та ін., 2005; Monnikes та ін., 2005). Досліджень із порівнянням тривалої терапії езомепразолом та лансопразолом при НЕРХ ідентифіковано не було.
В одному з цих документів (Armstrong та ін., 2004) було наведено три дослідження, у яких здійснювалось порівняння: А (n = 1282) — езомепразолу 40 мг, езомепразолу 20 мг або омепразолу 20 мг один раз на день; В (n = 693) — езомепразолу 40 мг або омепразолу 20 мг один раз на день; С (n = 670) — езомепразолу 20 мг або омепразолу 20 мг один раз на день. Усунення симптомів печії на 4-му тижні (відсутність симптомів печії протягом останніх 7 днів) відбулося в однакового відсотка пацієнтів у кожній групі лікування дослідження А (езомепразолу 40 мг, 56,7 %; езомепразолу 20 мг, 60,5 %; омепразолу 20 мг, 58,1 %), дослідження В (езомепразолу 40 мг, 70,3 %; омепразолу 20 мг, 67,9 %) і дослідження С (езомепразолу 20 мг, 61,9 %; омепразолу 20 мг, 59,6 %). Вірогідної різниці між групами лікування в жодному дослідженні не спостерігалось. Таким чином, порівнюване лікування езомепразолом та омепразолом, а також і езомепразолом 40 мг та езомепразолом 20 мг один раз на день не дали статистично вірогідної різниці результатів після 4 тижнів у пацієнтів із НЕРХ (Armstrong та ін., 2004).
В іншому клінічному випробуванні за участю пацієнтів з Азії (n = 127) із НЕРХ здійснювалось порівняння езомепразолу 20 мг із рабепразолом 10 мг один раз на день (Fock та ін., 2005). Через 4 тижні лікування два інгібітори протонної помпи були подібні відносно первинної кінцевої точки дослідження, що являла собою проміжок часу, необхідний для досягнення 24-годинного безсимптомного інтервалу щодо печії (езомепразол 20 мг, 9 днів; рабепразол 10 мг, 8,5 дня, р > 0,05) та регургітації (езомепразол 20 мг, 7,5 дня; рабепразол 10 мг, 6 днів, р > 0,05). Автори повідомляли, що обидва препарати були подібні з точки зору загальної оцінки пацієнта, при цьому 87,9 % пацієнтів, які отримували езомепразол, та 96 % пацієнтів, які отримували рабепразол, повідомляли про покращення симптомів (р > 0,05) (Fock та ін., 2005).
Третє дослідження з порівняння езомепразолу 20 мг з пантопразолом 20 мг один раз на день, призначених із метою лікування пацієнтів із НЕРХ (n = 529), продемонструвало медіану часового проміжку до першого купірування симптому, рівну 2,0 дня для обох ІПП (Monnikes та ін., 2005). Дане дослідження розроблене з метою засвідчення не гіршої ефективності в групі пантопразолу порівняно з групою езомепразолу з рівнем вірогідності 5 %. Було підраховано показник середнього Ходжеса — Лемана, а також 95% ДІ за Мозесом. Висновок про не гіршу ефективність отримували за умови, якщо нижня межа 95% ДІ перевищувала –2 дні, оскільки різниця в 2 дні вважалась статистично вірогідною. Для перемінної первинної кінцевої точки (проміжок часу до першого купірування симптомів) односторонній 95% ДІ був рівний нулю (0,00). З огляду на встановлену на рівні –2 дні межу не гіршої ефективності нижня межа 95% ДІ (0,00) була вищою. Таким чином, автори дійшли висновку про те, що пантопразол є так само ефективним, як езомепразол, щодо проміжку часу до першого купірування симптому. Аналогічні результати були стосовно часового проміжку до отримання стабільного купірування симптомів (Monnikes та ін., 2005).
Незважаючи на те, що жодного випробування, присвяченого порівнянню постійної терапії езомепразолом із лансопразолом, ідентифіковано не було, у нещодавно проведеному односторонньому сліпому дослідженні порівнювали езомепразол 20 мг за потреби з лансопразолом 15 мг один раз на день (Tsai та ін., 2004). Сімсот сімдесят чотири пацієнти з НЕРХ, які досягли повного усунення симптомів печії після короткотривалого лікування (2–4 тижні) езомепразолом 20 мг, були рандомізовані для отримання або езомепразолу 20 мг за потребою, або лансопразолу 15 мг щоденно постійно. Після 6 місяців значно більша кількість пацієнтів виявили бажання продовжувати приймати езомепразол за потребою, аніж лансопразол один раз на день (93 проти 88 %, р = 0,02). Автори дійшли висновку про те, що езомепразол 20 мг за потребою був більш прийнятним для пацієнтів із НЕРХ порівняно з лансопразолом 15 мг один раз на день (Tsai та ін., 2004). Тим не менше слід звернути увагу на те, що дане випробування було одностороннім сліпим (через дизайн), що може серйозно ускладнювати отримання доказових даних переваг езомепразолу над лансопразолом при НЕРХ, оскільки обидва ІПП приймались по-різному. Отож, результати даного дослідження можуть слабо відображати надавання пацієнтами переваги терапії за потребою.
Тривале (6 місяців) лікування езомепразолом за потребою продемонструвало переваги над плацебо в лікуванні пацієнтів із НЕРХ згідно з результатами двох подвійних сліпих рандомізованих клінічних випробувань, у яких пацієнти з НЕРХ брали участь після досягнення повного усунення печії після короткотривалого лікування езомепразолом або омепразолом (Talley та ін., 2001, 2002). В одному з них 342 пацієнти з НЕРХ були рандомізовані для отримання або езомепразолу 20 мг, або плацебо за потребою протягом 6 місяців (Talley та ін., 2001). Частка пацієнтів, які передчасно завершили лікування через недостатній контроль печії, була значно вищою в групі плацебо порівняно з пацієнтами, які приймали езомепразол (51 проти 14 %, р < 0,0001). У другому дослідженні 721 пацієнт був рандомізований у групи езомепразолу 20, 40 мг або плацебо, які приймались за потребою протягом 6 місяців (Talley та ін., 2002). Протягом даного періоду 42 % пацієнтів, які приймали плацебо, передчасно завершили лікування через небажання продовжувати його порівняно з 8 та 11 % пацієнтів, які отримували езомепразол 20 та 40 мг відповідно. Незважаючи на те, що підрахований показник р становив < 0,0001 для порівнянь між групами езомепразолу та плацебо, вірогідної різниці між групами езомепразолу встановлено не було (р = 0,15). Таким чином, автори зробили висновок про те, що езомепразол 20 мг має переваги над плацебо в рамках лікування НЕРХ за потребою, а також про те, що вищі дози езомепразолу не дають додаткового позитивного клінічного ефекту. Однак слід звернути увагу на те, що практично 60 % (58 %) пацієнтів, які були рандомізовані в групу плацебо, виявили бажання продовжувати лікування (Talley та ін., 2002). Дані результати чітко свідчать про те, що не всі пацієнти, у яких настало усунення симптомів після 4 тижнів терапії ІПП, будуть потребувати постійного лікування в подальшому.
Езомепразол у лікуванні ГЕРХ та покращенні якості життя, пов’язаної зі здоров’ям
Останнім часом усе більший інтерес викликає оцінка повідомлених пацієнтом результатів, таких як якість життя, пов’язана зі здоров’ям. Широко відомо, що в пацієнтів, які переносять ГЕРХ, має місце погіршення якості життя, пов’язаної зі здоров’ям, порівняно із загальною популяцією (Revicki та ін., 1998; Prasad та ін., 2003; Pace та ін., 2005), що властиво також іншим пацієнтам з іншими хронічними захворюваннями (Kulig та ін., 2003). Повідомлялось про те, що пацієнти з неерозивною ГЕРХ, ерозивною ГЕРХ, стравоходом Барретта мають подібні прояви порушення якості життя, пов’язаної зі здоров’ям (Kulig та ін., 2003). Успішне лікування ГЕРХ з усуненням симптомів сприяє покращенню пов’язаної зі здоров’ям якості життя (Revicki та ін., 1998; Prasad та ін., 2003).
У нещодавно проведеному широкомасштабному неконтрольованому дослідженні з аналізом впливу ГЕРХ на якість життя, а також ефекту короткотривалої терапії езомепразолом на якість життя було проведено оцінку показників (Kulig та ін., 2003). Сумарно 6215 пацієнтів, у яких було проспективно діагностовано ГЕРХ, пройшли ендоскопію та отримували лікування езомепразолом 20 мг один раз на день (пацієнти з НЕРХ) або 40 мг один раз на день (ерозивна ГЕРХ). Симптоми та якість життя, пов’язана зі здоров’ям, були проаналізовані на вихідному рівні та після 2 тижнів лікування з використанням валідованих анкет (Kulig та ін., 2003). На вихідному рівні якість життя пацієнтів із ГЕРХ була нижчою за таку в загальній популяції, однак протягом 2 тижнів після лікування езомепразолом спостерігалась позитивна динаміка як симптомів, так і якості життя за всіма підшкалами (Kulig та ін., 2003).
У нещодавно проведеному широкомасштабному рандомізованому дослідженні було здійснено оцінку довготривалого ефекту обох варіантів підтримуючого лікування езомепразолом при неерозивній та ерозивній ГЕРХ легкого ступеня (Pace та ін., 2005). Всього 6017 пацієнтів із симптомами ГЕРХ (максимальний ступінь езофагіту I відповідно до класифікації Саварі — Міллера при ендоскопії на вихідному рівні) отримували короткотривале лікування езомепразолом 40 мг один раз на день протягом 4 тижнів. При досягненні успіху в лікуванні вони були рандомізовані в групу або езомепразолу 20 мг один раз на день, або езомепразолу 20 мг за потребою протягом 6 місяців. Пов’язану зі здоров’ям якість життя оцінювали за допомогою валідованих анкет на вихідному рівні, а також на початку та наприкінці періоду підтримуючої терапії. На вихідному рівні в пацієнтів із ГЕРХ спостерігались значно знижені показники якості життя, однак короткотривале лікування езомепразолом протягом 4 тижнів зумовило статистично вірогідне покращення всіх показників якості життя (р < 0,0001). Статистично вірогідна різниця в балах щодо якості життя була зареєстрована наприкінці етапу підтримуючого лікування на користь постійного режиму (Pace та ін., 2005).
Нарешті, у проведеному в Норвегії дослідженні проводилась оцінка ефективності трьох режимів лікування з метою покращення пов’язаної зі здоров’ям якості життя у пацієнтів із симптомами ГЕРХ (Hansen та ін., 2006). Після 4-тижневої фази контролю симптомів (езомепразол 40 мг один раз на день) пацієнти були рандомізовані в групу лікування езомепразолом 20 мг один раз на день постійно протягом 6 місяців (n = 658), езомепразолом 20 мг один раз на день за потребою (n = 634) або ранітидином 150 мг два рази на день постійно (n = 610). Якість життя, пов’язана зі здоров’ям, була оцінена за допомогою валідованих анкет на вихідному рівні, а також на початку та наприкінці періоду підтримуючої терапії. Езомепразол 40 мг один раз на день сприяв покращенню якості життя під час короткотривалого етапу контролю симптомів. На 6-му місяці обидва режими лікування езомепразолом були більш ефективними, аніж ранітидин, за всіма показниками якості життя (р < 0,0001). Проте постійний прийом езомепразолу 20 мг один раз на день відобразився більш позитивно на якості життя порівняно з режимом прийому езомепразолу за потребою й асоціювався з більш вираженою задоволеністю пацієнта (Hansen та ін., 2006).
Таким чином, існують дані на користь лікування езомепразолом, що асоціюється з покращенням пов’язаної зі здоров’ям якості життя у пацієнтів із ГЕРХ при порівнянні як мінімум із ранітидином. Однак на даний момент бракує подвійних сліпих рандомізованих досліджень із порівнянням впливу езомепразолу та інших ІПП на показники якості життя при лікуванні ГЕРХ.
Висновок
У пацієнтів із гастроезофагеальною рефлюксною хворобою стандартні дози езомепразолу підтримують рівень інтрагастрального показника рН понад 4 протягом значно тривалішого часу порівняно зі стандартними дозами інших ІПП після 5 днів лікування. Незважаючи на певні розбіжності, дані клінічних досліджень та метааналізів свідчать про те, що лікування езомепразолом 40 мг один раз на день до 8 тижнів зумовлює вищу частоту загоєння ерозивної ГЕРХ, а також вищий відсоток тривалого усунення печії порівняно з омепразолом 20 мг, лансопразолом 30 мг або пантопразолом 40 мг один раз на день. Також було продемонстровано, що езомепразол 20 мг один раз на день був більш ефективним стосовно підтримування загоєння ерозивної ГЕРХ порівняно з лансопразолом 15 мг один раз на день або пантопразолом 20 мг один раз на день. Однак залишається невідомим, чи має статистично вірогідна різниця суттєве клінічне значення. Порівняльних досліджень ефективності езомепразолу та рабепразолу в лікуванні та підтримуючій терапії загоєної ерозивної ГЕРХ, а також порівняння езомепразолу та омепразолу або рабепразолу в підтримуючій терапії загоєної ерозивної ГЕРХ також бракує. Езомепразол 20 мг один раз на день має переваги над плацебо в лікуванні НЕРХ, проте клінічні випробування вірогідної різниці в ефективності між езомепразолом 20 мг та омепразолом 20 мг або пантопразолом 20 мг один раз на день в даній групі пацієнтів не виявили. Даних порівняльних досліджень езомепразолу та лансопразолу або рабепразолу при НЕРХ ідентифіковано не було. Наприкінці слід додати, що, незважаючи на повідомлення про те, що лікування езомепразолом при ГЕРХ призводить до покращення показників пов’язаної зі здоров’ям якості життя, у клінічних випробуваннях до сьогодні можливі диференційні ефекти різних ІПП щодо якості життя пацієнтів із ГЕРХ не досліджувались.
1. Armstrong D., Talley N.J., Lauritsen K. et al. The role of acid suppression in patients with endoscopy–negative reflux disease: the effect of treatment with esomeprazole or omeprazole // Aliment. Pharmacol. Ther. — 2004. — 20. — 413–21.
2. Bell N.J., Burget D., Howden et al. Appropriate acid suppression for the management of gastro–oesophageal reflux disease // Digestion. — 1992. — 51(Suppl. 1). — 59–67.
3. Bjornsson E., Abrahamsson H., Simren M. et al. Discontinuation of proton pump inhibitors in patients on long–term therapy: a double–blind, placebo–controlled trial // Aliment. Pharmacol. Ther. — 2006. — 24. — 945–54.
4. Castell D.O., Kahrilas P.J., Richter J.E. et al. Esomeprazole 40 mg. compared with lansoprazole 30 mg. in the treatment of erosive esophagitis // Am. J. Gastroenterol. — 2002. — 97. — 575–83.
5. Delaney B., McColl K. Review article: Helicobacter pylori and gastro–oesophageal reflux disease // Aliment. Pharmacol. Ther. — 2005. — 22(Suppl. 1). — 32–40.
6. Dent J., El–Serag H.B., Wallander M.A. et al. Epidemiology of gastro–oesophageal reflux disease: a systematic review // Gut. — 2005. — 54. — 710–17.
7. DeVault K.R., Castell D.O. Updated guidelines for the diagnosis and treatment of gastroesophageal reflux disease // Am. J. Gastroenterol. — 2005. — 100. — 190–200.
8. DeVault K.R., Johanson J.F., Johnson D.A. et al. Maintenance of healed erosive esophagitis: a randomized six–month comparison of esomeprazole twenty milligrams with lansoprazole fifteen milligrams // Clin. Gastroenterol. Hepatol. — 2006. — 4. — 852–9.
9. Edwards S.J., Lind T., Lundell L. Systematic review of proton pump inhibitors for the acute treatment of reflux oesophagitis // Aliment. Pharmacol. Ther. — 2001. — 15. — 1729–36.
10. Edwards S.J., Lind T., Lundell L. Systematic review: proton pump inhibitors PPIs. for the healing of reflux oeso–phagitis — a comparison of esomeprazole with other PPIs // Aliment. Pharmacol. Ther. — 2006. — 24. — 743–50.
11. Fennerty M.B., Johanson J.F., Hwang C. et al. Efficacy of esomeprazole 40 mg vs lansoprazole 30 mg for healing moderate to severe erosive oesophagitis // Aliment. Pharmacol. Ther. — 2005. — 21. — 455–63.
12. Fock K.M., Teo E.K., Ang T.L. et al. Rabeprazole vs esomeprazole in non–erosive gastro–esophageal reflux di–sease: a randomized, doubleblind study in urban Asia // World J. Gastroenterol. — 2005. — 11. — 3091–8.
13. Frazzoni M., De Micheli E., Savarino V. Different patterns of oesophageal acid exposure distinguish complicated reflux disease from either erosive reflux oesophagitis or non–erosive reflux disease // Aliment. Pharmacol. Ther. — 2003. — 18. — 1091–8.
14. Frazzoni M., Manno M., De Micheli E. et al. Intra–oesophageal acid suppression in complicated gastro–oeso–phageal reflux disease: esomeprazole versus lansoprazole // Dig. Liver. Dis. — 2006. — 38. — 85–90.
15. Gillessen A., Beil W., Modlin I.M. et al. 40 mg pantoprazole and 40 mg esomeprazole are equivalent in the healing of esophageal lesions and relief from gastroesophageal reflux disease–related symptoms // J. Clin. Gastroenterol. — 2004. — 38. — 332–40.
16. Gralnek I.M., Dulai G.S., Fennerty M.B. et al. Esomeprazole Versus Other Proton Pump Inhibitors in Erosive Esophagitis: A Meta–Analysis of Randomized Clinical Trials // Clin. Gastroenterol. Hepatol. — 2006. — 4. — 1452–8.
17. Hansen A.N., Bergheim R., Fagertun H. et al. Long–term management of patients with symptoms of gastro–oesophageal reflux disease — a Norwegian randomised prospective study comparing the effects of esomeprazole and ranitidine treatment strategies on health–related quality of life in a general practitioners setting // Int. J. Clin. Pract. — 2006. — 60. — 15–22.
18. Hatlebakk J.G. Review article: gastric acidity — comparison of esomeprazole with other proton pump inhibitors // Aliment. Pharmacol. Ther. — 2003. — 17(Suppl. 1). — 10–15; discussion 16–17.
19. Hellstrom P.M., Vitols S. The choice of proton pump inhibitor: does it matter? // Basic. Clin. Pharmacol. Toxicol. — 2004. — 94. — 106–11.
20. Holtmann G., Cain C., Malfertheiner P. Gastric Helicobacter pylori infection accelerates healing of refl ux esophagitis during treatment with the proton pump inhibitor pantoprazole // Gastroenterology. — 1999. — 117. — 11–16.
21. Howden C.W., Ballard E.D. II, Robieson W. Evidence for therapeutic equivalence of lansoprazole 30 mg and esomeprazole in the treatment of erosive esophagitis // Clin. Drug Investig. — 2002. — 22. — 99–109.
22. Hunt R.H. Importance of pH control in the management of GERD // Arch. Intern. Med. — 1999. — 159. — 649–57.
23. Johansson K.E., Ask P., Boeryd B. et al. Oesophagitis, signs of reflux, and gastric acid secretion in patients with symptoms of gastrooesophageal reflux disease // Scand. J. Gastroenterol. — 1986. — 21. — 837–47.
24. Johnson D.A., Benjamin S.B., Vakil N.B. et al. Esomeprazole once daily for 6 months is effective therapy for maintaining healed erosive esophagitis and for controlling gastroesophageal reflux disease symptoms: a randomized, double–blind, placebo–controlled study of efficacy and safety // Am. J. Gastroenterol. — 2001. — 96. — 27–34.
25. Johnson D.A., Stacy T., Ryan M. et al. A comparison of esomeprazole and lansoprazole for control of intragastric pH in patients with symptoms of gastro–oesophageal reflux disease // Aliment. Pharmacol. Ther. — 2005. — 22. — 129–34.
26. Johnsson F., Joelsson B., Gudmundsson K. et al. Symptoms and endoscopic findings in the diagnosis of gastroesophageal reflux disease // Scand. J. Gastroenterol. — 1987. — 22. — 714–18.
27. Kahrilas P.J., Falk G.W., Johnson D.A. et al. Esomeprazole improves healing and symptom resolution as compared with omeprazole in reflux oesophagitis patients: a randomized controlled trial. The Esomeprazole Study Investigators // Aliment. Pharmacol. Ther. — 2000. — 14. — 1249–58.
28. Katz P.O., Castell D.O., Chen Y. et al. Intragastric acid suppression and pharmacokinetics of twice–daily esomeprazole: a randomized, threeway crossover study // Aliment. Pharmacol. Ther. — 2004. — 20. — 399–406.
29. Kendall M.J. Review article: Esomeprazole — the first proton pump inhibitor to be developed as an isomer // Aliment. Pharmacol. Ther. — 2003. — 17(Suppl. 1). — 1–4.
30. Klok R.M., Postma M.J., van Hout B.A. et al. Meta–analysis: comparing the efficacy of proton pump inhibitors in short–term use // Aliment. Pharmacol. Ther. — 2003. — 17. — 1237–45.
31. Kuipers E.J., Nelis G.F., Klinkenberg–Knol E.C. et al. Cure of Helicobacter pylori infection in patients with reflux oesophagitis treated with long term omeprazole reve–rses gastritis without exacerbation of reflux disease: results of a randomised controlled trial // Gut. — 2004. — 53. — 12–20.
32. Kulig M., Leodolter A., Vieth M. et al. Quality of life in relation to symptoms in patients with gastro–oesophageal refl ux disease — an analysis based on the ProGERD initiative // Aliment. Pharmacol. Ther. — 2003. — 18. — 767–76.
33. Labenz J., Armstrong D., Lauritsen K. et al. Esomeprazole 20 mg vs pantoprazole 20 mg for maintenance therapy of healed erosive oesophagitis: results from the EXPO study // Aliment. Pharmacol. Ther. — 2005а. — 22. — 803–11.
34. Labenz J., Armstrong D., Lauritsen K. et al. A randomized comparative study of esomeprazole 40 mg versus pantoprazole 40 mg for healing erosive oesophagitis: the EXPO study // Aliment. Pharmacol. Ther. — 2005. — 21. — 739–46.
35. Labenz J., Tillenburg B., Peitz U. et al. Helicobacter pylori augments the pH–increasing effect of omeprazole in patients with duodenal ulcer // Gastroenterology. — 1996. — 110. — 725–32.
36. Lauritsen K., Deviere J., Bigard M.A. et al. Esomeprazole 20 mg and lansoprazole 15 mg in maintaining healed reflux oesophagitis: Metropole study results // Aliment. Pharmacol. Ther. — 2003. — 17. — 333–41.
37. Lind T., Havelund T., Carlsson R. et al. Heartburn without oesophagitis: efficacy of omeprazole therapy and features determining therapeutic response // Scand. J. Gastroenterol. — 1997. — 32. — 974–9.
38. Lind T., Rydberg L., Kyleback A. et al. Esomeprazole provides improved acid control vs omeprazole In patients with symptoms of gastrooesophageal reflux disease // Aliment. Pharmacol. Ther. — 2000. — 14. — 861–7.
39. Martinez S.D., Malagon I.B., Garewal H.S. et al. Non–erosive reflux disease NERD — acid reflux and symptom patterns // Aliment. Pharmacol. Ther. — 2003. — 17. — 537–45.
40. Miehlke S., Madisch A., Kirsch C. et al. Intragastric acidity during treatment with esomeprazole 40 mg twice daily or pantoprazole 40 mg twice daily — a randomized, two–way crossover stud // Aliment. Pharmacol. Ther. — 2005. — 21. — 963–7.
41. Miner P. Jr, Katz P.O., Chen Y. et al. Gastric acid control with esomeprazole, lansoprazole, omeprazole, pantoprazole, and rabeprazole: a five–way crossover study // Am. J. Gastroenterol. — 2003. — 98. — 2616–20.
42. Moayyedi P., Talley N.J. Gastro–oesophageal reflux disease // Lancet. — 2006. — 367. — 2086–100.
43. Monnikes H., Pfaffenberger B., Gatz G. et al. Novel measurement of rapid treatment success with ReQuest: first and sustained symptom relief as outcome parameters in patients with endoscopy–negative GERD receiving 20 mg pantoprazole or 20 mg esomeprazole // Digestion. — 2005. — 71. — 152–8.
44. Pace F., Negrini C., Wiklund I. et al. Quality of life in acute and maintenance treatment of non–erosive and mild erosive gastro–oesophageal reflux disease // Aliment. Pharmacol. Ther. — 2005. — 22. — 349–56.
45. Prasad M., Rentz A.M., Revicki D.A. The impact of treatment for gastro–oesophageal reflux disease on health–related quality of life: a literature review // Pharmacoecono–mics. — 2003. — 21. — 769–90.
46. Revicki D.A., Wood M., Maton P.N. et al. The impact of gastroesophageal reflux disease on health–related quality of life // Am. J. Med. — 1998. — 104. — 252–8.
47. Richter J.E., Kahrilas P.J., Johanson J. et al. Efficacy and safety of esomeprazole compared with omeprazole in GERD patients with erosive esophagitis: a randomized controlled trial // Am. J. Gastroenterol. — 2001. — 96. — 656–65.
48. Rohss K., Hasselgren G., Hedenstrom H. Effect of esomeprazole 40 mg vs omeprazole 40 mg on 24–hour intragastric pH in patients with symptoms of gastroesophageal reflux disease // Dig.Dis. Sci. — 2002. — 47. — 954–8.
49. Rohss K., Lind T., Wilder–Smith C. Esomeprazole 40 mg provides more effective intragastric acid control than lansoprazole 30 mg, omeprazole 20 mg, pantoprazole 40 mg and rabeprazole 20 mg in patients with gastro–oesophageal reflux symptoms // Eur. J. Clin. Pharmacol. — 2004. — 60. — 531–9.
50. Schmitt C., Lightdale C.J., Hwang C. et al. A multicenter, randomized, double–blind, 8–week comparative trial of standard doses of esomeprazole 40 mg and omeprazole 20 mg for the treatment of erosive esophagitis // Dig. Dis. Sci. — 2006. — 51. — 844–50.
51. Scholten T., Gatz G., Hole U. Once–daily pantoprazole 40 mg and esomeprazole 40 mg have equivalent overall efficacy in relieving GERD–related symptoms // Aliment. Pharmacol. Ther. — 2003. — 18. — 587–94.
52. Simon B., Muller P., Pascu O. et al. Intra–oesophageal pH profiles and pharmacokinetics of pantoprazole and esomeprazole: a crossover study in patients with gastro–oesophageal reflux disease // Eur. J. Gastroenterol. Hepatol. — 2003. — 15. — 791–9.
53. Talley N.J., Lauritsen K., Tunturi–Hihnala H. et al. Esomeprazole 20 mg maintains symptom control in endoscopy–negative gastro–oesophageal reflux disease: a controlled trial of on–demand therapy for 6 months // Aliment. Pharmacol. Ther. — 2001. — 15. — 347–54.
54. Talley N.J., Venables T.L., Green J.R. et al. Esomeprazole 40 mg and 20 mg is efficacious in the long–term management of patients with endoscopy–negative gastro–oeso–phageal reflux disease: a placebocontrolled trial of on–demand therapy for 6 months // Eur. J. Gastroenterol. Hepatol. — 2002. — 14. — 857–63.
55. Tsai H.H., Chapman R., Shepherd A. et al. Esomeprazole 20 mg on–demand is more acceptable to patients than continuous lansoprazole 15 mg in the long–term maintenance of endoscopy–negative gastro–oesophageal reflux patients: the COMMAND Study // Aliment. Pharmacol. Ther. — 2004. — 20. — 657–65.
56. Vakil N., Fennerty M.B. Direct comparative trials of the efficacy of proton pump inhibitors in the management of gastro–oesophageal reflux disease and peptic ulcer disease // Aliment. Pharmacol. Ther. — 2003. — 18. — 559–68.
57. Vakil N.B., Shaker R., Johnson D.A. et al. The new proton pump inhibitor esomeprazole is effective as a maintenance therapy in GERD patients with healed erosive oesophagitis: a 6–month, randomized, double–blind, placebo–controlled study of efficacy and safety // Aliment. Pharmacol. Ther. — 2001. — 15. — 927–35.
58. Vakil N., van Zanten S.V., Kahrilas P. et al. The Montreal definition and classification of gastroesophageal reflux disease: a global evidencebased consensus // Am. J. Gastroenterol. — 2006. — 101. — 1900–20; quiz 1943.
59. Verdu E.F., Armstrong D., Fraser R. et al. Effect of Helicobacter pylori status on intragastric pH during treatment with omeprazole // Gut. — 1995. — 36. — 539–43.
60. Wilder–Smith C.H., Rohss K., Nilsson–Pieschl C. et al. Esomeprazole 40 mg provides improved intragastric acid control as compared with lansoprazole 30 mg and rabeprazole 20 mg in healthy volunteers // Digestion. — 2003. — 68. — 184–8.
61. Wu J.C., Chan F.K., Ching J.Y. et al. Effect of Helicobacter pylori eradication on treatment of gastro–oesophageal reflux disease: a double blind, placebo controlled, randomised trial // Gut. — 2004. — 53. — 174–9.