Международный эндокринологический журнал 4 (68) 2015
Вернуться к номеру
Селенодефицит и возрастзависимая патология (в фокусе дейодиназы)
Авторы: Гончарова О.А. - Харьковская медицинская академия последипломного образования; Ильина И.М. - ГУ «Институт проблем эндокринной патологии им. В.Я. Данилевского НАМН Украины», г. Харьков
Рубрики: Эндокринология
Разделы: Справочник специалиста
Версия для печати
Проанализированы данные литературы, касающиеся наличия метаболической памяти, связанной с формированием адаптивных реакций в результате влияния разнообразных факторов внешней среды. На примере селенопротеинов дейодиназ прослежены механизмы коррекции метаболизма в условиях селенодефицита, подтверждающие наличие теории сортировки (triage theory). Приведены данные собственных наблюдений, позволяющие сделать предварительный вывод о недостаточном обеспечении селеном, как минимум, в некоторых зонах Украины.
Проаналізовано дані літератури стосовно наявності метаболічної пам’яті, пов’язаної з формуванням адаптивних реакцій у результаті впливу різноманітних чинників зовнішнього середовища. На прикладі селенопротеїнів де-йодиназ простежено механізми корекції метаболізму за умов селенодефіциту, що підтверджує положення теорії сортування (triage theory). Наведено дані власних спостережень, що дозволяють зробити попередній висновок про недостатнє забезпечення селеном принаймні в деяких регіонах України.
The article analyzes the published data concerning the presence of metabolic memory associated with the formation of adaptive reactions to the result of the influence of various environmental factors. In terms of deiodinase selenoproteins, mechanisms of metabolic correction under selenium deficiency confirming the existence of the triage theory were investigated. The data of our own observations which made it possible to draw a preliminary conclusion about the lack of selenium at least in some regions of Ukraine are provided.
селенодефицит, селенопротеины дейодиназы, возрастзависимая патология, метаболическая память.
селенодефіцит, селенопротеїни дейодинази, залежна від віку патологія, метаболічна пам’ять.
selenium deficiency, deiodinase selenoproteins, age-related pathology, metabolic memory.
Статья опубликована на с. 87-92
В настоящее время введено такое понятие, как «метаболическая память» — необратимые, прогностически неблагоприятные нарушения, связанные с особенностями формирования адаптивных реакций в результате взаимодействия организма с разнообразием факторов внешней среды [1].
Экспериментальные исследования, проведенные на различных моделях — от клеточных культур до млекопитающих, показали, что в основе адаптациогенеза лежат два уровня организации: эпигенетическая и метаболическая память, которые являются единой системой, обеспечивающей выбор стратегии адаптации [2]. А.И. Божков высказал предположение, что в основе выбора метаболической стратегии адаптации лежат три основных принципа: принцип исходного состояния (ответная реакция в процессе адаптации зависит от функциональных характеристик в момент воздействия); принцип эпигенетической памяти — сформировавшиеся в процессе функционирования паттерны экспрессии генов обеспечивают самоподдержание взаимосвязанных метаболических циклов; принцип пороговой необратимости эпигенетических изменений, который поясняет формирование хронических патологий, доля которых увеличивается с увеличением времени функционирования биологических систем. Необратимость метаболических изменений объясняется формированием стойкой метаболической памяти [3, 4].
Харьковскими учеными разработана биологическая модель, демонстрирующая эффект метаболической памяти к токсическому действию сернокислой меди [5]. Причем результаты исследования указывают на зависимость этого процесса от времени формирования.
Метаболической памятью, в частности, объясняют сохраняющуюся повышенной сердечно–сосудистую смертность у лиц с длительной декомпенсацией сахарного диабета (СД) даже при последующей эффективной терапии, практически нормализующей гликемию, что подтверждено в исследованиях ADVANCE и ACCORD [6–8].
Установлено, что у мышц есть метаболическая память, которая фиксирует состояние ожирения как нормальное. Это объясняет, почему так трудно бывает удержать вес после его сбрасывания в желаемых границах. Неправильное питание в критические периоды развития накладывает на обмен веществ отпечаток, сохраняемый и во взрослом периоде. Существует мнение, что неблагоприятное течение беременности и родов в сочетании с низким артериальным давлением у матери во время беременности формируют негативную метаболическую память у плода и вегетативную дисфункцию по гипотоническому типу у детей чаще всего подросткового возраста [9].
Все больший интерес исследователей вызывает проблема связи возрастзависимой хронической неинфекционной патологии с имевшими место в раннем возрасте либо в пренатальном периоде продолжительными эпизодами тяжелого либо даже умеренного минерального дефицита. Получены убедительные данные, что связанные с возрастом такие состояния, как кардиоваскулярная патология, рак, деменция, могут быть следствием механизмов, которые развились как протекторные на фоне эпизодов минеральной недостаточности: она приучает организм использовать все возможные ресурсы для сохранения жизни и обеспечения репродуктивных возможностей, а это ведет к повышению риска развития патологии во второй половине жизни [9].
В значительной степени это касается умеренной или тяжелой недостаточности селена (Se). Способность Se разнообразно воздействовать на организм осуществляется через механизм модификации экспрессии почти 200 селенопротеинов (СП), функции большинства из которых установлены недавно [10–12]. СП жизненно необходимы. Это продемонстрировано летальностью трансгенных мышей КО, неспособных инкорпорировать Se в СП, а также тяжелой патологией, если синтез СП был отключен в специфических тканях [13, 14]. Иерархия СП преду–сматривает группы эссенциальных (незаменимых) СП и тех, функции которых хотя бы частично перекрываются (дублируются) другими СП, — они являются неэссенциальными [15–17]. Результаты имеющихся исследований позволяют сделать вывод, что снижение активности именно неэссенциальных СП либо их отсутствие важны как маркеры предрасположенности к хроническим болезням [18, 19].
Доказательную базу теории составили: материалы web–сайтов; экспериментальные исследования на мышиных геномных моделях, касающихся КО–мутантов; люди, имеющие генетическую «поломку» в экспрессии определенных СП.
В частности, был установлен эффект дублирования ферментной активности в трех основных классах СП: глутатионпероксидаз (GPXs), тиоредоксинредуктаз (TRs) и дейодиназ (Ds) [19].
Насколько этот факт важен организму при умеренном либо выраженном селенодефиците, рассмотрим на примере Ds (D1, D2 и D3). Известно, что эти СП являются необходимым участником процесса перевода тироксина (Т4) в активный гормон трийодтиронин (Т3) путем дейодирования молекулы Т4. В ней йод занимает 4 позиции: по две в бензольных кольцах в позициях 3, 5 и 3΄, 5΄. Потеря молекулой Т4 под действием Ds атома йода в положении 5΄ способствует образованию активного Т3, а в положении 5 — реверсивного Т3 (rT3) (рис. 1) [20–22].
/88/88.jpg)
Идентифицированы три Ds (D1, D2 и D3), все они являются мембранными протеинами. Каждый из этих энзимов имеет селеноцистеиновый остаток в активном центре, что обеспечивает их высокую каталитическую активность [23, 24]. Ds имеют выраженную ткане– и времяспецифическую экспрессию, в том числе в фетальном периоде, и поэтому участвуют в важных регуляторных процессах на разных этапах онтогенеза. Рассмотрим судьбу каждой из дейодиназ в условиях селенодефицита.
Из трех Ds только D3 является эссенциальным СП, то есть ее действие не дублируется никакой другой Ds. Она способна переводить Т4 и активный Т3 в реверсивную форму Т3. Локализация ее деятельности: беременная матка, плацента, печень плода, фетальный и неонатальный мозг, кожа новорожденных. Такая локализация и определяет период ее деятельности: пре– и постнатальный. D3 как эссенциальная — наиболее устойчива к Se–дефициту. В то же время в эксперименте на моделях мышей КО с отключением D3 большинство эмбрионов погибает, а у выживших в последующие периоды жизни имеют место серьезные нарушения репродуктивной функции. Объяснением этого является тот факт, что D3, переводя Т4 и Т3 только в реверсивную форму Т3, предотвращает высокую концентрацию активного Т3, которая является токсичной для плода. Именно поэтому дефицит D3 у КО–потомков характеризуется частичной летальностью плодов. Менее понятен механизм выраженного снижения фертильности при дефиците D3 у КО–потомков. Тем не менее установлено, что яички у этих животных необыкновенно маленькие. Кроме того, известно, что D3 экспрессируется в той части неонатального мозга, которая участвует в половой дифференцировке [25, 26].
Что касается неэссенциальных D1 и D2, то при тяжелом селенодефиците к нему оказалась в высокой степени устойчивой только D1 в щитовидной железе (ЩЖ). Кроме того, после тяжелого селенодефицита D1 была в большей степени сохранена в гипофизе. В то же время D2 была ниже определяемого предела в крови при умеренном и тяжелом селенодефиците, но оставалась в достаточном количестве в гипофизе.
D1 способна конвертировать Т4 и в активный Т3, и в неактивный rT3, а Т3 — в rT3 или дийодтиронин (Т2) [31]. При достаточной обеспеченности Se главным органом синтеза D1 является печень. D1 наиболее чувствительна к недостатку Se в организме — ее синтез в печени резко снижается, а это чревато нарушением баланса между Т4 и Т3. В этих условиях ведущую роль в синтезе D1 берет на себя ЩЖ путем включения адаптационного механизма, предусмотренного в организме.
Активность процесса образования Т4 в ЩЖ регулируется соотношением между перекисью водорода (Н2О2) и неэссенциальным СП GPX3 [32]. При селенодефиците активность GPX3 значительно снижается. В противовес этому повышается выработка Н2О2, а значит, и тиреоглобулинопосредованная секреция Т4. Но в это же время в печени активность D1 (тоже неэссенциального СП) снижается (в результате снижается дейодинация Т4 в активный Т3). В этой ситуации (как проявление адаптации) ЩЖ становится основным местом синтеза D1 (вместо печени), что необходимо для поддержания баланса Т4/Т3. Более высокая устойчивость вырабатываемой в ЩЖ D1 к селенодефициту позволила считать ее условно неэссенциальным СП, который в период селенодефицита становится эссенциальным.
D2 — неэссенциальный СП — конвертирует Т4 в Т3 и Т3 в Т2 [33]. Локализация синтеза: ЩЖ, центральная нервная система (ЦНС), гипофиз, скелетные и сердечные мышцы, костная система. D2 является короткоживущим СП (менее одного часа). Она участвует в поддержании определенного баланса Т4/Т3 в различных периферических тканях для нормального их функционирования. Установленную связь в отдаленном периоде после селенодефицита с целым рядом болезней и состояний, включая остеоартрит и другую костную патологию, когнитивную дисфункцию и СД 2–го типа, прежде всего ассоциируют с адаптационными изменениями регионарного метаболизма на фоне дефицита именно D2 [34].
Нормальное развитие и функционирование скелета требует поддержания костеспецифического соотношения Т4/Т3, для которого экспрессия D2 играет важную роль [35]. В мышцах усвоение глюкозы опосредуется инсулинчувствительным глюкозным транспортером GLUT4. Его активность регулируется Т3, который, в свою очередь, регулируется экспрессией D2, обеспечивающей мышцеспецифический баланс Т4/Т3. Этот механизм в некоторой степени объясняет связь между D2 и СД 2–го типа [36].
При cеленодефиците моделируется новый алгоритм метаболизма, который влияет на дальнейшую судьбу метаболических процессов, что и называют метаболической памятью.
Можно сделать вывод, что при умеренном Se–дефиците, когда за счет эссенциальных СП сохраняются жизнеобеспечение и репродуктивные функции организма, страдают периферические (непривилегированные) ткани. Поэтому умеренный Se–дефицит является фактором риска развития в будущем патологии, обоснованной метаболической памятью организма, например заболеваний костно–мышечного аппарата или развития СД 2–го типа через механизм взаимодействия неэссенциальной D2 и GLUT4.
Таким образом, на примере СП дейодиназ можно конкретизировать роль эссенциальных и неэссенциальных СП в условиях Se–дефицита (табл. 1).
Представленные данные четко укладываются в теорию сортировки (triage theory), выдвинутую американскими учеными [16]. Согласно этой теории, умеренный дефицит определенного минерала может повысить риск возрастзависимой патологии за счет недостаточности неэссенциальных протеинов, связанных с минералом, так как эссенциальные минерало–белковые комплексы используются для сохранения жизни и фертильности. Применительно к Ds, на фоне селенодефицита именно эссенциальная D3 отвечает за сохранение жизни плода и фертильность в последующей жизни потомка. Неэссенциальная D1 начинает в большей мере экспрессироваться в ЩЖ и гипофизе (при значительном снижении секреции в печени), чем сохраняет метаболизм в этих органах. При этом наибольший недостаток в Se испытывают периферические органы: снижается экспрессия неэссенциальной D2 в костно–мышечной системе, из–за чего нарушается тканеспецифическое соотношение Т4/Т3. Закрепление такой модификации метаболизма в дальнейшем повышает риск костно–суставной патологии и может быть одной из причин развития СД 2–го типа в связи с нарушением метаболизма GLUT4, требующего достаточного количества D2.
Установленная на сегодняшний день схема перестройки организма в ответ на Se–дефицит заставляет более серьезно относиться к проблеме обеспеченности селеном даже начиная с пре– и постнатального периода. В этом плане, естественно, возникает вопрос, является ли достаточной обеспеченность данным микроэлементом на территории Украины. В литературе имеются данные относительно Se–дефицита у детей Черниговской области [37]. Исследованиями в Беларуси доказано, что вся территория страны имеет умеренный Se–дефицит [38].
Попыткой внести некоторую ясность в этот вопрос было проведенное нами исследование уровня Se в волосах у женщин в возрасте 25–55 лет, проживающих не менее 10 лет в Одессе, Сумах и Харькове, то есть в различных географических зонах Украины [39, 40].
Группы обследования составили отобранные методом случайной выборки женщины — жительницы г. Одессы (n = 40), г. Сумы (n = 50) и г. Харькова (n = 50). Исследование проведено с помощью атомно–абсорбционного спектрометра ICE 3500 (Thermo Fisher Scientific, USA). За нормальные показатели принят уровень Se > 0,8 мкг/г, приведенный в литературе [41].
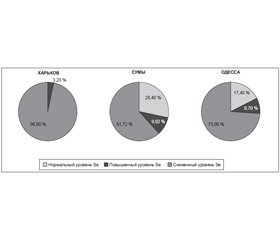
Результаты исследования показали, что у большинства жительниц данных областей уровень Se в волосах был ниже нормы (рис. 2). При этом удельный вес женщин с наличием селенодефицита оказался наиболее высоким в Харьковской области.
Для оценки степени Se–дефицита в обследованных контингентах сравнили уровни селена в волосах в подгруппах с его уровнем ниже нормальных значений (табл. 2).
Данные проведенного исследования позволяют сделать предварительный вывод о недостаточном обеспечении Se в Одесской, Сумской и Харьковской областях. Не вызывает сомнения необходимость проведения эпидемиологического исследования на всей территории страны для выявления зон с Se–дефицитом и профилактики Se–дефицитной патологии с использованием опыта других стран. Известно, что в Финляндии эту профилактику осуществили путем добавления селена в удобрения, в отдельных районах Китая — селенацией соли [42, 43]. Для индивидуальной коррекции уровня селена рекомендуются селеносодержащие препараты.
1. Intine R.V. Metabolic Memory and Chronic Diabetes Complications: Potential Role for Epigenetic Mechanisms [Text] / R.V. Intine, M.P. Jr Sarras // Curr. Diab. Rep. — 2012. — Vol. 12(5). — P. 551–559.
2. Божков А.И. Внешние повреждающие воздействия как факторы ускорения и замедления старения [Текст] / А.И. Божков // Проблемы старения и долголетия. — 2013. — Т. 22 (приложение). — С. 15.
3. Божков А.И. Гормезисная модель метаболической памяти и возможности регуляции темпов старения [Текст] / А.И. Божков, Ю.В. Никитченко и др. // Проблемы старения и долголетия. — 2012. — Т. 21, № 3. — С. 245–254.
4. Полторак В.В., Красова Н.С., Горшунская М.Ю. Гликемическая память как патогенетическое основание для формирования алгоритма современной антидиабетической терапии // Міжнародний ендокринологічний журнал. — 2014. — № 3(59). — С. 15–21.
5. Сидоров В.И. Модель определения метаболической памяти и формирования возрастзависимых стратегий адаптации [Текст] / В.И. Сидоров, Н.И. Кургузова, В.Л. Длубовская и др. // Х Междунар. симп. «Биологические механизмы старения». Тез. докл. (Харьков, 16–19 мая 2012 года). — Х., 2012. — С. 51.
6. Тронько М.Д., Полторак В.В., Соколова Л.К. Дослі–дження ORIGIN (передумови, результати) // Міжнародний ендокринологічний журнал. — 2013. — № 1(49). — С. 15–22.
7. Ceriello A. Clinical review 2: The «metabolic memory»: is more than just tight glucose control necessary to prevent diabetic complications [Text] / A. Ceriello, M.A. Ihnat, J.E. Thorpe // J. Clin. Endocrinol. Metab. — 2009. — Vol. 94. — P. 410–415.
8. Riddle M.C. Effects of intensive glucose lowering in the management of patients with type 2 diabetes mellitus in the Action to Control Cardiovascular Risk in Diabetes (ACCORD) trial [Text] / M.C. Riddle // Circulation. — 2010. — Vol. 122. — P. 844–846.
9. Архипова Н.Н. Артериальная гипотензия у детей и подростков [Текст] / Н.Н. Архипова // Кардиология. — 2008. — № 4(28). — С. 63–65.
10. Bosl M.R. Early embryonic lethality caused by targeted disruption of the mouse selenocysteine tRNA gene (Trsp) [Text] / M.R. Bosl, K. Takaku, M. Oshima et al. // Proc. Natl. Acad. Sci. USA. — 1997. — Vol. 94. — P. 5531–5534.
11. Sengupta A. Selenoproteins are essential for proper keratinocyte function and skin development [Text] / A. Sengupta, U.F. Lichti, B.A. Carlson et al. // PLoS One. — 2010. — E. 12249.
12. Carlson B.A. Mouse models targeting selenocysteine tRNA expression for elucidating the role of selenoproteins in health and development [Text] / B.A. Carlson, M.H. Yoo, P.A. Tsuji et al. // Molecules. — 2009. — Vol. 14. — P. 3509–3527.
13. Lee B.C. Functions and evolution of selenoprotein methionine sulfoxide reductases [Text] / B.C. Lee, A. Dikiy, H.Y. Kim, V.N. Gladyshev // Biochim. Biophys. Acta. — 2009. — Vol. 1790. — P. 1471–1477.
14. Hatfield D.L. Selenocysteine incorporation machinery and the role of selenoproteins in development and health [Text] / D.L. Hatfield, B.A. Carlson, X.M. Xu et al. // Prog. Nucleic Acids Res. Mol. Biol. — 2006. — Vol. 81. — P. 97–142.
15. Schomburg L. Hierarchical regulation of selenoprotein expression and sex–specific effects of selenium [Text] / L. Schomburg, U. Schweizer // Biochim. Biophys. Acta. — 2009. — Vol. 1790. — P. 1453–1462.
16. McCann J.C. Adaptive dysfunction of selenoproteins from the perspective of the triage theory: why modest selenium deficiency may increase risk of diseases of aging [Text] / J.C. McCann, B.N. Ames // FASEB J. — 2011. — Vol. 25(6). — P. 1793–1814.
17. Гоголева И.В. Селен. Итоги и перспективы применения в педиатрии [Текст] / И.В. Гоголева, О.А. Громова // Практика педиатра. — 2009. — № 3. — С. 6–9.
18. Blankenberg S. Glutathione peroxidase activity and cardiovascular events in patients with coronary artery disease [Text] / S. Blankenberg, H.J. Rupprecht, С. Bickel et al. // N. Engl. J. Med. — 2003. — Vol. 349. — P. 1605–1613.
19. Kryukov G.V. Characterization of mammalian selenoproteomes [Text] / G.V. Kryukov, S. Castellano, S.V. Novoselov [et al.] // Science. — 2003. — Vol. 300. — P. 1439–1443.
20. Kоhrle J. Selenium, the thyroid and the endocrine system [Text] / J. Kоhrle, F. Jakob, B. Contempre [et al.] // Endocrinol. Rev. — 2005. — Vol. 26. — P. 944–984.
21. Gereben B. Cellular and molecular basis of deiodinase–regulated thyroid hormone signaling [Text] / B. Gereben, A.M. Zavacki, S. Ribich et al. // Endocr. Rev. — 2008. — Vol. 29. — P. 898.
22. Schneider M.J. Targeted disruption of the type 1 selenodeiodinase gene (Dio1) results in marked changes in thyroid hormone economy in mice [Text] / M.J. Schneider, S.N. Fiering, B. Thai et al. // Endocrinology. — 2006. — Vol. 147. — P. 580–589.
23. Beckett G.J., Arthur J.R. Selenium and endocrine systems [Text] / G.J. Beckett, J.R. Arthur // Journal of Endocrinology. — 2005. — Vol. 184. — P. 455–465.
24. Гончарова О.А. Селен і автоімунний тиреоїдит [Текст] / О.А. Гончарова, І.М. Ільїна // Міжнародний ендокринологічний журнал. — 2010. — № 6(30). — С. 71–74.
25. Huang S.A. Physiology and pathophysiology of type 3 deiodinase in humans [Text] / S.A. Huang // Thyroid. — 2005. — Vol. 15, № 8. — Р. 875–881.
26. Hernandez A. Type 3 deiodinase is critical for the maturation and function of the thyroid axis [Text] / A. Hernandez, M.E. Martinez, S. Fiering et al. // J. Clin. Invest. — 2006. — Vol. 116. — P. 476–484.
27. Germain D.L. Insights into the role of deiodinases from studies of genetically modified animals [Text] / D.L. Germain, A. Hernandez, M.J. Schneider, V.A. Galton // Thyroid. — 2005. — Vol. 15. — P. 905–916.
28. Kester M.H. Iodothyronine levels in the human developing brain: major regulatory roles of iodothyronine deiodinases in different areas [Text] / M.H. Kester, R. Martinez de Mena, M.J. Obregon et al. // Journal of Clinical Endocrinology and Metabolism. — 2004. — Vol. 89. — P. 3117–3128.
29. Zagrodzki P. Selenium status, sex hormones, and thyroid function in young women [Text] / P. Zagrodzki, R. Ratajczak // J. Trace Elem. Med. Biol. — 2008. — Vol. 22(4). — P. 296–304.
30. Blankenberg S. Glutathione peroxidase activity and cardiovascular events in patients with coronary artery disease [Text] / S. Blankenberg, H.J. Rupprecht, С. Bickel et al. // N. Engl. J. Med. — 2003. — Vol. 349. — P. 1605–1613.
31. Peeters R.P. Genetic variation in thyroid hormone pathway genes; polymorphisms in the TSH receptor and the iodothyronine deiodinases [Text] / R.P. Peeters, W.M. van der Deure, T.J. Visser // Eur. J.Endocrinol. — 2006. — Vol. 155. — P. 655–662.
32. Dayan C.M. Novel insights into thyroid hormones from the study of common genetic variation [Text] / C.M. Dayan, V. Pani–cker // Nat. Rev. Endocrinol. — 2009. — Vol. 5. — P. 211–218.
33. Heemstra K.A. The type 2 deiodinase Thr92Ala polymorphism is associated with increased bone turnover and decreased femoral neck bone mineral density [Text] / K.A. Heemstra, H. Hoftijzer, W.M. van der Deure // J. Bone Miner. Res. — 2010. — Vol. 25. — P. 1385–1391.
34. Dora J.M. Association of the type 2 deiodinase Thr92Ala polymorphism with type 2 diabetes: case–control study and meta–analysis [Text] / J.M. Dora, W.E. Machado, J. Rheinheimer et al. // Eur. J. Endocrinol. — 2010. — Vol. 163. — P. 427–434.
35. Gogakos A.I. Thyroid and bone [Text] / A.I. Gogakos, D.J.H. Bassett, G.R. Williams // Arch. Biochem. Biophys. — 2010. — Vol. 503. — P. 129–136.
36. Chidakel A. Peripheral metabolism of thyroid hormone and glucose homeostasis [Text] / A. Chidakel, D. Mentuccia, F.S. Celi // Thyroid. — 2005. — Vol. 15. — P. 899–903.
37. Кравченко В.І. Дослідження впливу дефіциту селену на розвиток дифузного зоба в дітей Чернігівської області [Текст] / В.І. Кравченко, О.І. Осадців, І.М. Андрусишина // Ендокринологія. — 2012. — Т. 17, № 3. — Р. 7–12.
38. Mityukova T. Asswsment of iodine and selenium supplementation in different regions of Belarus [Text] / T. Mityukova, V. Drozd, T. Leonova et al. // Eur. Thyroid J. — 2011. — P. 163–164.
39. Karachentsev Y.I. Security selenium separate regions of Sumy region and especially the frequency of thyroid cancer [Text] / Y.I. Karachentsеv, O.A. Goncharova, E.I. Podoroga et al. // Международный эндокринологический журнал. — 2013. — № 5(53). — P. 17–20.
40. Караченцев Ю.И. Микроэлементный дисбаланс при диффузно–очаговой форме аутоиммунного тиреоидита [Текст] / Ю.И. Караченцев, О.А. Гончарова, И.М. Ильина // Международный эндокринологический журнал. — 2014. — № 5(61). — С. 39–42.
41. Иванов С.И. Определение химических элементов в биологических средах и препаратах методами атомно–эмиссионной спектрометрии с индуктивно связанной плазмой и масс–спектрометрией [Текст] / С.И. Иванов, П.Л. Годунова, В.Б. Скачков и др. — М.: ФЦГСН России, 2003. — 56 с.
42. Aro A. Effects of supplementation of fertilizers on human selenium status in Finland [Text] / A. Aro, G. Alfthan // Analyst. — 1995. — Vol. 120. — P. 841–843.
43. Hensrud D.D. Antioxidant status, erythrocyte fatty acids, and mortality from cardiovascular disease and Keshan disease in China [Text] / D.D. Hensrud, D.C. Heimburger, J. Chen, B. Parpia // Eur. J. Clin. Nutr. — 1994. — Vol. 48(7). — Р. 455–464.

/89/89.jpg)
/90/90.jpg)
/90/90_2.jpg)