Статья опубликована на с. 33-41
Инсульт является распространенным во всем мире инвалидизирующим заболеванием, которое представляет собой серьезную проблему для здравоохранения [1]. В странах с высоким уровнем доходов инсульт занимает третье место в списке самых частых причин смерти и служит основной причиной приобретенной инвалидности взрослого населения [1, 2]. Однако, поскольку большинство пациентов с инсультом не умирают от исходного повреждения мозга, самое большое воздействие на пациентов и их семьи обычно оказывают стойкие нарушения функций организма, ограничение жизнедеятельности (инвалидность) и участия в жизни общества [1–3].
Существенное влияние на качество жизни больных, а также эффективность реабилитации оказывают когнитивные нарушения, которые развиваются в различные периоды мозгового инсульта. Когнитивные нарушения, достигающие степени деменции, развиваются у 25 % больных к концу первого года после перенесенного мозгового инсульта [4]. В результате популяционного исследования, проводимого в течение 24 лет во Франции, обнаружено, что среди 3201 пациента с впервые развившимся инсультом у 20,4 % была выявлена пост-инсультная деменция. Растущая распространенность постинсультной деменции связана с постарением населения планеты, сосудистыми факторами риска [5]. На основании данных многочисленных исследований сделан вывод, что когнитивные нарушения часто развиваются после инсульта и являются тяжелым бременем для мирового здравоохранения. Проблема будет усугубляться по мере старения населения, что диктует крайнюю необходимость разработки эффективных методов лечения [6].
Так как ишемический инсульт встречается в несколько раз чаще, чем геморрагический, то частота развития –постинсультных когнитивных нарушений (КН) у больных, перенесших ишемический инсульт, значительно превышает их частоту при других подтипах мозговых инсультов.
Постинсультные КН — одно из наиболее серьезных последствий церебральной ишемии, которое зачастую препятствует реабилитации пациентов или удлиняет ее сроки. Имеющиеся в настоящее время методы лечения не всегда являются эффективными. Несмотря на создание и внедрение в клиническую практику большого количества лекарственных препаратов с потенциально нейропротективным эффектом, защита мозга во время и после инсульта путем влияния на каскад развивающихся повреждений остается нерешенной задачей.
Одним из направлений лечения и профилактики постинсультных когнитивных нарушений наряду с физической реабилитацией является применение лекарственных средств, точками приложения которых являются сразу несколько патогенетических механизмов, а также препаратов, обеспечивающих защиту нейронов и способствующих процессу регенерации.
К таким препаратам с гетерогенным механизмом действия и потенциально нейропротекторным эффектом относится препарат Тиоцетам® (Корпорация «Артериум»*).
Тиоцетам® относится к группе цереброактивных средств, обладающих комплексным нейрометаболическим воздействием [7]. Препарат обладает способностью усиливать метаболизм глюкозы в реакциях аэробного и анаэробного окисления, нормализует биоэнергетические процессы, повышает уровень АТФ, стабилизирует метаболизм в тканях мозга. Тиоцетам® тормозит образование активных форм кислорода, реактивирует антиоксидантную систему ферментов, особенно супероксиддисмутазу, замедляет свободнорадикальные процессы в тканях мозга при ишемии, улучшает реологические свойства крови за счет активации фибринолитической системы, стабилизирует и уменьшает зоны некроза и ишемии, повышает интенсивность работы метаболического ГАМК-шунта и концентрацию ГАМК в ишемизированных тканях [8].
Такие свойства препарата способствуют улучшению интегративной и когнитивной деятельности мозга, процессу обучения, повышают показатели кратко- и долговременной памяти. Как показали проведенные исследования, Тиоцетам® смягчает последствия стресса (чувство тревоги, фобии, депрессии, нарушение сна), уменьшает отставание в физическом и умственном развитии недоношенных детей [9].
Тиоцетам® — оригинальная комбинация тиотриазолина и пирацетама. Эффект его обусловлен взаимопотенцирующим действием тиотриазолина и пирацетама, которые находятся в структуре препарата в соотношении 1 : 4. Механизм действия препарата –Тиоцетам® обусловлен фармакологическими эффектами пирацетама, а тиотриазолин, обладающий выраженным антиоксидантным эффектом, стабилизирует клеточные мембраны в условиях ишемии и противодействует патологическому апоптозу. Подобный механизм действия обеспечивает нейропротекторный эффект тиотриазолина, подтвержденный результатами доклинических исследований [8–11].
Эффективность препарата Тиоцетам® в плане восстановления нарушенных вследствие инсульта функций исследована недостаточно, что послужило мотивом для проведения в нескольких лечебных центрах Украины и Казахстана оригинального мультицентрового рандомизированного клинического исследования среди больных в остром и раннем восстановительном периодах ишемического инсульта.
Исследование проводилось на базе отдела сосудистой патологии головного мозга ГУ «Институт неврологии, психиатрии и наркологии НАМН Украины», г. Харьков (клиническая база 1) и на кафедре неврологии Южно-Казахстанской медицинской академии на базе отделения неврологии областной клинической больницы ЮКО, Казахстан (клиническая база 2). Данное исследование по оценке терапевтической эффективности было выполнено по протоколу исследования с соблюдением этических принципов Хельсинкской декларации, надлежащей клинической практики (GCP), надлежащей лабораторной практики (GLP), руководящих документов Европейского союза, Всемирной организации здравоохранения, а также национальных рекомендаций Украины [12–15].
Целью данного исследования явилась оценка эффективности и безопасности препаратов Тиоцетам®, раствор для инъекций, и Тиоцетам® форте, таблетки, в остром и раннем восстановительном периодах ишемического инсульта.
Задачи исследования:
— на основе комплексного (клинико-неврологического, психодиагностического, биохимического) исследования оценить эффективность препарата Тиоцетам® (таблетки и раствор для инъекций) в остром и раннем восстановительном периодах ишемического инсульта;
— оценить превышающую эффективность лечения с использованием Тиоцетама (таблетки и раствор для инъекций) на фоне базисной терапии по сравнению с базисной терапией (основная задача);
— изучить безопасность препарата Тиоцетам® (таблетки и раствор для инъекций) в остром и раннем восстановительном периодах ишемического инсульта; выявить и проанализировать возможные побочные эффекты исследуемых препаратов.
Критерии включения в данное исследование были следующими:
— мужчины и женщины в возрасте 18–70 лет;
— клинический диагноз: острое нарушение мозгового кровообращения (ОНМК) по ишемическому типу в каротидном и/или вертебробазилярном бассейне;
— оценка по шкале комы Глазго при скрининге от 12 до 15 баллов включительно;
— оценка по шкале NIHSS при скрининге от 3 до 12 баллов включительно;
— оценка по шкале MMSE при скрининге от 11 до 27 баллов включительно;
— возможность введения исследуемого препарата не позже чем на 10-е сутки с момента возникновения ОНМК;
— наличие результатов МРТ или КТ, подтверждающих клинический диагноз ишемического инсульта;
— отрицательный тест на беременность у женщин с детородным потенциалом (не стерилизованных хирургически и не находящихся в менопаузе более 2 лет);
— для женщин с детородным потенциалом — согласие использовать адекватные методы контрацепции (барьерная, химическая или гормональная контрацепция или внутриматочные устройства) на протяжении всего исследования;
— способность пациента к адекватному сотрудничеству в процессе исследования;
— подписание больным и/или его близким родственником (законным представителем) формы информированного согласия на участие в исследовании.
В исследование не включались пациенты:
— с тяжелыми или умеренными проявлениями афазии;
— тяжелой дисфагией;
— выраженной деменцией при скрининге (10 и менее баллов по шкале MMSE);
— умеренными или выраженными проявлениями деменции до развития ишемического инсульта (оценка 104 балла и более по шкале IQCODE или ранее диагностированная деменция);
— тяжелой дизартрией;
— психическими расстройствами;
— психомоторным возбуждением;
— судорожным синдромом;
— внутричерепным кровоизлиянием (геморрагический инсульт);
— систолическим артериальным давлением менее 90 мм рт.ст.;
— брадикардией с частотой сердечных сокращений менее 50 в 1 минуту;
— стрессовым повышением уровня глюкозы крови более 15 ммоль/л;
— повышением температуры тела выше 38 °С;
— подтвержденным тромбом в левых отделах сердца;
— острым инфарктом миокарда за последние 90 дней;
— с наличием декомпенсированных сопутствующих заболеваний или принимающие лекарства, которые, по мнению исследователя, могут повлиять на ход и результаты исследования;
— с наличием сопутствующих неврологических заболеваний (метаболическая или токсическая энцефалопатия, болезнь Альцгеймера, эпилепсия, паркинсонизм, инфекционные, демиелинизирующие и наследственные дегенеративные заболевания центральной нервной системы);
— клинически значимыми отклонениями от нормы лабораторных показателей (в частности, клинически значимым считается повышение АЛТ или АСТ более чем в 3 раза от верхней границы нормы или повышение креатинина крови более 130 мкмоль/л);
— злокачественными новообразованиями в анамнезе;
— алкоголизмом или наркоманией в анамнезе;
— проведенным за последние 30 дней или планируемым тромболизисом;
— планируемым нейрохирургическим вмешательством;
— известной гиперчувствительностью к любому из компонентов используемых препаратов;
— участвующие в любом другом клиническом испытании в настоящий момент или в течение последних 90 дней;
— с беременностью, лактацией.
Материалы и методы исследования
В исследование было включено 160 госпитализированных больных с подтвержденным диагнозом ОНМК по ишемическому типу, соответствующих всем критериям включения/невключения, по 80 человек в основную группу и группу сравнения. КТ/МРТ головного мозга проводили в первые сутки заболевания — до начала терапии. На томограммах определяли наличие, локализацию, размеры очага поражения мозга.
В первые 12–14 дней исследования препарат Тиоцетам® вводился внутривенно в условиях стационара, следующие 14 дней принимался перорально в форме таблеток. Было предусмотрено 5 визитов — скрининг, 1, 5, 12 (14) и 26-й (28-й) день исследования. Общая продолжительность исследования для пациента составила не более 30 суток.
Пациентам основной группы на 12–14 суток назначали исследуемый препарат Тиоцетам®, раствор для инъекций, внутривенно капельно по 20 мл в разведении на 100 мл 0,9% раствора натрия хлорида 1 раз в сутки. Скорость введения — 40–60 капель в 1 минуту. Рекомендовалось введение препарата в одно и то же время суток (с интервалом 24 часа).
Тиоцетам® форте, таблетки, покрытые оболочкой, больными принимался перорально по 1 таблетке 3 раза в сутки со следующего дня после последней инъекции препарата Тиоцетам® на протяжении как минимум 14 суток.
Лечение проводилось на фоне базисной терапии, направленной на коррекцию нарушения дыхания и кровообращения, стабилизацию гомеостаза и преду-преждение осложнений.
В процессе исследования не разрешалось назначение препаратов, содержащих пирацетам и/или тиотриазолин, а также ноотропных, нейропротекторных и вазоактивных препаратов.
Для оценки эффективности препарата Тиоцетам® были применены следующие клинические шкалы: NIHSS для оценки выраженности неврологического дефицита, шкала комы Глазго для оценки состояния сознания, шкала Рэнкина для оценки степени выраженности инвалидизации, шкалы MMSE, батарея лобных тестов для оценки состояния когнитивных функций, шкала депрессии Монтгомери — Асберга (MADRS).
Шкала MADRS интерпретируется следующим образом:
— 0–15 баллов — депрессия отсутствует;
— 16–25 баллов — малая депрессия;
— 26–30 баллов — умеренная депрессия;
— 25 баллов и более — выраженная депрессия.
Были проведены в динамике до и после лечения биохимические исследования (исследовались маркеры перекисного окисления липидов (ПОЛ) и антиоксидантной системы (АОС)).
Оценка безопасности лекарственного средства проводилась на основании жалоб пациента и объективных данных, полученных исследователем в процессе лечения. Учитывалась динамика лабораторных показателей, а также частота возникновения и характер побочных реакций. Анализ данных проводился при помощи встроенных средств статистического анализа электронных таблиц Microsoft Excel и пакета прикладных программ SPSS 13.1.
Результаты исследования
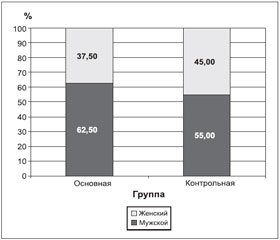
В исследование было включено 87 мужчин и 73 женщины.
Распределение пациентов по полу в группах приведено в табл. 1 и на рис. 1.
Распределение больных по локализации и характеру острого ишемического поражения мозгового кровообращения представлено в табл. 2.
Как свидетельствуют данные табл. 2, пациенты основной и контрольной групп существенно не отличались по локализации и механизму развития острой церебральной ишемии.
Степень тяжести ишемического инсульта, определяемая по шкале NIHSS, в основной и контрольной группах была одинакова и составила в среднем по группам 9 баллов.
Выраженность неврологического дефицита по шкале NIHSS на различных этапах исследования представлена на рис. 2.
Приведенные на рис. 2 данные свидетельствуют о следующем. Начиная с 5-го дня исследования (3-й визит) неврологический дефицит по шкале NIHSS стал отличаться в основной и контрольной группах. На 4-м и 5-м визитах снижение баллов по NIHSS статистически значимо больше в основной группе по сравнению с контрольной (р < 0,001) Так, на 12–14-й день лечения (4-й визит) неврологический дефицит в основной группе был на уровне 4,9 балла, а в контрольной — 6,1 балла. Таким образом, разница по шкале NIHSS в этих группах составила 1,2 балла. На 5-м визите (26–28-й день исследования) неврологический дефицит в основной группе составил 3,9 балла, а в контрольной — 5,5 балла, с разницей между группами 1,6 балла.
Таким образом, курсовое лечение препаратом Тиоцетам® достоверно улучшает исходы ишемического инсульта по степени регресса неврологического дефицита. Действие препарата наиболее эффективно спустя 2 недели после начала лечения.
Среднее значение показателей по шкале комы Глазго у пациентов основной и контрольной групп составило 14,13 и 14,85 соответственно. На 5, 10, 14 и 28-й дни по сравнению с исходным уровнем наблюдалось увеличение показателей в обеих группах (рис. 3). Однако статистически значимых различий между группами по изменению оценок шкалы комы Глазго выявлено не было.
Также была оценена динамика показателей жизненной активности (ПЖА), определяемая с помощью шкалы Рэнкина. Показатели жизненной активности на различных этапах исследования представлены на рис. 4.
Как видно на рис. 3, улучшение ПЖА по шкале Рэнкина в основной группе более значимо, чем в контрольной, и начинается на 5, 10, 14 и 28-й дни (р < 0,001 для всех точек времени). Таким образом, лечение препаратом Тиоцетам® достоверно улучшает исходы ишемического инсульта по ПЖА.
Одной из основных задач исследования была оценка влияния препарата Тиоцетам® на состояние когнитивных функций у обследованных больных в постинсультном периоде. Основные показатели когнитивных функций, определяемые с помощью шкалы MMSE, в основной и контрольной группах представлены на рис. 5.
Оценки состояния пациентов по шкале MMSE статистически значимо больше (р < 0,001) на 3, 4 и 5-м визитах по сравнению с 1-м визитом в обеих группах, что свидетельствует об улучшении психического статуса пациентов в процессе наблюдения. Так, если на 1-м визите различия между группами по категориальным оценкам психического статуса пациентов статистически значимо не различались (р = 1,000), то на 4-м и 5-м визитах были выявлены статистически значимые различия (р = 0,029 на 4-м визите и р = 0,025 на 5-м визите) в пользу основной группы по сравнению с контрольной, что свидетельствует о более выраженном влиянии лечения с применением препарата Тиоцетам® на улучшение психического статуса пациентов, оцениваемого по шкале MMSE.
Оценка состояния когнитивных функций в данном исследовании также проводилась с помощью шкалы «батарея лобных тестов» (FAB). По этой шкале количество баллов 17–18 соответствует норме, 12–16 — легким когнитивным расстройствам, 11 баллов и менее — деменции лобного типа. Динамика средних показателей по шкале FAB представлена на рис. 6.
Как и по показателям шкалы MMSE, состояние когнитивных функций пациентов по шкале FAB статистически значимо больше (р < 0,001) на 3, 4 и 5-м визитах по сравнению с 1-м визитом в обеих группах. Вместе с тем обнаружены различия между группами. Если на визите 1 наблюдались различия между группами в пользу контрольной группы (p = 0,045), то на 5-м визите, наоборот, были выявлены статистически значимые различия в пользу основной группы (р < 0,001) по сравнению с контрольной, что свидетельствует о более выраженном влиянии лечения с применением препарата Тиоцетам® на улучшение состояния пациентов, оцениваемого по шкале FAB.
Психоэмоциональное состояние больных в данном исследовании оценивалось с помощью шкалы депрессии Монтгомери — Асберга.
Динамика средних значений оценок состояния пациентов по шкале MADRS в обеих группах представлена на рис. 7.
Оценки выраженности депрессии по шкале MADRS статистически значимо меньше (р < 0,001) на 3, 4 и 5-м визитах по сравнению с 1-м визитом в обеих группах. Категориальные оценки шкалы MADRS показывают тенденцию к понижению уровня депрессии в обеих группах. Однако в основной группе начиная с 3-го визита наблюдаются статистически значимо лучшие результаты (р = 0,006 на 3-м визите и р < 0,001 на 4-м и 5-м визитах) по сравнению с контрольной группой, что свидетельствует о более выраженном влиянии лечения с применением препарата Тиоцетам® на уменьшение депрессии, оцениваемой по шкале MADRS.
Одним из критериев оценки эффективности препарата Тиоцетам® были лабораторные показатели, характеризующие состояние ПОЛ и АОС (малоновый диадельгид (МДА), диеновые конъюгаты (ДК), супер-оксиддисмутаза (СОД), каталаза крови).
При анализе численных значений МДА, ДК, СОД и каталазы в исходном состоянии (на визите 1) были выявлены статистически значимые различия между группами по МДА, ДК и СОД. Поэтому в дальнейшем при сравнении групп по этим показателям был применен ковариационный анализ. По численным значениям каталазы группы в исходном состоянии не различались. При сравнении групп в исходном состоянии по соответствию МДА, ДК, СОД и каталазы нормальным значениям статистически значимых различий выявлено не было.
Динамика средних значений МДА, ДК, СОД и каталазы представлена на рис. 8–11.
Как свидетельствуют результаты проведенных биохимических исследований, изменение МДА, ДК, СОД и каталазы в основной группе было статистически значимым на 4-м и 5-м визитах по сравнению с 1-м визитом. В исходном состоянии (визит 1) группы статистически значимо не различались. В дальнейшем произошло статистически значимое снижение МДА и ДК, а также статистически значимое увеличение СОД и каталазы.
Выявлены статистически значимые различия между основной и контрольной группами (р < 0,001) по нормализации параметра МДА на 5-м визите. Так, доля пациентов с нормальными значениями МДА в основной группе составляла на 5-м визите 65 %, в то время как в контрольной — 7,5 %.
Выявлены статистически значимые различия (р < 0,001) между основной и контрольной группами по соответствию нормальным значениям параметра ДК на 4-м и 5-м визитах. Так, на 4-м визите в основной группе доля пациентов с нормальными значениями ДК составила 42,5 %, а в контрольной — 10,0 %. На 5-м визите доля таких пациентов составила 92,5 % в основной группе и 12,5 % — в контрольной.
Выявлены статистически значимые различия между основной и контрольной группами (р < 0,001) по нормализации параметра СОД на 5-м визите. Так, доля пациентов с нормальными значениями СОД в основной группе составляла на 5-м визите 40,0 %, в то время как в контрольной — 2,5 %.
Также были выявлены статистически значимые различия (р < 0,001) между основной и контрольной группами по соответствию нормальным значениям каталазы на 4-м и 5-м визитах. Так, на 4-м визите в основной группе доля пациентов с нормальными значениями каталазы составила 72,5 %, а в контрольной — 32,5 %. На 5-м визите доля таких пациентов составила 90,0 % в основной группе и 37,5 % — в контрольной.
Таким образом, результаты проведенных исследований свидетельствуют о следующем. Относительное снижение МДА и ДК на 4-м и 5-м визитах в сравнении с 1-м визитом в основной группе статистически значимо выше (р < 0,001), чем в контрольной, что свидетельствует в пользу большей эффективности терапии с применением препарата Тиоцетам®.
Относительное увеличение СОД и каталазы на 4-м и 5-м визитах в сравнении с 1-м визитом в основной группе статистически значимо выше (р < 0,001), чем в контрольной, что свидетельствует в пользу большей эффективности терапии с применением препарата Тиоцетам®.
Безопасность препарата Тиоцетам® оценивалась в данном исследовании на основании жалоб пациента и лабораторных исследований. В процессе лечения у 4 пациентов (10 %) в основной группе развились побочные реакции/побочные явления (ПР/ПЯ) в виде сухости во рту, диареи, легкой головной боли, тошноты, инсомнии, тревожности. Данные ПР/ПЯ были несерьезные, легкой и средней степени тяжести, не требовали отмены применяемого препарата.
Основываясь на данных анализа крови, мочи, печеночных проб, можно констатировать, что существенного отрицательного влияния проводимого лечения на показатели биохимического анализа крови выявлено не было, что свидетельствует о хорошей переносимости испытуемого препарата.
Согласно протоколу исследования была оценена общая переносимость препарата (табл. 3).
Как видно из табл. 3, переносимость препарата была хорошей (у 95 %) или удовлетворительной (у 5 %).
Таким образом, результаты проведенного мультицентрового исследования показали, что лечение препаратами Тиоцетам® и Тиоцетам® форте в остром и раннем восстановительном периодах ишемического инсульта позволяет достоверно ускорить восстановление нарушенных неврологических функций, в том числе устранить очаговую неврологическую симптоматику, повысить показатели повседневной жизненной активности и улучшить когнитивные функции.
Выводы
1. Доказана большая эффективность терапии, включающей препарат Тиоцетам®, раствор для инъекций (Корпорация «Артериум»*) и Тиоцетам® форте, таблетки, покрытые оболочкой, в остром и раннем восстановительном периодах ишемического инсульта по сравнению с базисной терапией. Так, снижение баллов по NIHSS статистически значимо больше в основной группе по сравнению с контрольной на 4-м и 5-м визитах (р < 0,001 на обоих визитах) и усиливается с каждым визитом (р < 0,001 на 4-м и 5-м визитах), что свидетельствует о большей эффективности терапии в основной группе.
2. Относительное снижение МДА и ДК на 4-м и 5-м визитах в сравнении с 1-м визитом в основной группе была статистически значимо выше (р < 0,001), чем в контрольной, что свидетельствует в пользу большей эффективности терапии с применением препарата Тиоцетам®.
3. Относительное увеличение СОД и каталазы на 4-м и 5-м визитах в сравнении с 1-м визитом в основной группе было статистически значимо выше (р < 0,001), чем в контрольной группе, что свидетельствует в пользу большей эффективности терапии с применением препарата Тиоцетам®.
4. Доля пациентов, у которых произошла нормализация уровней МДА, ДК, СОД и каталазы, была статистически значимо больше (р < 0,001) в основной группе, чем в контрольной, что свидетельствует в пользу большей эффективности терапии, включающей Тиоцетам®.
5. Увеличение оценок психического статуса пациентов по шкале ММSЕ в основной группе было статистически значимо больше на 4-м и 5-м визитах (р < 0,001 для обоих визитов) по сравнению с контрольной группой, что свидетельствует о положительном влиянии комплексной терапии с применением Тиоцетама® на данные оценки.
6. Переносимость препарата была хорошей у 95 % пациентов и удовлетворительной у 5 %, наблюдаемые ПР/ПЯ по степени тяжести классифицировались как легкие или средние, являлись предвиденными, несерьезными и не требовали отмены применяемого препарата.
7. Рекомендовано применение препарата Тиоцетам® в составе комплексной терапии при лечении больных в остром и раннем восстановительном периодах острого нарушения мозгового кровообращения по ишемическому типу.

/36-1.jpg)
/36-2.jpg)
/37-1.jpg)
/38-1.jpg)
/39-1.jpg)
/40-1.jpg)