Статья опубликована на с. 178-180
Термин «пустое турецкое седло» (ПТС) предложил в 1951 году патологоанатом В. Буш (W. Busch) после изучения аутопсийного материала 788 умерших от заболеваний, не связанных с патологией гипофиза. Аналогичная патология описывалась и ранее другими патологоанатомами, однако Busch был первым, кто связал частично пустое турецкое седло с недостаточностью его диафрагмы. Эта связь была подтверждена и более поздними исследованиями. В литературе словосочетанием «пустое турецкое седло» обозначают различные нозологические формы, общим признаком которых является расширение субарахноидального пространства в интраселлярную область. Гипофизарная ямка при этом, как правило, увеличена. По данным W. Busch, у 40–50 % людей имеет место недоразвитие или отсутствие диафрагмы турецкого седла. Синдром ПТС наблюдается у 10 % населения и в 9 случаях из 10 не сопровождается симптомами гипоталамо-гипофизарной дисфункции. В 80 % случаев синдром ПТС встречается у женщин, при этом 75 % пациентов страдают ожирением. Полная форма синдрома ПТС диагностируется примерно в 75 % случаев, тогда как в 25 % случаев имеется лишь частичное заполнение полости турецкого седла цереброспинальной жидкостью.
Этиология и патогенез синдрома ПТС до конца не выяснены. Полагают, что для развития пустого турецкого седла необходима недостаточность его диафрагмы (утолщенного выпячивания твердой мозговой оболочки, образующего крышу турецкого седла и закрывающего выход из него). Диафрагма отделяет полость седла от субарахноидального пространства, исключая лишь отверстие, через которое проходит ножка гипофиза. Прикрепление диафрагмы, ее толщина и характер отверстия в ней подвержены значительным анатомическим вариациям. В основе патогенеза первичного синдрома ПТС лежит недоразвитие диафрагмы турецкого седла, как правило, в сочетании с факторами, приводящими к его недостаточности. К этим факторам можно отнести: повышение внутричерепного давления (легочная, сердечная недостаточность, артериальная гипертензия и т.д.); физиологическую или патологическую гиперплазию гипофиза или его стебля (многочисленные беременности, длительный прием оральных контрацептивов, длительная неадекватная заместительная терапия недостаточности периферических эндокринных желез); спонтанные некрозы опухолей, появление и изменение размера кист гипофиза.
Опухоли надпочечников считаются одним из сложных в диагностическом и лечебном плане разделов клинической эндокринологии. Социальная значимость опухолей надпочечников определяется рядом существенных обстоятельств. Во-первых, большинство новообразований надпочечников выявляется у пациентов в возрасте от 40 до 70 лет, причем пик заболеваемости приходится на возрастную категорию 45–50 лет. Во-вторых, одним из ведущих клинических проявлений заболевания у большинства пациентов является артериальная гипертензия (АГ), которая в ряде случаев, протекая злокачественно, приводит к развитию тяжелых, нередко смертельных, сердечно-сосудистых осложнений. И, наконец, злокачественные опухоли надпочечников, хотя и относятся к числу редких заболеваний, характеризуются крайней агрессивностью и тяжестью клинического течения, неудовлетворительными результатами лечения и неблагоприятным прогнозом [1].
Ниже описан случай сочетания синдрома ПТС и опухоли надпочечника с ложным преждевременным половым развитием у четырехлетнего мальчика. Под нашим амбулаторным наблюдением находится мальчик Р., 1999 г.р., проживающий в г. Ташкенте. Со слов родителей, пациент жалуется на низкорос-лость, остановку роста, увеличение половых органов, повышение тембра голоса, подъемы артериального давления (АД), головные боли, потемнение кожных покровов, пониженный аппетит. Анамнез жизни: ребенок родился в срок, рост при рождении 50 см, вес 3000 г. Психомоторное развитие — с опозданием. Родители ребенка обратились к эндокринологу впервые в 2003 г. в четырехлетнем возрасте (сейчас ему 16 лет), был госпитализирован в детское отделение РСНПМЦ эндокринологии МЗ РУз с диагнозом: опухоль левого надпочечника, преждевременное половое развитие. Тогда ему был выставлен следующий клинический диагноз. Основной: опухоль левого надпочечника смешанного генеза. Сопутствующий: миопия легкой степени. Осложнение: ложное преждевременное половое развитие (ППР) надпочечникового генеза.
В связи с этим в 2008 г. в той же клинике больной прооперирован: удаление опухоли левого надпочечника. Рекомендации принимать глюкокортикоиды не выполнялись. С 2010 года стало повышаться АД, назначен эналаприл 5 мг, сульфат магнезии. С такими жалобами больной ежегодно поступает в детское отделение РСНПМЦ эндокринологии на стационарное лечение. Учится в колледже.
Объективно: общее состояние удовлетворительное. Кожные покровы и видимые слизистые темного цвета. В легких аускультативно везикулярное дыхание. Тоны сердца ритмичные, пульс 78 уд/мин, АД 180/120 мм рт.ст. Живот мягкий, безболезненный. Печень и селезенка не увеличены, при пальпации безболезненны. Стул и диурез в норме. Рост 154 см, вес 57 кг. Рост отца 170 см, рост матери — 160 см. Пубертатный статус: Ах2Рх3, testis 20,0 × 20,0 мл, penis длиной 9,0 см. Пубертатный статус по Таннеру соответствует 3–4-й стадии, что наблюдается с четырехлетнего возраста.
Гормональные исследования крови: СТГ — 1,1 мМЕ/л (в норме у детей от 5 до 16 лет 2,10 ± ± 0,53 мМЕ/л), АКТГ — 21,7 пг/мл (до 50), ЛГ — 3,9 мМЕ/л (в норме в пубертате от 6 мМЕ/л), ФСГ — 4,6 мМЕ/л (в норме от 6 мМЕ/л), ДГЭА — 126 мкг/100 мл, альдостерон — 140,1 (8,0–172,0 пг/мл),
ангиотензин — 1,7 нг/мл/час (0,5–1,9 нг/мл/час), 17-альфагидроксипрогестерон — 0,83 нмоль/л, св. тестостерон — 5,9 нмоль/л (10–40 нмоль/л), кортизол — в 08.00 утра — 368 нмоль/л (250–720 нмоль/л), в 18.00 — 292 нмоль/л, в полночь — 148,1 нмоль/л (ритм секреции кортизола в норме). Общеклинические исследования крови и мочи в норме. Гликемия натощак — 4,8 ммоль/л, ферменты и электролиты крови в норме.
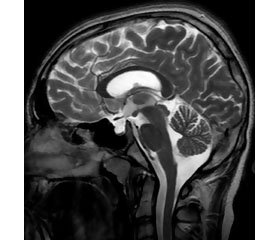
На МРТ турецкого седла и головного мозга (от 16.01.2015 г.) гипофиз расположен в центре турецкого седла, бобовидной формы, размерами (передне-задний, вертикальный, поперечный) 10 × 4 × 12 мм. Передняя доля однородной структуры, с интенсивными сигнальными характеристиками. Задняя доля расположена обычно. Воронка не смещена (синдром ПТС). В структуре субкортикального и перивентрикулярного белого вещества полушарий головного мозга с двух сторон — множество участков патологической интенсивности. В передних отделах височной доли справа — небольшой внутримозговой участок патологической интенсивности. Умеренная атрофия лобно-височных долей с обеих сторон.
На рентгенограмме кисти (от 02.12.2014 г.) костный возраст 16–17 лет, зоны роста открыты. КТ надпочечников (от 16.01.2015): состояние после операции на левом надпочечнике, признаки диффузной гиперплазии обоих надпочечников. ЭКГ — ритм синусовый, ЧСС 75 уд/мин, гипертрофия левого желудочка. Консультация окулиста: миопия тяжелой степени. Начинающийся застой диска зрительных нервов. Консультация уролога: гипогонадизм. На основании вышеуказанного был выставлен клинический диагноз. Основной: состояние после удаления опухоли левого надпочечника смешанного генеза (2008 г.). Сопутствующий: синдром ПТС (первичная форма). Внутричерепная гипертензия. Миопия высокой степени. Осложнение: синдром артериальной гипертензии. Задержка роста и полового развития. Гипогонадотропный гипогонадизм. Дефицит гормона роста.
Пациенту рекомендовано проведение консервативной терапии: бромергон по 1/4 табл. перед сном, эутирокс 25 мкг ежедневно утром, идеос 500 по 1 табл. в день, бисопролол 5 мг 2 раза в день, норваск 5 мг 2 раза в день, глицин и др.
Таким образом, если у пациента до удаления опухоли надпочечника отмечалось ложное прежде-временное половое развитие, то после ее удаления отмечается гипогонадотропный гипогонадизм и низкорослость на фоне синдрома ПТС. Это определяет назначение терапии генно-инженерным гормоном роста (у пациента зоны роста открыты), а также курсов терапии хорионическим гонадотропином.
Таким образом, наличие синдрома ПТС влечет за собой вероятность развития низкорослости и гипогонадотропного гипогонадизма у подростков с необходимостью последующей соответствующей заместительной гормональной терапии. У пациентов с ППР на фоне опухоли надпочечника в послеоперационном периоде может развиться задержка пубертата при наличии синдрома ПТС.