Газета «Новости медицины и фармации» Аллергология. Пульмонология. Антимикробная и противовирусная терапия (555) 2015 (тематический номер)
Вернуться к номеру
Критическая оценка биластина для лечения аллергического риноконъюнктивита и крапивницы
Авторы: Belen Sadaba, Jose Ramon Azanza, Almundena Gomez-Guiu, Raquel Rodil
Clinical Pharmacology Service, Clinica Universidad de Navarra, Navarra, Spain
Рубрики: Аллергология , Пульмонология
Разделы: Справочник специалиста
Версия для печати
Статья опубликована на с. 5-11
Биластин
Биластин является новым препаратом на фармацевтическом рынке и представляет собой антигистаминный пероральный препарат для лечения аллергического риноконъюнктивита и хронической крапивницы у взрослых и подростков [1]. Антигистаминные средства второго поколения превзошли препараты первого поколения прежде всего благодаря более высокой толерантности, основанной на отсутствии антихолинергических эффектов и низком риске кардиотоксичности. Тем не менее антигистаминные препараты второго поколения способны проникать через гематоэнцефалический барьер и, следовательно, могут вызывать сонливость. Кроме того, многие из этих антигистаминных препаратов метаболизируются ферментами цитохрома Р450 и, таким образом, могут потенциально взаимодействовать с другими препаратами. Как будет обсуждаться ниже, эти характеристики были рассмотрены и модифицированы путем применения препарата биластин. Целью данной статьи является оценка биластина как средства для лечения хронической крапивницы и аллергического риноконъюнктивита путем анализа опубликованных результатов эффективности и безопасности этого препарата.
Фармакодинамика
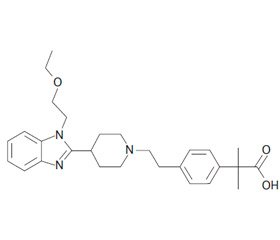
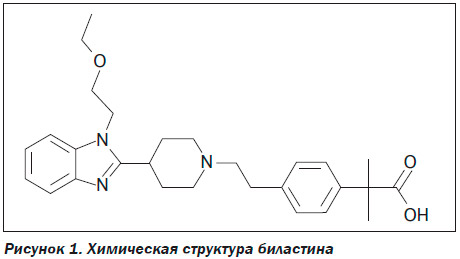
Молекула биластина, или 2-[4-[2-[4-[1-(2-бензимидазол-2-ил] пиперидин-1-ил]этил]фенил]-2-метилпропионовой кислоты (рис. 1), имеет молекулярную массу 463,6 дальтон. Судя по структуре оригинальной молекулы биластина, он относится к группе новых антигистаминных препаратов второго поколения.
Биластин весьма избирателен в отношении связывания с H1-гистаминовыми рецепторами и не оказывает ингибирующего действия на другие виды рецепторов (мускариновые, адренергические, серотонинергические, другие гистаминовые рецепторы, брадикининовые, рецепторы к лейкотриену D4 или кальциевые рецепторы). Он обладает большим сродством к Н1-рецепторам, сравним с другими антигистаминными препаратами, такими как астемизол или дифенгидрамин, и имеет в 3 и 5 раз большее химическое сродство к этим рецепторам, чем фексофенадин и цетиризин соответственно [2]. Степень блокады этих рецепторов зависит от дозы. В равной мере в доклинических исследованиях и на здоровых добровольцах специально изучался антимускариновый эффект. Этот эффект не наблюдался в клеточных моделях. После лечения различными дозами биластина (20, 40 и 80 мг/день) в течение 7-дневного периода у человека не наблюдалось никаких изменений в реакции зрачков [3]. Таким образом, можно сделать вывод, что биластин не обладает нежелательными антихолинергическими эффектами, которые имеются у антигистаминных препаратов первого поколения.
В различных моделях на мышах биластин противодействует эффекту гистамина в зависимости от концентрации (ингибирует повышенную проницаемость капилляров, понижает микрососудистую транссудацию и уменьшает бронхоспазм); его эффект аналогичен фексофенадину и более сильный, чем у цетиризина. Антигистаминный эффект биластина имел большую продолжительность, чем цетиризина [4].
В результате терапии биластином в тучных клетках и гранулоцитах периферической крови наблюдалось ингибирование высвобождения гистамина, интерлейкина (ИЛ)-4 и фактора некроза опухоли альфа [5].
В I фазе исследования на здоровых добровольцах, в котором оценивали дозы 2,5 и 50 мг, наблюдалось снижение гистамин-индуцированной гиперемии и аллергической сыпи, аналогичное таковому при терапии цетиризином, хотя для достижения быстрых результатов предполагалось применение более высоких доз биластина (20 и 50 мг) [6].
Фармакокинетика
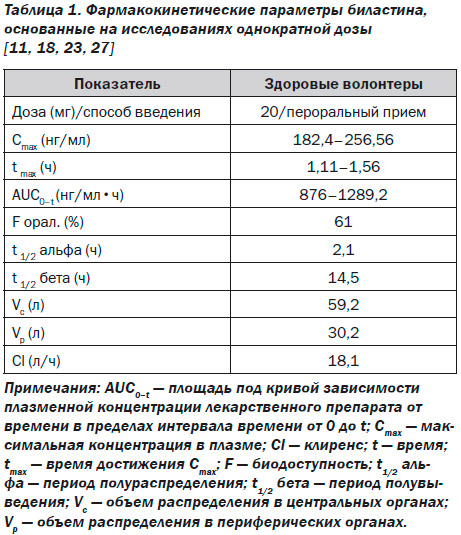
Биластин доступен в таблетированной форме; его фармакокинетические свойства были оценены в доклинических и клинических испытаниях, некоторые из которых представляли I фазу исследования (табл. 1). Фармакокинетические параметры биластина приведены в табл. 1.
После перорального приема биластин быстро всасывается, достигая максимальной концентрации (Cmax) через 1–1,5 часа. Всасывание является первым процессом, отслеживающим линейность дозы в диапазоне от 2,5 до 220 мг, одинаково как для однократного, так и для многократного приема, без признаков аккумуляции препарата после 14 дней лечения [78]. Это быстрый процесс, коэффициент всасывания равняется 1,5 ч–1 [7]. Считается, что при пероральном приеме терапевтической дозы 20 мг средняя максимальная концентрация в 220 нг/мл достигается в течение 1,3 ч после введения, с последующей биэкспоненциальной элиминацией.
Биодоступность биластина составляет 60 %. Он является субстратом из мембранных белков-переносчиков, присутствующих в клетках просвета кишечника: Р-гликопротеина и полипептида — переносчика органических анионов. Р-гликопротеин, выступая в роли белка, способствующего оттоку веществ из клеток, содействует снижению его биодоступности, в то время как полипептид — переносчик органических анионов повышает его всасывание. Оба переносчика присутствуют в люминальной мембране двенадцатиперстной кишки, что указывает на сильное взаимодействие между ними, работающими в противоположных направлениях. Оба переносчика склонны взаимодействовать с принимаемыми с пищей фруктовыми соками и некоторыми лекарственными препаратами [9].
Биодоступность уменьшается при совместном приеме с пищей, богатой жирами и веществами, которые влияют на активность мембранного переносчика. В исследовании с участием здоровых добровольцев наблюдалось снижение биодоступности на 30 % при совместном приеме препарата с пищей, содержащей высокое количество жиров, и снижение на 25 %, когда пища содержала стандартное количество жира [10, 11]. В частности, грейпфрутовый сок способствовал снижению биодоступности на 30 % [10, 11].
Биластин имеет двухкамерную модель распределения, кажущийся объем распределения составляет 1,29 л/кг.
Он на 84–90 % связывается с белками плазмы.
В исследованиях на животных с радиоактивным меченым биластином препарат распределялся в желудочно-кишечном тракте и печени, не достигая головного мозга [12].
Биластин почти не метаболизируется и выводится в неизмененном виде через почки и с калом. Масса балансовых исследований показала, что 33 % биластина выводится из организма с мочой и 67 % — с калом [13]. Исследование с культурами гепатоцитов и микросомами печени показало отсутствие метаболизма, опосредованного цитохромом Р450, а также отсутствие какого-либо ингибирующего или стимулирующего эффекта со стороны этого фермента [7]. Отсутствие ингибирования является одной из характеристик, которые вызывают интерес к биластину в соответствии с рекомендациями, опубликованными группой экспертов по лечению аллергического ринита [1]; 96 % введенной дозы выводится из организма в течение 24 часов, а через 72 часа он полностью элиминируется с мочой; период полувыведения составляет около 14 часов. Почечная функция существенно не влияет на фармакокинетику биластина [10], хотя при ее снижении наблюдалось увеличение плазменной концентрации данного антигистаминного препарата. В целом это говорит об отсутствии необходимости в коррекции дозы препарата в случае почечной недостаточности, хотя данную меру предосторожности необходимо принимать в ситуациях, когда концентрация биластина в крови может увеличиваться в результате сопутствующего введения ингибиторов гликопротеина P, как это наблюдалось в случае с кетоконазолом [14].
У пациентов с нарушением функции печени оценка коррекции дозы биластина не проводилась, хотя, учитывая тот факт, что биластин не метаболизируется в печени, в этой группе пациентов вообще не следует ожидать изменений фармакокинетики данного препарата или необходимости регулировки его дозы.
В фармакокинетике биластина не наблюдалось никаких различий, связанных с полом и возрастом, за исключением того, что самые высокие значения максимальной концентрации в плазме (Cmax) наблюдались у женщин в возрасте 18–35 лет. Влияния различных ковариант (возраст, вес, рост, пол, ЧСС, сывороточный альбумин, креатинин, билирубин, печеночные транс–аминазы, щелочная фосфатаза или мочевина) при анализе фармакокинетики популяции не наблюдалось [7].
На основании данных, полученных у взрослого населения, было подсчитано, что доза для детей в возрасте от 2 до 12 лет должна составлять 10 мг в сутки, а для детей в возрасте до 2 лет — 5 мг в сутки [15], хотя для подтверждения этих доз в настоящее время проводятся дополнительные исследования.
Ранее была оценена возможность взаимодействия биластина с пищей и другими препаратами. Как уже упоминалось, грейпфрутовый сок уменьшает биодоступность биластина [10, 11]. Ингибирование мембранного полипептида — переносчика органических анионов, который облегчает всасывание некоторых лекарственных средств, вероятно, являлось механизмом, ответственным за это взаимодействие [9]. Данного эффекта на белок-переносчик можно было бы избежать, если принимать биластин либо за час до, либо через два часа после употребления пищи или соков. Некоторые субстратные препараты или ингибиторы этого белка-переносчика, такие как ритонавир или рифампицин, могли приводить к снижению концентрации биластина в плазме [16], хотя данный конкретный вопрос не был оценен.
Влияния биластина на фармакокинетику кетоконазола у здоровых добровольцев не наблюдалось [14]. С другой стороны, эффект биластина усиливался вдвое в результате совместного приема препарата с кетоконазолом, что, вероятно, было связано с ингибирующим эффектом последнего на мембранные белки-переносчики, такие как P-гликопротеин, в клетках стенки кишечника, не оказывающим влияния на печеночный клиренс [17].
Также не наблюдалось никакого взаимодействия биластина с препаратами, оказывающими успокаивающее действие на центральную нервную систему, такими как лоразепам [18] или спирт [19].
Фармакокинетика/фармакодинамика
При комплексной оценке фармакокинетических и фармакодинамических данных был сделан вывод, что биластин характеризуется двухкамерной моделью кинетики: быстрой фазой всасывания и максимальным эффектом через 4 часа после приема препарата. Фармакодинамика исчезновения аллергической сыпи или гиперемии была установлена на основе косвенной модели ответов для определения концентрации, которая приводит к 50% ингибирующей концентрации (ИК50) 5,15 нг/мл и 1,25 нг/мл соответственно. При суточной дозе биластина 20 мг взрослым плазменные концентрации остаются выше этих значений в течение 20 и 24 ч соответственно, что указывает на то, что однократный прием препарата в сутки считается адекватным [7]. В моделировании, выполненном для детей в возрасте от 2 до 12 лет, доза 10 мг была достаточной для поддержания плазменной концентрации препарата выше этого значения в течение всего срока приема препарата [15].
Эффективность
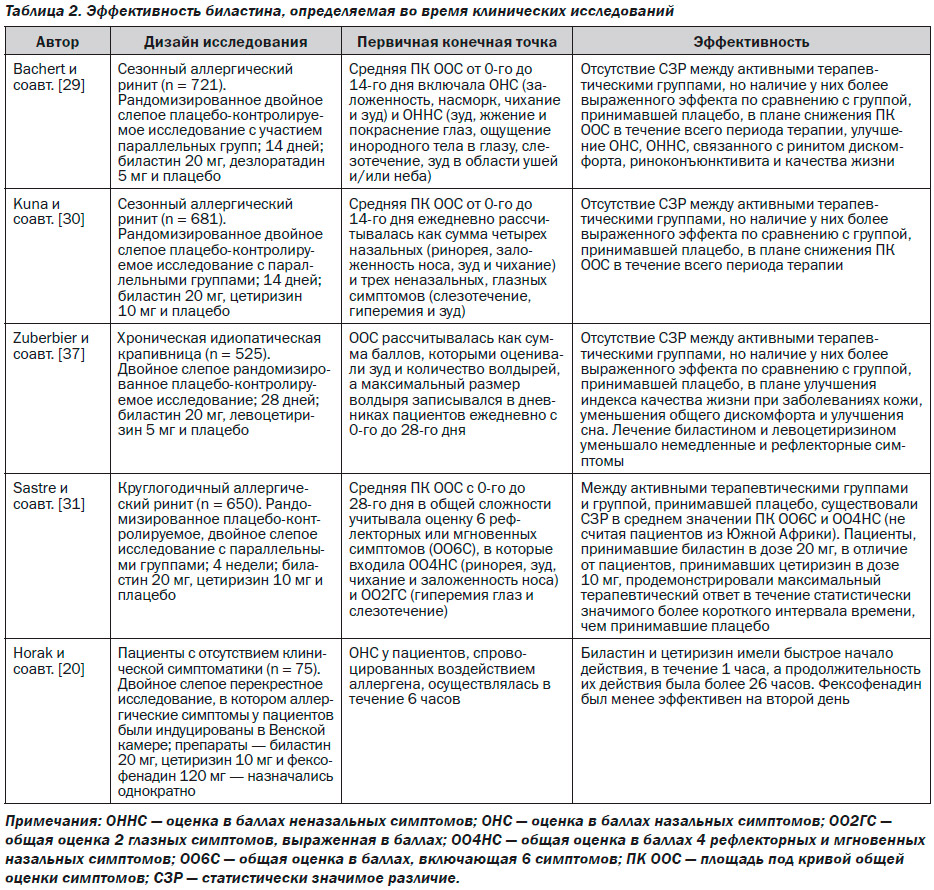
Оценка эффективности биластина, основанная на клинических исследованиях, показана в табл. 2.
При выборе антигистаминного препарата решающими факторами являются начало его действия и продолжительность антигистаминного эффекта. Наряду с этими сведениями была выполнена оценка эффекта биластина в отношении купирования аллергениндуцированных назальных и глазных симптомов у 75 пациентов с аллергией на пыльцу. Пациенты подвергались воздействию контролируемых концентраций пыльцы с использованием стандартного метода индукции аллергии (Венской камерой для вызова реакции) [20]. Пациентам проводили два провокационных теста с пыльцой в течение двух дней подряд, в течение 6 часов в первый день и в течение 4 часов во второй день. Назальные симптомы оценивали каждые 15 минут. Четыре из этих симптомов (насморк, заложенность носа, чихание и носовой зуд) считались главными показателями данного исследования. Экспериментальная терапия включала использование 20 мг биластина, 10 мг цетиризина, 120 мг фексофенадина или плацебо, которые пациенты принимали через 2 часа после первой провокации. В данном исследовании у биластина и цетиризина начало действия наблюдалось приблизительно через 1 час, а продолжительность действия составляла не менее 26 часов. Продолжительность действия фексофенадина, как предполагалось, была короче; при этом учитывался тот факт, что он был менее эффективен на второй день исследования [20]. Было проведено аналогичное исследование, в котором сравнивался эффект 20 и 50 мг биластина и 10 мг цетиризина в отношении ингибирования кожной сыпи и гиперемии после скарификационной пробы в разное время по отношению к применению препарата. Реакция на прием 20 мг биластина и 10 мг цетиризина в различных точках оценки была одинаковой, за исключением анализа, полученного через 1,5 часа после приема, который показал, что биластин имел более быстрое начало действия. Прием 50 мг биластина продлевал антигистаминный эффект. В исследовании на здоровых добровольцах наблюдаемые результаты показали существование определенного дозозависимого эффекта в отношении ингибирования аллергической сыпи, возникшего в результате подкожной инъекции гистамина [3].
Клинические исследования
Аллергический риноконъюнктивит (сезонный и круглогодичный)
Блокаторы H1-гистаминовых рецепторов являются препаратами первого ряда для лечения аллергического риноконъюнктивита. Аллергический ринит — это одно из наиболее распространенных хронических заболеваний в мире, его распространенность, по оценкам, составляет 10–25 % [22]. Наиболее частыми симптомами аллергического ринита являются назальный зуд, чихание, ринорея и заложенность носа [23]. У пациентов с аллергическим ринитом снижено качество жизни [24] по причине симптомов ринита и патофизиологических факторов, которые могут привести к расстройству сна [25].
Назальный ответ на стимуляцию аллергеном провоцирует все симптомы, характерные для аллергического ринита. Этот ответ включает в себя два этапа. Реакция немедленного типа возникает спустя 20 минут после контакта с аллергеном и может продолжаться несколько часов после его воздействия. Это прежде всего результат дегрануляции тучных клеток. Данная фаза характеризуется зудом, чиханием и ринореей. Тучные клетки выделяют хемотаксические вещества и цитокины, которые способны привлечь в очаг воспаления и другие клетки, в том числе эозинофилы. Это приводит к поздней фазе аллергической реакции (возникающей спустя 48 часов), которая содержит клеточный ответ. Основным симптомом в этой фазе выступает заложенность носа [26].
Гистамин является одной из субстанций, которые высвобождают тучные клетки и базофилы. Этот амин выделяется в течение нескольких секунд в результате реакции гиперчувствительности, опосредованной иммуноглобулином E (IgE). Спустя минуту после стимуляции слизистой носа аллергеном высвобожденный гистамин достигает максимальной концентрации. Спустя десять минут после этого пика происходит резкое падение его концентрации [27]. Гистамин вызывает повышение хемотаксиса эозинофилов, увеличение высвобождения цитокинов (ИЛ-1β, ИЛ-6, ИЛ-4 и –ИЛ-5), повышение высвобождения молекул адгезии сосудистого эндотелия 1-го типа (МАСЭ)-1 и активацию ядерного фактора (ЯФ)-κВ. Гистамин вызывает характерную симптоматику аллергического ринита, включая заложенность носа.
H1-гистаминоблокаторы могут иметь разные механизмы действия: они противодействуют эффектам гистамина на H1-рецепторы, а также способны ингибировать его высвобождение из тучных клеток и базофилов, что является основным патогенетическим звеном развития поздней фазы аллергической реакции [28]. Биластин является весьма избирательным антигистаминным препаратом, имеющим среднее и высокое химическое сродство с H1-рецепторами. Кроме того, исследования in vitro продемонстрировали противовоспалительную активность путем ингибирования высвобождения гистамина, ИЛ-4 и фактора некроза опухоли (ФНО) α, а также за счет индукции высвобождения различных стимуляторов [5].
Эффективность биластина при аллергическом риноконъюнктивите была подтверждена в ряде исследований, сравнивающих его с плацебо или с другими антигистаминными препаратами.
Bachert и соавт. провели многоцентровое исследование для анализа клинической эффективности посредством оценки назальных и неназальных симптомов перед началом терапии и спустя 14 дней лечения, а также безопасность биластина в дозе 20 мг по сравнению с дезлоратадином в дозе 5 мг и плацебо у пациентов с сезонным аллергическим ринитом (n = 721). При использовании обоих препаратов наблюдалось статистически значимое снижение назальных и неназальных симптомов у пациентов по сравнению с плацебо. В то же время наблюдалось снижение степени дискомфорта, оцениваемой самими пациентами, и повышение оценки общего клинического наблюдения, проводимой исследователем. Тем не менее между биластином и дезлоратадином не было обнаружено никаких достоверных различий [29].
В дальнейшем исследовании сравнивали эффективность биластина в дозе 20 мг, цетиризина в дозе 10 мг и плацебо у пациентов с сезонным ринитом. Были обнаружены статистически значимые различия в улучшении назальных симптомов в группе пациентов, принимавших биластин (–43,8 % после 7 дней и –48,5 % после 14 дней терапии) и цетиризин (–40,2 % после 7 дней и –50,6 % после 14 дней терапии), по сравнению с группой, принимавшей плацебо (P < 0,001). При этом не наблюдалось никаких достоверных различий между терапевтическими группами [30].
Ежедневный прием 2 мг биластина был эффективен для лечения круглогодичного аллергического ринита, болезни, которая поражает значительную часть населения (10–15 %). Оценка выполнялась на основании назальных (ринорея, чихание, заложенность носа и назальный зуд) и глазных симптомов (гипере–мия и слезотечение) в сравнении с эффектом от плацебо. Результаты показали, что биластин и цетиризин имеют аналогичный эффект среди пациентов в Европе и более выраженный эффект среди пациентов в Аргентине; спустя 28 дней терапии облегчение назальных симптомов отмечалось приблизительно в 34 % случаев [31].
Bartra и соавт. провели обзор клинических исследований, посвященных изучению биластина, с целью оценки его действия на глазные симптомы при аллергическом риноконъюнктивите (зуд, гиперемия и слезотечение). Результаты клинических исследований показали, что для купирования глазных симптомов при сезонном аллергическом рините биластин является столь же эффективным, как и препараты сравнения [32].
Аналогичным образом была выполнена и оценка действия биластина на заложенность носа при аллергическом рините. Для купирования этого симптома была протестирована эффективность 20 мг биластина. В результате было установлено, что эффективность биластина аналогична эффективности его активных препаратов сравнения (5 мг дезлоратадина и 10 мг цетиризина) [23].
Недавно также был отдельно проанализирован параметр качества жизни. Он был оценен вторично в трех клинических исследованиях, посвященных изучению аллергического ринита, с помощью вопросника по качеству жизни больных с риноконъюнктивитом, охватывавшего в общей сложности 2 335 пациентов, и пациентов с хронической крапивницей с помощью вопросника для оценки индекса качества жизни при заболеваниях кожи, охватывавшего 525 пациентов; итоговые оценки сравнивались с аналогичными оценками после приема плацебо и левоцетиризина [33]. Полученные данные были параллельны результатам эффективности, наблюдаемым в клинических исследованиях.
Хроническая крапивница
Хроническая крапивница оказывает значительное влияние на качество жизни пациентов. Она характеризуется появлением зудящих эритематозных папул. Продолжительность существования папул меньше 24 часов, они могут появляться в течение дня или более одного раза в неделю в течение 6 недель. В 50 % случаев она может проявляться ангионевротическим –отеком [34].
Клинические рекомендации по лечению хронической крапивницы предполагают возможность увеличения обычной дозировки антигистаминных препаратов до 4 раз, если обычные терапевтические дозировки оказываются неэффективными [35]. Тем не менее в литературе отсутствуют рандомизированные двойные слепые исследования, которые бы изу–чали различия в эффективности между терапевтическими дозами и высокими дозами, применяемыми для купирования проявлений хронической крапивницы. В этом плане имеются предварительные данные касательно биластина, например данные, полученные в I фазе двойного слепого клинического исследования, изучавшего прием однократной дозы с четырьмя перекрестными периодами на 21 добровольце, которые были разделены на терапевтические группы для приема плацебо, 10 мг цетиризина или 2,5; 5; 10 или 50 мг биластина. Выполнялась оценка взаимосвязи между дозой биластина и ингибированием кожного ответа на гистамин (посредством оценки волдырей и очага гиперемии). Каждая из доз биластина снижала количество гистамининдуцированных волдырей в течение 1,5–12 часов и гипе–ремии в течение 4–24 часов после приема препарата, демонстрируя реакцию, которая была аналогичной или лучше выраженной, чем после приема цетиризина. Очевидного дозозависимого эффекта не наблюдалось, тем не менее дозы препарата 20 и 50 мг оказывали более длительный эффект [13].
Audicana и соавт. провели II фазу исследования, которая охватывала 222 пациента с хронической крапивницей. Эффект биластина (в дозах 10, 20, и 30 мг) оценивали в сравнении с плацебо в контрольной группе на основании появления папул и кожного зуда. Статистически значимые различия наблюдались в трех терапевтических группах, которые принимали биластин, по сравнению с группой, принимавшей плацебо; при этом, согласно данным Ferrer и соавт., дозозависимого эффекта не наблюдалось [36].
Эффект биластина также оценивали в двойном слепом контролируемом клиническом исследовании в сравнении с плацебо и левоцетиризином, которые пациенты принимали в течение 28 дней. Оценивали сложный показатель путем расчета данных касательно зуда, количества волдырей и максимального их размера, основываясь на дневниках пациентов. Симптомы утихали на второй день терапии биластином в дозе 20 мг, а также в случае приема левоцетиризина, демонстрируя лучшие результаты по сравнению с плацебо [37].
Переносимость и безопасность
В различных исследованиях, проведенных в ходе доклинической разработки биластина, не было продемонстрировано выраженной токсичности. Острая токсичность биластина была исследована с помощью орального и внутривенного введения у мышей и крыс. После орального введения 5 000 и 2 000 мг/кг у мышей и крыс соответственно случаев смерти не наблюдалось. Тем не менее после внутривенного введения летальная доза для 50 % животных составляла 33 мг/кг для мышей и 45–75 мг/кг для крыс [38].
В исследованиях, изучавших хроническую токсичность биластина, никаких признаков токсичности не наблюдалось ни в одном из органов как при оральном, так и при внутривенном введении препарата [38]. В исследованиях, проведенных на мышах и кроликах, не наблюдалось воздействия на рождаемость, а также токсичности и тератогенности данного препарата в отношении эмбриона и плода [39].
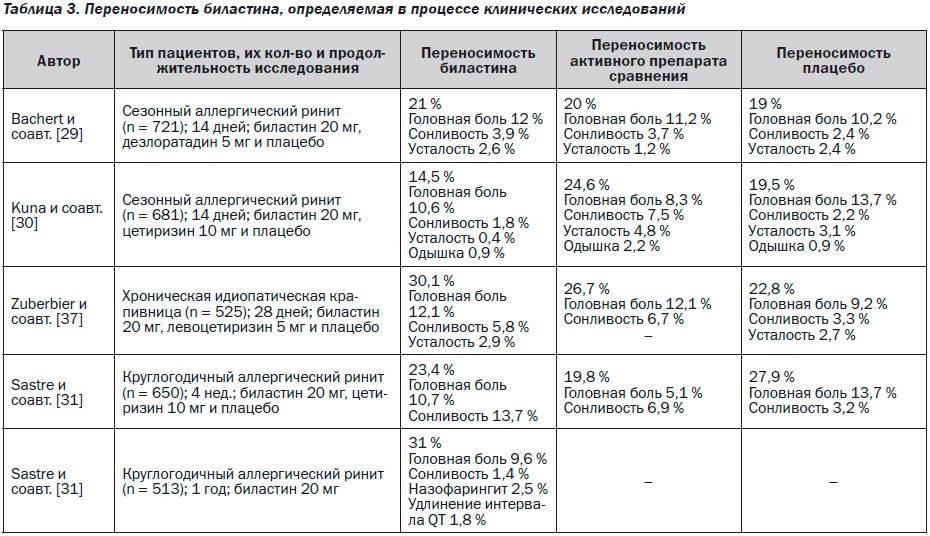
В исследованиях, проведенных на людях в процессе оценки эффективности биластина при терапии хронической крапивницы и аллергического ринита переносимость изучалась в сравнении с плацебо и другими антигистаминными препаратами (левоцетиризин, дез–лоратадин и цетиризин); большая часть данных сообщает о терапевтической дозе 10 мг в сутки; в табл. 3 приведены результаты этих клинических исследований. Конкретные исследования также были проведены с целью оценки частоты проблем, обычно связанных с приемом антигистаминных препаратов, таких как сон–ливость и нарушения сердечного ритма.
В целом биластин хорошо переносился, и большинство описанных побочных эффектов имели легкую и среднюю степень выраженности. Частота возникновения побочных эффектов, связанных с приемом препарата, составляла 15–30 % и была аналогична наблюдаемой при приеме плацебо. Никаких серьезных побочных эффектов, связанных с приемом препарата, в каком-либо из клинических испытаний обнаружено не было. Никаких значимых изменений в показателях жизненно важных функций (ЧСС или артериальное давление), параметрах электрокардиограммы (ЭКГ) или лабораторных тестах (гематологические данные и функции печени и почек) отмечено не было [29, 30, 37].
Побочными эффектами, которые наиболее часто описывались пациентами в процессе терапии биластином и в некоторой степени были связаны с данным препаратом, являлись головная боль, сонливость, головокружение и усталость [29, 30, 37, 40]. В исследовании, в котором терапия проводилась в течение 1 года, наиболее часто описываемыми побочными эффектами были головная боль (9,6 %) и назофарингит (2,5 %), в то время как другие, менее распространенные побочные эффекты, связанные с приемом биластина, включали некоторые изменения кривой ЭКГ, которые не были стойкими и исчезали с течением времени [31].
Никаких особенностей в переносимости биластина по сравнению с цетиризином и дезлоратадином не наблюдалось [29, 37]. В одном исследовании, в котором сравнивали эффект биластина в дозе 20 мг в день с эффектом цетиризина в обычных дозах, описывалось статистически значимое незначительное появление сон–ливости (у 1,8 % пациентов, принимавших биластин, по сравнению с 7,5 % пациентов, принимавших цетиризин) и усталости (у 0,4 % пациентов, принимавших биластин, по сравнению с 4,8 % пациентов, принимавших цетиризин) [30].
Прием некоторых антигистаминных препаратов второго поколения был связан с такими неблагоприятными сердечными эффектами, как удлинение интервала QT и развитие полиморфной желудочковой тахикардии типа «пируэт». Эти эффекты были отнесены к прямой блокаде калиевых каналов. По этой причине и следуя рекомендациям Международной конференции по гармонизации (МКГ) E14, было проведено исследование с целью оценки влияния терапевтической дозы 20 мг и сверхтерапевтической дозы 100 мг на интервал QTc. Это было многодозовое рандомизированное двойное слепое перекрестное исследование с применением плацебо и моксифлоксацина в дозе 400 мг (в роли второго активного препарата сравнения), отвечающего за подобного рода изменения. В это исследование была включена пятая терапевтическая группа, пациентам из которой назначали 20 мг биластина в комбинации с 400 мг кетоконазола. В обеих терапевтических группах, принимавших 20 или 100 мг биластина соответственно, на электрокардиограмме не наблюдалось никаких эффектов, в частности касающихся длительности интервала QTc или морфологии зубца Т. Увеличение величины интервала QTc на 5 миллисекунд или менее подтверждает отсутствие этого влияния. Никаких статистически значимых эффектов на интервал QTc не наблюдалось в любой из оцениваемых доз. Изменения, отмечаемые в терапевтической группе, принимавшей комбинированную терапию биластином с кетокона–золом, были связаны с противогрибковым препаратом, учитывая тот факт, что плазменные концентрации биластина в этом совместном приеме были меньше по сравнению с теми, которые наблюдались у пациентов, принимавших сверхтерапевтическую дозу 100 мг [41, 42]. Эти результаты согласуются с другими исследованиями, посвященными биластину, и с клиническими исследованиями с участием пациентов, у которых не наблюдалось изменений в ЭКГ или кардиотоксических побочных эффектов.
Оценка неврологической толерантности проводилась в отдельных исследованиях для анализа появления сонливости/седации и влияния на внимание при вождении автомобиля после терапии биластином. Седативный эффект антигистаминных препаратов первого поколения широко известен, в связи с этим данные препараты в некоторых случаях используются в качестве снотворного средства [43]. Этот эффект связан с химическим сродством молекулы биластина с P-гликопротеином, который вызывает отток препаратов и других веществ из центральной нервной системы, и с липофильностью препаратов: чем больше это сродство и ниже липофильность, тем ниже проницаемость гематоэнцефалического барьера.
В клиническом перекрестном исследовании повторных доз на здоровых добровольцах проводили сравнение трех доз биластина (20, 40 и 80 мг) с гидро–ксизином в дозе 25 мг и плацебо после 7 дней терапии и с периодом отмывки 15 дней между каждым запланированным введением. Дана оценка их влияния на функцию психомоторного (двигательная активность, восприятие, внимание и ассоциативная интеграция) и психического состояния. Гидроксизин вызвал увеличение времени реакции, уменьшение частоты мигания глаз и ухудшение внимания и двигательной активности. При приеме биластина в дозе 20 и 40 мг никаких изменений в оцениваемых параметрах не наблюдалось, хотя при оценке объективных параметров отмечались изменения при приеме самой высокой дозы (80 мг). Только доза 20 мг была субъективно отличима от плацебо [3].
Для оценки влияния препарата на сонливость у людей, управляющих автомобилем, было проведено клиническое испытание на 22 здоровых добровольцах: две терапевтические группы ежедневно принимали биластин в дозах 20 и 40 мг соответственно в течение 8-дневного периода, а две другие (контрольные) группы принимали плацебо и гидроксизин в дозе 50 мг в день (положительный контроль). Это было перекрестное исследование с 7-дневным интервалом между периодами терапии. Положение автомобиля оценивали на постоянной скорости, записывая отклонение автомобиля по отношению к стандартному отклонению латерального положения. Оценка выполнялась на первый и восьмой день терапии. В терапевтических группах, принимавших биластин в дозах 20 и 40 мг, не наблюдалось никаких изменений: представленные результаты были аналогичны результатам в группе, принимавшей плацебо. В терапевтической группе, принимавшей гидроксизин, наблюдалось значительное увеличение в отклонении для всех измерений, несмотря на то что доза препарата была снижена по сравнению с первым приемом, при наличии фармакокинетического баланса после последней дозы [44].
В общем анализе данных о развитии сонливости, наблюдаемой в различных исследованиях, проведенных с биластином, был сделан вывод, что она аналогична сонливости, наблюдаемой при приеме плацебо, и значительно менее выражена, чем при приеме цетиризина [45].
Были проведены дальнейшие исследования с целью оценки эффектов биластина на центральную нервную систему в комбинации с другими препаратами, такими как лоразепам, или веществами, такими как алкоголь, седативный эффект которых хорошо известен. Ни в одном из этих исследований биластин в дозе 20 мг не оказывал такого эффекта и не усиливал эффект известных препаратов, оказывающих успокаивающее действие на центральную нервную систему [18, 19].
Заключение
Биластин является антигистаминным препаратом второго поколения, разработанным для терапии аллергического риноконъюнктивита и хронической крапивницы. Это препарат, который не подвергается метаболизму в печени и не оказывает влияния на активность изоферментов цитохрома Р450. Его не следует принимать совместно с пищей, которая может повышать его биодоступность. Терапия биластином в дозе 20 мг, принимаемым перорально, эффективна в борьбе с симптомами вышеуказанных заболеваний и улучшает качество жизни данных пациентов. Исследования показывают, что биластин имеет приемлемый профиль переносимости; у данного препарата не наблюдалось кардиотоксических эффектов, а терапевтическая доза биластина не влияет на концентрацию внимания пациента.
Перевод с англ. П. Огилько
Впервые опубликовано в журнале Therapeutics and Clinical Risk Management. 2013. № 9
Впервые опубликовано в журнале Therapeutics and Clinical Risk Management. 2013. № 9
Список литературы
находится в редакции