Статтю опубліковано на с. 140-144
Хронічна ішемія мозку (ХІМ) становить 96 % у структурі поширеності всіх форм цереброваскулярних захворювань і являє собою повільно прогресуючу недостатність кровопостачання головного мозку, що призводить до розвитку множинних дрібновогнищевих змін мозкової тканини та проявляється поступово наростаючим дефектом функцій мозку [10, 11, 19].
Етіопатогенетичними чинниками, що провокують розвиток ХІМ, є артеріальна гіпертензія, оклюзія магістральних артерій голови, порушення системного кровообігу, ураження екстра- та інтракраніальних судин при системних захворюваннях, порушення реологічних властивостей крові.
Основними клінічними проявами ХІМ є прогресуючі когнітивні порушення та розлади психоемоційної сфери, мультиформні рухові розлади, а її клінічними особливостями — прогресуючий перебіг, стадійність і синдромальність [8, 19, 20].
Слід зазначити зворотну залежність між наявністю скарг, особливо тих, що відображають здатність до пізнавальної діяльності (увага, пам’ять), і ступенем вираженості ХІМ: чим більше страждають когнітивні функції, тим менше скарг висловлює пацієнт. Таким чином, суб’єктивні прояви у вигляді скарг не відображають ні тяжкість, ні характер процесу [8, 21, 24].
Одним із найменш вивчених проявів ХІМ є гідроцефалія (ГЦ), незважаючи на те, що їх поєднання є досить поширеним явищем [5, 15, 19].
З одного боку, така комбінація можлива при морфологічній стадійності прогресування ХІМ (як приклад — замісна ГЦ при атрофічних процесах), з іншого — пояснюється поєднанням ХІМ та нормотензивної ГЦ [2, 6, 15, 22].
ГЦ дорослих — самостійна нозологічна форма або ускладнення ряду захворювань головного мозку, що характеризується активним прогресуючим процесом надмірного накопичення спинномозкової рідини в лікворних просторах, що обумовлено порушеннями її циркуляції [5, 12, 22].
Згідно із класифікацією, ГЦ поділяється: на внутрішню (шлуночкову), що характеризується скупченням ліквору переважно в шлуночках головного мозку; зовнішню — зі скупченням ліквору переважно в субарахноїдальному просторі; загальну (змішану) — зі скупченням ліквору як в шлуночках, так і в субарахноїдальному просторі [7, 23].
Довготривала ГЦ здатна призводити до незворотніх ішемічних і дегенеративних змін білої речовини та кори великого мозку та супроводжується феноменом їх «розщеплення».
У численних наукових дослідженнях доведене часте поєднання хронічної цереброваскулярної недостатності та ГЦ: в літературі існує цілий ряд робіт, що вказують на те, що хронічні судинні захворювання головного мозку сприяють виникненню ГЦ [4, 13, 22].
У дослідженнях доведена роль артеріальної гіпертензії як причинного фактора хронічної ГЦ у літніх людей та з’ясовані особливості деменції при судинній патології та нормотензивній ГЦ [5, 14, 22].
Згідно з даними нейровізуалізації, розширення шлуночкової системи при ХІМ, як правило, більш виражене, ніж розширення кіркових борозен, і може відображати не лише атрофічні зміни мозкової речовини в глибинних відділах мозку, але й зниження резистентності перивентрикулярних тканин до ліквородинамічних змін [3, 4]. Смужка перивентрикулярного набряку (лейкоареозу) навколо тіла шлуночка або його передніх і задніх рогів пов’язана з транссудацією цереброспінальної рідини, свідчить про активний процес та підвищення внутрішньочеревного тиску, розширення кіркових борозен — про ГЦ ex vacuo [16, 17, 19].
Про можливість поєднання нормотензивної ГЦ і цереброваскулярної недостатності свідчать і дані ней-ровізуалізації пацієнтів із нормотензивною ГЦ, у значної кількості яких знаходять безліч дрібних ішемічних вогнищ або вогнищ лейкоареозу, що не суперечить діагнозу нормотензивної ГЦ [4, 18].
Досить цікавими є дані про клініко-нейровізуалізаційні порівняння, згідно з якими наявність і тяжкість симптомів депресії залежать від вираженості вогнищевих змін білої речовини лобних часток головного мозку, наявності гідроцефалії та ознак ішемічного пошкодження базальних гангліїв [20].
Не виключено, що і когнітивні розлади, які є першими суб’єктивними та об’єктивними ознаками хронічної цереброваскулярної недостатності, вираженість яких варіює від мінімальних розладів до деменції та визначається цілим рядом до кінця не вивчених чинників, мають чітке морфометричне підгрунтя [18].
Провідну роль у формуванні когнітивних порушень при судинній мозковій недостатності відіграє роз’єднання лобних часток і підкіркових утворень, що призводить до виникнення вторинної дисфункції лобних часток головного мозку. Не виключено, що ГЦ здатна посилювати роз’єднання цих структур, які мають дуже важливе значення в когнітивній діяльності [4].
Численні експериментальні та клініко-інструментальні дослідження останніх років [6, 18] дозволили дещо по-новому розглядати анатомо-функціональну основу когнітивних функцій. Були отримані нові дані про роль підкіркових базальних гангліїв у формуванні вищих мозкових функцій. Зорові горби, смугасті тіла та інші підкіркові структури знаходяться в тісному зв’язку з передніми відділами головного мозку, утворюючи так звані лобно-стріарні кола. Циркуляція збудження за вказаними замкнутими кільцями в нейрональних системах необхідна для створення емоційної переваги вибору одного з декількох можливих у даній ситуації рішень. На сьогодні описано п’ять основних лобно-стріарних кіл, три з яких тісно пов’язані з забезпеченням когнітивної діяльності. Вони мають загальні ланки — лобні частки, смугасті тіла, бліду кулю, чорну субстанцію та таламус. Пошкодження будь-якої ланки може призводити до рухових, когнітивних, емоційних, поведінкових порушень, що дуже близькі за феноменологією до симптомів лобної дисфункції (психічна і рухова сповільненість, зменшення інтелектуальної гнучкості, зниження фону настрою тощо) [19].
Метою нашого дослідження було вивчити стан когнітивної сфери та встановити взаємозв’язок між морфометричними показниками головного мозку та змінами когнітивних функцій у хворих на ГЦ при ХІМ.
Матеріали та методи
Нами було обстежено 72 хворі на ХІМ (чоловіків — 43 (60 %), жінок — 29 (40 %)). Середній вік хворих становив 63,4 ± 9,3 року. Фоновим захворюванням у 60 (83,3 %) пацієнтів була гіпертонічна хвороба, симптоматична артеріальна гіпертензія — у 12 (16,7 %), церебральний атеросклероз — у 47 (65,3 %). ХІМ І ст. була встановлена в 19 (26,4 %), ХІМ ІІ ст. — у 44 (61,1 %), ХІМ ІІІ ст. — у 9 (12,5 %) хворих.
Усі хворі були розподілені на 2 групи. До 1-ї групи увійшло 56 (75 %) хворих із ГЦ при ХІМ, чоловіків серед них було 38 (67,9 %), жінок — 18 (32,1 %), середній вік яких становив 63,00 ± 8,74 року. Залежно від переважної локалізації, внутрішню форму ГЦ було виявлено в 17 (30,4 %) пацієнтів, зовнішню — у 9 (16 %), змішану — у 30 (53,6 %).
До 2-ї групи (групи порівняння) увійшли 16 (32,65 %) пацієнтів із ХІМ без ГЦ, чоловіків серед них було 5 (31,25 %), жінок — 11 (68,75 %), середній вік яких становив 62,56 ± 9,49 року.
Стан когнітивних функцій оцінювали по Монреальській шкалі когнітивних функцій (МоСА-тест). Шкала МоСА, порівняно з іншими нейропсихологічними тестами, є більш чутливою для швидкої діагностики когнітивної дисфункції та дає можливість характеризувати такі параметри когнітивної сфери, як зорово-конструктивні навички, увага та концентрація, пам’ять, мова, абстрактне мислення, рахунок, орієнтація.
Морфометрія мозку виконувалася за даними KТ (апарат Asteion Super-4, Toshiba (Японія)) та МРТ (Siemens Magnetom Avanto 1,5T) і включала в себе такий показник, як ширина субарахноїдальних просторів на рівні полюса лобних часток та сільвієвої борозни; для оцінки шлуночкової системи вимірювали такі характеристики: В — максимальна відстань між бічними шлуночками, C — максимальна відстань між передніми рогами по латеральному краю; D — мінімальний розмір бічних шлуночків; E — максимальний розмір 3-го шлуночка; F — максимальна відстань між задніми рогами бічних шлуночків, Ac — внутрішній розмір черепа на рівні краю передніх рогів бічного шлуночка; Ad — внутрішній розмір черепа на рівні хвостатого ядра; Aa — максимальний внутрішній розмір черепа; A — максимальний зовнішній розмір черепа. Для введення поправки на загальний розмір голови дані оцінювалися у вигляді співвідношень: біфронтальний індекс (БФІ = С/Ас. × 100 %) (маркер кіркової атрофії), бікаудальний індекс (БКІ = D/Аd × 100 %) (маркер підкіркової атрофії), індекс центральної частини бічного шлуночка (ІЦЧБШ = А/D), індекс лобового рога (ІЛР = Ас/С), шлуночковий індекс (ШІ = D/С), індекс фронтальних рогів (ІФР = С/F), число Хакмана (ЧХ = С/D) [15].
Статистичний аналіз проводився на персональному комп’ютері з використанням програми Statistica v. 6.1.
Результати та їх обговорення
За результатами МоСА-тесту, когнітивні порушення різного ступеня вираженості були присутніми у всіх хворих на ХІМ і були вірогідно нижчими порівняно з нормою (p < 0,05) (табл. 1).
Легкі та помірні когнітивні порушення були виявлені в 40 (55,6 %) пацієнтів, виражені — у 32 (44,4 %) обстежуваних.
У пацієнтів із ХІМ за наявності ГЦ (група 1) легкі та помірні когнітивні порушення були встановлені в 24 (42,9 %) пацієнтів, виражені — у 32 (57,1 %) хворих. У групі 2 (без ГЦ) легкі та помірні когнітивні порушення були виявлені в 14 (87,5 %) пацієнтів, виражені — у 2 (12,5 %) хворих.
Середній бал за шкалою МоСА в пацієнтів групи 1 становив 14,91 ± 4,11, що був вірогідно (р < 0,01) нижчим порівняно з групою 2 — 20,64 ± 2,59.
Для більш детального вивчення порушення функціонування когнітивної сфери ми оцінили дані, що були отримані за кожною із підшкал тесту МоСА (табл. 1).
За результатами шкали МоСА в пацієнтів із ХІМ та ГЦ ми зафіксували вірогідне (p < 0,05) зниження показників за наступними категоріями: «зорово-конструктивні навички» (2,15 ± 0,22 проти 3,08 ± 0,19), «увага» (2,46 ± 0,17 проти 4,41 ± 0,23), «абстракція» (0,67 ± 0,11 проти 1,24 ± 0,11) та «орієнтація» (3,31 ± 0,10 проти 5,70 ± 0,10).
Вірогідної різниці між балами за виконання рубрик «назви», «пам’ять», «мовлення» у даних хворих виявлено не було.
Для визначення впливу форми ГЦ на окремі складові когнітивної сфери ми розподілили результати за кожною з категорій шкали МоСА залежно від локалізації ГЦ.
Отримані результати наведено в табл. 2.
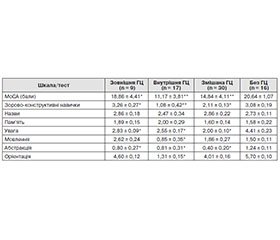
Проаналізувавши отримані дані, ми встановили, що найнижчий середній бал за шкалою МоСА був зафіксований у пацієнтів із внутрішньою ГЦ та становив 11,17 ± 3,81; у хворих із зовнішньою ГЦ — 18,86 ± 4,41, зі змішаною — 14,84 ± 4,11.
Хворі з внутрішньою ГЦ продемонстрували вірогідно (p < 0,05) найгірші результати порівняно з хворими із зовнішньою та змішаною ГЦ згідно з балами, отриманими за рубрикою «зорово-конструктивні навички» (1,08 ± 0,42 проти 3,26 ± 0,27 і 2,11 ± 0,13), «мовлення» (0,85 ± 0,35 проти 2,62 ± 0,24 і 1,86 ± 0,27) та «орієнтація» (1,31 ± 0,15 проти 4,60 ± 0,12 і 4,01 ± 0,16).
Хворі зі змішаною ГЦ продемонстрували вірогідно (p < 0,05) найгірші результати порівняно із хворими з зовнішньою та внутрішньою ГЦ згідно з балами, отриманими за рубрикою «абстракція» (0,40 ± 0,20 проти 0,80 ± 0,27 і 1,31 ± 0,15).
За підшкалами «назви» та «увага» вірогідних особливостей виявлено не було.
Враховуючи, що нами були виявлені деякі особливості стану когнітивних функцій залежно від локалізації ГЦ, ми вирішили дослідити залежність результатів шкали МоСА та морфометричних показників головного мозку за допомогою визначення між ними кореляційних зв’язків.
Так, у пацієнтів із зовнішньою ГЦ при ХІМ був виявлений помірний зворотній кореляційний зв’язок між рівнем пам’яті та БФІ (r = –0,52).
У пацієнтів із внутрішньою ГЦ при ХІМ були виявлені такі кореляційні зв’язки: помірний зворотній — між зорово-конструктивними навичками та ІФР (r = –0,42), помірний зворотній — між балами за підшкалою мовлення та БКІ (r = –0,64), помірний зворотній — між балами за орієнтацію та БКІ (r = –0,48).
У пацієнтів зі змішаною гідроцефалією при ХІМ був виявлений кореляційний зв’язок між балами за орієнтацію та БКІ (r = –0,55), а також між балами за абстракцію та БФІ (r = –0,47) та балами за абстракцію та БКІ (r = –0,55).
Висновки
1. При ГЦ у пацієнтів із ХІМ середній бал за шкалою МоСА становив 14,91 ± 4,11, що був вірогідно (р < 0,01) нижчим порівняно із хворими на ХІМ без ГЦ (20,64 ± 2,59), причому виражені когнітивні порушення, що включають до свого складу і судинну деменцію, вірогідно зустрічалися в 4,6 раза частіше (р < 0,05), ніж в обстежуваних без ГЦ.
2. У групі пацієнтів із ГЦ при ХІМ вірогідно зниженими (р < 0,05) були показники за чотирма рубриками із семи, а саме за «зорово-конструктивними навичками», «увагою», «абстракцією» та «орієнтацією».
3. Установлено, що на вираженість когнітивних розладів має вплив форма ГЦ. У пацієнтів із зовнішньою ГЦ при ХІМ був виявлений помірний зворотній зв’язок (r = –0,52) між маркером кіркової атрофії (БФІ) та рівнем пам’яті; з внутрішньою ГЦ — помірний зворотній між маркерами підкіркової атрофії (БКІ, ІФР) та зорово-конструктивними навичками (r = –0,42), мовленням (r = –0,64), орієнтацією (r = 0,48); зі змішаною ГЦ — помірний зворотній між маркерами підкіркової (БКІ) (r = –0,55) та кіркової атрофії (БФІ), БФІ (r = –0,47) та абстракцією, а також між маркером підкіркової атрофії (БКІ) та орієнтацією (r = –0,55).
4. Наявність ГЦ у пацієнтів із ХІМ поглиблює вираженість когнітивного дефіциту та є предиктором розвитку судинної деменції.
Список литературы
1. Гнездицкий В.В. Когнитивные ВП и доказательная фармакотерапия когнитивных расстройств (начальных проявлений и деменции) / В.В. Гнездицкий, О.С. Корепина, А.В. Чацкая, С.Л. Тимербаева // Материалы XV Международной конференции «Основные направления фармакотерапии в неврологии», 24–26 апреля 2013 г., г. Судак. — Судак, 2013. — С. 197-200.
2. Дамулин И.В. Болезнь Альцгеймера и сосудистая деменция / Под ред. Н.Н. Яхно. — М., 2002.
3. Дамулин И.В. Постинсультная деменция: некоторые диагностические и терапевтические аспекты // Психиатрия и психофармакотерапия. — 2005. — Т. 7, № 1. — С. 1-7.
4. Дамулин И.В., Парфенов В.А., Скоромец А.А., Яхно Н.Н. Болезни нервной системы. Руководство для врачей / Н.Н. Яхно, Д.Р. Штульман (ред.). — М., 2003. — С. 231-302.
5. Дац Ю.В. Вплив форми і вираженості гідроцефалії на клініку, діагностику, перебіг і прогнозування дисциркуляторної енцефалопатії: Автореф. дис… канд. мед. наук. — Х., 2003. — 19 с.
6. Дюба Д.Ш., Евтушенко И.С. Мультимодальный подход в лечении хронической ишемии мозга // Междунар. невролог. журн. — 2012. — № 8(54). — С. 137-140.
7. Евтушенко И.С. Ноотропы и нейропротекторы в современной клинической нейрофармакологии // Международный неврологический журнал. — 2013. — № 3. — С. 20-27.
8. Захаров В.В. Синдром умеренных когнитивных расстройств в пожилом и старческом возрасте: диагностика и лечение / В.В. Захаров, Н.Н. Яхно // РМЖ. — 2004. — № 10. — С. 573-576.
9. Зозуля І.С. Епідеміологія цереброваскулярних захворювань в Україні / І.С. Зозуля, А.І. Зозуля // Укр. мед. часопис. — 2011. — 5(85). — С. 38-41.
10. Маньковский Н.Б. Синдром умеренных когнитивных нарушений (mild cognitive impairment) у лиц старшего возраста / Н.Б. Маньковский, Н.Ю. Бачинская, В.А. Холин, К.Н. Полетаева // Украинский неврологический журнал. — 2006. — № 1. — С. 47-53.
11. Мищенко Т.С. Значимость когнитивных нарушений в клинической практике невролога / Т.С. Мищенко // Журнал клинических нейронаук. Нейрон-ревю. — 2007. — № 4. — C. 2-3.
12. Мищенко Т.С. Новые мишени терапевтического воздействия у пациентов с хронической ишемией головного мозга / Т.С. Мищенко, И.В. Здесенко, А.В. Линская, В.Н. Мищенко // Междунар. невролог. журн. — 2011. — № 2(40). — С. 7-17.
13. Мороз В.А. Дисциркуляторная энцефалопатия: современные подходы к лечению и профилактике / В.А. Мороз // Провизор. — 2008. — № 9. — С. 20-23.
14. Салий З.В. Клинико-морфологические соотношения у больных с последствиями тяжелой черепно-мозговой травмы // Universum: Медицина и фармакология: электрон. научн. журн. — 2014. — № 3(4). — URL: http://7universum.com/ru/med/archive/item/1103
15. Хобзей М.К., Зінченко О.М., Голубчиков М.В., Міщенко Т.С. Стан неврологічної служби України у 2009 році // Неврология. — 2010. — № 339 (тематический номер) / Неврологическая служба Украины.
16. Хомская Е.Д. Нейропсихология. — Питер, 2007. — 496 с.
17. Шмырев В.И., Васильев А.С., Рудас М.С. Дисциркуляторная энцефалопатия — вопросы патогенеза, диагностики, дифференциальной диагностики и лечения на современном этапе //Ліки України. — 2010. — № 9(145). — С. 62-69.
18. Яворская В.А. Подходы к исследованию когнитивных функций при цереброваскулярных заболеваниях и других органических поражениях головного мозга: обзор иностранной литературы / В.А. Яворская, Ю.В. Фломин, А.В. Гребенюк // Междунар. неврол. журн. — 2008. — № 2(18). — С. 131-137.
19. Bech-Azeddine R., Hogh P., Juhler M., Gjerris F., Waldemar G. Idiopathic normal-pressure hydrocephalus: clinical comorbidity correlated with cerebral biopsy findings and outcome of cerebrospinal fluid shunting // J. Neurol. Neurosurg. Psychiatry. — Feb 2007. — 78(2). — 157-61.
20. De Haan E.H. Cognitive function following stroke and vascular cognitive impairment / E.H. De Haan, G.M. Nys, M.J.V. Van Zandvoort // Curr. Opin. Neurol. — 2006. — Vol. 19. — P. 559-564.
21. Launer L.J. Midlife blood pressure and dementia: The Honolulu-Asia aging study / J. Launer, G.W. Ross, H. Petrovich et al. // Neurobiology of Aging. — 2000. — Vol. 21. — P. 49-55.
22. Petersen R.S. Consensus on mild cognitive impairment / R.S. Petersen, J. Touchon // Research and Practice in Alzheimer’s Disease. — 2005. — Vol. 10. — P. 24-32.
23. Petersen R.S. Mild cognitive impairment as a diagnostic entity / R.S. Petersen // J. Intern. Med. — 2004. — Vol. 256. — P. 183-194.
24. Prencipe M., Santini M., Casini A.R. et al. Prevalence of nondementing cognitive disturbances and their association with vascular risk factors in an elderly population // J. Neurol. — 2003. — 250. — 907-912.

/142.jpg)