Международный эндокринологический журнал 6 (70) 2015
Вернуться к номеру
Особенности течения и лечения ишемической болезни сердца у больных с нарушениями метаболизма глюкозы и сахарным диабетом
Авторы: Радченко Е.М., Королюк О.Я. - Львовский национальный медицинский университет им. Данила Галицкого
Рубрики: Эндокринология
Разделы: Клинические исследования
Версия для печати
Поєднання ішемічної хвороби серця та цукрового діабету характеризується особливостями клініки та недостатньою ефективністю лікування ішемічної хвороби серця. Із метою вивчення патогенетичних механізмів та особливостей клінічного перебігу ішемічної хвороби серця за умов порушення гомеостазу глюкози проведене обстеження 116 хворих (медіана віку 63 роки) (нормальна регуляція глюкози (24), порушення глікемії натще (23), порушення толерантності до глюкози (21), комбіноване порушення (24), цукровий діабет (24)) та їх проспективне спостереження впродовж 40 місяців із кінцевими точками — госпіталізація з приводу серцево-судинних ускладнень або смерть від них та виникнення цукрового діабету. Встановлено, що ішемічна хвороба серця за умов предіабетичних порушень та цукрового діабету має особливості: більш рання клінічна маніфестація в жінок, частіша та тяжча серцева недостатність, нижча толерантність до навантаження, атипові прояви ангінозного болю (довший, атиповий або відсутній), супутні порушення ритму та провідності, ураження декількох коронарних артерій, ускладнений перебіг інфаркту, ексцентричний тип ремоделювання лівого шлуночка, кальциноз клапанів серця. Принципи лікування ішемічної хвороби: зниження маси тіла, корекція порушень метаболізму глюкози медикаментами навіть на етапі предіабету, при хронічних формах ішемічної хвороби серця метформін суттєво покращує обмін глюкози, зменшує інсулінорезистентність, не спричиняє зростання частоти серцево-судинних ускладнень та декомпенсацію серцевої недостатності. Вибір препаратів базового лікування ішемічної хвороби серця повинен проводитись з урахуванням їх впливу на метаболізм глюкози, слід уникати засобів, що його погіршують. Повинні використовуватися препарати з чіткими показаннями, оскільки їх взаємодія непередбачувана.
Сочетание ишемической болезни сердца и сахарного диабета характеризуется изменениями клиники и недостаточной эффективностью лечения ишемической болезни сердца. С целью изучения патогенетических механизмов и особенностей клинического течения ишемической болезни сердца при нарушении гомеостаза глюкозы проведено обследование 116 больных (медиана возраста 63 года) (нормальная регуляция глюкозы (24), нарушение гликемии натощак (23), нарушение толерантности к глюкозе (21), комбинированное нарушение (24), сахарный диабет (24)) и их проспективное наблюдение в течение 40 месяцев с конечными точками — госпитализация/смерть по поводу сердечно-сосудистых осложнений и возникновение сахарного дабета. Установлено, что ишемическая болезнь сердца при предиабетических нарушениях и сахарном диабете имеет особенности: более ранняя клиническая манифестация у женщин, более частая и тяжелая сердечная недостаточность, более низкая толерантность к нагрузкам, атипичные проявления ангинозной боли (более длительная, атипичная или отсутствует), сопутствующие нарушения ритма и проводимости, поражение нескольких коронарных артерий, осложненное течение инфаркта, эксцентрический тип ремоделирования левого желудочка, кальциноз клапанов сердца. Принципы лечения ишемической болезни сердца: снижение массы тела, коррекция нарушений метаболизма глюкозы медикаментами даже на этапе предиабета, при хронических формах ишемической болезни сердца метформин значительно улучшает обмен глюкозы, уменьшает инсулинорезистентность, не увеличивает частоту сердечно-сосудистых осложнений и декомпенсации сердечной недостаточности. Выбор препаратов базового лечения ишемической болезни сердца должен проводиться с учетом их влияния на метаболизм глюкозы, не стоит использовать средства, которые его ухудшают. Применяются препараты с четкими показаниями, поскольку взаимодействие непредсказуемо.
Combination of ischemic heart disease and diabetes mellitus is characterized by certain features of clinical picture and insufficient effectiveness of treatment of ischemic heart disease. With the aim of investigation of pathogenic mechanisms and features of the clinical course of ischemic heart disease associated with glucose homeostasis violation we examined 116 patients (51 women, 65 men, median of age 63 years old) with normal regulation of glucose metabolism (NRG, n = 24), changes in fasting glucose (n = 23), violated glucose tolerance (n = 21), combined violation (n = 24) and diabetes mellitus (n = 24). We also conducted their prospective observation for 40 months with the following endpoints — hospitalization because of cardiovascular complications, death from them and the emergence of diabetes. It was established that ischemic heart disease associated with prediabetic disorders and diabetes mellitus has the following peculiarities: earlier clinical manifestation in women; more frequent and severe heart failure; lower tolerance to physical load in patients with angina pectoris; atypical manifestation of ischemic pain: longer attacks, atypical localization or absent pain; frequent combination with arrhythmias and conduction disorders; frequent affection of multiple coronary arteries, which leads to myocardial infarction with complicated course; eccentric type of left ventricle remodeling; significant calcification of mitral and aortic valves of heart.
The main principles of treatment of ischemic heart disease: weight loss; active correction of glucose metabolism violations using medications (metformin) even at the stage of prediabetes, because in chronic stable forms of ischemic heart disease metformin significantly improves glucose metabolism, decreases insulin resistance and does not increase the incidence of cardiovascular complications and decompensations of heart failure; the basic drugs for treatment of ischemic heart disease should be chosen taking into account their impact on glucose metabolism with avoidance of drugs and treatment schemes, which lead to its impairment; usage of well-targeted drugs with clear indications as there is a lasting need for large number of drugs with unpredictable interactions.
ішемічна хвороба серця, цукровий діабет, порушення глікемії натще, порушення толерантності до глюкози, комбіноване порушення, особливості перебігу, принципи лікування.
ишемическая болезнь сердца, сахарный диабет, нарушение гликемии натощак, нарушение толерантности к глюкозе, комбинированное нарушение, особенности течения, принципы лечения.
ischemic heart disease, diabetes mellitus, changes in fasting glucose, violated glucose tolerance, combined violation, course peculiarities, principles of treatment.
Статтю опубліковано на с. 11-16
Дані про патогенетичний зв’язок цукрового діабету (ЦД) з атеросклерозом з’явилися майже відразу після відкриття інсуліну в 1922 році. Зараз уже ніхто не має сумнівів щодо тісного зв’язку порушень ліпідного та вуглеводного метаболізму, що було підтверджено даними доказової медицини. Більше того, результати дослідження DECODE (Diabetes Epidemiology: Collaborative Analysis of Diagnostic Criteria in Europe, 2003) довели, що серцево-судинний ризик та глікемія лінійно пов’язані між собою уже з нормальних рівнів глюкози. При цьому з ризиком корелює як показник глікемії натще, так і постпрандіальної [12]. На сьогодні відомі 5 механізмів атерогенезу за умов ЦД: метаболічний (гіперглікемія, глікування, вільні жирні кислоти, інсулінорезистентність, діабетична гіперліпідемія), окисний стрес, ендотеліальна дисфункція (порушення синтезу та біодоступності оксиду азоту), запалення (надлишок цитокінів та розчинних ліпопротеїновмісних імунних комплексів), тромбоз (підвищення фібриногену, надлишок інгібітору активатора плазміногену 1), однак у кожному випадку їх роль може різнитись, що створює додаткові труднощі для діагностики та лікування.
Результати і обговорення
/14.jpg)
Висновки
1. Королюк О.Я., Радченко О.М. Уперше виявлена гіперглікемія у хворих на ішемічну хворобу серця з точки зору кардіолога // Міжнародний ендокринологічний журнал. — 2011. — № 7. — С. 95-102.
2. Королюк О.Я., Радченко О.М., Горбач Л.О., Горбач М.О. Особливості діагностики вперше виявленої гіперглікемії у хворих на ішемічну хворобу серця // Кровообіг та гемостаз. — 2011. — № 3–4. — С. 23-28.
3. Радченко О.М., Королюк О.Я. Бета-адреноблокатори: вплив на вуглеводний метаболізм // Рациональная фармакотерапия. — 2013. — № 3. — С. 40-44.
4. Радченко О.М., Королюк О.Я. Застосування діуретиків за умов порушеного вуглеводного метаболізму // Рациональная фармакотерапия. — 2013. — № 2. — С. 14-17.
5. Сахарный диабет и ишемическая болезнь сердца: поиски решения / Александров А.А., Бондаренко И.З., Кухаренко С.С. [и др.] // Електр. ресурс. Режим доступу: http://cyberleninka.ru/article/n/saharnyy-diabet-i-ishemicheskaya-bolezn-serdtsa-poiski-resheniya
6. Andreotti F., Marchese N. Women and coronary disease // Heart. — 2008. — Vol. 94. — P. 108-116.
7. Association between plasma LDL particle size, valvular accumulation of oxidized LDL, and inflammation in patients with aortic stenosis / D. Mohty, P. Pibarot, J.-P. Després [et al.] // Arterioscler. Thromb. Vasc. Biol. — 2008. — Vol. 28. — P. 187-193
8. Atypical chest pain in the elderly: prevalence, possible mechanisms and prognosis / C.-L. Hung, C.J.-Y. Hou, H.-I. Yeh, W.-H. Chang // International Journal of Gerontology. — 2010. — Vol. 4. — P. 1-8.
9. Effects of 1-year treatment with metformin on metabolic and cardiovascular risk factors in non-diabetic upper-body obese subjects with mild glucose anomalies: A post-hoc analysis of the BIGPRO1 trial / A. Fontbonne, I. Diouf, M. Baccara-Dinet [et al.] // Diabetes and Metabolism. — 2009. — Vol. 35. — P. 385-391.
10. Impaired Fasting Glucose and Impaired Glucose Tolerance: Implications for care / D.M. Nathan, M.B. Davidson, R.A. DeFronzo [et al.] // Diabetes Care. — 2007. — Vol. 30. — P. 753-759.
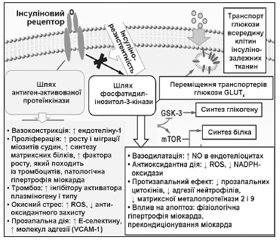
11. Insulin signaling in the heart / L. Bertrand, S. Horman, C. Beauloye, J.L. Vanoverschelde // Cardiovasc. Res. — 2008. — Vol. 79. — P. 238-248.
12. Is the current definition for diabetes relevant to mortality risk from all causes and cardiovascular and noncardiovascular diseases? / The DECODE Study Group, European Diabetes Epidemiology Group // Diabetes Care. — 2003. — Vol. 26. — P. 688-696.
13. Maddalone S.T.M. Metformin use in patients with diabetes and heart failure: cause for concern? // Diabetes Spectrum. — 2009. — Vol. 22. — P. 18-20.
14. The prevalence of abnormal glucose regulation in patients with coronary artery disease across Europe. The Euro Heart Survey on diabetes and the heart / M. Bartnik, L. Rydén, R. Ferrari [et al.] // Eur. Heart J. — 2004. — Vol. 25. — P. 1880-1890.
15. What is a normal glucose value? Differences in indexes of plasma glucose homeostasis in subjects with normal fasting glucose / M.V. Piche, J.-F. Arcand-Bosse, J.-P. Despres [et al.] // Diabetes Care. — 2004. — Vol. 27. — P. 2470-2477.

/13.jpg)