Статтю опубліковано на с. 72-80
Травматизм є епідемією сьогодення. Від травм у світі щороку гине понад 5 млн людей, що становить 9 % глобальної смертності [12, 13]. Збільшення травматизму обумовлено не лише урбанізацією та зростанням кількості транспорту, але й соціально-економічними умовами [1, 9, 17, 23, 25]. За даними Всесвітньої організації охорони здоров’я (ВООЗ), травматизм та насилля в Європі є основними факторами насильницької смерті [9]. Дорожньо-транспортні травми в країнах із низьким та середнім рівнем доходів в 1,5 раза бувають частіше, ніж у країнах із високим рівнем доходів [9, 10, 11, 26]. За всіма показниками Україна належить до країн із низьким рівнем доходів — передостаннє місце в Європейському регіоні. Підтвердженням цього є кількість померлих від травм на 100 тис. населення: у США — 56, Англії — 50–56, Польщі — 75, Угорщині — 115, Україні — 132 [11, 14, 16]. Щодня в Європейському регіоні через травми гине понад 2000 осіб, 60 тис. потрапляють у лікарні та 600 тис. звертаються по амбулаторну допомогу. Травми є основною причиною смерті серед людей віком до 45 років [9, 10]. Середня вартість надання медико-санітарної допомоги в Європі становить 1250–7250 євро на одну смертельну травму і 4800–12000 євро на одну несмертельну травму, відповідно від 1 до 6 млрд євро витрачається щорічно на смертельні травми і від 80 до 290 млрд євро на лікування несмертельних травм [20]. Використовуючи досвід країн Європи з найменшою кількістю травм, можна було б –запобігти 68 % травм, тобто щорічно врятовувати до 500 тис. життів [9, 20]. В Європейському регіоні у 2002 р. травми спричинили смерть близько 800 тис. людей (8,3 % усіх смертей). Причому одна третина смертей від травм припадає на вік 30–44 роки. Від травм чоловіки помирають у трьох випадках із чотирьох [5, 12]. Від різних видів травм в Україні щороку гине 60–70 тис. людей [2]. Згідно з даними Держкомстату України щодо населення на 1 січня 2009 р., співвідношення жінок і чоловіків віком від 30 до 60 років становило 1,47 : 1, тобто на 147 жінок припадало 100 чоловіків, тоді як віком до 30 років більшість становили чоловіки [2]. Причинами такого зменшення частки чоловіків після 30 років в основному є зовнішні фактори, у тому числі травми. Найбільш тяжкі ушкодження виникають при дорожньо-транспортних пригодах (ДТП). Щороку в Україні фіксується понад 200 тис. ДТП, в яких гинуть понад 7 тис. осіб та 40 тис. отримують травми різної тяжкості [8]. За даними Всесвітнього банку, економічні витрати в Україні внаслідок ДТП оцінюються у сумі понад 5 млрд дол. США щорічно [20]. Дорожньо-транспортні травми в країнах із низьким та середнім рівнем доходів в 1,5 раза бувають частіше, ніж у країнах із високим рівнем доходів, отруєння — у 18 разів частіше, падіння — у 8 разів, утоплення — у 9 разів, насильницька смерть від пожеж — у 8 разів, як результат членоушкоджень та самовбивств — у 2,5 раза, від міжособистих злочинів — у 14 разів, від алкоголю — 40–70 % випадків різних ушкоджень (до 75 % — чоловіки). Основними причинами смерті в Європейському регіоні від травми є членоушкодження (21 %), отруєння (14 %) та дорожньо-транспортні травми (ДТТ) — 16 %. Згідно з даними ВООЗ, віз ДТТ щороку гине понад 127 тис. людей, причому 55 % — віком 15–44 років. Окрім цього ще 2,4 млн людей отримують травми, у 75 % усіх випадків це особи чоловічої статі. Ризик смерті від травми серед чоловіків у країнах Співдружності Незалежних Держав у чотири рази вищий, ніж у країнах Європейського Союзу. Вивчаючи дані про травматизм у Європі, країнах із найменшою кількістю травм, можна запобігти 68 % травм, тобто щорічно рятувати 500 тис. життів.
Чоловіки помирають у трьох випадках із чотирьох. Від різних видів травм в Україні щорічно гине 60–70 тис. людей.
Епідеміологічне вивчення черепно-мозкової травми (ЧМТ) свідчить про її значну поширеність [5]. Зменшення кількості померлих та постраждалих при травмах має важливе соціально-економічне значення і сприятиме покращенню демографічних показників [9–11].
ЧМТ є одним з найбільш складних і невирішених завдань травматології, має надзвичайно важливе соціальне значення через свою поширеність, тяжкість медичних та економічних наслідків [10].
Виділяють такі форми ЧМТ:
— струс головного мозку (ГМ);
— забій ГМ (легкого, середнього та тяжкого ступенів тяжкості);
— дифузне аксональне ушкодження мозку (ДАУ);
— стиснення ГМ.
Ушкодження мозку та його тяжкість залежать як від сили удару, так і від біомеханіки травми.
Імпресійний локальний вид викликає ушкодження на місці травми, де нерідко виникають переломи та локальні забої ГМ.
Ударно-протиударний механізм (перепад тиску на місці удару та з протилежної сторони) призводить до тяжких ушкоджень мозку як на місці травми, так і за типом протиудару на протилежній стороні.
Прискорено-загальмований механізм (зміщення та ротація півкуль мозку щодо фіксованої основи та стовбура мозку) — травматичні ушкодження виникають у різних структурах ГМ, нерідко виникає ДАУ.
Поєднані ушкодження (одночасна дія всіх факторів) — найбільш тяжкий механізм травми.
За типом ушкодження мозку розподіляються на вогнищеві та дифузні. Вогнищеві ушкодження характерні для локального імпресійного механізму травми, а також для ударно-протиударного. Вони характеризуються локальними макроструктурними ушкодженнями мозкової речовини різного ступеня (геморагії, детрити, крововиливи) на місці удару, на протилежній стороні по ходу ударної хвилі. Дифузні ушкодження в основному виникають внаслідок травми прискорення-загальмування і характеризуються розривами, натяжінням аксонів, дрібними крововиливами в підкірку, мозолисте тіло. Коли вогнищеві ушкодження поєднуються з дифузними, констатують поєднані ушкодження.
Струс головного мозку (СГМ) — найбільш легка та часта форма травматичного ушкодження мозку — 70–80 % всіх ЧМТ. Стан свідомості за шкалою коми Глазго (ШКГ) 14–15 балів. Морфологічні зміни виявляються лише на клітинному та субклітинному рівнях. Вважається, що це єдино функціонально оборотна форма травми ГМ, що характеризується короткочасним виключенням (втратою) свідомості — від декількох секунд до 2–3 хвилин. Можуть бути випадіння пам’яті на короткий проміжок часу, конградна ретроантероградна амнезія, нерідко буває нудота, разова блювота, характерними є скарги на головний біль, головокружіння, слабкість, шум у вухах, вегетативні розлади, болі при рухах очей, вестибулярна гіперестезія тощо. СГМ — найбільш складна форма для діагностики та експертизи.
При струсі ГМ страждають усі відділи центральної нервової системи (ЦНС); кора, підкірка, гіпоталамічна зона, рідко стовбурові відділи. Зразу після травми мозку в перші 2–3 дні СГМ визначається стійка робота вегетативних регуляторних центрів та серцево-судинної системи, що працюють у цей час у режимі автономного контура.
Об’єктивними ознаками СГМ є дрібнорозмашистий ністагм, порушення конвергенції, негруба асиметрія рефлексів, симптом Маринеску — Радовічі, що минають протягом 3–7 діб. Хворий із СГМ не може читати: біль в очах, головний біль підсилюються, букви розпливаються. Якщо хворий читає, дивиться телевізор, користується Інтернетом — СГМ немає. За КТ, МРТ, ЕЕГ характерних СГМ-ознак не виявляють. Окорухові порушення: нестійкий дрібнорозмашистий ністагм, що з’являється зразу після травми або на 2–4-й день після неї, утримується від 2 до 8 днів. Незначний швидкоминучий парез погляду наверх та врізнобіч, підсилення при цьому головного болю (симптом Гуревича — Манна). Порушення конвергенції, що проявляється неможливістю читати дрібний текст (синдром Седана). Це пояснюється тим, що конвергенція — філогенетично молодий асоціативний рух очних яблук. Навіть незначне порушення в системі заднього поздовжнього пучка призводить до появи окорухових дисоціацій. Ці порушення можуть бути швидкоминучими, а можуть утримуватися і протягом 6–8 днів. Свідченням слабкості заднього поздовжнього пучка може бути симптом Парино (парез погляду вгору з одночасним розходженням очних яблук). Цей симптом, як і млявість зіничних реакцій, може минути через декількох годин після травми.
У хворих із СГМ бувають слабо виражені менінгеальні симптоми (світлобоязнь, симптом Керніга, ригідність потиличних м’язів), лабільна, негруба асиметрія сухожилкових та періостальних рефлексів, слабопозитивні розгинальні рефлекси, незначна м’язова слабкість.
Надзвичайно важливе значення при легкій ЧМТ мають субкортикальні рефлекси, а саме симптом Маринеску — Радовічі. Цей симптом — найбільш часта ознака СГМ в осіб молодого віку (90 %). Важливість цього симптому зростає, якщо брати до уваги бідність та непостійність інших проявів при СГМ. Динаміка долонно-підборідного рефлексу при СГМ: не з’являється зразу після травми; слабопозитивний через 6–8 годин; найбільш часто з’являється через 7–18 годин. Рефлекс чітко виражений на 3–5-й день після СГМ, може бути асиметричним, викликатися з розширених рефлексогенних зон. Часто сторона його викликання відповідає місцю прикладення травмуючої сили. Двосторонній симптом характерний для травми в потиличну ділянку голови, лобну по середній лінії та при множинних ударах по голові.
Лікування хворих із СГМ симптоматичне. Строк ліжкового режиму — 5–7 днів.
Забій головного мозку (ЗГМ) буває у 20–30 % усіх хворих із ЧМТ. ЗГМ має 3 ступені тяжкості: легкий, середньотяжкий і тяжкий, залежно від тривалості втрати свідомості, рівня її порушення на момент госпіталізації, наявності неврологічної симптоматики, даних комп’ютерної томографії.
Патоморфологічною основою ЗГМ є сукупність тканинних порушень різного ступеня та характеру з первинними крововиливами, тобто контузійні вогнища та геморагії в корі та білій речовині. Контузійні вогнища — це зони травматичного некрозу, що виникають внаслідок удару великих півкуль у кісткові виступи, за типом удару та протиудару, прискорення, ротації мозку, по ходу ударної хвилі з супутніми дисгемічними, дисциркуляторними та дистрофічними порушеннями. Клінічні прояви ЗГМ характеризуються складним поєднанням функціональних перехідних та стійких неврологічних проявів, обумовлених судинними, лікворо-, нейродинамічними порушеннями внаслідок травматичних ушкоджень мозку та супутніх внутрішньочерепних крововиливів. Суттєвий вплив на перебіг забоїв мозку мають анатомо-фізіологічні вікові особливості організму.
ЗГМ легкого ступеня характеризується короткочасним виключенням (втратою або порушенням) свідомості. Втрата або порушення свідомості після травми можуть бути короткочасними. Як правило, не більше як на 5–10 хвилини. Свідомість порушена за типом приглушення — 13–14 балів за ШКГ.
Стан хворих відразу після травми можна характеризувати як відносно задовільний, середньої тяжкості: частіше за все спостерігається помірне приглушення, рідше — виражене приглушення. Хворі можуть бути дезорієнтовані в місці та часі, збуджені, сонливі, швидко виснажуються. Через 1–3 години свідомість, як правило, ясна, хворі орієнтуються, проте частіше, ніж при СГМ, спостерігаються амнестичні порушення (40–50 % спостережень) у вигляді конградної, ретро- та антероградної амнезії. Блювота, нудота часті, деколи повторні. Життєво важливі функції не порушені. Можуть бути помірні бради- або тахікардія, деколи артеріальна гіпертензія. Дихання, а також температурна реакція без суттєвих змін, незначний субфебрилітет. Для ЗГМ легкого ступеня характерними є скарги на біль голови, частіше — в скронево-лобній ділянці або дифузний, головокружіння, вегетативні порушення за типом симпато- чи ваготонії, підвищена метеочутливість. Як загальномозкова реакція спостерігається менінгеальний синдром: світлобоязнь, ригідність потиличних м’язів, симптом Керніга.
Неврологічні прояви ЗГМ зазвичай м’які (ністагм, легка анізокорія, симптоми Седана, Гуревича — Манна, Маринеску — Родовічі, ротовий феномен Бехтерева — Фуа, анізорефлексія, слабка пірамідна недостатність, чутливі порушення). Можливі переломи кісток черепа, субарахноїдальні крововиливи. Ліквор може бути прозорим або зі слідами крові.
При ЗГМ легкого ступеня неврологічна симптоматика регресує протягом 2–3 тижнів. Хворий непраце-здатний упродовж 4–6 тижнів за умов, що перебіг травми неускладнений.
ЗГМ середнього ступеня тяжкості характеризується тривалою втратою свідомості — декілька десятків хвилин, декілька годин. Порушення свідомості за типом вираженого приглушення, сопору (9–12 балів за ШКГ). Коматозне порушення свідомості не буває частим і тривалим. Часто спостерігається психомоторне збудження. Тривало виражена ретро-, кон-, антероградна амнезія. Можуть бути головний біль, блювота, нерідко багаторазова, минущі розлади життєво важливих функцій: брадикардія, тахікардія, підвищення артеріального тиску, тахіпное без порушення ритму дихання та прохідності трахеобронхіального дерева, субфебрилітет. Як правило, у хворих виявляється менінгеальний синдром, чітка неврологічна симптоматика у вигляді окорухових порушень (ністагм не виражений, парези VI, III пар черепно-мозкових нервів), парез лицьового нерва центрального або периферійного типу. Часто спостерігається пірамідна недостатність у вигляді гемі-, монопарезів, розладів чутливості, можуть бути мовні розлади (моторна, амнестична, сенсорна афазія). Вогнищева симптоматика визначається локалізацією забоїв мозку. У хворих можуть бути стовбурові симптоми у вигляді ністагму, парезів зору, змін м’язового тонусу та сухожилкових рефлексів по осі тулуба. Вогнищеві симптоми ушкодження нервової системи поступово (протягом 3–5 тижнів) згладжуються, але можуть утримуватися і більше, деколи залишаються. При забоях середнього ступеня, як правило, виявляється кров у спинномозковій рідині. Часто бувають переломи кісток черепа. Хворі надходять у клініку в стані середньої тяжкості або у тяжкому стані.
ЗГМ тяжкого ступеня характеризується тривалою втратою свідомості — декілька годин, діб, тижнів, можливо до смертельного наслідку. У хворих грубі розлади свідомості за типом вираженого психомоторного збудження, сопору, коми (3–8, рідше — 9 балів за ШКГ). Часто спостерігаються вітальні порушення: брадикардія, тахікардія, артеріальна гіпер- або гіпотензія, порушення частоти ритму дихання, може бути порушення прохідності дихальних шляхів, підвищення температури тулуба. Наявний менінгеальний синдром. Виражена –субарахноїдальна геморагія. Грубі неврологічні симптоми вогнищевого та загальномозкового характеру: стовбурові, ушкодження півкуль ГМ, мозочку: плаваючі очні яблука, анізокорія, парези III–VI пар черепно-мозкових нервів, парез VII нерва центральний або периферійний, судоми загальні або вогнищеві, децеребраційна ригідність, зміна тонусу м’язів кінцівок, порушення чутливості, патологічні стопні симптоми. Загальномозкові симптоми в ранні строки переважають над вогнищевими. Неврологічна симптоматика регресує, як правило, повільно, часто залишається виражена загальномозкова та вогнищева симптоматика. При забоях тяжкого ступеня часто бувають переломи склепіння та основи черепа.
При ЗГМ часто бувають переломи кісток черепа, субарахноїдальні, внутрішньомозкові крововиливи, частота яких корелює з тяжкістю травми, часто спостерігається набряк мозку, як локальний, так і генералізований. При забоях ГМ геморагічне ушкодження часто прогресує протягом кількох годин після травми, крім того можливе виникнення нових вогнищ, віддалених від місця первинного ушкодження, тобто вторинна геморагічна прогресія забою (ВГПЗ). Місця первинної контузії внаслідок ВГПЗ та набряку створюють мас-ефект, що зумовлює компресію сусідніх тканин і без належної корекції викликають подальшу ішемію, підвищення внутрішньочерепного тиску (ВЧТ), що може спричинити вклинення і необхідність подальшої хірургічної декомпресії для уникнення смерті хворого.
Особливості забоїв у дітей характеризуються вираженою загальномозковою симптоматикою, вегетативними реакціями гіперергічного характеру. Залежно від локалізації та поширеності забою вони проявляються по-різному: тяжкі забої півкуль із вираженими вогнищевими неврологічними порушеннями, вітальні порушення; тяжкі забої мозку з переважними первинно стовбуровими порушеннями, вітальними розладами та змішані форми забоїв.
В осіб похилого та старечого віку тяжкі забої призводять до раннього прояву вітальних розладів та, як правило, закінчуються летально, оскільки супутні гемодинамічні кардіоцеребральні порушення швидко декомпенсуються, незважаючи на лікування.
Дифузне аксональне ушкодження характерне для травми прискорення, ротації з ударно-протиударним механізмом характеризується наявністю дрібних крововиливів у мозолисте тіло, білу речовину мозку, дорсолатеральні відділи стовбура, відповідно до ушкоджень і симптоматики. Частіше виникає у дітей та осіб молодого віку. ДАУ мозку характеризується тривалою, багатодобовою втратою свідомості за типом коми. Втрата свідомості настає відразу після травми. У постраждалих наявні стовбурові симптоми: парез рефлекторного погляду вгору, різне положення очних яблук по вертикалі, пригнічення фотореакції зіниць, порушення або відсутність окулоцефалічного рефлексу, порушення частоти та ритму дихання, типові позотонічні реакції (кома супроводжується децеребрацією або декортикацією, що настають спонтанно або при мінімальних подразненнях). Зміни тонусу м’язів надзвичайно варіабельні переважно у вигляді горметонії або дифузної гіпотонії. Часто виявляються пірамідно-екстрапірамідні парези кінцівок, характерні асиметричні тетрапарези. Виражені вегетативні розлади: артеріальна гіпертензія, гіпертермія, гіпергідроз, гіперсалівація тощо.
Характерною особливістю ДАУ є перехід із тривалої коми в стійкий або транзиторний вегетативний стан, про настання якого свідчить розплющення очей у відповідь на різні подразники. Ознаки слідкування, фіксації погляду відсутні навіть на елементарні інструкції. Вегетативний стан при ДАУ тягнеться від декількох діб до декількох місяців. ДАУ характеризується симптомами функціонального або анатомічного роз’єднання великих півкуль та стовбура мозку. Грубі ознаки ушкодження кори частіше за все відсутні. Поряд із цим визначається розгальмування підкіркових, орально-стовбурових, каудально-стовбурових та спінальних рефлексів. Ці структури функціонують хаотично, автоматизовано, що може проявлятися різними симптомами та рефлексами, що не постійні, часто мінливі. Сегментарні стовбурові рефлекси активізуються на всіх рівнях, тоді як координаційна діяльність кори відсутня. Цим пояснюється така різноманітність та мозаїчність клініки ДАУ: відновлення живої реакції зіниць на світло, наявність та зникнення анізокорії, звуження зіниць змінюється значним розширенням, повільно змінюються плаваючі очні яблука, дивергенція очних яблук по горизонтальній або вертикальній осі, спазми зору (частіше донизу). Больові реакції призводять до тонічного зведення очей та появи великорозмашистого ністагму. У хворих часто бувають тризм, лицеві синкінезії (жування, смоктання, прицмокування, скрегіт зубами, позіхання, ковтальні автоматизми). При відсутності фіксації зору деколи появляється міміка болю, плачу.
На фоні пірамідно-екстрапірамідного синдрому з двосторонньою зміною м’язового тонусу та сухожилкових рефлексів у відповідь на різні подразники, в тому числі на зміну положення тулуба, може з’явитися багато позотонічних та некоординованих захисних реакцій у вигляді згинальних тонічних спазмів у кінцівках, поворотів корпуса, голови, пароксизмальні напруження м’язів живота, великоамплітудні рухи та складні, вигадливі положення рук, рухові стереотипи, тремор кистей рук та інше. Перерахувати симптоми, що можуть з’являтися в різні періоди ДАУ, надзвичайно складно. Проте можна прослідкувати на всіх етапах слабкість функцій структур мозку: в гострому та ранньому періоді слабкість стовбура мозку та підкіркових структур, що маскують усі інші прояви. В подальшому при сприятливому перебігу захворювання з’являються стабільність стовбурових функцій і виражена слабкість підкірки та кори мозку. Коркова слабкість залишається найбільш тривалою та стійкою. Тобто відновлення функцій різних структур мозку настає в їх філогенетичній послідовності: спочатку відновлюються більш древні, важливі для життя відділи мозку, потім більш диференційовані, філогенетично молоді відділи — підкірка, а потім кора ГМ.
Наявність грубих вогнищевих симптомів та ознак ДАУ слід розцінювати як сукупність вогнищевого та дифузного аксонального ушкоджень мозку.
Після виходу з вегетативного стану домінує екстрапірамідний синдром із вираженою скутістю, дискоординацією, брадикінезією, олігофазією, гіпомімією, атаксіями тощо. Спостерігаються порушення психіки, афективні розлади.
Стиснення ГМ спостерігається в 3–5 % постраждалих із ЧМТ, що взагалі становить 10–15 % усіх хворих нейрохірургічних стаціонарів. У таких пацієнтів наявні епідуральні, субдуральні гематоми, внутрішньомозкові та внутрішлуночкові крововиливи, а також втиснені переломи склепіння черепа, як правило, із компресією ГМ. Більшість із них вимагає ургентного хірургічного втручання, що повинно проводитися не пізніше 3 годин із моменту госпіталізації пацієнта до лікарні або встановлення діагнозу.
У клініці ЧМТ виділяють три періоди: гострий — взаємодія реакції ушкодження та реакції захисту — 2–10 тижнів залежно від тяжкості травматичного ушкодження мозку, проміжний — розсмоктування, організація ділянок ушкоджень, подальше включення компенсаторно-пристосувальних процесів — 2–6 місяців, віддалені — завершення або співіснування місцевих та дистанційно-деструктивно-дегенеративних та регенеративно-репаративних процесів — до 2 років при прогредієнтному перебігу або необмежено — при ремітуючому перебігу.
Чітке розуміння процесів, що відбуваються на всіх етапах під час та після ЧМТ, допомагає покращити результати лікування хворих і зменшити витрати на їх утримання. Для визначення обсягу діагностичного дослідження загальноприйнятним є оцінка ризику виникнення внутрішньочерепних ускладнень (РВВУ) [7].
Клінічні симптоми низького РВВУ: забої і садна м’яких тканин голови, головний біль, запаморочення. У хворих цієї групи дані рентгенографії негативні, КТ проводити недоцільно. Необхідність її проведення може виникнути при зниженні рівня свідомості хворого, появі неврологічних симптомів, а також необхідності вирішення правових питань.
Клінічні симптоми середнього РВВУ: втрата свідомості або зниження її рівня, пов’язане з травмою голови, прогресуючий головний біль, алкогольна або інша інтоксикація, післятравматичні епіприступи, відсутність або недостатня інформація про наявність травми, вік до 2 років, блювання, післятравматична амнезія, ознаки перелому основи черепа, множинна травма, тяжка травма лицьового черепа, припущення про побиття дитини батьками.
Клінічні симптоми високого РВВУ: зниження рівня свідомості — 3–8 балів за ШКГ, не пов’язане з уживанням алкоголю, лікарських засобів, метаболітів, епіприступами; вогнищевий неврологічний дефіцит, негативна динаміка порушення свідомості за ШКГ, проникаюча ЧМТ або втиснений перелом.
За середнього та високого РВВУ потрібні такі дії.
1. Госпіталізація хворого у нейрохірургічне відділення для спостереження в динаміці за клінічним станом з метою запобігання внутрішньочерепним ускладненням (клінічно проявляються погіршенням неврологічного стану). Навіть якщо дані візуального обстеження нормальні, медикаментозне лікування тільки симптоматичне: при головному болі — аналгетики; при нудоті та блюванні — антиміметики.
2. Профілактичне призначення антиконвульсантів.
3. Контроль неврологічного стану та рівня свідомості за ШКГ через кожні півгодини.
4. Повторне КТ-сканування, якщо погіршився неврологічний стан, а за стабільного стану — через 3 доби.
5. Контроль ВЧТ та інші заходи за протоколом ЧМТ: ступеня тяжкості або якщо стан хворого погіршився (менше 8 балів за ШКГ).
6. Хірургічне лікування за показаннями.
7. Контрольне обстеження хворого після виписки — через 2 тижні, 3, 6 і 12 місяців після травми.
Ушкодження ГМ поділяють на первинні та вторинні. До первинних належать: механічні та судинні фактори, до вторинних — гіпоксемія, гіпотонія, гіпертермія, гіпер- і гіпоглікемія, гіпер- і гіпокапнія. Необхідно пам’ятати про особливості доктрини профілактики вторинного ушкодження мозку — анатомічні фактори. Череп являє собою щільний кістковий контейнер, в якому переважно містяться речовини, що не стискаються. Отже, при появі гематоми чи набряку відбувається зміщення речовини мозку та защемлення в природних отворах (доктрина Монро — Келлі) (Monro A., 1783; Kellie G., 1824).
Зменшенню летальності при тяжкій ЧМТ сприяли такі фактори:
1. Створення відділень інтенсивної терапії зі штучною вентиляцією легень та комплексним підходом різних фахівців до надання допомоги — кінець 50-х років ХХ століття.
2. Уніфікація оцінки та підходів до надання допомоги — 70-ті роки ХХ століття.
3. Впровадження КТ — середина 70-х років ХХ століття, відмова від АГ, ПЕГ, пошукових фрезових отворів та поява наприкінці 80-х років ХХ століття.
4. Концепція вторинних ішемічних розладів, що змінили уяву про визначення ролі первинного травматичного ушкодження та кардинально покращили результати лікування ЧМТ.
Основні принципи ведення пацієнтів із ЧМТ полягають у підтримці оптимального церебрального перфузійного тистку (ЦПТ), лікуванні внутрішньочерепної гіпертензії, запобіганні вторинній ішемії мозку, метаболічному захисті мозку, поповненні енергетичних субстратів мозку, регенерації і відновленні міжнейронних зв’язків, прекондиціонуванні. Внутрішньочерепна гіпертензія виникає в 50 % коматозних пацієнтів із патологією на КТ та 10–15 % пацієнтів із нормальною КТ ГМ. Усі пацієнти із рівнем свідомості нижче від 8 балів потребують моніторингу ВЧТ. Допустимі межі ВЧТ — менше 20 мм рт.ст., середній АТ — більше 90 мм рт.ст. (нормальні показники ВЧТ — 5–15 мм рт.ст.). Достатнім слід вважати ВЧТ, що забезпечує ЦПТ не менше ніж 70 мм рт.ст.
Маючи на увазі те, що ЦПТ = середній артеріальний тиск (СрАТ) – ВЧТ, важається, що ЦПТ нижчий за 70 мм рт.ст. є фактором, що провокує виникнення ішемії ней-ронів і вторинної церебральної гіпоксії. Оптимальний рівень ЦПТ (вище від 80 мм рт.ст.) досягається підвищенням СрАТ і зниженням ВЧТ відповідно до рекомендацій лікування хворих у нейрохірургічних стаціонарах. СрАТ = діастолічний тиск + 1/3 пульсового тиску. Отже, при АТ 120/80 мм рт.ст. СрАТ = 93 мм рт.ст.
У лікуванні хворих із ЧМТ необхідно дотримуватися правила трьох «Г» (гіпертензія, гіперволемія, близька до нормоволемії, гемодилюція). Першим і найбільш важливим є забезпечення оксигенації мозку, усунення гіпоксії та гіповолемії.
Нормальна перфузія мозкової тканини у людей становить близько 54 мл на 100 г тканини за хвилину. У випадках зниження церебрального кровотоку до 10 мл/100 г/хв і нижче через 5 хв розвивається стійка аноксична деполяризація клітинної мембрани нейронів внаслідок енергетичного голоду і нездатності підтримувати свій внутрішньоклітинний, іонний гомеостаз (на це використовується до 50 % внутрішньоклітинного АТФ). У цей період ушкоджені нейрони звільняють велику кількість збуджуючого нейромедіатора — глутамінової кислоти, що активує NMDA-рецептори мембрани сусідніх нейронів із запуском патологічного глутаматного каскаду, що призводить до загибелі нейронів. У цих випадках використання магнію блокує NMDA-рецептори і глутаматний збуджуючий каскад та зупиняє вторинне ушкодження ГМ.
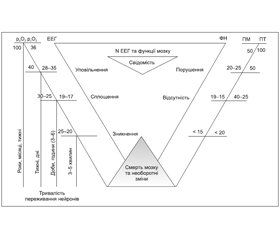
Нижче наводимо трикутник функціонування життя та смерті мозку (рис. 1).
Перфузійний тиск мозку (ПТМ) — один з основних визначальних показників наслідків ЧМТ. ПТМ залежить від середнього артеріального тиску і ВЧТ. Без моніторингу ВЧТ визначити ПТМ неможливо. Зміни SiVo2 випереджають зміни показників ПТМ. Отже, моніторинг ВЧТ та визначення ПТМ і SiVo2 є обов’язковим при лікуванні хворих із тяжкою ЧМТ.
Деякий метаболічний захист мозку забезпечують анестетики, серед яких тіопентал натрію, ізофлюран і його аналоги, пропофол, етомідат натрію, що знижують перфузію мозкової тканини та потребу мозку в кисні, проте мають побічні ефекти, які потрібно враховувати в кожному випадку їх використання. Важливо також відзначити, що корекція гіперглікемії зменшує ступінь мозкового ушкодження і також є свого роду церебропротекцією. Оптимальні рівні — 5,5–10 ммоль/л, гіпоглікемія — 2,2 ммоль/л і нижче повинна бути терміново усунена.
Протягом останніх років у хворих із ЧМТ з метою корекції ВЧТ використовується помірна гіпервентиляція, що викликає гіпокапнію, зменшує церебральний кровотік, кровонаповнення мозку.
Гіпертермія дуже часто зустрічається у хворих із тяжкою ЧМТ у відділенні інтенсивної терапії. Лихоманка погіршує перебіг травми ГМ в експериментах на тваринних моделях, а також асоціюється з несприятливими результатами лікування у хворих з травмою ГМ. Ефективним у зменшені температури є введення парацетамолу (інфулган) внутрішньовенно. Препарат має і аналгезуючий ефект.
Зважаючи на те, що нормотермічний мозок ушкоджується через 5 хв тотальної ішемії, гіпотермія ГМ підвищує стійкість до ішемії до 30 хв. Терапевтичний ефект гіпотермії включає широкий спектр нейропротекторних механізмів, серед яких модуляція виділення збуджуючих амінокислот та утворення вільних радикалів. Церебральний метаболізм зменшується на 6 % при зниженні температури мозку на 1 °С [22]. Терапевтична гіпотермія зменшує витрати енергії органічних фосфатів, уповільнює темпи метаболізму та накопичення молочної кислоти, а також знижує церебральне споживання кисню, покращуючи засвоєння глюкози.
З регенерацією нейронів і відновленням міжнейрональних зв’язків пов’язують майбутнє церебропротекції у хворих із ЧМТ. Сьогодні найбільш перспективними засобами вважаються препарати з нейротрофічною активністю. Крім того, застосувуються донатори холіну.
Чи займають належне місце нейропротектори в схемі лікування при тяжкій ЧМТ? Безумовно, тому що крім виживання пацієнта з ЧМТ необхідно відновити і функціонування ГМ, а відповідно і належну якість життя після травми.
Нейротрофічний препарат Церебролізин уже багато десятиліть використовується як при порушеннях мозкового кровообігу, так і при ЧМТ у різні періоди захворювання. Засіб діє мультимодально, тобто водночас чинить нейропротекторну та нейрорегенераторну дію, що сприяє ремоделюванню нейросудинної одиниці в гострій фазі та в періоді реабілітації. Препарат успішно застосовується також при хронічній патології центральної та периферичної нервової системи, в тому числі при нейродегенеративних захворюваннях. Велика кількість експериментальних досліджень доводять його нейротрофічну активність [1–6] завдяки наявності у складі Церебролізину фрагментів природних нейротрофічних факторів. Декілька мультицентрових рандомізованих плацебо-контрольованих клінічних досліджень демонструють позитивний вплив препарату на стан хворих після інсульту та ЧМТ [28, 29].
Досвід застосування Церебролізину в клініці невідкладної нейрохірургії протягом майже 30 років показав ефективність препарату в різні періоди ПМК та ЧМТ, жодного разу не було відзначено ускладнень [19, 27]. Лікування Церебролізином сприяло більш ранньому та більш швидкому відновленню пацієнтів, особливо їх когнітивних функцій та повсякденної активності, що в цілому дуже важливо для покращення результатів лікування та зниження рівня інвалідності. Наш досвід дозволяє стверджувати, що препарат справляє нейротрофічну мультимодальну дію при пошкожденні ЦНС, забезпечуючи нейропротекцію, нейропластичність та ней-рогенез. Оптимальна доза Церебролізину — 50 мл/добу внутрішньовенно.
Отже, Церебролізин визнаний ефективним та безпечним. На цей час Церебролізин рекомендовано про-ектною групою з вивчення доказів клінічної ефективності та безпеки при ЧМТ (ERABI, Канада, 2010) для лікування та профілактики післятравматичної деменції [27].
Про широке застосування препарату, його роль у сучасній нейронауці свідчать численні дослідження та публікації. На жаль, сьогодні в Україні можуть з’являтися препарати, виробники яких заявляють про їх подібність до Церебролізину, хоча вірогідних доказів належного рівня щодо їх ефективності та безпеки немає.
Заслуговує на увагу препарат тівортін (аргініну гідрохлорид). Препарат на основі незамінної амінокислоти аргініну є активним та різнобічним клітинним стимулятором численних життєво важливих функцій організму. У критичних станах чинить протекторну дію. Аргінін справляє антигіпоксичний, мембраностабілізуючий ефект, є активним регулятором міжклітинного обміну та процесів енергозабезпечення. L-аргінін — єдиний субстрат для синтезу NO. Перетворення L-аргініну в NO є фізіологічним процесом, спрямованим на підтримку нормального функціонування ендотелію. Як відомо, NO є фізіологічним ангіопротектором, тому що знижує адгезію лейкоцитів до судинної стінки та їх ушкоджуючу дію на ендотелій, знижує проліферацію гладком’язових клітин та патологічне ремоделювання стінки судини, пригнічує агрегацію тромбоцитів та пристінкове тромбоутворення. Отже, беручи до уваги важливе значення гемодинамічного фактора та оксигенації крові для функціонування нейронів при ЧМТ, можна стверджувати, що тівортін має нейропротекторну дію і є важливим препаратом для проведення інфузійної терапії при травмі.
У період відновлення після ЧМТ поповнення енергетичних субстратів мозку досягається призначенням препаратів, що містять кофактори біохімічних реакцій енергозабезпечення мозку: вітаміни В1, В6, В12, препарати нікотинової та фолієвої кислот.
Отже, для покращення результатів лікування хворих із ЧМТ у гострому періоді є необхідним прийняття певних детально розроблених стандартів, спрямованих на діагностику характеру ЧМТ (а саме групи хворих із низьким, середнім та високим ризиком внутрішньочерепних ускладнень), що дозволить раціонально використати наявні ресурси в медичній галузі (відповідних консультантів, застосування нейровізуалізуючих методик). Надзвичайно важливими питаннями щодо нейротравми є сучасні стандартні протоколи ведення цих хворих, а саме сучасна нейрореанімація. Моніторинг життєво важливих функцій організму є необхідним з обов’язковим вимірюванням внутрішньочерепного тиску, церебрального перфузійного тиску та вчасним їх корегуванням [4, 18, 24]. Впровадження моніторингу цих технологій є обов’язковим для ведення хворих із тяжкою ЧМТ, особливо з поєднаною ЧМТ.
Основні лікувальні процедури у хворих із тяжкою ЧМТ повинні бути спрямовані на збереження життя та відновлення порушених функцій, тобто ліквідацію первинних ушкоджуючих факторів та запобігання вторинним ушкоджуючим факторам.
Послідовність дій така:
1. Тяжкохворим із порушенням свідомості 8 балів за ШКГ та нижче проводиться інтубація трахеї з метою профілактики регургітації та забезпечення адекватного дихання.
2. Нормалізація порушеної гемодинаміки (систолічний артеріальний тиск — 90 мм рт.ст. та вище), помірна гемодилюція та гіперволемія.
3. Протягом першої години (20–30 хв після надходження) необхідно провести КТ для встановлення характеру черепно-мозкових ушкоджень. При наявності ознак стиснення мозку (гематома, вдавлений перелом) — ліквідація стиснення в перші 3 години і встановлення датчика для вимірювання ВЧТ. Перевагу слід віддавати вентрикулярним датчикам, тому що вони більш точно відображають ВЧТ і при необхідності, «стравлюючи» ліквор, дозволяють швидко знижувати ВЧТ. Паренхіматозні датчики більше свідчать про регіо-нарні та локальні ВЧТ.
4. Обов’язкове призначення антибіотиків, нейропротекторних і нейротрофічних препаратів.
5. Артеріальний тиск краще контролювати інвазивно на a. radialis. Не допускати зниження ЦПТ нижче від 70 мм рт.ст. Положення хворого з піднятим (не нижче ніж 30 °) головним кінцем ліжка. Оксигенація не менше 96–98 % (визначення пульсоксиметром), обов’язково моніторинг водно-електролітного балансу.
6. Гіповолемія є небезпечною через те, що разом із гіпотензією та згущенням крові призводить до гіпоксії.
7. Для корекції ВЧТ та покращення ЦПТ пропонують такі методи:
— підняття головного кінця ліжка на 30 градусів забезпечує зниження ВЧТ близько 10 % завдяки покращенню венозного відтоку;
— підвищується СрАТ для досягнення ЦПТ не менше ніж 70 мм рт.ст. (шляхом введення кристалоїдів, колоїдів та симпатоміметиків);
— уведення осмодіуретиків (манітол, сорбітол, реосорбілакт) під контролем електролітів;
— виведення ліквору через вентрикулодренування;
— при агресивному набряку мозку проводиться декомпресивна гемікраніоектомія розміром не менше 10 на 12 см — при латеральній дислокації та 12 на 15 см — при скронево-тенторіальному вклинені. При забоях лобних часток і компресії діенцефальних структур (компремовані, розвернуті передні роги) проводиться біфронтальна декомпресія (кістково-пластична зі збереженням кістки для пластики), особливо в осіб молодого та середнього віку.
Обов’язковим є також контроль стану електролітів крові, напруження кисню, вуглекислого газу як в артеріальній, так і венозній крові і крові, що відтікає від мозку [3].
При лікуванні хворих із тяжкою ЧМТ завданням лікарів є ліквідація механічних факторів загроз, що виникли внаслідок травми: видалення патологічних внутрішньочерепних об’ємних процесів (гематоми, вдавлені переломи), зупинка кровотечі, дренування шлуночків мозку, декомпресія ГМ, основне — профілактика виникнення вторинних факторів.
При ЧМТ виникають первинні ушкодження ГМ — механічні та судинні фактори (забої, крововиливи, розриви тощо) та вторинні фактори, такі як гіпоксія, гіпотонія, гіпертермія, гіпер- та гіпоглікемія, гіпер- та гіпокапнія. Серед вторинних факторів на першому місці виділено гіпоксію через те, що будь-який наступний фактор призводить до гіпоксії, а отже, до смерті мозку.
Перенесена ЧМТ, як правило, не буває без наслідків. Якщо вогнищеві ушкодження ГМ викликають парези, паралічі, розлади, то дифузні ушкодження, навіть такі легкі, як струс ГМ, небезпечні через загальномозкові зміні, такі як когнітивні, вегетативні розлади, зниження імунітету, загострення наявних або прояви латентних захворювань. Отже, процес лікування ЧМТ зазвичай не закінчується лише гострим періодом.
Зміни у лікуванні хворих із ЧМТ необхідні, і тільки комплексний, мультидисциплінарний та доказовий підхід до вивчення нейротравми, а також патофізіологічно обґрунтована церебропротекція дозволять знизити кількість, тяжкість ЧМТ, зменшити летальність, інвалідність та покращити якість життя постраждалих із травмою нервової системи.

/77.jpg)