Статья опубликована на с. 96-100
Острые нарушения мозгового кровообращения (ОНМК) занимают второе место в списке ведущих причин смерти на земном шаре, уступая лишь заболеваниям сердца. Ежегодно от сердечно-сосудистых заболеваний в мире погибает около 16 млн человек, смерть 5,1 млн из них связана с инсультами. Количество больных в Казахстане, получающих пособие по инвалидности в связи с перенесенным инсультом, превышает 200 тысяч человек. Заболеваемость инсультом в различных регионах Казахстана составляет 250–370 случаев на 100 тыс. человек [1, 2].
Одним из факторов, определяющих течение ишемического или геморрагического инсульта, является отек мозга, выраженность которого напрямую зависит от размеров патологического очага. При этом развивающаяся гипоксия организма способствует нарушению проницаемости клеточной мембраны с изменениями в показателях постоянства внутренней среды. Внутри- и внеклеточный отек вызывает увеличение объема мозга и развитие внутричерепной гипертензии, течение которой во многом определяет клинический исход заболевания [3–5].
В свое время великий нейрохирург Н.Н. Бурденко считал, что ключ к жизни пациента находится в руках того врача, который умеет вести борьбу с отеком головного мозга. Эти высказывания великого ученого сохраняют свою значимость и по сей день. С ростом количества случаев поражения нервной системы частота летальных исходов не снижается, а инвалидизация с тяжелыми последствиями ОНМК увеличивается [6].
В настоящее время по показаниям применяются как хирургические, так и консервативные методы лечения отека мозга.
С развитием анестезиологии и реанимации применяется в основном консервативное лечение, которое проводится и у хирургических больных.
В клиническую практику внедряются новые достижения медицинской науки и технологии. При критических состояниях используются новые фармакологические препараты.
Традиционно с противоотечной целью на практике применяются давно известные препараты — осмодиуретики. Следует отметить, что диуретики не лишены недостатков и при необоснованном использовании могут быть причиной тяжелых повреждений клеточной структуры мозга, т.е. они не идеальны. На фоне коррекции метаболических нарушений и обеспечения адекватности гемодинамики в борьбе с отеком мозга проводится искусственная вентиляция легких (ИВЛ) в специально выбранных режимах, нейровегетативная блокада, краниоцеребральная гипотермия и т.д.
Несмотря на достигнутые успехи, проблема отека головного мозга при многих заболеваниях ЦНС, в том числе при ОНМК, остается актуальной. Некоторые вопросы требуют дальнейшего изучения и разработки организационно-методических, клинико-диагностических и патогенетически обоснованных подходов к лечению больных с поражением ЦНС.
Вышеизложенное является основанием для поиска новых методов диагностики, профилактики и эффективных способов лечения отека мозга у больных с поражением мозга. В литературе появились сообщения о применении L-лизина эсцината для лечения отека мозга [7, 8]. L-лизина эсцинат — препарат, синтезированный государственным научным центром лекарственных средств (ГНЦЛС) и выпускающийся АО «Галичфарм» (Львов). Он представляет собой водорастворимую соль сапонина каштана конского (эсцина) и аминокислоты L-лизина. Препарат быстро диссоциирует в крови на ионы лизина и эсцина. Основным действующим веществом, определяющим фармакологические свойства препарата, является β-эсцин. Экспериментально-клиническим исследованиям эффективности данного препарата посвящены работы многих исследователей. Возможность его применения в нейрохирургии впервые доказана экспериментально S. Gorini и R. Caponi (1967). T. Tzonos и Н. Riebeling (1968) подтвердили эффективность препарата при лечении отека мозга у больных с черепно-мозговой травмой, a M. Cerisoli — при отеке мозга ишемического генеза. В работах последних лет отмечено, что эффективность L-лизина эсцината проявляется в результате стабилизации сосудисто-тканевой проницаемости, улучшения тонуса микрососудов, венозного и лимфатического оттока. Доказано его антиагрегантное, гипогликемическое, противовоспалительное действие.
Целью настоящего исследования стало клиническое изучение эффективности L-лизина эсцината в остром периоде ОНМК.
Методы исследования
Исследование проводилось на базе инсультного центра Областного медицинского центра г. Караганды. Было обследовано 60 больных, включенных в исследование с 03.05.15 по 15.11.15 г. Все больные были разделены на основную и контрольную группы по 30 человек. При отборе больных соблюдались определенные требования по критериям включения.
Из методов исследования были применены клиническое, лабораторное и инструментальное обследования.
Клиническое обследование:
— опрос (жалобы — на каждом визите, анамнез — при скрининге);
— физикальное обследование и оценка витальных функций (АД, ЧСС, частота дыхательных движений, температура тела) — на каждом визите;
— оценка степени инвалидизации по шкале Рэнкина — ежедневно на протяжении первых 12 дней исследования и на последнем визите;
— оценка тяжести инсульта по шкале Национального института здоровья США (NIHSS) — на каждом визите.
Лабораторные исследования:
— развернутый общий анализ крови (эритроциты, гемоглобин, гематокрит, лейкоциты, тромбоциты, СОЭ) — при скрининге;
— общий анализ мочи (рН, белок, сахар, лейкоциты, эритроциты) — при скрининге;
— биохимический анализ крови (АЛТ, АСТ, глюкоза, мочевина, креатинин, общий билирубин, общий холестерин, натрий, калий, фибриноген, протромбиновое время) — при скрининге.
Инструментальные исследования:
— КТ или МРТ головного мозга — при скрининге;
— ЭКГ в 12 отведениях — при скрининге.
Пациентам основной группы на протяжении 12–14 суток назначали исследуемый препарат L-лизина эсцинат, раствор для инъекций, внутривенно капельно по 10 мл в разведении на 200 мл 0,9 % раствора натрия хлорида 2 раза в сутки. Скорость введения — 40–60 капель в 1 минуту. Препарат вводился в одно и то же время суток (с максимальной выдержкой интервала в 12 часов).
Пациентам контрольной группы проводилось стандартное лечение, применение референтного препарата предусмотрено не было.
Были определены критерии оценки эффективности в исследовании:
— изменение выраженности неврологического дефицита по шкале NIHSS;
— динамика выраженности неврологического дефицита по Скандинавской шкале;
— динамика степени инвалидизации по шкале Бартел;
— динамика выраженности субъективных жалоб (головная боль, диплопия, системное головокружение, несистемное головокружение, тошнота и/или рвота, несостоятельность движений, слабость/онемение левых конечностей, слабость/онемение правых конечностей, нарушение речи, шаткость при ходьбе, общая слабость, снижение памяти). Выраженность указанных субъективных жалоб оценивалась при помощи вербальной аналоговой шкалы: 0 — жалоба отсутствует, 1 — слабо выражена, 2 — умеренно выражена, 3 — резко выражена.
Оценка безопасности лекарственного средства проводилась на основании жалоб пациента и объективных данных, полученных исследователем в процессе лечения. Учитывалась динамика лабораторных показателей, а также частота возникновения и характер побочных реакций.
Результаты исследования
1. Доказана превышающая эффективность терапии, включающей препарат L-лизина эсцинат, в остром периоде ишемического и геморрагического инсультов (ИИ, ГИ) по сравнению с базисной терапией.
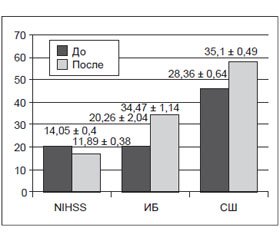
2. По результатам анкетирования по Скандинавской шкале (СШ, max = 60 б.) у пациентов основной группы средний балл после применения комплексной терапии составил 45,90 ± 2,68, тогда как в контрольной группе — 35,10 ± 0,49, что свидетельствует в пользу превышающей эффективности терапии, включающей L-лизина эсцинат (табл. 1).
3. Оценка двигательных расстройств и навыков самообслуживания по индексу Бартел (ИБ, max = 100 б.): в основной группе по результатам лечения средний балл составил 51,4 ± 5,6, в контрольной — 34,47 ± 1,14, что свидетельствует в пользу превышающей эффективности терапии, включающей L-лизина эсцинат (табл. 1).
4. Обследование пациентов с использованием шкалы NIHSS (max = 69 б.): по завершении лечения средний балл уменьшился и составил в основной группе 7,4 ± 1,3, в контрольной — 11,89 ± 0,38, что свидетельствует в пользу превышающей эффективности терапии, включающей L-лизина эсцинат (табл. 1).
Доля пациентов, у которых восстановились двигательные функции по Скандинавской шкале, в основной группе составляет 31,6 %, в то время как в контрольной — 12 %. Данные различия статистически значимы (р < 0,001).
Доля пациентов, у которых восстановились двигательные функции и навыки самообслуживания по индексу Бартел, в основной группе составляет 34,2 %, в то время как в контрольной — 14,2 %. Данные различия статистически значимы (р < 0,001).
Доля пациентов, у которых восстановились двигательные функции по шкале NIHSS, в основной группе составляет 8,62 %, в то время как в контрольной — 3,3 %. Данные различия статистически значимы (р < 0,001).
При оценке по Скандинавской шкале динамики двигательных нарушений в процессе лечения у пациентов основной группы с ишемическим инсультом средний балл составил 44,1, с геморрагическим — 52,8, по индексу Бартел с ишемическим инсультом — 49,75, у пациентов с геморрагическим инсультом — 58, по шкале NIHSS у пациентов с ИИ — 7,8, с ГИ — 6. Данные результаты исследования свидетельствуют о большей эффективности препарата L-лизина эсцинат в составе комплексной терапии у пациентов с геморрагическим инсультом.
Результаты оценки переносимости: серьезные ПЯ (побочные явления)/ПР (побочные реакции) не выявлены.
Выводы
1. Доказана превышающая эффективность терапии, включающей препарат L-лизина эсцинат, в остром периоде ишемического и геморрагического инсультов по сравнению с базисной терапией.
Так, доля пациентов, у которых восстановились двигательные функции по шкале NIHSS, в основной группе составляет 8,62 %, в то время как в контрольной — 3,3 %. Данные различия статистически значимы (р < 0,001). По результатам завершения лечения средний балл уменьшился и составил в основной группе 7,4 ± 1,3, в контрольной — 11,89 ± 0,38, что свидетельствует в пользу превышающей эффективности терапии, включающей L-лизина эсцинат.
2. Доля пациентов, у которых восстановились двигательные функции и навыки самообслуживания по индексу Бартел, в основной группе составляет 34,2 %, в то время как в контрольной — 14,2 %. Данные различия статистически значимы (р < 0,001). В основной группе по результатам лечения средний балл составил 51,4 ± 5,6, в контрольной — 34,47 ± 1,14, что свидетельствует в пользу превышающей эффективности терапии, включающей L-лизина эсцинат.
3. Доля пациентов, у которых восстановились двигательные функции по Скандинавской шкале, в основной группе составляет 31,6 %, в то время как в контрольной — 12 %. Данные различия статистически значимы (р < 0,001). У пациентов основной группы средний балл после применения комплексной терапии составил 45,90 ± 2,68, тогда как в контрольной группе — 35,10 ± 0,49, что свидетельствует в пользу превышающей эффективности терапии, включающей L-лизина эсцинат
4. При оценке динамики двигательных нарушений при ОНМК в процессе лечения у пациентов основной группы выявлена большая эффективность препарата L-лизина эсцинат в составе комплексной терапии у пациентов с геморрагическим инсультом.
Переносимость препарата была хорошей (95 %) или удовлетворительной (5 %), наблюдаемые ПР/ПЯ по степени тяжести классифицировались как легкие или средние, являлись предвиденными, несерьезными и не требовали отмены применяемого препарата.
Рекомендации
Рекомендовано применение препарата L-лизина эсцинат в составе комплексной терапии при лечении больных в остром и раннем восстановительном периодах острого нарушения мозгового кровообращения по ишемическому и геморрагическому типу.
/98.jpg)

/98_2.jpg)
/99.jpg)