Журнал "Хирургия детского возраста" 3-4 (48-49) 2015
Вернуться к номеру
Застосування біогенних стимуляторів у лікуванні статичної плоскостопості у дітей
Авторы: Данилов О.А., Шульга О.В., Талько М.О. - Національна медична академія післядипломної освіти імені П.Л. Шупика МОЗ України, м. Київ, Україна; Київська дитяча обласна лікарня № 2, м. Біла Церква, Україна
Рубрики: Педиатрия/Неонатология, Хирургия
Разделы: Клинические исследования
Версия для печати
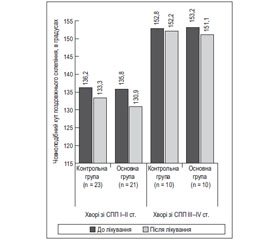
Мета роботи: дослідити ефективність поєднаного застосування біогенних стимуляторів і фармако-електро-кінезотерапії нейром’язового апарату гомілки та стопи у комплексному лікуванні хворих із статичною поздовжньою плоскостопостю (СПП), а також вивчити на основі аналізу літературних джерел можливі причини виникнення даної патології на ранніх стадіях ембріонального розвитку. Матеріали і методи. Під наглядом перебувало 64 хворі із патологією стопи на базі Київської дитячої обласної лікарні № 2. У всіх хворих діагностовано СПП, що підтверджувалось клінічно та рентгенологічно. До основної групи увійшов 31 пацієнт віком від 14 до 18 років, 21 із них із СПП І–ІІ ступеня тяжкості та 10 хворих із СПП ІІІ–ІV ступеня. Контрольну групу становили 33 хворі із СПП того ж віку, серед яких 23 зі СПП І–ІІ ступеня та 10 хворих із ІІІ–ІV ступенем тяжкості. У процесі обстеження використовувались клінічні та інструментальні методи дослідження: плантографія, рентгенографія стопи в боковій проекції з навантаженням стопи, реовазографія, електроміографія, ультразвукове дослідження (УЗД) м’язів стопи та гомілки. Результати плантографії оцінювались за методом Штрітера. Дослідження структури та діаметра м’язів проводили на апараті для ультразвукових досліджень ALOCA з лінійним датчиком із частотою 5 МГц. Хворі контрольної групи отримували стандартне консервативне лікування — фармако-електро-кінезотерапію нейром’язового апарату гомілки та стопи. У пацієнтів основної групи дану терапію було доповнено застосуванням біогенного стимулятора — екстракту плаценти. Результати. За даними рентгенологічного дослідження, після проведеного лікування відмічалося більш виражене зменшення човноподібного кута поздовжнього склепіння в основній групі (середні показники в основній групі: І–ІІ ст. — 4,9° (p > 0,05), ІІІ–ІV ст. — 2,1° (p > 0,05); у контрольній групі: І–ІІ ст. — 2,9° (p > 0,05), ІІІ–ІV ст. — 0,6° (p > 0,05)). Під впливом лікування як в контрольній, так і в основній групах відмічалося покращення електроміографічної картини, але значно кращі показники спостерігалися в останній: біоелектрична активність довгого та короткого згиначів пальців стопи після лікування в основній групі з І–ІІ ст. СПП збільшилась на 100 і 60 мкВ відповідно, а у хворих із СПП ІІІ–ІVст. — на 20 і 10 мкВ; у контрольній групі біоелектрична активність відповідних м’язів у хворих із СПП І–ІІ ст. зросла на 40 і 30 мкВ, а у хворих із СПП ІІІ–ІV ст. — на 10 та 10 мкВ. При аналізі результатів ультразвукового дослідження після закінчення курсу терапії виявлено в основній групі більш виражене збільшення діаметра м’язів гомілки та стопи порівняно із контрольною. Плантографічні показники характеризувались зменшенням індексу Штрітера, однак більш виражене покращення досліджуваних параметрів виявлено в основній групі. Проаналізувавши дані реовазографічного обстеження у хворих зі СПП I–II ст., можна відмітити покращення реосистолічного індексу в контрольній групі та значне покращення результатів в основній групі: зростання показників реосистолічного індексу в контрольній групі: лівої стопи — на 0,17 умовних одиниць (у.о.) та правої стопи — на 0,19 у.о., в основній: лівої стопи — на 0,33 у.о. та правої стопи — на 0,35 у.о. У хворих із СПП ІІІ–ІV ст. суттєвого покращення гемодинаміки не спостерігалось. Висновки. Загальна клінічна картина, терміни реабілітації хворих, дані рентгенографії, УЗД, міографії, плантографії, реовазографії свідчать про ефективність застосування біогенних стимуляторів у комплексній терапії СПП у дітей. Поєднане використання останніх та фармако-електро-кінезотерапії є патогенетично та саногенетично обґрунтованим і ефективним методом лікування СПП на початкових стадіях, однак потребує подальшого вивчення. Хворим із ІІІ–ІV ст. тяжкості показане оперативне лікування.
Цель работы: исследовать эффективность сочетанного применения биогенных стимуляторов и фармако-электро-кинезотерапии нейромышечного аппарата голени и стопы в комплексном лечении больных со статическим продольным плоскостопием (СПП), а также изучить на основе анализа литературных источников возможные причины возникновения данной патологии на ранних стадиях эмбрионального развития. Материалы и методы. Под наблюдением находилось 64 больных с патологией стопы на базе Киевской детской областной больницы № 2. У всех больных диагностировано СПП, что подтверждалось клинически и рентгенологически. В основную группу вошел 31 пациент в возрасте от 14 до 18 лет, 21 из них с СПП I–II степени тяжести и 10 больных с СПП III–IV степени. Контрольную группу составили 33 больных с СПП того же возраста, среди которых 23 с СПП I–II степени и 10 больных с III–IV степенью тяжести. В процессе обследования использовались клинические и инструментальные методы исследования: плантография, рентгенография стопы в боковой проекции с нагрузкой стопы, реовазография, электромиография, ультразвуковое исследование (УЗИ) мышц стопы и голени. Результаты плантографии оценивались по методу Штритера. Исследование структуры и диаметра мышц проводили на аппарате для ультразвуковых исследований ALOCA с линейным датчиком с частотой 5 МГц. Больные контрольной группы получали стандартное консервативное лечение — фармако-электро-кинезотерапию нейромышечного аппарата голени и стопы. У пациентов основной группы данная терапия была дополнена применением биогенного стимулятора — экстракта плаценты. Результаты и обсуждение. По данным рентгенологического исследования, после проведенного лечения отмечалось более выраженное уменьшение ладьевидного угла продольного свода в основной группе (средние показатели в основной группе: I–II ст. — 4,9° (p < 0,05), III–IV ст. — 2,1° (p < 0,05); в контрольной группе: I–II ст. — 2,9° (p < 0,05), III–IV ст. — 0,6° (p > 0,05)). Под влиянием лечения как в контрольной, так и в основной группах отмечалось улучшение электромиографической картины, но значительно лучшие показатели наблюдались в последней: биоэлектрическая активность длинного и короткого сгибателей пальцев стопы после лечения в основной группе с I–II ст. СПП увеличилась на 100 и 60 мкВ соответственно, а у больных с СПП III–IV ст. — на 20 и 10 мкВ; в контрольной группе биоэлектрическая активность соответствующих мышц у больных с СПП I–II ст. выросла на 40 и 30 мкВ, а у больных с СПП III–IV ст. — на 10 и 10 мкВ. При анализе результатов ультразвукового исследования по окончании курса терапии выявлено в основной группе более выраженное увеличение диаметра мышц голени и стопы по сравнению с контрольной. Плантографические показатели характеризовались уменьшением индекса Штритера, однако более выраженное улучшение исследуемых параметров выявлено в основной группе. Проанализировав данные реовазографического обследования у больных с СПП I–II ст., можно отметить улучшение реосистолического индекса в контрольной группе и значительное улучшение результатов в основной группе: рост показателей реосистолического индекса в контрольной группе: левой стопы — на 0,17 условных единиц (у.е.) и правой стопы — на 0,19 у.е., в основной: левой стопы — на 0,33 у.е. и правой стопы — на 0,35 у.е. У больных с СПП III–IV ст. существенного улучшения гемодинамики не наблюдалось. Выводы. Клиническая картина, сроки реабилитации больных, данные рентгенографии, УЗИ, миографии, плантографии, реовазографии свидетельствуют об эффективности применения биогенных стимуляторов в комплексной терапии СПП у детей. Совместное использование последних и фармако-электро-кинезотерапии является патогенетически и саногенетически обоснованным и эффективным методом лечения СПП на начальных стадиях, однако требует дальнейшего изучения. Больным с III–IV ст. тяжести показано оперативное лечение.
The aim was to investigate the effectiveness of combined use of biogenic stimulators and pharmaco-electro-kinesotherapy neuromuscular apparatus of the leg and foot in the complex treatment of patients with static longitudinal flatfoot (SLF), and explore, based on the analysis of literary sources, possible causes of this disease in the early stages of embryonic development. Materials and methods. We observed 64 patients with pathology of the foot on the base of Kyiv Regional Children’s Hospital № 2. SLF diagnosed in all patients which was confirmed clinically and radiographically. The study group included 31 patients aged 14–18 years old, 21 of them with SLF of the I–II degree and 10 patients had SLF of the III–IV degree. The control group consisted of 33 patients of the same age with SLF, including 23 with SLF of the I–II degree, and 10 patients with SLF III–IV degree. During the survey there were used clinical and instrumental methods of research: plantography, X-rays of the foot in the lateral projection of the load foot, rheovasography, electromyography, ultrasound examination of the foot and lower leg muscles. Plantography results were evaluated by Shtriter’s method. Investigation of the structure and the diameter of the muscle was performed on the apparatus for ultrasound studies «ALOCA» with linear sensor and 5 MHz frequency. The patients in the control group received standard treatment — pharmaco-electro-kinesitherapy of neuromuscular apparatus of the leg and foot. For the patients of the study group this therapy was supplemented by biogenic stimulator — placenta extract. Results and discussion. According to X-ray examination the treatment led to a greater reduction in the navicular angle to the longitudinal arch in the study group (average parameters: in the study group, I–II degree — 4.90 (p < 0.05), III–IV degree — 2.1 (p < 0.05); in the control group, I–II degree — 2.90 (p < 0.05), III–IV degree — 0.60 (p > 0.05). Both in control and study groups treatment improved electromyographic pattern and significantly better parameters were registered in the study group: after treatment in the patients with the I–II degree of CPR bioelectrical activity of long and short flexors of the toes increased by 100 and 60 mV, respectively, and in the patients with SLF II–IV degree by 20 and 10 mV, respectively. In the control group the bioelectrical activity of these muscles in patients with SLF I–II degree increased by 40 and 30 mV, and in the patients with SLF III–IV degree by 10 and. 10 mV. The analysis of ultrasound results, after a course of therapy, showed a more pronounced increase in diameter of the foot and leg muscles in the study group as compared to the control one. Plantography parameters decreased in Shtriter’s index, but greater improvement in the studied parameters were registered in the study group. The analysis of the reovasografic data of the patients with SLF I–II degree showed improvement in reosistolic index in the control group and a significant improvement in the study group: by 0.17 and 0.33 units on the left foot, respectively, and 0.19 and 0.35 units on the right foot, respectively. The patients with SLF III–IV degree had no ignificant improvement of hemodynamic changes. Conclusions. Clinical picture, terms of rehabilitation, X-ray data, ultrasound results, the indices of myography, plantography, rheovasography evidence the effectiveness of the biogenic stimulants for the treatment of SLF in children. Combined usage of the biogenic stimulators and pharmaco-electro-kinesitherapy is pathogenetically and sanogenetic reasonable and effective method for the treatment on the initial stages of SLF, however, requires further study. Patients with III–IV degree need operative treatment.
екстракт плаценти, статична поздовжня плоскостопість, мезенхіма, дисплазія сполучної тканини.
экстракт плаценты, статическое продольное плоскостопие, мезенхима, дисплазия соединительной ткани.
placenta extract, static longitudinal flat feet, mesenchyme, connective tissue dysplasia.
Статтю опубліковано на с. 77-85
Вступ
Матеріали та методи
Результати та їх обговорення
/81.jpg)
Висновки
1. Бадалян. Детская неврология. — М.: Медицина, 1984. — 578 с.
2. Битхем У.П. Клиническое исследование суставов. — М.: Медицина, 1970. — 187 с.
3. Букуп Клаус. Клиническое исследование костей, суставов и мышц. — М.: Медицинская литература, 2010. — 320 с.
4. Гафаров Х.З. Лечение детей и подростков с ортопедическими заболеваниями нижних конечностей. — Казань: Татар. кн. изд-во, 1995. — 384 с.
5. Зенков Л.Р., Ронкин М.А. Функциональная диагностика нервных болезней. — М.: Медпресс-информ, 2013. — 488 с.
6. Исаков Ю.Ф. Операционные хирургические состояния с анатомией детского возраста. — М., 1989. — 452 с.
7. Кашуба В.А. Биомеханика стопы. — К.: Олимпийская литература, 2003. — 279 с.
8. Коваль Г.Ю. Променева діагностика. — Т. 1 — К., 2002. — 325 с.
9. Лобзин С.В. Пункции и блокады в нейроортопедии. — СПб.: Гиппократ, 2005. — 136 с.
10. Лябах А.П. Діагностика та хірургічне лікування набутих деформацій стопи: Дис... д-ра мед. наук. — К., 2004. — 273 с.
11. Лябах А.П. Клінічна діагностика деформацій стопи. — К.: ЗАТ «Атлант ЮемСі», 2003. — 110 с.
12. Мазуров В.И. Лечение и профилактика болезней суставов. — СПб., 2006. — 360 с.
13. Маркс В.О. Ортопедическая диагностика. — Минск: Наука и техника, 1978. — 512 с.
14. Мартынюк В.Ю. Мат. науч.-практ. конф. «Актуальные проблемы реабилитации в детской ортопедии» // Вестник физиотерапии и курортологии. — 2000. — № 3. — С. 75-76.
15. Мирзаев И.И. Ортопедия детей первого года жизни. — Ленинград, 1983. — 260 с.
16. Мохаммад Мохаммад Юсеф. Профилактика и лечение осложнений миотенопластической коррекции поперечно распластанной стопы: Дис… канд. мед. наук — К., 2007. — 203 с.
17. Недригайлова О.В., Яременко Д.А. Развитие свода стопы у детей // Ортопедия, травматология и протезирование. — 1969. — № 2. — С. 18-23.
18. Олекса А.П. Травматологія і ортопедія. — К., 1993. — 512 с.
19. Очерет А.А. Как жить с плоскостопием. — М.: Советский спорт, 2000. — 96 с.
20. Проценко В.Н. Вертеброневрология и нейроортопедия. — Запорожье, 2000. — 158 с.
21. Процко В.Г., Загородний Н.В., Султанов Э.М., Хамоков З.Х., Олейник А.В. Биомеханические нарушения опорно-двигательного аппарата при плосковальгусной деформации стоп и новый метод лечения плоскостопия // Ортопедия, травматология и протезирование. — 1990. — № 5. — С. 22-26.
22. Сергиенко К.Н. К вопросу о диагностике деформации стоп // Физическое воспитание студентов творческих специальностей: Сб. науч. тр. — Харьков, 2002. — № 7. — С. 75-78.
23. Сергиенко К.Н. Определение информативности и эффективности методов, используемых при оценке сводов стопы человека // Физическое воспитание студентов творческих специальностей: Сб. науч. тр.; под ред. Ермакова С.С. — Харьков: ХХПИ, 2001. — № 6. — С. 55-59.
24. Ситенко М.И. Ортопедия и травматология: Избран. тр. — К.: Наукова думка, 1991. — 136 с.
25. Скляренко Є.Т. Травматологія і ортопедія. — К., 2005. — 480 с.
26. Фишер Юрген. Локальное лечение боли. — М.: МЕДпресс-информ, 2005. — 160 с.
27. Фищенко П.Р. Современные методы изучения в детской травматологии и ортопедии. — Ленинград, 1984. — 284 с.
28. Циркунова Н.А. Плоскостопие у детей и подростков // Амбулаторная помощь детям с ортопедическими заболеваниями: Сборник научных работ. — Харьков, 2006. — № 2. — С. 165-178.
29. Шпирт М.Б., Сыдыков Ж.С. К диагностике уплощения свода стопы и плоскостопия // Ортопедия, травматология и протезирование. — 1990. — № 9. — С. 12-14.
30. Юмашев Г.С. Травматология и ортопедия. — М., 1990. — 560 с.
31. Яременко Д.А. Диагностика и классификация статической деформации стоп // Ортопедия, травматология и протезирование. — 1985. — № 11. — С. 59-67.
32. Cox J.M. Low Back Pain Mechanism/Diagnosis and Treatment. — 6th ed. — Williams Wilkins, Baltimore, 1999. — 435 p.
33. Davids J.R., Valadie A.L., Ferguson R.L. et al. Surgical management of ankle valgus in children: use of a transphyseal medial malleolar screw // Journal of Pediatric Orthopaedics. — 1997. — Vol. 17. — Р. 3-8.
34. Dennis R. Wenger, Mercer Rang. The Art and Practice of children’s orthopedics. — Raven PRESS, New York, 1993. — 752 p.
35. Halliwell B., Gutteridge J.M.C. Free radicals in biology and medicine. — Oxford, Clarendon Press, 1995. — 385 p.
36. Wiltse L.L. Valgus deformity of the ankle // The Journal of Bone and Joint Surgery. — 1972. — Vol. 54-A, № 3 (April). — Р. 595-606.

/77.jpg)
/80.jpg)
/80_2.jpg)
/81_2.jpg)
/82.jpg)