Статья опубликована на с. 59-72
Сахарный диабет (СД) представляет собой существенную проблему мирового здравоохранения в связи с его высокой глобальной распространенностью, неуклонным ростом и ассоциированными сосудистыми осложнениями.
По последним данным Международной диабетической федерации, количество взрослых больных СД в 2015 г. достигло 415 млн (к 2040 г. прогнозируется увеличение до 642 млн), при этом СД и связанная с ним коморбидная патология стали причиной 5 млн смертей [17].
СД — заболевание, которое характеризуется повышенным уровнем глюкозы в плазме крови. При СД 1-го типа отмечается недостаточная выработка инсулина вследствие разрушения β-клеток поджелудочной железы аутоиммунного генеза [3, 42]. Заболевание является хронической патологией, наиболее распространенной у детей, но может развиться в любом возрасте. СД 2-го типа чаще отмечается у взрослых и развивается по причине инсулинорезистентности (ИР) в сочетании с постепенным угасанием функции β-клеток поджелудочной железы [25].
Показано, что хроническая гипергликемия в дальнейшем вызывает сосудистые осложнения, в том числе повышенный риск кардиоваскулярных болезней, слепоту, почечную недостаточность и приводит к ампутации нижних конечностей, а долгосрочные эффекты эпизодов низкого уровня глюкозы в плазме крови включают увеличение массы тела, ухудшение ментальной функции и деменцию [1, 38]. Следует акцентировать, что согласно последним представлениям дисгликемия при диабете как 1-го, так и 2-го типа описывается в виде триумвирата (в отличие от бытовавшей в недавнее время теории глюкоцентричности) с тремя главными компонентами, лежащими в основе развития и прогрессирования диабетических осложнений: стойкой хронической гипергликемией, вариабельностью глюкозы и гипогликемическими эпизодами [23].
По причине быстрой потери β-клеток поджелудочной железы лица с СД 1-го типа нуждаются в обязательной пожизненной инсулинотерапии, что, несомненно, влияет на качество жизни. Соответственно, введение инсулина должно быть удобным и поддерживать гликемический самоконтроль и самоадаптацию менеджмента заболевания к индивидуальному образу жизни. Вместе с тем, несмотря на достижения в базальной инсулинотерапии, контроль уровня глюкозы крови часто остается субоптимальным, с уровнем гликированного гемоглобина (НbА1с) выше нормального и клинически существенными темпами гипогликемии, включая ночную и тяжелую гипогликемию. Гипогликемия является наиболее частым неблагоприятным событием у больных СД, получающих инсулинотерапию. Несмотря на расширяющийся спектр режимов лечения, многим больным СД 2-го типа в конечном итоге также необходима инсулинотерапия для достижения адекватного гликемического контроля [14]. Современный стандарт лечения включает комбинацию инсулина длительного действия и болюсного быстродействующего (прандиального) инсулина, который вводят во время еды. Потребность инициировать инсулинотерапию у больных СД 2-го типа зависит от особенностей образа жизни и течения болезни, а именно индивидуального стиля жизни и стадии заболевания. На первых этапах больные СД 2-го типа часто достигают гликемического контроля без введения инсулина путем изменения образа жизни или приема ≥ 1 перорального антигипергликемического препарата. Однако по мере прогрессирования болезни многим пациентам необходима экзогенная инсулинотерапия. Часто терапия только базальным инсулином является предпочтительным начальным инсулиновым режимом в связи с более низким риском индуцируемых гипогликемий и меньшей прибавкой массы тела по сравнению с премиксовым инсулином или многократными инъекциями («базис + болюс» терапия). По мере прогрессирования заболевания может понадобиться дополнительная терапия, а именно быстродействующий инсулин или агонисты рецептора глюкагоноподобного пептида 1. Следовательно, базальный инсулин должен быть эффективным при широком спектре стадий заболевания, начиная от «инсулин-наивных» (не получавших инсулин) больных СД 2-го типа до получающих комбинированную терапию, с минимальным нарушением повседневной жизни. Однако в менеджменте СД инициация введения инсулина часто задерживается и, несмотря на доказанную эффективность, инсулинотерапия ограничивается пациентами и врачами, частично из-за боязни гипогликемии и увеличения массы тела. Гипогликемия и страх перед ней могут ограничивать адекватную титрацию дозы инсулина и приводить к раннему прекращению терапии. Вышеотмеченное является основанием для разработки новых инсулинов. Инсулин применяют для лечения больных СД почти столетие. За это время предпринято множество попыток разработки идеальной заместительной инсулинотерапии. Поскольку целью лечения является имитация физиологической секреции инсулина, его аналоги длительного действия разрабатывались для получения плоского беспикового профиля фармакокинетики препарата в сочетании с пролонгированным сроком действия, позволяющим вводить препарат 1 раз в сутки.
К настоящему времени прошли оценку и рекомендованы для клинической имплементации такие новые формы инсулина, как деглюдек (Тресиба®) и новейший препарат инсулина гларгин 300 Ед/мл (Gla‑300) — Тожео СолоСтар (Toujeo® SoloStar®) [13, 34]. Отметим, что разработка новых аналогов базального инсулина длительного действия, таких как Gla‑300 и деглюдек, отражает потребность рынка в препаратах, обладающих меньшей вариабельностью, обеспечивающих пролонгированную концентрацию инсулина, а также реже вызывающих гипогликемию. Полагают, что перечисленные недостатки можно преодолеть путем создания аналогов с оптимальными показателями абсорбции, плоским пролонгированным профилем фармакокинетики, который позволит вводить препарат 1 раз в сутки. Gla‑300 (Тожео СолоСтар, Toujeo® SoloStar®) — та же молекула инсулина гларгин, доставляющая то же его количество, что и инсулина гларгин 100 Ед/мл (Gla‑100) (Лантус®, Lantus®), но в 1/3 объема — 300 Ед/мл (рис. 1).
/60.jpg)
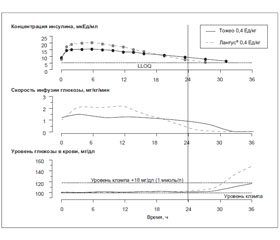
Следовательно, лекарственный препарат Gla‑300 (Тожео СолоСтар, Toujeo® SoloStar®) применяют 1 раз в сутки и при этом вместо 100 Ед/мл он содержит 300 Ед/мл. После инъекции Gla‑300 происходит образование меньшего подкожного депо вещества, что обеспечивает четкий фармакокинетический профиль с более последовательным и пролонгированным высвобождением инсулина (рис. 2) [6]. Подчеркнем высокую репрезентативность фармакокинетических/фармакодинамических характеристик, полученных с использованием техники эугликемического гиперинсулинемического клэмпа (зажима) — золотого стандарта при изучении новых препаратов инсулина. Эта техника подразумевает создание заведомо избыточной концентрации инсулина и внутривенное введение глюкозы со скоростью, необходимой для поддержания нормогликемии. Поскольку пациент при таком исследовании находится в покое, можно считать, что скорость инфузии глюкозы (СИГ), необходимая для поддержания нормогликемии, отражает внутри- и межындивидуальную вариабельность фармакологических свойств инсулина. Более того, эугликемический клэмп проводили после многократного подкожного введения инсулина для создания равновесного состояния, при котором общее поступление лекарственного средства находится в динамическом равновесии с его выведением (кинетика насыщения), у больных СД 1-го типа. Это обеспечивает более точную экстраполяцию результатов на клинические исследования, чем результаты одноразового введения инсулина, поскольку последнее лишь частично захватывает профиль действия Gla‑300, связанный с его более постепенным началом и продолжительным действием. В исследовании R.H.А. Becker и соавт. (2015) [6] фармакокинетический и фармакодинамический профили Gla‑300 и Gla‑100 изучены у больных СД 1-го типа методом эугликемического клэмпа в равновесном состоянии после введения препарата 1 раз в сутки в течение восьми дней (что лучше отражает сценарий реальной жизни, чем разовый дизайн). Исследование проведено среди больных СД 1-го типа, у которых отсутствовала эндогенная продукция инсулина (уровень С-пептида в плазме крови натощак < 0,3 нмоль/л). В связи с этим отмечаемая фармакокинетика/фармакодинамика после подкожной инъекции инсулина была обусловлена исключительно введенным инсулином. После подкожного введения последней дозы Gla‑300 и Gla‑100 (0,4 Ед/кг на восьмой день) эугликемическое состояние сохранялось в течение 32,7 и 28,7 ч соответственно (рис. 2), в то время как для Gla‑300 в дозе 0,6 Ед/кг этот показатель составил 35,3 ч. СИГ-профили Gla‑300 в равновесном состоянии показали стабильную неизменную активность на протяжении 24 ч с медленным снижением впоследствии.
/61.jpg)
После введения равной дозы (0,4 Ед/кг/сут) СИГ распределилась более ровно с Gla‑300 (рис. 2) и оставалась более высокой спустя 24 ч после введения по сравнению с Gla‑100. Таким образом, СИГ-профили в равновесном состоянии отражают фармакокинетический паттерн с меньшими колебаниями при экспозиции. Жесткий гликемический контроль (≤ 105 мг%) Gla‑300 поддерживался на 5 ч дольше (медиана — 30 ч) по сравнению с Gla‑100. При этом концентрация инсулина и профили темпа инфузии глюкозы были более постоянны и распределены более равномерно на протяжении 24 ч для Gla‑300 по сравнению с верифицированными для Gla‑100. Таким образом, Gla‑300 обеспечивает более гладкие и пролонгированные фармакокинетические и фармакодинамические профили по сравнению с Gla‑100. Действие Gla‑300 усиливалось в зависимости от дозы, его концентрация в плазме крови была измерима через 32 и 36 ч после инъекции препарата в дозе 0,4 и 0,6 Ед/кг соответственно. При использовании гиперинсулинемического эугликемического клэмпа верифицирована низкая вариабельность 24-часовой экспозиции к Gla‑300 и его глюкодинамического профиля, а также высокая воспроизводимость этих показателей (низкая междневная вариабельность) у лиц с СД 1-го типа (табл. 1) [5].
/62.jpg)
Таким образом, полученные с использованием техники эугликемического клэмпа результаты свидетельствуют о том, что инсулин гларгин 300 Ед/мл (Тожео СолоСтар) имеет более стабильный и продолжительный фармакокинетический/фармакодинамический профиль, чем инсулин гларгин 100 Ед/мл (Lantus®) с периодом полужизни 18–19 ч и длительностью глюкозопонижающего действия, превышающей 24 ч (это действие более постоянно и равномерно распределено у инсулина гларгин 300 Ед/мл по сравнению с инсулином гларгин 100 Ед/мл с низкой внутрисуточной вариабельностью и высокой междневной воспроизводимостью экспозиции к инсулину). Следует отметить, что вышеприведенные показатели очень существенны для характеристики эффективности базального инсулина [4], поскольку непредсказуемые колебания экспозиции к инсулину в циркуляции могут вызывать гипогликемии и гипергликемии, что формирует барьер к инсулинотерапии [5]. Вместе с тем в 16-недельном open-label исследовании фармакодинамических свойств инсулина гларгин у пациентов с СД 1-го типа (n = 59) при использовании постоянного мониторирования глюкозы (CGM) показано отсутствие значимых различий между инсулином Gla‑300 и Gla‑100 относительно длительности колебаний глюкозы в пределах 4,4–7,8 ммоль/л во время последних двух недель каждого периода (введение утром или вечером) исследуемой инсулинотерапии (различие определено методом наименьших квадратов (МНК) среднего значения 0,75 %; 95% ДИ от –3,61 до 5,12) [8]. В то же время объединенные средние профили глюкозы свидетельствовали о более стабильных глюкозных профилях в течение дня с инсулином Gla‑300, чем с инсулином Gla‑100, как при утреннем, так и при вечернем режиме введения, а показатели внутрисубъектной вариабельности имели тенденцию быть более низкими с инсулином Gla‑300 vs Gla‑100 [8]. В японском исследовании пациентов с СД 1-го типа (n = 20) при использовании CGM не обнаружено значимых различий в вариабельности глюкозы между инсулином Gla‑300 и Gla‑100 (AUC среднее 24 ч — отношение терапии 0,96; 95% ДИ 0,79–1,16) [19].
Очевидно, что целью применения базального инсулина является достижение равновесного состояния, при котором темп выхода инсулина в циркуляцию равняется темпу его поглощения и элиминации в мишеневых тканях на протяжении всего 24-часового периода. В идеале это достигается с циркулирующими уровнями инсулина, которые остаются по возможности постоянными (т.е. низкое отношение «пик-минимум»), и направлено на имитацию физиологического гомеостаза (равновесия между секретируемым и утилизируемым гормоном) эндогенно секретируемого базального инсулина. В связи с вышеуказанным привлекает внимание тот факт, что соотношение колебаний концентрации инсулина в кровотоке «пик-минимум», определенное по формуле (ИНС-Cмакс — ИНС-Cмин)/ИНС-Cсредняя, составило 0,6 для Gla‑300. Это существенно меньше, чем 1,6 для Gla‑100 [7]. Следовательно, введение Gla‑300 (Тожео) в терапевтической дозе 0,4 Ед/кг (однократно/сутки) обеспечивает предсказуемое и равномерное 24-часовое покрытие благодаря низкой флюктуации экспозиции к инсулину Тожео при высоком уровне междневной воспроизводимости. Это создает большое преимущество в клиническом аспекте во время титрования индивидуальной дозы инсулина для каждого пациента.
Необходимо отметить наличие такого феномена, как «скирдование» инсулина (insulin stacking), которое может быть определено как аккумуляция инсулина в крови до несоответственно высоких уровней в результате абсорбции при повторном введении. Этот сценарий главным образом характерен для быстро абсорбируемых инсулинов (meal time insulins) короткого действия, когда производятся корректирующие добавочные инъекции, если ощущается, что первоначально введенная доза инсулина недостаточна для ограничения постпрандиального повышения глюкозы. Результатом этого может быть сверхкомпенсация, ведущая к гипогликемическому событию.
Сопоставительный анализ фармакокинетических и фармакодинамических профилей инсулина Тожео в равновесном состоянии обосновывает высоковероятное прогнозирование отсутствия феномена гиперинсулинемии («скирдования») при режиме однократного в сутки п/к введения инсулина с длительностью действия более 24 часов: 24-часовой темп элиминации лекарственного препарата (инсулин Тожео) равен 24-часовому темпу абсорбции, что обеспечивает постоянный уровень инсулина в циркуляции [6, 24]. Кроме того, отсутствие «скирдования» подтверждается и результатами исследований программы EDITION.
Анализ фармакокинетических/фармакодинамических параметров инсулина Тожео свидетельствует о большей имитации Тожео по сравнению с инсулином Лантус® физиологической секреции базального инсулина, что обосновывает высоковероятную предсказуемость:
— меньшей частоты гипогликемических событий;
— большей гибкости режимов инсулинотерапии;
— упрощения титрации дозы инъецируемого инсулина;
— повышения терапевтической эффективности за счет преодоления психологической ИР (страха гипогликемии);
— потенциального ингибирующего эффекта на ангиопатии и феномен «гипергликемической памяти».
Гипотеза, что Gla‑300 может быть более полезным, чем Gla‑100, в качестве замещения базального инсулина при СД 1-го и 2-го типа путем достижения близкой к норме ночной гликемии с меньшим риском возникновения гипогликемии, проверена в серии исследований EDITION. Исследования EDITION охватили > 3500 лиц с неконтролируемым СД, при этом исследования EDITION 1–3 включали больных СД 2-го типа, а EDITION 4 — СД 1-го типа (табл. 2).
/64.jpg)
Исследования EDITION JP1 и EDITION JP2 проведены среди японцев с СД 1-го и 2-го типа соответственно. Первичной конечной точкой было изменение HbА1с от базального уровня до шестого месяца или последнего визита в ходе терапии. Главной вторичной конечной точкой, заранее определенной в исследованиях 1, 2 и 3, был процент участников с одной или более подтвержденной или тяжелой ночной (00:00–05:59 ч) гипогликемией между началом девятой недели и концом шестого месяца. Подтвержденные гипогликемии верифицировались как глюкоза плазмы ≤ 3,9 ммоль/л (≤ 70 мг%) при самостоятельном измерении глюкозы плазмы (SMPG). Статистическая значимость различий относительно частоты гипогликемических событий в группах больных СД, получавших инсулин Gla‑300 и Gla‑100, определялась с использованием таких показателей, как относительный риск (для частоты) и отношение темпов (для годовых темпов события).
Другие вторичные конечные точки включали изменения базальных уровней глюкозы плазмы натощак (ГПН), процент пациентов, достигших HbА1с < 7,0 % (5 ммоль/л) и ≤ 6,5 % (4,8 ммоль/л) или ГПН ≤ 6,7 и < 5,6 ммоль/л; изменения среднего значения и вариабельности 24-часовой глюкозы плазмы, основанной на преинъекционном 8-точечном профиле SMPG, изменения в вариабельности преинъекционной SMPG и изменения базальной и общей суточной дозы инсулина и веса тела. Процент участников с гипогликемическими событиями и годовые темпы последних были рассчитаны с использованием категоризации Американской диабетической ассоциации [2]. Подчеркнем, что относительно гликемического контроля клинические исследования EDITION фазы 3а верифицировали сопоставимый потенциал Gla‑300 и Gla‑100 в снижении уровня HbA1c (табл. 3). По результатам объединенного ретроспективного анализа (EDITION 1, 2 и 3, n = 2498) изменение МНК-среднего уровня HbА1с от базального и через 6 месяцев в обеих группах составило –1,02 % и около 36 % пациентов достигли HbА1с < 7 % [30]. У пациентов с СД обоих типов Gla‑300 и Gla‑100 вызывали подобную степень улучшения гликемического контроля: Gla‑300 не уступал Gla‑100 относительно главной первичной конечной точки, HbА1с (табл. 3), а также других первичных конечных точек, включая процент пациентов, достигших уровня HbА1с < 7 %, изменения ГПН от базального до уровня спустя шесть месяцев. В исследованиях EDITION 1–3 изменения в преинъекционном уровне SMPG, преинъекционной вариабельности SMPG и в 8-точечном профиле SMPG были в целом подобны у пациентов, получающих инсулин Gla‑300 и Gla‑100 [10, 27, 30, 40]. Так, лабораторно определенная ГПН подобным образом уменьшалась в обеих группах пациентов с СД 2-го типа: изменение МНК-среднего значения (ОС) через 6 месяцев составило –2,04 (0,07) ммоль/л с Gla‑300 и –2,26 (0,07) ммоль/л с Gla‑100 (различие МНК-средних значений (ОС) 0,21, 95% ДИ 0,03–0,40 ммоль/л). Средняя преинъекционная SMPG также уменьшалась в обеих леченых группах, и уменьшение от базального уровня до шести месяцев было подобным для Gla‑300 и Gla‑100 (изменение МНК-среднего уровня (ОС) –1,34 (0,08) ммоль/л; различие МНК-среднего уровня глюкозы: 0,09, 95% ДИ от 0,31 до 0,14 ммоль/л). Отсутствовало также различие в терапии относительно вариабельности преинъекционной SMPG через 6 месяцев: МНК-среднее значение (ОС) через 6 месяцев было 20,0 % (0,32) с Gla‑300 и 20,0 (0,33) с Gla‑100 (различие МНК-среднего 0,02 %, 95% ДИ от 0,89 до 0,93) [30]. При СД 1-го типа не было клинически релевантных различий между инсулином Gla‑300 и Gla‑100 в преинъекционной SMPG, в вариабельности преинъекционной SMPG или 8-точечного профиля SMPG [16]. Однако следует отметить, что фармакокинетические/фармакодинамические свойства инсулина гларгин 300 Ед/мл, верифицированные при проведении исследований с использованием эугликемического клэмпа, не обязательно ведут к различиям между этими инсулинами по отдельным параметрам при клинических исследованиях [9]. Так, вышеприведенные результаты свидетельствуют об отсутствии различий в вариабельности преинъекционных уровней SMPG. С другой стороны, более длительное действие инсулина гларгин 300 Ед/мл, не реализуемое в большем снижении преинъекционных уровней SMPG, обеспечивало гибкость временных режимов введения инсулина гларгин 300 Ед/мл (24 ± 3 ч) без изменения выраженности благоприятных эффектов на гликемический контроль и частоту гипогликемических событий [18]. Основные препятствия в достижении удовлетворительного контроля гликемии у лиц с СД, получающих инсулинотерапию, включают сложность режима лечения и частоту инъекций. Оба фактора влияют на приверженность пациентов к режиму терапии. B этом контексте Gla‑300 очень удобен, поскольку эффективен при введении 1 раз в сутки. Бóльшая длительность действия Gla‑300 по сравнению с Gla‑100 позволяет не только вводить препарат 1 раз в сутки всем больным СД, но и обеспечивает бóльшую гибкость интервалов между инъекциями, что может создавать преимущества для тех, кто не может вводить базальный инсулин в одно и то же время ежедневно. При этом инъекции можно выполнять как утром, так и вечером, а также со сдвигом 24 ± 3 ч (гибкий режим инсулинотерапии) при сохранении схожего гликемического контроля [15, 18].
Еще один фактор, препятствующий началу или интенсификации инсулинотерапии, — склонность к увеличению массы тела на фоне лечения инсулином. Во всех исследованиях EDITION Gla‑300 (Toujeo® SoloStar®) продемонстрировал нейтралитет относительно базального уровня (увеличение массы тела < 1 кг через 6 мес.) (табл. 3).
Более того, прирост массы тела был значительно меньшим на фоне терапии Gla‑300 (Toujeo® SoloStar®) по сравнению с Gla‑100 (Lantus®) в исследованиях EDITION 2, EDITION 4 и EDITION JP1, в которых различие в массе тела через 6 мес. составило –0,58 кг (р = 0,015), —0,56 кг (р = 0,037) и –0,6 кг (р = 0,0347) соответственно.
Учитывая, что лицам с диабетом зачастую необходимо проведение пожизненной инсулинотерапии, уменьшение прибавки массы тела при применении Gla‑300 является его преимуществом перед Gla‑100, особенно для больных СД 2-го типа, изначально имеющих избыточную массу тела или ожирение. Gla‑300 также может способствовать улучшению выполнения режимов терапии, поскольку при необходимости введения инсулина в высокой дозе использование Gla‑300 позволит осуществить задачу за одну инъекцию. Эффективность инсулина гларгин 300 Ед/мл у больных СД 2-го типа сохранялась и дольше 6 месяцев. Об этом свидетельствуют результаты продленных на 6 месяцев исследований EDITION 1 и 2 [28, 41], а также объединенный анализ 1-годичных данных (patient-level) EDITION 1, 2 и 3 [31]. Гликемический контроль поддерживался в обеих группах пациентов, получавших Gla‑300 и Gla‑100, что верифицировано по стабильному HbА1с и ГПН-понижающим эффектам. Однако изменение МНК-среднего значения HbА1с через 12 месяцев терапии было значимо большим с Gla‑300 vs Gla‑100 в EDITION 1 (–0,86 vs –0,69 %, р = 0,007) [28] и в объединенном анализе EDITION 1, 2 и 3 (–0,91 vs –0,80 %, р = 0,0174) [31]; изменения в EDITION 2 составили соответственно —0,55 vs 0,50 % [41]. Следует отметить, что прибавка веса была значимо меньшей у пациентов, получавших инсулин Gla‑300, по сравнению с Gla‑100 в EDITION 2 (+0,4 vs +1,2 кг, р = 0,009) [41] и в объединенном анализе EDITION 1, 2 и 3 (+1,2 vs +1,5 кг, р = 0,0117) [31]. В EDITION 1 среднее изменение массы тела значимо не отличалось между двумя лечеными группами (соответственно +1,2 vs +1,4 кг) [28]. Особый акцент следует сделать на преимуществе Gla‑300 перед Gla‑100 относительно гипогликемии, поскольку ее развитие, к сожалению, является огромным недостатком существующих препаратов инсулина. Гипогликемия отрицательно влияет на эффективность и безопасность антигипергликемических лекарственных средств. В настоящее время общепризнано, что главной причиной потери массы β-клеток поджелудочной железы при СД является усиленный апоптоз; снижение его интенсивности рассматривают как новую перспективную мишень для своевременной инсулинотерапии больных СД 1-го и 2-го типа [45]. В связи с этим отметим имеющиеся свидетельства того, что не только гипер-, но и гипогликемия способна вызвать апоптоз β-клеток поджелудочной железы [20, 26], поэтому предпочтение при выборе инсулина следует отдавать препаратам, доказавшим свою клиническую эффективность и безопасность в отношении развития гипогликемических состояний. Кроме того, снижение частоты гипогликемий при инсулинотерапии Gla‑300 может также формировать его потенциальные преимущества относительно феномена «плохой гликемической памяти» [44].
Целесообразно заметить, что результаты эпидемиологических исследований и клинических испытаний свидетельствуют о том, что гипогликемия может иметь отрицательное влияние на кардиоваскулярную заболеваемость и/или смертность [39]. Что касается клинического применения инсулина, то страх перед гипогликемией может быть причиной отказа от начала терапии или увеличения ее интенсивности. Также вероятно ухудшение соблюдения режима лечения, поскольку пациенты корригируют дозу препарата во избежание повторений эпизодов гипогликемии. Описывая результаты лечения с точки зрения пациента, отметим, что случаи гипогликемии негативно влияют на качество жизни, усугубляя тяжесть заболевания. Этот фактор представляет особую опасность для лиц пожилого возраста с СД, у которых часто присутствует почечная недостаточность, поскольку при этой патологии вероятность гипогликемии значительно выше, а ее последствия серьезнее. Кроме того, случаи гипогликемии снижают экономическую эффективность лечения, особенно эпизоды, требующие оказания медицинской помощи или госпитализации. В клинических исследованиях EDITION среди участников, получавших Gla‑300, отмечено меньшее количество пациентов, испытавших гипогликемии (%), по сравнению с получавшими Gla‑100, а также более низкий темп их развития (количество событий/пациент-год) (табл. 4–6).
/67.jpg)
/68.jpg)
Так, у больных СД 2-го типа на базальной и базис-болюсной инсулинотерапии до начала исследования инсулин Gla‑300 был связан со значимо более низкой частотой ночных гипогликемий, чем инсулин Gla‑100, в частности, в период с девятой недели по шестой месяц включительно. Вместе с тем у больных СД 2-го типа, не получавших инсулинотерапию до начала исследования («инсулин-наивные» пациенты), отсутствовали значимые различия в частоте подтвержденных или тяжелых ночных гипогликемий в вышеотмеченный период при терапии Gla‑300 vs Gla‑100 как по проценту участников, испытавших гипогликемию, так и по годовому темпу событий [10] (табл. 4). Однако необходимо отметить, что частота ночных гипогликемий была значимо меньшей за весь 6-месячный период у леченных Gla‑300 vs Gla‑100: ОР 0,76; 95% ДИ 0,59–0,99. В добавление отметим, что при сравнении гипогликемий в любое время суток (24 ч) и оценке годовых темпов их развития относительный риск для Gla‑300 уменьшался на 25 % vs Gla‑100 (ОР 0,75; 95% ДИ 0,57–0,99). Различие между EDITION 3 и EDITION 1 и 2 относительно основной вторичной конечной точки может быть связано с существенно более низкой их частотой, что могло снижать статистическую мощность, необходимую для определения различий между типами лечения (в EDITION 3 вовлечены «инсулин-наивные» пациенты с вероятной большей сохранностью остаточной функции β-клеток, с меньшей длительностью диабета, чем в исследовании EDITION 1 и 2, кроме того, в последних двух исследованиях пациенты имели опыт инсулинотерапии на протяжении ряда лет). Эти различия предсказывают больший гипогликемический риск [36] в исследованиях EDITION 1 и 2 всякий раз, когда гликемический контроль оптимизируется с помощью инсулина. Отметим, что Gla‑100 демонстрировал относительно низкую частоту развития гипогликемии по сравнению со стандартным лечением [22]. Результаты объединенного анализа (patient-level) исследований EDITION 1, 2 и 3 показывают, что количество лиц с СД 2-го типа, перенесших ≥ 1 эпизода гипогликемии в любое время суток, приблизительно на 6 % меньше среди получавших Gla‑300. Что касается ночных эпизодов гипогликемии, представляющих особый интерес, разница между группами Gla‑300 и Gla‑100 была более существенна, чем для случаев гипогликемии в любое время суток. По сравнению с Gla‑100 в группе Gla‑300 примерно на 10 % меньшее число участников сообщало о хотя бы одном ночном эпизоде гипогликемии [30].
Объединенный анализ EDITION 1, 2 и 3 выявил, что на протяжении 6-месячного периода терапии годовые темпы подтвержденных или тяжелых гипогликемий были значимо (р < 0,05) ниже с инсулином Gla‑300, чем с инсулином Gla‑100, в течение ночи (2,10 vs 3,06 события/пациент-год; отношение темпа 0,69; 95% ДИ 0,57–0,84) и в любое время дня (15,22 vs 17,73 события/пациент-год; отношение темпа 0,86; 95% ДИ 0,77–0,97) [30]. Соответствующие темпы за 1 год составили 2,0 vs 2,4 события/пациент-год (отношение темпа 0,82; 95% ДИ 0,67–0,99) и 13,7 vs 14,1 события/пациент-год (отношение темпа 0,97; 95% ДИ 0,87–1,09) [31]. Годовые темпы гипогликемий были значимо ниже с инсулином Gla‑300 Ед/мл, чем с инсулином Gla‑100 Ед/мл, уже в течение первых восьми недель терапии, т.е. в период титрации, когда встречаются наибольшие дозы инсулина [30]. Если рассматривать только период титрации, то отношение темпа подтвержденных или тяжелых гипогликемий составило 0,58 (95% ДИ 0,47–0,73) ночью и 0,77 (95% ДИ 0,68–0,89) в любое время дня [30]. В течение 24-часового периода наибольшее количество эпизодов подтвержденных или тяжелых гипогликемий наблюдалось между 6 и 10 часами [30]. Так, между 6 и 10 часами отмечалось около четырех событий/пациент-год с инсулином Gla‑100 и около трех событий/пациент-год с инсулином Gla‑300. Это позволяет предполагать, что полезные эффекты инсулина гларгин распространяются за пределами ночного периода. Следует отметить, что полезные эффекты Gla‑300 на ночные гипогликемии были также доказаны, когда ночной период был клинически определен как 22 ч до времени перед завтраком с помощью SMРG [29]. У больных с СД 2-го типа тяжелые гипогликемии были нечастыми при использовании как инсулина Gla‑300, так и инсулина Gla‑100 [27, 35, 40]. Объединенный рost-hoc-анализ EDITION 1, 2 и 3 показал, что годовой темп тяжелых гипогликемий в любое время был 0,11 события/пациент-год в обеих группах (отношение темпа 0,98; 95% ДИ 0,51–1,86) [30]. Значимо меньший риск подтвержденных или тяжелых гипогликемий с инсулином Gla‑300 vs инсулин Gla‑100 не зависел от возраста (< 65 или ≥ 65 лет) или ИМТ (< 30 или ≥ 30 кг/м2) [37]. Подобно вышеотмеченному в объединенном анализе EDITION 1, 2 и 3 (n = 2488) и EDITION 1 и 2 (n = 1994) темп задокументированных симптоматических гипогликемий, составивший 4,4 события/пациент-год с инсулином Gla‑300 и 5,2 события/пациент-год с инсулином Gla‑100 (отношение темпа 0,84; 95% ДИ 0,76–0,92; р < 0,001), не зависел от таких характеристик пациентов, как пол, ИМТ, длительность диабета и коморбидные заболевания [32]. Следует еще раз отметить, что в дополнение к уменьшенному темпу ночных событий гипогликемии во время фазы поддерживающей терапии (3–6-й месяцы) Gla‑300 показывал снижение гипогликемий в первые 8 недель терапии (post-hoc-анализ), потенциально демонстрируя более безопасную титрацию до цели по сравнению с Gla‑100 (Лантус®). Так, в EDITION 1 и 2 частота любого тяжелого или подтвержденного ночного эпизода низкого уровня глюкозы в плазме крови (доля лиц с не менее чем одним эпизодом) была меньше в группе Gla‑300 (Toujeo® SoloStar®) в течение первых восьми недель, когда отмечали наибольшие изменения в дозе инсулина, по сравнению с группой пациентов, применявших препарат Лантус® (EDITION 1: относительный риск (ОР) 0,79; 95% ДИ 0,64–0,98); EDITION 2: ОР 0,53; 95% ДИ 0,39–0,72). В объединенном анализе EDITION 1–3 (больные СД 2-го типа) более выраженное значимое снижение частоты ночных событий низкого уровня глюкозы в плазме крови (доля пациентов с не менее чем одной гипогликемией) отмечено во время первых восьми недель на фоне наибольших изменений дозы инсулина: –17 % в любое время суток и –31 % — в ночное время при сравнении Тожео СолоСтар с Лантус® (post-hoc-анализ). Эти результаты достигнуты на фоне применения Gla‑300 с более высокой на 10–17 % дозой инсулина и меньшим увеличением массы тела, различие было умеренным в абсолютном выражении (≈ 0,56 и ≈ 0,26 кг при СД 1-го и 2-го типа соответственно), но постоянно присутствовало во всех исследованиях EDITION и было значимым. Вышеотмеченное повышение дозы инсулина могло быть связано с тем, что часть препарата Gla‑300 разрушалась локально быстрее, чем полностью абсорбировалась. Маловероятно, что небольшое уменьшение в увеличении массы тела — результат меньшего компенсаторного приема пищи, необходимого для противодействия гипогликемии, поскольку это наблюдалось и когда Gla‑300 снижал риск возникновения гипогликемии, и когда не влиял на него. Таким образом, в отношении случаев гипогликемии Gla‑300 имеет преимущество перед Gla‑100. Еще раз подчеркнем, что во всех исследованиях EDITION Gla‑300 не уступал Gla‑100 по снижению уровня HbА1с, в то же время демонстрируя снижение риска развития гипогликемии, главным образом ночной, у больных СД 2-го типа [10, 11, 27, 30, 35]. Более того, несмотря на отсутствие существенных различий в темпах частоты любых и ночных гипогликемий (событие/пациент-год), у больных СД 1-го типа (исследование EDITION4) верифицировано существенное снижение риска подтвержденной ночной или тяжелой гипогликемии при применении Gla‑300 в первые 8 недель инсулинотерапии: отношение темпов 0,69; 95% ДИ 0,53–0,91 [15, 16]. Вместе с тем в японской популяции пациентов с СД 1-го типа (EDITION JP1) преимущества инсулина Gla‑300 vs Gla‑100 были более выражены [21]. Так, меньше пациентов, получавших Gla‑300, испытывали подтвержденные (≤ 3,9 ммоль/л) или тяжелые ночные гипогликемии на протяжении всего 6-месячного периода с наибольшей разницей в первые 8 недель. Так, в EDITION JP1 на 29 % меньше участников с СД 1-го типа испытывали эпизоды низкого уровня глюкозы в плазме крови на фоне применения Тожео СолоСтар по сравнению с препаратом Лантус® во время первых восьми недель лечения (post-hoc-анализ). Темп гипогликемических событий/пациент-год в любое время дня был ниже с Gla‑300 vs Gla‑100 во все исследуемые временные точки. Находки у больных СД 1-го типа (EDITION 4) отличаются от полученных у японских пациентов (EDITION JP1), где наблюдалась культурологически более гомогенная популяция. На протяжении всего 6-месячного периода терапии большинство (93–98 %) пациентов с СД 1-го типа в обеих группах с лечением испытывали ≥ 1 эпизода подтвержденной или тяжелой гипогликемии [16, 21]. Частота тяжелых гипогликемий была низкой в обеих группах [16, 21]. В EDITION 4 риск гипогликемий не изменялся при введении гларгина утром или вечером в отсутствие клинически значимых различий в динамике снижения HbА1с [15].
Все полученные данные свидетельствуют о том, что Gla‑300 (Тожео СолоСтар) является более предпочтительным по сравнению с Gla‑100 (Лантус®) препаратом базального инсулина, поскольку при подобном стабильном снижении хронической гипергликемии и вариабельности гликемии он более эффективен относительно третьей составляющей диабетической дисгликемии, а именно гипогликемических эпизодов. В будущем можно ожидать постепенного замещения инсулином Тожео СолоСтар препарата Лантус® многими пациентами. В заключение подчеркнем, что инсулин Тожео СолоСтар обладает множеством желаемых характеристик оптимального базального инсулина:
— длительным действием (> 24 ч);
— плоским фармакодинамическим профилем;
— низкой междневной вариабельностью, обосновывающей прогнозируемость глюкозных экскурсий;
— более низким уровнем риска возникновения гипогликемии при одинаковом уровне гликемии;
— эффективным гликемическим контролем при режиме одноразового суточного введения.
Во всех клинических исследованиях, проведенных до настоящего времени, сообщено о безопасности и хорошей переносимости препарата Gla-300. Также не отмечалось разницы в частоте возникновения нежелательных явлений между Gla-300 и Gla-100 [литература в обзоре 46].
Базальный инсулин Тожео СолоСтар одобрен Управлением по контролю за продуктами питания и лекарственными средствами США (Food and Drug Administration) и получил положительное заключение Европейского агентства по оценке лекарственных средств (European Medicines Agency — ЕМА) в конце февраля 2015 г. 28 апреля 2015 г. компания «Санофи» объявила, что ЕМА дала разрешение на продажу в странах Европы препарата Toujeo® SoloStar® для лечения взрослых пациентов с СД [47]. В Украине новый инсулин зарегистрирован в ноябре 2015 г. под торговым наименованием Тожео СолоСтар [43].
Список литературы
1. Ahsen B. Avoiding hypoglycemia: a key to success for glucose-lowering therapy in type 2 diabetes // Vasc. Healht. Risk. Man. — 2013. — Vol. 9 — P. 155-163.
2. American Diabetes Association Workgroup On Hypoglycemia. Defining and Reporting Hypoglycemia in Diabetes // Diabetes Care. — 2005. — Vol. 28, № 5. — P. 1245-1249.
3. Atkinson M.A., Herrath M., Powers A.C., Clare-Salzer M. Current concepts of the pathogenesis of type 1 diabetes — considerations for attempts to prevent and reverse the disease // Diabetes Care. — 2015. — Vol. 38 — P. 979-988.
4. Becker R.H., Frick A.D., Teichert L. et al. Fluctuation and reproducibility of exposure and effect of insulin glargine in healthy subjects // Diabetes Obes. Metab. — 2008. — Vol. 10, № 11. — P. 1105-1113.
5. Becker R.H.A., Nowotny I., Teichert L. et al. Low within- and between-day variability in exposure to new insulin glargine 300 U/ml // Diabetes Obes. Metab. — 2015. — Vol. 17, № 3. — P. 261-267.
6. Becker R.H.A., Dahmen R., Bergmann K. et al. New insulin glargin 300 U.mL‑1 provides a more even activity profile and prolonged glycemic control at steady state compared with insulin glargine 100 U.ml‑1 // Diabetes Care. — 2015. — Vol. 38. — P. 637-643.
7. Becker R.H.А. et al. Poster presentation at EASD2014; Abstract 953. — [Electronic resourse]. — Available at: http://www.easdvirtualmeeting.org/resources/18262 Accessed September 2014.
8. Bergenstal R., Bailey T., Robard D. et al. Insulin glargine 300 U/ml vs 100 U/ml: glucose profiles of morning vs evening injections in adults with T1DM measured with continuous glucose monitoring (CGM) // Diabetes Technol. Ther. — 2015. — Vol. 17. — P. A16-17 (abstract 39).
9. Blair H.A., Keating G.M. Insulin Glargine 300 U/mL: A Review in Diabetes Mellitus // Drugs. — 2016. — Vol. 76, № 3. — P. 363-374. doi: 10.1007/s40265-016-0541-z.
10. Bolli G.B., Riddle M.C., Bergenstal R.M. et al. New insulin glargine 300 U/ml compared with glargine 100U/ml in insulin naїve people with type 2 diabetes on oral glucose-lowering drugs: a randomized controlled trial (EDITION 3) // Diabetes Obes. Metab. — 2015. — Vol. 17. — P. 386-394.
11. Bolli G.B., De Vries J.H. New long-acting insulin analogs: from clamp studies to clinical practice // Diabetes Care. — 2015. — Vol. 38. — P. 541-543.
12. European Medicines Agency. Toujeo (insulin glargine U300): summary of product characteristics. 2015. — [Electronic resourse]. — Available at: http://www.ema.europa.eu/.
13. Garber A.J., King A.B., Del Prato S. et al. Insulin Degludec an ultra-longating basal insulin, versus insulin glargine in basal bolus treatment with mealtime insulin apart in type 2 diabetes (BEGIN Basal-Bolus Type 2): a phase 3, randomized open-label, treat-to-target non-inferiority trial // Lancet. — 2012. — Vol. 379. — P. 1498-1507.
14. Hirsh I.B., Bergenstal R.M., Parkin Ch.G. et al. A Real-World Approach to Insulin Therapy in Primary Care Practice // Clin. Diabetes. — 2005. — Vol. 23. — P. 78-86.
15. Home P.D., Bergenstal R.M., Riddle M.C. et al. Glycemic control and hypoglycemia with new insulin glargine 300U/ml in people with T1DM (EDITION 4) // 74th Scientific sessions of ADA, San Francisco, USA, 13-17 June 2014. — 2014. — Abstract 80-LB.
16. Home P.D., Bergenstal R.M., Bolli G.B. et al. New insulin glargine 300 Units/mL versus glargine 100 units/mL in people with type 1 diabetes: a randomized, phase 3a, open-label clinical trial (EDITION 4) // Diabetes Care. — 2015. — Vol. 38, № 12. — P. 2217-2225.
17. International Diabetes Federation. Diabetes Atlas / International Diabetes Federation. 2015. — 7th edition. — Brussels, Belgium. — 143 р. — [Electronic resourse]. — Available at: http://www.idf.org.
18. Jeandidier N., Riddle M.C., Bolli G.B. et al. New insulin Glargine 300 U/ml: efficacy and safety of flexible vs fixed dosing intervals in people with 2 diabetes mellitus // 50th Annual meeting of the European Association for the Study Diabetes, Vienna, Austria, 15-19 September 2014. — 2014. — Abstract 961.
19. Jinnouchi H., Koyama M., Amano A. et al. Continuous glucose monitoring during basal-bolus therapy using insulin glargine 300 U mL‑1 and glargine 100 U mL‑1 in Japanese people with type 1 diabetes mellitus: a crossover pilot study // Diabetes Ther. — 2015. — Vol. 6, № 2. — P. 143-152.
20. Martens G.A., Van de Casteele M. Glycemic control of apoptosis in the pancreatic beta cell: danger of extremes? // Antioxid. Redox. Sygnal. — 2007. — Vol. 9. — P. 309-317.
21. Matsuhisa M., Koyama M., Cheng X. et al. New insulin glargine 300 U/mL: glycemic control and hypoglycemia in Japanese people with T1DM (EDITION JP I) // 74th Scientific sessions of ADA, San Francisco, USA, 13-17 June 2014. — 2014. — Abstract 88-LB.
22. Monami M., Adalsteinsson J.E., Desireri C.M. et al. Fasting and post-prandial glucose and diabetic complication. A meta-analysis // Nurt. Metab. Cardiovasc. Dis. — 2013. — Vol. 23. — P. 591-598.
23. Monnier L., Colette C., Owens D. The glycemic triumvirate and diabetic complicatyions: Is the whole greater than the sum of its component parts? // Diabetes Res. Clin. Pract. — 2012. — Vol. 95. — P. 303-311.
24. Monnier L., Owens D.R., Bolli G.B. The new insulin glargine U300 achieves an early steady state with low risk of accumulation // Diabetes Metab. — 2015. — [Electronic resourse]. — Available at: http://dx.doi.org/10.1016/j.diabet.2015.11.005.
25. Nolan C.J., Damm P., Prentki M. Type 2 diabetes across generations: from pathophysiology to prevention and management // Lancet. — 2011. — Vol. 378. — P. 169-181.
26. Ricci C., Pastukh V., Mozafarri M., Shaffer S.W. Insulin withdrawal induces apoptosis via a free radical mediated mechanism // Can. J. Physiol. Pharmacol. — 2007 — Vol. 85. — P. 455-464.
27. Riddle M.C., Bolli G.B., Ziemen M. et al. New insulin glargine 300 units/ml versus glargine 100 Units/ml in people with type 2 diabetes using basal and mealtime insulin: glucose control and hypoglycemia in a 6-month randomize controlled trial (EDITION 1) // Diabetes Care. — 20l4. — Vol. 37. — P. 2755-2762.
28. Riddle M.C., Bolli G.B., Yki-Jarvinen H. et al. Sustained glycemic control and hypoglycemia with new insulin glargine 300 U/mL compared with 100 U/ml: one-year results in people with T2DM using basal + mealtime insulin (EDITION 1) // 74th Scientific sessions of ADA, San Francisco, USA, 13-17 June 2014. — 2014. — Abstract 81-LB.
29. Riddle M.C., Home P.D., Avogaro A. et al. A clinically-defined nocturnal window for analysis of hypoglycemia with new insulin glargine 300 U/mL in type 2 diabetes (T2DM) // Diabetes. — 2015. — Vol. 64, Suppl. 1. — P. A263.
30. Ritzel R., Roussel R., Bolli G.B. et al. Patient-level meta-analysis of the EDITION 1, 2 and 3 studies: glycaemic control and hypoglycaemia with new insulin glargine 300 U/ml versus glargine 100 U/ml in people with type 2 diabetes // Diabetes Obes. Metab. — 2015. — Vol. 9. — P. 859-867.
31. Ritzel R., Roussel R., Giaccari A. et al. Glycemic control and hypoglycemia with insulin glargine 300 U/mL (Gla‑300) vs glargine 100 U/mL (Gla‑100) in type 2 diabetes (T2DM) in a patient-level meta-analysis of 1-year phase 3a EDITION studies // 75th Scientific sessions of ADA, Boston, USA, 5-9 June 2015. — 2015. — Abstract 1030-P.
32. Rosenstock J., Zhang Q., Gerrits C. et al. Is hypoglycemia a modifiable patient risk in type 2 diabetes? A pooled analysis of insulin glargine 300U/ml (Gla‑300) vs. 100U/ml (Gla‑100) trials // Diabetes. — 2015. — Vol. 64, Suppl. 1. — P. A110.
33. Steinstaresser A., Schmidt R., Bergmann K. et al. Investigational new insulin glargine 300 U/ml has the same metabolism as insulin glargine 100 U/ml /research letter // Diabetes Obes. Metab. — 2014. — Vol. 16. — P. 873-876.
34. Sutton G., Minguet J., Ferrero C. Bramlage P. U300, A novel long-acting insulin formulation // Expert Opin. Biol. Ther. — 2014. — Vol. 14. — P. 1849-1860.
35. Terauchi Y., Koyama M., Cheng X. et al. Glycemic control and hypoglycaemia in Japanese people with T2DM receiving New insulin Glargine 300 U/ml in combination with OADs (EDITION JP 2) // 50th Annual meeting of the European Association for the Study Diabetes, Vienna, Austria, 15-19 September 2014. — 2014. — Abstract 976.
36. Tschope D., Bramlage P., Binz C. et al. Incidence and predictors of hypoglycaemia in type 2 diabetes — an analysis of the prospective // DiaRegis. registry. BMC Endocr. Disord. — 2012. — Vol. 12. — P. 23.
37. Twigg S.M., Escalada J., Grisoni M.-L. et al. Age, BMI, and diabetes duration: effect on glycemic control and hypoglycemia with insulin glargine 300 U/mL in type 2 diabetes (T2DM) // 75th Scientific sessions of ADA, Boston, USA, 5-9 June 2015. — 2015. — Abstract 1017-P.
38. Xie L., Wei W., Pan C., Baser O. Real-world rates, predictors and associated costs of hypoglycemia among patients with type 2 diabetes mellitus treated with insulin glargine: results of a pooled analysis of six retrospective observational studies // J. Med. Econ. — 2013. — Vol. 16. — P. 1137-1145.
39. Yakubovich N., Gerstein H.C. Serious cardiovascular outcomes in diabetes: the role of hypoglycemia // Circulation. — 2011. — Vol. 123. — P. 342-348.
40. Yki-Jarvinen H., Bergenstal R., Ziemen M. et al. New insulin glargine 300 U/mL versus glargine 100 U/mL in people with type 2 diabetes using oral agents and basal insulin: glucose control and hypoglycemia in a 6-month randomized controlled trial (EDITION 2) // Diabetes Care. — 2014. — Vol. 37. — P. 3235-3243.
41. Yki-Jarvinen H., Bergenstal R.M., Bolli G.B. et al. Less nocturnal hypoglycemia and weight gain with new insulin glargine 300 U/ml compared with 100 U/ml: 1-year results in people with T2DM using basal insulin with OADs (EDITION 2) // 74th Scientific sessions of ADA, San Francisco, USA, 13-17 June 2014. — 2014. — Abstract 93-LB.
42. Ефимов А.С., Полторак В.В. Аутоиммунные аспекты инсулинзависимого сахарного диабета. Попытки иммунокоррекции на ранних стадиях заболевания // Пробл. эндокринологии. — 1989. — Т. 35. — С. 85-90.
43. Компендиум — лекарственные препараты (2015) / Под ред. В.Н. Коваленко [Электрон. ресурс]. — Режим доступа: http://compendium.com.ua/info/252094/sanofi/tozheo-solostar.
44. Полторак В.В., Красова Н.С., Горшунская М.Ю. Гликемическая память как патогенетическое основание для формирования алгоритма современной антидиабетической терапии // Международный эндокринологический журнал. — 2014. — T. 59. — C. 15-22.
45. Полторак В.В., Красова Н.С., Горшунская М.Ю. Апоптоз панкреатических бета-клеток как новая мишень для инсулинотерапии больных сахарным диабетом 1-го и 2-го типа // Проблемы эндокринной патологии. — 2015. — № 1. — C. 90-102.
46. Полторак В.В., Кравчун Н.А., Горшунская М.Ю. Инсулин Тожео Солостар — новый базальный инсулин длительного действия. Часть 2. Клиническая эффективность и безопасность // Международный эндокринологический журнал. — 2015. — Т. 72. — С. 3-22.
47. Препарат Тожео® (Toujeo®) затверджений у Європейському Союзі для лікування діабету у дорослих — новий базальний інсулін показав глікемічний контроль із меншою кількістю випадків підтвердженої гіпоглікемії // МЭЖ. — 2015. — Т. 67. — С. 96-98.

/60.jpg)
/61.jpg)
/62.jpg)
/64.jpg)
/65.jpg)
/67.jpg)
/68.jpg)