Газета «Новости медицины и фармации» 10 (584) 2016
Вернуться к номеру
Сравнительное исследование эффективности и переносимости двух лекарственных форм ацетилсалициловой кислоты: Ацекор Кардио и ацетилсалициловая кислота с защитными агентами
Авторы: Запровальная О.Е.(1), Копица Н.П.(1), Крайз И.Г.(2), Рудык Ю.С.(1), Серик С.А.(1), Целуйко В.И.(3)
(1) ГУ «Национальный институт терапии им. Л.Т. Малой НАМН Украины», г. Харьков, Украина; (2) ГЛПУ «Центральная клиническая больница Украинской железной дороги», г. Харьков, Украина; (3) Харьковская медицинская академия последипломного образования врачей, г. Харьков, Украина
Рубрики: Кардиология
Разделы: Клинические исследования
Версия для печати
Статья опубликована на с. 14-19 (Укр.)
Антиагрегантная терапия является основной составляющей профилактики сердечно-сосудистых заболеваний, предотвращая развитие атеротромботических осложнений, связанных с нарушением целостности атеросклеротической бляшки. Тесная взаимосвязь процессов атерогенеза и тромбообразования у пациентов с ишемической болезнью сердца (ИБС) делает патогенетически оправданным проведение долговременной антитромботической терапии, тормозящей на ранних этапах формирование артериального тромба [1].
Ацетилсалициловая кислота (АСК, аспирин) является одним из уникальных лекарственных средств. Несмотря на более чем столетнюю историю применения, АСК и сегодня остается одним из самых востребованных препаратов во всем мире. Золотой стандарт антитромбоцитарной терапии, как уже не одно десятилетие называют АСК, не уступил своего места ни одному из новых антитромбоцитарных препаратов, и в настоящее время продолжает занимать основные позиции в профилактике и лечении сердечно-сосудистых заболеваний.
Доказано, что низкие дозы АСК обладают выраженной антитромбоцитарной активностью, а при более высоких дозах аспирин также имеет жаропонижающее, обезболивающее, противовоспалительное и, предположительно, даже противораковое свойства [2]. В кардиологии терапевтическое применение аспирина охватывает континуум от первичной профилактики сердечно-сосудистых заболеваний до лечения всех атеротромботических осложнений, в первую очередь острого коронарного синдрома.
Целесообразность применения АСК для вторичной профилактики сердечно-сосудистых заболеваний была установлена еще в 1980-х. Первым серьезным доказательством стало исследование ISIS-2, убедительно показавшее превосходство АСК перед плацебо у пациентов с острым инфарктом миокарда (ИМ) с подъемом сегмента ST [3]. В 15-месячном наблюдении всего один месяц приема низких доз аспирина (162,5 мг кишечнорастворимой формы АСК), отдельно или в комбинации с фибринолитиком (стрептокиназа), приводил к существенному снижению относительного риска нефатального повторного ИМ (23 %) и смерти (42 %) [3, 4]. Еще в 4 исследованиях [5–7] подтвержден эффект АСК при остром коронарном синдроме без подъема сегмента ST.
Крупные метаанализы окончательно закрепили АСК в списке основных препаратов для лечения ИБС [9, 10]. Комплексный метаанализ, включивший более 200 000 пациентов с сердечно-сосудистыми заболеваниями с высоким риском, неопровержимо доказал, что аспирин на 25 % уменьшает частоту серьезных сосудистых событий (нефатальный инфаркт миокарда, нефатальный инсульт или смерть от сосудистых причин) по сравнению с плацебо [10]. Кроме того, при дальнейшем наблюдении за 6213 из 17 187 участников этого исследования показано, что увеличение выживаемости, достигнутое в первые месяцы, сохраняется еще в течение десяти лет.
Назначение АСК пациентам со стабильными формами ИБС также сопровождается значительным снижением (на 33 %) риска серьезных сердечно-сосудистых событий. Доказательную базу составляют результаты 7 рандомизированных исследований, в которых принимали участие около 3 тыс. пациентов со стабильной стенокардией [9]. В клиническом исследовании American Physicians Health Study прием АСК пациентами со стабильной стенокардией по 325 мг через день в течение 5 лет привел к снижению у них количества первичных ИМ на 87 % (p < 0,001) [11]. Также веские доказательства профилактического действия АСК при стабильной стенокардии были получены в крупном рандомизированном исследовании SAPAT [12]. У пациентов, принимавших небольшую дозу АСК (75 мг), ИМ и внезапная коронарная смерть наблюдались на 34 % реже, чем в группе плацебо. Также в этой когорте зарегистрировано на 26 % меньше смертельных исходов от любых сердечно-сосудистых причин. Очень важным аспектом терапии является возможность применения АСК при артериальной гипертензии (АГ). В соответствии с рекомендациями ESH/ESC 2013 г. [13] по лечению АГ, больным с контролируемой АГ, ранее перенесшим сердечно-сосудистые события, также следует назначать антитромбоцитарные препараты, в частности малые дозы АСК.
За последние годы появились убедительные клинические данные о пользе применения АСК у пациентов с атеросклерозом церебральных артерий. Согласно результатам метаанализа, объединившего результаты 21 исследования по вторичной профилактике инсульта и преходящих нарушений мозгового кровообращения, снижение риска повторных сосудистых событий при терапии антиагрегантами составило 22 % [14]. Зарегистрировано уменьшение риска развития ишемического инсульта на 6,9 на 1000 леченых пациентов, что демонстрирует высокую эффективность использования АСК у этой категории больных [14].
Не вызывает сомнений целесообразность назначения АСК в настоящее время для профилактики сердечно-сосудистых осложнений у больных с мультифокальными проявлениями атеросклероза. В метаанализе 42 исследований [15], включившем более 9000 пациентов с атеросклерозом периферических артерий нижних конечностей, показано, что при назначении антитромбоцитарной терапии суммарный риск развития сосудистых событий у этих пациентов снижается на 23 % (р = 0,004), причем независимо от выбранной тактики лечения — консервативной или хирургической (сосудистое шунтирование или эндоваскулярное вмешательство).
Кроме того, по результатам ряда метаанализов установлена целесообразность назначения АСК больным с фибрилляцией предсердия (в качестве альтернативы варфарину), заболеваниями периферических артерий (стеноз сонных артерий) и терминальной хронической почечной недостаточностью (требующей проведения гемодиализа).
Таким образом, в настоящее время эффективность назначения АСК с целью вторичной профилактики атеротромботических событий считается абсолютно доказанной. Этот факт, а также соотношение цена/качество позволяют считать, что популярность препаратов АСК в качестве средства первой линии вряд ли будет превзойдена в обозримом будущем.
Наиболее дискутабельным вопросом является назначение АСК с целью первичной профилактики сердечно-сосудистых заболеваний. Хотя аспирин — единственный из антитромботических препаратов, который в настоящее время применяют для первичной профилактики, его назначение требует серьезного подхода. Поскольку при использовании АСК на протяжении 5 лет для первичной профилактики на 1000 пролеченных больных в среднем у 2–4 развиваются серьезные кровотечения из желудочно-кишечного тракта (ЖКТ) и у 2 — геморрагические инсульты, назначение АСК возможно только после обязательного определения соотношения тромботических и геморрагических рисков [16].
Выбор оптимальной дозировки АСК базируется на представлениях о том, что ее антитромботический эффект связан с подавлением агрегации тромбоцитов за счет необратимой блокады в них циклооксигеназы-1 (ЦОГ-1) и почти полного подавления продукции тромбоксана А2. Особенностью ЦОГ-1 является ее чрезвычайно высокая чувствительность к действию АСК, которая в десятки раз превышает таковую циклооксигеназы-2 (ЦОГ-2), ответственной за продукцию простациклина в эндотелии сосудов. Таким образом, в малых дозах АСК, блокируя только ЦОГ-1 и оставляя интактной ЦОГ-2, вызывает преимущественное снижение продукции тромбоксана А2, в то время как уровень простациклина, мощного естественного вазодилататора и антиагреганта, остается достаточно высоким. В текущих клинических руководствах рекомендуют использование низких доз аспирина (75–162 мг) один раз в день у пациентов с ИБС [17, 18].
Основной клинической проблемой применения АСК являются осложнения со стороны желудочно-кишечного тракта в виде развития диспептических расстройств и эрозивно-язвенного гастрита. В сочетании с присущим АСК антитромбоцитарным действием это повышает риск желудочно-кишечных кровотечений. В течение года желудочно-кишечные кровотечения, требующие госпитализации, возникают (по данным крупных регистров западных стран) у 2 из 1000 больных при лечении низкими дозами АСК. Риск кровотечений при этом является дозозависимым: частота желудочно-кишечных кровотечений удваивается при повышении дозы АСК с 75–100 до 200 мг/сут.
Для предупреждения развития побочных реакций со стороны пищеварительного тракта у пациентов, которым показана длительная антитромбоцитарная терапия, препарат АСК был выпущен в виде таблеток, покрытых кишечнорастворимой оболочкой. Благодаря этой оболочке таблетка проходит через желудок целиком и растворяется в кишечнике, где абсорбируются активные ингредиенты, что позволяет защитить желудок от негативного влияния АСК при длительном применении. Результаты рандомизированного проспективного исследования, проводимого на протяжении 2 лет с участием 2739 пациентов, показали, что при переходе с простых форм АСК на кишечнорастворимую форму препарата у 1570 больных на 60 % уменьшилось количество побочных реакций со стороны верхних отделов пище–арительного тракта.
Однако в отдельных исследованиях продемонстрировано, что эрозии и язвы желудка из-за системного действия АСК могут возникать даже при применении защитной оболочки, и рубцуются они в 90 % случаев (на фоне терапии циметидином и антацидами) только после отмены АСК. Таким образом, кишечнорастворимые лекарственные формы способны уменьшать частоту диспептических нарушений. Вопрос о влиянии кишечнорастворимых форм на риск развития язв, кровотечений и перфораций остается открытым и требует дополнительного изучения.
Таким образом, АСК является самым доступным и широко используемым антитромбоцитарным препаратом, рекомендованным как для вторичной, так и для первичной профилактики сердечно-сосудистых событий, эффективность которого подтверждена многочисленными крупными плацебо-контролируемыми исследованиями и данными метаанализов.
В настоящее время существует две основные формы выпуска АСК: кишечнорастворимая и форма в виде комплекса с агентами, оказывающими защитное действие на слизистую оболочку желудка.
Для сравнительной оценки было проведено исследование эффективности и переносимости антиагрегантной терапии с применением двух различных форм АСК, обеспечивающих защиту слизистой оболочки желудка, но различающихся по типу защитного действия и окну всасывания. В качестве представителя кишечнорастворимой формы АСК был взят препарат Ацекор Кардио (кишечнорастворимые таблетки по 100 мг производства ООО «НПФ «Микрохим»). В качестве препарата сравнения использованы препараты АСК по 75 и 150 мг, которые представляют собой комбинацию АСК и невсасывающегося антацида — гидроксида магния.
Данное клиническое исследование (пострегистрационное, IV фаза) проводилось как открытое многоцентровое рандомизированное сравнительное в параллельных группах пациентов с верифицированным диагнозом ИБС и по характеру вмешательства в обычную тактику ведения пациента было неинтервенционным клиническим.
В исследование были включены амбулаторные пациенты 35–75 лет со стабильным течением ИБС (стабильная стенокардия напряжения давностью более 3 мес.), получающие стандартную лекарственную терапию в постоянных дозировках (≥ 1 мес.), подписавшие информированное согласие на участие в исследовании, соответствующие критериям включения и имеющие как минимум 1 основной и 1 дополнительный факторы риска.
Основные факторы сердечно-сосудистого риска:
- перенесенный ИМ (давностью > 12 мес.);
- доказательства многососудистого поражения коронарного русла, независимо от статуса реваскуляризации (последняя реваскуляризация миокарда выполнена более 12 мес. назад), или
- доказательства однососудистого поражения без реваскуляризации, с положительным результатом неинвазивной нагрузочной пробы, либо выписка из стационара с документально подтвержденной нестабильной стенокардией давностью от 6 до 12 мес.
Дополнительные факторы сердечно-сосудистого риска:
- сахарный диабет 1-го или 2-го типа;
- заболевание периферических артерий;
- курение в настоящее время (≥ 10 сигарет в сутки); мужчины и женщины в возрасте от 35 до 75 лет, подписавшие информированное согласие на участие в исследовании и имеющие верифицированную ИБС, постинфарктный кардиосклероз, перенесенный атеротромбоз других сосудистых бассейнов, а именно — наличие постинфарктного кардиосклероза;
- наличие контролируемой артериальной гипертензии.
В исследование не включались пациенты, имеющие:
- выраженную систолическую дисфункцию (фракция выброса < 40 %);
- гиперчувствительность к компонентам исследуемого препарата;
- значительные нарушения функции печени (повышение уровней аспартатаминотрансферазы (АСТ) и аланинаминотрансферазы (АЛТ) более чем в 3 раза);
- выраженные нарушения функции почек (клиренс креатинина менее 45 мл/мин);
- ангионевротический отек в анамнезе;
- эрозивно-язвенные поражения ЖКТ (в фазе обострения);
- бронхиальную астму, индуцированную приемом салицилатов;
- геморрагический диатез;
- любые другие сопутствующие декомпенсированные заболевания или острые состояния, наличие которых, по мнению исследователя, способно повлиять на результаты исследования.
Согласно схеме рандомизации больные были распределены в 3 группы. В составе комплексной терапии основного заболевания пациенты 1-й группы получали препарат Ацекор Кардио в дозировке 100 мг, 2-й — 75 мг препарата АСК с защитными агентами, 3-й — препарат АСК с защитными агентами в дозировке 150 мг. Длительность лечения антиагрегантами составила 4 недели.
Сравнительная оценка эффективности таблеток Ацекор Кардио и АСК с защитными агентами в двух дозировках как средств антиагрегантной терапии пациентов с верифицированным диагнозом ИБС проводилась по показателям дезагрегантного действия тестируемого и референтного препаратов — индуцированной агрегации тромбоцитов до начала и по завершении 4-недельного курса терапии.
Сравнительная оценка переносимости исследуемых лекарственных средств выполнялась с учетом частоты и выраженности побочных эффектов (тошнота, рвота, диспепсия, диарея, запор, изжога, боли в эпигастральной области и абдоминальная боль, воспаление ЖКТ, эрозивно-язвенные поражения ЖКТ с соответствующими лабораторными показателями и клиническими симптомами), которые выявлялись при опросе пациентов и по данным гастроскопии. При проведении исследования не разрешалось применение дополнительных лекарственных средств, обладающих антитромбоцитарным и антитромботическим действием, а также нестероидных противовоспалительных средств, кортикостероидов, метотрексата.
Всего было обследовано 146 пациентов. Распределение пациентов по группам осуществлено методом простой рандомизации.
Оценка эффективности
Первую группу составили 49 пациентов, получавших исследуемый препарат Ацекор Кардио. Группы сравнения: 2-я — 49 больных, которым назначали АСК с защитными агентами в дозировке 75 мг, и 3-я — 48 пациентов, получавших АСК с защитными агентами в дозировке 150 мг. Сравниваемые группы не отличались между собой по характеру распределения пола и возраста (табл. 1).
Оценка эффективности препаратов ацетилсалициловой кислоты в исследуемых группах проводилась на основании анализа параметров тромбоцитарного гемостаза (количество тромбоцитов, спонтанная и индуцированная агрегация тромбоцитов, определенные с помощью клинического анализа крови).
Определение эффективности выполнено по приведенной ниже шкале:
- хорошая эффективность
Антиагрегантный эффект тестируемого препарата Ацекор Кардио выше или равен эффекту референтных препаратов АСК с защитными агентами в дозировке 75 и 150 мг при сравнении значений индуцированной агрегации тромбоцитов по завершении 4-недельного периода лечения;
- отсутствие эффекта
Антиагрегантный эффект тестируемого препарата Ацекор Кардио ниже эффекта референтных препаратов АСК с защитными агентами в дозировке 75 и 150 мг при сравнении значений индуцированной агрегации тромбоцитов по завершении 4-недельного периода лечения.
Как показали данные лабораторных исследований, параметры общего и биохимического анализов крови достоверно не отличались между группами в период рандомизации (табл. 2).
При оценке исходных показателей тромбоцитарного гемостаза (спонтанная и индуцированная агрегация) не выявлено достоверных отличий между сравниваемыми группами пациентов с ИБС. В то же время агрегационная активность тромбоцитарного звена гемостаза была существенно выше контрольных показателей во всех трех группах (табл. 3–5).
В настоящее время показано, что повышение агрегации тромбоцитов является важным элементом патогенеза как развития, прогрессирования сердечно-сосудистых заболеваний, так и возникновения осложнений. Механизмы активации тромбоцитов могут быть различными и зависят от состава плазмы крови, изменений функционального состояния и структуры мембран тромбоцитов. Значительная роль принадлежит и динамике функционального состояния эндотелия с утратой эндотелиальными клетками их дезагрегантных и антиадгезивных свойств. Особое значение имеет спонтанная агрегация тромбоцитов, когда избыток агрегатов тромбоцитов циркулирует в системном кровотоке. Спонтанная агрегация встречается всего лишь в 2–3 % случаев у здоровых людей.
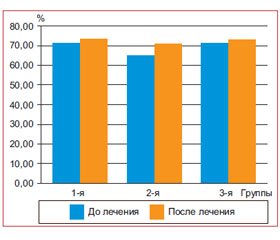
По результатам, полученным нами, зафиксировано существенное повышение частоты спонтанной агрегации во всех трех группах (табл. 3, рис. 1), что свидетельствует о циркуляции в кровотоке потенциально активных клеток, которые могут при прочих условиях инициировать внутрисосудистое тромбообразование, высвобождать активные вещества, приводящие к нарушению микроциркуляции и коронарного кровотока.
Несмотря на проводимую терапию, ни в одной группе не удалось достигнуть достоверного снижения этого показателя в процессе лечения.
В последнее время спонтанная агрегация тромбоцитов, наряду с общеизвестными факторами риска атеротромбоза, выделяется как независимый фактор риска [29]. Основанием для этого послужили результаты многоцентрового проспективного исследования HAPARG (Haemostaseologische Parameter als Risikofaktoren bei Gesunden: haemostatic parameters as risk factors in healthy volunteers), в котором участвовало 1884 мужчины и 989 женщин [30].
Авторы исследования HAPARG обнаружили повышенную спонтанную агрегацию, ассоциированную с высоким риском тромботических осложнений, у пациентов с сахарным диабетом, заболеваниями периферических и коронарных артерий, тогда как другие известные факторы риска не коррелировали с указанными расстройствами. Частота спонтанной агрегации увеличивалась с возрастом и чаще выявлялась у женщин, чем у мужчин, во всех возрастных группах. Однако число конечных точек (сердечно-сосудистые и церебральные события, тромбозы периферических вен) было значительно выше у мужчин, чем у женщин (50 против 3). В исследовании M.D. Trip и коллег [31] наличие выраженной агрегации у пациентов, перенесших инфаркт миокарда за 3 месяца до исследования, связано с высокой летальностью от сердечно-сосудистых событий (34,6 %) в течение последующих 5 лет по сравнению с пациентами, у которых отмечены умеренно выраженная спонтанная агрегация тромбоцитов (10,3 %) или ее отсутствие (6,4 %). Выявлены факторы, ассоциированные с увеличением частоты спонтанной агрегации: курение, низкий уровень липопротеинов высокой плотности, повышенный уровень глюкозы и высокое диастолическое давление. Показано повышение спонтанной агрегации тромбоцитов у пациентов с сахарным диабетом 2-го типа и микроангиопатией по сравнению с людьми, не страдавшими диабетом. Как выявлено в исследовании PARD, наличие спонтанной агрегации ассоциировано с высоким риском новых сосудистых окклюзий у больных сахарным диабетом [32]. В исследовании О.В. Сироткиной и коллег спонтанная агрегация тромбоцитов коррелировала с количеством GP IIb/IIIa на поверхности тромбоцитов (r = 0,39, p < 0,05) [33].
Остается спорным вопрос об участии тромбоксана А2 в спонтанной агрегации тромбоцитов. Результаты нашего исследования не подтверждают связи угнетения тромбоксана А2 под влиянием исследуемых препаратов ацетилсалициловой кислоты с частотой возникновения спонтанной агрегации. Причем это отмечалось при использовании как препарата Ацекор Кардио, так и обеих дозировок АСК с защитными агентами.
При анализе параметров индуцированной агрегации тромбоцитов выявлено исходное повышение суммарного индекса агрегации тромбоцитов (СИАТ) во всех группах пациентов с ИБС в момент рандомизации.
В динамике лечения отмечалось ингибирование агрегации тромбоцитов, индуцированной арахидоновой кислотой (АК), о чем свидетельствовало снижение суммарного индекса тромбоцитов (СИАТ-АК) (табл. 4, рис. 2).
Арахидоновая кислота — природный агонист агрегации, причем ее действие опосредовано эффектами простагландинов G2 и H2 и тромбоксана А2 и включает активацию как фосфолипазы C с последующим образованием вторичных посредников, мобилизацией внутриклеточного кальция и расширением процесса активации клеток, так и фосфолипазы А2, что непосредственно приводит к высвобождению эндогенной арахидоновой кислоты.
Активация тромбоцитов под действием арахидоновой кислоты происходит достаточно быстро, поэтому кривая, характеризующая этот процесс, чаще носит одноволновой характер.
Поскольку на агрегацию с арахидоновой кислотой непосредственно влияет ацетилсалициловая кислота, эффективность сравниваемых препаратов прямо зависит от СИАТ-АК, что подтверждается результатами наших исследований.
Для оценки агрегации тромбоцитов, индуцированной аденозиндифосфатом (АДФ), нами было использовано две концентрации индуктора — 2,5 и 10 мкмоль.
При воздействии малых доз АДФ на агрегатограмме регистрируют двойную волну агрегации. Первая фаза (первичная волна) зависит от добавленного экзогенного АДФ, а вторая (вторичная волна агрегации) — от реакции высвобождения собственных агонистов, содержащихся в гранулах тромбоцитов. Вводимые извне большие дозы АДФ (обычно 10 мкмоль) приводят к слиянию первой и второй волн агрегации.
При оценке агрегатограмм с различной концентрацией АДФ не выявлено дополнительного ингибирующего влияния на агрегацию тромбоцитов как препарата Ацекор Кардио, так и АСК с защитными агентами (табл. 5, рис. 3, 4). А при использовании АДФ в концентрации 2,5 мкмоль обнаружено даже достоверное повышение СИАТ в динамике лечения у пациентов, получавших 75 мг АСК с защитными агентами.
Важно отметить, что появление двухволновой агрегации при стимуляции АДФ в концентрациях, вызывающих в норме обратимую агрегацию (обычно 1–5 мкмоль), указывает на повышение чувствительности тромбоцитов к этим индукторам, а развитие одноволновой неполной (а часто и обратимой) агрегации при стимуляции ими в концентрациях 10–6 моль и более — на нарушение реакции высвобождения тромбоцитов.
Особенно интересной представляется оценка дезагрегации тромбоцитов (табл. 6–8, рис. 5–7). Как видно из представленных данных, при использовании препарата Ацекор Кардио и обеих дозировок АСК с защитными агентами число лиц с наличием дезагрегации тромбоцитов достоверно не изменилось.
Совсем другая ситуация наблюдается при анализе дезагрегации при использовании арахидоновой кислоты. Если при назначении малых доз ацетилсалициловой кислоты — препарата Ацекор Кардио и АСК с защитными агентами в дозировке 75 мг — не отмечалось какого-либо влияния на этот этап, то применение 150 мг АСК с защитными агентами приводило к достоверному снижению количества лиц, имеющих дезагрегацию (р < 0,01).
Таким образом, показан хороший антитромбоцитарный эффект исследуемого препарата Ацекор Кардио, не уступающий, а в определенных моментах и превосходящий таковой референтных препаратов АСК с защитными агентами в двух дозировках.
Оценка переносимости и безопасности исследуемых препаратов
В анализ переносимости включали всех пациентов, принимавших препарат хотя бы один раз и выбывших из исследования по причине возникновения побочных эффектов или отказа от участия в исследовании. Переносимость препарата оценивалась на основании субъективных симптомов и ощущений, сообщаемых пациентом, и объективных данных, полученных исследователем в процессе лечения. Учитывалась динамика лабораторных показателей, эндоскопических показателей, а также частота возникновения и характер побочных реакций.
Побочные реакции, наблюдаемые пациентом и/или врачом в процессе исследования, включая также явления, не имеющие прямой связи с исследуемым препаратом, были проанализированы и зарегистрированы в истории болезни и индивидуальной регистрационной форме с указанием характера, степени тяжести, описания мероприятий, которые потребовались для их ликвидации.
Полученные результаты
Из 150 больных, включенных в клиническое исследование, его завершили 146 человек. Четыре пациента досрочно прекратили исследование по причине возникновения побочных эффектов: по 1 пациенту в группах 75 мг АСК с защитными агентами (головные боли) и препарата Ацекор Кардио (носовое кровотечение) и 2 больных, принимавших 150 мг АСК с защитными агентами (пекущие боли в эпигастрии).
В данном исследовании после приема пациентами с ИБС препаратов ацетилсалициловой кислоты зарегистрированы 72 нежелательных явления у 59 (39,3 %) чел.
В целом переносимость препаратов как хорошую (отсутствие каких-либо побочных эффектов) отметили 31 (63,3 %) больной, принимавший АСК с защитными агентами в дозе 75 мг, и 28 (58,3 %) пациентов, получавших АСК с защитными агентами в дозе 150 мг. В группе препарата Ацекор Кардио хорошая переносимость наблюдалась у 32 (65,3 %) чел. У 18 (36,0 %) лиц, получавших АСК с защитными агентами в дозе 75 мг, и у 20 (40,0 %) пациентов, принимавших АСК с защитными агентами в дозе 150 мг, наблюдались незначительные побочные эффекты, не доставляющие серьезных проблем и не требующие отмены препарата. В группе препарата Ацекор Кардио таких больных было 17 (34,0 %). Неудовлетворительная переносимость, требующая отмены препарата, зарегистрирована у 1 (2 %) пациента, принимавшего 75 мг АСК с защитными агентами, у 1 (2 %) — Ацекор Кардио и у 2 (4 %) больных из группы 150 мг АСК с защитными агентами.
Все зарегистрированные случаи побочных реакций/побочных явлений были несерьезными, легкой степени тяжести и не требовали проведения терапии и/или каких-либо действий. Общих и местных аллергических реакций не наблюдалось. Ухудшения функционального состояния сердца, печени, почек в процессе исследования не выявлено. Ухудшения состава периферической крови и мочи не обнаружено ни у одного больного.
У 1 (2,0 %) пациента, получавшего Ацекор Кардио, произошло носовое кровотечение, ставшее причиной выбывания из исследования. У 1 (2,0 %) больного из группы АСК с защитными агентами в дозировке 75 мг после приема препарата возникла интенсивная головная боль, из-за чего пациент отказался от дальнейшего участия в исследовании.
В основном побочные реакции наблюдались со стороны желудочно-кишечного тракта. За время приема исследуемых препаратов наиболее часто у обследуемых пациентов отмечались абдоминальная боль, диспептические расстройства.
Клинические проявления побочных реакций у обследованных пациентов представлены в табл. 9.
Как видно из представленной табл. 9, клинические симптомы гастропатии реже фиксировались у больных, принимавших АСК с защитными агентами 75 мг и Ацекор Кардио, чем у получавших АСК с защитными агентами 150 мг. Существенных различий между группами пациентов, принимавших АСК с защитными агентами в дозе 75 мг и Ацекор Кардио, выявлено не было. Так, при назначении АСК с защитными агентами в дозе 75 мг абдоминальную боль различной интенсивности испытывали 6 (12,2 %) больных, в группе пациентов, принимавших 150 мг, абдоминальная боль наблюдалась в 9 (18,8 %) случаях. В группе пациентов, которые получали Ацекор Кардио, на боль в эпигастрии жаловались 5 (10,2 %) чел., причем интенсивную пекущую, в том числе ночную, боль испытывали всего 2 (4,1 %), что меньше по сравнению с группой пациентов, принимавших 150 мг АСК с защитными агентами. Изжога возникала на фоне приема 75 мг АСК с защитными агентами несколько чаще, чем в группе препарата Ацекор Кардио. Так, у пациентов, принимавших АСК с защитными агентами в дозе 75 мг, изжога наблюдалась в 9 (18,4 %) случаях, при приеме дозы 150 мг — в 12 (25,0 %). В группе препарата Ацекор Кардио только 6 (12,2 %) пациентов жаловались на изжогу. Другие диспептические явления наблюдались у 6 (12,2 %) больных, принимавших АСК с защитными агентами в дозе 75 мг, и у 4 (8,3 %) — АСК с защитными агентами в дозировке 150 мг. В группе пациентов, получавших Ацекор Кардио, диспептические явления отмечены у 5 (10,2 %) человек, т.е. достоверных различий между группами не было. Нарушения стула зарегистрированы у 6 (12,2 %) больных, получавших АСК с защитными агентами в дозе 75 мг, и у 8 (16,7 %) — 150 мг АСК с защитными агентами. В группе препарата Ацекор Кардио нарушения стула зафиксированы у 4 (8,2 %) пациентов.
С целью определения состояния слизистой оболочки ЖКТ на фоне лечения у 45 больных было проведено эндоскопическое исследование верхних отделов ЖКТ. Влияние исследуемых препаратов на слизистую оболочку желудка и двенадцатиперстной кишки оценивалось на основании визуальных данных фиброэзофагогастродуоденоскопии (ФЭГДС) после четырехнедельной терапии, включавшей препарат АСК.
Суммарная частота гастроинтестинальных осложнений при использовании АСК с защитными агентами в дозе 75 мг составила 40,0 % (6 больных), в дозе 150 мг — 57,1 % (8 чел.), что было больше в сравнении с препаратом Ацекор Кардио — 31,2 % (5 пациентов).
Полученные данные приведены в табл. 10.
Таким образом, во всех обследованных группах наблюдались изменения слизистой оболочки желудка в виде гиперемии, эрозий и геморрагий (табл. 10). На фоне лечения язвы желудка и двенадцатиперстной кишки выявлены не были. Также не зафиксировано таких опасных осложнений со стороны ЖКТ, как кровотечение или перфорация язвы.
Во время проведения ФЭГДС (4-я неделя терапии) в группе пациентов, принимавших АСК с защитными агентами в дозе 75 мг, гиперемия слизистой оболочки желудка отмечена в 5 (33,3 %) случаях, при приеме дозы 150 мг — в 6 (42,8 %). Гиперемия двенадцатиперстной кишки наблюдалась у 2 (13,3 %) больных, которым назначили АСК с защитными агентами в дозе 75 мг, и у 2 (14,3 %) — АСК с защитными агентами в дозе 150 мг. В группе препарата Ацекор Кардио явления воспалений слизистой желудка в виде гиперемии наблюдались у 4 (25,0 %) чел., что было меньше по сравнению с группой АСК с защитными агентами в дозировке 150 мг, гиперемия двенадцатиперстной кишки отмечена у 2 (12,5 %) больных. Терапия АСК с защитными агентами в дозах 75 и 150 мг чаще, чем терапия препаратом Ацекор Кардио, приводила к эрозивному повреждению слизистой оболочки желудка и двенадцатиперстной кишки. Так, единичные эрозии желудка выявлены у 2 (13,3 %) пациентов, принимавших АСК с защитными агентами в дозе 75 мг, и у 2 (14,3 %) больных, получавших АСК с защитными агентами в дозировке 150 мг. В группе препарата Ацекор Кардио единичные эрозии желудка отмечены только у 1 (6,2 %) чел., что было реже по сравнению с группой АСК с защитными агентами в дозировке 75 мг. При применении 75 мг АСК с защитными агентами множественные эрозии желудка обнаружены у 3 (20,0 %) больных при приеме суточной дозы 75 мг и у 3 (21,4 %) — при приеме 150 мг. В группе пациентов, принимавших Ацекор Кардио, множественные эрозии желудка выявлены у 2 (12,5 %) пациентов, что было достоверно меньше по сравнению с группой 75 мг АСК с защитными агентами. Достоверных различий в появлении единичных эрозий в двенадцатиперстной кишке на фоне приема АСК с защитными агентами в дозировке 75 мг и препарата Ацекор Кардио не отмечено. Они наблюдались у 2 (13,3 %) больных, принимавших АСК с защитными агентами в дозе 75 мг, у 2 (14,3 %) — в дозе 150 мг и у 2 (12,5 %) пациентов, которые получали Ацекор Кардио. Субэпителиальные геморрагии чаще обнаруживались у лиц, принимавших 75 мг АСК с защитными агентами, — 2 (13,3 %) случая, 150 мг — 2 (14,3 %) случая соответственно, тогда как в группе препарата Ацекор Кардио геморрагии были выявлены у 1 (6,2 %) чел.
Следует отметить, что у 12 больных (26,7 %) повреждения слизистой оболочки желудка наблюдались в отсутствие каких-либо гастроэнтерологических клинических симптомов.
При изучении клинического анализа крови и показателей обмена железа в динамике лечения исследуемыми препаратами существенных различий между группами до и после лечения не наблюдалось.
Таким образом, исследуемый препарат Ацекор Кардио удовлетворительно переносился пациентами с ИБС и имел лучший профиль гастроэнтерологической безопасности по сравнению с АСК с защитными агентами в дозе 75 и 150 мг.
Выводы
1. Кишечнорастворимая форма АСК — лекарственное средство Ацекор Кардио производства ООО «НПФ «Микрохим» (Украина) — оказывает достоверное влияние на параметры тромбоцитарного гемостаза у пациентов со стабильными формами ИБС, по антиагрегантному эффекту не уступает препаратам сравнения с гидроокисью магния, а в определенных моментах и превосходит их.
2. Таблетки Ацекор Кардио хорошо переносятся пациентами с ИБС, не вызывают патологических изменений лабораторных показателей биологических сред организма и имеют лучший профиль гастроэнтерологической безопасности по сравнению с АСК с защитными агентами в дозе 75 и 150 мг.
3. Результаты исследования свидетельствовали об оптимальном соотношении эффективности и безопасности препарата Ацекор Кардио в дозе 100 мг.
Список литературы
Список литературы находится в редакции

/15_u.jpg)
/15_u2.jpg)
/16_u.jpg)
/16_u3.jpg)
/16_u2.jpg)
/16_u4.jpg)
/17_u.jpg)
/17_u2.jpg)
/17_u3.jpg)
/18_u.jpg)
/18_u2.jpg)