Газета «Новости медицины и фармации» 11 (585) 2016
Вернуться к номеру
Противовирусная и антибактериальная терапия в лечении внебольничных пневмоний
Авторы: Лоскутов О.А., Дружина А.Н. - Кафедра анестезиологии и интенсивной терапии НМАПО имени П.Л. Шупика, г. Киев, Украина; ГУ «Институт сердца МЗ Украины», г. Киев, Украина; Колесников В.Г. - Кафедра анестезиологии и интенсивной терапии НМАПО имени П.Л. Шупика, г. Киев, Украина
Рубрики: Пульмонология
Разделы: Справочник специалиста
Версия для печати
Статья опубликована на с. 16-17 (Мир)
Введение
Более 100 лет назад Уильям Ослер отметил, что «пневмония остается… самым серьезным острым заболеванием, с которым врачи имеют дело» [1].
И в настоящее время пневмония является основной причиной летальности среди всех инфекционных осложнений во всех возрастных группах и шестой ведущей причиной смерти у подобной категории больных старше 65 лет [2].
А если учесть, что к 2050 году 20 % населения земного шара будет старше 65 лет [3], то роль пневмонии, связанной с летальностью у пожилых пациентов, приобретает особое значение.
R. Lozano и соавт. в рамках исследования Global Burden of Disease Study сообщают, что инфекции нижних дыхательных путей, включая пневмонию, являются четвертой наиболее распространенной причиной смерти во всем мире, уступая лишь ишемической болезни сердца, стенокардии и хронической обструктивной болезни легких, и второй по частоте причиной потерянных лет жизни [4].
По оценкам Всемирной организации здравоохранения, инфекция нижних дыхательных путей является причиной смерти у 3,5 млн человек ежегодно [5].
В Соединенных Штатах среди инфекционных заболеваний пневмония является основной причиной госпитализации, а медицинские расходы на лечение данной патологии в 2011 г. превысили $ 10 млрд [6].
Этиопатогенез внебольничных пневмоний
С каждым годом клинические проявления пневмонии и этиологические факторы ее возникновения изменяются и становятся более разнообразными и сложными.
Так, в 1977 году этиология внебольничных пневмоний состояла в основном из атипичной пневмонии, аспирационной пневмонии и классических бактериальных пневмоний, вызванных Streptococcus pneumoniae, Haemophilus influenzae, реже Moraxella catarrhalis, Staphylococcus aureus, Streptococcal species и Enterobacteriaecae [7].
В настоящее время особое место начинают занимать пневмонии, связанные с ослаблением иммунитета (у пациентов с ВИЧ/СПИДом), пневмонии у пациентов со злокачественными опухолями на фоне приема цитостатической терапии [7].
Кроме того, появление тяжелого острого респираторного дистресс-синдрома (ОРДС), вызванного вирусом птичьего гриппа А (H5N1), и пандемия гриппа А в 2009 г. (pH1N1) подчеркивают определяющую роль вирусной этиологии внебольничных пневмоний [8].
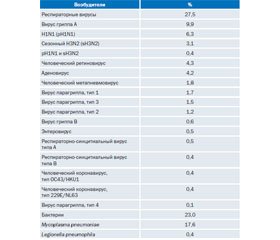
В многоцентровом проспективном исследовании, проведенном Jiu-Xin Qu и соавт., приводится верификация внебольничных пневмоний 2010–2012 гг. (табл. 1) [8].
Согласно данным Andrew T. Pavia, респираторные вирусы обнаруживались в 45–75 % случаев у детей и в 15–54 % случаев — у взрослых, госпитализированных с внебольничной пневмонией [9]. Коинфекция вирусов и бактерий верифицировалась в 22–33 % посевов у детей и в 4–30 % случаев у взрослых [9].
В конце 2009 — начале 2010 г. ведущей инфекционной причиной ОРДС были пневмонии, вызванные вирусом гриппа А(H1N1). В течение недели, с 27 сентября по 3 октября 2009 г., в общей сложности 28 национальных центров гриппа сообщили в ВОЗ о 6378 случаях выявления вируса гриппа [10]. Из этого числа 6250 (98 %) были вирусами гриппа А и 128 (2 %) — вирусами гриппа В. В 1785 случаях (29 %) подтип вируса гриппа А не определялся [10].
Из тех вирусов гриппа А, подтип которых определялся, 4012 (89,5 %) были вирусами пандемии человеческого гриппа А(H1N1), 59 (1,3 %) были вирусами сезонного гриппа А и 394 (8,8 %) — вирусами гриппа А(Н3) [11].
По состоянию на 11 октября 2009 г. в мире было зарегистрировано свыше 399 000 лабораторно подтвержденных случаев пандемического гриппа А(H1N1), большинство из которых имели легкое течение с обычными симптомами острой респираторной вирусной инфекции [12]. Однако регистрировались и тяжелые случаи заболевания, сопровождавшиеся летальными исходами [13].
По сообщениям Американского центра по оценке, контролю и профилактике заболеваний (US Centers for Disease Control and Prevention estimated), с апреля 2009 по 10 апреля 2010 г. было зарегистрировано 12 470 смертельных случаев, вызванных гриппом А(H1N1) [14].
В Украине с 29.10.2009 по 28.03.2010 г. общее количество заболевших гриппом и острыми респираторными заболеваниями с начала эпидемии гриппа составило 6,2 млн человек [15]. При этом на 28.03.2010 г. количество фатальных случаев гриппа и острых респираторных инфекций достигло 1127 [15].
Наибольшее число жертв было зафиксировано в Донецкой, Львовской, Харьковской, Днепропетровской областях и г. Киеве [15]. За все время эпидемии гриппа А(H1N1) 2009 г. в Украине около 65 тысяч медработников переболели этой инфекцией, а 68 из них умерли [15].
Большинство случаев смерти было обусловлено манифестацией вирусной пневмонии, а в 50–80 % случаев прогрессирующая легочная дисфункция была зарегистрирована у пациентов с такими сопутствующими состояниями, как хронические заболевания легких (включая бронхиальную астму), сердечно-сосудистые заболевания, диабет и иммунодепрессия [16].
Кроме того, тяжелое течение заболевания и летальный исход имели место у беременных женщин в третьем триместре и у лиц с ожирением [17].
Лишь в небольшой части обширной научной литературы, посвященной гриппу А(H1N1), анализируются патологоанатомические находки. При этом авторы подобных работ приходят к выводу, что по показателю летальности грипп А(H1N1) существенно менее агрессивен, чем грипп 1918 г., но опаснее гриппа других пандемий двадцатого столетия [18].
Трудности в лечении тяжелых случаев гриппа А(H1N1) и нередко безуспешность мероприятий интенсивной терапии привлекают особое внимание лечащих врачей к патологоанатомическим и патоморфологическим исследованиям этого заболевания.
Исследователи из США (Нью-Йорк), проводя клинико-анатомический анализ группы умерших от гриппа А(H1N1) (34 случая), выявили среди факторов, предрасполагающих к более тяжелому течению болезни, такие как наличие ожирения — у 72 % умерших пациентов, кардиореспираторные заболевания и иммунодепрессия — у 91 % погибших [19].
О.В. Зайратьянц и соавт. в своих работах отмечают, что среди фоновых и сопутствующих заболеваний в группе с летальным исходом в г. Москве наиболее часто встречалось ожирение 2–4-й ст. (43 %), алкоголизм (35 %), а также вторичный иммунодефицит (5 %), беременность (5 %), сахарный диабет 2-го типа (5 %) и гипертоническая болезнь (5 %) [20].
При этом патоморфологические изменения легких, согласно описаниям, приведенным в различных публикациях, представляли собой следующее [18–20]:
- легкие увеличены в размерах, тяжелые, вишнево-синюшного цвета (геморрагическая индурация легких), безвоздушны;
- в бронхах всех калибров отмечались десквамативные изменения;
- на разрезе отмечалась резкая гиперемия, сетчатость, подплевральные геморрагические инфаркты;
- микроскопически обнаруживалось диффузное повреждение альвеол с десквамацией альвеолярного эпителия и формированием гиалиновых мембран, что является морфологической картиной ОРДС;
- на внутренних стенках бронхиол определялись фибриновые гомогенные массы — гиалиновые мембраны.
Причина гибели альвеолярного эпителия, очевидно, вирусы, попадающие в альвеолы из воздухоносных путей. В частности, J. Guarner и соавт., проводя иммуногистохимические исследования легочной ткани больных, умерших от пневмонии вирусной этиологии, показали, что вирус гриппа А(H1N1) поражает не только эпителий верхнего респираторного тракта, бронхов и бронхиол, но и альвеолярный эпителий и альвеолярные макрофаги с развитием диффузного альвеолярного поражения, тогда как сезонный грипп повреждает альвеолярный эпителий в значительно меньшей степени [21].
Появление на стенках альвеол гиалиновых мембран свидетельствует о резком и сильном повышении проницаемости капилляров, расположенных в межальвеолярных перегородках. У погибших встречались также интерстициальные макрофагально-лимфоцитарные инфильтраты, свойственные интерстициальной вирусной пневмонии [22, 23], очаги серозно-геморрагического экссудата в альвеолах и бронхиолах как проявление вирусной бронхопневмонии или микроскопические признаки бактериальной инфекции [19].
Изучение публикаций, посвященных патоморфологии гриппа А(H1N1), показало, что внимание исследователей концентрируется в основном на гистологической картине альвеол и альвеолярного эпителия. При этом развитие повышенной проницаемости капилляров межальвеолярных перегородок связывают преимущественно с гипоксическим и токсическим повреждением эндотелия, хотя прямое вирусное повреждение эндотелиоцитов при гриппе — известный факт.
В работе О.В. Зайратьянца и соавт. [20] высказано мнение, что диффузное повреждение альвеол в сочетании с цитотоксическим действием вируса на эпителий трахеи, бронхов, альвеол, а также эндотелий сосудов является ведущим звеном в патогенезе вирусного поражения А(H1N1), с последующим развитием шока в результате децентрализации кровотока, скоплением крови в микроциркуляторном русле, развитием ДВС-синдрома.
Как показала эпидемия гриппа сезона 2009–2010 гг., вирус А(Н1N1) относится к инфекциям, которые нередко могут принимать тяжелое течение и требовать проведения интенсивной терапии. К сожалению, все еще бытует мнение о том, что интенсивная терапия — это прежде всего большое количество препаратов, назначаемых больному.
Однако, как подчеркивал профессор А.И. Трещинский, суть интенсивной терапии определяется прежде всего своевременным выявлением ведущих нарушений функций органов и систем, которые требуют коррекции. По его мнению, проведение этой коррекции всегда должно осуществляться с помощью минимального количества медикаментозных препаратов и различных методик интенсивной терапии.
Проведение антивирусной терапии следует начинать на раннем этапе заболевания, основываясь на клинической картине течения болезни, не дожидаясь лабораторного подтверждения гриппа, т.к. разброс чувствительности к экспресс-тестам может составлять от 10 до 70 %.
У больных гриппом А(H1N1) существует прямая корреляция между началом специфической антивирусной терапии и количеством, а также тяжестью осложнений.
Наименьшее количество осложнений отмечается у пациентов, которым антивирусная терапия начата в течение первых 48 часов от начала заболевания [8]. Однако следует отметить, что антивирусную терапию можно использовать на любой активной стадии заболевания, когда предполагается или документально подтверждена возможность репликации текущей вирусной инфекции.
В некоторых случаях репликация вируса возможна в течение продолжительного времени вследствие предшествующего нарушения иммунитета. Такие пациенты нуждаются в более длительном приеме антивирусных препаратов.
Противовирусная и антибактериальная терапия
Ингибиторы нейраминидазы являются одними из основных препаратов для лечения вирусных пневмоний и гриппоподобных заболеваний как у взрослых, так и у детей [8, 24].
Препараты данной группы высокоселективно ингибируют нейраминидазу — поверхностный фермент вируса гриппа, в т.ч. все известные подтипы нейраминидазы вируса гриппа А, блокируя репликацию вирусов гриппа А и В, препятствуют высвобождению новых вирусных частиц из инфицированных клеток, взаимодействию вирусов с поверхностью эпителиальных клеток дыхательных путей и их инфицированию [24, 25].
Как подчеркивает в своих публикациях Andrew T. Pavia, ингибиторы нейраминидазы снижают процент возможных осложнений и смертности среди пациентов, госпитализированных с гриппом, в том числе и с пневмонией, и должны быть использованы даже при подозрении на грипп [9].
В других исследованиях указывается, что у пациентов с лабораторно подтвержденной гриппозной инфекцией назначение осельтамивира по сравнению с плацебо значительно уменьшало продолжительность заболевания — на 25–32 % и снижало тяжесть клинических проявлений болезни в среднем на 18–38 % [26].
В то же время в исследованиях Barbara Michiels и соавт. указывается, что использование ингибиторов нейраминидазы не оказывало какого-либо значимого влияния на развитие осложнений у подобного контингента больных [25]. Однако авторы данной работы отмечают, что «…занамивир и озельтамивир эффективны в качестве профилактического средства у пациентов с лабораторно подтвержденным сезонным гриппом и гриппом А(H1N1) независимо от модальности использования (до контакта или после контакта)» [25].
В работе T. Jefferson и соавт. подчеркивается, что при использовании ингибиторов нейраминидазы не наблюдалось улучшения клинических результатов, но их профилактическое применение снижало риск развития симптоматики гриппа [27]. В этой же работе авторы делают вывод, что при принятии решения об использовании ингибиторов нейраминидазы для профилактики или лечения гриппа и его осложнений следует найти баланс между пользой и возможным вредом, который может возникнуть при использовании данных препаратов [27].
Важным компонентом в комплексном лечении больных с гриппозной пневмонией, осложненной бактериальной инфекцией, является своевременное назначение адекватной антибактериальной терапии.
Американскими исследователями было проведено тщательное патоморфологическое обследование образцов легочной ткани, взятых у 77 умерших с подтвержденным диагнозом гриппа А(H1N1), с использованием наиболее современных методов выявления возбудителей [28]. В результате бактериальные возбудители, которые могли вызывать очаги пневмонии, были выявлены только у 22 пациентов, что составляло 29 % [28]. По данным других исследований, у больных с фатальным течением гриппа А(H1N1) частота сопутствующей бактериальной инфекции составляла от 26 до 38 % [29].
Среди наиболее часто регистрируемых бактерий отмечались Strept.рneumoniae и S.аureus (включая в некоторых случаях штаммы, устойчивые к метициллину), St.рyogenes, St.mitis и Haemophilus influenzaе [30].
Таким образом, проведение ранней эмпирической антимикробной терапии целесообразно у больных с признаками вирусного поражения легких при наличии у них сопутствующих гнойно-воспалительных процессов, таких как:
- воспаление нижних дыхательных путей;
- гнойный тонзиллит;
- затылочная лимфаденопатия или лимфаденит;
- гнойный отит;
- синусит;
- хронические обструктивные заболевания легких;
- бронхиальная астма.
Рекомендовано назначение антибактериальных препаратов при сопутствующей кардиальной патологии:
- после протезирования клапана(-ов) сердца и больным с перенесенным инфекционным эндокардитом;
- при наличии сложного цианотического врожденного порока сердца (напр.: общий желудочек, транспозиция магистральных сосудов, тетрада Фалло и т.д.);
- больным, имеющим искусственный аорто-легочный шунт или кондуит;
- больным с врожденной клапанной патологией (особенно пациентам, имеющим двухстворчатый аортальный клапан) и больным с приобретенной клапанной дисфункцией (напр., ревмокардит);
- пациентам, перенесшим пластику клапана(-ов) сердца;
- пациентам с гипертрофической кардиомиопатией;
- больным с гемодинамически значимым пролапсом митрального клапана и утолщением клапанной створки (по данным эхокардиографии).
Проведение ранней эмпирической антибактериальной терапии также целесообразно при следующих состояниях:
- заболевания с нарушением нейромышечной проводимости;
- больным с иммуносупрессией;
- с хронической почечной недостаточностью;
- с хронической печеночной недостаточностью;
- с сахарным диабетом;
- ослабленным, часто болеющим пациентам, а также больным, принимающим глюкокортикоиды;
- при ухудшении клинической симптоматики на фоне проводимой терапии (возобновляющаяся лихорадка, нарастание острой дыхательной недостаточности и т.д.) [31, 32].
Проводить антибактериальную терапию у подобного контингента больных нужно с учетом следующих основных положений:
- у пациентов с подозрением на внебольничную пневмонию антибактериальную терапию следует начинать как можно раньше после взятия соответствующих образцов материала для посева и верификации возбудителя [33];
- в настоящее время практические рекомендации Американского общества инфекционных болезней и Американского торакального общества (IDSA-АТС) не определяют четкое время для начала антибактериальной терапии, но отмечают, что она должна быть назначена сразу после установления диагноза. Исключение сделано для пациентов, находящихся в состоянии септического шока, когда антибиотики должны быть назначены в течение первого часа после начала гипотензии [34]. Исследование, проведенное A. Kumar и соавт., показало, что выживаемость у пациентов с септическим шоком снижается каждый час на 8 % при промедлении в назначении антибактериальной терапии [35];
- рекомендуемая схема антибактериальной терапии представляет собой комбинацию из β-лактамного антибиотика (амоксициллин/клавуланат или ампициллин/сульбактам) в сочетании с антибиотиком макролидового ряда (как альтернативу β-лактамным антибиотикам можно использовать цефподоксим и цефуроксим) [34];
- в случаях непереносимости β-лактамного антибиотика предпочтительно назначение антибиотика фторхинолонового ряда (моксифлоксацин в дозе 400 мг в сутки или левофлоксацин 750 мг в сутки) [33, 36];
- решение о способе введения антибиотика (перорально или парентерально) должно приниматься, исходя из клинического состояния пациента;
- критериями достаточности антибактериальной терапии следует считать:
аксиллярную температуру тела < 37,5 °С (не менее чем в двух последовательных измерениях с интервалом 8 ч);
снижение индекса интоксикации;
снижение степени выраженности дыхательной недостаточности;
повышение оксигенации крови и респираторного индекса (PaO2/FiO2);
уменьшение количества мокроты и изменение ее характера;
снижение количества бактерий в мокроте или аспирате трахеи;
отсутствие в мокроте или аспирате трахеи новых микроорганизмов;
отсутствие отрицательной динамики на рентгенограмме (отсутствие поражения новых долей легких, уменьшение размеров инфильтрата, отсутствие новых очагов деструкции, уменьшение или отсутствие плеврального выпота);
положительную динамику развернутой клинической картины крови (количество лейкоцитов в развернутом клиническом анализе крови менее 10 • 109/л, нейтрофилов < 80 %, юных форм < 6 %);
снижение уровня С-реактивного белка и прокальцитонина на 90 % по сравнению с исходным значением;
- при контрольных ЭхоКГ-исследованиях — отсутствие вегетаций на клапанах сердца;
- если отсутствует положительная клиническая динамика при проведении антибактериальной терапии в течение 48–72 ч, необходимо провести исследования на выявление атипичных возбудителей, лекарственной устойчивости и т.д.;
- хотя в настоящее время отсутствуют достоверные свидетельства того, что комбинированная антибактериальная терапия превосходит монотерапию, все же лечение рекомендуется начинать, используя комбинацию антибиотиков;
- в случае верификации возбудителя и/или улучшения клинического состояния пациента антибактериальную терапию следует продолжать в течение последующих 7 дней с дальнейшей оценкой посевов и клинического состояния;
- у пациентов с сохраняющимся индексом тяжести состояния по MODS > 13 баллов или SOFA > 5 баллов курс терапии антибиотиками продлевается до 10 дней, при этом к проводимой терапии целесообразно добавление препарата из класса гликопептидов (ванкомицин, тейкопланин) [31];
- в случаях неэффективности начальной эмпирической антибиотикотерапии и верификации штаммов MRSA или при выявлении мультирезистентной грамотрицательной флоры курс антибактериальной терапии продлевается до 14–21 дня [31];
- у пациентов со злокачественными заболеваниями крови, иммуносупрессией или нейтропенией при продлении курса антибактериальной терапии (более 5 дней) и/или верификации грибковой флоры целесообразно параллельное назначение антимикозных препаратов (флуконазол или вориконазол). В других случаях антимикотическая терапия назначается, только если течение пневмонии осложняется инвазивными микозами.
Заключение
Таким образом, важным компонентом в комплексном лечении больных с гриппозной пневмонией, осложненной бактериальной инфекцией, является своевременное назначение адекватной антивирусной и антибактериальной терапии.
Противовирусная терапия основана на использовании ингибиторов нейраминидазы, которые являются одними из основных препаратов для лечения вирусных пневмоний и гриппоподобных заболеваний как у взрослых, так и у детей. А проведение ранней эмпирической антимикробной терапии целесообразно у больных с признаками вирусного поражения легких при наличии у них сопутствующих гнойно-воспалительных процессов.
Однако следует отметить, что успех интенсивной терапии подобного контингента больных должен базироваться на комплексном патофизиологическом подходе, не ограничиваться только антивирусной и антибактериальной терапией, учитывать такие ключевые повреждающие факторы, как нерегулируемая активация комплемента и медиаторов воспаления. Данные положения, с нашей точки зрения, должны стать в настоящее время предметом активного научного изучения и сыграть решающую роль в терапии ОРДС.
Список литературы
Список литературы находится в редакции

/16_m.jpg)