Статтю опубліковано на с. 6-11
Вступ
Рак шийки матки (РШМ) є другим за поширеністю видом раку в жінок. Ризик розвитку раку шийки матки у жінок віком до 65 років коливається від 0,8 % в розвинених країнах до 1,5 % — у країнах, що розвиваються. Щороку спостерігається близько 530 000 нових випадків і 275 000 смертей від РШМ. Близько 85 % цих випадків мають місце в країнах, що розвиваються, у яких програми скринінгу функціонують несистемно. У країнах з ефективними програмами скринінгу відбулося різке скорочення захворюваності й зменшення стадії, на якій діагностується рак [1, 2].
Досвід країн, що досягли успіхів у боротьбі з раком шийки матки, переконливо демонструє, що найбільш потужним і ефективним інструментом є цервікальний скринінг. Саме шляхом запровадження обов’язкових скринінгових програм вдасться взяти під нагляд усіх жінок із групи ризику (або більшу їх частину), своєчасно діагностувати передракові захворювання і, відповідно, запобігти РШМ [3].
Розвиток раку шийки матки є багатоступінчастим процесом, оскільки спочатку клітини епітелію шийки матки зазнають змін і стають аномальними. Ці відхилення називаються дисплазією, і вони пов’язані з підвищеним ризиком подальшого розвитку інвазивного раку шийки матки [1].
Дисплазія є найбільш поширеною передраковою патологією з атиповими змінами плоских клітин шийки матки в зоні трансформації. Якщо дисплазія прогресує, вона трансформується в плоскоклітинний рак [4].
Для опису результатів цитологічного дослідження сьогодні використовують загальноприйняту Бетесдинську класифікацію (Bethesda system), розроблену в 1998 році Національним інститутом раку США. З того часу класифікацію неодноразово переглядали та доопрацьовували, востаннє — у 2001 році. Саме в останній версії її сьогодні застосовують у всьому світі.
Класифікація дозволяє віднести цитологічний мазок до одного з трьох варіантів:
— нормальний (без патологічних змін);
— невизначений (ASCUS, що не є нормальним, але не дозволяє точно судити про характер ураження);
— плоскоклітинне інтраепітеліальне ураження низького (low grade squamous intraepithelial lesions, LSIL) або високого (high grade squamous intraepithelial lesions, HSIL) ступеня тяжкості.
Слід звернути увагу, що дуже часто вітчизняні цитологи використовують класифікацію цервікальних інтраепітеліальних неоплазій (cervical intraepithelial neoplasia — СIN), розроблену в 1968 році. Однак це не зовсім правильно: CIN-класифікація призначена для гістологічного, а не для цитологічного висновку. Крім того, широко застосовують у практиці класифікацію дисплазій епітелію шийки матки [5].
Існують ексцизійні й аблятивні методи лікування дисплазії епітелію шийки матки (ДЕШМ). Конізація й петльова ексцизія є ефективними варіантами для лікування дисплазії тяжкого ступеня, але вони вимагають наявності висококваліфікованого персоналу, дорогі та можуть привести до порушення репродуктивної функції. Отже, більш консервативні аблятивні методи можуть бути кращими для молодих пацієнток фертильного віку, тому що дозволяють забезпечити, з одного боку, надійність та радикальність лікування, а з іншого — є найбільш щадними для пацієнток, які не народжували. Раціонально також їх використовувати в умовах обмежених ресурсів. Аблятивні методи, у тому числі кріотерапія, лазерна абляція, як правило, використовуються для лікування дисплазії легкого та середнього ступеня й можуть бути виконані в амбулаторних умовах [6].
Відповідно до рекомендацій ASCCP (2012), при виявленні HSIL (за винятком вагітних і жінок віком до 24 років) кращою тактикою є невідкладна (під час того ж прийому, на який пацієнтка прийшла з метою дізнатися результати цитологічного дослідження) петльова електрохірургічна ексцизія ураженої ділянки з наступним гістологічним дослідженням матеріалу [7].
Необхідність процедури обумовлена високим ризиком CIN III/carcinoma in situ та цервікального раку в жінок із HSIL, старших за 30 років: 50 і 7 % відповідно протягом 5 років при позитивному результаті тесту на вірус папіломи людини, 29 і 7 % — при негативному [8].
Ексцизійні методи тісно пов’язані зі збільшення ризику акушерських ускладнень, таких як передчасні пологи, передчасний розрив оболонок, низька маса тіла при народженні й кесарів розтин. Хоча показник ефективності консервативного лікування дисплазії перевищує 95 %, у пацієнток після застосування даних методів відмічається значна кількість рецидивів [9].
При виборі між двома цими видами лікування важливо враховувати ситуації, у яких показана виключно конізація шийки матки й категорично протипоказана абляція:
— незадовільні результати кольпоскопії при персистуючій CIN I;
— ураження ендоцервіксу CIN будь-якого ступеня тяжкості;
— пацієнтка вже отримувала лікування раніше.
У жінок із CIN II–III спостереження неприйнятне, оптимальною тактикою є лікування за допомогою ексцизії або абляції (допустима при CIN II, але неприйнятна при CIN III) за умови задовільних результатів кольпоскопії. При неможливості візуалізувати зону трансформації, а також у жінок із рецидивом CIN II–III або ураженням ендоцервіксу показана конізація [7].
Кріохірургія є руйнівним (абляційним) методом, що був упроваджений у гінекологію в кінці 1960-х років для лікування дисплазії епітелію шийки матки. Десятки тисяч пацієнток пройшли лікування кріотерапією, яка виявилася передбачуваною, надійною технікою лікування з мінімумом побічних ефектів і ускладнень. Кріохірургія є безпечною, недорогою та нескладною процедурою лікування передракових захворювань нижніх відділів статевих шляхів без погіршення фертильності пацієнток [10].
Кріотерапія знищує ектоцервікс шляхом заморожування за допомогою стиснутого газоподібного холодоагенту. Цей метод демонструє високі показники ефективності лікування в усіх регіонах світу (94 % для CIN І, 92 % для CIN ІІ і 85 % для CIN ІІІ) [6].
Загоєння рани відбувається шляхом формування під зоною кріонекрозу ексудату, що змінюється фібриноїдним некрозом і шаром незрілої грануляційної тканини. Зовнішні шари поступово відділяються, залишаючи на поверхні грануляції, вкриті фіброцитами або сполучною тканиною. Потім на поверхні розвиваються незрілі клітини плоского епітелію та резервні клітини підлеглого циліндричного епітелію. У процесі загоєння рани синтезується колаген III типу, що першим знаходиться в стромі, а згодом перетворюється на колаген I типу. Після цього повністю формується нормальний плоскоклітинний шар епітелію [11].
Перманентна дія стресових факторів, несприятлива екологічна ситуація та напружений радіаційний фон, що склався після Чорнобильської катастрофи, знижують здатність жіночого організму до повноцінної самостійної репарації уражених чи зруйнованих клітин слизової оболонки шийки матки. Це вимагає від лікарів постійного пошуку засобів, що допомагають покращити регенеративну здатність ектоцервіксу для успішного лікування передракової цервікальної патології.
Одним із таких засобів є вагінальний гель Інтінова — біологічна добавка, що сприятливо впливає на стан статевих органів за рахунок природних компонентів, які входять до її складу.
Екстракт алое має регенеративні властивості, сприяє підвищенню пружності м’язів піхви, а також забезпечує зволоження, усунення сухості піхви та пов’язаних з нею симптомів (свербіж, подразнення, дискомфорт). Екстракт алое також має протизапальні, антибактеріальні й протигрибкові властивості.
Екстракт мигдалю містить велику кількість біологічно активних речовин: поліненасичені жирні кислоти, вітаміни А, Е, групи В, Н, РР, мікроелементи, амінокислоти, за рахунок чого покращує живлення тканин піхви, кровообіг статевих органів жінки, стимулює вироблення ендогенного колагену, сприяє підвищенню еластичності й зміцненню тканин.
Екстракт гамамелісу містить дубильні речовини, за рахунок чого чинить в’яжучий й судинозміцнюючий вплив. Рослина тонізує м’язи піхви й ущільнює її слизову оболонку. Відзначаючись антимікробною, противірусною й фунгіцидною фармакологічною дією, гамамеліс є профілактичним компонентом засобу Інтінова, що запобігає виникненню вагінальних інфекцій.
Екстракт пуерарії є фітоестрогеном, що сприяє відновленню слизової оболонки піхви, підвищенню синтетичних процесів у клітинах, посиленню циркуляції крові.
Екстракт женьшеню має біостимулюючі, імуностимулюючі й адаптогенні властивості. Женьшень є ефективним тонізуючим засобом, підвищує кровообіг у статевих органах.
Екстракт гранатового дерева чинить антиоксидантний і репаративний фармакологічний вплив, стимулює синтез білків, еластину й колагену в слизовій оболонці піхви. Ця рослина перешкоджає коливанням рН і виникненню дисбактеріозу піхви.
Гіалуронова кислота, як полісахарид, сприяє зволоженню піхви та репарації слизової оболонки. Також даний компонент гелю Інтінова покриває слизову оболонку піхви, захищаючи її від негативного впливу екзогенних факторів
Отже, завдяки наявності у складі препарату великої кількості біологічно активних речовин природного походження (і їх високій терапевтичній концентрації порівняно з іншими лікарськими засобами) гель Інтінова зволожує, відновлює слизову оболонку піхви, сприяє підвищенню її тонусу й еластичності, забезпечує її захист від патогенної флори.
Метою нашого дослідження було визначити ефективність застосування вагінального гелю Інтінова щодо покращення репаративно-регенеративних процесів у слизовій оболонці шийки матки після кріодеструкції.
Матеріали й методи
У дослідженні брали участь 70 жінок, які перебували під спостереженням у Київському міському центрі репродуктивної та перинатальної медицини.
Критерії включення в дослідження: відсутність вагітності, вік від 18 до 45 років, стан після кріотерапії дисплазії епітелію шийки матки, відсутність тяжкої соматичної патології.
Перед включенням у дослідження жінки були обстежені на наявність інфекцій, що передаються статевим шляхом, пройшли відповідне етіотропне лікування при визначенні запальних процесів, після чого всім жінкам була проведена кріодеструкція шийки матки.
Дисплазія епітелію шийки матки легкого та середнього ступеня тяжкості була виявлена кольпоскопічно й підтверджена цитологічним та гістологічним методом. Кольпоцервікоскопію проводили із застосуванням діагностичного розчину (3% acіdi acetici) та проби Шиллера. Цитологічні препарати забарвлювали за методиками Папаніколау, Паппенгейма, Романовського — Гімзи.
Усі жінки, які брали участь в дослідженні, були розподілені на дві рівноцінні групи методом випадкової вибірки. У результаті було створено 2 групи: І — група спостереження (40 жінок) та ІІ — група контролю (30 пацієнток).
Розподіл жінок у групах відповідно до ступеня тяжкості ДЕШМ був таким. У І групі CIN I визначалася у 28 жінок (70 %), CIN II — у 12 жінок (30 %). У ІІ групі CIN I діагностували в 67,7 % випадків (21 жінка), CIN II — в 32,3 %, тобто у 9 жінок.
Усім жінкам групи спостереження на 14-й день після кріодеструкції була призначена регенеруюча терапія із застосуванням вагінального гелю Інтінова протягом 14 днів.
Пацієнткам групи контролю на 14-й день після кріо-деструкції призначалась відновлювальна місцева терапія згідно з рекомендаціями уніфікованих клінічних протоколів.
Ступінь регенерації ектоцервіксу та ефективність лікування оцінювались кольпоскопічно, бактеріоскопічно та цитологічно кожні 5–7 днів після кріодеструкції. Критерієм успішного вилікування були: кольпоскопічно — вчасна репарація епітелію шийки матки, відсутність деформацій епітелію шийки матки, відсутність запалення судин, цитологічно — нормальне відновлення структури клітин, нормальний вагінальний біоценоз.
Також до показників ефективності лікування входила переносимість призначеної терапії, тобто відсоток токсико-алергічних реакцій на основі об’єктивних та суб’єктивних ознак.
Результати та їх обговорення
Основна кількість хворих — 82,9 % (58 пацієнток) — були віком від 20 до 35 років. Середній вік пацієнток становив 31,50 ± 3,95 року.
Серед обстежуваних жінок лише 22 (31,4 %) мали постійного статевого партнера, а 68,6 % (48 пацієнток) мали від 2 до 7 статевих партнерів в анамнезі.
Клінічний ефект — повна репарація цервікального епітелію виявлений у всіх хворих основної групи (І) та 27 пацієнток (90 %) контрольної групи (ІІ). Решта — 3 (10 %) жінок — потребували повторного курсу лікування до досягнення позитивного результату.
При цьому в основній групі повна регенерація ектоцервіксу відбулась на 3–4-й тиждень лікування, на той час як у жінок контрольної групи ознаки репарації спостерігались на 6–7-й тиждень.
Регенерація відбувається як в епітеліальних, так і в сполучнотканинних шарах слизової оболонки. Ці зміни можна констатувати як цитологічно, так і кольпоскопічно після періоду некрозу протягом перших 3 тижнів.
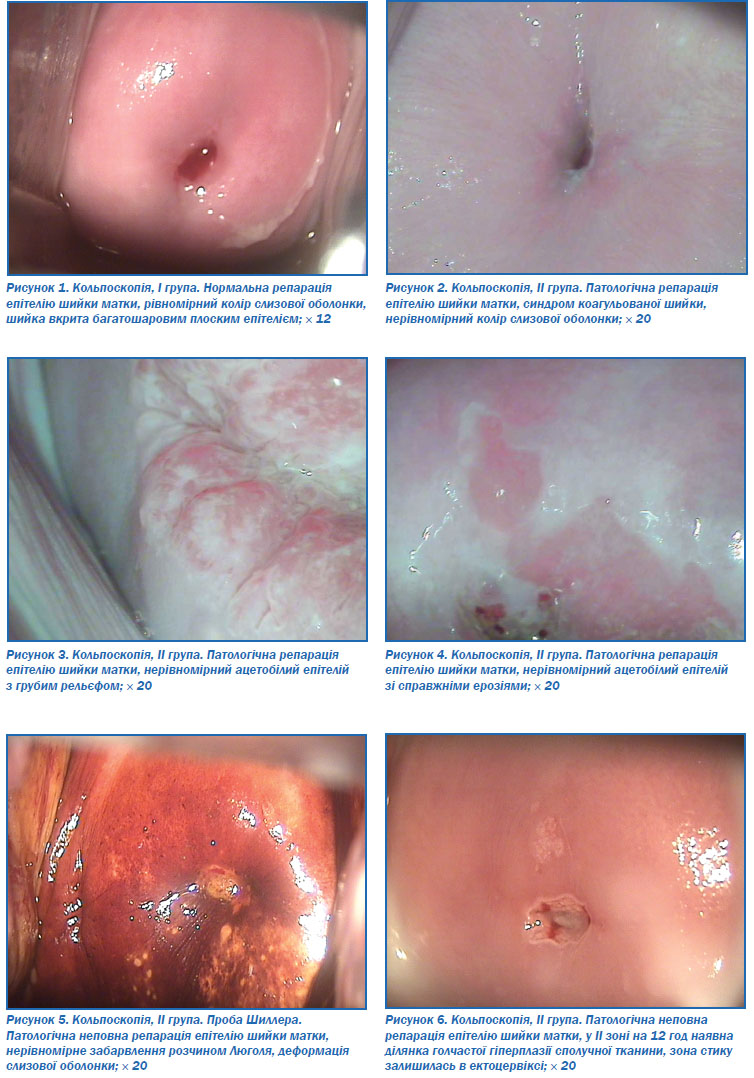
Основними кольпоскопічними критеріями якісної репарації шийки матки були: наявність багатошарового плоского епітелію рівномірної та нормальної товщини, рожевого забарвлення, що свідчить про адекватне гормональне насичення (рис. 1).
До кольпоскопічних ознак неповної, патологічної репарації ектоцервіксу належить: рельєфний, нерівномірний характер слизової оболонки (рис. 3, 5) з вогнищами справжньої ерозії (рис. 4), синдромом коагульованої шийки матки (рис. 2), субепітеліальним ендометріозом, голчастою гіперплазією сполучної тканини (рис. 6).
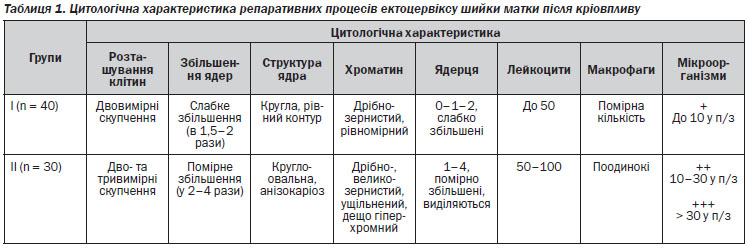
Нормальна цитологічна картина характеризувалась двовимірним розташуванням клітин без нашарування, причому полярність клітин зберігалась. Відзначався помірний ступінь збільшення ядер (у 2–3 рази). Ядра мали рівний округлий чи овальний контур, ядерна мембрана при цьому була цілою, не потовщеною, анізокаріоз слабкий. Хроматин у ядрах дрібнозернистий, рівномірно розташований, дещо ущільнений. Ця ущільненість хроматину обумовлювала слабку гіперхромазію ядра. Ядерця в ядрах помітні, трохи збільшені в розмірах. Цитоплазма вакуолізована. При репарації, як правило, наявна гіперплазія субциліндричних клітин із подальшими метапластичними змінами. У більшості випадків фоном є лейкоцитарний інфільтрат, у якому переважали нейтрофіли й помірна кількість макрофагів. Лімфоїдні елементи відсутні.
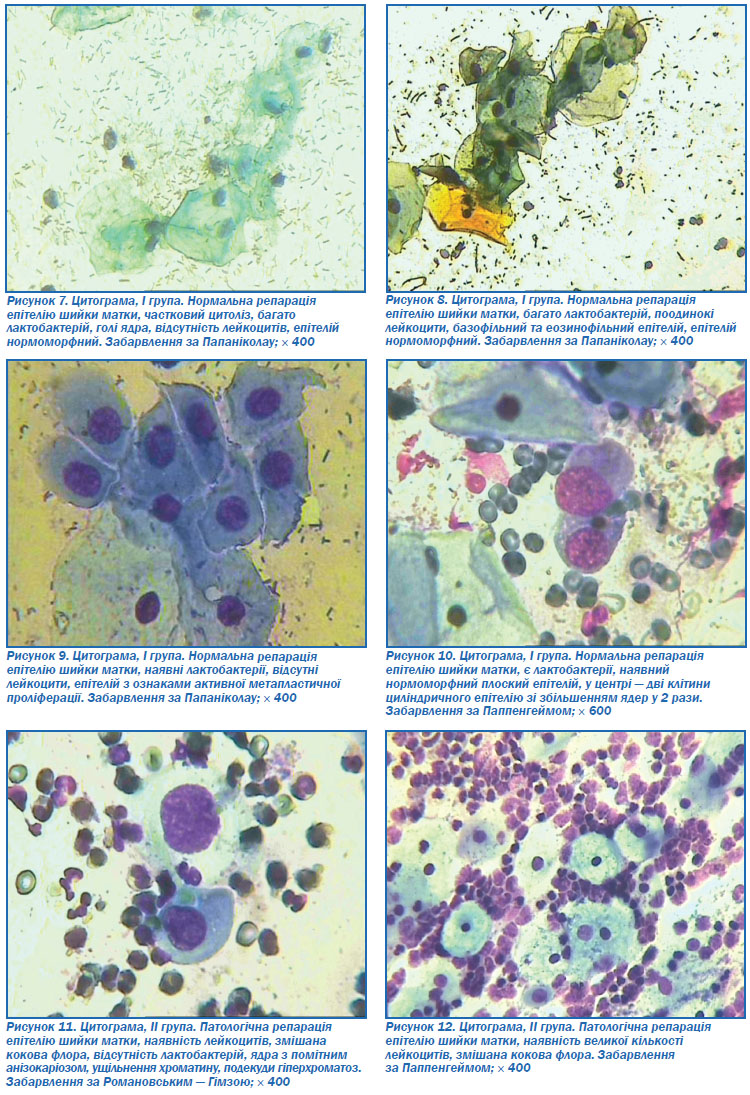
Гіперплазія резервних клітин з ознаками активної метапластичної проліферації (рис. 9) сприяє переміщенню зони стику багатошарового й циліндричного епітелію вглиб ендоцервіксу. Тому при добрій репарації зона стику епітелію кольпоскопічно не візуалізується. І навпаки, у жінок ІІ групи зона стику не переміщується, затримується в ектоцервіксі, що є свідченням поганої репарації.
Отже, у пацієнток І групи переважно відмічалось деяке пришвидшення регенеративних процесів порівняно з нормою, вони характеризувались такими цитологічними ознаками: розташування клітин у вигляді двовимірних скупчень, без нашарувань, незначне збільшення ядер, ядра округлі, з рівними контурами (рис. 10), дрібнозернистим гомогенним хроматином, поодинокими невеликими ядерцями, незначною лейкоцитарною інфільтрацією, помірною кількістю макрофагальних клітин.
У ІІ групі цитологічна картина свідчила про не зовсім нормальний перебіг репаративного процесу, а саме: у слизовій оболонці шийки матки наявні тривимірні скупчення клітин ектоцервіксу зі збільшенням ядер (максимум у 4 рази), анізокаріозом (рис. 11), ущільненням великозернистого хроматину, вираженими, дещо збільшеними ядерцями. Присутня виражена лейкоцитарна інфільтрація з поодинокими макрофагами та лімфоїдними елементами.
У пацієнток І групи у 35 випадках (87,5 %) була наявна лактобактеріальна мікрофлора (рис. 7, 8), а в пацієнток ІІ групи лактобактерії зустрічались у 7 (23,3 %) жінок, у решти — змішана кокобактеріальна мікрофлора (рис. 12) та елементи грибів роду Candida.
У 25 жінок ІІ групи (83,3 %) серед лейкоцитарного інфільтрату замість макрофагів виявляється до 20 % лімфоїдних елементів, що свідчить про розмноження поодиноких мікроорганізмів, які залишились після санації слизової оболонки шийки матки й у відновлювальному періоді обумовили патологічний репаративний процес та зміни, характерні для запалення.
Повна реепітелізація ектоцервіксу на 21–25-й день відмічена в 32 жінок (80 %) основної групи; у 8 жінок (20 %) повна репарація епітелію шийки матки відбулась на 27-й день після кріохірургії.
У контрольній групі процеси репарації епітелію шийки матки перебігали повільніше. Зокрема, тільки
в 13 пацієнток (43,3 %) повна реепітелізація шийки матки спостерігалась на 35-й день, у 9 (30 %) — на 40-й день, у 5 (16,7 %) досліджуваних — на 45-й день. У 3 (10 %) жінок групи контролю не відмічено кольпоскопічних та мікроскопічних ознак повної епітелізації шийки матки.
Жодного випадку токсико-алергічних реакцій при застосуванні досліджуваного лікувального засобу під час спостереження не відмічалось.
Висновки
За результатами проведених клініко-лабораторних спостережень можна зробити висновок, що застосування вагінального гелю Інтінова покращує якість та швидкість регенеративно-репаративних процесів в ектоцервіксі.
У жінок основної групи (І) відмічалась нормальна цитологічна та кольпоскопічна картина репаративних процесів в ектоцервіксі, які завершились на 21–28-й день після кріодеструкції.
У жінок контрольної групи (ІІ) кольпоскопічні та цитологічні характеристики ектоцервіксу не відповідали нормальній репаративній картині, що свідчить про порушення процесів регенерації слизової оболонки шийки матки. Про порушення відновних процесів у ектоцервіксі свідчить і тривалість репарації, яка у жінок контрольної групи становила від 5 до 7 тижнів.
У 87,5 % пацієнток І групи у процесі репарації була відмічена лактобактеріальна мікрофлора. У 83,3 % жінок контрольної групи відмічались лімфоїдна інфільтрація та порушення вагінального біоценозу, що свідчить про персистенцію хронічного запального процесу в екто- та ендоцервіксі.
Отже, включення вагінального гелю Інтінова в місцеве лікування шийки матки після кріодекструкції обґрунтоване й клінічно виправдане.
Результати клінічного випробування показали добру переносимість гелю Інтінова й відсутність патологічних побічних реакцій при його застосуванні в пацієнток.