Статья опубликована на с. 8-12
Сложные иммунобиологические взаимосвязи между развивающимся эмбрионом и материнским организмом, которые возникают с первых недель беременности, определяют не только дальнейшее благополучное течение беременности, внутриутробное развитие плода, но и состояние здоровья новорожденного ребенка. Ведь иммунная система, эволюционно предназначенная для распознавания и элиминации чужеродных антигенов, нередко служит причиной неадекватного ответа организма матери на развитие беременности. Во время беременности иммунный ответ со стороны матери развивается в отношении плода, получившего 50 % набора хромосом отца: для материнского организма фетоплацентарная система представляет собой иммунологически наполовину чужеродный трансплантат, вызывающий реакцию со стороны ее иммунной системы [7, 8, 12, 19, 22]. Такой аллотрансплантат в соответствии с общими иммунологическими законами подлежит отторжению под действием клеточного и гуморального иммунитета.
Природой предусмотрен специальный механизм, который реализуется только во время беременности. В качестве чужеродной ткани в этом случае выступает трофобласт, который включает определенную последовательность иммунных механизмов в организме женщины, направленных на сохранение беременности.
После распознавания антигенов трофобласта организм матери активирует собственную лимфоцитарную систему, при этом уровень прогестерона в крови повышается (желтое тело продуцирует большее количество прогестерона), при этом повышается также и экспрессия прогестероновых рецепторов на поверхности лимфоцитов и децидуальных клеток [7, 8, 12, 19, 21]. Взаимодействие прогестерона с рецепторами лимфоцитов приводит к синтезу прогестерон-индуцированного блокирующего фактора (ПИБФ) лимфоцитами и децидуальными клетками, ему и отведена ключевая роль в регуляции иммунного ответа матери. ПИБФ обладает антиабортивным эффектом, блокируя основные механизмы отторжения плода [19, 21].
Антиабортивный эффект ПИБФ на фоне достаточного уровня прогестерона вызывает следующие эффекты [7, 8, 12, 19–22]:
1. Синтез асимметричных антител — они скрывают антигены плода от материнской иммунной системы.
2. Подавление активности лимфокин-активированных клеток (ЛАК), которые способны разрушать клетки трофобласта и эмбриона. Под воздействием ПИБФ не происходит трансформации NK (естественные киллеры) в ЛАК.
3. Т-хелперы (Th) — посредники в развитии воспалительных и иммунных реакций в системе мать — плацента — плод. Под воздействием ПИБФ происходит «сдвиг» в сторону противовоспалительных цитокинов Th2 — Th2 > Th1.
Все вышеперечисленное можно отнести к общим механизмам иммунологического выживания беременности (аллотрансплантата) и роли основного протектора беременности — прогестерона — в этом процессе [7, 8, 9, 22].
После успешного преодоления вышеописанного первого иммунологического барьера благополучию беременности может угрожать еще один вариант иммунологической несовместимости — материнская аллоиммунизация на основе Rh-несовместимости или АВО-несовместимости с развивающимся плодом [4, 15–18]. В данном сообщении остановимся на основных механизмах развития данной патологии, методах диагностики и тактики ведения беременных. Чрезвычайно важным моментом является возможность эффективной профилактики грозных осложнений для развивающегося плода при помощи введения иммуноглобулина антирезус Rh0(D)
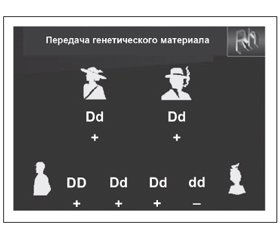
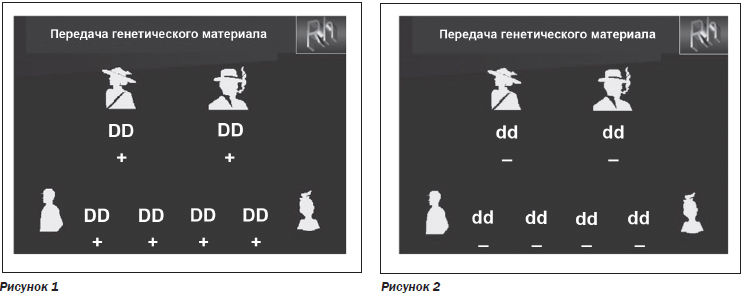
Необходимо напомнить некоторые аспекты передачи генетического материала от родителей к потомству [4, 5, 15, 16, 18, 20]. При наличии гомозиготных антигенов DD у обоих родителей (Rh-положительный тип крови) — дети будут также Rh-положительными. Соответственно наличие гомозиготных антигенов dd свидетельствует о Rh-отрицательном типе крови как у родителей, так и у их детей (рис. 1, 2).
Если один из родителей имеет гомозиготный тип антигенов DD, а другой — гомозиготные антигены dd, то их дети приобретают гетерозиготные антигены Dd, имея при этом Rh-положительный тип крови (рис. 3).
В настоящее время не представляется возможным отличить случаи гомозиготности и гетерозиготности при Rh-положительном типе крови из-за отсутствия сыворотки против антигена d [13, 20].
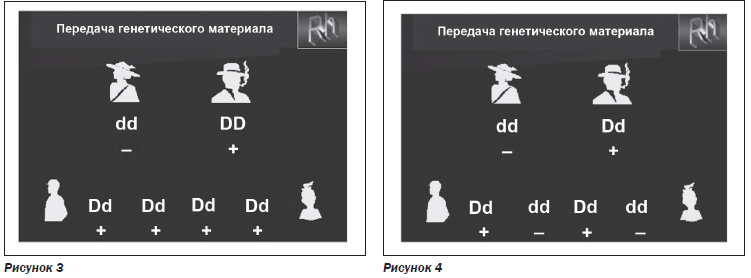
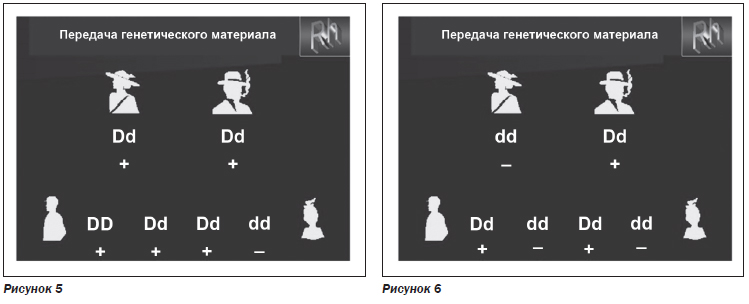
При наличии гомозиготности dd и гетерозиготных антигенов Dd у родителей возможно несколько вариантов Rh-принадлежности крови у их потомства (рис. 4, 5).
Исходя из всего вышеизложенного, развитие Rh-сенсибилизации возможно только при наличии трех условий:
1. Плод должен иметь Rh-положительные эритроциты, а мать — Rh-отрицательные.
2. Мать должна иметь иммуногенетическую способность вырабатывать антитела, направленные против D-антигена.
3. В материнский кровоток должно попасть достаточное количество эритроцитов плода.
Согласно шифру МКБ (МКБ-10-О36), изоиммунизация — это одна из клинических форм иммунопатологии, которая возникает при несовместимости организма матери и плода по различным антигенам и приводит к тяжелым нарушениям состояния плода и новорожденного [1]. Чаще всего в клинической практике встречается изоиммунизация по Rh-фактору и по АВО-системе (МКБ-10-О36.0, О36.1).
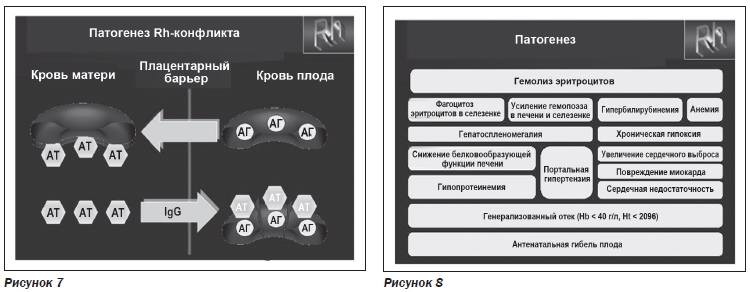
Rh-изоиммунизация представляет собой гуморальный ответ на эритроцитарные антигены (АГ) плода (включая Сс, Dd і Ее — кодируются Rh-аллелями) [1]. Для выработки анти-Rh (анти-D) антител у Rh-отрицательной беременной женщины достаточно попадания в кровоток матери от 0,1 до 250 мл D-положительных эритроцитов плода. Образованные в организме матери антитела (АТ), проникая через плаценту, вызывают экстраваскулярный гемолиз и анемию у плода, приводя к развитию у него эритробластоза (рис. 7).
И тем не менее у 30–35 % Rh-отрицательных женщин отсутствует реакция на резус-положительный антиген крови плода, т.е. они не иммунизируются. Данный феномен объясняется тем, что иммунологические реакции находятся под генетическим контролем [5, 6]. Нужно отметить, что есть еще одно показание к применению анти-D-иммуноглобулина — первичная аутоиммунная тромбоцитопения (приобретенное, но иммуноопосредованное заболевание), когда механизм действия анти-D не до конца понятен. Однако после введения анти-D-иммуноглобулина антитела как бы прикрывают тромбоциты через другие механизмы, что приводит к преимущественному разрушению эритроцитов [14]. Анти-D рекомендуется в качестве терапии первой линии для ИТП наряду с кортикостероидами и внутривенным иммуноглобулином (ВВИГ).
Все Rh-отрицательные женщины, имевшие в анамнезе искусственный или самопроизвольный аборт, внематочную беременность и не получившие специфической профилактики Rh-конфликта, составляют группу риска по развитию его в будущем. Это также касается тех женщин, которые имели Rh-конфликт при предыдущих беременностях или переливание Rh-положительной крови [1–3, 5, 13].
Риск Rh-иммунизации увеличивается при неблагоприятном течении беременности (преждевременная отслойка плаценты), при оперативных вмешательствах во время беременности и родов (амниоцентез, ручное отделение плаценты, кесарево сечение). Распространенные виды вирусной инфекции (герпетическая, цитомегаловирусная), которые сами по себе чрезвычайно влияют на иммунный статус, также увеличивают риск Rh-иммунизации [1–3, 5, 13].
Диагностика Rh-иммунизации основана на сборе анамнеза и определении титра Rh-антител в динамике, показатели и динамика роста которого дают возможность спрогнозировать риск развития гемолитической болезни новорожденного и даже риск внутриутробной гибели плода. Титры Rh-антител определяют также необходимость проведения трансабдоминального амниоцентеза и кордоцентеза [1, 2].
Патогенез гемолитической болезни новорожденного многоступенчатый и имеет влияние на все жизненно важные системы и функции [1–3, 10, 13, 18] — на фоне гемолиза эритроцитов, анемии и гипербилирубинемии, развития повреждений функции печени, миокарда, сердечной недостаточности, что в конечном итоге приводит к антенатальной гибели плода (рис. 8).
Основным методом предотвращения гемолитической болезни плода и новорожденного является иммунопрофилактика анти-Rh0(D)-иммуноглобулином, который представляет собой лекарственное средство, являющееся белковой фракцией из крови резус-иммунизированных людей [1–3, 10, 13]. Основными компонентами иммуноглобулина анти-Rh0(D) человека являются антитела к человеческому резус-фактору. Доказанным фактом является то, что если антиген (в данном случае — резус-фактор) и антитела к нему попадают в организм практически одновременно, то сенсибилизации организма (выработки собственных антител) не происходит.
Возможность использования качественного иммунологического препарата этой группы в Украине есть. Им является анти-Rh0(D)-иммуноглобулин (ООО «Био-
фарма Плазма»), содержащий специфические антитела к анти-Rh0(D) — 300 мкг в одной дозе препарата и необходимый высокий титр антител к анти-Rh0(D) — 1 : 2000. Препарат является иммунологически активной белковой фракцией плазмы крови иммунизированных (или реиммунизированных) доноров, в которой подтверждено отсутствие антител к ВИЧ-1, ВИЧ-2, к вирусу гепатита С и поверхностного антигена вируса гепатита В. Белковая фракция плазмы крови иммунизированных доноров очищена и сконцентрирована методом фракционирования этиловым спиртом, прошла стадию вирусной инактивации сольвент-детергентным методом. Содержание белка в 1,0 мл препарата — от 0,09 до 0,11 г. Препарат также не содержит консервантов и антибиотиков.
Показания к профилактике Rh-сенсибилизации при беременности — доза 300 мкг [1, 2]:
— в срок беременности 28–32 недели;
— в случае появления симптомов угрозы прерывания беременности до 28 недель;
— после амниоцентеза и кордоцентеза, биопсии хориона;
— после удаления пузырного заноса;
— после внематочной беременности;
— после прерывания беременности (не позднее 48 часов после аборта);
— при отслойке плаценты и маточном кровотечении (неясной этиологии);
— после случайной трансфузии Rh-положительной крови Rh-отрицательной женщине;
— после переливания тромбоцитарной массы;
— при травмировании беременной (например, автомобильная катастрофа).
Доза иммунопрепарата зависит от срока беременности: в сроке до 13 недель доза анти-Rh0(D)-иммуноглобулина составляет 75 мкг [1, 2], при сроке беременности более 13 недель — 300 мкг, препарат вводится в/м.
Профилактика Rh-сенсибилизации в послеродовом периоде проводится только при рождении Rh-положительного ребенка — в течение первых 72 часов в/м вводится 1 доза (300 мкг) анти-Rh0(D)-иммуноглобулина [1, 2].
Необходимо четко следовать предписанным противопоказаниям к использованию анти-Rh0(D)-иммуноглобулина [1, 2]:
— Rh-положительным роженицам, а также Rh-отрицательным роженицам, сенсибилизированным к антигену Rh0(D), в сыворотке которых выявлены резус-антитела;
— Rh-отрицательным женщинам, сенсибилизированным к антигену Rh0(D), в плазме которых выявлены резус-антитела;
— лицам, имевшим в анамнезе тяжелые аллергические реакции на введение белковых препаратов крови человека;
— при селективном дефиците IgА при условии наличия антител против IgА, лицам, имеющим тяжелые аллергические реакции на введение белковых препаратов крови человека в анамнезе, а также реакции гиперчувствительности к донорским иммуноглобулинам человека;
— в случае тяжелой тромбоцитопении и других нарушений гемостаза.
Практическим врачам-гинекологам необходимо четко выделить группы женщин с Rh-отрицательным типом крови — это неиммунизированные первобеременные и повторнобеременные женщины, у которых при первом антенатальном обследовании изоантитела не были обнаружены. Этой категории женщин необходимо проводить тест на наличие Rh-антител либо в качестве прегравидарного скрининга, либо на ранних сроках беременности. При сборе анамнеза побудительным мотивом к проведению данного исследования будет рождение детей с необъяснимой желтухой, гибель плода, переливание крови [1–3, 13].
При отрицательных результатах скрининга можно определить следующие задачи в наблюдении за беременной: оценить степень риска развития изоиммунизации, принять меры для выявления возможной изоиммунизации и обеспечить адекватную профилактику в дородовом и послеродовом периодах.
Результаты проведенных статистических исследований [5, 6] свидетельствуют, что у иммунизированных беременных с неотягощенным акушерским анамнезом при титрах антител до 1 : 64 внутри-утробная гибель плода в сроках до 37 недель беременности может иметь место в 4 % случаев. В тех же сроках беременности (37 нед.) и при том же титре антител (1 : 64) рождение ребенка с гемолитической болезнью и/или мертворождение возможно уже в 32 % случаев [5, 6].
При титрах антител выше 1 : 64 у беременных с не-отягощенным анамнезом процент мертворождения достигает 17,2. А у женщин, ранее родивших детей с гемолитической болезнью, этот показатель равен 67,8 % [5, 6].
Выводы
1. Беременность может сопровождаться одним из вариантов иммунологической несовместимости — материнской аллоиммунизацией на основе Rh-несовместимости или АВО-несовместимости с развивающимся плодом.
2. Изоиммунизация — это клиническая форма иммунопатологии, которая возникает при несовместимости организма матери и плода по различным антигенам и приводит к тяжелым нарушениям состояния плода и новорожденного.
3. Для аллоиммунизации беременной с Rh-отрицательным типом крови необходимо попадание в ее кровоток определенного количества D-положительных эритроцитов плода.
4. Современные исследования по вопросам иммунопрофилактики предусматривают отдельный перечень показаний для назначения анти-Rh0(D)-иммуноглобулина, в том числе и при лечебно-диагностических операциях, что нашло отражение в соответствующих приказах МЗ Украины.
5. Профилактику анти-Rh0(D)-иммуноглобулином при беременности проводят при отсутствии иммунизации беременной, с четкой дозировкой иммунопрепарата и с учетом срока беременности, а также в послеродовом периоде.
6. Проведенная иммунопрофилактика качественным, современным анти-Rh0(D)-иммуноглобулином является эффективной мерой предупреждения гемолитической болезни новорожденного и его инвалидизации, а также мертворождения.
Список литературы
1. Наказ МОЗ України від 15.07.2011 № 417 «Методичні рекомендації щодо організації надання амбулаторної акушерсько-гінекологічної допомоги».
2. Наказ МОЗ України від 31.12.2004 № 676 «Про затвердження клінічних протоколів з акушерської та гінекологічної допомоги».
3. British national formulary: BNF 69 (69 ed.). — British Medical Association, 2015. — Р. 871.
4. Pregnancy — routine anti-D prophylaxis for RhD-negative women. — National Institute for Health and Clinical Excellence, 2002.
5. Bowman J.M. The Prevention of Rh Immunization // Transfus. Med. Rev. — 1988. — 2. — 129-50.
6. Bowman J.M. Hemolytic disease (Erythroblastosis fetalis) / J.M. Bowman [et al.] // Maternal-fetal medicine. — 4th ed. — Philadelphia: W.B. Saunders, 1999. — P. 736-767.
7. Delves P.J., Roitt I.M. The immune system. Advances in Immunology // N. Engl. J. Med. — 2000. — 343. — 37-49.
8. Fatemi H.M., Bourgain C., Donoso P. et al. // Hum. Reprod. — 2007. — 22 (5). — 1260-1263.
9. Karanth L., Jaafar S.H., Kanagasabai S., Nair N.S., Barua A. Anti-D administration after spontaneous miscarriage for preventing Rhesus alloimmunisation // The Cochrane database of systematic reviews. — Mar 28, 2013.
10. Klein H.G., Anstee D.J. Haemolytic Disease of the Fetus and Newborn // Mollison’s Blood Transfusion in Clinical Medicine. — 11th еd. Oxford: Blackwell, 2005. — 496-545.
11. Neunert C., Lim W., Crowther M. еt al. The American Society of Hematology 2011 evidence-based practice guideline for immunethrombocytopenia. — 2011. — 117 (16). — Р. 4190-4207.
12. Ober C., Hyslop T., Elias S., Weikamp L.R., Hauck W.W. Human leucocyte antigen matching and foetal loss: result of a 10 year prospective study // Hum. Reprod. — 1998. — 13. — 33-38.
13. Prevention of Rh D Alloimmunization. ACOG Practice Bulletin Number 4. — Washington: American College of Obstetricians and Gynecologists, 1999.
14. Provan D., Stasi R., Newland A.C. еt al. International consensus report on the investigation and management of primary immunethrombocytopenia // Blood. — 2010. — 115 (2). — Р. 168-186.
15. Rho(D) Immune Globulin. The American Society of Health-System Pharmacists. Retrieved, 8 January 2017.
16. RhoGAM Ultra-Filtered PLUS Rho(D) Immune Globulin (Human). Information Site.
17. Roback С. еt al. AABB Technical Manual. — 16th еd. — Bethesda: AABB Press, 2008.
18. Rudmann А., Sally V. Textbook of Blood Banking and Transfusion Medicine. — 2nd еdition. — Elsevier Saunders. — 2005. — Р. 439-44.
19. Szekeres-Bartho J. Immunological relationship between the mother and the foetus // Int. Rev. Immunol. — 2002. — 21. — 471-495.
20. Use of Anti-D Immunoglobulin for Rh Prophylaxis: Royal College of Obstetricians and Gynaecologists. May 2002.
21. WHO Model List of Essential Medicines: World Health Organization. April 2015. Retrieved 8 December 2016.
22. http://medicalplanet.su/Patfiz/305.html