Журнал «Почки» Том 6, №1, 2017
Вернуться к номеру
Коррекция вторичной карнитиновой недостаточности у пациентов, находящихся на хроническом гемодиализе: фокус на левокарнитин
Авторы: Чистик Т.В.
Рубрики: Нефрология
Разделы: Справочник специалиста
Версия для печати
Хроническая почечная недостаточность (ХПН) является исходом многих длительно протекающих соматических заболеваний: хронического гломерулонефрита, хронического пиелонефрита, гипертонической болезни, сахарного диабета, интерстициальных нефритов, системных заболеваний соединительной ткани, подагры [1, 2]. Согласно данным European Renal Association (ERA-EDTA) Registry [3], в программном гемодиализе (ПГ) нуждаются 300 человек с терминальной почечной недостаточностью (ТПН) на 1 млн населения. Ежегодный прирост числа больных, нуждающихся в лечении ПГ, составляет 150–200 на 1 млн жителей, а с учетом уже получающих данное лечение — от 460 до 900 на 1 млн жителей [4].
В настоящее время коррекция терминальной почечной недостаточности осуществляется за счет программного гемодиализа, перитонеального диализа и трансплантации почки. При этом преимущественно применяется ПГ. Так, по данным ERA-EDTA, в 2001 году программный гемодиализ получали около 80 % больных, перитонеальный диализ — 15–18 %, и лишь 1–2 % в качестве первичного метода коррекции ТПН выполнялась пересадка почки [3, 5].
Улучшение качества лечения и снижение общей смертности больных ТПН возможно при решении ряда проблем, главная из которых — это совершенствование методов ранней диагностики осложнений, возникающих при программном гемодиализе, и их своевременная коррекция [1, 6]. Известно, что нередко при программном гемодиализе развивается вторичная карнитиновая недостаточность, сопровождающаяся нарушением сердечной деятельности, почечной анемией, гипертриглицеридемией, мышечными судорогами и гипотонией, снижением толерантности к физическим нагрузкам [7].
Роль карнитина в метаболизме
Карнитин — низкомолекулярное вещество, впервые выделенное из мышечных экстрактов и получившее название от латинского слова carnis (мясо) [8]. Его физиологической формой является левовращающий (L-) изомер — левокарнитин. У человека около 25 % запасов карнитина синтезируется в печени, почках и головном мозге из эссенциальных аминокислот лизина и метионина. Остальные 75 % карнитина поступают в организм с продуктами животного происхождения, главным образом с мясом, рыбой и молочными продуктами [9, 10].
Карнитин, включающий катионную триметиламмониевую группу и анионную гидроксильную группу, является амфотерным соединением и принадлежит к бетаинам. В организме млекопитающих он присутствует в виде свободного и ацетилированного карнитина [11]. Концентрация свободного карнитина в плазме здоровых взрослых лиц составляет 40–60 мкмоль/л, общего карнитина (свободный + ацилкарнитин) — около 50–70 мкмоль/л [9]. Карнитин распределен в различных органах организма. У здорового человека весом 70 кг общий пул карнитина составляет приблизительно 130 ммоль (21 г). Более 98 % общего пула карнитина находится в скелетных и сердечной мышцах, 1–1,5 % — в печени и менее 0,5 % — в крови. Это распределение отражает высокую потребность мышц в окислении жирных кислот, для которого необходим L-карнитин. Последний не синтезируется мышцами, и его уровень в мышечной ткани поддерживается за счет поступления из крови.
В организме человека синтезируется приблизительно 1–2 мкмоль L-карнитина на 1 кг массы тела в день (в среднем у взрослого — 10–20 мг в день). Этого эндогенного синтеза вполне достаточно для поддержания пула карнитина у здоровых лиц [10, 11]. Эссенциальная кислота лизин конвертируется в различных тканях в триметиллизин. Пройдя через серию метаболических реакций, ферменты для осуществления которых присутствуют во многих тканях, но главным образом в скелетных мышцах, первоначально связанный с белком триметиллизин превращается в γ-бутиробетаин. Конечное превращение γ-бутиробетаина в карнитин катализируется ферментом, обнаруженным преимущественно в печени, почках и головном мозге.
Основным местом регуляции концентрации карнитина в плазме являются почки. У здоровых лиц карнитин свободно фильтруется через клубочковую мембрану, свободный карнитин почти полностью реабсорбируется, с мочой выделяется ацилкарнитин [15]. Почечный клиренс ацилкарнитина в 4–8 раз выше почечного клиренса свободного карнитина. Ухудшение почечной функции приводит к снижению клиренса карнитина и ухудшению нормальной экскреции ацилкарнитина, что, в свою очередь, способствует повышению плазменных уровней карнитина. Таким образом, у уремических больных, которые еще не начали лечение диализом, отмечается повышение уровней свободного и общего карнитина и заметное повышение концентраций ацилкарнитина.
Основная функция карнитина — энергетическая — достигается посредством транспорта остатков длинноцепочечных жирных кислот в форме ацилкарнитина через митохондриальную мембрану с целью дальнейшего β-окисления и образования АТФ [11, 12]. Кроме того, карнитин учувствует в окислении среднецепочечных жирных кислот и поддерживает необходимый для нормального течения метаболических процессов пул свободного коэнзима А. Он, защищая клетки от избытка ацил-СоА-соединений, ингибирующих активность многих ферментов, сохраняет целостность мембран, подавляет образование лактата и процессы апоптоза [13, 14].
Механизмы развития вторичной карнитиновой недостаточности у пациентов, находящихся на гемодиализе
В условиях тканевой гипоксии, сопровождающей уремию, главным источником энергии для клеток являются жирные кислоты, так как в отличие от глюкозы они могут окисляться при низких значениях кислорода в крови, но требуют большего количества карнитина, запасы которого в организме человека ограничены.
Дефицит карнитина при хронической почечной недостаточности носит вторичный характер и может быть связан с алиментарным дефицитом карнитина вследствие модифицированной диеты таких пациентов либо с гиперкатаболическими состояниями с преобладанием потерь карнитина над его поступлением.
У пациентов с вторичной карнитиновой недостаточностью также отмечается значительное повышение экскреции карнитина за счет снижения его реабсорбции в почках. Кроме того, у пациентов с уремией снижается активность митохондриальной карнитин-пальмитоил-трансферазы в сердечной и скелетной мускулатуре, что дополнительно может приводить к ослаблению действия карнитина. Признаками недостаточности карнитина являются сонливость, мышечная слабость, гипотония, сердечная недостаточность и аритмии, преходящие судороги. Проявления недостаточности карнитина усугубляются при сопутствующем нарушении питания, когда жирные кислоты, как необходимый источник энергии, поступают в недостаточном количестве [16, 17].
Длительное лечение программным гемодиализом — одна из основных причин развития вторичного дефицита карнитина [18]. Карнитин выводится во время процедуры гемодиализа, а его запасы в мышцах исчерпываются. Пациенты, находящиеся на диализе, имеют тенденцию к снижению свободного плазменного карнитина и заметному увеличению уровня ацилкарнитина, что приводит к повышению нормального соотношения ацилкарнитина со свободным карнитином. Общий плазменный карнитин, однако, может быть нормальным в зависимости от количества ацилкарнитина.
Так, в исследовании A.M. Evans et al. [19] было показано, что средняя (± SD) плазменная концентрация карнитина у больных с терминальной почечной недостаточностью, которые еще не начали лечение гемодиализом, составила 50,6 ± 20,0 мкмоль/л. Через 12 месяцев (29,7 ± 10,5 мкмоль/л) и более 12 месяцев (22,0 ± 5,4 мкмоль/л) лечения гемодиализом отмечались значимо более низкие концентрации. Ацетилкарнитин также снижается с длительностью диализа, в то время как плазменный неацетилированный ацилкарнитин с продолжением терапии гемодиализом продолжал увеличиваться. Выявлена обратная зависимость между длительностью диализного лечения и мышечной концентрацией карнитина.
Таким образом, длительное лечение гемодиализом связано со значительным снижением эндогенных уровней плазменного и мышечного карнитина и существенным повышением уровня ацилкарнитина в плазме. Наибольшие изменения плазменных концентраций встречаются в течение первых нескольких месяцев гемодиализа, в то время как уровни карнитина в мышцах продолжают снижаться после 12 месяцев лечения.
Подобные результаты были получены и в ряде других исследований [20–22].
Из-за связанной с диализом потери карнитина и его недостаточного синтеза в почках происходит истощение его резервных запасов, что оказывает негативное влияние на миокард, скелетные мышцы, печень, головной мозг, иммунную систему [12]. Возможно развитие таких осложнений, как обострение ишемической болезни сердца, возникновение аритмий [23], сердечной недостаточности [24]. Известна роль дефицита карнитина в генезе кардиомиопатий и артериальной гипертензии [24].
Применение левокарнитина для коррекции сердечной функции у пациентов на гемодиализе
Наиболее частыми осложнениями у пациентов с терминальной почечной недостаточностью являются кардиологические осложнения, составляющие почти 50 % [25]. Согласно исследованию D.F. Pauly и C.J. Pepine [26] установлено, что левокарнитин может играть важную роль в коррекции нарушений сердечной функции, вызванных гипоксией и оксидативным стрессом, что объясняется его кардиопротективным действием.
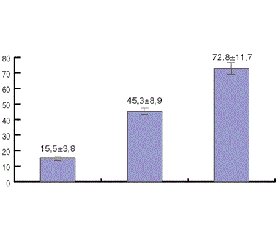
Поскольку окисление жирных кислот — это главный источник энергии для миокарда, крайне важен адекватный уровень карнитина. В исследовании Suzuki et al. было выявлено, что истощение запасов карнитина в миокарде нередко сопровождается развитием аритмий и стенокардии, связанных с диализом [27]. У 11 пациентов из 17, находящихся на гемодиализе, в течение 20–30 минут от начала процедуры развивалась желудочковая и наджелудочковая аритмия, сохраняющаяся до конца гемодиализа. При этом концентрация карнитина снижалась с 24,8 ± 7,9 мкмоль/л до диализа до 8,2 ± 5,9 мкмоль/л в конце процедуры. Назначение левокарнитина за 2 часа до проведения гемодиализа в дозе 2 г/сутки в течение 4–8 недель значимо уменьшало частоту аритмий и ангинозных приступов. Мышечная сила и субъективное самочувствие больных также улучшалось.
Роль дефицита карнитина в развитии кардиомегалии у больных, находящихся на хроническом гемодиализе, была описана Kudoh et al. [28]. В исследовании, включавшем 33 больных на хроническом гемодиализе, были отмечены значимо сниженные концентрации карнитина в плазме, которые обратно коррелировали с размером сердца, определявшимся по кардиоторакальному соотношению на рентгенограммах грудной клетки. Многофакторный регрессионный анализ показал, что гипокарнитинемия и анемия независимо друг от друга были основными причинами кардиомегалии. Основываясь на этих результатах, авторы предложили использовать терапию левокарнитином для уменьшения кардиомегалии у хронических гемодиализных больных.
В двух нерандомизированных исследованиях [7] на фоне терапии левокарнитином оценивалась фракция выброса как показатель функции левого желудочка (Van E.S. et al.). Левокарнитин назначался по 1 г внутривенно после каждого сеанса гемодиализа на протяжении 3 месяцев. У 13 пациентов было продемонстрировано статистически значимое увеличение фракции выброса, составившее в среднем от 42,4 до 48,6 %.
Гемодиализ и гипертриглицеридемия
К достаточно частым явлениям, развивающимся у пациентов, находящихся на гемодиализе, относится гипертриглицеридемия [29]. При этом ряд исследований показал, что лечение левокарнитином приводит к уменьшению сывороточных уровней триглицеридов [31–33].
Так, в работе Elisaf et al. [30] изучались эффекты левокарнитина для ацетатного (n = 14) и бикарбонатного (n = 14) диализа у пациентов в возрасте от 21 до 61 года, которым диализ проводился в среднем в течение 25 месяцев. В течение 6 месяцев все больные получали относительно низкие в/в дозы
(5 мг/кг массы тела) левокарнитина в конце каждого диализа. Результаты исследования позволили выявить, что назначение низких доз левокарнитина приводило к уменьшению сывороточных концентраций триглицеридов — от 225 ± 76 мг/дл
до 201 ± 75 мг/дл (p = 0,03), у больных с высокими уровнями триглицеридов снижение было более явным — от 260 ± 64 мг/дл до 226 ± 82 мг/дл
(p < 0,05), независимо от применявшегося на диализе буфера (ацетат или бикарбонат). Авторы пришли к выводу, что низкие дозы левокарнитина целесообразны для воздействия на уровни триглицеридов у больных на гемодиализе.
Роль левокарнитина в коррекции астенического синдрома, гипотонии и мышечных судорог у пациентов на гемодиализе [7]
Ahmad et al. в рандомизированном исследовании с двойным слепым плацебо-контролем было показано уменьшение постдиализной астении, мышечных судорог и гипотонии у пациентов, получающих левокарнитин.
Sakurauchi et al. сообщили, что симптомы утомляемости уменьшились у 14 из 21 пациента, находящихся на гемодиализе, а мышечная слабость снизилась у 14 из 24 больных (р < 0,05) после 3 месяцев терапии левокарнитином.
В сравнительном исследовании Sohn et al. с участием 30 пациентов на гемодиализе было показано, что в группе больных, получающих левокарнитин (n = 15), отмечается существенное уменьшение мышечных судорог и улучшение самочувствия в сравнении с группой, принимающей плацебо (n = 15).
Casciani et al. провели нерандомизированное перекрестное исследование среди 18 пациентов и показали существенное улучшение самочувствия после двухмесячного курса левокарнитина. В исследовании Bellinghieri et al. оценивали мышечную утомляемость непосредственно после диализа и в междиализном интервале. Они выявили, что постдиализная астения существенно уменьшается уже после 15 дней применения левокарнитина, в то время как астения в ходе диализа уменьшалась только после 30 дней лечения. Когда применение левокарнитина прекращалось, астения возобновлялась в интервале от 15 до 30 дней.
Положительная роль левокарнитина в улучшении толерантности к физическим нагрузкам у пациентов на гемодиализе
Коррекция анемии, гиперпаратиреоза и дефицита 1,25-OH витамина D3, а также обеспечение адекватного диализа не восстанавливают полностью мышечную функцию и толерантность к физической нагрузке у больных с терминальной почечной недостаточностью. В норме карнитин в избытке присутствует в мышечной ткани, но с течением диализной терапии его уровень снижается. Поэтому снабжение левокарнитином может восстановить мышечную массу и функцию. Детально были рассмотрены пять исследований [7], описывающих различные аспекты физической активности. Физическая активность оценивалась по индексу активности пациента (activity score), длительности физических упражнений, максимальному потреблению кислорода и площади сечения мышц середины плеча, измерению максимальной силы, физической рабочей нагрузке (exercise workload) и субъективной мышечной силе. Длительность лечения варьировала от 1 до 6 месяцев. Левокарнитин применялся внутривенно в конце сеанса диализа по 2 г в течение 6 недель или 6 месяцев по 20 мг/кг.
В исследовании, проведенном Siami et al., была отмечена тенденция (р = 0,07) к улучшению субъективной оценки физической активности при назначении левокарнитина в дозе 2 г в/в после сеанса на протяжении 6 месяцев.
Ahmad et al. сообщили о значимом увеличении площади сечения мышц в середине плеча (р = 0,05) у пациентов, получающих левокарнитин, при отсутствии изменений в группе плацебо. Также в группе больных, получавших левокарнитин, отмечались значимое увеличение максимального потребления кислорода (в среднем на 111 мл/мин;
р < 0,03) и тенденция к увеличению длительности физических упражнений.
В исследовании, проведенном Fagher et al., наблюдалось увеличение максимальной мышечной силы в сравнении с исходными значениями (р < 0,01) в группе пациентов, получающих 2 г левокарнитина в/в после диализа. Курс лечения составил 6 недель.
Mioli et al. сообщили об увеличении максимальной рабочей нагрузки после 45 дней перорального применения левокарнитина, которое сохранялось и через 60 дней после лечения (р < 0,05).
Эффективность терапии левокарнитином при лечении анемии у больных, находящихся на гемодиализе
Высказано предположение о том, что дефицит карнитина может уменьшать время полужизни эритроцитов, отрицательно влияя на целостность эритроцитарных мембран. Kooistra et al. показали связь между уровнем анемии и потребностью в эритропоэтине, с одной стороны, и уровнем свободного карнитина в сыворотке диализных пациентов — с другой. Несмотря на доступность рекомбинантного эритропоэтина и более широкое использование декстрана железа внутривенно в последние годы, значительная часть пациентов на гемодиализе продолжают страдать от анемии или требовать больших доз эритропоэтина для поддержания гемоглобина на рекомендованном уровне. Эпидемиологические исследования постоянно демонстрируют меньшую летальность среди пациентов с уровнем гематокрита в диапазоне 30–36 %, а рабочая группа по лечению анемии NKF-DOQI рекомендовала целевой гематокрит от 33 до 36 %, основываясь на детальном обзоре литературы группой экспертов [7].
Kavadias et al., назначавшие 8 больным левокарнитин в дозе 2 г внутривенно, обнаружили повышение уровня гематокрита и снижение дозы рекомбинантного человеческого эритропоэтина (рчЭПО) приблизительно до 50 % от его начальной дозы [34]. Сходные результаты были получены Vesela et al., у которых отмечалась редукция ЭПО до 64 % [35]. После трехмесячной терапии левокарнитином в дозе 40–60 мг/кг массы тела в неделю Boran et al. наблюдали 22% увеличение уровня гематокрита и 42% — потребности в рчЭПО [36].
В течение шести месяцев Labonia et al. лечили группу из 13 больных, находящихся на гемодиализе, левокарнитином в дозе 1 г в/в после диализа и сравнили их результаты с результатами группы плацебо (n = 11) [37]. Лечение левокарнитином уменьшило расход ЭПО на 38 % (от 102,2 ± 52,6 Ед/кг МТ/нед до 63,3 ± 37,8 Ед/кг
МТ/нед), тогда как концентрации эндогенного ЭПО остались неизменными. Здесь также были пациенты, ответившие и не ответившие на лечение. Из 13 больных 7 ответили на терапию карнитином со снижением потребности в ЭПО, тогда как у оставшихся 6 участников исследования поддерживающая первоначальная доза ЭПО осталась неизменной. Весьма интересным результатом было то, что больные, ответившие на лечение, имели более высокую потребность в ЭПО и более высокие исходные концентрации эндогенного ЭПО в плазме, чем не ответившие. Авторы предположили, что дефицит карнитина у больных на гемодиализе способен приводить к более высокой резистентности к ЭПО, которая может быть корригирована дополнительным назначением карнитина, в результате чего потребность в дополнительном ЭПО снижается.
В рандомизированном плацебо-контролируемом исследовании, проведенном Trovato et al., было продемонстрировано, что применение левокарнитина у пациентов на гемодиализе за 12 месяцев терапии повышает гематокрит с 25,5 до 37,4 %, тогда как в группе контроля отмечено его снижение с 24,0 до 21,8 % за данный промежуток времени [7].
В рандомизированном плацебо-контролируемом исследовании Caruso et al. с участием 31 пациента изучались дозы эритропоэтина и показатель гематокрита при назначении 1 г в/в левокарнитина и плацебо после каждого сеанса гемодиализа. Было установлено, что в группе пациентов старше 65 лет (n = 21) применение левокарнитина сопровождалось значимым увеличением гематокрита (в среднем с 28,1 до 32,8 %) и снижением необходимой дозы эритропоэтина (в среднем с 141,3 до 92,8 Ед/кг),
что значительно превосходило показатели группы плацебо [7].
Ряд членов рабочей группы считают, что пробное лечение L-карнитином перорально или внутривенно (примерно 1 г после диализа) обосновано у отдельных пациентов с анемией и/или очень высокой потребностью в эритропоэтине. Четырехмесячный период лечения достаточен для оценки ответа на левокарнитин [7].
Рекомендации к назначению левокарнитина при хроническом гемодиализе
Левокарнитин был синтезирован в 1960 г., а в 1962 г. была определена его роль как основного переносчика в транспортировке длинноцепочечных жирных кислот в митохондрии через их внутреннюю мембрану. В митохондриях происходит β-окисление жирных кислот, которые являются главным источником энергии для тканей сердца и скелетных мышц. Поэтому адекватные уровни карнитина очень важны для нормальной функции этих органов [38].
В 1994 г. консенсусная группа по карнитину Американской ассоциации почечных больных (American Association of Kidney Patients — AAKP) выполнила обзор литературы по применению левокарнитина и, основываясь на 42 опубликованных исследованиях, включавших приблизительно 600 гемодиализных больных, разработала рекомендации по показаниям к лечению левокарнитином [39].
В декабре 1999 г. американская администрация по пищевым продуктам и лекарственным средствам (FDA) одобрила применение инъекционной формы левокарнитина (Carnitor®, SigmаTau Pharmaceuticals, Inc.) для профилактики и лечения дефицита карнитина у больных с терминальной почечной недостаточностью на поддерживающем гемодиализе [40]. Клинические практические рекмендации NKF-K/DOQI по питанию при ХПН [41], опубликованные в 2000 г., предлагают применять карнитин преимущественно для лечения ЭПО-резистентной анемии, ссылаясь на малое число доказательств для рутинного применения карнитина у больных на поддерживающем гемодиализе. В то же время рабочая группа по питанию при ХПН рекомендовала продолжить исследования по лечению карнитином некоторых больных с симптомами недомогания, мышечной слабости, судорогами во время процедур гемодиализа, диализной гипотонией, плохим качеством жизни, которые не ответили на стандартные методы лечения [40, 41].
В 2003 году National Kidney Foundation была проведена конференция, посвященная консенсусу по карнитину (The Carnitine Consensus Conference), результаты которой были опубликованы в American Journal of Kidney Disease [42]. Результаты конференции позволили сделать несколько выводов:
— назначение левокарнитина не должно быть стандартным, необходим индивидуальный подход к пациентам с ТПН, находящимся на гемодиализе;
— несмотря на сравнительно небольшое количество исследований, посвященных изучению и доказательству эффекта карнитина у пациентов с хронической болзнью почек (ХБП) на гемодиализе, специалисты склоняются к назначению препарата данным больным. Левокарнитин оказывает множество положительных эффектов на осложнения гемодиализа и снижает нежелательные явления, развивающиеся на его фоне;
— имеется много исследований, доказывающих значительное снижение нежелательного гипотензивного эффекта у пациентов с ХБП на ГД;
— рекомендовано оценивать уровень улучшений в результате применения данного препарата каждые три месяца на протяжении лечения пациентов с ХБП на ГД.
Хотя руководства K-DOQI не декларируют рекомендации по назначению карнитина пациентам с ХБП на ГД, его использование в качестве дополнительной терапии ввиду множества положительных влияний на осложнения ГД может быть многообещающим [42].
Пациенты, находящиеся на ГД, могут получать карнитин и пероральным, и внутривенным путем. Уровни карнитина в мышечной ткани повышаются на 60–200 % через 6 недель использования. Данных о токсичности опубликовано не было [43].
Вместе с тем центры координации программ «Медикэр» и «Медикэйд» (Centers for Medicare and Medicaid Services) в США после тщательного обзора литературы в 2003 году опубликовали национальный меморандум по решению страховых вопросов, связанных с терапией левокарнитином при ТПН, который отныне обеспечивает компенсацию «Медикэр» при наличии следующих показаний:
1. ЭПО-резистентная анемия (уровень гематокрита < 30 %), которая не отвечает на стандартную дозу ЭПО и заместительную терапию железом, при условии исследования иных причин анемии и их адекватного лечения.
2. Гипотония на гемодиализе, не отвечающая на обычное лечение (например, контроль жидкостного баланса), которая мешает проведению диализных процедур и требует дополнительных лечебных мер, причем такие эпизоды гипотонии должны встречаться не реже чем на 2 диализных процедурах за 30-дневный период [11].
Заключение
Подводя итоги данным настоящего обзора, можно сделать следующие выводы:
1. Карнитин является важным фактором в метаболизме длинноцепочечных жирных кислот. Вследствие его центрального положения в промежуточном обмене веществ он оказывает влияние на различные системы органов.
2. Концентрации общего и плазменного карнитина у больных в додиализной стадии ХПН зависят от степени повреждения почек — остаточной синтетической способности почек (биосинтеза) и возможностей почечной экскреции, а также потребления карнитина с пищей.
3. Хронический гемодиализ приводит к истощению запасов свободного и общего карнитина в сыворотке и мышечных тканях больных.
4. Заместительная терапия левокарнитином вызывает у больных на ГД длительную нормализацию концентраций карнитина в крови и тканях.
5. Левокарнитин оказывает кардиопротективное (антиангинальное и противоаритмическое действие, профилактика кардиомегалии), противоанемическое (коррекция анемии и уменьшение потребности в эритропоэтине) и анаболическое влияние, что нередко сопровождается увеличением мышечной силы и максимального потребления кислорода, уменьшением процедурных осложнений (эпизодов гипотонии и мышечных судорог), улучшением качества жизни.
На сегодняшний день на фармацевтическом рынке Украины появился левокарнитин европейского качества Метакартин (World Medicine). Метакартин выпускается в форме раствора для инъекций. При дефиците карнитина у пациентов, находящихся на гемодиализе, начальная доза препарата составляет 10–20 мг/кг в виде медленной в/в инъекции после сеанса гемодиализа 3 раза в неделю. Внутривенное назначение Метакартина должно продолжаться минимум 3 месяца для восстановления запасов карнитина в мышцах. Необходимость повторного назначения определяется на основании контроля (с регулярными интервалами) уровня карнитина в плазме и мониторинга состояния пациента.
Подготовила Татьяна Чистик
Список литературы
1. Ермоленко В.М. Хроническая почечная недостаточность // Нефрология / Под ред. И.Е. Тареевой. — М.: Медицина, 1995.
2. Стецюк Е.А. Современный гемодиализ. — М.: МИД, 1998.
3. European Renal Association (ERA-EDTA) Registry // Nephron. 2001; 54.
4. United States Renal Data System: USRDS. 1997 Annual Data Report / The National Institutes of Health, National Institute of Diabetes and Digestive and Kidney Diseases. Bethesda, M.D.
5. Foley R.N., Parfrey P.S., Sarnak M.J. Clinical epidemiology of cardiovascular disease in chronic renal disease // Am. J. Kidney Dis. 1998; Vol. 32 (suppl. 3): S112-S119.
6. Levey A.S., Beto J.A., Coronado B.E. et al. Controlling the epidemic of cardiovascular disease in chronic renal disease: what do we know? What do we need to learn? Where do we go from here? National Kidney Foundation Task Force on Cardiovascular Disease // Am. J. Kidney. Dis. 1998; 32: 853-906.
7. Приложение Х. Возможное использование L-карнитина у больных на программном диализе / National Kidney Foundation, Inc. web version created by cyber Nephrology and the Nephron Information Center, 2000.
8. Gulewitsch W., Krimberg R. Zur Kenntnis der Extraktions–stoffe der Muskeln. 2. Mitteilung über das Carnitin // Hoppe-Seyler’s Z Physiol. Chem. 1905; 45: 326-330.
9. Schreiber B, Lewis V. Management of carnitine deficiency in ESRD patients undergoing dialysis: challenges and considerations // Dialysis & Transplantation. 2001; 30: 207-212.
10. Evans A. Dialysis-related carnitine disorder and levocarnitine pharmacology // Am. J. Kidney Dis. 2003; 41 (suppl. 4): S13-S26.
11. Hoppel Ch. The role of carnitine in normal and alterd fatty acid metabolism // Am. J. Kidney Dis. 2003; 41: S4S12.
12. Löster H. Carnitin and cardiovascular diseases. — Ponte Press Verlags-GmbH, Bochum, 2003.
13. Borum P.R. Carnitine function / Ed. by P.R. Borum // Clinical Aspects of Human Carnitine Deficiency. — Elmsford, NY: Pergamon Press, 1986. —16-27.
14. DeVivo D.C., Tein I. Primary and secondary disorders of carnitine metabolism // Int. Pediatr. 1990; 5: 134-41.
15. Ahmad S. L-carnitine in dialysis patients // Seminars in Dialysis. 2001; 14(3): 209-217.
16. Scholte H.R., Pereira R.R., de Jonge P.C., Luyt-Houwen I.E.M., Hedwig M., Verduin M., Ross J.D. Primary carnitine deficiency // J. Clin. Chem. Clin. Biochem. 1990; 28: 351-357.
17. Tanphaichitr V., Leelahagul P. Carnitine metabolism and human carnitine deficiency // Nutrition. 1993; 9: 246-254.
18. Reddi A.S., Moquete M., Keshav G., DeAngelis B., Frank O., Baker H. Plasma Carnitine Levels in Patients Undergoing Hemodialysis Departments of Medicine and Preventive Medicine and Community Health, UMDNJ-New Jersey Medical School. — Newark, N.J., USA: Nephron, 1998. — 80. — 87-88.
19. Evans A.M., Faull R.J., Nation R.L., Prasad S., Elias T., Reuter S.E., Fornasini G. Impact of hemodialysis on endogenous plasma and muscle carnitine levels in patients with end-stage renal disease // Kidney Int. 2004; 66 (4): 1527-1534.
20. Moorthy A.V., Rosenblum M., Rajaram R., Smug A.L. A comparison of plasma and muscle carnitine levels in patients on peritoneal or hemodialysis for chronic renal failure // Am. J. Nephrol. 1983; 3: 205-208.
21. Leschke M., Rumpf K.W., Eisenhauer T., Fuchs C., Becker K., Kothe U., Scheler F. Quantitative assessment of carnitine loss during hemodialysis and hemofiltration // Kidney Int. 1983; Suppl. 16: S143-S146.
22. Zilleruelo G., Novak M., Hsia S.L., Goldberg R., Abitbol C., Monkus E., Strauss J. Effect of dialysate composition on the lipid response to L-carnitine supplementation // Kidney Int. 1989; Suppl. 27: S259-S263.
23. Borum P.R., Taggart E.M. Carnitine nutriture of dialysis patients // J. Am. Diet. Assoc. 1986; 86: 644-647.
24. Bohmer T., Bergrem H., Eiklid K. Carnitine deficiency induced during intermittent haemodialysis for renal failure // Lancet. 1978; 8056: 126-128.
25. US Renal Data System: Excerpts from the USRDS2001 Annual Data Report: Atlas of end-stage renal disease in the United States // Am. J. Kidney Dis. 2001; 38 (suppl. 3): S135-S146.
26. Pauly D.F., Pepine C.J. The role of carnitine in myocardial dysfunction // Am. J. Kidney Dis. 2003; 41 (suppl. 4): S35-S43.
27. Suzuki Y., Narita M., Yamazaki M. Effects of L-carnitine on arrhythmias during hemodialysis // Jpn Heart. 1982; J 23: 349-359.
28. Kudoh Y., Shoji T., Oimatsu H., Yoshida S., Kikuchi K., Iimura O. The role of L-carnitine in the pathogenesis of cardiomegaly in patients with chronic hemodialysis // Jpn Circ. J. 1983; 47: 1391-1397.
29. Chan M.K., Persaud J.W., Varghese Z., Baillod R.A., Moorhead J.F. Response patterns to DL-carnitine in patients on maintenance haemodialysis // Nephron. 1982; 30: 240-243.
30. Elisaf M., Bairaktari E., Katopodis K., Pappas M., Sferopoulos G., Tzallas C., Tsolas O., Siamopoulos K.C. Effect of L-carnitine supplementation on lipid parameters in hemodialysis patients // Am. J. Nephrol. 1998; 18: 416-421.
31. Bertoli M., Battistella P.A., Vergani L., Naso A., Gasparotto M.L., Angelini C. Carnitine deficiency induced during hemodialysis and hyperlipidemia: effect of replacement therapy // Amer. J. Clin. Nutr. 1981; 34: 1496-1500.
32. Lacour B., Di Giijlio S., Chanard J., Ciancioni C., Haguet M., Lebkiri B., Basile C., Drueke T., Assam R., Funck-Brentano J.L. Carnitine improves lipid anomalies in haemodialysis patients // Lancet. 1980; 11 (8198): 763-764.
33. Vacha G.M., Giorcelli G., Siliprandi N., Corsi M. Favorable effects of L-carnitine treatment on hypertriglyceridemia in hemodialysis patients: decisive role of low levels of high-density lipoprotein-cholesterol // Am. J. Clin. Nutr. 1983; 38: 532-540.
34. Kavadias D., Fourtounas C., Tsouchnikas J., Barboutis K.
L-carnitine and erythropoietin requirements in hemodialysis patients // Am. J. Kidney Dis. 1996; 28: 156.
35. Vesela E., Racek J., Trefil L., Jankovy’ch V., Pojer M. Effect of L-carnitine supplementation in hemodialysis patients // Nephron. 2001; 88: 218-223.
36. Boran M., Dalva I., Gonenc F., Cetin S. Response to recombinant human erythropoietin (r-Hu EPO) and Lcarnitine combination in patients with anemia of endstage renal disease // Nephron. 1996; 73: 314-315.
37. Labonia W.D. L-carnitine effects on anemia in hemodialyzed patients treated with erythropoietin // Am. J. Kidney Dis. 1995; 26: 757-764.
38. Eknoyan G., Lindberg J.S. On the evolving nature of understanding dialysis-related disorders // American Journal of Kidney Disease. 2003; 41 (suppl. 4): S1-S3.
39. Ahmad S., Brass E., Hoppel C., Koople J., Lasagna L., Lundin A.P., Schreiner G., Sheridan M. Consensus Group Statement: Role of carnitine in treating renal dialysis patients // Dial. Transpl. 1994; 23: 177-181.
40. Schreiber B., Lewis V. Management of carnitine deficiency in ESRD patients undergoing dialysis: challenges and considerations // Dialysis & Transplantation. 2001; 30: 207-212.
41. NKF-DOQI Clinical Practice Guidelines for Nutrition in Chro–nic Renal Failure. — New York, National Kidney Foundation, 2000.
42. National Kidney Foundation Carnitine Consensus Conference Practice Recommendations // American Journal of Kidney Diseases. 2003; 41: 868-876.
43. Chazot C., Jean G., Vo Van C., Charra B., Terrat J.C., Laurent G. Serum carnitine as a marker of protein malnutrition (Abstract) // J. Am. Soc. Nephrol. 1997; 8: 230A