Введение
Системная красная волчанка (СКВ), ревматоидный артрит (РА), геморрагический васкулит Шенлейна — Геноха (ВШГ) и микроскопический полиангиит (МПА) объединены в группу системных аутоиммунных ревматических заболеваний (СРЗ) [11, 13, 15], распространенность которых повсеместно растет [21]. Общностью этих болезней считается наличие в крови различных аутоантител [26] и изменений со стороны сосудов почек [2]. Ангиопатия является одним из основных проявлений СКВ [3, 17] и РА [1, 5, 10], а что касается больных ВШГ и МПА, то воспалительный сосудистый процесс фигурирует уже в самом определении названий заболеваний [12, 22].
Патогенез повреждений сосудов почек при волчаночном и ревматоидном гломерулонефритах (ВГН и РГН) остается изученным недостаточно [20, 25], хотя тяжесть такой васкулопатии определяет прогноз как СКВ [23], так и РА [18]. Сказанное в полной мере относится и к пациентам, страдающим ВШГ и МПА [14, 24].
Необходимо отметить, что для СРЗ свойственны нарушения функции эндотелия сосудов [6, 27] с гиперпродукцией сосудистого эндотелиального фактора роста (VEGF), эндотелина-1 (ЕТ1) и Е-селектина (ЕSel) [4, 16]. Эти процессы играют немаловажную роль в повреждении при СРЗ клубочковых капилляров и артериол почек [7], что доказано экспериментальными исследованиями на животных [19]. В первую очередь именно почечный эндотелий реагирует на системную эндотелиальную дисфункцию сосудов (ЭДС) в организме больных [8, 9]. Вместе с тем характер морфологических изменений эндотелия капилляров и артериол почек при СКВ, РА, ВШГ и МПА изучен недостаточно, требуют выяснения патогенетические механизмы сосудистой депозиции иммунных компонентов, взаимосвязь с клинико-лабораторными факторами течения заболеваний и влияние системной ЭДС. Сказанное стало целью и задачами данного исследования.
Материалы и методы
Проанализированы результаты нефробиопсии и данные лабораторного исследования эндотелиальной функции сосудов у 94 больных с СРЗ, среди которых 41 человек страдал СКВ, 17 — РА, 24 — ВШГ и 12 — МПА. Соотношение мужчин и женщин в этих группах составило соответственно 1 : 7, 1 : 2, 2 : 1 и 1 : 3, средний возраст обследованных — 37,60 ± 1,63, 50,10 ± 2,33, 27,50 ± 2,19 и 40,50 ± 3,70 года, длительность заболевания от его манифестации — 11,90 ± 1,28, 12,40 ± 1,99, 10,20 ± 1,77, 4,00 ± 1,02 года, распределение пациентов по І, ІІ и ІІІ степени активности патологического процесса — 1 : 2 : 3, 1 : 2 : 2, 2 : 1 : 1, 1 : 2 : 9. При СКВ хроническое течение встречалось в 5 раз чаще, чем подострое, при РА соотношение I : II : III : IV стадий болезни было как 2 : 9 : 5 : 1, показатель активности артрита DAS составил 4,90 ± 0,30 о.е., а индекс Лансбури — 155,80 ± 13,35 балла, при ВШГ сугубо почечная форма заболевания, кожно-суставно-почечная, кожно-почечная, суставно-почечная, кожно-суставно-абдоминально-почечная, кожно-абдоминально-почечная, суставно-абдоминально-почечная и абдоминально-почечная по частоте соотносились 20 : 13 : 11 : 8 : 6 : 3 : 2 : 1. Клиническими сосудистыми проявлениями СРЗ считали наличие кожной пурпуры, телеангиэктазий, капилляритов кистей и стоп, антифосфолипидного синдрома, синдрома Рейно, увеита, хейлита, лейкоцитокластической энантемы, периферической вазонейропатии, дисциркуляторной энцефалопатии и легочной гипертензии, степень которых оценивали в баллах от 1 до 3 (с градациями «минимальная», «умеренная», «выраженная»). Изучали индекс клинического течения ангиопатии (Ω) по формуле: Ω = (Σ : E) × √Y, где Σ — сумма баллов всех клинических признаков СРЗ, E — число признаков, Y — степень активности заболевания.
Больным выполняли эхокардиографию (Acuson-Aspen-Siemens, Германия, и HD-11-XE-Philips, Нидерланды), ультразвуковую допплерографию плечевых артерий (Aplia-XG-Toshiba, Япония) и биомикроскопию сосудов конъюнктивы (щелевая лампа Haag-Streit-Bern-900, Швейцария). Определяли также инструментальный сосудистый индекс (Ψ), при этом средний показатель у больного (X) c его стандартным отклонением (ς) оценивали в 1 балл в случаях < X + ς, при X + ς ↔ X + 2ς — в 2 балла, при X + 2ς ↔ Х + 3ς — в 3 балла, при > Х + 3ς — в 4 балла. Высчитывали Ψ на одного больного по формуле: Ψ = (A + 2B + 3Г + 4∆) : E, где А, В, Г, ∆ — число больных соответственно с 1, 2, 3 и 4 баллами, E — число показателей, среди которых учитывалось следующие: среднее периферическое артериальное и легочное давление, периферическое и легочное сосудистое сопротивление, сосудистый вегетативный индекс, диаметр устья аорты, исходный диаметр (ДИ) плечевой артерии и ее диаметр во время вазодилатации (ДВ), степень вазодилатации, индекс напряжения сосудистой стенки, интравазальный, вазальный и экстравазальный конъюнктивальные индексы.
С помощью биохимического анализатора Olympus-AU-640 (Япония) исследовали в крови концентрации креатинина, иммуноглобулина (Ig) A и ревматоидного фактора (RF), иммуноферментным методом (ридер PR2100 Sanofi diagnostic pasteur, Франция) изучали уровни антител к нативной дезоксирибонуклеиновой кислоте (aDNA), кардиолипину (aCL), циклическому цитруллиновому пептиду (aCCP), показатели VEGF, ET1, тромбоксана А2 (TxA2), гомоцистеина (HCys), простациклина (PgI2), циклического гуанозинмонофосфата (cGMP), ESel, Р-селектина (PSel), а иммуноблотовым методом (аппарат Euroline-Euroimmun, Германия) определяли параметры антинуклеарного фактора (ANF) и антинейтрофильных цитоплазматических антител (ANCA) — к миелопероксидазе (аМР) и протеиназе-3 (аР3). Серопозитивность СКВ по наличию ANF встречалась у 85,4 % от числа больных, по aDNA — у 68,3 % и по aCL — у 31,7 %, серопозитивность РА по RF (> 14 МЕ/мл) — у 53 % и по aCCP (> 17 Е/мл) — у 94,1 %, серопозитивность ВШГ по IgA (> 3 ммоль/л) — у 41,7 % и по RF — у 29,2 %, серопозитивность МПА по ANCA была во всех случаях, а соотношение aMP к aP3 составило 5 : 1. Во время оценки функционального состояния почек использовалось определение скорости клубочковой фильтрации (СКФ) по формуле Кокрофта — Голта. Для изучения интегрального показателя ЭДС (Θ) высчитывали степень изменения (∆) показателей вазоконстрикторов — VEGF, ЕТ1 и ТхА2, а также вазодилататора PgI2 по формуле: Х = [(П1 – П2) : ς]2, где П1 и П2 — показатели у больных и здоровых, ς — стандартное отклонение у здоровых. Θ определяли по формуле: Θ = √(K + L + M) : N, где К — VEGF, Λ — ET1, М — TxA2, N — PgI2 (ЭДС диагностировали при Θ > 5 о.е.). В качестве контроля лабораторные показатели исследованы у 30 практически здоровых людей (13 мужчин и 17 женщин в возрасте 18–65 лет).
Нефробиопсию выполняли на фоне атаралгезии под контролем ультразвукового исследования почки. Использовалась методика True-Cut («настоящего среза») с применением высокоскоростного пистолета Biopty-Bard. Гистологические срезы почек окрашивали гематоксилином-эозином, альциановым синим (на гликопротеиды) и по Ван Гизону (коллагеновые и эластические волокна), ставилась PAS-реакция. Кроме того, проводили иммуноферментный (с пероксидазной меткой) и иммунофлюоресцентный методы исследования тканей почек. Изучали отложения IgA, IgG, IgM, C3- и Cq1-компонентов комплемента. Микроскопическое исследование осуществляли на микроскопах Olympus-AX40 и Olympus-AX70-Provis с цифровой видеокамерой Olympus-DP50. Поражение отдельных почечных структур (клубочков, канальцев, стромы, сосудов) оценивали в баллах (от 0 до 3). При этом подсчитывали средний показатель повреждений (ϑ) по формуле: ϑ = (a + 2b + 3g) : (a + b + g + δ), где a, b, g — число больных с 1, 2 и 3 баллами, а δ — число больных с отсутствием данного признака.
Биопсия почки проведена только пациентам с наличием протеинурии; нефротический синдром был у 4 больных СКВ и соответственно у 2 РА и ВШГ. Соотношение ХБП I, II, III и IV стадий при СКВ составило 10 : 7 : 2 : 1, при РА — 9 : 5 : 2 : 1, при ВШГ — 4 : 4 : 1 : 1, при МПА — 5 : 4 : 2 : 1, а средняя СКФ в этих группах оказалась примерно одинаковой, составляя 96,10 ± 4,17, 97,00 ± 7,35, 100,70 ± 3,61, 88,40 ± 7,12 мл/мин/1,73 м2. При РА из разработки исключены пациенты с вторичным АА-амилоидозом почек, а в группу обследования вошли лица, страдающие РГН в соотношении мезангиопролиферативный к мезангиокапиллярному РГН как 2 : 1. Распределение частоты II : III : V : IV классов ВГН составляло 1 : 2 : 4 : 13, а V : VI : IV : III : II типов геноховского гломерулонефрита (ГГН) при ВШГ — 1 : 3 : 4 : 6 : 10. Следует подчеркнуть, что у всех 94 обследованных пациентов с СРЗ имели место тубулоинтерстициальные изменения в почках.
Статистическая обработка полученных результатов исследований проведена путем компьютерного вариационного, непараметрического, корреляционного, регрессионного, одно- (ANOVA) и многофакторного (ANOVA/MANOVA) дисперсионного анализа (программы Microsoft Excel и Statistica StatSoft, США). Оценивали средние значения (Х), их стандартные отклонения (ς) и ошибки (µ), коэффициенты параметрической корреляции Пирсона (r) и непараметрической Кендалла (τ), критерии дисперсии Брауна — Форсайта (BF), множественной регрессии (R), Стьюдента, Уилкоксона — Рао (WR), Макнемара — Фишера и достоверность статистических показателей (р).
Результаты и обсуждение
Обращал на себя внимание факт определенных количественных отличий характера сосудистых повреждений почек при отдельных СРЗ. Так, ϑ у больных РА составил 0,430 ± 0,050 о.е., в случаях ВШГ — 0,690 ± 0,059 о.е., СКВ — 0,890 ± 0,043 о.е., МПА — 1,010 ± 0,130 о.е. При этом ЭДС констатирована у 35,3, 51,9, 39 и 100 % от числа обследованных, а Θ составил 4,50 ± 0,36, 5,30 ± 0,35, 4,80 ± 0,14 и 6,50 ± 0,55 о.е. Таким образом, наименее существенные сосудистые изменения наблюдались при РА, а самые выраженные — при МПА. Только группы больных МПА и СКВ не отличались между собой по частоте иммунных депозитов в сосудах почек, что продемонстрировал выполненный анализ Макнемара — Фишера.
Частота отдельных морфологических признаков поражения эндотелия сосудов при СРЗ представлена в табл. 1. Пролиферация эндотелия капилляров в большей степени была присущей СКВ и МПА, а эндотелия артериол — только МПА, тогда как такие изменения для РА оказались нехарактерными. Как и предполагалось, депозиты IgA в сосудах были наиболее типичны для ГГН, а C1q — для ВГН и МПА.
С показателем Ψ при СРЗ слабо связаны морфологические признаки поражения почечного эндотелия, в свою очередь, Ω оказывает существенное влияние на депозицию IgA в капиллярах клубочков (BF = 2,78, p = 0,048) и артериолах (BF = 3,49, p = 0,019), а также отложений в последних IgG (BF = 2,99, p = 0,036), что показал дисперсионный анализ Брауна — Форсайта. По данным анализа Кендалла, существуют прямые корреляционные связи значений Ω с частотой депозиций IgA как в капиллярах (τ = +0,187, p = 0,005), так и в артериолах почек (τ = +0,141, p = 0,036). С учетом сказанного показатель Ω > 1,5 о.е. (> Х + ς больных СРЗ) является фактором риска высокого уровня отложений IgA в эндотелии почечных сосудов.
/65-1.gif)
Как свидетельствует выполненный ANOVA/MANOVA, нозологические формы СРЗ оказывают высокодостоверное (p < 0,001) воздействие на интегральное состояние эндотелия капилляров (WR = 3,60) и артериол (WR = 2,29). По результатам многофакторного анализа Уилкоксона — Рао, поражения эндотелия капилляров и артериол почек зависят от тяжести течения кожного синдрома (соответственно WR = 2,49, p = 0,002, и WR = 2,05, p = 0,027), а также периферической нейропатии (WR = 1,92, p = 0,022, и WR = 1,97, p = 0,035). Кроме того, пролиферация эндотелия артериол и формирование в нем иммунных депозитов тесно связаны с лейкоцитокластической энантемой (WR = 2,31, p = 0,014) и капилляритами кистей и стоп (WR = 1,85, p = 0,049).
Однофакторный дисперсионный анализ Брауна — Форсайта показал, что на ϑ при ВГН влияют значения сосудисто-вегетативного индекса (BF = 4,24, p = 0,046), а при МПА — Ω (BF = 4,49, p = 0,045). Кроме того, ϑ у больных РГН имеют место прямые корреляционные связи Пирсона с уровнями Ω (r = +0,671, p = 0,003), Ψ (r = +0,754, p < 0,001) и интраваскулярного конъюнктивального индекса (r = +0,501, p = 0,041), а в случаях ГГН — только с Ψ (r = +0,447, p = 0,029), что нашло свое отражение на рис. 1, 2. При МПА (рис. 3) ϑ обратно коррелирует с показателями ДИ (r = –0,603, p = 0,038) и ДВ (r = –0,640, p = 0,025).
/66-1.gif)
Наличие ЭДС в целом оказывает воздействие на характер изменений эндотелия артериол (WR = 1,47, p = 0,046). У больных СКВ показатели системной ЭДС влияют на повреждения эндотелия капилляров (WR = 2,95, p = 0,042), что подтверждает и прямая зависимость интегральных морфологических показателей от Θ (R = +7,42, p < 0,001). Кроме того, анализ множественной регрессии установил позитивную связь Θ с изменениями эндотелия капилляров и артериол при ВШГ (соответственно R = +2,98, p = 0,008, и R = +9,73, p < 0,001) и МПА (R = +6,81, p = 0,001, и R = +6,50, p = 0,002).
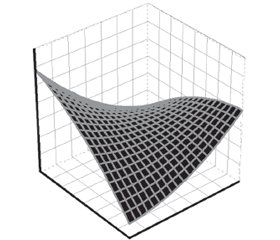
Показатели эндотелиальной функции сосудов у здоровых людей контрольной группы и больных СРЗ нашли свое отражение в табл. 2. Общими чертами для всех СРЗ являлись достоверно высокие показатели в крови ET1, HCys, cGMP и PSel на фоне неизмененной концентрации ТхА2. При этом только для РА оказалось нетипичным повышение содержания VEGF и лишь в этой группе констатировано уменьшение ESel. Трехмерные интегральные гистограммы вазоконстрикторов (VEGF + ET1 + TxA2) в крови здоровых и больных СРЗ с поражением почек представлены на рис. 4.
У больных ВГН показатель Θ влияет на пролиферацию эндотелия и капилляров клубочков (BF = 3,38, p = 0,028), и артериол (BF = 3,25, p = 0,033), что демонстрирует дисперсионный анализ Брауна — Форсайта. В свою очередь, при РГН такая связь касается только эндотелия артериол (BF = 10,81, p = 0,002), при МПА — лишь капилляров (BF = 5,29, p = 0,027), а в случаях ГГН зависимости изменений эндотелия сосудов почек от Θ вообще не выявлено.
C Θ при ВГН тесно связаны отложения в эндотелии капилляров клубочков С3 (BF = 3,96, p = 0,015), при ГГН — IgM (BF = 3,19, p = 0,048), а при МПА — IgA (BF = 7,99, p = 0,010), IgG (BF = 4,42, p = 0,041), IgM (BF = 4,26, p = 0,045), C1q (BF = 20,24, p < 0,001). Депозиты в артериолах почек при СКВ касаются C1q (BF = 23,63, p < 0,001), при ВШГ — IgA (BF = 6,84, p = 0,002), IgG (BF = 9,76, p < 0,001) и C1q (BF = 24,48, p < 0,001), при РА — IgA (BF = 4,47, p = 0,032), IgG (BF = 3,39, p = 0,048), IgM (BF = 19,74, p = 0,001), C3 (BF = 9,65, p = 0,007) и C1q (BF = 9,65, p = 0,007). Таким образом, ЭДС принимает участие в процессах депозиции иммуноглобулинов и компонентов комплемента в эндотелии сосудов почек при всех СРЗ, но РА свойственны отложения исключительно в артериолах, а МПА — в капиллярах клубочков.
Помимо дисперсионной связи, депозиция в эндотелии капилляров C3 при СКВ и С1q у больных МПА прямо коррелирует с параметром Θ, что отражает анализ Кендалла (соответственно τ = +0,224, р = 0,045, и τ = +0,464, р = 0,036). В связи с этим можно считать, что Θ > 4 o.e. в случаях ВГН и Θ > 8 o.e. при МПА (> Х + ς соответствующих больных) являются прогнознегативными критериями отложений компонентов комплемента в капиллярах клубочков.
Мы отобрали те показатели эндотелиальной функции сосудов в крови, с которыми отдельные морфологические признаки изменений сосудистого эндотелия почек одновременно имели и дисперсионные, и корреляционные связи. Так, при ВГН степень пролиферации эндотелия капилляров клубочков прямо зависит от содержания ЕТ1 (BF = 3,16, p = 0,036; τ = +0,261, p = 0,016), а эндотелия артериол — от ESel (BF = 3,06, p = 0,040; τ = +0,234, p = 0,031). Отложения IgG в капиллярах и артериолах у больных РГН тесно связаны с концентрацией PSel (соответственно BF = 9,84, p = 0,002; τ = +0,389, p = 0,029, и BF = 16,66, p < 0,001; τ = +0,369, p = 0,039), а IgA при ГГН — с уровнем HCys (BF = 7,78, p = 0,003; τ = +0,449, p = 0,002, и BF = 4,05, p = 0,033; τ = +0,390, p = 0,030). У пациентов, страдающих МПА, на пролиферацию клубочкового эндотелия влияют значения VEGF (BF = 27,64, p < 0,001; τ = +0,436, p = 0,049). Можно считать, что перечисленные факторы ЭДС участвуют в патогенетических механизмах повреждений сосудов почек при тех или иных СРЗ.
Выводы
1. ЭДС в виде дисбаланса вазоконстрикторов VEGF, ET1, TxA2 и вазодилататора PgI2 возникает у 35 % от числа больных РА с поражением почек, у 39 % — СКВ, у 52 % — ВШГ и у 100 % — МПА, участвуя в патогенезе изменений эндотелия капилляров клубочков и артериол.
2. Морфологические повреждения эндотелия почечных сосудов тесно связаны с тяжестью клинико-инструментальных признаков системной экстраренальной ангиопатии (с поражением кожи, слизистых оболочек и периферической нервной системы, с параметрами биомикроскопии сосудов конъюнктивы и вазодилатации плечевой артерии).
3. Пролиферацию клубочкового эндотелия у больных МПА определяет сывороточная концентрация VEGF, а в развитии почечных иммунных эндотелиальных депозитов (IgA, IgG, IgM, C3, C1q) при ВГН участвуют ЕТ1 и ESel, при РГН — PSel, при ГГН — HCys.
Конфликт интересов. Авторы заявляют об отсутствии какого-либо конфликта интересов при подготовке данной статьи.
Список литературы
1. Baerwald C. Extra-articular manifestations of rheumatoid arthritis / C. Baerwald, C. Kneitz, M. Bach, M. Licht // Z. Rheumatol. — 2012. — Vol. 71, № 10. — P. 841-849.
2. De Groot K. Renal manifestations in rheumatic diseases / K. De Groot // Internist. — 2009. — Vol. 48, № 8. — P. 779-785.
3. Dey-Rao R. Genome-wide transcriptional profiling data from chronic cutaneous lupus erythematosus (CCLE) peripheral blood / R. Dey-Rao, A.A. Sinha // Data Brief. — 2014. — Vol. 11, № 2. — P. 39-41.
4. Ding Y. Association of miRNA‑145 expression in vascular smooth muscle cells with vascular damages in patients with lupus nephritis / Y. Ding, W. Liao, Z. Yi [et al.] // Int. J. Clin. Exp. Pathol. — 2015. — Vol. 8, № 10. — P. 12646-12656.
5. Elshabrawy H.A. The pathogenic role of angiogenesis in rheumatoid arthritis / H.A. Elshabrawy, Z. Chen, M.V. Volin [et al.] // Angiogenesis. — 2015. — Vol. 18, № 4. — P. 433-448.
6. Ferrante A. Endothelial progenitor cells: Are they displaying a function in autoimmune disorders? / A. Ferrante, G. Guggino, D. Di Liberto [et al.] // Mech. Ageing. Dev. — 2016. — Vol. 3, № 5. — P. 122-128.
7. Fujita E. Glomerular capillary and endothelial cell injury is associated with the formation of necrotizing and crescentic lesions in crescentic glomerulonephritis / E. Fujita, K. Nagahama, A. Shimizu [et al.] // J. Nippon Med. Sch. — 2015. — Vol. 82, № 1. — P. 27-35.
8. González-Suárez I. Brain microvasculature involvement in ANCA positive vasculitis / I. González-Suárez, J. Arpa, J.J. Ríos-Blanco // Cerebrovasc. Dis. — 2016. — Vol. 41, № 5–6. — P. 313-321.
9. Guo L. Anti-endothelin receptor type a autoantibodies in systemic lupus erythematosus-associated pulmonary arterial hypertension / L. Guo, M. Li, Y. Chen [et al.] // Arthritis Rheumatol. — 2015. — Vol. 67, № 9. — P. 2394-2402.
10. Haavisto M. Influence of triple disease modifying anti-rheumatic drug therapy on carotid artery inflammation in drug-naive patients with recent onset of rheumatoid arthritis / M. Haavisto, A. Saraste, L. Pirilä [et al.] // Rheumatology. — 2016. — Vol. 55, № 10. — P. 1777-1785.
11. Heijnen T. Outcome of patients with systemic diseases admitted to the medical intensive care unit of a tertiary referral hospital: a single-centre retrospective study / T. Heijnen, A. Wilmer, D. Blockmans, L. Henckaerts // Scand. J. Rheumatol. — 2016. — Vol. 45, № 2. — P. 146-150.
12. Hoffman G.S., Calabrese L.H. Vasculitis: determinants of disease patterns / G.S. Hoffman, L.H. Calabrese // Nat. Rev. Rheumatol. — 2014. — Vol. 10, № 8. — P. 454-462.
13. Holle J.U. ANCA-associated vasculitis / J.U. Holle // Internist. — 2015. — Vol. 56, № 1. — P. 41-50.
14. Iwasaki S. Fatal cardiac small-vessel involvement in ANCA-associated vasculitis: an autopsy case report / S. Iwasaki, A. Suzuki, T. Fujisawa [et al.] // Cardiovasc. Pathol. — 2015. — Vol. 24, № 6. — P. 408-410.
15. Kuo C.F. Familial aggregation of systemic lupus erythematosus and coaggregation of autoimmune diseases in affected families / C.F. Kuo, M.J. Grainge, A.M. Valdes [et al.] // JAMA Intern. Med. — 2015. — Vol. 175, № 9. — P. 1518-1526.
16. Latuskiewicz-Potemska J. Nailfold capillaroscopy assessment of microcirculation abnormalities and endothelial dysfunction in children with primary or secondary Raynaud syndrome / J. Latuskiewicz-Potemska, A. Chmura-Skirlinska, R.J. Gurbiel, E. Smolewska // Clin. Rheumatol. — 2016. — Vol. 35, № 8. — P. 1993-2001.
17. Maldonado A. Medium vessel vasculitis in systemic lupus erythematosus / A. Maldonado, J.N. Blanzari, P. Asbert [et al.] // Rev. Fac. Cien. Med. Univ. Nac. Cordoba. — 2016. — Vol. 73, № 1. — P. 50-52.
18. Marszałek A. Patient with rheumatoid arthritis and acute renal failure: a case report and review of literature / A. Marszałek, N. Skoczylas-Makowska, A. Kardymowicz, J. Manitius // Pol. J. Pathol. — 2010. — Vol. 61, № 4. — P. 229-233.
19. Palma Zochio Tozzato G. Collagen-induced arthritis increases inducible nitric oxide synthase not only in aorta but also in the cardiac and renal microcirculation of mice / G. Palma Zochio Tozzato, E.F. Taipeiro, M.A. Spadella [et al.] // Clin. Exp. Immunol. — 2016. — Vol. 183, № 3. — P. 341-349.
20. Petrucci I. Clinical scenarios in chronic kidney disease: parenchymal chronic renal diseases / I. Petrucci, S. Samoni, M. Meola [et al.] // Contrib. Nephrol. — 2016. — Vol. 188. — P. 98-107.
21. Ramos-Casals M. Google-driven search for big data in autoimmune geoepidemiology: analysis of 394,827 patients with systemic autoimmune diseases / M. Ramos-Casals, P. Brito-Zerón, B. Kostov [et al.] // Autoimmun. Rev. — 2015. — Vol. 14, № 8. — P. 670-679.
22. Rawlings C.R. A rheumatology perspective on cutaneous vasculitis: assessment and investigation for the non-rheumatologist / C.R. Rawlings, G.A. Fremlin, J. Nash, K. Harding // Int. Wound J. — 2016. — Vol. 13, № 1. — P. 17-21.
23. Song D. The spectrum of renal thrombotic microangiopathy in lupus nephritis / D. Song, L.H. Wu, Wang, // Arthritis Res. Ther. — 2013. — Vol. 15, № 1. — R. 12.
24. Tesar V. Conventional induction and maintenance treatment of antineutrophil cytoplasmic antibodies-associated vasculitis — still of value for our patients? / V. Tesar, Z. Hruskova // Expert. Opin. Pharmacother. — 2015. — Vol. 16, № 11. — P. 1683-1702.
25. Wilhelmus S. The Revisited classification of GN in SLE at 10 years: Time to re-eEvaluate histopathologic lesions / S. Wilhelmus, C.E. Alpers, H.T. Cook [et al.] // J. Am. Soc. Nephrol. — 2015. — Vol. 26, № 12. — P. 2938-2946.
26. Yang Z. Prevalence of systemic autoimmune rheumatic diseases and clinical significance of ANA profile: data from a tertiary hospital in Shanghai, China / Z. Yang, Y. Ren, D. Liu [et al.] // APMIS. — 2016. — Vol. 124, № 9. — P. 805-811.
27. Yildiz A. Diastolic dysfunction and endothelial dysfunction in systemic lupus erythematosus / A. Yildiz, S. Soydinc // Rheumatol. Int. — 2015. — Vol. 35, № 7. — P. 1281-1282.

/65-1.gif)
/66-1.gif)
/67-1.gif)