Введение
В настоящее время в мире сохраняется актуальность проблемы мозгового инсульта (МИ), обусловленная увеличением числа перенесших это заболевание в течение последних 50 лет. В мире ежегодно происходит больше 16 млн инсультов и 6 млн человек умирает вследствие их. Заболеваемость инсультом в разных странах возрастает в зависимости от экономической ситуации на 40–100 % [1, 2]. По данным статистики Министерства здравоохранения, в 2015 году в Украине произошло 96 319 случаев инсульта, что на 100 тыс. населения составляет 274,1. В результате инсульта за истекший период в Украине умерло 33 753 человека, что на 100 тыс. населения составляет 78,9 [3]. За последние десятилетия значительно выросла когорта населения, потенциально предрасположенная к МИ. Несмотря на то что в ряде развитых стран Европы прогнозируется снижение заболеваемости инсультом, ожидается, что общее число больных с МИ увеличится через 20 лет на 11 %, главным образом из-за постарения населения [4, 5].
Из числа выживших больше 60 % перенесших МИ становятся инвалидами, причем значительная их часть зависят от окружающих или нуждаются в постороннем уходе [1, 2].
Одной из причин инвалидизации постинсультных больных являются двигательные нарушения. До 50–70 % больных, перенесших инсульт, имеют нарушения двигательной функции руки в виде пареза или параличей. По данным проведенных Регистров инсульта, к концу острого периода МИ гемипарез наблюдается у 80 % больных, среди них гемиплегия — в 11 % случаев, значительно выраженный гемипарез — в 11 %, умеренный и легкий — в 59 % случаев [6–9].
Наряду с двигательным дефицитом существенно влияет на инвалидизацию пациентов спастичность, которая имеет место более чем у половины больных, перенесших инсульт [10, 11]. По данным разных исследований, распространенность постинсультной спастичности варьирует от 4 до 42,6 %, что связано с разной выборкой пациентов. Так, по данным Йорга Виззеля (2013 г.), спастичность развивается через 1–4 нед. после инсульта у 4–27 % пациентов, через 1–3 мес. — у 19–26,7 %, более 3 мес. — у 17–42,6 % [12]. В среднем от 25 до 43 % больных в течение года после инсульта страдают спастичностью.
В развитии спастичности после инсульта центральную роль играет ослабление тормозного воздействия на альфа-мотонейроны, которые управляют мышцами, противодействующими силам гравитации.
Результаты большинства проведенных исследований свидетельствуют о том, что степень выраженности спастичности зависит от локализации очага поражения, изначальной глубины пареза и симптомов, сочетающихся с парезом (чувствительные нарушения на стороне паралича, мозжечковые симптомы). Предикторами развития спастичности являются: низкие баллы по шкале Бартел; постинсультная боль; сенсорный дефицит; выраженный парез [9]. Чаще всего спастичность оказывается одновременно в верхней и нижней конечностях (68 %), однако возможно и изолированное появление этого симптома в руке (15 %) или ноге (18 %) [13]. Для «пирамидной» гипертонии при инсульте характерно повышение тонуса преимущественно в определенных мышечных группах. На верхних конечностях это пронаторы и сгибатели предплечья, кисти, пальцы, на нижних конечностях — разгибатели голени, сгибатели стопы. Вследствие этого возникают типичные позы с характерным внешним видом пациента (поза Вернике — Манна), что не только значительно усложняет самообслуживание больного, но и может приводить к падениям [14].
Спастичность в паретичных конечностях нарастает после инсульта на протяжении нескольких недель и часто ухудшает двигательные функции, обусловливая развитие контрактур и деформации конечностей. Также спастичность мешает осуществлению ухода за обездвиженным больным и может сопровождаться болезненными мышечными спазмами. Сравнительно редко спастичность может проходить спонтанно, обычно это бывает при восстановлении двигательной активности в конечностях. При длительной (несколько месяцев) сохранности пареза после инсульта возможно развитие структурных изменений в спинном мозге — укорочения дендритов альфа-мотонейронов, коллатерального ветвления афферентных волокон, что способствует дальнейшему усугублению спастичности. К тому же вторичные изменения возникают и в мышцах, сухожилиях, суставах в пораженной парезом области, что усугубляет двигательные расстройства.
Таким образом, повышение мышечного тонуса существенно влияет на процесс восстановления нарушенных функций. Однако некоторое повышение мышечного тонуса может иметь компенсаторное значение при параличе. Поэтому, прежде чем начать лечение, необходимо решить, насколько необходимо и целесообразно снижение мышечного тонуса конечности [15].
Лечение обусловленной перенесенным инсультом спастичности лучше начинать как можно раньше, поскольку вероятность достижения эффекта лечения тем выше, чем меньше времени прошло после инсульта.
В комплекс мероприятий по борьбе со спастичностью необходимо включать физиотерапию, гидропроцедуры, лечение положением, специальные лечебно-гимнастические приемы, направленные на расслабление, биологическую обратную связь, избирательный массаж, иглорефлексотерапию, фармакотерапию. Менеджмент спастичности включает следующие позиции: активные упражнения прогрессивного сопротивления, программы аэробных упражнений, Бобат-подход (нейроразвивающая терапия), нейромышечная электростимуляция, частичная поддержка веса тела, механический тренер ходьбы, ментальные практики; пассивные движения и растяжки суставов (динамические/статические), статическое позиционирование, аппараты непрерывного пассивного движения (СРМ), рефлекс-ингибирующее лонгетирование; дополнительные — криотерапия, теплолечение, инфракрасная термотерапия, гидротерапия, ультразвук, ударно-волновая терапия, чрескожная электростимуляция нервов (TENS), электростимуляция, основанная на биологической обратной связи, многократная краниосакральная магнитная стимуляция, вибрационные раздражители, акупунктура.
Наиболее часто для достижения эффекта приходится использовать несколько из вышеперечисленных процедур [16].
Последние исследования указывают на необходимость мультидисциплинарного подхода к ведению пациентов со спастичностью [17].
Таким образом, основой лечения спастичности являются лечебная гимнастика и физиотерапия, которые воздействуют на естественные процессы восстановления и наиболее эффективны, если их применение начато в раннюю фазу развития спастичности. Достижению благоприятного исхода в значительной мере способствует прием центральных миорелаксантов, инъекции препаратов ботулинического токсина; иногда применяются также хирургические вмешательства и химическая денервация [17].
Использование препаратов ботулинического токсина более оправданно в ситуациях, когда мышечный спазм носит преимущественно локальный характер. Длительность эффекта определяется дозой введенного препарата, размером мышцы, активностью мышцы и рядом факторов, в том числе одновременным проведением физиотерапевтических процедур. Эффект от введения препарата сохраняется в течение нескольких месяцев, после чего обычно необходимы повторные инъекции, которые, однако, у части больных оказываются менее эффективными вследствие образования антител к ботулотоксину и блокирования его действия. Следует отметить, что использование препаратов ботулинического токсина в значительной мере ограничено из-за их высокой стоимости.
Фармакотерапия постинсультной спастичности включает назначение миорелаксантов [18]. По механизму действия различают миорелаксанты центрального действия (влияют на синаптическую передачу возбуждения в центральной нервной системе) и периферического действия (угнетают прямую возбудимость поперечнополосатых мышц).
Недавно на фармакологическом рынке Украины появился препарат для блокирования мышечного спазма Мускомед (производства компании World Medicine). В составе этого лекарства имеется полусинтетический миорелаксант — тиоколхикозид. Его получают из колхизида. Мускомед действует при разных спазмах — как центрального происхождения, так и местного, поскольку обладает селективными свойствами к ГАМК и глициновым рецепторам. Прием Мускомеда не оказывает парализующего действия и не влияет на функции дыхания и работу кардиоваскулярной системы.
При поступлении Мускомеда в организм с помощью в/м введения в течение 15–45 минут в плазме достигается пик концентрации и при введении 1 ампулы составляет 61 нг/мл. Спустя 2–2,5 часа наступает период полувыведения — 4/5 выводится через кишечник и 1/5 — через почки. В инструкции по применению указано, что Мускомед показан больным с болезненными мышечными спазмами, дорсалгиями и люмбалгиями, вертеброгенными спазмами шейных мышц (преходящая кривошея), другими неврологическими нарушениями, сопровождающимися спастичностью (цервикобрахиальная невралгия, ишиалгия или седалищная боль (седалищная невралгия)), спортивными травмами, послеоперационными болевыми синдромами, в период физической реабилитации для устранения мышечной контрактуры.
Однако мало известно о клинической эффективности данного препарата у пациентов с постинсультной спастичностью.
В связи с этим представляло интерес изучить влияние препарата Мускомед на постинсультную спастичность у пациентов, перенесших мозговой инсульт.
Целью нашего исследования была оценка клинической эффективности и безопасности препарата Мускомед в лечении спастичности у пациентов в восстановительном периоде ишемического мозгового инсульта.
Задачи исследования:
1. Изучить клиническую эффективность препарата Мускомед у пациентов с постинсультной спастичностью.
2. Оценить переносимость и безопасность препарата Мускомед у пациентов с постинсультной спастичностью.
Материалы и методы
Для осуществления поставленной цели и задач исследования были применены следующие методы обследования: оценка неврологического статуса, оценка спастичности по шкале Эшворта, оценка интенсивности болевого синдрома по визульно-аналоговой шкале боли (ВАШ), оценка степени нарушения двигательных функций по индексу мобильности Ривермида, а также лабораторные обследования.
Оценка эффективности препарата Мускомед проводилась на основании клинико-неврологического обследования, степень выраженности спастичности определялась по шкале Эшворта (Modified Ashworth Scale for Grading Spasticity). Оценка интенсивности болевого синдрома проводилась по визуальным и вербальным критериям в баллах от 0 до 10 (визуально-аналоговая шкала боли (ВАШ)). Степень нарушения двигательных функций определялась по индексу мобильности Ривермида. Также проводились: общий анализ крови — эритроциты, гемоглобин, лейкоциты, тромбоциты, СОЭ, сахар крови; общий анализ мочи — удельная плотность, лейкоциты, эритроциты, белок, сахар; биохимический анализ крови — АЛТ, АСТ.
Оценка переносимости. Переносимость препарата Мускомед оценивали на основании субъективных ощущений пациентов и результатов объективных клинических данных.
Статистическая обработка проводилась с использованием методов вариационной статистики. Достоверность различий между средними значениями исследуемых показателей определяли по критерию Стьюдента, оценивая вероятность на уровне значимости не менее 95 % (р ≤ 0,05).
Критерии включения и исключения. Критерии включения: пациенты обоих полов в возрасте старше 40 лет; пациенты в восстановительном периоде ишемического мозгового инсульта с болезненной мышечной спастичностью в паретичных конечностях; получение информированного письменного согласия пациента на участие в исследовании и выполнение его требований. Критерии исключения: здоровые пациенты без вышеперечисленной симптоматики; лица, имеющие повышенную чувствительность к компонентам препарата, с тяжелой миастенией, беременные, больные с выраженной деменцией, болезнью Альцгеймера, болезнью Паркинсона, эпилепсией; больные, принимающие другие миорелаксанты.
Преждевременное выбывание из исследования. Лечение исследуемым препаратом должно быть прекращено в случае, если наблюдались выраженные или серьезные побочные эффекты, а также при отказе больного от дальнейшего приема препарата. Исключение из исследования и удаление регистрационной формы пациента из процесса обработки данных происходило в случае несоблюдения больным инструкций исследования или нарушения им протокола исследования. Причины исключения пациента из исследования указывались в индивидуальной регистрационной карте.
Дизайн исследования. В исследование было включено 30 больных с постинсультной болевой спастичностью в восстановительном периоде ишемического мозгового инсульта. Пациенты получали препарат Мускомед в дозировке 2,0 мл в/м 2 раза в сутки в течение 5 дней. Средний возраст больных составлял 61,5 ± 3,8 года (от 48 до 69 лет), из них мужчин было 18 (60,0 %), женщин — 12 (40,0 %).
Для оценки эффективности препарата Мускомед в качестве группы сравнения было включено в исследование 28 больных после перенесенного инсульта, которым препарат не назначался, однако они получали лечение, направленное на предотвращение повторного инсульта или других сердечно-сосудистых заболеваний. Средний возраст этих больных составил 60,3 ± 2,1 года.
Результаты
Основным сосудистым заболеванием у больных, участвующих в исследовании, было сочетание атеросклероза с артериальной гипертензией. При анализе нейровизуализационных данных у 40 % больных инфаркт локализовался в правом, у 60 % — в левом полушарии мозга. В зависимости от локализации инфаркта больные были разделены на 3 подгруппы: с корково-подкорковой — 11 больных (36,6 %), подкорковой — 13 (43,3 %) и корковой — 6 больных (20,1 %). Патогенетический подтип ишемического инсульта определялся в соответствии с классификацией TOAST. Атеротромботический подтип имел место у 18 пациентов (60,0 %), кардиоэмболический — у 10 (33,3 %), криптогенный — у 2 пациентов (6,7 %).
У всех обследованных пациентов были обнаружены двигательные нарушения. У 12 больных (40,0 %) был выраженный спастический парез, у 14 (46,7 %) — умеренно выраженный и у 4 больных (13,3 %) — легкий.
Для оценки спастичности, как было указано выше, мы использовали шкалу Эшворта, которая является признанным инструментом для регистрации и контроля клинической динамики спастичности во время лечения. В табл. 1 представлена динамика результатов тестирования больных по шкале Эшворта до и после лечения (табл. 1).
После завершения курса лечения состояние двигательной системы существенно улучшилось у всех исследуемых больных. Средний балл спастичности по шкале Эшворта до лечения составлял 3,1 ± 0,7 балла. По завершении исследования показатель по шкале Эшворта снизился на 0,6 балла и составил 2,6 ± 0,6 балла. Динамика показателей по шкале Эшворта у больных, которые не получали препарат Мускомед, представлена в табл. 2.
Таким образом, существенной динамики у этих пациентов не было выявлено. Как показали результаты исследования, включение Мускомеда в комплекс реабилитационных мероприятий у больных со спастическим гемипарезом вследствие ишемического мозгового инсульта способствовало и улучшению двигательных функций (индекс мобильности Ривермида составил 12,1 ± 0,3 балла, p < 0,01). В группе сравнения индекс мобильности Ривермида не применялся и составил 11,2 ± 0,7 и 11,7 ± 0,3 балла).
Интенсивность болевого синдрома, обусловленного спастическим гемипарезом, оценивалась по 10-балльной ВАШ (табл. 3) до и после лечения препаратом Мускомед.
По ВАШ исходная субъективная оценка боли у всех пациентов составила в среднем 4,2 ± 0,5 балла. После лечения этот показатель составил 3,3 ± 0,4 балла. В группе сравнения этот показатель был на I визите 4,1 ± 0,4 балла, на II визите — 4,1 ± 0,2 балла.
По результатам анализа показателей неврологического статуса было выявлено, что препарат Мускомед оказывал положительное влияние на двигательную активность. Можно отметить и уменьшение болевого синдрома при терапии препаратом Мускомед у постинсультных больных со спастическим гемипарезом. Это способствовало повышению эффективности реабилитационных мероприятий.
Таким образом, после лечения отмечалась положительная динамика по показателям ВАШ, шкалы Эшворта и индекса мобильности Ривермида у больных с постинсультной спастичностью. Таких результатов не было у пациентов из группы сравнения, которые не получали препарат Мускомед.
Осмотр и опрос пациентов в ходе проведенного клинического исследования не обнаружили каких-либо жалоб, неожиданных побочных реакций, осложнений или явлений непереносимости препарата Мускомед. Ни один из пациентов не предъявлял жалоб и не испытывал каких-либо неприятных ощущений, которые можно было бы связать с действием исследуемого препарата. Ни один из больных, получавших Мускомед, не прекратил лечение вследствие побочных эффектов. В результате проведенного лечения было установлено, что переносимость препарата Мускомед была хорошей или удовлетворительной (табл. 4).
Как видно из табл. 4, переносимость препарата была хорошей у 28 (93,3 %) больных, удовлетворительной — у 2 (6,7 %) больных.
Препарат продемонстрировал безопасность у больных с последствиями ишемического мозгового инсульта и спастичностью (табл. 4).
По нашим данным, применение препарата Мускомед снижает не только степень спастичности, но и уровень болевого синдрома, а также улучшает повседневную активность больных, облегчает их уход за собой при отсутствии нежелательных явлений в ходе терапии.
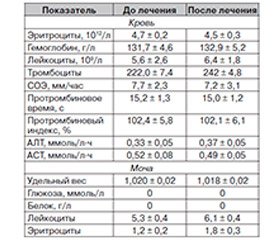
Изменения морфологических и биохимических показателей крови и мочи у обследованных больных в ходе применения препарата Мускомед представлены в табл. 5.
Назначение препарата Мускомед не оказывало негативного влияния на показатели морфологического состава периферической крови, на уровень ее основных биохимических констант и не отразилось на показателях клинического анализа мочи (табл. 5). В целом на основании результатов объективных клинических и лабораторных исследований переносимость препарата Мускомед характеризовалась как хорошая у всех пациентов.
Выводы
1. Спастичность и связанный с ней болевой синдром оказывают негативное воздействие на эффективность реабилитации у больных в восстановительном периоде ишемического мозгового инсульта.
2. Включение препарата Мускомед в комплексную реабилитацию постинсультных больных с целью устранения спастичности и связанного с ней болевого синдрома приводит к увеличению мышечной силы и объема движений в паретичных конечностях. Это повышает эффективность реабилитации, улучшает адаптацию больных с двигательными нарушениями после перенесенного ишемического инсульта.
Конфликт интересов. Не заявлен.
Список литературы
1. Claiborne J.S., Mendis S., Mathers C.D. Global variation in stroke burden 9 and mortality: estimates from monitoring, surveillance, and modelling // Lancet Neuml. — 2009. — 8, 4. — 345-354.
2. Feigin V.L., Carlene M., Derrick A., Barker-Collo S.L., Pa–rag P. Worldwide stroke incidence and early case fatality reported in 56 population-based studies: a systematic review // Lancet Neurol. — 2009. — 8, 4. — 355-369.
3. Міщенко Т.С. Стан неврологічної служби України в 2015 році. — Харків, 2016. — 23 с.
4. Sanossian N., Ovbiagele B. Prevention and management of stroke in very elderly patients // The Lancet Neurology. — 2009. — 8, 11. — 1031-1041.
5. Timsit S., Goas P., Rouhart F., Nowak E. High incidence disparities between three French population-based registry: Dijon, Brest, Lille. 22th European 13. Stroke Conference. Abstracts. — London. — 559.
6. Суслина З.А., Гулевская Т.С., Максимова М.Ю., Моргунов В.А. Нарушения мозгового кровообращения: диагностика, лечение, профилактика. — М.: МЕДпресс-информ, 2016.
7. Гусев Е.И., Коновалов А.Н., Гехт А.Б. Реабилитация в неврологии // Кремлевская медицина. — 2001. — 5. — 29-32.
8. Суслина З.А., Варакин Ю.Я. Клиническое руководство по ранней диагностике, лечению и профилактике сосудистых заболеваний головного мозга. — М.: МЕДпресс-информ, 2015.
9. Кадыков А.С., Черникова Л.А., Шахпаронова Н.В. Реабилитация неврологических больных. — М.: МЕДпресс-информ, 2008.
10. Дамулин И.В., Кононенко E.B. Двигательные нарушения после инсульта: патогенетические и терапевтические аспекты // Consilium Medicum. — 2007. — 9 (2).
11. Urban P.P., Wolf T., Vebele M. et al. Occurrence and clinical predictors of spasticity after ischemic stroke // Stroke. — 2010. — № 41. — Р. 2016-20.
12. Wissel J., Manack A., Brainin M. Toward an epidemiology of poststroke spasticity // Neurology. — 2013. — № 80. — S13.
13. Boyd R. Physiotherapy management of spasticity / Boyd R. // Upper motor neuron syndrome and spasticity. — Cambridge University Press, 2001. — P. 96-121.
14. Марутенков Г.Л. Снижение риска падений и повышение уровня повседневной жизненной активности пациентов после инсульта с помощью занятий на тренажере «Баланс-система SD» / Г.Л. Марутенков, В.В. Ковальчук // Медико-социальная экспертиза и реабилитация. — 2010. — № 1. — С. 16-19.
15. Козелкин А.А. Современные аспекты нейрореабилитации постинсультных больных / А.А. Козелкин [и др.] // Міжнародний неврологічний журнал. — 2010. — № 8. — С. 20-24.
16. Стаднік С.М. Мультидисциплінарний підхід при реабілітації пацієнтів із мозковим інсультом / С.М. Стаднік, Р.І. Данилков // Міжнародний неврологічний журнал. — 2010. — № 8. — С. 28-32.
17. Demetrios М., Khan F., Turner-Stokes L., Brand C., McSweeney S. Multidisciplinaiy rehabilitation following botulinum toxin and other focal intramuscular treatment for post-stroke spasticity // Cochrane Database Syst. Rev. — 2013 Jun.
18. Carolee J. Winstein et al. Guidelines for Adult Stroke Rehab–ilitation and Recovery / Carolee J. Winstein, PhD, PT, Chair et al. // Stroke. — 2016.

/98-1.jpg)
/98-2.jpg)
/98-3.jpg)
/98-4.jpg)
/99-1.jpg)