Резюме
Стаття присвячена питанням покращання діагностики, застосування методик оцінки тяжкості стану хворих при надходженні у відділення інтенсивної терапії, у динаміці спостереження за ними, оптимізації інтенсивної терапії (ІТ) вторинного гнійного менінгоенцефаліту (ВГМЕ). Загальна схема відбору пацієнтів, їх рандомізації, включення в дослідження й аналіз можуть бути подані в такий спосіб. Пацієнти з підтвердженим ВГМЕ методом рандомізації з урахуванням тяжкості стану та варіанту ІТ були розподілені на 2 групи. У I групу увійшли 22 пацієнти, котрим проводилася базисна ІТ із позицій доказової медицини відповідно до міжнародних рекомендацій Surviving Sepsis Campaign: International guidelines for management of severe sepsis and septiс shock 2012, що доповнювалася включенням дексаметазону. У II групу увійшов 21 пацієнт, у яких ІТ, що проводилась у I групі, доповнювалась в/в введенням розчину реамберин. На початку дослідження не виявлено вірогідних відмінностей між групами за статтю, віком, локалізацією септичного вогнища, частотою реєстрації 4 ознак синдрому системної запальної відповіді, позитивних результатів бактеріологічних посівів ліквору та матеріалів із первинного вогнища, тобто вибірки були порівняними за цими ознаками. У цей же час серед пацієнтів II групи було в 2,8 раза більше хворих із рівнем свідомості «сопор» або «кома I ступеня» (76,2 % проти 27,2 %; р < 0,001). Несприятливий прогноз (центральний перфузійний тиск < 50 мм рт.ст.) при надходженні до стаціонару мали 22,7 % хворих із I групи і 28,6 % — із II (р > 0,60). Незважаючи на початково більш тяжкий стан хворих із ВГМЕ в II групі, додавання до базисної терапії в/в введення розчину реамберин сприяло тому, що санація ліквору в II групі проходила більш плавно, без вторинного сплеску цитозу, характерного для I групи на 5-ту добу дослідження. Установлено, що в I групі С-реактивний білок у лікворі зникав до 3-ї доби дослідження, з’являвся на 5-ту добу і був відсутнім до 7-ї доби дослідження. У II групі наявність С-реактивного білка було зафіксовано лише на початку і 1-шу добу дослідження, що свідчить про більш стійкий характер відновлення функціонального стану гематоенцефалічного бар’єра в II групі, без вторинного (повторного) його прориву. Оцінка ефективності ІТ на 28-му добу дослідження показала, що відмічалось зменшення когнітивних дисфункцій у I групі на 28,4 %, у II — на 37,7 %; органних дисфункцій у I групі — з 76,3 до 43,8 %; у II — з 88,7 до 36,9 %. Показники істинної летальності становили 27,27 і 23,81 % (р > 0,90) відповідно. Зниження прогнозованої летальності в I групі становило 4,73 %, у II — 16,19 %.
Статья посвящена вопросам улучшения диагностики, применения методик оценки тяжести состояния больных при поступлении в отделение интенсивной терапии, в динамике наблюдения за ними, оптимизации интенсивной терапии (ИТ) вторичного гнойного менингоэнцефалита (ВГМЭ). Общая схема отбора пациентов, их рандомизации, включения в исследование и анализ могут быть представлены следующим образом. Пациенты с подтвержденным ВГМЭ методом рандомизации с учетом тяжести состояния и варианта ИТ были распределены на 2 группы. В I группу вошли 22 пациента, которым проводилась базисная ИТ с позиций доказательной медицины в соответствии с международными рекомендациями Surviving Sepsis Campaign: International guidelines for management of severe sepsis and septic shock 2012, которая дополнялась включением дексаметазона. Во II группу вошел 21 пациент, у которых ИТ, проводимая в I группе, дополнялась в/в введением раствора реамберин. При исследовании исходно не выявлено достоверных различий между группами по полу, возрасту, локализации септического очага, частоте регистрации 4 признаков синдрома системного воспалительного ответа, положительных результатов бактериологических посевов ликвора и материалов из первичного очага, то есть выборки были сравнимы по этим признакам. В то же время среди пациентов II группы было в 2,8 раза больше больных с уровнем сознания «сопор» или «кома I степени» (76,2 % против 27,2 %; р < 0,001). Неблагоприятный прогноз (центральное перфузионное давление < 50 мм рт.ст.) при поступлении в стационар был у 22,7 % больных из I группы и у 28,6 % — из II (р > 0,60). Несмотря на исходно более тяжелое состояние больных с ВГМЭ во II группе, добавление к базисной терапии в/в введения раствора реамберин способствовало тому, что санация ликвора во II группе происходила плавно, без вторичного всплеска цитоза, характерного для I группы на 5-е сутки исследования. Установлено, что в I группе С-реактивный белок в ликворе исчезал к 3-м суткам исследования, появлялся на 5-е сутки и отсутствовал до 7-х суток исследования. Во II группе наличие С-реактивного белка фиксировалось только исходно и на 1-е сутки исследования, что свидетельствует о более устойчивом характере восстановления функционального состояния гематоэнцефалического барьера во II группе, без вторичного (повторного) его прорыва. Оценка эффективности ИТ на 28-е сутки исследования показала, что отмечалось уменьшение когнитивных дисфункций в I группе на 28,4 %, во II — на 37,7 %; органных дисфункций в I группе — с 76,3 до 43,8 %; во II — с 88,7 до 36,9 %. Показатели истинной летальности составляли 27,27 и 23,81 % (р > 0,90) соответственно. Снижение предполагаемой летальности в I группе составило 4,73 %, во II — 16,19 %.
A range of algorithms of the intensive therapy of secondary meningoencephalitis are applied in the clinical practice. However, they do not provide such treatment strategies as prophylaxis and treatment of secondary brain injuries by providing the well-ordered process of mitochondrial function that is the key factor for life-support systems disfunction/insufficiency correction. In this respect, reamberin attracts our attention. Research objective: to study the indicators dynamics in systemic inflammatory response syndrome, APACHE ІІ and SOFA scores, cerebral perfusions, metabolism and functional status of blood-brain barrier in patients with secondary purulent meningoencephalitis at the research stage using the protocol that adheres Surviving Sepsis Campaign International Guidelines: International guidelines for management of severe sepsis and septic shock: 2008, supplemented with dexamethasone inclusion basing on Management of bacterial meningitis and meningococcal septicemia in children and young people younger than 16 years in primary and secondary care. Full guideline: to include 2010 (I group) to the basic reamberin protocol (II group). General scheme of selection of patients and their randomization, included in the research and analysis, may be represented as follows. Patients with secondary purulent meningoencephalitis approved by randomization method were classified into 2 groups on the basis of their emergency state and intensive therapy (IT) option. Group I included 22 patients treated with basis IT from the position of evidence-based medicine meeting Surviving Sepsis Campaign International Guidelines: International guidelines for management of severe sepsis and septic shock: 2012, supplemented with dexamethasone inclusion. Group II included 21 patients treated with IT equal to group I and supplemented with intravenous injection of reamberin solution. Patients were examined according to 2001 SCCM/ESISM/ACCP/ATS/SIS International Sepsis Definition Conference guidelines, being primary steps or points for efficiency assessment, while mortality/recovery within 28 days of disease was considered as endpoints. The following diagnostic algorithm of secondary purulent meningoencephalitis included: medical history; related professionals’ consultations; chest and paranasal sinuses roentgenograms; CT scan, MRI, and brain spiral computed tomography; cerebral vessels Doppler sonography; clinical picture; lumbar puncture; initial cerebrospinal fluid pressure; clinical and bacteriological cerebrospinal fluid testing. The following criteria were applied for bacterial and viral meningoencephalitis differential diagnostics: septic focus; previous viral infections; immunodeficiency; the number of cells > 1000 × 106/liter during CSF examination; prevalence of granulocytes; obtaining bacteriological confirmation; PCR in cerebrospinal fluid: DNA of herpes types I and II viruses, Epstein — Barr virus, cytomegalovirus, etc.; procalcitonin (PCT) in blood plasma. Criteria for hospitalization of patients with secondary purulent meningoencephalitis sepsis to ICU were the following: two or more SIRS clinical signs; infection, contemplated or documented according to SCCM/ESISM/ACCP/ATS/SIS International Sepsis Definition Conference; patient’s emergency state assessment and prediction of mortality probability at sepsis (Mortality in Emergency Department Sepsis Score — MEDS, 1998). The descriptive statistics results were used to describe primary dataset. During the research no significant differences between groups in terms of gender, age, septic focus localization, registration frequency of four SIRS signs, positive results of the cerebrospinal fluid and primary focus materials bacteriological tests were determined initially, i.e. samples were compared according to these features. Meanwhile, there were 2.8 times more patients with the sopor or coma I level in group II (76.2 % vs. 27.2 %; p < 0.001). 22.7 % of patients from group I and 28.6 % of patients from group II (p > 0.60) had a poor prognosis (CPP < 50 mm Hg) at hospitalization. Despite the initially more emergent state of patients with secondary purulent meningoencephalitis in group II, implementation of intravenous injection of reamberin solution to the basic therapy helped smooth sanitation of cerebrospinal fluid in group II without secondary splash of cytosis, specific for group I on the 5th day of research. It was determined that CRP in cerebrospinal fluid in group I disappeared to the 3rd day of research, occurred on the 5th day and was absent to the 7th day of the research. In group II, CRP was found only initially on the 1st day of the research that proves more stable character of the restoration of BBB functional state in group II, without its secondary duplicative breakthrough. IT efficiency assessment on the 28th day of the research showed the decrease of cognitive dysfunctions by 28.4 % in group I, and by 37.7 % in group II; organ dysfunctions — from 76.3 % to 43.8 % in group I, and from 88.7 % to 36.9 % in group II. Genuine lethality indicators constituted 27.27 and 23.81 % (р > 0.90) in groups, respectively. Decrease of the estimated lethality in group I was 4.73 %, while in group II 16.19 %.
Введение
В клинической практике используется ряд алгоритмов интенсивной терапии вторичных гнойных менингоэнцефалитов (ВГМЭ) [3, 5]. Однако в них не предусмотрены такие лечебные стратегии, как предупреждение и лечение вторичных повреждений головного мозга путем обеспечения упорядоченными процессами митохондриальной функции, что является ключевым фактором для коррекции дисфункции недостаточности систем жизнеобес–печения, тогда как главным действующим веществом реамберина является янтарная кислота (сукцинат) — промежуточный метаболит цикла Кребса. Сукцинат служит субстратом анаплеротических реакций цикла трикарбоновых кислот, имеет каталитический механизм действия на продуктивность всего цикла Кребса с восстановлением деятельности митохондриальных ферментов [4, 6].
Цель исследования: изучить динамику показателей синдрома системного воспалительного ответа (ССВО), систем Acute physiology age chronic health evaluation, 1981 (АРАСНЕ II), SOFA (Sequential (Sepsis — related) Organ Failure Assessment), церебральной перфузии, метаболизма и функционального состояния гематоэнцефалического барьера у пациентов с ВГМЭ на этапах исследования при использовании протокола, отвечающего международным рекомендациям Surviving Sepsis Campaign: International guidelines for management of severe sepsis and septic shock 2012, согласно которым базисная интенсивная терапия (ИТ) дополнялась включением дексаметазона (группа I), исходя из позиций Management of bacterial meningitis and meningococcal septicaemia in children and young people younger than 16 years in primary and secondary care. Full guideline 2010, и реамберина (группа II) [1, 2].
Материал и методы
Всего включено в исследование 109 пациентов:
— 40 чел. для выбора и обоснования способа оценки интракраниального давления неинвазивным методом;
— 69 чел. с целью исключения/подтверждения диагноза «вторичный гнойный менингоэнцефалит» и последующей дифференцированной ИТ.
Критерии включения в исследование: мужчины и женщины в возрасте от 18 до 70 лет с подтвержденным диагнозом ВГМЭ; наличие проявлений ССВО с источником инфекции; проведение до рандомизации пациентов забора биологических материалов для бактериологического исследования; получение информированного согласия пациента или его законного представителя на исследование.
Критерии исключения из исследования: изменение диагноза после поступления в отделение интенсивной терапии (ОИТ); нерадикальная хирургическая санация септических очагов; неадекватная стартовая эмпирическая антибактериальная химиотерапия; наличие сопутствующих хронических заболеваний в стадии декомпенсации; более чем 40 баллов по системе APACHE II; предварительное использование иммунодепрессантов, преднизолона или других гормональных препаратов; декомпенсация сахарного диабета; заранее известная чувствительность к препаратам или их ингредиентам, которые могут быть использованы; нейтропения; беременные женщины; нарушение протокола исследования.
Пациенты с подтвержденным ВГМЭ методом рандомизации с учетом тяжести состояния и варианта ИТ были распределены на 2 группы. Предварительно из исследования были исключены пациенты, которые не соответствуют критериям включения в исследование (n = 26). В итоге группу исследования составили 43 пациента. В I группу вошли 22 пациента, которым проводилась базисная ИТ с позиций доказательной медицины в соответствии с международными рекомендациями Surviving Sepsis Campaign: International guidelines for management of severe sepsis and septic shock 2012, которая дополнялась включением дексаметазона в дозе 0,15 мг/кг каждые 6 ч до введения антибактериальных препаратов в течение 3–4 дней, исходя из позиций Management of bacterial meningitis and meningococcal septicaemia in children and young people younger than 16 years in primary and secondary care. Full guideline 2010. Во II группу вошел 21 пациент, у которых ИТ, проведенная в I группе, дополнялась раствором реамберина с использованием методики, разработанной Н.Н. Мосенцевым (2008) на основе фармакокинетической характеристики препарата.
Пациенты были обследованы согласно рекомендациям 2001 SCCM/ESISM/ACCP/ATS/SIS. International Sepsis Definition Conference, которые являются первичными пунктами или точками для оценки эффективности; конечными точками были летальность/выздоровление до 28-х суток заболевания. Клинические признаки и симптомы оценивались ежедневно, лабораторные анализы — соответственно графику исследований.
Регистрация побочных реакций осуществлялась в соответствии с приказом МЗ Украины от 27.12.2006 г. № 898 «Про затвердження порядку здійснення нагляду за побічними реакціями лікарських засобів, дозволених для медичного використання».
У всех больных были использованы рутинные лабораторные исследования: определение уровня биохимических маркеров системного воспаления и органных дисфункций для оценки по шкалам APACHE II и SOFА, которые применялись в сертифицированной клинико-диагностической лаборатории КУ «Днепропетровская областная клиническая больница им. И.И. Мечникова». Концентрации мочевины, креатинина, альбумина, билирубина, С-реактивного белка (СРБ) в сыворотке крови определяли с помощью полуавтоматического биохимического анализатора РА-50 Bayer Diagnostics (США), глюкозы крови — глюкозно-оксидазным методом на анализаторе глюкозы Beckman-Coulter, Fulletron, CA (США), электролиты (К+, Na+, Сl–) — на анализаторе электролитов Bayer М-644 (Англия); кислотно-основное состояние, газы крови — с помощью автоматического анализатора рН и газов крови EasyBloodGas фирмы Medica (США), показатели коагулограммы — коагулометром Amelung KC-4A (Германия); активность ферментов (аланинаминотрансфераза, аспартат–аминотрансфераза) — кинетическим методом с наборами реактивов для колометрического измерения HumanCarb H (Германия) с использованием полуавтоматического биохимического анализатора ВА-88 фирмы Mindray (Китай). Для исследования функционального состояния гематоэнцефалического барьера проводилось определение в ликворе СРБ и соотношение СРБ крови и ликвора.
Использовался алгоритм диагностики ВГМЭ: история заболевания; консультации смежных специалистов; Rg-граммы органов грудной клетки и придаточных пазух носа; компьютерная, спиральная компьютерная, магнитно-резонансная томография головного мозга; допплерографическое исследование сосудов головного мозга; клиническая картина; люмбальная пункция; исходное ликворное давление; клиническое и бактериологическое исследование ликвора.
С целью дифференциальной диагностики менингоэнцефалитов бактериальной и вирусной этиологии использовались такие критерии: наличие септического очага; перенесенные вирусные инфекции; иммунодефициты; при исследовании цереброспинальной жидкости (ЦСЖ) количество клеток > 1000 • 106/л; преобладание гранулоцитов; получение бактериологического подтверждения; исследование методом полимеразной цепной реакции в ЦСЖ ДНК вирусов герпеса 1-го и 2-го типов, Эпштейна — Барр, цитомегаловируса и др.; уровень прокальцитонина в плазме крови.
Критериями для госпитализации пациентов с ВГМЭ в ОИТ сепсиса были: наличие 2 или более клинических признаков ССВО; инфекция, подозреваемая или документированная по 2001 SCCM/ESISM/ACCP/ATS/SIS. International Sepsis Definition Conference; оценка тяжести пациента и прогнозирование вероятности летальности при сепсисе (Mortality in Emergency Department Sepsis Score, 1998).
В условиях специализированного ОИТ сепсиса исходные диагностические критерии расширялись за счет:
— оценки тяжести состояния пациентов с помощью шкалы APACHE II с дальнейшей интерпретацией результатов по W.A. Knaus et al., 1985; оценки органной недостаточности с помощью шкалы SOFA, принятой Европейским обществом интенсивной терапии (European Society of Intensive Care Medicine — ESICM) по согласованию с рабочей группой ESICM по проблемам сепсиса, с интерпретацией результатов по J.L. Vincent et al., 1998; дополнительно использовалась Лозаннская шкала гастроинтестинальной недостаточности (Lausanne Intestinal Failure Estimation, 2008), основанная на идеологии модели SOFA;
— оценки обратного развития коматозного состояния и восстановления когнитивных функций по модифицированной шкале RLAS (Modified Rancho Los Amigos Scale, 2007) с учетом пациентов, которые достигали VII уровня за отведенное время;
— оценки композитного времени до разрешения органных дисфункций (Composite Timeto Complete Organ Failure Resultion, 2003): при завершении синдрома полиорганной недостаточности на протяжении 1–14 суток — 1 балл, после 14 суток — 15 баллов, до 28 суток — 16 баллов.
Для описания первичного массивного объема данных использовались результаты дескриптивной (описательной) статистики. Количественные данные проверки гипотезы о законе нормального распределения случайной величины использовали в соответствии с критерием Колмогорова — Смирнова. В случаях действия закона нормального распределения данные статистической характеристики были представлены в виде: объема выборки (n — количество наблюдений), средней арифметической, стандартной ошибки среднего, стандартного отклонения, 95% доверительного интервала. В случаях отклонения гипотезы о законе нормального распределения данных определяли значение медианы, нижний квартиль — 25 %, верхний квартиль — 75 %.
Результаты
Исследуя пациентов с подтвержденным ВГМЭ, выяснили, что при поступлении больных в ОИТ не было выявлено достоверных различий между группами по полу (мужчин — 63,6 и 71,4 %; p > 0,20), возрасту (44,2 ± 11,4 и 43,6 ± 11,9 года; p > 0,80), локализации септического очага (p > 0,90), частоте регистрации 4 признаков ССВО (90,9 и 90,5 %; p > 0,90), позитивных результатов бактериологических посевов ликвора и материалов из первичного очага (40,9 и 33,3 %; p > 0,60), то есть выборки были сопоставимы по этим признакам. В то же время среди пациентов II группы было в 2,8 раза больше больных с уровнем сознания «сопор» или «кома I степени» (76,2 % против 27,2 %; p < 0,001). Неблагоприятный прогноз «церебральное перфузионное давление» (< 50 мм рт.ст.) при поступлении в стационар был у 22,7 % больных из І группы и 28,6 % — из ІІ (p > 0,60).
Оценка глубины нарушения сознания показала, что при поступлении в стационар пациенты ІI группы имели по шкале комы Глазго (GSC) 10,68 ± 0,46 балла против 12,16 ± 0,59 балла в I группе (р < 0,05). Однако благодаря более высоким темпам улучшения сознания у больных во ІI группе под влиянием терапии групповые показатели достоверно не отличались уже начиная с 1-х суток (р > 0,20 при всех сравнениях) (рис. 1).
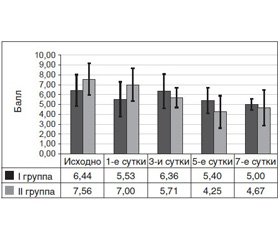
Похожие закономерности выявлялись при сравнении динамики по шкалам APACHE II и SOFA в обеих группах (рис. 2, 3).
Так, при поступлении в стационар пациенты II группы имели по шкале APACHE II 7,56 ± 0,76 балла против 6,44 ± 0,75 балла в I группе, то есть выше на 17,39 %, в 1-е сутки количество баллов во II группе было выше на 26,58 %. Начиная с 3-х суток количество баллов во II группе снижалось быстрее и составляло, соответственно этапам исследования, 89,78; 78,70 и 93,4 % относительно I группы. Причем на 7-е сутки групповые показатели достоверно не отличались (р > 0,10).
Показатели шкалы SOFA во II группе исходно составляли 3,06 ± 0,30 балла, в 1-е сутки — 3,00 ± 0,31 и 2,1 ± 0,2 — к 7-м суткам, которые превышали таковые в I группе на 31,33 (р < 0,10), 27,12 и 25,75 % –соответственно; на 3-и сутки они составляли 60,25 % (р < 0,05) и практически соответствовали данным I группы на 5-е сутки.
Сравнение динамики показателей цитоза у пациентов I и II групп на этапах исследования представлено на рис. 4. Динамика показателей плеоцитоза свидетельствовала, что в I группе исходно он был выше на 91,7 % (р< 0,01), в 1-е сутки — на 48,6 % (р < 0,05). Для 3-х суток исследования характерна быстрая санация ликвора в I группе, проявление цитоза во II группе было больше на 105,9 % (р < 0,001). На 5-е сутки отмечалось возрастание показателей цитоза в I группе на 115,1 % по отношению к 3-м суткам, в результате его уровень превышает данные II группы на 95,5 % (р < 0,001). На 7-е сутки показатели цитоза во II группе превышали аналогичные данные I группы на 46,7 % (р < 0,05). Следует отметить, что санация ликвора во II группе проходила плавно, без вторичного всплеска, характерного для I группы на 5-е сутки исследования.
/63-1.jpg)
При сравнении содержания агранулоцитов в ликворе у пациентов I и II групп на этапах исследования отмечено достоверное их преобладание в I группе исходно (на 114,3 %, р < 0,001), на 3-и сутки (на 30,4 %, р < 0,05) и на 7-е сутки (на 22,6 %, р < 0,05).
В 1-е сутки количество агранулоцитов в ликворе было одинаковым и составляло 10,0 ± 2,0 %, к 5-м суткам количество агранулоцитов в I группе составляло 76,1 % (р < 0,01) от количества агранулоцитов во II группе исследования. Сравнение содержания гранулоцитов в ликворе у пациентов I и II групп на этапах исследования указывало на их достоверное расхождение лишь исходно (количество гранулоцитов на 9,42 % больше во II группе, р < 0,001) и на 5-е сутки (количество гранулоцитов на 7,14 % выше в I группе, р < 0,05).
Динамика содержания белка в ликворе у пациентов I и II групп свидетельствовала о преобладании протеинархии во II группе исходно на 71,56 %, в 1-е сутки — на 47,41 %, на 3-и сутки — на 10,64 %, на 5-е сутки — на 32,95 % и на 7-е сутки — на 5,06 %. Причем достоверный характер отличия имели только при поступлении больных в ОИТ. На 7-е сутки исследования показатели протеинархии в группах практически не отличались. Концентрация глюкозы в ликворе при поступлении была выше в I группе на 182,09 % (р < 0,01); для дальнейшей динамики глюкозы в ЦСЖ характерно ее преобладание в I группе по отношению ко II группе на 1-е и 7-е сутки исследования, однако эти различия имели недостоверный характер.
Обсуждение
Несмотря на исходно более тяжелое состояние больных с ВГМЭ во ІІ группе, дополнение к стандартной терапии раствора реамберин способствовало ускорению восстановительных процессов, что проявлялось в нормализации клинических и биохимических показателей практически в то же время, что и у пациентов І группы. Одновременно установлено, что в I группе СРБ в ликворе исчезал до 3-х суток, появлялся на 5-е сутки и исчезал на 7-е сутки исследования. Во II группе наличие СРБ фиксировалось исходно и на 1-е сутки исследования, то есть восстановление функционального состояния гематоэнцефалического барьера во II группе имело более стойкий характер, без вторичного (повторного) его прорыва.
Оценка эффективности ИТ на 28-е сутки показала, что произошло уменьшение когнитивных дисфункций в I группе на 28,4 %, во II группе — на 37,7 %; органных дисфункций в I группе — с 76,3 до 43,8 %, во II группе — с 88,7 до 36,9 %. Показатели истинной летальности составляли 27,27 и 23,81 % (р > 0,90) соответственно группам. Снижение прогнозированной летальности в I группе составило 4,73 %; во II — 16,19 %.
Выводы
1. При оценке эффективности использования базисной интенсивной терапии, соответствующей международным рекомендациям Surviving Sepsis Campaign: Internationa l guidelines for management of severe sepsis and septic shock 2012, которая дополнялась включением дексаметазона в дозе 0,15 мг/кг каждые 6 часов в течение 3–4 дней до введения антибактериальных препаратов, исходя из позиций Management of bacterial meningitis and meningococcal septicaemia in children and young people younger than 16 years in primary and secondary care. Full guideline 2010, установлено, что по отношению к предполагаемой летальности, которая составляла исходно 32 %, истинная летальность составила 27,27 %, то есть снижение летальности составляло 4,73 % (р > 0,90).
2. Дополнительное введение реамберина в дозе 400 мл в/в капельно показало, что по отношению к предполагаемой летальности, которая составляла исходно 40 %, истинная летальность составляла 23,81 %, то есть во II группе снижение предполагаемой летальности по отношению к истинной летальности составило 16,19 % (р > 0,90).
3. Несмотря на исходно более тяжелое состояние больных с ВГМЭ во II группе, добавление к базисной терапии в/в введения реамберина способствовало ускорению восстановительных процессов, что привело на 28-е сутки исследования к уменьшению когнитивных дисфункций на 9,3 %, органных дисфункций — на 15,3 %, истинной летальности — на 11,46 % по отношению к I группе.
Конфликт интересов. Авторы заявляют об отсутствии какого-либо конфликта интересов при подготовке данной статьи.

/63-1.jpg)