Введение
Леветирацетам — это антиэпилептический препарат второго поколения, обладающий уникальным фармакологическим профилем по сравнению с традиционными противосудорожными препаратами. В последнее время появляются работы от исследователей из разных стран мира, раскрывающие дополнительные эффекты леветирацетама, позволяющие использовать его не только как противоэпилептический, но и как нейропротективный и антигипералгезивный препарат. Обзору таких данных посвящена данная публикация.
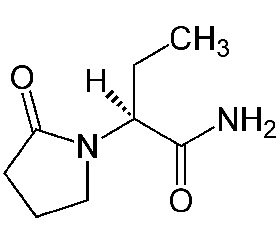
Леветирацетам был синтезирован в начале 1980-х годов. Молекула принадлежит к семейству пирролидонов, классу препаратов, обладающих широким спектром действия. Начальные фармакологические исследования леветирацетама показали его способность влиять на холинергическую нейротрансмиссию. Леветирацетам был одобрен в США в 1999 году Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов, а в 2000 году он был одобрен в Европе для использования у взрослых пациентов с миоклоническими судорогами, ювенильной миоклонической эпилепсией и при первичных генерализованных тонико-клонических судорогах [30]. В 2012 году FDA одобрило леветирацетам для использования в качестве вспомогательной терапии парциальных припадков у детей в возрасте 1 месяца и старше [8].
Леветирацетам обладает хорошим фармакокинетическим профилем и используется в разнообразных клинически сложных ситуациях. Леветирацетам доказал свою эффективность в профилактике различных форм эпилепсии, применялся в качестве монотерапии [2, 27] и дополнительного лечения для предотвращения ранних посттравматических припадков [1, 10, 13, 33]. В последнее время появились данные об эффективности и безопасности леветирацетама при лечении приступов эпилепсии у новорожденных [31]. Кроме того, исследования показали, что леветирацетам обладает значительными нейропротективными свойствами при купировании неэпилептических [30] и эпилептических приступов [18, 25]. Экспериментальные данные свидетельствуют о том, что леветирацетам оказывает антигипералгическое действие при ноцицептивной [20, 26] и нейропатической боли [9, 23].
Механизм действия леветирацетама
Несмотря на множество исследований, посвященных изучению эффективности леветирацетама в качестве нейропротектора, антиконвульсанта и анальгетика, фармакодинамика этого препарата до конца не выяснена. Данные литературы свидетельствуют о следующих трех основных молекулярных объектах: воздействие на белок SV2A; ингибирование Ca2+- и Nа+-каналов и нейромодуляторное действие на ГАМК-, 5HT-, α2-адренергические и μ-опиоидергические пути. Фармакокинетические свойства, эффективность, высокая переносимость, низкое взаимодействие с другими лекарственными средствами и различные механизмы действия, характеризующие леветирацетам, вызвали большой интерес и открыли новые пути для клинических исследований.
В головном мозге леветирацетам связывается с белком SV2A, который представляет собой интегральный мембранный белок, присутствующий в синаптических везикулах и некоторых нейроэндокринных клетках [12]. Экспрессия изоформ SV2 была отмечена в нескольких участках центральной нервной системы и особенно выражена в подкорковых областях, таких как таламус, базальные ганглии, кора и гиппокамп [19]. Точная роль SV2A в синаптической везикуле и высвобождении нейротрансмиттера остается неопределенной, однако предполагается, что белок SV2A может действовать как транспортер или может модулировать экзоцитоз синаптических везикул и модифицировать синаптическую функцию.
Механизм действия леветирацетама включает в себя каскад эффектов, который в первую очередь проявляется связыванием с белком SV2A путем модуляции возбудимости нейронов и генерации различных изменений в ЦНС. Существует необходимость в новых направлениях исследований, которые смогут прояснить фармакодинамику леветирацетама, что чрезвычайно важно для расширения знаний о возможности использования этого препарата в качестве альтернативного лечения повреждения нейронов и гипералгезии.
Леветирацетам в лечении эпилепсии
Эпилепсия включает в себя группу расстройств, характеризующихся двумя или более неспровоцированными судорогами. Леветирацетам удобен в применении (два раза в день), не взаимодействует с другими противосудорожными препаратами, имеет хороший профиль безопасности и не требует мониторинга сывороточной концентрации препарата. Такой благоприятный фармакологический профиль делает леветирацетам привлекательным препаратом, который можно использовать в качестве базисной или вспомогательной терапии при эпилептических припадках.
Christoph Helmstaedter с коллегами сравнивал противоэпилептические эффекты монотерапии леветирацетамом и карбамазепином, а также их влияние на когнитивные функции пациентов, которые оценивались до лечения и через 6 месяцев после его начала [7]. В исследовании участвовали 498 пациентов: 370 из них получали леветирацетам и 128 — карбамазепин. Авторы пришли к выводу, что леветирацетам и карбамазепин одинаково эффективны в качестве противосудорожной монотерапии, однако на фоне приема леветирацетама у пациентов отмечалось улучшение когнитивных показателей в отличие от пациентов, принимавших карбамазепин.
Согласно исследованию, проведенному Lambrechts с коллегами, леветирацетам был эффективен и безопасен в комплексной терапии при парциальной эпилепсии у взрослых [13]. Леветирацетам уменьшал частоту парциальных приступов (тип I) на 62,2 %, всех типов судорог (типы I + II + III) — на 61,7 %, а у 56,6 % пациентов уменьшал частоту приступов на ≥ 50 %.
Эффективность и переносимость леветирацетама в комплексной терапии у пациентов с неконтролируемыми генерализованными тонико-клоническими судорогами при идиопатической генерализованной эпилепсии была изучена Berkovic с коллегами [11]. У 56,5 % пациентов было отмечено снижение частоты генерализованных тонико-клонических припадков в неделю на фоне лечения по сравнению с плацебо-терапией, при которой среднее снижение частоты приступов составляло 28,2 %. В течение периода наблюдения доля пациентов без генерализованных тонико-клонических судорог составила 24,1 % для леветирацетама против 8,3 % для плацебо (р < 0,009).
Леветирацетам в лечении эпилепсии у детей
Эффективность леветирацетама у детей с эпилепсией, не поддающейся лечению с использованием существующих противоэпилептических препаратов (со средним периодом наблюдения 13 месяцев и максимальным периодом наблюдения 21 месяц), была изучена Lee с коллегами [14]. Они наблюдали у 48 % пациентов снижение частоты приступов на ≥ 50 %, а у 22 % пациентов — их отсутствие. По данным авторов, у 130 детей с труднокурабельной эпилепсией, получавших леветирацетам в качестве дополнительной терапии, наблюдалось сокращение приступов более чем на 50 %: у 52 % детей с парциальными приступами и у 44 % детей с генерализованными судорогами.
Данные об эффективности, безопасности и переносимости леветирацетама у детей в возрасте от 1 месяца с эпизодическими судорогами были рассмотрены Cormier с соавторами [8]. Они пришли к выводу, что леветирацетам может быть безопасным и эффективным вариантом лечения детей с парциальными приступами различной этиологии. Эффективность и переносимость леветирацетама в качестве дополнительной терапии у пациентов с первичной эпилепсией была изучена и Gurses с коллегами [10], который обнаружил, что 60 % пациентов ответили на лечение препаратом.
В открытом исследовании, проведенном Morrell с соавторами, приняли участие более 300 исследователей [21]. Авторы изучали безопасность и переносимость леветирацетама, а также эффективность препарата в качестве дополнительной терапии парциальных приступов. По их данным, 57,9 % пациентов, получавших леветирацетам, отмечали снижение частоты парциальных приступов на 50 % и более, 40,1 % пациентов отмечали сокращение частоты припадков по меньшей мере на 75 %, а 20 % пациентов продемонстрировали полную редукцию судорог.
Монотерапия леветирацетамом в лечении эпилепсии
Эффективность и переносимость леветирацетама в дозе 1500 мг два раза в день в качестве монотерапии оценивали в многоцентровом рандомизированном двойном слепом параллельном исследовании, проведенном Ben-Menachem с коллегами [2]. Авторы обнаружили, что в группе пациентов, получавших монотерапию леветирацетамом, средний процент снижения частоты парциальных приступов по сравнению с исходным уровнем составил 73,8 % при частоте ответа 59,2 %. Переход на назначение леветирацетама в качестве монотерапии (1500 мг два раза в день) является эффективным и хорошо переносимым у пациентов с рефрактерными парциальными приступами, которые ответили на 3000 мг/сут леветирацетама в качестве дополнительной терапии. Поэтому авторы рекомендуют леветирацетам в качестве эффективного и хорошо переносимого препарата для взрослых пациентов с впервые выявленной или трудно контролируемой эпилепсией.
Леветирацетам в лечении эпилепсии, вызванной травмами головного мозга
Ряд исследований показал эффективность леветирацетама при травматических повреждениях головного мозга и в профилактической терапии послеоперационных судорог. В сравнительном исследовании монотерапии леветирацетамом и фенитоином для профилактики припадков при тяжелой черепно-мозговой травме Jones с соавторами [11] пришли к выводу, что леветирацетам столь же эффективен, как и фенитоин, для предотвращения ранних посттравматических приступов. Однако монотерапия леветирацетамом была связана с увеличением частоты патологических электроэнцефалографических данных.
В ретроспективном исследовании, посвященном изучению эффективности и переносимости леветирацетама для периоперативной профилактики припадков у пациентов с супратенториальными опухолями головного мозга [32], была продемонстрирована его периоперационная эффективность — снижение частоты постоперационных судорог (2,6 % в первую послеоперационную неделю) и возникновение незначительных и обратимых побочных эффектов (у 6,4 % пациентов). Преимуществом леветирацетама является то, что он не вызывает индукцию фермента цитохрома P450, что делает возможным раннее начало послеоперационной химиотерапии у пациентов со злокачественной глиомой.
Основной целью экспериментального исследования, проведенного Lim с соавторами [15], была оценка безопасности и возможности перехода от лечения фенитоином к монотерапии леветирацетамом после краниотомии и резекции глиомы у пациентов с судорожным синдромом, связанным с опухолью. Авторы пришли к выводу, что после выполнения краниотомии и удаления супратенториальной глиомы безопасно и целесо–образно переводить пациентов с лечения фенитоином на монотерапию леветирацетамом.
В открытом проспективном пилотном исследовании, проведенном Bahr с соавторами [1], исследователи оценили эффективность и переносимость внутривенного и перорального приема леветирацетама у пациентов с подозрением на первичные опухоли головного мозга и связанные с опухолью судороги. Они пришли к выводу, что пероральный и внутривенный прием является безопасным и эффективным при периоперационном лечении судорог, связанных с опухолью. Отсутствие эффекта от лечения даже после увеличения дозы свыше 3000 мг/сут отмечалось лишь у трех пациентов.
Леветирацетам как нейропротективное средство
Все большее внимание уделяется использованию леветирацетама с нейропротективной целью. В нескольких исследованиях было показано, что леветирацетам обладает значительными нейропротекторными свойствами как при эпилептических, так и при неэпилептических расстройствах.
Lopez-Gongora с коллегами оценивали изменения когнитивных функций и качество жизни пациентов с эпилепсией в течение одного года лечения леветирацетамом в качестве дополнительной терапии [17]. В исследовании участвовали 32 пациента (16 женщин, 16 мужчин), которые получали леветирацетам в качестве дополнительного лечения, из них 27 человек завершили однолетний период наблюдения. Пациенты получали леветирацетам в дозе 2000 мг/день. Нейропсихологические исследования и оценка качества жизни проводились в начале лечения и через один, три, шесть и двенадцать месяцев. Авторы отметили, что при однолетнем наблюдении отмечалось улучшение параметров памяти, моторных функций, вербальной беглости, внимания и качества жизни. Несмотря на ограниченные размеры выборки и отсутствие контрольной группы, авторы считают, что однолетний период лечения дает ценную информацию о долгосрочном влиянии препарата.
Проспективное одноцентровое рандомизированное сравнительное исследование применения леветирацетама и внутривенного фенитоина у пациентов с тяжелой черепно-мозговой травмой [28] показало, что леветирацетам может быть подходящей альтернативой внутривенному фенитоину с целью предотвращения припадков у данной категории пациентов. При назначении леветирацетама отмечалось уменьшение нежелательных побочных явлений и улучшение долгосрочных эффектов.
Клиническую эффективность, когнитивные и нейропсихологические эффекты леветирацетама при эпилепсии в ходе проспективного многоцентрового открытого исследования оценивал Tony Wu с коллегами [29]. У 69 пациентов оценивался противоэпилептический эффект, познавательные и нейропсихологические функции, а также качество жизни через 3 и 12 месяцев наблюдения. Результаты исследования показали, что леветирацетам не только эффективно уменьшает частоту приступов (68 % пациентов имели снижение частоты на 50 % и более после 1 года лечения), но и, возможно, способствует улучшению нейропсихологических и познавательных функций и качества жизни.
Проспективное сравнительное исследование, в котором были рандомизированы 52 пациента с травматическим черепно-мозговым повреждением или субарахноидальным кровоизлиянием, получавших профилактически леветирацетам или фосфенитоин, было проведено Steinbaugh с соавторами [25]. Его цель состояла в том, чтобы оценить возможность использования профилактического лечения, а также данных электроэнцефалографии в качестве предиктора появления приступов. Вывод состоял в том, что более выраженное снижение электроэнцефалографической активности было связано с худшими исходами и что профилактическое применение леветирацетама эффективнее фосфенитоина.
Сравнение эффектов леветирацетама и топирамата в лечении резистентной эпилепсии провел Chin-Wei Huang
с соавторами [6]. В исследование вошло 79 пациентов; 40 из них получали топирамат, а 39 — леветирацетам в течение года. Сравнивался противоэпилептический эффект, когнитивные функции в начале и через 12 месяцев лечения. Авторы показали, что на фоне приема леветирацетама когнитивные функции сохраняются, тогда как по поводу эффектов топирамата однозначных выводов получено не было. В связи с тем что исследование не было рандомизированным и размер выборки был относительно небольшим, авторы считают, что для окончательных выводов необходимы дальнейшие исследования.
Oliveira с коллегами исследовал головной мозг мышей, обработанный пилокарпином, и показал, что предварительная обработка леветирацетамом противодействует оксидативному стрессу за счет поддержания перекисного окисления липидов, нормальных уровней нитрит-нитрата, активности каталазы и глутатиона в гиппокампе [22]. Авторы пришли к выводу, что леветирацетам противодействует пилокарпининдуцированному оксидативному стрессу в гиппокампе и может рассматриваться как возможный нейропротективный агент.
Леветирацетам и гипералгезия
Леветирацетам является новым противосудорожным препаратом с доказанными анальгетическими свойствами. Его антиноцицептивные/антигипералгические эффекты были продемонстрированы в ряде работ на животных [20, 23, 26].
Влияние леветирацетама на пациентов с центральной нейропатической болью при рассеянном склерозе было исследовано в рандомизированном двойном слепом плацебо-контролируемом перекрестном исследовании [9]. Его цель состояла в том, чтобы исследовать независимые эффекты леветирацетама и сопутствующего лечения при нейропатической боли. Авторы сообщили, что леветирацетам не оказывал влияния на группу пациентов с центральной нейропатической болью при рассеянном склерозе.
Rossi с соавторами [24] также исследовали воздействие леветирацетама на центральную нейропатическую боль при рассеянном склерозе. Они провели одноцентровое перспективное рандомизированное однократное слепое плацебо-контролируемое исследование на выборке пациентов, которые не отвечали на базисную терапию. Их данные свидетельствуют о том, что леветирацетам является хорошо переносимым препаратом и действует на центральные механизмы боли, тем самым улучшая качество жизни пациентов с рассеянным склерозом.
Эффективность леветирацетама в профилактическом лечении мигрени была показана в небольшом открытом исследовании, проведенном Brighina с коллегами [4], в котором пациенты получали леветирацетам в дозе 1000 мг/сут в течение 6 месяцев. Авторы показали, что леветирацетам обычно хорошо переносится и эффективен при лечении мигрени.
Выводы
Таким образом, результаты многих исследований
показывают, что леветирацетам является достаточно высокоэффективным препаратом, обладающим противоэпилептическими, нейропротекторными и антигипер–алгическими свойствами. В связи с тем что фармакодинамика препарата не до конца изучена, необходимы дальнейшие исследования, которые выявят новые механизмы действия и показания к применению.
Конфликт интересов. Не заявлен.
Список литературы
1. Bahr O., Hermisson M., Rona S., Rieger J., Nussbaum S., Kortvelyessy P. et al. Intravenous and oral levetiracetam in patients with a suspected primary brain tumor and symptomatic seizures undergoing neurosurgery: The HELLO Trial // Acta Neurochir. (Wien). — 2012. — 154. — 229-35.
2. Ben-Menachem E., Falter U. Efficacy and tolerability of levetiracetam 3000 mg/d in patients with refractory partial seizures: A multicenter, double-blind, responder-selected study evaluating monothe–rapy // Epilepsia. — 2000. — 41 (10). — 1276-83.
3. Berkovic S.F., Knowlton R.C., Leroy R.F., Schiemann J., Falter U. Placebo-controlled study of levetiracetam in idiopathic genera–lized epilepsy // Neurology. — 2007. — 30 (69). — 1751-60.
4. Brighina F., Palermo A., Aloisio A., Francolini M., Giglia G., Fierro B. Levetiracetam in the prophylaxis of migraine with aura: A 6-month open-label study // Clin. Neuropharmacol. — 2006. — 29. — 338-42.
5. Brodie M.J., Perucca E., Ryvilin P., Ben-Menachem E., Meencke H.J. Comparison of levetiracetam and controlled release carbamazepine in newly diagnosed epilepsy // Neurology. — 2007. — 68. — 402-8.
6. Chin-Wei Huang, Ming-Chyi Pai, Jing-Jane Tsai. Comparative cognitive effects of levetiracetam and topiramate in intractable epilepsy // Psychiatry and Clinical Neurosciences. — 2008. — 62. — 548-553.
7. Christoph Helmstaedter, Juri-Alexander Witt. Cognitive outcome of antiepileptic treatment with levetiracetam versus carbamazepine monotherapy: A non-interventional surveillance trial //Epilepsy and Behavior. — 2010. — 18. — 74-80.
8. Cormier J., Catherine J.C. Safety and efficacy of levetiracetam for the treatment of partial onset seizures in children from one month of age // Neuropsychiatr. Dis. Treat. — 2013. — 9. — 295-306.
9. Falah M., Madsen C., Holbech J.V., Sindrup S.H. A rando–mized, placebo-controlled trial of levetiracetam in central pain in multiple sclerosis // Eur. J. Pain. — 2012. — 16. — 860-9.
10. Gurses C., Alpay K., Ciftci F.D., Bebek N., Baykan B., Gokyigit A. The efficacy and tolerability of levetiracetam as an add-on therapy in patients with startle epilepsy // Seizure. — 2008. — 17. — 625-30.
11. Jones K.E., Puccio A.M., Harshman K.J., Falcione B., Benedict N., Jankowitz B.T. et al. Levetiracetam versus phenytoin for seizure prophylaxis in severe traumatic brain injury // Neurosurg. Focus. — 2008. — 25. — 1-10.
12. Kozlowski P., Czepińska-Ćwik W., Kozlowska M., Kozlowska K. Levetiracetam-epilepsy treatment, pharmacokinetics, mechanism of action, interaction and toxicity // J. Educ. Health Sport. — 2015. — 5. — 143-50.
13. Lambrechts D.A.J.E., Sadzot B., van Paesschen W., van Leusdend A., Carpaye J., Bourgeois P. et al. Efficacy and safety of levetiracetam in clinical practice: Results of the SKATETM trial from Belgium and The Netherlands // Seizure. — 2006. — 15. — 434-42.
14. Lee Y.J., Kang H.C., Kim H.D., Lee J.S. Efficacy and safety of adjunctive levetiracetam therapy in pediatric intractable epilepsy // Pediatr. Neurol. — 2010. — 42. — 86-92.
15. Lim D.A., Chang E., Burt M., Chang S., Lamborn K.R., Tarapore L. et al. Safety and feasibility of switching from phenytoin to levetiracetam monotherapy for glioma-related seizure control following craniotomy: A randomized phase II pilot study // J. Neurooncol. — 2009. — 93. — 349-54.
16. Loscher W., Schmidt D. Which animal models should be used in the search for new antiepileptic drugs? A proposal based on experimental and clinical considerations // Epilepsy Res. — 1988. — 2. — 145-81.
17. Mariana Lopez-Gongora, Alejandro Martlnez-Dameno, Carmen Garcia, Antonio Escartfn Effect of levetiracetam on cognitive functions and quality of life: a one-year follow-up study // Epileptic. Disord. — 2008. — 10 (4). — 297-305.
18. Marini H., Costa C., Passaniti M., Esposito M., Campo G.M., Ientile R. et al. Levetiracetam protects against kainic acid-induced to–xicity // Life Sci. — 2004. — 74. — 1253-64.
19. Mendoza-Torreblanca J.G., Vanoye-Carlo A., Phillips-Farfa V.B., Carmona-Aparicio L., Gómez-Lira G. Synaptic vesicle protein 2A: Basic facts and role in synaptic function // Eur. J. Neurosci. — 2013. — 38. — 3529-39.
20. Micov A., Tomic M., Popovic B., Stepanovic-Petrovic R. The antihyperalgesic effect of levetiracetam in an inflammatory model of pain in rats: Mechanism of action // Br. J. Pharmacol. — 2010. — 161. — 384-92.
21. Morrell M.J., Leppik I., French J., Ferrendelli J., Han J., Magnus L. The KEEPER trial: Levetiracetam adjunctive treatment of partial-onset seizures in an open-label community-based study // Epilepsy Res. — 2003. — 54. — 153-61.
22. Oliveira A.A., Almeida J.P., Freitas R.M., Nascimento V.S., Aguiar L.M., Júnior H.V. et al. Effects of levetiracetam in lipid peroxidation level, nitrite-nitrate formation and antioxidant enzymatic activity in mice brain after pilocarpine-induced seizures // Cell. Mol. Neurobiol. — 2007. — 27. — 395-406.
23. Ozcan M., Ayar A., Canpolat S., Kutlu S. Antinociceptive efficacy of levetiracetam in a mice model for painful diabetic neuropathy // Acta Anaesthesiol. Scand. — 2008. — 52. — 926-30.
24. Rossi S., Mataluni G., Codecà C., Fiore S., Buttari F., Musel–la A. et al. Effects of levetiracetam on chronic pain in multiple sclerosis: Results of a pilot, randomized, placebo-controlled study // Eur. J. Neurol. — 2009. — 16. — 360-6.
25. Steinbaugh L.A., Lindsell C.J., Shutter L.A., Szaflarski J.P. Initial EEG predicts out- comes in a trial of levetiracetam vs. fosphenytoin for seizure prevention // Epilepsy Behav. — 2012. — 23. — 280-4.
26. Stepanovic-Petrovic R.M., Micov A., Tomic M., Ugresic N.D. The local peripheral antihyperalgesic effect of levetiracetam and its mechanism of action in an inflammatory pain model // Anesth. Analg. — 2012. — 115. — 1457-66.
27. Swaroop H.S., Ananya C., Nithin K., Jayashankar C.A., Satish Babu H.V., Srinivas B.N. Levetiracetam: A review of its use in the treatment of epilepsy // Int. J. Med. Biomed. Res. — 2013. — 2. — 166-72.
28. Szaflarski J.P., Sangha K.S., Lindsell C.J., Shutter L.A. Prospective, randomized, single-blinded comparative trial of intravenous levetiracetam versus phenytoin for seizure prophylaxis // Neurocrit. Care. — 2010. — 12. — 165-72.
29. Tony Wua, Chih-Chuan Chen, Ta-Cheng Chen, Yuan-Fu Tseng, Chen-Bang Chiang, Chin-Chuan Hung, Horng-Huei Liou. Clinical efficacy and cognitive and neuropsychological effects of levetiracetam in epilepsy: An open-label multicenter study // Epilepsy & Behavior. — 2009. —16. — 468-474.
30. Wang H., Gao J., Lassiter T.F., McDonagh D.L., Sheng H., Warner D.S. et al. Levetiracetam is neuroprotective in murine mo–dels of closed head injury and subarachnoid hemorrhage // Neurocrit. Care. — 2006. — 5. — 71-8.
31. Weinstock A., Ruiz M., Gerard D., Toublanc N., Stockis A., Faroo O. et al. Prospective open-label, single-arm, multicenter, safety, tolerability and pharmacokinetic studies of intravenous levetiracetam in children with epilepsy // J. Child Neurol. — 2013. — 28. — 1423-9.
32. Zachenhofer I., Donat M., Oberndorfer S., Roessler K. Peri–operative levetiracetam for prevention of seizures in supratentorial brain tumor surgery // J. Neuro Oncol. — 2011. — 101. — 101-6.