Вступ
Поширеність, різноманітність патологічних станів та потенційний ризик злоякісної трансформації епітелію шийки матки визначають високу значущість прогностичних критеріїв розвитку цервікальної інтраепітеліальної неоплазії [5]. Світові показники захворюваності на передракові патології шийки матки становлять, за даними різних авторів, від 1,5 до 20,0 % [5].
Як відомо, мішенню для онкогенного впливу є патологічні процеси, асоційовані з різними мікроорганізмами. Багаторічними дослідженнями встановлено, що в етіології передраку та раку шийки матки велику роль відіграє вірус папіломи людини (ВПЛ), що має тропність до багатошарового плоского епітелію [1]. ВПЛ був виявлений у 99,8 % випадків інвазивної карциноми шийки матки й більше ніж у 60 % випадків цервікальної інтраепітеліальної неоплазії (ЦІН). ВПЛ-обумовлена інфекція супроводжується глибоким пригніченням механізмів локального імунітету (клітинного та гуморального), а також відсутністю віремії й активного запалення [4].
До того ж на сьогодні немає єдиної думки про достатню клінічну ефективність використання існуючих методів лікування передракової патології шийки матки, що спонукає до більш детального вивчення даного питання [6].
У разі лабораторно доведеної ВПЛ-інфекції доцільною є противірусна та імуномодулююча терапія. З цією метою застосовують препарати, що містять інтерферон (ІФН), а також індуктори ендогенного інтерферону. Ці лікарські засоби можуть застосовуватися в рамках як системної, так і місцевої терапії. Особливостями індукційного механізму інтерферону є те, що вироблення ендогенного ІФН відбувається повільно. Потенціал клітин до вироблення ІФН швидко вичерпується (особливо в уражених клітинах), що обмежує захисні можливості організму. Не існує однозначних даних про таргетний вплив індукторів на одну лише систему ІФН: не можна з упевненістю говорити про безпеку прийому індукторів. Крім того, багато індукторів швидше руйнуються в організмі, ніж цитокіни [2].
З препаратів, зареєстрованих для застосування при лікуванні папіломавірусної інфекції, використовуються рекомбінантний інтерферон альфа-2b системно або у вигляді мазі, гелю та супозиторіїв, рекомбінантний інтерферон альфа-2а та очищений інтерферон альфа-n1, що застосовують підшкірно [2].
Останнім часом підвищену увагу клініцистів привернув ІФН-альфа-2b рекомбінантний (Лаферомакс, свічки, 3 000 000 ОД), що має виражену антивірусну, антипроліферативну й імуномодулюючу дію. Комплексний склад Лаферомаксу обумовлює ряд нових ефектів: при поєднанні з токоферолу ацетатом та аскорбіновою кислотою противірусна активність ІФН-альфа-2b рекомбінантного збільшується у 10–14 разів, підсилюється його імуномодулююча дія на Т- та В-лімфоцити, нормалізується вміст IgЕ, не утворюються антитіла, що нейтралізують антивірусну активність ІФН, навіть при його тривалому застосуванні (аж до 2 років). Після введення Лаферомаксу запускається цілий каскад реакцій: синтез протеїнів, пригнічення процесів проліферації, імуномодулююча активність (за допомогою фагоцитів, макрофагів та лімфоцитів), пригнічення реплікації вірусів у заражених клітинах [2].
Саме тому метою нашого проспективного клінічного дослідження стала оцінка ефективності ректальних супозиторіїв Лаферомакс у комплексному лікуванні пацієнток із цервікальною інтраепітеліальною неоплазією.
Матеріали та методи
У дослідженні брали участь 98 пацієнток із передраковою патологією шийки матки (ЦІН ІІ). Жінки були розподілені на дві групи: до дослідної клінічної групи були зараховані 28 пацієнток із верифікованою ЦІН ІІ та 20 пацієнток із ЦІН ІІІ, яким поряд із лазерною вапоризацією та радіохвильовою терапією (ексцизія та конізація) призначався препарат Лаферомакс по 1 свічці 3 000 000 МО ректально 2 рази на добу протягом 10 днів, повторний курс проводили через 1 міс. 30 жінок із ЦІН ІІ та 20 — із ЦІН ІІІ входили до групи порівняння, їм проводили хірургічне лікування та застосовували терапію згідно з Наказом № 236 МОЗ України від 02.04.2014 (без призначення Лаферомаксу). Середній вік жінок основної групи становив 29,6 ± 3,3 року, групи порівняння — 31,2 ± 4,6 року.
Лазерна вапоризація здійснювалася при застосуванні діодного лазера «Ліка-хірург», що працює в інфрачервоному діапазоні з довжиною хвилі 940 нм, терапевтичною вихідною потужністю 18 Вт (свідоцтво про державну реєстрацію № 4710/2006). При обробці за допомогою лазера патологічної ділянки застосовували вплив розфокусованим лазером 1 см2. Радіохвильовий високочастотний генератор «Сургітрон» мав одну істотну особливість: радіохвилі високої частоти 3,8–4,0 МГц виконували «холодний» розріз тканин при температурі від 38 до 80 °С.
Маніфестні форми папіломавірусної інфекції верифікувалися візуально, субклінічні — за наявності цитологічних змін і за відсутності клінічних проявів, латентні — при позитивних результатах полімеразної ланцюгової реакції на ВПЛ і за відсутності клінічних і цитологічних проявів папіломавірусної інфекції. При виявленні атипових клітин при цитологічному дослідженні і/або візуальному виявленні патології шийки матки проводилося розширене кольпоскопічне дослідження із застосуванням тесту з розчином 3% оцтової кислоти (Acetic acid test) для виключення патологічних станів (мозаїка, пунктація, атипові судини), тесту з розчином Люголя (Lugol’s test) для виявлення йод-негативних аномальних зон і здійснення за показаннями біопсії й гістологічного дослідження.
Дослідження було виконано на клінічних базах кафедри акушерства, гінекології та медицини плода Національної медичної академії післядипломної освіти імені П.Л. Шупика, кафедри акушерства й гінекології № 1 Вінницького національного медичного університету ім. М.І. Пирогова. Дослідження відповідало принципам, викладеним у Гельсінській декларації (1989) перегляду 2008 року, м. Сеул. Жінки, які були задіяні в дослідженні, давали письмову згоду на участь в ньому.
Первинний огляд після лікування проводили через 7–10 діб. Наступний огляд здійснювали через 5–6 тижнів, оскільки початкова епітелізація триває понад 24 дні (кольпоскопія). Через три місяці всім пацієнткам була виконана розширена кольпоскопія. Остаточний огляд виконували через 6 місяців після проведення терапії.
Клінічна оцінка терапевтичної ефективності зазначених методик лікування була нами проведена за такими критеріями:
— терміни відторгнення струпа та тривалість лім-фореї;
— терміни завершення епітелізації шийки матки;
— повноцінність епітелізації;
— ускладнення під час лікування;
— рецидиви захворювань шийки матки в ранні та віддалені терміни.
Для оцінки результатів лікування враховувалися дані огляду шийки матки в дзеркалах та результати кольпо-скопічного дослідження.
Статистичну обробку даних виконували з використанням методів варіаційної статистики, t-критерію Стьюдента.
Результати та обговорення
При порівняльному вивченні динаміки клінічних симптомів після проведеного лікування між групами були виявлені такі відмінності (табл. 1).
Ниючі болі внизу живота відзначали лише по 2 жінки з клінічних груп дослідження (7,1 та 6,7 % відповідно) із ЦІН ІІ, при тому що больовий синдром (ниючі, періодичні болі внизу живота) зберігався не більше ніж 10–14 діб після лікування. У 7 пацієнток із ЦІН ІІІ (17,5 %) також спостерігався больовий синдром: у 3 пацієнток з основної групи дослідження (15,0 %) та 4 — із групи порівняння (20,0 %).
У деяких пацієнток із патологією шийки матки після проведеного хірургічного лікування відзначалися серозно-сукровичні виділення зі статевих шляхів.
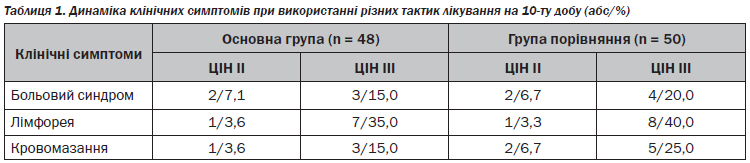
Кількість виділень оцінювали зі слів хворих та при огляді. Рясними вважалися виділення, при яких пацієнтка використовувала по 2 і більше прокладки на добу. Серед жінок клінічних груп дослідження через 10 днів від моменту лікування рясні серозно-сукровичні виділення зі статевих шляхів відзначали в 1 хворої в основній групі (3,6 %) та 1 (3,3 %) пацієнтки в групі порівняння із ЦІН ІІ, у 7 хворих жінок із ЦІН ІІІ, які отримували Лаферомакс (35,0 %), та 8 (40,0 %) пацієнток із ЦІН ІІІ, які використовували лише терапію згідно з Наказом № 236 МОЗ України від 02.04.2014. Через 5–6 тижнів вищевказаних скарг у пацієнток груп клінічного дослідження зареєстровано не було. Окремо ми хотіли б зупинитись на появі кровомазання у 8 пацієнток (20,0 %) із ЦІН ІІІ після 10-ї доби від початку радіохвильової хірургічної процедури. Через 5–6 тижнів подібних випадків не було зареєстровано в жодній клінічній групі проспективного дослідження.
Підвищення температури тіла не було нами зареєстровано в жодної пацієнтки на всіх етапах спостереження. Отже, клінічні симптоми (болі й виділення зі статевих шляхів) у групах проспективного дослідження не мали статистично вірогідної залежності від виду терапії.
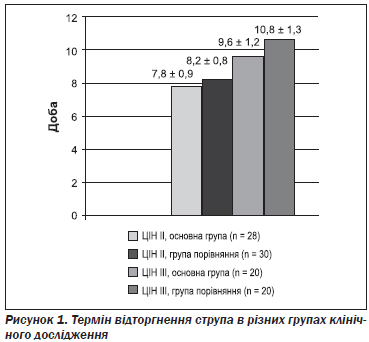
Огляд шийки матки в дзеркалах та кольпоскопічне дослідження шийки матки дозволили встановити, що застосування Лаферомаксу статистично вірогідно не сприяло більш ранньому відторгненню струпа (рис. 1).
У хворих жінок із ЦІН ІІ струп на фоні терапії препаратом, що містив ІФН-альфа-2b рекомбінантний, після лазерної вапоризації відпадав на 7,8 ± 0,9 доби в середньому. У пацієнток групи порівняння (ЦІН ІІ), які попередньо не отримували терапію Лаферомаксом та використовували базову терапію згідно з Наказом
№ 236 МОЗ України від 02.04.2014 р., фібринова плівка відторгалася на 8,2 ± 0,8 доби після лазерної вапоризації. На місці плівки при кольпоскопії визначалося рожевого кольору грануляційна тканина з поодинокими діапедезними крововиливами. Краї рани були згладженими.
При порівнянні термінів відторгнення струпа залежно від призначення Лаферомаксу у хворих жінок із ЦІН ІІІ, яким проводили радіохвильову терапію, також не було отримано статистично вірогідних відмінностей, у пацієнток з основної групи струп відторгався в середньому на 9,6 ± 1,2 доби. Тоді як у хворих, яким не призначалася імуномодулююча терапія, а використовувалася тільки базова терапія згідно з Наказом № 236 МОЗ України від 02.04.2014, він відторгався на 10,6 ± 1,3 доби.
Отже, за терміном відторгнення струпа відзначалася певна тенденція до пришвидшення перебігу початкової фази загоєння післяопераційної рани на фоні призначення запропонованого комплексу лікування. У пацієнток із ЦІН ІІ пришвидшення відторгнення струпа досягало 0,4 доби, у хворих на ЦІН ІІІ воно становило до однієї доби в середньому. Хоча й занотовані нами, ці зміни не мали статистичної відмінності.
Наступним етапом нашого дослідження стало визначення термінів постранової епітелізації дефектів шийки матки залежно від виду терапії.
При аналізі результатів лікування патології шийки матки різними методами ми виділяли такі дефінітиви:
— повний ефект — наявність завершеного процесу епітелізації, що характеризувалося кольпоскопічними ознаками багатошарового плоского епітелію по всій поверхні екзоцервікса через 5–6 тижнів після лікування;
— відсутність або неповний ефект — наявність неповної епітелізації шийки матки або збереження патологічної ділянки меншого діаметра протягом 3 місяців після констатації неповного ефекту;
— рецидив — повторна поява того ж захворювання шийки матки через 3 та більше місяці після досягнення повного ефекту.
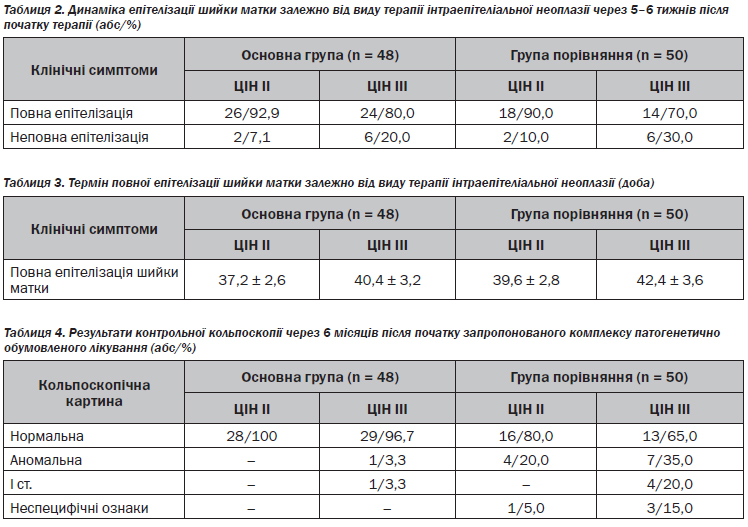
Через 5–6 тижнів після застосування хірургічних методів лікування передракової патології шийки матки були виявлені кольпоскопічні пейзажі повної та неповної епітелізації, а також аномальна кольпоскопічна картина (табл. 2).
Нормальна кольпоскопічна картина (або повна епітелізація) характеризувалася наявністю багатошарового плоского епітелію по всіх зонах та квадрантах шийки матки, епітеліальний стик збережений, строма звичайна, судини задовільно реагували на 3% розчин оцтової кислоти, проба Шиллера була позитивною.
З табл. 2 видно, що в пацієнток із верифікованою ЦІН ІІ відзначалось збільшення випадків повної епітелізації при використанні запропонованого комплексу патогенетично обумовленого лікування (26 — 92,9 %) на відміну від групи порівняння (24 — 80,0 %), відношення ризику (ВР) 2,80; 95% довірчий інтервал (ДІ) 0,61–12,70; р = 0,18.
При аналізі завершення процесу епітелізації у хворих жінок із ЦІН ІІІ після радіохвильової терапії нами було виявлено, що у 18 пацієнток (90,0 %) основної групи була діагностована повна епітелізація шийки матки. Тоді як тільки в 14 хворих жінок (70,0 %) із групи порівняння було відзначено такий результат, ВР 3,0; 95% ДІ 0,69–13,11; р = 0,14.
Кольпоскопічна картина в переважної кількості жінок, які були задіяні у клінічному дослідженні, на 5–6-й тиждень після оперативного лікування характеризувалася наявністю багатошарового плоского епітелію по всіх зонах і квадрантах шийки матки, епітеліальний стик був збережений, строма звичайна, судини задовільно реагували на 3% розчин оцтової кислоти, проба Шиллера була позитивною.
З аномальних кольпоскопічних пейзажів хотілося б звернути увагу на ацетобілий епітелій, пунктацію, мозаїку, йод-негативну зону, атипові судини як у зоні трансформації, так і за її межами. Подібні знахідки в переважній більшості випадків спостерігалися після лікування ЦІН ІІІ.
Що стосується часу повної репарації постопераційних ранових дефектів шийки матки, то у пацієнток із ЦІН ІІ повна епітелізація ранової поверхні шийки матки діагностувалася на 37,2 ± 2,6 доби (основна група) та 40,4 ± 3,2 доби (група порівняння) (табл. 3).
У хворих жінок, які отримували радіохвильову терапію з приводу ЦІН ІІІ, термін повної епітелізації при ініціальному лікуванні Лаферомаксом напередодні хірургічного лікування становив у середньому 39,6 ± 2,8 доби. Пацієнтки з групи порівняння, які отримували терапію, що регламентована Наказом № 236 МОЗ України від 02.04.2014, мали дещо пролонгований час повної епітелізації ранового дефекту — 42,4 ± 3,6 доби.
Через три місяці після оперативного лікування хотілося б зазначити, що однією з особливостей репаративних процесів після впливу діодного лазера, виявлених за допомогою кольпоскопії, була виражена васкуляризація епітеліальної поверхні. Загоєння операційної рани в пацієнток відбувалося на тлі формування під впливом лазерного променя тонкого, ніжного струпа без подальшого розвитку рубцевої тканини.
Через 6 місяців після лікування в основній групі скарги на виділення зі статевих шляхів пред’явили 5 (25,0 %) жінок із групи порівняння (ЦІН ІІІ), болі при статевому акті були в 1 (5,0 %) жінки, також після перенесеної радіохвильової хірургічної терапії. Менструальна функція була збережена в усіх пацієнток, причому менструальний цикл у них не змінився. Випадки рецидиву в клінічних групах дослідження у відведений термін спостереження (6 місяців) відзначались у двох жінок із ЦІН ІІ (6,7 %), що входили до групи порівняння.
Через 6 місяців після лікування Лаферомаксом серед пацієнток, які отримували хірургічне лікування (лазерна вапоризація та радіохвильова терапія), більше випадків нормальної кольпоскопічної картини спостерігалося у хворих на ЦІН ІІ — 28 (100,0 %) (табл. 4).
При порівняльному аналізі нормальної кольпоскопічної картини до та після лікування виявлені статистично значущі відмінності в усіх групах нашого проспективного клінічного дослідження. Результати контрольної кольпоскопії також свідчили про відсутність грубого рубцювання на шийці матки в усіх клінічних групах.
Аномальна кольпоскопічна картина у вигляді слабкого ураження (I ступеня) була діагностована в 1 (3,3 %) пацієнтки із ЦІН ІІ з групи порівняння після лазерної вапоризації (ВПЛ-позитивна) та 4 (20,0 %) пацієнток із ЦІН ІІІ, також з групи порівняння (ВПЛ-позитивні), після радіохвильової терапії; у вигляді йод-негативних ділянок — у 3 (15,0 %) ВПЛ-позитивних жінок із ЦІН ІІІ з групи порівняння після лікування.
Отже, відбулося вірогідне зниження (p < 0,05) кількості аномальних кольпоскопічних картин після проведеного комплексного лікування (хірургічна та імунокоригувальна терапія) в усіх групах даного клінічного дослідження. Подані вище результати позитивно характеризують методи лазерної вапоризації та радіохірургії в комбінації з імунокоригувальною терапією як прийнятні для пацієнток репродуктивного віку. Додавання Лаферомаксу в схему лікування пацієнток із ЦІН ІІ та ЦІН ІІІ дозволило підвищити клінічну ефективність традиційної терапії та домогтися позитивного результату в лікуванні.
Відсутність повного ефекту лікування ВПЛ може бути пов’язана з персистенцією вірусу поруч з ділянкою ураження в незміненому епітелії шийки матки, що не піддавався деструкції або видаленню при хірургічному втручанні.
Висновки
1. Для лікування ЦІН ІІ та ЦІН ІІІ, асоційованих із ВПЛ, доцільно використовувати хірургічне лікування (лазерна вапоризація та радіохвильова ексцизія відповідно) з додатковим призначенням Лаферомаксу по 1 свічці 3 000 000 МО ректально 2 рази на добу протягом 10 днів, повторний курс проводили через 1 міс.
2. Критеріями ефективності комплексного лікування інтраепітеліальних неоплазій шийки матки, асоційованих із ВПЛ, варто вважати відсутність аномальних кольпоскопічних пейзажів.