В Украине в структуре общей онкологической заболеваемости у женщин рак шейки матки (РШМ) составляет 6 %. Среди злокачественных новообразований органов репродуктивной системы РШМ занимает третье место после рака молочной железы и рака эндометрия. Ежегодно в Украине регистрируется свыше 5 тысяч первичных больных РШМ. Рак шейки матки является в мире четвертым по частоте встречаемости среди самых распространенных видов рака у женщин [1, 3, 5, 8].
Скрининговые обследования шейки матки позволяют выявлять большинство предраковых состояний на стадиях, когда их можно легко лечить. Раннее лечение позволяет предотвратить до 80 % случаев развития рака шейки матки. Лечение болезни на поздних стадиях малоперспективно и приводит к высокому уровню смертности от рака шейки матки. Высокую глобальную смертность от рака шейки матки (52 %) можно снизить благодаря эффективным программам скрининга на наличие вируса папилломы человека (ВПЧ) и предраковых изменений и вовремя проведенным терапевтическим мероприятиям [5–8]. ВПЧ является самой распространенной вирусной инфекцией, передающейся половым путем. Пиковый период приобретения инфекции как для женщин, так и для мужчин начинается сразу после того, как они становятся сексуально активными. Большинство случаев инфицирования ВПЧ не приводят к появлению симптомов или болезни и проходят самостоятельно. Однако устойчивая инфекция, вызванная определенными типами ВПЧ (чаще всего типами 16 и 18), может приводить к развитию предраковых патологических состояний шейки матки — дисплазии различной степени тяжести. Без лечения эти состояния в течение нескольких лет могут трансформироваться в рак шейки матки [6, 7].
На сегодняшний день рак шейки матки является самой распространенной болезнью, связанной с ВПЧ. Существует более 100 типов ВПЧ, из которых по меньшей мере 13 приводят к развитию рака. Несмотря на ограниченные данные об аногенитальных видах рака, отличных от рака шейки матки, все большее число фактических данных свидетельствует о связи ВПЧ с раком ануса, вульвы и влагалища. И хотя эти виды рака менее распространены, чем рак шейки матки, их связь с ВПЧ делает их потенциально предотвратимыми благодаря использованию таких же стратегий первичной профилактики, как и для рака шейки матки. Типы ВПЧ, не приводящие к раку (особенно типы 6 и 11), могут вызывать остроконечные кондиломы и респираторный папилломатоз. И хотя эти состояния очень редко приводят к смерти, они часто могут вызывать заболевания. Остроконечные кондиломы широко распространены и крайне контагиозны [2, 3, 6].
Хотя большинство инфекций ВПЧ проходят самостоятельно, существует риск того, что инфекция ВПЧ может стать хронической, а предраковые патологические состояния разовьются в инвазивный рак шейки матки. У женщин с нормально функционирующей иммунной системой рак шейки матки может развиться за 15–20 лет. У женщин с ослаб-ленной иммунной системой при отсутствии лечения на его развитие может потребоваться лишь 5–10 лет [4, 6, 8].
Иммунная система имеет важное значение в определении исхода ВПЧ-инфекции. Иммунная реакция на ВПЧ проявляется в виде системной защиты путем образования антител и местного иммунитета, индуцируя естественные киллеры. При эндометриозе отмечаются выраженные нарушения системного и локального звеньев иммунитета. Иммунодефицит создает благоприятные условия для развития клинических проявлений вирусного поражения [9, 10].
При лечении ВПЧ-инфекции целесообразно использовать принцип комбинированной терапии, включающей препараты, действие которых направлено на поддержку и укрепление защитных сил организма — иммунокорригирующие лекарственные средства.
Что касается хирургического лечения дисплазии шейки матки, то следует отметить, что, несмотря на его широкую распространенность и доказанную эффективность, нередки случаи рецидивов предраковых изменений, что обусловлено персистированием ВПЧ-инфекции. С учетом этого особое значение в терапии пациентов с ВПЧ имеет воздействие на иммунную систему с целью эрадикации ВПЧ [2, 3].
Цель исследования: изучение клинической эффективности свечей «Лаферомакс» в комплексном лечении пациенток репродуктивного возраста с дис-плазией шейки матки, ассоциированной с ВПЧ, при генитальном эндометриозе.
Материалы и методы исследования
В клиническую группу обследования были включены 48 женщин репродуктивного возраста (от 19 до 42 лет) с генитальным эндометриозом, которые в ходе обследования имели дисплазию шейки матки, ассоциированную с ВПЧ и микст-инфекцией урогенитального тракта.
План обследования пациенток включал сбор жалоб, анамнез заболевания и жизни, репродуктивной функции, общеклиническое исследование крови, гормональной функции щитовидной железы (пациентки с функциональными нарушениями щитовидной железы исключались из данной группы наблюдения), иммунограмму, гинекологический осмотр, расширенную кольпоскопию, ультразвуковое исследование органов малого таза, цитологическое исследование эпителия из экзоцервикса и цервикального канала, микроскопию урогенитальных выделений, выявление инфекций, передающихся половым путем (ИППП) (Chlamydia trachomatis, Ureaplasma urealyticum, Ureaplasma parvum, Mycoplasma hominis, Mycoplasma genitalium, ВПЧ высокоонкогенные и низкоонкогенные типы) методом полимеразной цепной реакции (ПЦР).
После полного обследования лечебные мероприятия включали назначение общей и местной комбинированной антибактериальной терапии, антимикотических препаратов, при необходимости — десенсибилизирующую терапию и гепатопротекторы. После применения местных антибактериальных свечей (6–10 дней) назначали иммуномодулирующую терапию (интерферон рекомбинантный альфа 2b) на протяжении 14 дней по 3 000 000 МЕ вагинально на ночь. В ряде случаев использовалась комбинированная иммуномодулирующая терапия (препарат рекомбинантного интерферона альфа 2b и индуктор синтеза эндогенного интерферона (аллоферон)).
Одним из наиболее изученных и эффективных препаратов интерферона для местного применения является препарат «Лаферомакс» (производства ООО «ФЗ «Биофарма», Украина). «Лаферомакс» обладает выраженными противовирусными, иммуномодулирующими и антипролиферативными свойствами, поскольку содержит в качестве активного компонента рекомбинантный интерферон альфа-2b в дозе 1 000 000 МЕ и 3 000 000 МЕ в форме ректальных суппозиториев. Важно, что «Лаферомакс» содержит токоферола ацетат и аскорбиновую кислоту, что выгодно отличает его от многих представителей данной фармакологической группы. Экспериментально установлено потенцирование противовирусных свойств рекомбинантного интерферона альфа-2b в 10–14 раз благодаря добавлению токоферола ацетата и аскорбиновой кислоты, а также иммуномодулирующее влияние на Т- и В-лимфоциты [1, 3, 4].
В ходе клинических исследований установлено, что даже на протяжении длительного приема «Лаферомакса» (около 2 лет) отсутствует выработка антител, которые способны инактивировать противовирусные свойства активного компонента препарата. Кроме того, на фоне применения «Лаферомакса» наблюдается улучшение функций эндогенных факторов иммунной системы. Суппозитории «Лаферомакс» предназначены для применения исключительно взрослыми пациентами при наличии ВПЧ-ассоциированных заболеваний, ИППП, микст-инфекций урогенитального тракта. Как правило, возникающие на фоне приема «Лаферомакса» побочные эффекты носят временный и умеренный характер. Суппозитории «Лаферомакс» не рекомендуется назначать при наличии индивидуальной невосприимчивости компонентов препарата, дисфункции щитовидной железы, тяжелых висцеральных нарушений у пациентов с саркомой Капоши, при наличии острых и хронических заболеваний сердечно-сосудистой системы, псориаза, гепато- и нефропатологии, заболеваний ЦНС, цирроза печени, хронического гепатита, возникновение которого может быть связано с иммунодепрессивной терапией (кроме кортикостероидов), аутоиммунных заболеваний, нарушения миелоидного ростка кроветворения [1, 3, 4].
Контроль эффективности терапии проводили через 2,5–3 недели после полного курса лечения. Под контролем кольпоскопического исследования производили забор для контроля цитологии из экзоцервикса и цервикального канала, наличие ИППП определяли методом ПЦР. При необходимости продолжали применение иммуномодулирующей терапии по 3 000 000 МЕ вагинально 3–4 раза в неделю на протяжении 1–2 месяцев под контролем иммунограммы и гормональной функции щитовидной железы.
Результаты и обсуждение
В ходе обследования у 22 (45,8 %) пациенток выявлен аденомиоз, у 11 (22,9 %) — наружный эндометриоз (подтвержден лапароскопически ранее — сочетание эндометриом и перитонеального эндометриоза), 15 (31,2 %) пациенток имели сочетанные формы наружного и внутреннего эндометриоза.
Среди жалоб отмечались более обильные бели у 11 (22,9 %) пациенток, изменения характера выделений и частые циститы у 12 (25 %) женщин. У 25 (52 %) пациенток изменения эпителия шейки матки и наличие ВПЧ были выявлены в ходе обследования по поводу бесплодия.
Результаты иммунного статуса характеризовались нарушением гомеостаза, а именно снижением В- и Т-лимфоцитов в 1,9 раза, снижением IgG в 3 раза, IgА — в 4,2 раза и IgМ — в 1,8 раза по сравнению с нормальными показателями иммунограммы (р < 0,05).
Высокоонкогенные типы ВПЧ были обнаружены у 32 (66,6 %) пациенток, низкоонкогенные — у 16 (33,3 %) женщин. Микст-инфекция была представлена уреаплазмой и микоплазмой у 26 (54,1 %) пациенток, уреаплазма, микоплазма и хламидиоз — у 12 (25 %), 10 (20,8 %) пациенток имели неспецифический воспалительный процесс и ВПЧ.
Кольпоскопические и цитологические изменения эпителия шейки матки были следующими: 25 (52 %) пациенток c CINI, CINII наблюдался у 21 (43,7 %) женщины, 2 (4,1 %) пациентки имели CINIIIa (путем взятия биопсии на стыке нормального и пораженного эпителия были исключены инвазивные процессы шейки матки).
После проведения полного курса лечения отмечалась значительная положительная кольпоскопическая динамика, а именно уменьшение площади с признаками дисплазии (лейкоплакия, ацетобелый эпителий, пунктация, шероховатый рельеф папиллярной зоны дисплазии). У 26 (81,2 %) женщин с высокоонкогенным ВПЧ и у 15 (93,7 %) с низкоонкогенным ВПЧ получены отрицательные результаты при повторном ПЦР-исследовании, а также отрицательные результаты микст-инфекций. 7 (14,5 %) пациенткам была продолжена терапия «Лаферомаксом» по схеме 3 000 000 МЕ по 1 свече на ночь 4 раза в неделю на протяжении 1,5–2 месяцев под цитологическим контролем. 4 (8,3 %) пациенткам под контролем кольпоскопа и пробы Шиллера была проведена радиоволновая хирургия шейки матки путем конусовидного иссечения пораженных тканей, с последующим гистологическим исследованием.
Контроль эффективности лечения проводился через 6–8 недель после лечебных мероприятий и показал нормальную кольпоскопическую картину у 47 (97,9 %) пациенток и отсутствие CIN и воспалительного процесса.
Клинический случай
Пациентка М., 27 лет, обратилась в клинику для лечения бесплодия путем проведения вспомогательных репродуктивных технологий с диагнозом: вторичное бесплодие. Наружный и внутренний эндометриоз. Спаечная болезнь органов малого таза.
В анамнезе хламидиоз, проводилось лечение. Трижды оперативное вмешательство лапароскопическим доступом: 1 — по поводу правосторонней трубной беременности, произведено удаление правой маточной трубы, сальпингоовариолизис, коагуляция эндометриоидных очагов брюшины малого таза; 2 — энуклиация эндометриоидной кистомы левого яичника (кистома эндометриоидная, 8 × 6 см, капсула без папиллярных разрастаний); 3 — левосторонняя тубэктомия по поводу левосторонней внематочной трубной беременности.
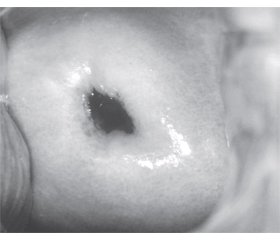
В ходе полного обследования и подготовки к IVF выявлена уреаплазма и ВПЧ типа 11, 16, 33, 56. Выявлены изменения эпителия экзоцервикса при кольпоскопическом обследовании (кольпоскопическая картина отвечает дисплазии эпителия шейки матки средней степени) — абнормальная кольпоскопическая картина, эктопия цилиндрического эпителия, незаконченная зона трансформации, ацетобелый эпителий (рис. 1). Заключение цитологического исследования — CINII.
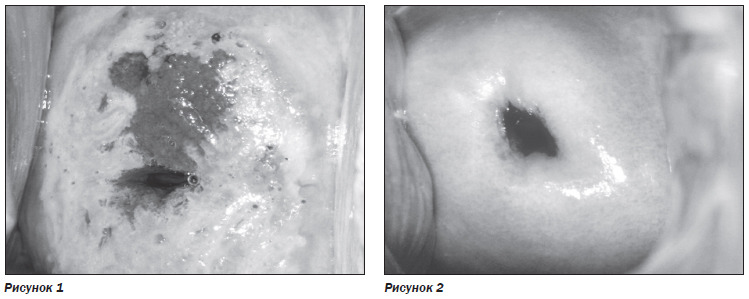
Было проведено лечение по вышеуказанной схеме в течение 3 циклов. В результате лечения была достигнута нормальная кольпоскопическая картина (рис. 2), цитология — тип I, результаты ИППП — не выявлены. Беременность наступила в первом цикле IVF и закончилась нормальными срочными родами и рождением здорового ребенка.
Выводы
Таким образом, результаты клинических наблюдений свидетельствуют о высокой эффективности применения иммуномодулирующей терапии свечами «Лаферомакс» в комплексном лечении пациенток репродуктивного возраста с дисплазией шейки матки, ассоциированной с ВПЧ и микст-инфекцией, что позволило на фоне иммунодефицита при эндометриозе добиться хорошего клинического эффекта, отрицательных результатов ВПЧ и микст-инфекции у 85,4 %, а также у 97,9 % — нормальных цитологических результатов исследования эпителия шейки матки и цервикального канала.