Журнал «Почки» Том 7, №1, 2018
Фокально-сегментарный гломерулосклероз: генетический анализ и целевая терапия
Резюме
При фокально-сегментарному гломерулосклерозі (ФСГС) відбувається початкове пошкодження подоцитів. Генетичні дослідження людини за останні кілька років показали, що ФСГС — це насамперед подоцитопатія з більш ніж 20 мутованими генами, що беруть участь у патогенезі даного захворювання. Нефрин (ген NPHS1) разом із подоцином (ген NPHS2) є основними білками щілинної діафрагми подоцитів. Аутосомно-рецесивні мутації NPHS1 та NPHS2 пов’язані з більш тяжким станом пацієнтів, що проявляється ранньою протеїнурією і термінальною нирковою недостатністю, ніж аутосомно-домінуючі мутації INF2, TRPC6 і ACTN4. Для ініціального лікування ФСГС Kidney Disease Improving Global Outcomes 2012 р. рекомендує використовувати кортикостероїдну й імуносупресивну терапію.
При фокально-сегментарном гломерулосклерозе (ФСГС) происходит исходное повреждение подоцитов. Генетические исследования человека за последние несколько лет показали, что ФСГС — это прежде всего подоцитопатия с более чем 20 мутированными генами, участвующими в патогенезе данного заболевания. Нефрин (ген NPHS1) вместе с подоцином (ген NPHS2) являются основными белками щелевой диафрагмы подоцитов. Аутосомно-рецессивные мутации NPHS1, NPHS2 связаны с более тяжелым состоянием пациентов, что проявляется ранней протеинурией и терминальной почечной недостаточностью, чем аутосомно-доминирующие мутации INF2, TRPC6 и ACTN4. Для инициального лечения ФСГС Kidney Disease Improving Global Outcomes 2012 г. рекомендует использовать кортикостероидную и иммуносупрессивную терапию.
With focal segmental glomerulosclerosis (FSGS) is associated with initial damage of podocytes. Human genetic studies over the last few years have shown that FSGS is primarily a podocytopathia with more than 20 mutated genes involved in the pathogenesis of this disease. Nephrin (NPHS1 gene) together with the podocine (NPHS2 gene) are the main proteins of podocyts slit diaphragm. Autosomal-recessive mutations of NPHS1, NPHS2 are associated with more severe condition of patients, which is manifested by early proteinuria and end-stage renal disease compared with autosomal-dominant mutations of INF2, TRPC6 and ACTN4. For initial treatment of FSGS, Kidney Disease Improving Global Outcomes (KDIGO) 2012 recommends the use of corticosteroid and immunosuppressive therapy.
Ключевые слова
фокально-сегментарний гломерулосклероз; подоцити; мутації білків; лікування
фокально-сегментарный гломерулосклероз; подоциты; мутации белков; лечение
focal segmental glomerulosclerosis; podocytes; protein mutations; treatment
Фокально-сегментарный гломерулосклероз (ФСГС), известный также как фокальный и сегментарный гиалиноз, фокальный гломерулярный склероз, фокальный гломерулосклероз, фокально-сегментарный гломерулонефрит, фокальный склероз с гиалинозом, является одной из наиболее распространенных форм гломерулярного заболевания почек, приводящей к терминальной стадии почечной недостаточности, которая требует заместительной почечной терапии. «Фокальный» означает, что некоторые из клубочков преобразуются в рубцовую ткань, в то время как другие остаются нормальными, а «сегментарный» свидетельствует о том, что повреждена только часть отдельного клубочка. ФСГС составляет 7–20 % идиопатического нефротического синдрома у детей и 40 % — у взрослых [1].
В 1925 г. немецкий врач-патологоанатом T. Fahr [2] опубликовал первый рисунок клубочка почки в мельчайших деталях. Позднее, в 1957 г., A. Rich [3] описал сегментный склероз с участием юкстамедуллярных клубочков в образцах после аутопсии у детей, умерших от нефротического синдрома, вызванного липоидным нефрозом. Ученый предположил, что развитие гломерулосклероза связано с прогрессированием почечной недостаточности, которая наблюдалась в группе детей с идиопатическим нефротическим синдромом.
ФСГС характеризуется мезангиальным склерозом, облитерацией капилляров, гиалинозом, пенистыми клетками и адгезией между гломерулярным пучком и капсулой Боумена (рис. 1).
В 2004 г. группа врачей-патологов определила гистологические варианты и предложила стандартизировать патологическую классификационную систему ФСГС, которая полностью основывается на световой микроскопии. Данная система, известная как Колумбийская классификация, определяет 5 гистологических вариантов: перихилярный, Tip lesions (периферический), коллапсирующий, клеточный и классический NOS (Not Otherwise Specified) [4] (рис. 2).
Если ни одна из вышеупомянутых конкретных вариаций не наблюдается при биопсии, болезнь называется классическим ФСГС. Not Otherwise Specified означает, что «не указано иное». Частота встречаемости вариантов ФСГС: классический — 42 %, перихилярный — 26 %, Tip Lesion — 17 %, коллапсирующий — 11 % и клеточный — 3 %.
Гистологические варианты ФСГС различаются этиологически.
Этиологическая классификация ФСГС [5]
— Первичный ФСГС (идиопатический). Причина развития данной патологии неизвестна.
— Вторичный ФСГС.
1. Генетические мутации: NPHS1, NPHS2, CD2AP, TRPC6, ACTN4, INF2, ANLN, ARHGAP24, ARHGDIA, WT-1, LMX1B, LAMB2, PAX2, COQ2, COQ6, PDSS2, ADCK4 и др.
2. Вирус-ассоциированные: HIV-1, парвовирус B19, вирус Эпштейна — Барр, вирус Коксаки.
3. Индуцированные лекарственными препаратами (интерферон-альфа, литий, памидронат/алендронат, анаболические стероиды, героин и др.).
4. Адаптивные структурно-функциональные ответы, такие как гломерулярная гипертрофия или гиперфильтрация.
4.1. Уменьшение массы почки: олигомеганефрония, односторонняя почечная недостаточность, дисплазия почки, рефлюкс-нефропатия, хирургическая абляция почки, хроническая нефропатия аллотрансплантата, заболевание почек с уменьшением функционирования нефронов.
4.2. Первоначально нормальная масса почки: сахарный диабет, гипертензия, ожирение, врожденные цианозные пороки сердца, серповидноклеточная анемия.
5. Злокачественные новообразования (лимфома).
6. Неспецифический характер ФСГС, вызванный сморщиванием почки.
Фокальные пролиферативные гломерулонефриты (IgA-нефропатия, волчаночный нефрит, иммунный фокальный некротизирующий и крестообразный гломерулонефриты). Наследственный нефрит (синдром Альпорта), мембранная гломерулопатия, тромботическая микроангиопатия.
При ФСГС происходит исходное повреждение подоцитов или подоцитопатия с дальнейшим прогрессированием гломерулосклероза и увеличением мезангиальной матрицы.
Подоциты и их дисфункция при ФСГС
У взрослого человека почка имеет 0,33–1,4 миллионов клубочков (гломерул), представляющих собой капиллярную сеть, состоящую из ~ 50 петель [6]. Функция гломерул состоит в фильтрации маленьких растворенных веществ и генерировании первичной мочи. Во время процесса фильтрации кровь течет в капиллярные пучки от афферентной артерии. Молекулы, молекулярный вес которых составляет менее 40 кДа, включая глюкозу, мочевину, неорганические ионы и воду, проходят через фильтрационный барьер и входят в капсулу Боумена.
Фильтрационный барьер представляет собой 3-слойную структуру [7]:
1. Внутренний слой — плотноупакованный эндотелий.
2. Средний слой — гломерулярная базальная мембрана (ГБМ), образованная отрицательно заряженными и гликозилированными белками внеклеточного матрикса.
3. Внешний слой — висцеральные эпителиальные клетки или подоциты (рис. 3).
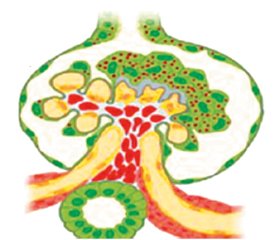
Подоциты являются высокодифференцированными и специализированными клетками, имеющими сложную цитоархитектуру, которые обертываются вокруг клубочковых капилляров и являются основным компонентом гломерулярного фильтрационного барьера (рис. 4).
/56-2.jpg)
Дисфункция подоцитов является главной особенностью современной парадигмы для патогенеза ФСГС [8]. В экспериментальных моделях с градуированными уровнями повреждения подоцитов степень подоцитопении сильно коррелировала с гистологической моделью повреждения [9]. Было показано, что потеря менее 20 % подоцитов может регенерироваться резидентными гломерулярными эпителиальными стволовыми клетками, которые мигрируют из ниши, прилегающей к капсуле Боумена в клубочек и заменяют поврежденные подоциты, которые могут теряться при некрозе или апоптозе. Если потеря подоцитов находится в диапазоне 20–40 %, появляются повреждения, характерные для ФСГС, а если потеря подоцитов превышает 40 %, то это приводит к глобальному склерозу. Хотя детали патогенеза ФСГС полностью не установлены, тем не менее доказано, что мутации генов, кодирующие белки щелевой мембраны подоцитов, лежат в основе развития наследственных форм этого заболевания [10]. У нескольких семей обнаружены и описаны разнообразные мутации генетических факторов при ФСГС [11].
Мутированные гены подоцитов и их участие в ФСГС
Генетические исследования человека за последние несколько лет показали, что ФСГС — это прежде всего подоцитопатия с более чем 20 мутированными генами подоцитов, участвующими в патогенезе данного заболевания [12] (рис. 5).
Основные белки и кодирующие их гены в подоцитах можно разделить на следующие категории (табл. 1):
1. Подоцит-ассоциированные молекулы щелевой диафрагмы и сигнальные белки.
2. Компоненты цитоскелета подоцита.
3. Ядерные белки.
4. Белки гломерулярной базальной мембраны.
5. Митохондриальные белки.
6. Лизосомальные белки.
7. Другие белки.
Характеристика наиболее важных белков подоцитов и мутации их генов, которые приводят к ФСГС
1. Нефрин
Первым геном подоцитов (NPHS1), обнаруженным у пациентов с врожденным нефротическим синдромом (ВНС) финского типа, был –мутированный белок нефрин, что явилось революционным открытием в понимании патогенеза ФСГС [13]. Частота заболеваемости новорожденных в Финляндии составляет 1 : 10 000 и реже в других странах. Несмотря на то, что идентифицированы миссенс-мутации у пациентов с ВНС, две мутации Fin-major (делеция нуклеотидов 121 и 122) и Fin-minor (преждевременная остановка синтеза аминокислоты 1109) составляют более 90 % случаев в Финляндии. Рецидив протеинурии после трансплантации почки в результате появления антинефриновых антител составляет 20 % у пациентов с генотипами Fin-major/Fin-major. Мутации в гене NPHS1, отвечающие за ВНС финского типа, являются аутосомно-рецессивным типом наследования, который характеризуется массивной протеинурией [14]. Ген человека NPHS1 расположен на длинном плече хромосомы 19q13.1 и содержит 29 экзонов. Продуцируемый белок, называемый «нефрин», принадлежит к суперсемейству иммуноглобулинов [15, 16]. Нефрин представляет собой большой трансмембранный белок, состоящий из 1241 аминокислоты, имеющий восемь внеклеточных мест Ig-связывающих участков, фибронектин III-связывающий участок, трансмембранный и внутриклеточный домен (рис. 6).
/57-2.jpg)
Механизм действия нефрина состоит в том, что он, являясь сигнальной молекулой, стимулирует митогенактивированные протеинкиназы. Сигнал, индуцированный нефрином, значительно усиливается подоцином, который связывает цитоплазматический домен нефрина. Анализ мутаций подтверждает, что патологическая или неэффективная сигнализация через нефрин-подоциновый комплекс приводит к дисфункции подоцитов и протеинурии [17]. К настоящему времени идентифицированы более 90 мутаций гена NPHS1, которые распределены по всему гену NPHS1 [18–21]. Эти мутации включают небольшие делеции, инсерции, нонсенс-, миссенс- и сплайс-сайт-мутации. Самое большое количество мутаций NPHS1 принадлежит миссенс-мутациям, что приводит к единичным заменам аминокислот. Классические мутации наблюдаются у детей с нефротическим синдромом в течение от нескольких дней после рождения и до 3 месяцев [22]. Недавно А. Philippe и др. идентифицировали мутации у детей от 5 месяцев до 8 лет [23]. У пациентов с мутациями NPHS1, кроме почечной патологии, могут наблюдаться неврологические симптомы, включающие мышечную гипотонию, дискинезию, церебральную атрофию и нарушение слуха [24].
2. Подоцин
Подоцин — член семейства стоматиновых белков, кодируется геном NPHS2, расположенным на 1q25-q31-хромосоме [25]. Мутации NPHS2 впервые были описаны у детей с семейным стероидрезистентным идиопатическим нефротическим синдромом. NPHS2-мутации у человека в основном связаны с аутосомно-рецессивным стероидрезистентным нефротическим синдромом (СРНС), однако могут встречаться спорадические случаи СРНС. Обнаружено более 116 патогенных мутаций, связанных с данным заболеванием [26–28]. Эти мутации изменяют экспрессию гена и структуру белка. Подоцин, как и нефрин, связан с липидным слоем, обеспечивая стабильный и правильно функционирующий фильтрационный барьер. СООН-терминальный домен подоцина связывается c NEPH-1, структурным белком щелевой мембраны подоцитов. Мутированный подоцин может вызвать нарушения при встраивании нефрина в плазматическую мембрану, что сопоставимо с отсутствием нефрина в щелевой мембране [29]. Подоцин с вариантом R229Q встречается наиболее часто и имеет 3,6% частоту аллелей в популяции. Также отмечена связь варианта R229Q с микроальбуминурией [30]. Мутантная форма NPHS2 с вариантом R138Q (одна из наиболее часто встречающихся мутаций) приводит к мутации подоцина в эндоплазматическом ретикулуме. Оба мутантных белка не способны взаимодействовать с нефрином, в результате чего нефрин теряет свои свойства сигнального белка [31]. У пациентов с мутацией NPHS2 не было отмечено рецидивов ФСГС после трансплантации почки по сравнению с пациентами с идиопатической ФСГС [32]. Пациенты с гетерозиготной мутацией NPHS2 имеют более высокий риск ФСГС в отличие от пациентов с гомозиготными мутациями [33].
3. CD2-ассоциированный белок
CD2-ассоциированный белок (СD2AР) представляет собой молекулу, первоначально идентифицированную как лиганд для Т-клеточного адгезивного белка 2. СD2AР — цитоплазматический белок с м.в. 80 кДа, который экспрессируется во всех тканях, кроме мозга. Играет ключевую роль в почках, где он необходим для функционирования щелевой диафрагмы для обеспечения фильтрационных функций. Первично экспрессируется в клубочках подоцитов и взаимодействует с нефрином и подоцином [34, 35]. Отсутствие гломерулярной экспрессии СD2AР у животных способствует продуцированию пролиферации мезангиальных клеток с осаждением внеклеточного матрикса и гломерулосклерозом [36]. Huber и др. показали, что как нефрин, так и СD2AР взаимодействуют с регуляторной субъединицей р85 фосфоинозитид-3-ОН-киназы (PI3K) и вместе с подоцином стимулируют PI3K-зависимый сигнал АКТ (протеинкиназа В или серин-треонин-киназа) в подоцитах (рис. 7).
Подоциты, лишенные СD2AР, становятся очень восприимчивы к апоптозу, что приводит к апоптической гибели подоцитов in vitro [37]. В кодирующей области гена СD2AР у пациентов с ФСГС обнаружены три мутации. Мутация р.К301М локализована на N-концевом остатке (аминокислоты 1-334), которая взаимодействует с регуляторной единицей р85 PI3K и вместе с подоцином и нефрином стимулирует активацию АКТ. Вторая мутация (р.delGlu525) приводит к удалению Glu525 с последующим образованием более короткого белка СD2AР. М. Lowik и др. [38] описали пациента с нефротическим синдромом, связанным с гомозиготной мутацией СD2AР (с.1834С>Т) в С-терминальном участке, что привело к изменению белка (аминокислота в позиции 612 (р.R612X)).
4. Транспортный рецептор белка катионного канала 6
Транспортный рецептор белка катионного канала 6 (TRPC6) представляет собой неселективный катионный канал классического субсемейства TRPC [39, 40]. TRPC опосредуют поступление кальция через гормональную стимуляцию через фосфолипазу С и последующее расщепление фосфатидилинозитидов с образованием диацилглицерола, который напрямую активирует TRPC6 [41]. В почках TRPC6 обнаруживается вдоль гломерул и собирающего канальца. TRPC6 взаимодействует с подоцином, белком щелевой диафрагмы, интегрированным в сигнальный комплекс подоцита. Описано шесть мутаций TRPC6 (P112Q, N143S, S270T, K874*, R895C и E897K) [42, 43], а также мутации в гене TRPC6 человека (P15S, N110H, G109S, N125S, L780P, M132T, R175Q, R360H, L395A, A404V, Q889K, G757D, H218L, R895L) [44]. При функциональном исследовании мутантных кДНК TPRC6 обнаружено увеличение поступления кальция по сравнению с диким типом [45, 46]. Повышение поступления кальция в подоциты приводит к гибели подоцитов и развитию ФСГС.
5. Альфа-актинин-4
Альфа-актинины — это стержневидные белки, образующие гомодимеры по типу «голова — хвост». Альфа-актининовые мономеры содержат три различных домена: N-терминальный актинсвязывающий домен, четыре спектринсвязывающих повтора и С-терминальный остаток. Существует четыре альфа-актинина человека (ACTN 1–4). ACTN4 представляет собой актин-связывающий белок, который играет важную роль в целостности структуры цитоскелета подоцита и связан с подвижностью клеток. Экспрессия ACTN4 значительно выражена во многих тканях человека, однако фенотип, ассоциированный с мутацией ACTN4, проявляется только в почках и связан с аутосомно-доминантной формой семейной ФСГС. У ACTN4-трансгенных мышей развиваются тяжелое гломерулярное заболевание и ФСГС [47]. К настоящему времени известны следующие миссенс-мутации ACTN4: K255E, T259I, S262P, W59R, I149del V801M, R348Q, R837Q и R310Q (48) (рис. 8).
/60-1.jpg)
Было показано, что мутированные ACTN4-белки имеют высокую связывающую аффинность к F-актину и могут изменять механические характеристики подоцитов [49]. Кроме того, конформационные изменения также приводят к увеличению актинсвязывающей стехиометрии и резистентности в регуляции Са2+ [50].
6. Инвертированный формин 2
Мутация INF2 является наиболее распространенной причиной аутосомно-доминантного ФСГС. Инвертированный формин 2 (INF2) является членом субсемейства актинрегулирующих белков (mDia), которые служат эффекторами для RhoA (небольшие ГТФ-азные белки), регулирующими актиновый цитоскелет и модулирующими клеточную поверхность, подвижность, полярность, клеточный цикл и транскрипцию. Избыточная активация RhoA индуцирует повреждение подоцитов и приводит к развитию ФСГС [51]. Большинство описанных мутаций INF2 являются гетерозиготными вариантами миссенс-мутаций, сгруппированных в экзонах 2–4, которые кодируют N-терминальный DID-белок [52]. Мутации INF2 приводят к утрате его ингибиторной функции и смещению баланса в сторону активации mDia. Мутации INF2 составляют 9–17 % семейных случаев ФСГС и редко связаны со спорадическими случаями [53].
7. Rho-GDP-диссоциации ингибитора 1
Мутации Rho-GDP-диссоциации ингибитора 1 (ARHGDIA) недавно были идентифицированы у младенцев [54]. ARHGDIA регулирует GDP/GTP-связывание с RHO GTF-азами. Он может действовать как регуляторный переключатель, определяя долю RHO GTF-аз для связывания GDP (неактивная) по сравнению с GTP (активная). Экспрессия мутантного ARHGDIA приводит к увеличению RAC1 и CDC42. Данные о мутации ARHGDIA необходимы для информации о регуляции актинового цитоскелета при функционировании подоцитов.
8. Белок опухоли Вильямса
Белок опухоли Вильямса (WT1) — фактор транскрипции, регулирующий несколько программ клеточной пролиферации и дифференциации. Белок WT1 содержит 92 аминокислоты и экспрессируется в почках плода и селезенке. Ген WT1 позиционируется в связи с его ролью в развитии опухоли Вильямса, являющейся наиболее распространенной формой рака у детей [55]. Гетерозиготные мутации WT1 вызывают синдром Дениса — Драша (урогенитальные аномалии, почечная недостаточность, псевдогермафродитизм и опухоль Вильямса) и синдром Фрайзера (мужской псевдогермафродитизм, прогрессирующая гломерулопатия). Это два перекрывающихся синдрома, характеризующиеся диффузным мезангиальным склерозом, ФСГС, мочеполовыми дефектами и высоким риском развития опухоли Вильямса [56]. Для синдрома Фрайзера характерно отсутствие опухоли Вильямса. WT1 имеет транскрипционно-регулирующий домен (экзоны 1–6) и ДНК-связывающий домен (экзоны 7–10).
9. Ламинин, субъединица бета-2
Мутации LAMB2 впервые были описаны у пациентов с нарушением центральной нервной системы в сочетании со сложными глазными аномалиями и тяжелыми нейродегенеративными расстройствами, например синдромом Пирсона [57]. Ген LAMB2 кодирует белок ламинин-β2, являющийся важным гликопротеиновым компонентом гломерулярной базальной мембраны, который связывает α3β1-интегрин, тем самым способствуя связи подоцитов с ГБМ [58]. Ламинин, связавшийся с ГБМ, может индуцировать модуляцию актинового цитоскелета. Синдром Пирсона наблюдается при усеченных мутациях LAMB2, в то время как пациенты с миссенс-мутациями, такими как R246Q и C321R, имеют нефротический синдром со значительно более мягкими экстраренальными дефектами [59].
10. Лизосомный мембранный белок 2 (LIMP2)
Гомозиготные усеченные мутации гена SCARB2, кодирующего LIMP2 (рецептор β-глюкоронидазы), связаны с миоклонусренальным синдромом [60]. Это аутосомально-рецессивный синдром, который проявляется у подростков и молодых людей как коллапсирующий ФСГС и прогрессирущий миоклонической эпилепсией. Неврологический фенотип подобен лизосомальной болезни накопления, наблюдаются дефекты аутофагии. При заболевании лизосомальной болезни накопления аутофагосомы не способны проникнуть в лизосомы, в результате чего происходят аккумуляция белков, митохондриальная дисфункция и гибель клетки [61]. Дисрегуляция аутофагии может рассматриваться как потенциальный механизм SCARB2-опосредованного повреждения подоцитов.
11. Митохондриальные белки
Идентификация мутаций в митохондриальных генах привела к пониманию важности митохондрий для функционирования подоцитов. Обнаруженные мутации A3243G в гене MT-TL1, кодирующем тРНК лейцина, вызывают респираторный дефект цепи и индуцируют ФСГС [62]. Некоторые генетические дефекты в синтезе михондриального коэнзима Q10 (CoQ10) приводят к подоцитопатиям: мутации в гене COQ2 (кодирует парагидро–ксибензоат-полипренил-трансферазу) были идентифицированы у некоторых пациентов с ранним началом нефротического синдрома с нейромышечными симптомами или без них [63]. Мутации в гене PDSS2, кодирующем субъединицу 2 фермента декапренилдифосфатсинтазы, идентифицированы у некоторых пациентов с синдромом Leigh и нефротической протеинурией [64]. Обнаружены мутации в гене COQ6, который кодирует CoQ10-биосинтез моноксигеназы-6 в семьях с ранней стадией нефротического синдрома и сенсорноневральной глухотой [65].
Лечение идиопатического ФСГС
1. Консервативное лечение
Независимо от клинической формы ФСГС рекомендуется консервативное лечение. При ФСГС артериальное давление должно быть < 130/80 мм рт.ст. с конечным показателем 125/75 мм рт.ст. для пациентов с протеинурией > 1 г/сутки. Неотьемлемой частью терапии является модификация образа жизни (ограничение соли, нормализация веса, регулярные физические упражнения, отказ от курения, потребление адекватного количества белка (0,8–1,0 г/кг/день) и ограничение жиров).
2. Инициальная терапия ФСГС
Пероральные кортикостероиды являются основным методом лечения ФСГС [66] (рис. 9).
Для инициального лечения ФСГС Kidney Disease Improving Global Outcomes (KDIGO) 2012 г. [67] рекомендует кортикостероидную и иммуносупрессивную терапию рассматривать только при идиопатическом ФСГС. KDIGO предлагает назначать преднизолон ежедневно в один прием в дозе 1 мг/кг (максимум 80 мг) или в режиме в один прием через день в дозе 2 мг/кг (максимально — 120 мг). KDIGO также предлагает назначать высокие дозы кортикостероидов в течение как минимум 4 недель и продолжать при удовлетворительной переносимости максимально до 16 недель или до достижения полной ремиссии, если она наступит до 16 недель. Предлагается снижать дозу кортикостероидов в течение 6 месяцев после достижения полной ремиссии. Ингибиторы кальциневрина считаются терапией первой линии для пациентов с относительными противопоказаниями или непереносимостью высоких доз кортикостероидов (неконтролируемый диабет, психические заболевания, остеопороз).
Лечение рецидивов у пациентов с ФСГС
Рецидив после ремиссии ФСГС является обычным явлением. Так, в большой когорте взрослых с ФСГС, 52 % из которых имели частичную ремиссию и 36 % — полную ремиссию, был отмечен рецидив в последующий период наблюдения [68]. В этом случае рекомендуется повторный курс стероидов, если инициальная терапия хорошо переносится. Возможно использование циклоспорина, так как его действие связано с более длительной ремиссией. Циклоспорин может уменьшить рецидив на 80 % [69]. Однако эти пациенты, как правило, становятся циклоспоринзависимыми. Скорость ремиссии выше при дозе циклоспорина от 4 до 6 мг/кг/день [70]. Однако остаются вопросы относительно продолжительности использования циклоспорина, потому что у пациентов может развиться почечная недостаточность из-за токсичности циклоспорина. Циклофосфамид может снизить риск рецидива. Комбинация циклофосфамида с кортикостероидами увеличивает продолжительность ремиссии в отличие от использования только циклофосфамида.
Лечение стероидзависимых пациентов с ФСГС
Пациенты с ФСГС считаются стероидзависимыми, если они имели два рецидива на протяжении 2 недель после завершения стероидной терапии. Для этих пациентов рекомендованы ингибиторы кальциневрина, такие как циклоспорин или такролимус. Антипротеинурическое действие ингибиторов кальциневрина состоит в стабилизации актинового скелета подоцитов через их иммуномодулирующий эффект на Т-клетки. Эта стратегия требует очень тщательного мониторинга их уровней [71, 72]. В двух небольших проспективных исследованиях было описано использование такролимуса с преднизолоном [73, 74]. В качестве второй линии могут быть предложены два альтернативных метода лечебной терапии, хотя имеется недостаточно данных об их эффективности. Они представляют собой алкилирующие агенты и моноклональные антитела против CD20. Алкилирующие агенты (пероральный циклофосфамид) связаны с высокой скоростью и более продолжительным временем ремиссии по сравнению с ингибиторами кальциневрина. Рекомендуемые дозы в различных клинических исследованиях для пациентов с ФСГС составляют от 2 до 2,5 мг/кг/день [75]. Ритуксимаб связан с более низкой скоростью рецидивов и необходим для уменьшения дозы других иммуносупрессоров у взрослых [76]. Роль ритуксимаба в физиопатологии ФСГС еще обсуждается.
Лечение стероидрезистентных пациентов с ФСГС
Стероидрезистентный ФСГС встречается в 40–60 % случаев. Он характеризуется стойкой протеинурией, несмотря на лечение преднизолоном 1 мг/кг/день (или 2 мг/кг/через день) в течение более четырех месяцев. В некоторых рандомизированных клинических исследованиях изучались различные иммуносупрессивные стратегии. Были предложены ингибиторы кальциневрина (такролимус и циклоспорин), которые показали одинаковую эффективность. Так, циклоспорин может вызвать ремиссию у приблизительно 60 % пациентов, которые устойчивы к стероидам [77]. Такролимус в дозе 0,1–0,2 мг/кг/день, разделенный на две дозы, был эффективен и хорошо переносился пациентами, что привело к полной ремиссии в 81 % случаев. Однако в этом исследовании пациенты получали и другие иммунодепрессанты. Рекомендованный целевой уровень для этих пациентов составлял от 5 до 7 нг/мл. Скорость ремиссии в исследованиях, в которых лечение проводилось такролимусом у пациентов, зависимых от кортикоидов или резистентных к ним, составляла 48–100 % [78]. Не была доказана разница в нефротоксичности между циклоспорином и такролимусом, которые имели такие побочные явления, как тремор, артериальная гипертензия и сахарный диабет.
Альтернативным лечением для пациентов с ФСГС после инициального лечения преднизолоном в течение 4 недель является метилпреднизолон в дозе 30 мг/кг/день с максимальной дозой 1 г каждый день в течение 2 недель. Протокол Mendoza относится к агрессивной стратегии лечения, основанной на высокодозовой терапии метилпреднизолоном и пероральным преднизолоном в течение 82 недель (табл. 2).
При использовании этого протокола для лечения ФСГС приблизительно 65 % пациентов имели полную ремиссию и только у 25 % было отмечено прогрессирование хронического заболевания почек. Однако длительное лечение стероидами вызывает значительные побочные явления, включающие ухудшение роста, ожирение, гипертонию, катаракту, остеопороз, подавление иммунитета, сахарный диабет, гирсутизм.
Циклофосфамид также является потенциальным вариантом для стероидрезистентных пациентов. Он может быть назначен в дозе 500 мг/м2. Циклофосфамид не должен назначаться детям.
Дополнительные методы лечения идиопатического ФСГС
Дополнительные методы лечения ФСГС могут помочь в лечении стероидзависимой, стероидрезистентной или рецидивирующей ФСГС. Эти методы пока не подтверждены клиническими исследованиями.
Ритуксимаб
Ритуксимаб представляет собой моноклональные антитела, действующие селективно на поверхностный ангтиген В-лимфоцитов CD20. Кроме того, ритуксимаб имеет прямое защитное действие на подо–циты [80]. Ритуксимаб вводят в виде 2 или 4 инъекций в дозе 375 мг/м2 в неделю или раз в две недели.
Мизорибин
Мизорибин ингибирует инозинмонофосфатсинтетазу и гуанозинмонофосфатсинтетазу, что приводит к ингибированию синтеза ДНК и делению клеток. Мизорибин вводится в дозе 3 мг/кг один раз ежедневно до завтрака.
Адалимумаб
Адалимумаб является моноклональным антителом человека, направленным против фактора некроза опухоли альфа. Адалимумаб уменьшает протеинурию более чем на 50 %. Не имеет серьезных побочных эффектов и хорошо переносится [81].
Фрезолимумаб
Фрезолимумаб — рекомбинантные полностью человеческие моноклональные антитела, которые ингибируют активность всех изоформ трансформирующего фактора роста β [82].
Синтетический аналог адренокортикотропина
Несколько лет назад инъекции синтетического аналога адренокортикотропина (АКТГ) использовались в качестве терапевтического лечения у детей с нефротическим синдромом. Недавно описано использование инъекции АКТГ у 24 взрослых с ФСГС. Вводимой дозой были 80 единиц подкожно два раза в неделю [83].
Галактоза
Галактоза представляет собой моносахарид. Имеется всего лишь несколько сообщений о частичной ремиссии после пероральной терапии галактозой в дозе 0,2 г/кг дважды в день. Используется как нетоксический и вспомогательный агент.
Лечение вторичных ФСГС
Первым шагом для лечения вторичного ФСГС является устранение причины заболевания. Например, при вторичном ФСГС у пациентов с ожирением или тех, которые использовали героин, необходимо добиться снижения веса и отказаться от героина [84]. Аналогично данному примеру является использование высокоактивной ретровирусной терапии, которая оказалась эффективной для ВИЧ-ассоциированной нефропатии [85].
Выводы
Молекулярные исследования последних лет позволили лучше понять структуру и функцию гломерулярного фильтрационного барьера почек. Генетические исследования пациентов с ФСГС являются очень важными для определения стратегии лечения и дальнейшего прогноза. Например, основная часть пациентов с мутациями NPHS2 устойчивы к стероидной терапии, поэтому лечение стероидами может быть прекращено после получения анализа ДНК. Кроме того, после почечной трансплантации у данных пациентов нет рецидива нефротического синдрома. При обнаружении мутации WT1 необходимы дальнейшие медицинские регулярные обследования с учетом более высокого риска развития злокачественных новообразований. Мутации митохондриальной ДНК могут вызвать многочисленные расстройства, которые требуют неврологического контроля и мониторинг гликемии. Аутосомно-рецессивные мутации NPHS1, NPHS2 связаны с более тяжелым заболеванием, характеризующимся ранней протеинурией и терминальной почечной недостаточностью, в то время как аутосомно-доминантные мутации INF2, TRPC6 и ACTN4 ассоциированы с проявлением более мягкого характера заболеваний. Понимание функции подоцитов при генетических нарушениях поможет объяснить действие лекарственных средств, используемых для лечения гломерулярных расстройств. Большинство препаратов, которые применяются при лечении ФСГС, оказывают прямое влияние на подоциты (кортикостероиды, циклоспорин, мизорибин и др.). Эти новые важные знания помогут клиницистам в решении вопроса: какой метод является наиболее подходящим для лечения пациентов с ФСГС?
Конфликт интересов. Автор заявляет об отсутствии какого-либо конфликта интересов при подготовке данной статьи.
Список литературы
1. Braden G.L., Mulhern J.G., O’Shea M.H., Nash S.V., Ucci Jr A.A., Germain M.J. Changing incidence of glomerular dise–ases in adults // Am. J. Kidney Dis. — 2000. — 35(5). — 878-83.
2. Fahr T. Pathologische Anatomie des Morbus Brightii // Handb der Spez Pathol Anat und Histol. — 1925. — 6. — 156-472. — doi: 10.1007/978-3-7091-3054-4.
3. Rich A.R. A hitherto undescribed vulnerability of the juxta-medullary glomeruli in lipoid nephrosis // Bull. Johns Hopkins Hosp. — 1957. — 100. — 173-186.
4. D’Agati V., Fogo A., Bruijn J. et al. Pathologic classification of focal segmental glomerulosclerosis: a working proposal // Am. J. Kidney Dis. — 2004. — 43. — 368-382.
5. Chapter 6: Idiopathic focal segmental glomerulosclerosis in adults // Kidney Int. Suppl. — 2012. — 2(2). — 181-185.
6. Basgen J.M., Steffes M.W., Stillman А.E., Mauer S.M. Estimating glomerular number in situ using magnetic resonance imaging and biopsy // Kidney Int. — 1994. — 45. — 1668-72.
7. Greka A., Mundel P. Cell biology and pathology of podocytes // Ann. Rev. Physiol. — 2012. — 74. — 299-323. — doi: 10.1146/annurev-physiol-020911-153238.
8. Barisoni L., Schnaper H.W., Kopp J.B. Advance in the bio–logy and genetics of the podocytopathies: implications for diagnosis and therapy // Arch. Pathol. Lab. Med. — 2009. — 133. — 201-16. — doi: 10.1043/1543-2165-133.2.201.
9. Wharram B.L., Goyal M., Wiggins J.E., Sanden S.K., Hussain S., Filipiak W.E., Saunders T.L., Dysko R.C., Kohno K., Holz–man L.B., Wiggins R.C. Podocyte depletion causes glomerulosclerosis: diphtheria toxin-induced podocyte depletion in rats expressing human diphtheria toxin receptor transgene // J. Am. Soc. Nephrol. — 2005. — 16. — 2941-52. — doi: 10.1681/ASN.2005010055.
10. Hildebrandt F. Genetic kidney diseases // Lancet. — 2010. — 375. — 1287-1295. — doi: 10.1016/S0140-6736(10)60236-X.
11. Sánchez de la Nieta M.D., Arias L.F. et al. Glomeruloesclerosis focal y segmentaria familia // Nefrologia. — 2003. — 23(2). — 172-6.
12. Schell C., Huber T.B. New players in the pathogenesis of focal segmental glomerulosclerosis // Nephrol. Dial. Transplant. — 2012. — 27(9). — 3406-12. — doi: 10.1093/ndt/gfs273.
13. Kestila M., Lenkkeri U., Mannikko M., Lamerdin J., McCready P., Putaala H., Ruotsalainen V., Morita T., Nissinen M., Herva R. et al. Positionally cloned gene for a novel glomerular protein-nephrin-is mutated in congenital nephrotic syndrome // Mol. Cell. — 1998. — 1(4). — 575-82.
14. Hvenainen E.K., Hallman N., Hjelt L. Nephrotic syndrome in newborn and young infants // Ann. Paediatr. Fenn. — 1956. — 2. — 227-241.
15. Khoshnoodi J., Sigmundsson K., Ofverstedt L.G. et al. Nephrin promotes cell-cell adhesion through homophilic interactions // Am. J. Pathol. — 2003. — 163. — 2337-2346. — doi: 10.1016/S002-9440(10)63590-0.
16. Patari-Sampo A., Ihalmo P., Holthofer H. Molecular basis of the glomerular filtration: nephrin and the emerging protein complex at the podocyte slit diaphragm // Ann. Med. — 2006. — 38. — 483-492. — doi: 10.1080/07853890600978149.
17. Barisoni L., Mundel Р. Podocyte biology and the emer–ging understanding of podocyte diseases // American Journal of Nephrology. — 2003. — Vol. 23. — № 5. — 353-360. — doi: 10.1159/000072917.
18. Lenkkeri U., Mannikko M., McCready P. et al. Structure of the gene for congenital nephrotic syndrome of the Finnish type (NPHS1) and characterization of mutations // Am. J. Hum. Genet. — 1999. — 64. — 51-61.
19. Beltcheva O., Martin P., Lenkkeri U. et al. Mutation spectrum in the nephrin gene (NPHS1) in congenital nephrotic syndrome // Hum. Mutat. — 2001. — 17. — 368-373. — doi: 10.1002/humu.1111.
20. Lahdenkari A.T., Kestila M., Holmberg C. et al. Nephrin gene (NPHS1) in patients with minimal change nephrotic syndrome (MCNS) // Kidney Int. — 2004. — 65. — 1856-1863. — doi: 10.1111/j.1523-1755.2004.00583.x.
21. Heeringa S.F., Vlangos C.N., Chernin G. et al. Thirteen novel NPHS1 mutations in a large cohort of children with congenital nephrotic syndrome // Nephrol. Dial. Transplant. — 2008. — 23. — 3527-3533. — doi: 10.1093/ndt/gfn271.
22. Hinkes B.G., Mucha B., Vlangos C.N. et al. Nephrotic syndrome in the first year of life: two thirds of cases are caused by mutations in 4 genes (NPHS1, NPHS2, WT1, and LAMB2) // Pediatrics. — 2007. — 119. — 907-919. — doi: 10.1542/peds.2006-2164.
23. Philippe A., Nevo F., Esquivel E.L. et al. Nephrin mutations can cause childhood-onset steroid-resistant nephrotic syndrome // J. Am. Soc. Nephrol. — 2008. — 19. — 1871-1878. — doi: 10.1681/ASN.2008010059.
24. Laakkonen H., Lönnqvist T., Uusimaa J. et al. Muscular dystonia and athetosis in six patients with congenital nephrotic syndrome of the Finnish type (NPHS1) // Pediatr. Nephrol. — 2006. — 21. — 182-189. — doi: 10.1007/s00467-005-2116-1.
25. Boute N., Gribouval О., Roselli S. et al. NPHS2, enco–ding the glomerular protein podocin, is mutated in autosomal recessive steroid-resistant nephrotic syndrome // Nature Genetics. — 2006. — Vol. 24. — № 4. — 349-354. — doi: 10.1038/74166.
26. Caridi G., Bertelli R., Di Duca M. et al. Broadening the spectrum of diseases related to podocin mutations // Journal of the American Society of Nephrology. — 2003. — Vol. 14. — № 5. — 1278-1286. — doi: 10.1097/01.ASN.0000060578.79050.E0.
27. Ruf R.G., Lichtenberger A., Karle S.M. et al. Patients with mutations in NPHS2 (Podocin) do not respond to standard steroid treatment of nephrotic syndrome // Journal of the American Society of Nephrology. — 2004. — Vol. 15. — № 3. — 722-732. — doi: 10.1097/01.ASN.0000113552.59155.72.
28. Weber S., Gribouval O., Esquivel E.L. et al. NPHS2 mutation analysis shows genetic heterogeneity of steroid-resistant nephrotic syndrome and low post-transplant recurrence // Kidney International. — 2004. — Vol. 66, № 2. — 571-579.
29. Roselli S., Heidet L., Sich M. et al. Early glomerular filtration defect and severe renal disease in podocin-deficient mice // Mol. Cell. Biol. — 2004. — 24. — 550-560.
30. Pereira A.C., Pereira A.B., Mota G.F. et al. NPHS2 R229Q functional variant is associated with micro-albuminuria in the general population // Kidney Int. — 2004. — 65. — 1026-1030. — doi: 10.1111/j.1523-1755.2004.00479.x.
31. Huber T.B., Simons M., Hartleben B. et al. Molecular basis of the functional podocin-nephrin complex: mutations in the NPHS2 gene disrupt nephrin targeting to lipid raft microdomains // Hum. Mol. Genet. — 2003. — 12. — 3397-3405. — doi: 10.1093/hmg/ddg360.
32. Bertelli R., Ginevri F., Caridi G. et al. Recurrence of focal segmental glomerulosclerosis after renal transplantation in patients with mutations of podocin // Am. J. Kidney Dis. — 2003. — 41. — 1314-1321.
33. Caridi G., Perfumo F., Ghiggeri G.M. NPHS2 (Podocin) mutations in nephrotic syndrome. Clinical spectrum and fine mechanisms // Pediatr. Res. — 2005. — 57. — 54-61. — doi: 10.1203/01.PDR.0000160446.01907.B1.
34. Shih N.Y., Li J., Cotran R. et al. CD2AP localizes to the slit diaphragm and binds to nephrin via a novel C-terminal domain // Am. J. Pathol. — 2001. — 159. — 2303-2308. — doi: 10.1016/S0002-9440(10)63080-5.
35. Schwarz K., Simons M., Resier J. et al. Podocin, a raft-associated component of the glomerular slit diaphragm, interacts with CD2AP and nephrin // J. Clin. Invest. — 2001. — 108. — 1621-1629. — doi: 10.1172/JC112849.
36. Shih N.Y., Li J., Karpitskii V. et al. Congenital nephrotic syndrome in mice lacking CD2-associated protein // Science. — 1999. — 286. — 312-315.
37. Huber T.B., Hartleben B., Kim J. et al. Nephrin and CD2AP associate with phosphoinositide 3-OH kinase and stimu–late AKT-dependent signaling // Mol. Cell. Biol. — 2003. — 23. — 4917-4928. — doi: 10.1128/MCB.23.14.4917-4928.2003.
38. Lowik M.M., Groenen P.J., Pronk I. et al. Focal segmental glomerulosclerosis in a patient homozygous for a CD2AP mutation // Kidney Int. — 2007. — 72. — 1198-1203. — doi: 10.1038/sj.ki.5002469.
39. Harteneck C., Plant T.D., Schultz G. From worm to man: Three subfamilies of TRP channels // Trends Neurosci. — 2000. — 23. — 159-166.
40. Montell C., Birnbaumer L., Flockerzi V. et al. A unified nomenclature for the superfamily of TRP cation channels // Mol. Cell. — 2002. — 9. — 229-231.
41. Hofmann T., Obukhov A.G., Schaefer M., Harteneck C., Gudermann T., Schultz G. Direct activation of human TRPC6 and TRPC3 channels by diacylglycerol // Nature. — 1999. — 397. — 259-263. — doi: 10.1038/16711.
42. Reiser J., Polu K.R., Möller C.C. еt al. TRPC6 is a glomerular slit diaphragm-associated channel required for normal renal function // Nat. Genet. — 2005. — 37. — 739-744. — doi: 10.1038/ng1592.
43. Winn M.P., Conlon P.J., Lynn K.L. еt al. A mutation in the TRPC6 cation channel causes familial focal segmental glomerulosclerosis // Science. — 2005. — 308. — 1801-1804. — doi: 10.1126/science.1106215.
44. Santín S., Ars E., Rossetti S., Salido E. et al. TRPC6 mutational analysis in a large cohort of patients with focal segmental glomerulosclerosis // Nephrol. Dial. Transplant. — 2009. — 24. — 3089-3096. — doi: 10.1093/ndt/gfp229.
45. Zhu B., Chen N., Wang Z.H., Pan X.X., Ren H., Zhang W., Wang W.M. Identification and functional analysis of a novel TRPC6 mutation associated with late onset familial focal segmental glomerulosclerosis in Chinese patients // Mutat. Res. — 2009. — 664. — 84-90. — doi: 10.1016/j.mrfmmm.2008.11.021.
46. Gigante M., Caridi G., Montemurno E., Soccio M., d’Apolito M., Cerullo G., Aucella F., Schirinzi A., Emma F., Massella L., Messina G., De Palo T., Ranieri E., Ghiggeri G.M., Gesualdo L. TRPC6 mutations in children with steroid-resistant nephrotic syndrome and atypical phenotype // Clin. J. Am. Soc. Nephrol. — 2011. — 6. — 1626-1634. — doi: 10.2215/CJN.07830910.
47. Michaud J.L., Lemieux L.I., Dube M. et al. Focal and segmental glomerulosclerosis in mice with podocyte-specific expression of mutant alpha-actinin-4 // J. Am. Soc. Nephrol. — 2003. — 14. —1200-1211.
48. Weins A., Kenlan P., Herbert S. et al. Mutational and biological analysis of alpha-actinin-4 in focal segmental glomerulosclerosis // J. Am. Soc. Nephrol. — 2005. — 16. — 3694-3701. — doi: 10.1681/ASN.2005070706.
49. Kaplan J.M., Kim S.H., North K.N. et al. Mutations in ACTN4, encoding alpha-actinin-4, cause familial focal segmental glomerulosclerosis // Nat. Genet. — 2000. — 24. — 251-256. — doi: 10.1038/73456.
50. Weins A., Schlondorff J., Nakamura F. et al. Diseaseassociated mutant alpha-actinin-4 reveals a mechanism for regula–ting its F-actin-binding affinity // Proc. Natl Acad. Sci. USA. — 2007. — 104. — 16080-16085. — doi: 10.1073/pnas.0702451104.
51. Zhu L., Jiang R., Aoudjit L., Jones N., Takano T. Activation of RhoA in podocytes induces focal segmental glomerulosclerosis // J. Am. Soc. Nephrol. — 2011. — 22. — 1621-1630. — doi: 10.1681/ASN/2010111146.
52. Sun H., Schlondorff J., Higgs H.N., Pollak M.R. Inverted formin 2 regulates actin dynamics by antagonizing Rho/diaphanous-related formin signaling // J. Am. Soc. Nephrol. — 2013. — 24. — 917-929. — doi: 10.1681/ASN.2012080834.
53. Brown E.J., Schlondorff J.S., Becker D.J., Tsukaguchi H., Tonna S.J., Uscinski A.L., Higgs H.N., Henderson J.M., Pollak M.R. Mutations in the formin gene INF2 cause focal segmental glomerulosclerosis // Nat. Genet. — 2010. — 42. — 72-76. — doi: 10.1038/ng.505.
54. Gee H.Y., Saisawat P., Ashraf S. et al. ARHGDIA mutations cause nephrotic syndrome via defective RHO GTPase signaling // J. Clin. Invest. — 2013. — 123. — 3243-3253. — doi: 10.1172/JCI69134.
55. Gessler M., Poustka A., Cavenee W. et al. Homozygous deletion in Wilms tumours of a zinc-finger gene identified by chromosome jumping // Nature. — 1990. — 343. — 774-778. — doi: 10.1038/343774a0.
56. McTaggart S.J., Algar E., Chow C.W. et al. Clinical spectrum of Denys-Drash and Frasier syndrome // Pediatr. Nephrol. — 2001. — 16. — 335-339.
57. Zenker M., Aigner T., Wendler O. et al. Human lami–nin beta2 deficiency causes congenital nephrosis with mesangial sclerosis and distinct eye abnormalities // Hum. Mol. Genet. — 2004. — 13. — 2625-2632. — doi: 10.1093/hmg/ddh284.
58. Pozzi A., Jarad G., Moeckel G.W. еt al. Beta1 integrin expression by podocytes is required to maintain glomerular structural integrity // Dev. Biol. — 2008. — 316. — 288-301. — doi: 10.1016/j.vdbio.2008.01.022.
59. Hasselbacher K., Wiggins R.C., Matejas V. еt al. Recessive missense mutations in LAMB2 expand the clinical spectrum of LAMB2-associated disorders // Kidney Int. — 2006. — 70. — 1008-1012. — doi: 10.1038/sj.ki.5001679.
60. Berkovic S.F., Dibbens L.M., Oshlack A. et al. Array-based gene discovery with three unrelated subjects shows SCARB2/LIMP-2 deficiency causes myoclonus epilepsy and glomerulosclerosis // Am. J. Hum. Genet. — 2008. — 82. — 673-684. — doi: 10.1016/j/ajhg.2007.12.019.
61. Settembre C., Fraldi A., Rubinsztein D.C., Ballabio A. Lysosomal storage diseases as disorders of autophagy // Autophagy. — 2008. — 4. — 113-114. — doi: 10.4161/auto.5227.
62. Lowik M.M., Hol F.A., Steenbergen E.J., Wetzels J.F., van den Heuvel L.P. Mitochondrial tRNALeu(UUR) mutation in a patient with steroid-resistant nephrotic syndrome and focal segmental glomerulosclerosis // Nephrol. Dial. Transplant. — 2005. — 20. — 336-341. — doi: 10.1093/ndt/gfh546.
63. Diomedi-Camassei F., Di Giandomenico S. et al. COQ2 nephropathy: a newly described inherited mitochondriopathy with primary renal involvement // J. Am. Soc. Nephrol. — 2007. — 18. — 2773-2780. — doi: 10.1681/ASN.2006080833.
64. Lopez L.C., Schuelke M., Quinzii C.M. еt al. Leigh syndrome with nephropathy and CoQ10 deficiency due to decaprenyl diphosphate synthase subunit 2 (PDSS2) mutations // Am. J. Hum. Genet. — 2006. — 79. — 1125-1129. — doi: 10.1086/510023.
65. Heeringa S.F., Chernin G., Chaki M. et al. COQ6 mutations in human patients produce nephrotic syndrome with sensorineural deafness // J. Clin. Invest. — 2011. — 121. — 2013-2024. — doi: 10.1172/JCI45693.
66. Beaudreuil S., Lorenzo H., Michele Elias M., Erika Nnang Obada E., Charpentier B., Durrbach A. Optimal management of primary focal segmental glomerulosclerosis in adults // International Journal of Nephrology and Renovascular Disease. — 2017. — 10. — 97-107. — doi: 10.2147/IJNRD.S126844.
67. Idiopathic focal segmental glomerulosclerosis in adults // Kidney Int. Suppl. — 2012. — 2.
68. Troyanov S., Wall C.A., Miller J.A., Scholey J.W., Cattran D.C. Focal and segmental glomerulosclerosis: definition and relevance of a partial remission // J. Am. Soc. Nephrol. — 2005. — 16(4). — 1061-1068. — doi: 10.1681/ASN.2004070593.
69. Niaudet P., Habib R. Cyclosporine in the treatment of idiopathic nephrosis // J. Am. Soc. Nephrol. — 1994. — 5(4). — 1049-1056.
70. Radhakrishnan J., Cattran D.C. The KDIGO practice guideline on glomerulonephritis: reading between the (guide)lines-application to the individual patient // Kidney Int. — 2012. — 82(8). — 840-856.
71. Faul C., Donnelly M., Merscher-Gomez S. et al. The actin cytoskeleton of kidney podocytes is a direct target of the antiproteinuric effect of cyclosporine A // Nat. Med. — 2008. — 14(9). — 931-938. — doi: 10.1038/nm/1857.
72. Okada T., Matsumoto H., Nagaoka Y. et al. Clinical evaluation of chronic nephrotoxicity of long-term cyclosporine A treatment in adult patients with steroid-dependent nephrotic syndrome // Nephrology (Carlton). — 2011. — 16(3). — 319-325.
73. Westhoff T.H., Schmidt S., Zidek W., Beige J., van der Giet M. Tacrolimus in steroid-resistant and steroid-dependent nephrotic syndrome // Clin. Nephrol. — 2006. — 65(6). — 393-400.
74. Ren H., Shen P., Li X., Pan X., Zhang W., Chen N. Tacrolimus versus cyclophosphamide in steroid-dependent or steroid-resistant focal segmental glomerulosclerosis: a randomized controlled trial // Am. J. Nephrol. — 2013. — 37(1). — 84-90. — doi: 10.1159/000346256.
75. Ponticelli C., Edefonti A., Ghio L. et al. Cyclosporin versus cyclophosphamide for patients with steroid-dependent and frequently relapsing idiopathic nephrotic syndrome: a multicentre randomized controlled trial // Nephrol. Dial. Transplant. — 1993. — 8(12). — 1326-1332.
76. Munyentwali H., Bouachi K., Audard V. et al. Rituximab is an efficient and safe treatment in adults with steroid-dependent minimal change disease // Kidney Int. — 2013. — 83(3). — 511-516. doi: 10.1038/ki.2012.444.
77. Cattran D.C., Appel G.B., Hebert L.A. et al. A randomized trial of cyclosporine in patients with steroid-resistant focal segmental glomerulosclerosis. North America Nephrotic Syndrome Study Group // Kidney Int. — 1999. — 56(6). — 2220-2226. — doi: 10.1046/j.1523-1755.1999.00778.x.
78. Duncan N., Dhaygude A., Owen J. et al. Treatment of focal and segmental glomerulosclerosis in adults with tacrolimus monotherapy // Nephrol. Dial. Transplant. — 2004. — 19(12). — 3062-3067. — doi: 10.1093/ndt/gfh536.
79. Gulati S., Pokhariyal S., Sharma R.K. et al. Pulse cyclophosphamide therapy in frequently relapsing nephrotic syndrome // Nephrol. Dial. Transplant. — 2001. — 16(10). — 2013-2017.
80. Fornoni A., Sageshima J., Wei C. et al. Rituximab targets podocytes in recurrent focal segmental glomerulosclerosis // Sci. Transl. Med. — 2011. — 3(85). — 85ra46. — doi: 10.1126/scitranslmed.3002231.
81. Joy M.S., Gipson D.S., Powell L. et al. Phase 1 trial of adalimumab in Focal Segmental Glomerulosclerosis (FSGS): II. Report of the FONT (Novel Therapies for Resistant FSGS) study group // Am. J. Kidney Dis. — 2010. — 55(1). — 50-60. — doi: 10.1053/j.ajkd.2009.08.019.
82. Trachtman H., Fervenza F.C., Gipson D.S. et al. A phase 1, single-dose study of fresolimumab, an anti-TGF-beta antibody, in treatment-resistant primary focal segmental glomerulosclerosis // Kidney Int. — 2011. — 79(11). — 1236-1243. — doi: 10.1038/ki.2011.33.
83. Mittal T., Dedhia P., Roy-Chaudhury P. et al. Complete remission of posttransplantation recurrence of focal segmental glomerulosclerosis with the use of adrenocorticotrophic hormone gel: case report // Transplant. Proc. — 2015. — 47(7). — 2219-2222. — doi: 10.1016/j.transproceed.2015.07.013.
84. Fowler S.M., Kon V., Ma L., Richards W.O., Fogo A.B., Hunley T.E. Obesity-related focal and segmental glomerulosclerosis: normalization of proteinuria in an adolescent after bariatric surgery // Pediatr. Nephrol. — 2009. — 24(4). — 851-5. — doi: 10.1007/s00467-008-1024-6.
85. Lescure F.X., Flateau C., Pacanowski J., Brocheriou I., Rondeau E., Girard P.M., Ronco P., Pialoux G., Plaisier E. HIV-associated kidney glomerular diseases:changes with time and HAART // Nephrol. Dial. Transplant. — 2012. — 27(6). — 2349-55. — doi: 10.1093/ndt/gfr676.

/55-1.jpg)
/55-2.jpg)
/56-1.jpg)
/56-2.jpg)
/57-1.jpg)
/53-1.jpg)
/54-1.jpg)
/57-2.jpg)
/58-1.jpg)
/60-1.jpg)
/61-1.jpg)