В современных условиях глобальной урбанизации отмечается неуклонный рост аутоиммунной патологии, в основе патогенеза которой лежит иммуносупрессия.
Аутоиммунный тиреоидит (АИТ) — это органоспецифическое, Т-клеточно–опосредованное аутоиммунное заболевание [2–4], характеризующееся образованием аутоантител к ткани щитовидной железы (ЩЖ) с последующим снижением ее функции. «Большими» диагностическими признаками, сочетание которых позволяет установить диагноз АИТ, являются:
► первичный гипотиреоз (манифестный или стойкий субклинический);
► наличие антител к ткани ЩЖ и ультразвуковые признаки аутоиммунной патологии.
При отсутствии хотя бы одного из «больших» диагностических признаков диагноз АИТ носит лишь вероятностный характер.
При манифестном гипотиреозе (повышение уровня тиреотропного гормона (ТТГ) и снижение уровня тироксина (Т4)) показана заместительная терапия левотироксином в средней дозе 1,6–1,8 мкг/кг массы тела пациента. Критерием адекватности указанной терапии является стойкое поддержание нормального уровня ТТГ в крови.
При субклиническом гипотиреозе (повышение уровня ТТГ в сочетании с нормальным уровнем Т4 в крови) рекомендуется:
► повторное гормональное исследование через 3–6 месяцев с целью подтверждения стойкого характера нарушения функции ЩЖ; если субклинический гипотиреоз выявлен во время беременности, терапия левотироксином в полной заместительной дозе назначается немедленно;
► заместительная терапия левотироксином показана при стойком субклиническом гипотиреозе (повышение уровня ТТГ в крови более 10 мЕд/л, а также в случае как минимум двукратного выявления уровня ТТГ между 5–10 мЕд/л); у лиц старше 55 лет и при наличии сердечно-сосудистых заболеваний заместительная терапия левотироксином проводится при хорошей переносимости препарата и отсутствии данных о декомпенсации этих заболеваний на фоне приема препарата;
► критерием адекватности заместительной терапии субклинического гипотиреоза является стойкое поддержание нормального уровня ТТГ в крови.
Актуальность поиска дополнительных способов коррекции гипотиреоза на фоне аутоиммунного процесса в ткани ЩЖ очевидна. В настоящее время отсутствуют эффективные методы воздействия на собственно аутоиммунный процесс в ЩЖ (препараты гормонов ЩЖ, иммуномодуляторы, которые наиболее часто используются в терапии АИТ, обладают минимальным воздействием на аутоиммунный процесс).
С давних пор народной медициной использовалась способность некоторых растений положительно влиять на функционирование ЩЖ. В настоящее время все шире применяют нетрадиционные вспомогательные средства, старейшими из которых являются растительные. Механизм регулирующего воздействия на функцию ЩЖ различных растений многообразен и до конца не изучен (некоторые растения, например корень лапчатки белой (Potentilla alba L.), содержат тиреотропные вещества, кроме этого, в состав растения входит большое количество микроэлементов). Так, в составе лапчатки белой было выделено и описано химическое соединение — альбинин, проявляющее тиреотропную и гонадотропную активность. В НИИ неорганической химии СО РАН (г. Новосибирск) был проведен ряд исследований по изучению свойств сырья из лапчатки белой. Установлено, что корень этого растения содержит в своем составе почти всю таблицу Менделеева, а также анионы йодистой кислоты, йод [5–8]. Одним из значимых биологических компонентов лапчатки белой, оказывающих положительное влияние на функционирование ЩЖ, является биофлавоноид кверцетин, обладающий выраженной антиоксидантной и мембраностимулирующей активностью [5, 6, 8–11]. Протекторное действие кверцетина в отношении ЩЖ реализуется благодаря эффекту стабилизации мембран тиреоцитов [11], регулируется проницаемость клеток ЩЖ, обеспечивается их защита от повреждающего воздействия аутоантител и свободных радикалов, восстанавливается рецепторная и гормоновыделительная функции.
На сегодняшний день на рынке Украи–ны представлена диетическая добавка Тиреофарм® (ООО ПТФ «Фармаком», Украина), которая, кроме лапчатки белой, содержит ламинарию. Ламинария имеет в своем составе огромный набор макро- и микроэлементов, по содержанию значительно превосходящий наземные растения. В составе 1 капсулы (400 мг) содержатся активные компоненты: экстракт лапчатки белой — 8 мг, экстракт ламинарии — 1,2 мг, лист грецкого ореха — 28 мг, экстракт валерианы — 4 мг, экстракт пустырника — 4 мг, экстракт куркумы — 4 мг, никотиновая кислота — 4 мг.
Известно, что йод и аминокислота тирозин являются главными структурными компонентами синтеза тиреоидных гормонов. В диетической добавке Тиреофарм® органически связанная форма йода наиболее благоприятно воздействует на организм человека. Органический йод из кишечника попадает в печень, где в дальнейшем под действием дейодиназ метаболизируется в неорганический йод. Важно отметить, что активность дейодиназ прямо пропорционально зависит от степени дефицита йода. Известно, что в ткань ЩЖ йод поступает только в неорганической форме. Именно зависимость активности дейодиназ от уровня йода обу–словливает безопасность относительно передозировки органического йода в составе диетической добавки Тиреофарм®.
Следовательно, у пациентов с АИТ и гипотиреозом применение органических форм йода безопасно и эффективно для достижения компенсации гипофункции ЩЖ.
Никотиновая кислота в составе диетической добавки Тиреофарм® обеспечивает активацию ферментов, участвующих в синтезе тиреоидных гормонов, что важно в условиях гипотиреоза. Пустырник и валериана проявляют седативный эффект. К настоящему времени установлено, что стресс является ключевым фактором в развитии иммуносупрессии. Лист грецкого ореха оказывает общеукрепляющее, противовоспалительное и антиоксидантное действие. Куркума уменьшает воспалительный процесс, обладает детоксикационным эффектом и является мощным антиоксидантом.
Следует подчеркнуть, что фитопрепараты, в отличие от синтетических средств, нетоксичны, оказывают мягкое иммуномодулирующее и противовоспалительное действие, могут длительно применяться без существенных побочных эффектов, прежде всего аллергических реакций, хорошо сочетаются с лекарственными веществами, усиливая их терапевтический эффект.
Комплексный состав диетической добавки Тиреофарм® обеспечивает разнонаправленную реализацию патогенетического лечения АИТ и достижение компенсации гипотиреоза, позволяющее снизить дозу препаратов левотироксина, что особенно актуально для пациентов пожилого возраста с сопутствующей кардиальной патологией.
На базе клиники ГУ «Институт проблем эндокринной патологии им. В.Я. Данилевского НАМН Украины» было проведено открытое клиническое исследование эффективности и переносимости диетической добавки Тиреофарм® у пациентов с аутоиммунным тирео–идитом и гипотиреозом средней степени тяжести и тяжелой формы.
Цель проведенного исследования — оценить эффективность и переносимость применения диетической добавки Тиреофарм® у пациентов с АИТ и гипотиреозом.
Материалы и методы
В исследовании принимали участие 30 пациентов с АИТ и гипотиреозом. Все пациенты были женского пола. Среди обследованных пациенток у 18 диагностирован гипертрофический вариант и у 12 — атрофический вариант АИТ, согласно существующим критериям диагностики. У всех женщин проведено исследование и выполнена оценка иммуноферментным методом Т-клеточного звена иммунитета: определены кластеры дифференцировки (CD) антигенов, расположенные на поверхности клеток, являющиеся своеобразными маркерами клеток. CD3+ — кластеры зрелых Т-лимфоцитов, CD4+ — кластеры Т-хелперов и CD8+ — кластеры Т-супрессоров. Рассчитано значение иммунорегуляторного индекса, CD4+/CD8+, которое в норме составляет 1,5–2,0.
Всем пациентам, включенным в исследование, проводили анализ анамнестических данных, оценку соматического статуса, результатов лабораторных и инструментальных методов (УЗИ щитовидной железы).
Состояние липидного обмена оценивали согласно определению уровней триглицеридов (ТГ), общего холестерина (ОХС), холестерина липопротеидов высокой плотности (ХС ЛПВП), холестерина липопротеидов низкой плотности (ХС ЛПНП), коэффициента атерогенности. Индекс атерогенности, на основании которого классифицируют дислипопротеидемии, рассчитывали по формуле (ОХС – ХС ЛПВП) / ХС ЛПВП.
Длительность АИТ составила от 3 до 9 лет. Средний возраст женщин, находящихся под наблюдением, составил 44,0 ± 6,9 года. Распределение пациенток по возрасту представлено в табл. 1.
Всем пациентам к комплексной терапии был добавлен прием фитокомплекса Тиреофарм® по 1 капсуле трижды в день. Длительность наблюдения за пациентами составила 3 месяца. Женщинам, получающим заместительную терапию препаратами левотироксина, на протяжении исследования не производилась коррекция суточной дозы препарата.
Всем пациентам, включенным в исследование, проводились лабораторные и инструментальные исследования.
Критерии включения в исследование:
► возраст от 18 до 70 лет;
► установленный диагноз АИТ, гипотиреоз;
► высокий комплайенс в соблюдении рекомендаций;
► отсутствие нарушений со стороны функции почек и печени;
► отсутствие значимой коморбидной патологии.
До включения в исследование все больные проходили комплексное обследование с определением уровня тиреоидных гормонов, тиреотропного гормона с целью выявления компенсации тиреоидной функции на фоне приема заместительной терапии, а также критериев, позволяющих включить пациентов в наблюдение.
Статистическая обработка данных выполнена на индивидуальном компьютере с помощью электронных таблиц Microsoft Excel и пакета прикладных программ Statistica for Windows v. 7.0, StatSoft Inc. (США). Для сравнения числовых данных (после проверки количественных данных по нормальному распределению) использовали метод вариационной статистики.
Результаты и их обсуждение
Анализ соматических проявлений показал, что наиболее частыми были общая слабость и снижение работоспособности — 30 (100 %) случаев, ощущение «кома» в области передней поверхности шеи — 30 (100 %), головные боли — у 30 больных (100 %), раздражительность — у 30 (100 %), кардиалгии и сердцебиение — у 30 (100 %), дис–сомния — у 24 (80 %) пациентов.
☼ Оценка эффективности и переносимости
Оценка эффективности применения фитокомплекса Тиреофарм® в составе комплексной терапии у пациентов с АИТ, гипотиреозом проводилась по следующим критериям:
► субъективный статус: чувство усталости, слабости; качество сна, частота приступов сердцебиения, степень эмоциональной лабильности, ощущения «кома»;
► показатели состояния липидного обмена;
► показатели Т-клеточного звена иммунной системы;
► показатели тиреоидного статуса;
► без существенных клинических изменений.
В табл. 2 представлены результаты оценки субъективного статуса. Отмечено уменьшение эмоциональной лабильности, исчезновение ощущения «кома» в передней области шеи, чувства усталости у 100 % пациентов, более чем у 80 % пациентов улучшилось качество сна, снизилась частота приступов головных болей, сердцебиений.
В результате добавления к комплексной терапии фитокомплекса Тиреофарм® отмечалась позитивная динамика в сфере соматических проявлений. Наиболее заметными были изменения в плане повышения работоспособности, толерантности к физическим нагрузкам, значительно меньшей выраженности астенических и соматовегетативных проявлений, улучшения качества сна, а соответственно, и качества жизни.
При исследовании состояния липидного обмена (рис. 1) отмечено клинически значимое снижение уровней ОХС у пациентов с АИТ и гипотиреозом с 7,3 ± 1,1 ммоль/л до 6,0 ± 0,8 ммоль/л (p < 0,01) и ТГ с 3,4 ± 1,4 ммоль/л до 2,2 ± 0,9 ммоль/л (p < 0,01).
Повышенное содержание ТГ в крови делает ее более вязкой, что способствует тромбообразованию. Особенно опасно сочетание высокого уровня триглицеридов с низким содержанием ХС ЛПВП. В этом случае даже нормальное содержание ОХС не снижает риска развития инфаркта миокарда.
В процессе наблюдения отмечено клинически значимое улучшение параметров состояния Т-клеточного звена иммунной системы (рис. 2). В начале исследования имел место Т-иммунодефицит; увеличение содержания Т-хелперов (CD4+) при значительном дефиците Т-супрессоров (CD8+); увеличение иммунорегуляторного индекса (хелпер-супрессорного соотношения). В динамике количество Т-супрессоров значимо увеличилось: с 16,20 ± 0,85 % до 22,8 ± 1,1 %, p < 0,05, за счет чего уменьшилось значение иммунорегуляторного индекса с 3,59 до 2,1; p < 0,05. Уменьшение значения иммунорегуляторного индекса свидетельствует о снижении аутоиммунной агрессии.
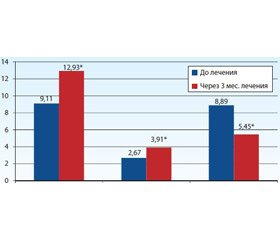
При оценке тиреоидного статуса в динамике установлено клинически значимое повышение уровней Т4св. (9,11; 12,93 пмоль/л) и трийодтиронина (Т3св.) (2,67; 3,91 пмоль/л) с одномоментным клинически значимым снижением уровня ТТГ (8,89; 5,45 мМЕд/мл) (рис. 3).
Вышеуказанную положительную динамику можно объяснить тиреотропным действием альбинина, входящего в экстракт корневища лапчатки белой.
В результате приема фитокомплекса Тиреофарм® выявлено клинически значимое снижение титра антител к тиреоглобулину (АТ-ТГ) (191,39; 97,68 МЕд/мл) и антител к тиреопероксидазе (АТ-ТПО) (708,43; 336,30 МЕд/мл), что свидетельствует о реализации его иммуномодулирующего и антиоксидантного эффектов (рис. 4).
При оценке динамики ультразвуковых параметров диагностики аутоиммунного поражения ткани ЩЖ выявлено клинически значимое уменьшение суммарного объема обеих долей (14,11; 11,1 см3 ), что указывает на уменьшение лимфоцитарного отека и подтверждает наличие противовоспалительного эффекта Тирео–фарма®.
Переносимость терапии оценивали по следующим критериям:
► хорошая переносимость — побочных реакций не отмечено;
► удовлетворительная переносимость — наблюдаются незначительные побочные реакции, не причиняющие серьезных проблем пациенту и не требующие отмены препарата;
► неудовлетворительная переносимость — имеют место серьезные побочные эффекты, оказывающие значительное отрицательное влияние на состояние больного, требующие отмены диетической добавки и проведения дополнительных медицинских мероприятий.
Клиническую безопасность фитокомплекса Тиреофарм® определяли на основании субъективных симптомов, сообщаемых пациентами (в процессе наблюдения — 3 контакта в течение трех месяцев), объективных данных и лабораторных показателей в динамике (при включении в исследование и на заключительном визите).
Анализ переносимости Тиреофарма® в комбинированной терапии показал, что в 100 % случаев она была хорошей.
Таким образом, благодаря сбалансированному составу Тиреофарм® может быть рекомендован к применению в клинической практике в составе комплексной терапии у пациентов с АИТ, гипотиреозом, при диффузном эутиреоидном зобе, а также лицам, проживающим в эндемичных районах.
Выводы
1. Фитокомплекс Тиреофарм® при назначении по 1 капсуле 3 раза в день в течение 3 месяцев оказывает регулирующее воздействие на щитовидную железу, проявляет иммуномодулирующую, антиоксидантную, противовоспалительную активность у пациентов с аутоиммунным тиреоидитом и гипотиреозом.
2. При добавлении к стандартному лечению (которое было неизменным в течение 6 мес. и на фоне которого не было достигнуто компенсации гипотиреоза) фитокомплекса Тиреофарм® отмечалось уменьшение субъективных астенических и соматовегетативных проявлений в виде снижения степени выраженности головной боли, отсутствия жалоб на ощущение «кома в горле», шума в голове, раздражительности, общей слабости, таким образом, в целом улучшается качество жизни.
3. Наиболее значимыми были изменения в повышении работоспособности и толерантности к физическим нагрузкам, уменьшении раздражительности у пациентов, принимавших Тиреофарм®, что способствовало повышению приверженности пациентов к лечению.
4. Тиреофарм® не вызывает побочных эффектов при применении в течение 3 месяцев, хорошо переносится пациентами, что свидетельствует о его безопасности и возможности использования для длительного лечения данного контингента больных.
5. Тиреофарм® позволяет снизить суточную дозу препаратов левотироксина, а также при декомпенсированном гипотиреозе на фоне приема неизменной дозы препаратов левотироксина дает возможность не повышать ее, что особенно актуально для пожилых пациентов с частой сопутствующей кардиальной патологией.
6. Тиреофарм®, используемый в комплексе со стандартным лечением, способствует компенсации гипотиреоза, уменьшает метаболические изменения, в первую очередь улучшая показатели липидного обмена, что особенно важно для пациентов с наличием риска прогрессирования кардиальной
патологии.
7. Фитокомплекс Тиреофарм® оказывает иммунокорректирующее действие путем нормализации дисбаланса в клеточном звене иммунитета, являющегося основным звеном патогенеза аутоиммунного заболевания.
Впервые опубликовано в журнале
«Проблеми ендокринної патології», № 1, 2018
Список литературы
находится в редакции

/u/6-1.jpg)
/u/8-1.jpg)