Журнал «Медицина неотложных состояний» №1(88), 2018
Вернуться к номеру
Эффективность применения мультимодального обезболивания у пациентов офтальмохирургического профиля при антиглаукомных операциях
Авторы: Кобеляцкий Ю.Ю.(2), Сердюк В.Н.(1), Алексеев В.П.(1), Мынка Н.В.(1, 2), Дорофеева А.С.(1, 2)
(1) — КУ «Днепропетровская областная клиническая офтальмологическая больница», г. Днепр, Украина
(2) — ГУ «Днепропетровская медицинская академия МЗ Украины», г. Днепр, Украина
Рубрики: Медицина неотложных состояний
Разделы: Клинические исследования
Версия для печати
Актуальність. У роботі висвітлюються результати проведення багатокомпонентного загального знеболювання при офтальмологічних оперативних втручаннях з метою поліпшення якості інтраопераційного і післяопераційного знеболювання, зниження кількості ускладнень, пов’язаних з анестезіологічною допомогою у післяопераційному періоді. Матеріали та методи. Дослідження було проведено у пацієнтів віком від 19 до 42 років, яким виконувалися антиглаукомні оперативні втручання. Для проведення порівняльного аналізу хворі були розподілені на групи з урахуванням виду обраного знеболювання: 1-ша група (n = 20) — пацієнти, у яких була застосована тактика профілактичного введення мелоксикаму під час премедикації, проводилася анестезія шляхом ретробульбарної блокади і седації пропофолом, знеболювання мелоксикамом продовжували в післяопераційному періоді за схемою запобіжної аналгезії; 2-га група (n = 24) — пацієнти, знеболювання яких здійснювалося за раніше прийнятою в нашій клініці схемою (премедикація сибазон + фентаніл), внутрішньовенний наркоз пропофолом зі збереженим спонтанним диханням і болюсним введенням фентанілу під час потенційно хворобливих етапів втручання. Післяопераційне знеболювання на вимогу пацієнтів внутрішньом’язовим введенням кетопрофену. Результати. Вираженість больового синдрому менше 3 балів за візуально-аналоговою шкалою в 1-й групі пацієнтів становила 90 і 85 %, у 2-й групі — 45,8 і 58,3 % на 6 і 12 годинах післяопераційного періоду відповідно. Розвиток післяопераційної нудоти і блювання в 1-й групі пацієнтів з використанням схеми мультимодального використання становив 5 % порівняно з 33,3 % в контрольній групі пацієнтів. Розвиток артеріальної гіпертензії в післяопераційному періоді в 1-й групі відзначався у 15 % пацієнтів порівняно з 45,8 % пацієнтів у 2-й групі. Розвиток артеріальної гіпотензії відзначався тільки у пацієнтів контрольної групи, і частота даного ускладнення становила 37,5 %. Не було зареєстровано жодного випадку гіпотензії у пацієнтів 1-ї групи. Висновки. Використання запропонованої схеми мультимодального знеболювання дозволяє підвищити ефективність і керованість анестезіологічного знеболювання у вигляді забезпечення адекватного знеболювання в післяопераційному періоді без застосування наркотичних анальгетиків, зниження ризику розвитку післяопераційних ускладнень (післяопераційної нудоти і блювання, артеріальної гіпертензії і гіпотензії).
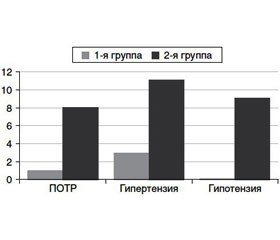
Актуальность. В работе освещаются результаты проведения многокомпонентного общего обезболивания при офтальмологических оперативных вмешательствах с целью улучшения качества интраоперационного и послеоперационного обезболивания, снижения количества осложнений, связанных с анестезиологическим пособием в послеоперационном периоде. Материалы и методы. Исследование было проведено у пациентов в возрасте от 19 до 42 лет, которым выполнялись антиглаукомные оперативные вмешательства. Для проведения сравнительного анализа больные были распределены на группы с учетом вида выбранного обезболивания: 1-я группа (n = 20) — пациенты, у которых была применена тактика профилактического введения мелоксикама во время премедикации, проводилась анестезия путем ретробульбарной блокады и седации пропофолом, обезболивание мелоксикамом продолжали в послеоперационном периоде по схеме упреждающей анальгезии; 2-я группа (n = 24) — пациенты, обезболивание которых осуществлялось по ранее принятой в нашей клинике схеме (премедикация сибазон + фентанил), внутривенный наркоз пропофолом с сохраненным спонтанным дыханием и болюсным введением фентанила во время потенциально болезненных этапов вмешательства. Послеоперационное обезболивание по требованию пациентов внутримышечным введением кетопрофена. Результаты. Выраженность болевого синдрома менее 3 баллов по визуально-аналоговой шкале в 1-й группе пациентов составила 90 и 85 %, во 2-й группе — 45,8 и 58,3 % на 6 и 12 часах послеоперационного периода соответственно. Развитие послеоперационной тошноты и рвоты в 1-й группе пациентов с использованием схемы мультимодального использования составило 5 % по сравнению с 33,3 % в контрольной группе пациентов. Развитие артериальной гипертензии в послеоперационном периоде в 1-й группе отмечалось у 15 % пациентов по сравнению с 45,8 % пациентов во 2-й группе. Развитие артериальной гипотензии отмечалось только у пациентов контрольной группы, и частота данного осложнения составила 37,5 %. Не было зарегистрировано ни одного случая артериальной гипотензии у пациентов 1-й группы. Выводы. Использование предложенной схемы мультимодального обезболивания позволяет повысить эффективность и управляемость анестезиологического обезболивания в виде обеспечения адекватного обезболивания в послеоперационном периоде без применения наркотических анальгетиков, снижения риска развития послеоперационных осложнений (послеоперационной тошноты и рвоты, артериальной гипертензии и гипотензии).
Background. The work covers the results of multicomponent general anesthesia with ophthalmic surgeries in order to improve the quality of intraoperative and postoperative analgesia, and to reduce the number of complications associated with anesthetic management in the postoperative period. Surgery for glaucoma belongs to operations with moderate pain syndrome. A number of studies have demonstrated that multimodal perioperative analgesia can reduce pre- and postoperative hyperalgesia. Materials and methods. The study included patients aged 19–42 years who underwent glaucoma surgery. For the comparative analysis, the patients were divided into groups taking into account the type of analgesia: group 1 (n = 20) — preventive administration of meloxicam during premedication, anesthesia was performed by retrobulbar block and sedation with propofol. Anesthesia with meloxicam was continued in the postoperative period according to the scheme of pre-emptive analgesia; group 2 (n = 24) — anesthesia was performed according to the scheme previously adopted in our clinic (premedication of diazepam + fentanyl), intravenous anesthesia using propofol with preserved spontaneous breathing and bolus injection of fentanyl during potentially painful stages of intervention. Postoperative analgesia was done by intramuscular injection of ketoprofen at the request of patients.The groups were comparable by sex, age and clinical manifestations of the disease. According to their physical status, all patients corresponded to class I–III of the American Society of Anesthesiologists (ASA). We studied the pain level on Visual Analogue Scale (VAS) (twice: 6 and 12 hours after surgery) and recorded complications within 24 hours after surgery. Results. Six and 12 hours after the surgery, the severity of the pain syndrome according to VAS was less than 3 in 90 and 85 % of group 1 patients, respectively, in group 2 — 45.8 and 58.3 %. Postoperative nausea and vomiting were detected in 5 % in group 1 with the use of multimodal analgesia as compared to 33.3 % in group 2 (controls). The development of arterial hypertension in the postoperative period in group 1 was noted in 15 % of patients vs. 45.8 % in group 2. Arterial hypotension was detected only in patients of group 2, and the incidence of this complication was 37.5 %. There were no cases of arterial hypotension in patients of group 1. Conclusions. Тhus, the use of multimodal analgesia involving premedication with meloxicam, anesthesia in combination of retrobulbar block and administration of propofol, and postoperative analgesia with meloxicam according to the scheme of anticipatory analgesia, makes it possible to increase the efficacy and control of anesthetic management during ophthalmic surgeries for glaucoma. The use of meloxicam in premedication and postoperative period allows you to achieve adequate postoperative analgesia, and without the use of narcotic analgesics. The administration of meloxicam as a component of multimodal anesthesia makes it possible to significantly reduce the risk of such postoperative complications as postoperative nausea of vomiting, development of arterial hypotension and hypertension, which is especially important in ophthalmic surgery, as the above complications cause an increased risk of suprachoroidal hemorrhage.
мультимодальна анестезія; офтальмохірургія; глаукома; мелоксикам; анестезіологія
мультимодальная анестезия; офтальмохирургия; глаукома; мелоксикам; анестезиология
multimodal anesthesia; ophthalmic surgery; glaucoma; meloxicam; anesthesiology

/89-1.jpg)
/90-1.jpg)