Резюме
Актуальність. Відповідно до постулатів Національної програми з вивчення холестерину (NCEP) цукровий діабет (ЦД) 2-го типу класифікується як «еквівалент ризику» ішемічної хвороби серця. Мета даної роботи — дослідити динаміку антропометричних показників, показників вуглеводного обміну, маркерів інсулінорезистентності (ІР), показників печінкового комплексу, коагулограми, сечової кислоти, швидкості клубочкової фільтрації (ШКФ), а також інструментальні показники у хворих на ЦД 2-го типу, які отримували шести- та дев’ятимісячну диференційовану цукрознижувальну терапію та метаболічну терапію препаратом Вазонат. Матеріали та методи. Під спостереженням перебувало 60 хворих на ЦД 2-го типу в стані декомпенсації, яким призначено у якості метаболічної терапії препарат Вазонат по 10 мл внутрішньовенно протягом 10 діб з початку дослідження та для пролонгації курсу 1000 мг/добу перорально протягом 6 та 9 місяців, з метою дослідження дії препарату протягом часу з урахуванням хронічного перебігу захворювання, наявності коморбідної патології. Вплив Вазонату вивчався на тлі диференційованої цукрознижувальної терапії: пероральними цукрознижувальними препаратами (метформін, 30 осіб), комбінацією метформіну та інсуліну НПХ (друга група, 30 осіб). Спостереження за хворими та вивчення динаміки показників вуглеводного обміну й маркерів ІР проводилося на початку дослідження та протягом шести- та дев’ятимісячного терміну. Результати. Вазонат підсилює вплив цукрознижувальної терапії, позитивно впливає на показники ІР та антропометричні параметри, змінює на краще значення ліпідограми, печінкового комплексу, сечової кислоти, протромбінового індексу, ШКФ та позитивно впливає на динаміку фракції викиду лівого шлуночка серця. Висновки. Препарат Вазонат доцільно призначати як додаткову метаболічну терапію для покращення клінічного перебігу та прогнозу захворювання, а також покращення якості життя пацієнтів з ЦД 2-го типу з гепато- та нефропатією, ішемічною хворобою серця, артеріальною гіпертензією, подагрою, порушеннями ліпідного спектра крові.
Актуальность. В соответствии с постулатами Национальной программы по изучению холестерина (NCEP) сахарный диабет (СД) 2-го типа классифицируется как «эквивалент риска» ишемической болезни сердца. Цель данной работы — исследовать динамику антропометрических показателей, показателей углеводного обмена, маркеров инсулинорезистентности (ИР), показателей печеночного комплекса, коагулограммы, мочевой кислоты, скорости клубочковой фильтрации (СКФ), а также инструментальные показатели у больных СД 2-го типа, которые получали шести- и девятимесячную дифференцированную сахароснижающую терапию и метаболическую терапию препаратом Вазонат. Материалы и методы. Под наблюдением находилось 60 больных СД 2-го типа в состоянии декомпенсации, которым назначен в качестве метаболической терапии препарат Вазонат по 10 мл внутривенно в течение 10 суток с начала исследования и для пролонгации курса 1000 мг/сут перорально в течение 6 и 9 месяцев, с целью исследования действия препарата с течением времени с учетом хронического течения заболевания, наличия коморбидной патологии. Влияние Вазоната изучалось на фоне дифференцированной сахароснижающей терапии: пероральными сахароснижающими препаратами (метформин, 30 человек), комбинацией метформина и инсулина НПХ (вторая группа, 30 человек). Наблюдение за больными и изучение динамики показателей углеводного обмена и маркеров ИР проводилось в начале исследования и в течение шести- и девятимесячного срока. Результаты. Вазонат усиливает влияние сахароснижающей терапии, положительно влияет на показатели ИР и антропометрические параметры, изменяет к лучшему значения липидограммы, печеночного комплекса, мочевой кислоты, протромбинового индекса и СКФ, положительно влияет на динамику фракции выброса левого желудочка сердца. Выводы. Препарат Вазонат целесообразно назначать в качестве дополнительной метаболической терапии для улучшения клинического течения и прогноза заболевания, а также улучшения качества жизни пациентов с СД 2-го типа с гепато- и нефропатией, ишемической болезнью сердца, артериальной гипертензией, подагрой, нарушениями липидного спектра крови.
Background. In accordance with the postulates of the National Cholesterol Education Program, type 2 diabetes mellitus (DM) is classified as coronary heart disease equivalent of risk. Purpose of this work is to investigate the dynamics of anthropometric indexes, parameters of carbohydrate metabolism, markers of insulin resistance (IR), indexes of hepatic complex, coagulogram, urinary acid, glomerular filtration rate (GFR), and also instrumental indexes in patients with type 2 DM during differentiated hypoglycemic and metabolic therapy by Vazonat preparation for 6 and 9 months. Materials and methods. Under supervision, there were 60 patients with type 2 DM in the state of decompensation, who received Vazonat 10 ml intravenously as metabolic therapy during 10 days from the beginning of the research and 1000 μg/day orally for prolongation of the course during 6 and 9 months. Influence of Vazonat was studied on the background the differentiated hypoglycemic therapy: by oral hypoglycemic preparations (metformin, 30 patients), combination therapy with metformin and NPH insulin (second group, 30 individuals). Study of the dynamics of carbohydrate metabolism indexes and IR markers was conducted in patients at the beginning of the research and during 6 and 9 months. Results. Vazonat strengthens the effect of hypoglycemic therapy, influences the IR indexes and anthropometric parameters, lipidogram values, hepatic complex, urinary acid level, prothrombin index, GFR and positively influences the dynamics of left ventricular ejection fraction. Conclusions. It is expedient to prescribe Vazonat as additional metabolic therapy for the improvement of clinical course and disease prognosis, and also for the improvement of quality of life in patients with type 2 DM and hepato- and nephropathy, coronary heart disease, arterial hypertension, gout, violations of blood lipid spectrum.
Вступ
Цукровий діабет (ЦД) — найбільш поширене ендокринне захворювання. Прогресивне збільшення кількості хворих відбувається здебільшого за рахунок хворих на ЦД 2-го типу. Поширеність захворювання в країнах Європи, США та Канаді сягає 8 % від загальної кількості дорослого населення [1]. За даними провідних наукових фахових та статистичних установ, найбільшу загрозу для життя та здоров’я хворих становлять хронічні ускладнення захворювання, із числа яких серцево-судинні та церебральні події посідають одне з перших місць серед причин смертності [2]. Найбільш вагомими факторами розвитку ускладнень є надлишкова маса тіла, дисліпідемія, інсулінорезистентність та декомпенсація вуглеводного обміну [3]. Саме ці фактори призводять до атеросклерозу, тромбогенезу, артеріальної гіпертензії та, як наслідок, до фатальних судинних подій. За даними ВООЗ 2016 року, у світі від серцево-судинних катастроф померло 7,25 млн осіб, від церебральних катастроф — 6,15 млн осіб, безпосередньо від ЦД — 1,26 млн осіб [4]. Загальновідомим фактом є те, що переважна більшість пацієнтів, які померли від серцево-судинних та церебральних захворювань, мали ЦД 2-го типу як фонову коморбідну патологію.
Доведено, що хворі на ЦД 2-го типу мають ризик розвитку гострого інфаркту міокарда, подібний до такого у хворих, які вже мали інфаркт в анамнезі, а також більш високу летальність після першого інфаркту, ніж контингент без ЦД 2-го типу. Окрім того, ризик ішемічної хвороби серця (ІХС) та фатального інфаркту міокарда, на противагу ситуації в недіабетичній популяції, вищий у жінок із ЦД 2-го типу порівняно з чоловіками [5]. Такі факти дають змогу багатьом вченим розглядати ЦД 2-го типу як хворобу, подібну до ІХС за походженням [6].
Відповідно до постулатів Національної програми з вивчення холестерину (NCEP) ЦД 2-го типу класифікується як «еквівалент ризику» ІХС — порушення, що становить абсолютний 10-річний ризик для розвитку нової коронарної події й дорівнює ризику, що відзначається у хворих без ЦД із діагностованою ІХС [7, 8].
Мета даної роботи — дослідити динаміку антропометричних показників (індекс маси тіла (ІМТ) та окружність талії (ОТ)), показників вуглеводного обміну (глюкоза натще, глікований гемоглобін (НbА1с)), маркерів ІР (індекс НОМА-IR), показників печінкового комплексу, коагулограми, сечової кислоти, швидкості клубочкової фільтрації (ШКФ) нирок за розрахунковою формулою CKD-EPI, а також інструментальних показників (ехокардіографія (ЕхоКГ)) у хворих на ЦД 2-го типу, які отримували шести- та дев’ятимісячну диференційовану цукро–знижувальну терапію та метаболічну терапію препаратом Вазонат.
Матеріали та методи
Загалом обстежено 60 хворих на ЦД 2-го типу. Із них до початку дослідження не отримували ніякої цукрознижувальної терапії 42 особи (70 %), отримували гіпокалорійне харчування зі зменшенням вмісту вуглеводів 3 особи (5 %), препарати метформіну в добовій дозі 500 мг — 7 осіб (11 %), препарати сульфонілсечовини — 5 осіб (8 %), –тіазолідиндіони — 2 (4 %); одна особа (2 %) отримувала акарбозу. Усі хворі спостерігалися амбулаторно в ендокринолога поліклінічного відділення КЗ «Дніпропетровська обласна клінічна лікарня імені І.І. Мечникова» (загальний термін спостереження становив 9 місяців). Відбір когорти хворих та обробка даних проводилася спільно амбулаторним та стаціонарними профільними підрозділами лікарні. У дослідження не були включені хворі, які на момент відбору когорти вже мали тяжкі ускладнення, а саме препроліферативну та проліферативну ретинопатію, нефропатію 3-го і більше ступеня за класифікацією Могенсена, синдром діа–бетичної стопи (ступінь > 1 за Вагнером), а також гострі порушення вуглеводного обміну. Приводом для вилучення з дослідження також була тяжка супутня кардіоваскулярна, онкологічна, легенева, нефрологічна, гінекологічна та гастроентерологічна патологія.
Хворі обстежені за стандартними клінічними методиками: антропометричні дослідження — вимірювання зросту, маси тіла, розрахунок індексу маси тіла, вимірювання окружності талії, артеріального тиску; біохімічні дослідження — вимірювання глюкози капілярної крові ферментативними калориметричними методами (автоматичний біохімічний аналізатор A25 Biosystems, Іспанія, 2005; гексокіназний — реактивами BIOCON®, Німеччина, та глюкозооксидазний — реактивами Biosystems, Іспанія); імунореактивний інсулін (мікропланшетний рідер Anthos, Австрія; імуноферментний аналіз (ELISA) — твердофазний метод); глікований гемоглобін — напівавтоматичний біохімічний аналізатор BTS 330 (Biosystems, Іспанія, методика високо–швидкісної хроматографії).
Усі лабораторні показники та розрахункові параметри надані центральною клінічною лабораторією КЗ «Дніпропетровська обласна клінічна лікарня імені І.І. Мечникова». За математичною методикою розраховано індекс HOMA-IR. Обробка даних проводилася за допомогою пакета програм «Статистика», програмного забезпечення Ехсеl (2015) та пакета прикладних програм. Функціональні дослідження проводилися у відділенні функціональної діагностики КЗ «Дніпропетровська обласна клінічна лікарня імені І.І. Мечникова»; дослідження ЕхоКГ проводилися на апараті Heart Screen 606 (Угорщина, 2010), УЗД печінки — на апараті Braintest (Харків, 2011). Розрахунки індексу інсулінорезистентності НОМА-IR здійснювалися за формулою: HOMA-IR = [інсулін (мкМО/мл) × глюкоза (ммоль/л)]/22,5. Значення індексу НОМА-IR понад 2,27 оцінюється як ІР. Визначення ШКФ проводилося за формулою СKD-EPІ.
Вік обстежених хворих становив від 27 до 67 років, середній вік — 42,00 ± 0,01 року, найбільша кількість хворих була віком від 38 до 62 років (55 %). Кількість жінок становила 42 особи (60 %), чоловіків — 18 осіб (40 %). На початку дослідження всі хворі мали некомпенсовані рівні глікемії натще (> 7,5 ммоль/л), некомпенсовану постпрандіальну глікемію (глікемія понад 10,0 ммоль/л) та ІМТ понад 25 кг/м2.
При аналізі обраної когорти хворих та визначенні основних скринінгових антропометричних і лабораторних показників: ІМТ, ОТ, глікемія натще, глікемія постпрандіальна, НbА1с, виявлено, що хворі мають ІМТ від 25 до 33 кг/м2, глікемію натще від 6,5 до 16,9 ммоль/л, глікемію постпрандіальну від 10,0 до 22,5 ммоль/л; параметри ОТ у чоловіків — від 101 до 113 см, у жінок — від 81 до 94 см, НbА1с — від 7,7 до 15,8 %.
Хворі були однорідними за біохімічними показниками та функціональними параметрами, вони розподілені на дві групи по 30 осіб у кожній. У першій групі хворі протягом усього курсу терапії отримували препарат Вазонат за визначеною схемою: по 10 мл внутрішньовенно протягом 10 діб з початку дослідження та 1000 мг/добу для пролонгації курсу перорально протягом 6 та 9 місяців. У другій групі пацієнти не отримували Вазонат.
Обидві групи хворих також були розподілені ще на дві підгрупи по 15 осіб на підставі рівнів глікемії натще (до 13,9 ммоль/л та більше); при рівні глікемії натще понад 13,9 ммоль/л була призначена комбінована терапія з препаратами інсуліну. Перша група розподілена на підгрупу 1А (метформін 2000 мкг/добу) та 1Б (метформін 2000 мкг/добу та інсулін НПХ із розрахунку 0,4 ОД/кг маси тіла з поступовою титрацією дози). Друга група розподілена на підгрупи 2А та 2Б з аналогічними схемами цукрознижувальної терапії. Інсулінотерапія проводилася інсуліновими шприцами Вecton Dicinson із незнімними голками в ділянку живота за стандартною методикою. Визначення груп та підгруп наведено на рис. 1.
Результати
Для оцінки ефективності терапії проводилось вивчення лабораторних та функціональних показників, розрахункових даних на початку дослідження (0-й тиждень), а потім на 24-му та 36-му тижнях.
При аналізі показників вуглеводного обміну виявлено, що показники глікемії натще на тлі лікування вірогідно знизилися в усіх групах; найбільше — у підгрупах 1Б та 2Б (табл. 1, рис. 2).
В усіх групах також вірогідно знизився рівень НbА1с, найбільше — у підгрупах 1Б та 2Б (табл. 2, рис. 3).
Більш вагоме зниження показників глікемії –натще та НbА1с у підгрупах 1Б та 2Б можна пояснити впливом призначення інсуліну пролонгованої дії (титраційна кінцева доза в підгрупі 1Б становить 24 ОД/добу, у 2Б — 32 ОД/добу).
В усіх підгрупах відзначалося зниження ІМТ, однак вірогідно та найбільш вагомо цей показник знизився в підгрупі 1А. Також вірогідне зменшення показника відбулося в підгрупі 2А. Значення ОТ вірогідно зменшилося лише в підгрупах 1А (з 104,80 ± 1,71 см до 96,80 ± 1,47 см, р < 0,05), з меншим ступенем вірогідності — у 2А (з 105,00 ± 1,29 см до 98,20 ± 1,35 см, р < 0,05).
Важливим також було вірогідне зниження показника ІР у підгрупах 1А і 2А (табл. 3, рис. 4).
У процесі спостереження привертає увагу динаміка показників ліпідного спектра крові. Вірогідне зниження вмісту тригліцеридів (ТГ) спостерігалося лише в підгрупах 1А (з 2,01 ± 0,09 ммоль/л до 1,09 ± 0,05 ммоль/л, р < 0,05) та 2А (з 2,06 ± ± 0,05 ммоль/л до 1,52 ± 0,05 ммоль/л, р < 0,05). У цих же підгрупах відзначалося вірогідне зниження вмісту холестерину ліпопротеїдів низької щільності (ЛПНЩ): у підгрупі 1А — з 4,89 ± 0,22 ммоль/л до 2,42 ± 0,19 ммоль/л (р < 0,05), у підгрупі 2А — з 4,98 ± 0,20 ммоль/л до 3,01 ± 0,18 ммоль/л (р < 0,05).
При цьому відбувалося вірогідне підвищення вмісту холестерину ліпопротеїдів високої щільності (ЛПВЩ) лише в підгрупі 1А (з 0,68 ± 0,02 ммоль/л до 0,99 ± 0,01 ммоль/л, р < 0,05).
Вірогідне зниження вмісту холестерину ліпопротеїдів дуже низької щільності (ЛПДНЩ) спостерігалося в підгрупах 1А та 2А (з 1,59 ± 0,03 ммоль/л до 0,99 ± 0,03 ммоль/л, р < 0,05 у підгрупі 1А та з 1,61 ± 0,04 ммоль/л до 1,18 ± 0,05 ммоль/л, р < 0,05 у підгрупі 2А). Однак у підгрупі 1А відзначалося більш вагоме зменшення зазначених показників (ТГ, ЛПНЩ, ЛПДНЩ).
У процесі спостереження відзначалось вірогідне зниження вмісту сечової кислоти в сироватці крові лише в підгрупах 1А та 1Б. У підгрупі 1А — з 428,00 ± 3,76 ммоль/л до 312,00 ± 4,83 ммоль/л (р < 0,05), у підгрупі 1Б — з 410,00 ± 4,81 ммоль/л до 298,00 ± 4,97 ммоль/л (р < 0,05).
У хворих з підгруп 1А та 1Б вірогідно покращилися показники функціонального стану печінки в процесі спостереження після 36-го тижня. Так, активність аспартатамінотрансферази (АСТ) вірогідно зменшилася у хворих підгрупи 1А — з 42,30 ± 0,56 Од/л до 14,80 ± 0,42 Од/л (р < 0,05) і підгрупи 1Б — з 40,90 ± 0,52 Од/л до 18,90 ± ± 0,39 Од/л (р < 0,05). Спостерігалося також вірогідне зниження активності аланінамінотрансферази (АЛТ) у хворих з підгрупи 1А (з 88,00 ± ± 0,70 Од/л до 17,00 ± 0,51 Од/л, р < 0,05) та підгрупи 1Б (з 85,00 ± 0,58 Од/л до 19,00 ± 0,55 Од/л, р < 0,05) (рис. 5, 6).
Важливим результатом дослідження було встановлення позитивного впливу додаткового призначення Вазонату на ШКФ у хворих на ЦД 2-го типу (табл. 4). У хворих із підгруп 1А та 1Б ШКФ вірогідно збільшилася з 66,20 ± 1,94 мл/хв/1,73 м2 до 75,70 ± ± 1,86 мл/хв/1,73 м2 та з 64,70 ± 2,13 мл/хв/ 1,73 м2 до 70,10 ± 1,74 мл/хв/1,73 м2 відповідно.
Вірогідне зменшення протромбінового індексу спостерігалося лише у хворих з підгрупи 1А: з 113,00 ± 1,49 % до 99,00 ± 1,37 % (р < 0,05).
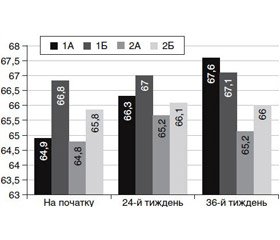
Особлива увага в процесі дослідження зверталася на показник фракції викиду лівого шлуночка (за даними ЕхоКГ). Нами встановлено, що лише у хворих з підгрупи 1А вірогідно підвищився зазначений показник — з 64,90 ± 0,83 % до 67,60 ± 0,81 % (р < 0,05) (табл. 5, рис. 7).
Обговорення
У процесі дослідження встановлено вагомий вплив додаткового призначення препарату Вазонат на низку показників у хворих на ЦД 2-го типу.
Аналізуючи динаміку показників печінкового комплексу, слід зазначити, що лише в підгрупах 1А та 1Б вірогідно знизилися показники активності АСТ та АЛТ. При цьому в підгрупах 2А та 2Б вірогідної динаміки не відзначалося. У процесі спостереження зміни розмірів печінки не спостерігалися.
Вміст сечової кислоти вірогідно знизився в підгрупах 1А та 1Б і не мав вірогідної динаміки в підгрупах 2А та 2Б. Вірогідне зниження вмісту тригліцеридів, а також холестерину ЛПНЩ і ЛПДНЩ відбувалося в 1А та 2А підгрупах, але в підгрупі 1А зменшення зазначених показників було більш вагомим та з більшим ступенем вірогідності. Однак лише у хворих у підгрупі 1А відзначалося вірогідне підвищення рівня холестерину ЛПВЩ.
Вірогідне зниження протромбінового індексу відбулося тільки в 1А групі.
Важливим результатом проведеного дослідження є вірогідне підвищення ШКФ у підгрупах 1А та 1Б і вірогідне збільшення фракції викиду лівого шлуночка у хворих 1А підгрупи.
Динаміка антропометричних характеристик, результатів вуглеводного обміну, лабораторних показників та функціональних даних дає підстави зазначити, що препарат Вазонат підсилює вплив цукрознижувальної терапії, впливає позитивним чином на показники ІР та антропометричні параметри, змінює на краще значення ліпідограми, печінкового комплексу, сечової кислоти, протромбінового індексу, ШКФ та позитивно впливає на динаміку фракції викиду лівого шлуночка серця.
Висновки
За результатами проведеного дослідження можна виділити такі категорії хворих, яким доцільно призначати препарат Вазонат як додаткову метаболічну терапію для покращення клінічного перебігу та прогнозу захворювання, а також покращення якості життя пацієнтів:
— хворі на цукровий діабет 2-го типу, які мають ускладнення, а саме діабетичну гепатопатію та –нефропатію;
— хворі на цукровий діабет 2-го типу, які мають супутню патологію, а саме ішемічну хворобу серця, артеріальну гіпертензію, подагру, порушення ліпідного спектра крові;
— хворі на цукровий діабет 2-го типу, які отримують інсулінотерапію в комбінації з пероральними цукрознижувальними препаратами;
— хворі без клінічного цукрового діабету, які, однак, мають компоненти метаболічного синдрому.
Конфлікт інтересів. Не заявлений.

/83-1.jpg)
/83-2.jpg)
/84-1.jpg)
/85-2.jpg)
/85-1.jpg)