Газета «Новости медицины и фармации» Репродуктология. Акушерство. Гинекология. Урология (641) 2018 (тематический номер)
Вернуться к номеру
ОПТИМІЗАЦІЯ ТЕРАПІЇ ЗАГРОЗЛИВОГО ВИКИДНЯ У ЖІНОК З ХРОНІЧНИМИ ЗАХВОРЮВАННЯМИ СЕЧОВИДІЛЬНИХ ШЛЯХІВ
Авторы: А.В. Старовєр, Д.Г. Коньков, О.Л. Очеретна
Вінницький національний медичний університет ім. М.І. Пирогова, м. Вінниця, Україна
Рубрики: Терапия, Урология
Разделы: Клинические исследования
Версия для печати
Вступ
Захворювання нирок та сечовидільних шляхів посідають провідне місце серед екстрагенітальної патології, що зустрічається у вагітних жінок. Незважаючи на застосування методів лікування та профілактики, на сьогодні майже кожна 4–5-та вагітна має те чи інше захворювання нирок та сечовивідних шляхів.
Захворювання сечовидільної системи чинять несприятливий вплив на перебіг вагітності, пологів, стан плода та новонародженого. Наявність даної патології корелює зі збільшенням частоти невиношування вагітності, затримки внутрішньоутробного росту плода, внутрішньоутробного інфікування плода, прееклампсії та еклампсії тощо. Однак навіть під час фізіологічного перебігу вагітності виникають фактори, що сприяють загостренню, прогресуванню чи виникненню патологічних станів сечовидільної системи. Уже в першій половині вагітності за рахунок впливу прогестерону відмічається розширення сечоводів та сфінктерів, збільшення об’єму та зниження тонусу сечового міхура, збільшення об’єму залишкової сечі, що формує умови для виникнення уростазу та висхідного поширення інфекції. Крім того, спостерігається зміна рН сечі. Зміщення рН сечі в той чи інший бік сприяє утворенню осаду різних солей: при рН нижче від 5,5 частіше утворюються уратні камені, при pH від 5,5 до 6,0 — оксалатні конкременти, при pH вище від 7,0 — фосфатні. Під час вагітності рН сечі зміщується в лужний бік, що сприяє виникненню гіперкристалурії, переважно фосфатурії, рідше — оксалатурії.
Навіть незначні зміни з боку сечовидільної системи можуть мати клінічну симптоматику, що нагадує акушерську патологію. Наприклад, клінічні прояви гіперкристалурії у вигляді больового синдрому можуть призводити до неправомірної постановки діагнозу загрозливого викидня, госпіталізації та неадекватного призначення гормональної терапії або ж при підтвердженні діагнозу можуть підтримувати його клініку, якщо лікування проводити без урахування супутньої патології сечовидільних шляхів.
У практиці акушера-гінеколога при призначенні лікування будь-якої патології, що виникає під час вагітності чи супроводжує її, завжди гостро стоїть питання медикаментозної терапії. З огляду на можливий негативний вплив лікарських засобів на ембріон і плід, а також необхідність у деяких випадках призначати довготривалу терапію, все ширше для лікування та профілактики різних патологічних станів лікарі застосовують фітотерапію. Переваги фітотерапії як монолікування, а також у комплексі з медикаментозними засобами полягають у тому, що фітотерапевтичні препарати мають виражену лікувальну активність та менший спектр побічних ефектів, ніж синтетичні препарати, менш токсичні, що особливо важливо в акушерській практиці, фармакодинаміка фітопрепаратів дозволяє впливати одночасно на декілька патогенетичних ланок, широкий діапазон терапевтичної дії дозволяє тривало (протягом 1–2 років) застосовувати фітопрепарати без ризику виникнення ускладнень та зниження ефективності лікування, особливо при хронічних захворюваннях, оптимізує базисну терапію патології, лікування фітопрепаратами можливе в амбулаторних умовах.
Незважаючи на цілий ряд позитивних ефектів, призначення фітотерапії вимагає певних умов, а саме: фітотерапія має бути комплексною (необхідне застосування фітокомпозицій, бо повний ефект може бути досягнутий лише при правильному поєднанні трав), слід використовувати лікарські рослини, які ростуть на територіях проживання пацієнтів (Європейський континент), що запобігає виникненню алергічних реакцій на антигени рослин, застосовувати стандартизовані екстракти рослин. Стандартизовані екстракти рослин розробляються особливим методом, вони проходять стандартизацію, що суворо встановлює кількість активних речовин кожної рослини та забезпечує єдність і послідовність у дозуванні кожної капсули, таблетки, краплі. Це має ряд переваг, а саме: постійний вміст діючих речовин та якість, які не залежать від пори року чи погоди, гарантують очікувальний ефект та безпеку застосування засобу, що особливо важливо під час вагітності.
Наявність в анамнезі захворювань сечовидільних шляхів у вагітних вимагає від лікаря ретельної уваги щодо виникнення можливих ускладнень, що можуть статися в будь-якому терміні вагітності, а також можуть супроводжувати патологію вагітності, та призначення довготривалої лікувальної й профілактичної терапії для запобігання цьому.
У зв’язку з вищевикладеним нашу увагу привернув фітопрепарат Солідагорен виробництва компанії Dr. Gustav Klein. Це полікомпонентний препарат, до складу якого входять трава золотушника звичайного (Solidago virgaurela), трава перстачу гусячого (Potentilla anserine) та трава хвоща польового (Equisetum arvense) у співвідношенні 4,2 : 1,4 : 1. Завдяки рослинами, що входять до його складу, препарат має антимікробну (помірна/висока), імуномодулюючу (підвищує фагоцитарну активність макрофагів, активує NK-клітини), протизапальну (знижує рівні прозапальних цитокінів, інгібує виділення протеаз, стимулює вироблення глюкокортикоїдів), знеболювальну, сечогінну, спазмолітичну, антиоксидантну, нефропротекторну дію, а також має в’яжучий (за рахунок вмісту кремнію та підтримки колоїдного стану сечі солями кремнію) та антикалькульозний ефект. Довіру до цього препарату викликає також те, що він виготовляється на одному виробництві методом стандартизації екстрактів, що дозволяє контролювати всі етапи його створення, підбір сировини здійснюється в екологічно чистих регіонах Європи, має вплив на широкий спектр нозологій: застосовується для лікування та профілактики інфекційних захворювань сечових шляхів, сечокам’яної хвороби в дорослих, дітей та вагітних жінок. Солідагорен присутній на ринку Європи з 1954 року, з того часу були проведені численні дослідження, що доводять ефективність та безпеку його застосування, зокрема під час вагітності.
Отже, метою нашого проспективного клінічного дослідження стала оцінка ефективності лікування загрозливого викидня в жінок із хронічними захворюваннями сечовидільних шляхів із додаванням до основної терапії фітопрепарату Солідагорен.
Матеріали та методи
У дослідженні брали участь 31 вагітна жінка із загрозливим викиднем та хронічною патологією сечовидільних шляхів, до стандартизованого протокольного лікування цим хворим додавався препарат Солідагорен (основна група, проспективне дослідження). Групу порівняння становили 30 жінок у першій половині вагітності, які отримували протокольне лікування загрозливого викидня за загальними рекомендаціями щодо покращення стану сечовидільних шляхів (дієта, достатній водний режим, позиційна терапія). Усі жінки на момент лікування перебували на клінічній базі кафедри акушерства і гінекології № 1 ВНМУ імені М.І. Пирогова, у гінекологічному відділенні Вінницького міського пологового будинку № 1.
Діагноз загрозливого викидня встановлювали на підставі скарг на болі внизу живота, наявність кров’яних виділень з піхви, відсутності структурних змін з боку шийки матки.
Обсяг обстеження включав аналіз скарг на момент надходження, а також у динаміці лікування, збір анамнезу, загальне та акушерське дослідження, клінічні аналізи при надходженні та в динаміці (перед випискою або через 7 днів лікування) — загальний аналіз крові, сечі, ультразвукове дослідження нирок та сечовидільних шляхів.
Загальноклінічні дослідження проводились за стандартною методикою, при цьому в загальному аналізі крові вивчався рівень гемоглобіну, еритроцитів, лейкоцитів, швидкість осідання еритроцитів (ШОЕ), у загальному аналізі сечі — питома вага, реакція, наявність білка, кількість лейкоцитів, наявність кристалурії. Загальний аналіз крові проводили натще, загальний аналіз сечі проводився з ранковою сечею.
Комплекс лікування загрозливого викидня був стандартним для обох груп та включав призначення прогестагену (у разі необхідності), фолієвої кислоти та препаратів транексамової кислоти за наявності кров’яних виділень. Жінки основної групи, крім того, отримували Солідагорен по 25 крапель тричі на добу, розводячи його в 100–200 мл рідини, протягом не менше від 1 місяця. Додатково призначався достатній водний режим — не менше від 2–2,5 л рідини на добу. Вагітним групи порівняння додатково до терапії загрозливого викидня пропонувалась дієтотерапія, достатній водний режим, постуральна терапія. Лікарських засобів, направлених на покращення стану сечовидільних шляхів, вагітні групи порівняння не отримували.
Критерії включення пацієнток у дослідження: вагітні з діагнозом «загрозливий викидень»; наявність в анамнезі хронічних захворювань сечовидільних шляхів; наявність змін у загальному аналізі сечі (гіперкристалурія); бажання та можливість жінок брати участь у дослідженні.
Основними критеріями порівняльної оцінки клінічної ефективності терапії вважали: термін зникнення клінічних симптомів захворювання (больовий синдром, дизурія, полакіурія); нормалізацію показників загального аналізу сечі, відсутність рецидивів захворювань сечовидільних шляхів протягом наступних 8 тижнів після закінчення лікування. Також ми враховували суб’єктивну оцінку дії прийому препарату вагітними (відсутність ефекту, задовільно, добре, дуже добре) через 7 діб та через 1 місяць лікування. Переносимість Солідагорену оцінювали на підставі виникнення побічних дій згідно зі скаргами пацієнток та суб’єктивною оцінкою жінками самопочуття при застосуванні препарату.
Дослідження відповідало принципам, викладеним у Гельсінській декларації (1989), Сеул (2008). Жінки, задіяні в дослідженні, давали письмову згоду на участь у дослідженні.
Статистичний аналіз був проведений із використанням програми Statistica 6.0. Відносний ризик, його стандартна похибка та 95% довірчий інтервал розраховувалися за наведеними нижче формулами.
Відносний ризик:
BR = a/(a + b) c/(c+ d),
де ВР — відносний ризик; а — кількість жінок із позитивним (поганим) результатом; b — кількість жінок із негативним (добрим) результатом досліджуваній групі; c — кількість жінок із позитивним (поганим) результатом у основній групі; d — кількість жінок із негативним (добрим) результатом у основній групі.
Стандартна похибка щодо ризику:
СП {ln(BP)} = √1 a + 1 c + 1 a + b – 1 c + d,
де СП — стандартна похибка; ВР — відносний ризик; а — кількість вагітних жінок із позитивним (поганим) результатом; b — кількість вагітних із негативним (добрим) результатом у досліджуваній групі; c — кількість вагітних із позитивним (поганим) результатом у основній групі; d — кількість жінок із негативним (добрим) результатом у основній групі.
95% довірчий інтервал:
95% ДІ = від exр(ln(BP) − 1,96 ´ СП{ln(BP)}) до exp(ln(ВР) + 1,96 × СП{ln(ВР)}),
де ДІ — довірчий інтервал; ВР — відносний ризик; СП — стандартна похибка.
Результати та обговорення
Середній вік вагітних основної клінічної групи становив 26,2 ± 3,7 року, групи порівняння — 26,3 ± 3,3 року відповідно. Серед жінок основної групи перша вагітність була в 16 пацієнток (51,6 %), у групі порівняння — у 15 (50,0 %) вагітних жінок відповідно. Згідно з аналізом анамнестичних даних нами було виявлено, що у вагітних основної групи відзначались сечокам’яна хвороба та гіперкристалурія у 26 випадках (83,9 %), хронічний цистит — у 6 жінок (19,3 %), хронічний пієлонефрит — у 4 (12,9 %) вагітних, поєднання патологій — у 5 (16,1 %) жінок із загрозливим викиднем. У групі порівняння супутня патологія сечовидільних шляхів була такою: сечокам’яна хвороба та гіперкристалурія — 29 вагітних жінок (96,7 %), хронічний цистит та хронічний пієлонефрит — по 6 (20,0 %) жінок із загрозливим викиднем. Отже, групи були репрезентативні щодо віку та супутньої патології сечовидільних шляхів.
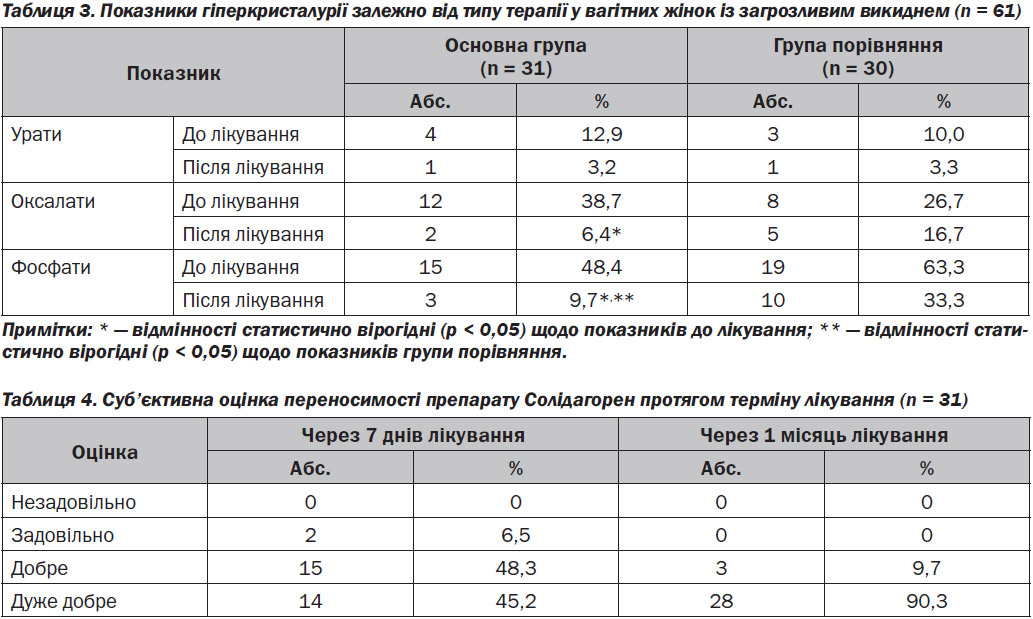
Розподіл скарг у жінок основної групи та групи порівняння на початку дослідження й у динаміці лікування подано на рис. 1.
На момент звернення до лікувального закладу по 10 вагітних жінок з основної групи (32,2 %) та групи порівняння (33,3 %) мали помірні та значні болі під час сечовипускання. Полакіурія відзначалась у 9 вагітних із загрозливим викиднем з основної групи (29,0 %) проти 8 у групі порівняння (26,6 %). На виражені болі внизу живота скаржились по 12 пацієнток з основної групи (38,7 %) та групи порівняння (40,0 %). Болі в попереку різного ступеня інтенсивності непокоїли 14 вагітних жінок з основної групи нашого проспективного дослідження (45,2 %) та 15 — із клінічної групи порівняння (50,0 %).
Після 3 днів терапії скарги на дизуричні розлади (помірної та слабкої інтенсивності) вказували 9 пацієнток, які додатково отримували Солідагорен (29,0 %), тоді як у групі порівняння 10 пацієнток скаржились на виражені та помірні болі під час сечевипускання (33,3 %), ВР = 0,87, ДІ 95% 0,41–1,84, р = 0,78. За симптомом полакіурії відмінність між основною та групою порівняння на 4-ту добу лікування становила: ВР = 0,97, ДІ 95% 0,42–2,24, р = 0,94.
На збереження болю внизу живота після трьох діб терапії вказували 10 жінок (32,2 %), які додатково отримували Солідагорен (біль помірний та слабкий).
Болі внизу живота (слабкі, помірні та виражені) відзначали 12 вагітних жінок із групи порівняння (40,0 %): ВР = 1,07, ДІ 95% 0,54–2,16, р = 0,84.
Біль у попереку відзначали 8 пацієнток основної групи (25,8 %) проти 12 (40,0 %) у групі порівняння: ВР = 0,86, ДІ 95% 0,40–1,84, р = 0,70.
На 8-му добу після початку лікування показники відмінності між основною та групою порівняння становили: ВР = 0,39, ДІ 95% 0,08–1,84, р = 0,23 (за дизуричними розладами), ВР = 0,32, ДІ 95% 0,07–1,47, р = 0,14 (за полакіурією) та ВР = 0,12, ДІ 95% 0,02–0,91, р = 0,04 (за випадками болю в попереку). Жодного випадку болю чи дискомфорту внизу живота не було визначено у вагітних, які додатково приймали Солідагорен. У групі порівняння на 8-му добу від початку лікування на біль внизу живота (дискомфорт та помірний біль) продовжували скаржитись 7 жінок (23,3 %).
За динамікою зменшення або зникнення больового синдрому спостерігалася вірогідне зменшення випадків болю у вагітних жінок, які отримували Солідагорен, проти пацієнток групи порівняння на 5-ту добу від початку лікування: ВР = 0,24, ДІ 95% 0,09–0,64, р = 0,004.
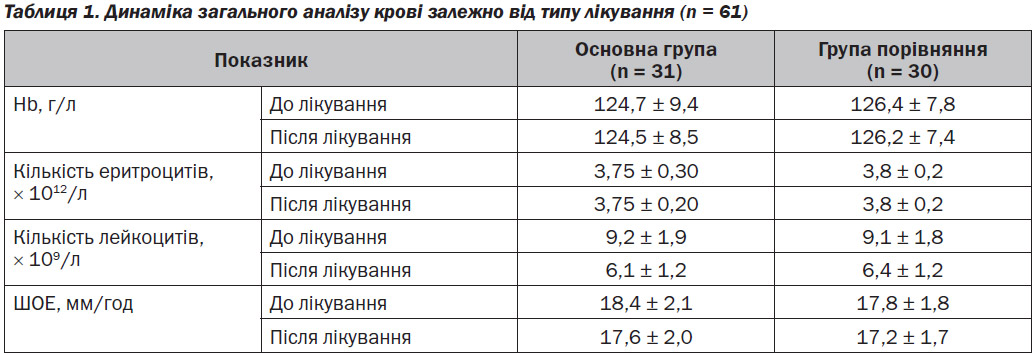
При дослідженні загального аналізу крові в динаміці отримані результати не мали статично вірогідної відмінності як в основній групі дослідження (додатково отримували Солідагорен), так й в групі порівняння (табл. 1). Також ми не знайшли будь-якої відмінності між групами дослідження (р > 0,05).
Хотілося б відзначити відносне зменшення кількості лейкоцитів у загальному аналізі крові за час проведення терапії, хоча й початкові показники були в межах референтних значень.
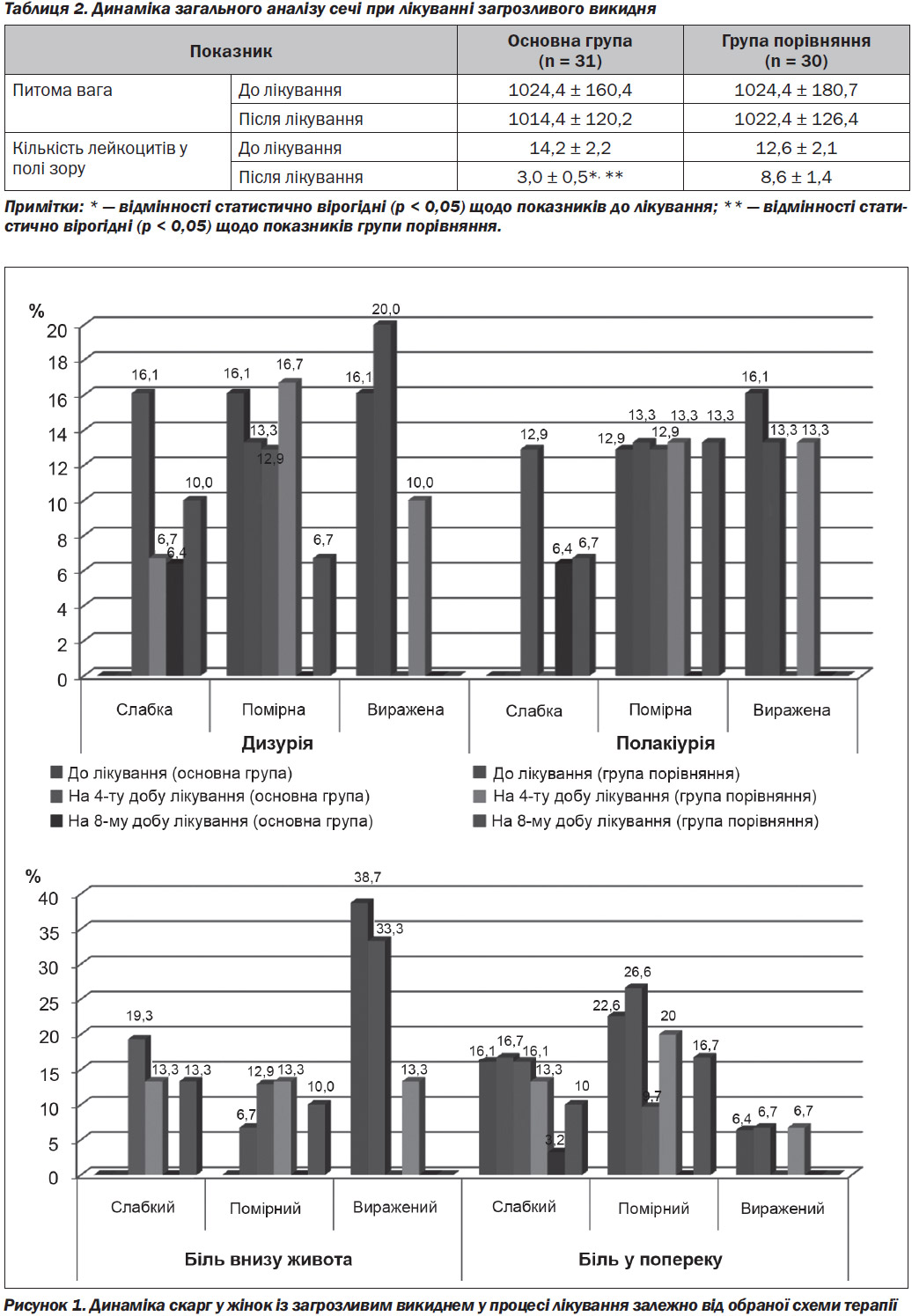
Згідно з результатами загального аналізу сечі, після лікування з додаванням Солідагорену відзначалося вірогідне зниження (р < 0,05) лейкоцитурії в пацієнток основної групи (табл. 2), при цьому кількість лейкоцитів (3,0 ± 0,5 у полі зору) у сечі була знижена не лише щодо початкових показників (14,2 ± 2,2 у полі зору), але й щодо аналогічних результатів в групі порівняння (8,6 ± 1,4 у полі зору). Щодо показника питомої ваги вірогідної різниці виявлено не було, однак після лікування з додаванням Солідагорену питома вага дещо знижувалась, що, можливо, пов’язано з діуретичною дією препарату. Протеїнурія не була виявлена в жодної жінки основної та групи порівняння.
Що стосується динаміки гіперкристалурії, то внаслідок додаткової терапії Солідагореном даний показник знизився у вагітних пацієнток основної групи (табл. 3).
Отримані результати показують, що після терапії Солідагореном в основній групі відбувалися вірогідні зміни щодо виявлення оксалатів та фосфатів (р < 0,05). До того ж відзначалось вірогідне зменшення частоти фосфатурії відносно групи порівняння: ВР = 0,29, ДІ 95% 0,09–0,95, р = 0,04.
За результатами УЗД нирок та сечовидільних шляхів структурних змін не було виявлено в жодної жінки основної та групи порівняння, конкременти менше від 2 мм виявлені у 18 вагітних (58,1 %) основної групи та 16 (53,3%) групи порівняння.
Нами також було проведено спостереження за жінками обох груп протягом наступних 8 тижнів після лікування. При цьому в основній групі в жодному випадку не відмічено рецидиву патології сечостатевої системи, 2 (6,5 %) вагітні були госпіталізовані з діагнозом загрозливого викидня на підставі змін з боку шийки матки при цервікометрії. Жодна жінка основної групи протягом терміну спостереження не мала скарг на дизуричні явища та больовий синдром. У групі порівняння протягом наступних 8 тижнів 14 жінок (46,7 %) відмітили дизуричні явища, 7 (23,3 %) — болі внизу живота, 6 (20,0 %) — болі в попереку та крижах. У 3 жінок (10 %) групи порівняння виникло загострення хронічного циститу, в 1 (3,3 %) — загострення хронічного пієлонефриту, що вимагало госпіталізації з подальшим етіопатогенетичним лікуванням.
Оцінка переносимості препарату показала, що на початку дослідження 1 жінка (3 %) з 33 відмітила значну нудоту після прийому препарату, 1 жінка (3 %) з 33 — посилення болів у попереку, внаслідок чого пацієнтки були виключені з дослідження, потребували дообстеження та зміни терапії.
Суб’єктивна оцінка переносимості препарату вагітними протягом лікування подана в табл. 4.
Усі пацієнтки основної клінічної групи відзначили добру безпеку та переносимість препарату: побічних ефектів і алергічних реакцій, які вимагали б відміни Солідагорену, за час спостереження відзначено не було. Щодо переносимості: препарату 3 жінки відзначили переносимість як добру через запах Солідагорену.
Висновки
1. Призначення фітопрепарату Солідагорен у комплексній терапії загрозливого викидня в жінок із хронічними захворюваннями сечовидільних шляхів значно покращує ефективність лікування.
2. Використання Солідагорену сприяло зменшенню проявів больового синдрому на 5-ту добу терапії: ВР = 0,24, ДІ 95% 0,09–0,64, р = 0,004 проти показників групи, у якій вказана терапія не проводилась.
3. При терапевтичному використанні Солідагорену відзначалось вірогідне зниження випадків лейкоцитурії (р < 0,05) як щодо початкових показників, так і щодо результату в групі порівняння.
4. Застосування препарату Солідагорен зумовлює зменшення числа випадків гіперкристалурії, особливо фосфатурії: ВР= 0,29, ДІ 95% 0,09–0,95, р = 0,04.
5. Прийом Солідагорену продемонстрував добру переносимість та безпеку його застосування, що виявлялося у відсутності побічних ефектів у пацієнток основної групи.
1. Медведь В.І. Неускладнені інфекції сечових шляхів у вагітних / В.І. Медведь, Л.Є. Туманова // Український медичний вісник. — 2007. — № 3(13).
2. Орджоникидзе К.В. Профилактика и лечение осложнений у беременных и родильниц с заболеваниями мочевыводящих путей / К.В. Орджоникидзе, С.Б. Петрова, А.И. Емельянова // Акушерство и гинекология. — 2009. — № 6. — С. 41-45.
3. Хилькевич Е.Г. Возможности фитотерапии при инфекции мочевых путей в акушерской практике / Е.Г. Хилькевич // Акушерство и гинекология. — 2011. — № 5. — С. 115-119.
5. Серов В.Н. Оценка опыта применения комбинированного растительного лекарственного препарата у беременных: Информационное письмо / В.Н. Серов, И.И. Баранов, Л.В. Ткаченко. — М., 2012. — 19 с.
6. Пасієшвілі Н.М. Оптимізація лікування сечових інфекцій у вагітних / Н.М. Пасієшвілі // Медицина неотложных состояний. — 2013. — № 5. — С. 92-95.
7. Наказ МОЗ України від 15. 07. 2011 р. № 417 «Про організацію амбулаторної акушерсько-гінекологічної допомоги в Україні».
8. Наказ МОЗ України від 03.11.2008 № 624 «Про внесення змін до наказу МОЗ України від 15 грудня 2003 року № 582 «Про затвердження клінічних протоколів з акушерської та гінекологічної допомоги», наказу МОЗ від 31.12.2004 року № 676 «Про затвердження клінічних протоколів з акушерської та гінекологічної допомоги».
9. Савустьяненко А.В. Применение золотарника обыкновенного, хвоща полевого и лапчатки гусиной (Солидагорен®) для лечения заболеваний мочевыводящих путей // Новости медицины и фармации в Украине. — 2015. — № 6(535). — С. 12-17.
10. Матайс К. Фитотерапевтическое лечение заболеваний почек и мочевыводящих путей / К. Матайс, С. Матайс // Acta medica empirica. — 1988. — № 4.
11. Хусс К. Препарат золотарника для лечения заболеваний мочевых путей / К. Хусс // Naturamed. — 1989. — № 12. — C. 730-735.
12. Черненко Д.В., Черненко В.В. Клінічна ефективність комбінованої терапії пацієнтів із сечокам’яною хворобою з використанням препарату Солідагорен // Здоровье мужчины. — 2016. — № 2. — С. 33-38.
13. Кирильчук М.Є., Ісламова О.В. Безсиптомна бактеріурія вагітних — фактор ризику перинатальних ускладнень. м. Київ.
14. Черненко В.В., Черненко Д.В., Клюс А.Л. Фитопрофилактика рецидивного нефролитиаза // Medical Nature. — 2010. — № 3. — С. 32-33.
15. Бойко А.И. Опыт применения комбинированной фитотерапии у больных с уретеролитиазом // Почки. — 2013. — № 1(03).
16. Никитин О.Д. Фитотерапия хронического рецидивирующего бактериального цистита // Семейная медицина. — 2015. — № 3(59). — С. 14-18.
17. European Goldenrod // Herbal Medicines. — 2013. — 4th edition. — 928 p.
18. Assessment report on Soidago virgaurea L. herba // European Medicines Agency. — 2008.
19. International clinical practice guidelines for the treatment of acute uncomplicated cystitis and pyelonephritis in women: A 2010 update by the Infectious Diseases Society of America and the European Society / Gupta K., Hooton T.M., Naber K.G. et al. // Clin. Infect. Dis. — 2011. — Vol. 52, № 5. — P. e103–e120. doi:10.1093/cid/ ciq257
20. Thiem B., Goślińska O. Antimicrobial activity of Solidago virgaurea L. from in vitro cultures // Fitoterapia. — 2002. — Vol. 73, № 6. — P. 514-516.
21. Koŀodziej B., Kowalski K., Kędzia B. Antibacterial and antimutagenic activity of extracts aboveground parts of three Solidago species: Solidago virgaurea L., Solidago canadensis L. and Solidago gigantea Ait // Journal of Medicinal Plants Research. — 2011. — Vol. 5, № 31. — P. 6770-6779.
22. Strehl E., Schneider W., Elstner E.F. Inhibition of dihydrofolate reductase activity by alcoholic extracts from Fraxinus excelsior, Populus tremula and Solidago virgaurea // Arzneimittelforschung. — 1995. — Vol. 45, № 2. — P. 172-173.
23. Study of the antiinflammatory activity of Populus tremula, Solidago virgaurea and Fraxinus excelsior / El Ghazaly M., Khayyal M.T., Okpanyi S.N., Arens-Corell M. // Arzneimittelforschung. — 1992. — Vol. 42. — P. 333-336.
24. Wagener H.H. Zur Pharmakologie eines Solidago Extrakthaltigen Venenmittels // Arzneimittelforschung. — 1966. — Vol. 16. — P. 859-866.