Журнал «Медицина неотложных состояний» №6(93), 2018
Вернуться к номеру
Результаты индивидуализированной химиотерапии у больных саркомой мягких тканей
Авторы: Коноваленко В.Ф.(1), Лисовенко Г.С.(1), Волков И.Б.(2), Литвиненко А.А.(2), Кобысь В.Л.(3), Рыжов А.Ю.(4), Проценко В.В.(5), Коноваленко С.В.(1)
(1) — Институт экспериментальной патологии, онкологии и радиобиологии им. Р.Е. Кавецкого НАН, г. Киев, Украина
(2) — Национальный институт рака МЗ Украины, г. Киев, Украина
(3) — Киевский городской клинический онкологический центр МЗ Украины, г. Киев, Украина
(4) — Киевский национальный университет имени Тараса Шевченко, г. Киев, Украина
(5) — ГУ «Институт травматологии и ортопедии НАМН Украины», г. Киев, Украина
Рубрики: Медицина неотложных состояний
Разделы: Клинические исследования
Версия для печати
Вивчено результати лікування 341 хворого на саркому м’яких тканин. Вони були розподілені на 2 групи: основну групу становив 121 пацієнт, який отримав комбіновану терапію з використанням хіміопрепаратів, попередньо підібраних за ефективністю в тесті in vitro; контрольну — 220 хворих на саркому м’яких тканин із порівнянними прогностичними характеристиками, які отримували стандартну хіміотерапію. Отримано дані про вірогідне підвищення показників загальної й безрецидивної виживаності в пацієнтів з індивідуалізацією хіміотерапії.
Изучены результаты лечения 341 больного саркомой мягких тканей. Они были разделены на 2 группы: основную группу составил 121 пациент, получивший комбинированную терапию с использованием химиопрепаратов, предварительно подобранных по эффективности в тесте in vitro; контрольную — 220 больных саркомой мягких тканей с сопоставимыми прогностическими характеристиками, которые получали стандартную химиотерапию. Получены данные о достоверном повышении показателей общей и безрецидивной выживаемости у пациентов с индивидуализацией химиотерапии.
The results of treatment in 341 patients with soft tissue sarcoma were studied. They were divided into 2 groups: the main group consisted of 121 patients who received combination treatment with chemotherapeutic agents previously selected in terms of the effectiveness in in vitro test; controls — 220 patients with soft tissue sarcoma with comparable prognostic characteristics who received standard chemotherapy. Data were obtained about a reliable increase in the rates of total and disease-free survival in patients with individualized chemotherapy.
саркома м’яких тканин; хіміотерапія; чутливість до хіміопрепаратів; клінічна ефективність
саркома мягких тканей; химиотерапия; чувствительность к химиопрепаратам; клиническая эффективность
soft tissue sarcoma; chemotherapy; sensitivity to sensitivity to chemotherapeutic agents; clinical efficacy
Введение
Саркомы мягких тканей (СМТ) — гетерогенная группа заболеваний, имеющих мезенхимальное и нейроэктодермальное происхождение, они составляют 0,5–2,0 % от всех впервые выявленных злокачественных новообразований, в равной степени поражают мужчин и женщин, чаще в возрасте 20–50 лет. Они отличаются агрессивным клиническим течением, быстрым инфильтрирующим ростом, стертостью границ между опухолью и окружающими тканями, упорным многократным рецидивированием и ранним метастазированием [1, 2]. Так, из всех больных с СМТ, впервые госпитализированных в онкологические учреждения, с рецидивами поступают почти 80 % [3].
Большинством авторов признается преимущество комбинированного подхода к лечению данных групп опухолей, при этом выбор терапии должен быть индивидуализирован и основан на ряде факторов, в первую очередь морфологическом строении опухоли и ее биологических характеристиках, а также состоянии пациента [2, 4]. Химиотерапия в настоящее время используется как в комплексном лечении, так и в качестве самостоятельного метода у больных с метастазами СМТ в другие органы. Для пациентов с распространенным процессом системная терапия все еще является паллиативной, однако может продлить выживаемость, улучшить общее состояние и качество жизни [4–6].
Следует признать, что разработка адекватных методов лечения СМТ существенно затруднена в связи c резистентностью и редкостью отдельных неоплазий [7–9]. Чувствительность опухолей разных органов и тканей к определенному препарату может колебаться в чрезвычайно широких границах, при этом большинство СМТ резистентны к действию цитостатиков [10]. Результаты полихимиотерапии рецидивных сарком менее оптимистичны из-за первичной или приобретенной резистентности опухолевых клеток к множеству цитостатических и цитотоксических препаратов, поэтому выбор пациентов, чувствительных к проведению химиотерапевтического лечения, является предметом современных клинических исследований [11, 12].
Методы индивидуальной оценки лекарственной чувствительности и устойчивости на сегодняшний день в повседневной медицинской практике широко не используются. Однако их преимущества в прогнозировании ответа опухолей на терапию, как и предпочтительность продиктованных in vitro персонифицированных режимов перед конвенциальными, активно обсуждаются [13–16]. Это диктуется растущим пониманием необходимости перехода от существующей групповой к персонифицированной комплексной терапии, которая имеет больше шансов на успех, чем стандартная, поскольку задействованные в канцерогенезе гены и их продукты отличаются не только типом и степенью злокачественности опухолей, но и персональными особенностями организма пациента [17, 18]. Их учет становится доминирующей стратегией в онкотерапии.
В равной мере к тому же побуждают как многофакторная общая медикаментозная, так и перекрестная резистентность новообразований, подверженная изменениям в ходе их развития, курации и представляющая одну из сложных проблем онкопатологии [7, 9, 13]. Отсюда определение химиочувствительности in vitro в сочетании с другими показателями (клинической картиной течения заболевания, результатами цитоморфологического, биохимического, молекулярно-генетического анализов) видится как магистральная линия повышения эффективности противоопухолевой терапии.
Перечисленные обстоятельства инициировали создание множества методов определения лекарственной чувствительности опухолевых клеток и прогнозирования их реакции на химиотерапию [15, 19, 20]. C этой целью разрабатываются различные методы: клонирование клеток первичных опухолей или метастазов в полужидком агаре или агаровых диффузионных камерах; трансплантация опухолевых клеток бестимусным мышам, под капсулу почки — линейным мышам; оценка уровня Р-гликопротеина опухолевых клеток; тетразолиевый тест; радионуклидный и антипролиферативный тесты и др. [14, 16, 17, 19].
Различаясь по принципиальным подходам, ориентирам и технологиям исполнения, они, тем не менее, включают одни и те же базовые принципы: выделение клеток из образцов опухолей, инкубацию посевов с химиопрепаратами, оценку выживаемости, митотического, клоногенного потенциала, ферментативной активности и интерпретацию полученных данных. Неся в себе позитивные моменты, рассмотренные методы вместе с тем связаны с техническими и теоретическими проблемами, требующими решения.
Таким образом, среди нескольких лекарств предполагаемо одинаковой эффективности тесты in vitro позволяют произвести выбор определенного химиотерапевтического средства, которое является наиболее эффективным для лечения конкретного пациента. Но, несмотря на значительную прогностическую ценность тестов in vitro, их широкое применение в клинике представляется весьма проблематичным из-за длительности их проведения и методических трудностей. Поэтому в настоящее время сохраняется потребность в разработке эффективных, краткосрочных, достаточно простых и нетрудоемких тестов.
Это побудило многих авторов обратиться к наиболее простому по исполнению, оперативному, относительно дешевому и вместе с тем не уступающему по чувствительности способу индикации лекарственной цитотоксичности, каковым является анализ эксклюзии красителя (dye exclusion assay) [13, 14, 16, 20]. Он исходит из принципа непроницаемости цитоплазматической мембраны нормальных клеток для специфических витальных красителей и утраты этой способности клетками, пострадавшими в результате дезинтеграции плазмалеммы. Анализ относительно скор, прост, малозатратен, обходится небольшим количеством клеток и при соблюдении ряда условий гарантирует достаточную результативность.
Особый интерес представляет прямое сопоставление результатов, полученных in vitro, с данными клинической химиотерапии.
Целью нашей работы была оценка эффективности использования химиопрепаратов, предварительно отобранных в тесте in vitro, у больных с СМТ.
Материалы и методы
Мы модифицировали способ оценки и отбора противоопухолевых химиопрепаратов для больных СМТ, используя метод агаровых капилляров в применении к биопсийному материалу [20, 21]. Метод нетрудоемкий, время тестирования составляет 24 часа, при этом может использоваться как операционный, так и биопсийный материал (5–10 мг живой опухолевой ткани, помещенной в питательную среду).
В исследование был включен 341 больной СМТ, все они проходили лечение в Национальном институте рака МЗ Украины в 2000–2003 гг. Основную группу составил 121 пациент, у них использовали химиопрепараты, предварительно отобранные тестированием in vitro, контрольную — 220 пациентов, получавших стандартную химиотерапию согласно протоколу без индивидуальной оценки чувствительности их опухоли к воздействию цитотоксических препаратов.
В основной группе было 58 (47,93 ± 4,54 %) мужчин и 63 (52,07 ± 4,54 %) женщины; в контрольной группе — 102 (46,36 ± 3,36 %) мужчины и 118 (53,64 ± ± 3,36 %) женщин. Средний возраст пациентов основной группы составил 38,9 ± 1,4 года, в контрольной — 42,9 ± 1,2 года при абсолютно одинаковых минимальных (8 лет) и максимальных (72 года) значениях. Более детальные данные о возрастной структуре основной и контрольной групп, а также локализации первичной опухоли представлены в табл. 1.
Важной является информация о локализации заболевания у пациентов с СМТ высокой степени риска. В обеих группах наиболее часто местом развития опухоли были нижние конечности — 72 случая (59,50 ± 4,46 %) в основной группе и 141 (64,09 ± 3,23 %) — в контрольной, среди них доминировали опухоли бедра — у 51 (42,15 ± 4,49 %) и 84 (38,18 ± 3,28 %) пациентов основной и контрольной групп соответственно. По возрасту и локализации первичной опухоли различия между группами были статистически не значимы (p > 0,05).
Анализ распределения опухолей по нозологическим формам в изучаемых группах пациентов представлен в табл. 2.
Суммируя вышеприведенные данные, можно сделать вывод, что по основным характеристикам основная и контрольная группа больных СМТ были сопоставимыми (p > 0,05).
Статистический анализ данных проводили, используя программу StatSoft Statistica 6.1. Для сравнения выживаемости в основной и контрольной группах использовали двусторонний log-rank тест. Статистический анализ достоверности полученных данных проводили с помощью t-критерия Стьюдента. Различия между величинами считались достоверными при р < 0,05.
Результаты и обсуждение
Анализ отдаленных результатов у больных СМТ в основной и контрольной группах показал тенденцию к повышению безрецидивной выживаемости в основной группе спустя 3 и больше года, тогда как в первые 2 года достоверных различий не наблюдалось (рис. 1А).
Так, показатель 3-летней безрецидивной выживаемости в основной группе составил 33,60 ± ± 4,40 %, в контрольной — 23,5 ± 2,9 %; 5-летней — 25,4 ± 4,1 % и 13,16 ± 2,31%; 8-летней — 14,9 ± 3,9 % и 3,70 ± 1,45 % соответственно (p < 0,05).
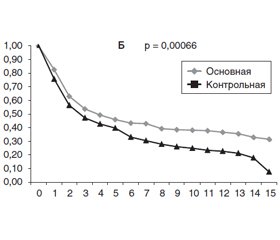
Что касается показателя общей выживаемости (рис. 1Б; табл. 3), то в первые пять лет наблюдалась лишь тенденция к его возрастанию в основной группе, тогда как начиная с 6-го года разница с контрольной группой стала статистически существенной.
Нами получены данные о достоверном повышении показателей общей и безрецидивной выживаемости больных CМТ при индивидуализации химиотерапии, основанной на предварительном тестировании биопсийного материала in vitro (с контрольной группой р = 0,00066 и р = 0,0054 соответственно). В доступной литературе мы не встретили подобных данных по СМТ. Что касается других онкологических заболеваний, то обнадеживающие результаты были получены К. Fujita et al. [22] при использовании для тестирования микротетразолиевого теста у больных раком желудка, которых после операции лечили химиопрепаратами, подобранными по эффективности в тесте in vitro. K.H. Link et al. [23] при региональной химиотерапии опухолей печени также использовали препараты, отобранные индивидуально с помощью колониеформирующего теста, и показали, что определенная in vitro чувствительность опухолевых клеток коррелировала с лучшей эффективностью подобранного химиопрепарата in vivo. Еще более высокие результаты индивидуализированной химиотерапии были достигнуты при использовании метода подкапсульной ксенотрансплантации [24].
Выводы
Таким образом, некоторые авторы показали преимущества методов персонифицированного определения химиочувствительности перед стандартной химиотерапией и, опираясь на высокую корреляцию культуральных ответов с клиническими (реакция опухолей, протяженность безрецидивного и общего выживания), высказались в поддержку развития методов таргетированного подхода [7, 13, 14, 16, 22, 25, 26]. Другие исследователи не смогли выявить преимуществ методов индивидуальной оценки химиочувствительности перед протокольными и заняли отрицательную позицию [27, 28]. Отсюда проистекает известная сдержанность в общей оценке проблемы. Отсутствие полной корреляции между данными, полученными in vitro и in vivo, по-видимому, объясняется тем, что в системе in vitro невозможно смоделировать все процессы, протекающие в организме с опухолью. Между тем, по мнению онкологов, поскольку персонифицированная стратегия, опирающаяся на культуральные исследования, имеет потенциальную перспективу, право на ее клиническое испытание остается приоритетным.
Конфликт интересов. Авторы заявляют об отсутствии какого-либо конфликта интересов при подготовке данной статьи.
1. Байзаков Б.Т., Шунько Е.Л., Арыбжанов Д.Т. Современные взгляды на методы лечения сарком мягких тканей (обзор литературы) // Современные проблемы науки и образования. — 2012. — № 1. — http://www.science-education.ru/ru/article/view?id=5320.
2. Зубарев А.Л., Кудрявцева Г.Т., Курильчик А.А. и др. Комбинированное лечение распространенных сарком мягких тканей // Саркомы костей, мягких тканей и опухоли кожи. — 2010. — № 2. — С. 35-38.
3. Pervaiz N., Colterjohn N., Farrokhyar F. et al. А systematic meta-analysis of randomized controlled trials of adjuvant chemotherapy for localized resectable soft-tissue sarcoma // Cancer. — 2008. — 113(3). — Р. 573-581.
4. Ravi V., Patel S., Benjamin R.S. Chemotherapy for Soft-Tissue Sarcomas // Oncology (Williston Park). — 2015. — 29(1). — pii: 203348.
5. Frustaci S., Gherlinzoni F., De Paoli A. et al. Adjuvant chemotherapy for adult soft tissue sarcomas of the extremities and girdles: results of the Italian randomized cooperative trial // J. Clin. Oncol. — 2001. — 19 (5). — Р. 1238-1247.
6. Ratan R., Patel S.R. Chemotherapy for soft tissue sarcoma // Cancer. — 2016. — 122(19). — Р. 2952-60.
7. Wang J., Seebacher N., Shi H. et al. Novel strategies to prevent the development of multidrug resistance (MDR) in cancer // Oncotarget. — 2017. — 8(48). — Р. 84559-84571.
8. Frenkel G.D., Caffrey P.B. A prevention strategy for circumventing drug resistance in cancer chemotherapy // Curr. Pharm. Des. — 2001. — 7. — Р. 1595-1614.
9. Kachalaki S., Ebrahimi M., Mohamed Khosroshahi L. et al. Cancer chemoresistance; biochemical and molecular aspects: a brief overview // Eur. J. Pharm. Sci. — 2016. — 89. — Р. 20-30.
10. Алиев М.Д., Мехтиева Н.И., Бохян Б.Ю. Факторы прогноза сарком мягких тканей // Вопр. онкологии. — 2005. — № 51(3). — С. 288-299.
11. Зубарев А.Л., Кудрявцева Г.Т., Курильчик А.А. Комбинированное лечение распространенных сарком мягких тканей // Саркомы костей, мягких тканей и опухоли кожи. — 2010. — № 2. — С. 35-38.
12. Fletcher C.D.M. Recently characterized soft tissue tumors that bring biologic insight // Modern Pathology. — 2014. — 27. — Р. 98-112.
13. Cortazar P., Johnson B. E. Review of the efficacy of individualized chemotherapy selected by in vitro drug sensitivity testing for patients with cancer // J. Clin. Oncol. — 1999. — 17(5). — Р. 1625-1631.
14. Чернов А.Н., Калюнов В.Н., Конопля Н.Е. Разработка варианта метода оценки чувствительности клеток интракраниальных новообразований к химиотерапевтическим препаратам in vitro // Злокачественные опухоли. — 2015. — № 14(3). — С. 40-52.
15. Свирновский А.И. Методологические исследования лекарственной чувствительности лейкозных клеток // Пробл. здоровья и экол. — 2011. — № 3. — С. 89-91.
16. Xu J.M., Song S.T., Tang Z.M. et al. Neoadjuvant chemotherapy in inoperable, locally advanced, and inflammatory breast carcinoma: a pilot study of MTT assay in vitro and outcome analysis of 10 patients // Am. J. Clin. Oncol. — 2001. — 24(3). — Р. 259-263.
17. Sequist L.V., Muzikansky A., Engelman J.A. A new BATTLE in the evolving war on cancer // Cancer Discov. — 2011. — 1(1). — Р. 14-16.
18. Чехун В.Ф. От системной биологии рака до методологии персонализированного лечения // Онкология. — 2012. — № 14(2). — С. 84-88.
19. Banerjee D., Longo-Sorbello G., Saydam J. et al. Cytotoxicity and cell growth assays // Cell Biology, Cell Tissue Culture. — 2006. — Р. 315-324.
20. Потебня Г.П., Шумилина В.В., Лисовенко Г.С. и др. Тестування in vitro чутливостi пухлинних клiтин до хiмiопрепаратiв // Укр. xiмiотерапевтичний журнал. — 2000. — № 2. — С. 26-29.
21. Sakurawa T. Тестирование in vitro чувствительности к препаратам с помощью содержащих агар стеклянных капилляров // Anticancer Res. — 1990. — 10(4). — Р. 1075-1078.
22. Fujita K., Kubota T., Matsuzaki S.W. et al. Further evidence for the value of the chemosensitivity test in deciding appropriate chemotherapy for advanced gastric cancer // Anticancer Res. — 1998. — 18(3B). — Р. 1973-1978.
23. Link K.H., Kornmann M., Leder G.H. et al. Regional chemotherapy directed by individual chemosensitivity testing in vitro: a prospective decision-aiding trial // Сlin. Cancer Res. — 1996. — 2(9). — Р. 1469-1474.
24. Егоров В.В., Чернов В.А., Соколова К.С. Системы in vitro для первичного поиска биологически активных веществ с канцеростатическим действием // Эксперим. онкология. — 1988. — № 10(4). — С. 11-15.
25. Matsuo K., Bond V. K., Eno M. L. et al. Low drug resistance to both platinum and taxane chemotherapy on an in vitro drug resistance assay predicts improved survival in patients with advanced epithelial ovarian, fallopian and peritoneal cancer // Int. J. Cancer. — 2009. — 125(11). — Р. 2721-2727.
26. Samson D.J., Seidenfeld J., Ziegler K. et al. Chemotherapy sensitivity and resistance assays: a systematic review // J. Clin. Oncol. — 2004. — 22(17). — Р. 3618-3630.
27. Hetland T.E., Kaern J., Skrede M. et al. Predicting platinum resistance in primary advanced ovarian cancer patients with an in vitro resistance index // Cancer Chemother. Pharmacol. — 2012. — 69(5). — Р. 1307-14.
28. Jun K.R., Jang S., Chi H.S. et al. Relationship between in vitro chemosensitivity assessed with MTT assay and clinical outcomes in 103 patients with acute leukemia // Korean J. Lab. Med. — 2007. — 27(2). — 89-95.

/69-1.jpg)
/70-1.jpg)