Журнал «Медицина неотложных состояний» №6(93), 2018
Вернуться к номеру
Застосування подовженої епідуральної анестезії в періопераційному періоді при великих резекціях печінки
Авторы: Черній В.І.(1), Колганова К.А.(2), Фрейгофер М.В.(3)
(1) — Державна наукова установа «Науково-практичний центр профілактичної та клінічної медицини» Державного управління справами, м. Київ, Україна
(2) — Державний заклад «Дніпропетровська медична академія Міністерства охорони здоров’я України», м. Дніпро, Україна
(3) — Комунальний заклад «Клінічний онкологічний диспансер Дніпропетровської обласної ради», м. Дніпро, Україна
Рубрики: Медицина неотложных состояний
Разделы: Клинические исследования
Версия для печати
Використано та проаналізовано оптимізовану схему мультимодальної аналгезії в 121 пацієнта в періопераційному періоді великих резекцій печінки з приводу новоутворень. Пацієнти розподілені на 3 групи залежно від методики анестезіологічного забезпечення: загальна, комбінована загальна й епідуральна анестезія. Для оцінки адекватності цієї методики застосований аналіз параметрів центральної гемодинаміки, варіаційної пульсометрії, сироваткових концентрацій кортизолу, глюкози, ступеня вираженості післяопераційного болю, частоти післяопераційних ускладнень. Установлено, що максимально ефективною та безпечною для пацієнтів є схема комбінованої низькопоточної інгаляційної анестезії з епідуральною аналгезією завдяки оптимальним гемодинамічним показникам, мінімальним рівням стресових маркерів та післяопераційного болю, зменшенню частоти ускладнень.
Использована и проанализирована схема мультимодальной аналгезии у 121 пациента в периоперационном периоде обширных резекций печени. Пациенты распределены на 3 группы в зависимости от методики анестезиологического обеспечения: общая, комбинированная общая и эпидуральная анестезия. Для оценки адекватности этой методики использован анализ параметров центральной гемодинамики, вариационной пульсометрии, сывороточных концентраций кортизола, глюкозы, степени выраженности послеоперационной боли, частоты послеоперационных осложнений. Установлено, что максимально эффективной и безопасной для пациентов является схема комбинированной низкопоточной ингаляционной анестезии с эпидуральной аналгезией благодаря оптимальным гемодинамическим показателям, минимальным уровням стрессовых маркеров и послеоперационной боли, уменьшению частоты осложнений.
Background. Major liver resections are the gold standard of medical care for patients with hepatocellular carcinoma. Such surgical procedure are traumatizing and cause massive nociceptive stimulation, intraoperative bleeding, total hypothermia. This requires using effective analgesic techniques and quality anesthesia control at all stages of anesthesia. The objective of the work was to improve the efficiency of anesthesia and to assess the adequacy of anesthesia during major liver resections in surgical oncology. Materials and methods. 121 patients scheduled for liver resections were enrolled in the clinical prospective randomized cohort study. All patients were randomized to one of three groups depending on the anesthesia and postoperative analgesia regimen. The groups were matched for age, sex, diagnosis, anthropometric indicators, nature and duration of operative intervention. The first group of patients (n = 41) underwent general anesthesia (total intravenous anesthesia (TIVA) with propofol and fentanyl) and opioid-based postoperative analgesia (morphine). The second group (n = 40) received thoracic epidural anesthesia (bupivacaine, no opioids) with TIVA (using propofol and fentanyl). The low-flow volatile regimen with sevoflurane combined with prolonged thoracic epidural bupivacaine analgesia was administered to the third group of patients (n = 40). Thromboprophylaxis with anticoagulants (bemiparin and enoxaparin) was started the day before liver resection and lasted for 10–14 days. The comparative analysis of efficacy and safety of described regimens has been made with important indicators of central hemodynamics, cardiac rhythm variability, serum cortisol concentration, glycemia, postoperative morbidity, clinical indicators of postoperative recovery period. Duration of mandatory mechanical ventilation, pain intensity by visual analog scale (VAS), level of sedation by the Richmond agitation-sedation scale (RASS), the duration of postoperative ileus, length of hospital stay, the incidence of complications were registered in the early postoperative period. Analyzing the research results, methods of biostatistics were used. Results. Initial parameters of central hemodynamics, heart rhythm variability, glycemia, serum cortisol were not statistically different in all three groups. Sympathetic surge was maximally presented in patients of the group 1 at all stages of liver resection. Parameters of mean arterial pressure, heart rate, total peripheral vascular resistance, heart rate variability (LF/HF), glycemia and cortisol were increased in the first group. During the early postoperative period, the quality of anesthesia was higher in patients with epidural anesthesia compared to opioid anesthesia. Pain intensity (VAS), hyperglycemia and level of sedation (RASS) were more significant in patients of the group 1 as compared to the groups 2 and 3. The use of epidural anesthesia in patients of the groups 2 and 3 compared with the group 1was found to reduce opioid and muscle relaxant consumption during surgery, to decrease the duration of mandatory lung ventilation, to start postoperative enteral feeding and to activate patients earlier, to reduce length of hospital stay and morbidity rate. Pleural effusions after liver resection were diagnosed in 2 patients (4.9 ± 3.4 %) of the group 1, one patient (2.5 ± 2.5 %) of the group 2 (p = 0.37), and subphrenic abscesses — in 6 patients (14.6 ± 5.5 %) of the group 1 (p = 0.002). Conclusions. Implementation of low flow sevoflurane anaesthesia combined with prolonged thoracic epidural analgesia prevents sympathetic surge, suppresses surgical stress response and improves recovery after major liver resections in surgical oncology.
епідуральна анестезія; резекції печінки; періопераційне знеболювання; оцінка адекватності
эпидуральная анестезия; резекции печени; периоперационное обезболивание; оценка адекватности
epidural anesthesia; liver resection; perioperative anesthesia; adequacy assessment
Вступ
Протягом останніх років у світі відзначається тенденція до зростання захворюваності та летальності від новоутворень печінки. Радикальне оперативне лікування раку печінки є золотим стандартом медичної допомоги та найчастіше єдиним шансом для пацієнта [1]. У зв’язку з прогресивним розвитком онкохірургії відбуваються постійне розширення показань та збільшення обсягів оперативних втручань [2]. Резекції печінки, що виконуються за загальноприйнятими принципами абластики, відзначаються великою травматичністю, супроводжуються значною крововтратою та мають вкрай високий рівень операційного стресу через масивну ноцицептивну стимуляцію. Післяопераційний період характеризується вираженим больовим синдромом та респіраторними ускладненнями через здійснення хірургами під час операції поперечного доступу до печінки за Calne «мерседес» із перетином більшості м’язів черевного пресу та порушенням біомеханіки дихання [1, 3]. Все це вимагає максимального використання різноманітних анестезіологічних методик для забезпечення високоякісного знеболювання на всіх етапах лікування та реабілітації хворих [4, 5]. Згідно з даними сучасних клінічних досліджень, адекватний захист пацієнта від хірургічної агресії забезпечують методики, що засновані на принципі мультимодальної аналгезії, та регіонарні техніки анестезії [3, 6, 7]. Під час вивчення проблеми вибору оптимальної схеми анестезії під час резекцій печінки [8, 9] неможливо не звернути увагу на необхідність проведення постійної оцінки адекватності анестезіологічного забезпечення [10–13] та якості знеболювання пацієнтів у періопераційному періоді [14–16].
Мета дослідження — підвищення ефективності анестезії й оцінка адекватності знеболювання під час та після великих резекцій печінки з приводу новоутворень.
Матеріали та методи
У проспективне рандомізоване когортне дослідження, що було проведено на базі відділення анестезіології ККЛПЗ «Донецький обласний протипухлинний центр» м. Донецька протягом 2009–2013 рр., увійшли пацієнти (n = 121) із новоутвореннями печінки віком від 18 до 78 років, у яких виконували
планові резекції печінки в такому обсязі: від сегментектомій до поширених гемігепатектомій. Усі хворі розподілені на 3 групи залежно від методики анестезії та післяопераційного знеболювання: 1-ша — загальна збалансована внутрішньовенна анестезія (total intravenous anaesthesia — TIVA) зі штучною вентиляцією легень (ШВЛ), 2-га — TIVA з ШВЛ у комбінації з подовженою грудною епідуральною аналгезією (ПГЕА); 3-тя — низькопоточна інгаляційна анестезія (low flow anaesthesia — LFA) у комбінації з ПГЕА. З метою рандомізації дослідження розподіл пацієнтів на групи здійснювався за допомогою таблиці випадкових чисел. Групи зіставні за віком, статтю, основним та супутнім діагнозами, характером та обсягом оперативного втручання, вихідним соматичним статусом (табл. 1, 2). Критерії виключення пацієнтів із дослідження: гіпертонічна хвороба 3-ї стадії, серцева недостатність 2–3-го ступеня, бронхіальна астма з дихальною недостатністю, цукровий діабет, цироз печінки 2–3-ї стадії за шкалою Чайлда — П’ю.
Групи відрізнялися між собою за особливостями анестезії та післяопераційного знеболювання. Пацієнтам всіх трьох груп призначали стандартну премедикацію за 30 хвилин до операції: М-холінолітики (атропін 0,015 мг/кг внутрішньовенно), антигістамінні препарати (димедрол 0,15 мг/кг внутрішньовенно), транквілізатори (діазепам 0,15 мг/кг внутрішньовенно). Відмінності між групами подано в табл. 3.
Аналгетичним компонентом премедикації в 1-й групі пацієнтів були опіоїди (морфін 0,15 мг/кг внутрішньовенно). З метою запобігаючої аналгезії у 2-й і 3-й групах за 30 хвилин до розрізу шкіри вводили нестероїдні протизапальні засоби (НПЗЗ) (декскетопрофен 0,7 мг/кг внутрішньовенно) і блокатори N-метил-D-аспартат (NMDA)-рецепторів (кетамін 0,5 мг/кг внутрішньовенно). Індукція анестезії не відрізнялася в усіх групах і здійснювалася внутрішньовенними гіпнотиками (пропофол 2 мг/кг або тіопентал натрію 5 мг/кг) й опіоїдами (фентаніл 8 мкг/кг).
Підтримка анестезії та її аналгетичний компонент відрізнялися в усіх групах. У 1-й групі хворих (n = 41) проводили TIVA з використанням пропофолу (1,5–2,0 мг/кг/год), фентанілу (3–6 мкг/кг/год) зі ШВЛ. Післяопераційна аналгезія досягалася парентеральним введенням морфіну в добовій дозі 0,4–0,6 мг/кг і НПЗЗ. У 2-й групі хворих (n = 40) проводили TIVA з використанням пропофолу (1,5–2,0 мг/кг/год), кетаміну (0,5 мг/кг/год), фентанілу (0,5–1,5 мкг/кг/год) зі ШВЛ комбінації з ПГЕА 0,125% розчином бупівакаїну (5–20 мг/год). Епідуральне введення 0,125% розчину бупівакаїну відповідно до концепції запобігаючої аналгезії починали за 30 хвилин до розрізу шкіри зі швидкістю 15–20 мг/год. Після введення початкової дози місцевого анестетика через 30–40 хвилин швидкість зменшували до 5–8 мг/год. Пацієнтам 3-ї групи (n = 40) проводили LFA севофлураном (0,8–1,5 об%) у потоці закису азоту з киснем у співвідношенні 1 : 1 у комбінації з ПГЕА 0,125% розчином бупівакаїну (5–15 мг/год). У післяопераційному періоді хворим 2-ї і 3-ї груп проводили ПГЕА 0,25–0,5% розчином бупівакаїну зі швидкістю 5–15 мг/год, яку доповнювали парентеральним введенням декскетопрофену (до 150 мг/доб) й нефопаму (до 60 мг/доб). Пацієнтам усіх груп здійснювали тромбопрофілактику антикоагулянтами, враховуючи високу поширеність тромбоемболічних ускладнень в онкологічній практиці.
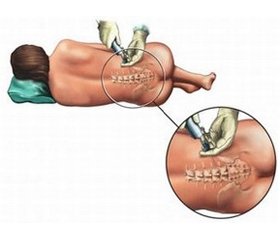
Методика катетеризації епідурального простору була такою. Напередодні оперативного втручання в умовах відділення інтенсивної терапії після проведення предилюції кристалоїдними плазмозамінниками в об’ємі до 15 мл/кг здійснювали пункцію та катетеризацію епідурального простору. В асептичних умовах під місцевою анестезією 0,5% розчином лідокаїну в положенні хворого лежачи на боці на рівні остистих відростків 8–10-го грудних хребців виконували пункцію епідурального простору з медіанного доступу. Катетер проводили краніально на 5 см, після аспіраційної проби вводили тест-дозу — 3 мл 2% розчину лідокаїну, фіксували асептичною пов’язкою та лейкопластиром. Після аналізу даних вітчизняних і зарубіжних літературних джерел вироблена така тактика встановлення та видалення епідурального катетера на фоні постійного введення низькомолекулярних гепаринів (НМГ). За 24 години до операції, вранці напередодні, здійснювали катетеризацію епідурального простору, а за 12 годин до операції, напередодні ввечері, — перше введення профілактичної дози антикоагулянту (еноксапарин 20 мг підшкірно). Таким чином, НМГ вводили після закінчення небезпечного в плані розвитку епідуральної гематоми проміжку часу (12 годин). Далі препарати НМГ призначали одноразово за добу до повної активізації пацієнта. Після відновлення моторної функції шлунково-кишкового тракту і зменшення вираженості больового синдрому, приблизно через 7–10 днів, катетер видаляли, але не раніше ніж через 12 годин від останнього введення НМГ.
Параметри центральної гемодинаміки (ЦГ) (частота серцевих скорочень (ЧСС), середній артеріальний тиск (САТ), сатурація крові киснем (SpO2) та варіабельність серцевого ритму (ВСР)) за методикою Р.М. Баєвського реєстрували до операції, під час інтубації трахеї, розрізу шкіри, резекції печінки, ушивання шкіри і після операції за допомогою реанімаційно-хірургічного монітора UTAS ЮМ-300Т/1. Показники ударного індексу (УІ), серцевого індексу (СІ), загального периферичного опору судин (ЗПОС), індексу доставки кисню (IDO2) визначали розрахунковим методом. Протягом операції в сироватці крові хворих досліджували стресові маркери: концентрації глюкози і кортизолу. Відбір проб крові для аналізу рівня кортизолу здійснювали тричі: до початку операції, під час основного етапу резекції печінки і після ушивання операційної рани, використовували радіоімунний аналіз (РІА-кортизол). Концентрацію глюкози в крові визначали портативним глюкометром Longevita до початку операції, під час розрізу шкіри, на етапі резекції печінки, після ушивання шкіри, в першу, другу, третю добу післяопераційного періоду. У ранньому післяопераційному періоді реєстрували тривалість примусової ШВЛ, інтенсивність болю за візуально-аналоговою шкалою (ВАШ), рівень седації за шкалою седації й ажитації Річмонда (RASS) у балах протягом трьох діб після операції, тривалість парезу шлунково-кишкового тракту, кількість діб, проведених у палаті інтенсивної терапії (ПІТ), частоту ускладнень. При проведенні аналізу результатів дослідження використані методи біостатистики. Розрахунки проводилися на персональному комп’ютері за допомогою програм MedStat і MedCalc.
Результати та обговорення
Доопераційні показники ЦГ, ВСР, глікемії та сироваткової концентрації кортизолу статистично значуще не відрізнялися в групах.
Після початку операції в групах пацієнтів відзначали такі відмінності в показниках хірургічного стресу. На всіх етапах резекцій печінки активація симпатоадреналової системи була максимально вираженою в пацієнтів 1-ї групи, яким проводили TIVA з ШВЛ. Про це свідчать найбільший рівень САТ, ЧСС, ЗПСО та зсув співвідношення ВСР LF/HF у бік симпатичної ланки вегетативної нервової системи (табл. 4). Співвідношення ВСР LF/HF (low frequency/high frequency) відображує симпатовагусний баланс та дорівнює 1,50 ± 0,7 у нормі [3, 4]. Значення СІ статистично значуще не відрізнялося в пацієнтів різних груп протягом операції. Проте використання ПГЕА сприяло поліпшенню стану гемодинаміки шляхом збільшення УІ та зменшення ЧСС і ЗПСО в 2-й і 3-й групах порівняно з TIVA у 1-й групі, де СІ підтримувався шляхом зростання ЧСС при низькому УІ. Менш виражена стрес-обумовлена гемодинамічна реакція в 2-й та 3-й групах може свідчити про більшу знеболюючу потужність комбінованої загальної та нейроаксіальної анестезії. Протягом періопераційного періоду в пацієнтів 3-ї групи зареєстровані оптимальні рівні гуморальних маркерів стресу: значення глікемії в пацієнтів 1-ї групи на етапах резекції печінки статистично значимо перевищувало таке у 2-й та 3-й групах, а сироваткова концентрація кортизолу була мінімальною в 3-й групі та максимальною — в 1-й. Це свідчить про гіперпродукцію гормонів наднирників, що пов’язана з недостатньою адекватністю ізольованої TIVA порівняно з комбінацією ПГЕА та загальної анестезії.
Протягом раннього післяопераційного періоду якість знеболювання була вищою в пацієнтів, яким проводили ПГЕА, порівняно зі знеболюванням опіоїдами. Інтенсивність болю за ВАШ та ступінь пригнічення свідомості були більш виражені в пацієнтів 1-ї групи, ніж у 2-й та 3-й групах (табл. 5). У хворих, які отримували морфін, відзначали гіперглікемію, подовження часу до екстубації трахеї та ШВЛ, пізнє відновлення перистальтики ШКТ, затримку початку ентерального харчування, пізню активізацію і збільшення термінів перебування в ПІТ та стаціонарного лікування (табл. 6).
У дослідженні вивчені структура і частота післяопераційних ускладнень. Ексудативний плеврит після резекцій печінки діагностовано у 2 пацієнтів 1-ї групи (4,9 ± 3,4 %) і в 1 пацієнта 2-ї групи (2,5 ± 2,5 %) (p = 0,37). Виявлено статистично значуще (p = 0,002) розходження між групами за частотою субдіафрагмальних абсцесів. Так, якщо в групі TIVA це ускладнення спостерігали в 6 (14,6 ± 5,5 %) пацієнтів, то в групах із ПГЕА це ускладнення не відмічали. Геморагічні ускладнення, що спостерігались тільки під час операції та були пов’язані з хірургічною тактикою, зареєстровано в 1-й і 2-й групах у 5 (12,2 ± 5,1 %) і 4 (10,0 ± 4,7 %) хворих відповідно. У післяопераційному періоді жодного випадку тромботичних або геморагічних подій зафіксовано не було.
На підставі наведених даних можна дійти висновку про найбільшу адекватність подовженої епідуральної аналгезії бупівакаїном у комбінації з внутрішньом’язовим введенням декскетопрофену й нефопаму порівняно з використанням морфіну парентерально завдяки поліпшенню перебігу відновного періоду та реабілітації пацієнтів після великих резекцій печінки.
Висновки
Таким чином, впровадження в практику схеми мультимодального анестезіологічного забезпечення великих резекцій печінки, що поєднує низькопоточну інгаляційну анестезію севофлураном, подовжену грудну епідуральну аналгезію бупівакаїном та парентеральне застосування ад’ювантів (нефопам та декскетопрофен), дозволило забезпечити максимально ефективний захист пацієнтів від операційного стресу, знизити сумарне фармакологічне навантаження на печінку, скоротити термін подовженої штучної вентиляції легень, проводити високоякісну післяопераційну аналгезію та профілактику респіраторних, тромботичних ускладнень та парезу шлунково-кишкового тракту.
Конфлікт інтересів. Автори заявляють про відсутність конфлікту інтересів при підготовці даної статті.
1. Вишневский В.А., Кубышкин В.А., Чжао А.В., Икрамов Р.А. Операции на печени. — М.: МИКЛОШ, 2008. — 157 с.
2. Заречнова Н.В., Бельский В.А., Загайнов В.Е. и др. Периоперационное сопровождение обширных резекций печени // Эфферентная терапия. — 2009. — 15(1–2). — С. 57-58.
3. Tzimas P., Prout J., Papadopoulos G., Mallett S.V. Epidural anaesthesia and analgesia for liver resection // Anaesthesia. — 2013. — 68(6). — Р. 628-635.
4. Salman N., Durukan A.B., Gurbuz H.A. Comparison of effects of epidural bupivacaine and intravenous meperidine analgesia on patient recovery following elective abdominal aortic surgery // Med. Sci. Monit. — 2013. — 19. — Р. 347-352.
5. Zimmitti G., Soliz J., Aloia T.A., Gottumukkala V., Cata J.P., Tzeng C.W., Vauthey J.N. Positive Impact of Epidural Analgesia on Oncologic Outcomes in Patients Undergoing Resection of Colorectal Liver Metastases // Ann. Surg. Oncol. — 2016. — 23(3). — Р. 1003-1011. doi: 10.1245/s10434-015-4933-1. Epub. 2015, Oct 28.
6. Kampe S., Weinreich G., Darr C., Eicker K., Stamatis G., Hachenberg T. The impact of epidural analgesia compared to systemic opioid-based analgesia with regard to length of hospital stay and recovery of bowel function: retrospective evaluation of 1555 patients undergoing thoracotomy // J. Cardiothorac. Surg. — 2014. — 23(9). — Р. 175. doi: 10.1186/s13019-014-0175-8.
7. Revie E.J., Massie L.J., McNally S.J., McKeown D.W., Garden O.J., Wigmore S.J. Effectiveness of epidural analgesia following open liver resection // HPB (Oxford). — 2011. — 13(3). — Р. 206-211. doi: 10.1111/j.1477-2574.2010.00274.x.
8. Song J.C., Sun Y.M., Yang L.Q. et al. A comparison of liver function after hepatectomy with inflow occlusion between sevoflurane and propofol anesthesia // Anesth. Analg. — 2010. — 111(4). — Р. 1036-1041.
9. Taurá P., Fuster J., Blasi A., Martinez-Ocon J., Anglada T., Beltran J., Balust J., Tercero J., Garcia-Valdecasas J.C. Postoperative pain relief after hepatic resection in cirrhotic patients: the efficacy of a single small dose of ketamine plus morphine epidurally // Anesth. Analg. — 2003. — 96(2). — Р. 475-480. PMID: 12538199.
10. Кирячков Ю.А., Салтанов И.А., Хмелевский Я.М. Компьютерный анализ вариабельности сердечного ритма. Новые возможности для анестезиолога и врачей других специальностей // Вестник интенсивной терапии. — 2002. — 1. — С. 3-8.
11. Різник Л., Пшесмицкі K. Варіабельність серцевого ритму як індикатор вегетативного балансу та глибини наркозу. 20-річний досвід застосування в анестезіології // Біль, знеболювання і інтенсивна терапія. — 2005. — 1. — С. 28-35.
12. Greisen J., Nielsen D.V., Sloth E., Jakobsen C.J. High thoracic epidural analgesia decreases stress hyperglycemia and insulin need in cardiac surgery patients // Acta Anaesthesiol. Scand. — 2013. — 57(2). — Р. 171-177.
13. Kawagoe I., Tajima K., Kanai M. et al. Comparison of intraoperative stress hormones release between propofol-remifentanil anesthesia and propofol with epidural anesthesia during gynecological surgery // Masui. — 2011. — 60(4). — Р. 1324-1327.
14. Nishimori M., Ballantyne J.C., Low J.H. Epidural pain relief versus systemic opioid-based pain relief for abdominal aortic surgery // Cochrane Database Syst. Rev. — 2006. — 19(3). — CD005059. doi: 10.1002/14651858.CD005059.pub2.
15. Oliveira R.M., Tenório S.B., Tanaka P.P., Precoma D. Control of pain through epidural block and incidence of cardiac dysrhythmias in postoperative period of thoracic and major abdominal surgical procedures: a comparative study // Rev. Bras. Anestesiol. — 2012. — 62(1). — Р. 10-18.
16. Wranicz P., Andersen H., Nordbø A., Kongsgaard U.E. Factors influencing the quality of postoperative epidural analgesia: an observational multicenter study // Local Reg. Anesth. — 2014. — 7(5). — Р. 39-45. doi: 10.2147/LRA.S67153.

/120-1.jpg)
/121-1.jpg)
/122-1.jpg)