Вступ
Операційний стрес — це стан поліфункціональних змін, які виникають в організмі хворого під впливом агресивних чинників оперативного втручання. Змінюються функції центральної нервової й ендокринної системи, кровообігу й дихання, печінки та нирок, імунітету і метаболізму. За відсутності антистресового захисту ці зміни стають небезпечними для життя хворого. Тому анестезіолог за допомогою раціонального комплексного анестезіо–логічного забезпечення має цьому запобігти (Бишовець С.М., 2013). Серед агресивних чинників, що викликають операційний стрес, головними є психоемоційний, біль, патологічні рефлекси небольового характеру, постуральні реакції кровообігу, дихання, крововтрата, ушкодження життєво важливих органів (Гомон М.Л., 2015, Потапов О.Л., 2011). У розвитку будь-якого операційного стресу розрізняють три етапи функціональних розладів. Спочатку виникає стан тривоги, збудження, які призначені для посилення діяльності життєво важливих органів та системи пригнічення другорядних. Внаслідок цього порушуються функції другорядних органів і тканин як результат тривалого «голодного» режиму, на якому вони знаходяться. І зрештою, настає розлад функцій життєво важливих органів, що пов’язаний із функціональними порушеннями, які виникли внаслідок тривалої дії стресу (Сорокіна Є.Ю., 2015).
Первинна реакція на чинники операційної агресії починається зі змін у ретикулярній формації та гіпоталамо-гіпофізарній системі, які втягують у процес симпатикоадреналову систему та інші ендокринні залози — щитоподібну, підшлункову, ренінангіотензинову тощо. В результаті цього розвивається полігландулярна ендокринна стимуляція зі всіма властивими їй ефектами. Деякі з них практично нереально прослідкувати, адже дія певних гормонів триває лічені хвилини і спостерігається лише в періоди найбільшого больового стимулу та, відповідно, найвищого рівня стресу. Інші, навпаки, викликають тривалі зміни і зазвичай потребують медикаментозної корекції (Дж. Едвард Морган, 2001).
Також під час операції низка патологічних рефлексів з операційної рани, дихальних шляхів тощо впливає на дихання і кровообіг, замикаючись через холінергічну систему і зумовлюючи ваговагальні та інші рефлекси. Під сумарним впливом гормонів в умовах оперативного втручання істотно змінюється навіть біохімічний та клітинний склад крові. Виникають лімфопенія й еозинопенія (через секвестрації еозинофілів у легенях і селезінці), стимулюється викид еритроцитів і тромбоцитів. Відбуваються зміни в травній системі: спостерігаються підвищена секреція шлункового соку і схильність слизової оболонки до автолізу (можуть виникнути стресові ерозії та виразки). Істотно змінюється метаболізм, зокрема, виникають гіперкаліємія, гіперглікемія, посилюються катаболізм білків і жирів, метаболічний ацидоз, респіраторний алкалоз та ін. (Обухова О.А., 2011).
Реакція організму на хірургічну агресію супроводжується зростанням енергетичних процесів і високим катаболізмом. Головною енергетичною «сировиною» організму є глюкоза і ненасичені жирні кислоти. Адреналін підвищує рівень глюкози в крові, стимулюючи розпад глікогену в печінці, і мобілізує жирні кислоти з ліпідів, активізуючи всі процеси витрати енергії через біологічне окислювання. Встановлено, що за умови операційної агресії в крові різко зростає рівень глюкози і вільних жирних кислот (Коваленко В.Л., 2010).
Операційний стрес закладає основи функціональних розладів, що діють у післяопераційному періоді. До них додаються стресові чинники післяопераційного періоду — біль, емоційне напруження, нерухомість тощо. У зв’язку з цим, починаючи з перших хвилин післяопераційного періоду, необхідно забезпечити потужний антистресовий захист, що включає профілактику болю, адекватну аналгезію, нормалізацію мікроциркуляції, корекцію об’єму циркулюючої крові, метаболізму, функцій нирок й печінки, спеціальні заходи респіраторної терапії (Руднов В.А., 2013, Горкавий Є.О., 2016).
Об’єктивізувати операційний стрес за допомогою спеціальних критеріїв нелегко, оскільки засоби контролю, які ми сьогодні маємо в повсякденній практиці, — це контроль гемодинаміки, газів крові, діурезу, кислотно-основного стану, електролітного балансу і ін. Перелічені критерії не належать до особливо надійних та вірогідних. Тому на сьогодні актуальним є пошук ефективних та доступних маркерів операційного стресу, серед яких є рівень глікемії крові (Бояркіна Г.В., 2013, Кобеляцький Ю.Ю., 2015).
Мета роботи — провести ретроспективний аналіз рівня глікемії у хворих, прооперованих із приводу гострої тонкокишкової непрохідності (ГТКН), та порівняти їх рівень при різному знеболюванні пацієнтів із метою можливого використання для об’єктивної оцінки адекватності анестезіологічного забезпечення хірургічних втручань, терапії тонкокишкової непрохідності.
Матеріали та методи
Виконано ретроспективний аналіз клінічного перебігу 40 пацієнтів, прооперованих у 2015–2017 рр. шляхом лапаротомії з приводу ГТКН, зумовленої спайковим процессом, на базі Національного військово-медичного клінічного центру «Головний військовий клінічний госпіталь». У 20 осіб (контрольна група) операція проходила під багатокомпонентною внутрішньовенною анестезією з інтубацією трахеї та штучної вентиляції легень, а післяопераційне знеболювання проводилось опіатами (промедол) та нестероїдними протизапальними препаратами (кейвер). У інших 20 осіб (дослідна група) анестезіологічне забезпечення й оперативне втручання здійснювались аналогічно, але для знеболювання вводили епідурально 1% р-н лідокаїну (4–6 мл/год) під час і після операції протягом 2 днів. За віком, статтю, індексом маси тіла, ризиком за ASA, тривалістю операції та супутньою патологією відмінностей між групами не було (табл. 1). У хворих при надходженні в стаціонар відмічалися водно-електролітні порушення, зумовлені ГТКН, які були скориговані за допомогою інтенсивної інфузійної терапії (ІТ), діурез при цьому був збережений. Після ІТ електроліти плазми крові були такими: К+ 4,0–4,8 ммоль/л, Cl– 99–108 ммоль/л, Na+ 137–146 ммоль/л, та не було проявів захворювань підшлункової залози чи інших ендокринних органів.
/70-1.jpg)
Рівень глікемії визначався до операції та в наступні 5 днів о 06:00 год глюкозооксидазним методом. Також у хворих визначалися рівень післяопераційного болю, настрій, наявність скарг на нудоту та блювання, стан перистальтики кишечника, поява випорожнень. Варто відмітити, що у хворих не використовувалися гормони (кортизол та інсулін), які могли вплинути на результат дослідження.
Результати та обговорення
У хворих, яким післяопераційне знеболювання здійснювалось опіатами та нестероїдними протизапальними препаратами, рівень болю в перші години після операції був вищим, ніж у пацієнтів з епідуральною аналгезією, і 13 із 20 хворих (65 %) потребували додаткового знеболювання промедолом зразу після операції та 7 (35 %) — у першу післяопераційну добу.
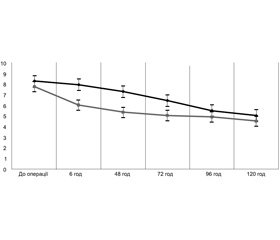
До операції рівень глікемії в контрольній групі становив 8,25 ± 0,69 ммоль/л, у дослідній — 7,76 ± 0,45 ммоль/л. Через 6 год після операції відповідно 7,64 ± 0,39 та 6,24 ± 0,52 ммоль/л, через добу — 7,20 ± 0,38 і 5,32 ± 0,24 ммоль/л, на третю добу — 6,42 ± 0,28 та 5,02 ± 0,23 ммоль/л, на четверту добу — 5,51 ± 0,40 та 4,90 ± 0,22 ммоль/л, на п’яту добу — 5,02 ± 0,36 та 4,53 ± 0,29 ммоль/л (рис. 1). Тобто у всіх пацієнтів з епідуральною аналгезією рівень глікемії крові був нижчим. Залежно від знеболювання статистична різниця рівня глікемії (pα < 0,05) зберігається на першу, другу і третю добу післяопераційного лікування.
/71-1.jpg)
Аналіз показав, що при застосуванні епідуральної аналгезії з лідокаїном після операції відмічалися добре знеболювання, відсутність нудоти і блювання, поява перистальтики на 2-гу добу післяопераційного лікування у 12 (60 %) хворих та в 7 (35 %) — на 3-тю. На 2-гу — 3-тю добу хворі пили, починали їсти, що сприяло їх ранній активізації та дозволило зменшити період стаціонарного лікування. Цікаво, що хворі, у яких глікемія була на рівні 4–5 ммоль/л, раніше активізовувались, починали їсти, ходити та виписувались на 8,6 ± 0,7 день, тоді як у тих пацієнтів, у яких рівень глікемії був вищим від 6 ммоль/л, — на 12,6 ± 2,6 день. При застосуванні промедолу та нестероїдного протизапального препарату для знеболювання в 11 (55 %) хворих відмічалась нудота, перистальтика з’явилася на 3-тю добу в 9 (45 %), а випорожнення — у 7 (45 %) на 4-ту добу. У всіх цих хворих був підвищений рівень глюкози, що призвело до повільного одужання.
Висновки
Клінічний аналіз лікування ГТКН показав, що при стрес-реакції і запаленні збільшується рівень глікемії плазми крові. Зменшення стрес-реакції залежить від анестезіологічного забезпечення і знеболювання. Використання місцевих анестетиків епідурально не лише дозволило досягти достатнього знеболювання, швидкого відновлення перистальтики й ентерального харчування хворих на фоні стабільної гемодинаміки і доброго самопочуття, а й допомогло підтримувати рівень нормоглікемії в післяопераційному періоді. Тоді як в аналогічних хворих при застосуванні опіатів і нестероїдних протизапальних препаратів та недостатньому анестезіо–логічному забезпеченні відмічались прояви стрес-реакції, що супроводжувались підвищенням рівня глюкози крові. Для об’єктивної оцінки пригнічення стрес-реакції і запалення, адекватності знеболювання може використовуватись рівень глюкози крові як простий, доступний і ефективний метод оцінки проявів стресу за відсутності захворювань підшлункової залози.
Конфлікт інтересів. Автори заявляють про відсутність конфлікту інтересів при підготовці даної статті.
Список литературы
1. Бишовець С.М. Стан гемодинаміки та глікемії при тотальній інтравенозній анестезії в абдомінальній хірургії / С.М. Бишовець, В.М. Орел, К.В. Гаєвський // Біль, знеболювання і інтенсивна терапія. — 2013. — № 2(63). — С. 58-64.
2. Гомон М.Л. Післяопераційна антиноцицептивна протекція в комплексі лікування хірургічних хворих абдомінального профілю / М.Л. Гомон, В.О. Шапринський // Медицина неотложных состояний. — 2015. — № 7(70). — С. 75-79.
3. Потапов О.Л. Знеболювання після об’ємних відкритих абдомінальних операцій — опіати чи епідуральна анестезія? / О.Л. Потапов, Ю.Ю. Кобеляцький // Біль, знеболення та інтенсивнатерапія. — 2011. — № 4(57). — С. 39-42.
4. Сорокіна О.Ю. Стрес-індукована гіперглікемія при критичних станах: концепція метаболічної терапії / О.Ю. Сорокіна // Біль, знеболювання і інтенсивна терапія. — 2015. — № 3(72). — С. 9-23.
5. Дж. Едвард Морган Клиническая анестезиология // Анестезиология. — 2001. — № 1. — С. 186-210.
6. Обухова О.А. Гипергликемия при критических состояниях: возможные пути решения проблемы / О.А. Обухова, Ш.Р. Кашия, И.А. Курмуков, А.И. Салтанов // Медицина неотложных состояний. — 2011. — № 4(35). — С. 49-53.
7. Коваленко В.Л. «Стрессовый сахар» в анестезиологии / В.Л. Коваленко, А.В. Мальцев, Е.В. Салиева // Біль, знеболювання і інтенсивна терапія. — 2010. — № 2. — С. 107-108.
8. Руднов В.А. Клиническая значимость и возможные пути коррекции гипергликемии при критических состояниях / В.А. Руднов // Новости медицины и фармаци. — 2013. — № 9. — С. 11-13.
9. Горкавий Є.О. Порівняння двох підходів периопераційного знеболення при хірургічному лікуванні пацієнтів на колоректальний рак / Є.О. Горкавий, І.І. Лісний // Біль, знеболювання і інтенсивна терапія. — 2016. — № 4(77). — С. 24-32.
10. Бояркіна Г.В. Інтенсивність болю післяоперації пов’язана з рівнем передопераційної тривоги і депресії / Г.В. Бояркіна, О.Л. Потапов // Біль, знеболювання і інтенсивна терапія. — 2013. — № 5. — С. 24-28.
11. Кобеляцький Ю.Ю. Сучасні методи об’єктивізації болю та ноцицепції / Ю.Ю. Кобеляцький // Медицина невідкладних станів. — 2015. — № 2(65). — С. 19-23.

/70-1.jpg)
/71-1.jpg)