Журнал «Медицина неотложных состояний» №2(97), 2019
Вернуться к номеру
Клінічне значення впливу інфузійної терапії за рестриктивним типом на відновлення моторики шлунково-кишкового тракту після панкреатодуоденальної резекції
Авторы: Кузьменко В.О.(1), Скумс А.В.(1), Мазур А.П.(1), Кучинська І.А.(2)
(1) — ДУ «Національний інститут хірургії і трансплантології імені О.О. Шалімова» НАМН України, м. Київ, Україна
(2) — Національна медична академія післядипломної освіти імені П.Л. Шупика, м. Київ, Україна
Рубрики: Медицина неотложных состояний
Разделы: Клинические исследования
Версия для печати
Актуальність. Сучасні досягнення в хірургічних та анестезіологічних технологіях дозволили знизити рівень летальності після панкреатодуоденальної резекції (ПДР) до 3 %, але післяопераційні ускладнення при даній патології досягають 29,5–70 %. Тому питання пошуку й уникнення факторів, що спричиняють виникнення ускладнень після ПДР, є одним із найважливіших у розвитку сучасної хірургічної панкреатології. Матеріали та методи. Для оцінки ефективності схем періопераційного лікування було проведено проспективно-ретроспективне дослідження результатів ПДР 78 хворих з доброякісною та злоякісною патологією біліопанкреатодуоденальної зони за період з 2003 по 2017 р. З 2015 року при виконанні операції розпочато застосування програми прискореного відновлення (ППВ). З метою порівняльного аналізу хворих було розподілено на дві групи: у I групу (основна) включено 39 пацієнтів за період із січня 2015 по грудень 2017 р., періопераційне ведення яких проводили відповідно до ППВ, у II групу (група порівняння) ретроспективно відібрано 39 пацієнтів за період із січня 2003 по жовтень 2014 р., періопераційне лікування яких проводилося за традиційним методом. Вивчали об’єм інтраопераційної інфузійної терапії, терміни відновлення моторики шлунково-кишкового тракту (ШКТ) та частоту розвитку гастростазу. Результати. Об’єм застосованих розчинів при інтраопераційній інфузійній терапії був значно нижчим в І групі (2100 мл, 95% CI: [1988; 2300] проти 3300 мл, 95% CI: [3100; 3500]; p < 0,001). Пацієнти І групи повернулися до звичайної дієти швидше, ніж пацієнти у ІІ групі (1,00, 95% CI: [1,00; 1,00] проти 6,00, 95% CI: [6,00; 7,00]; p < 0,001). При статистичному аналізі за даними ROC-кривої було виявлено взаємозв’язок між об’ємом інтраопераційної інфузійної терапії та терміном видалення назогастрального зонда й відновленням перорального харчування в післяопераційному періоді. Висновки. Застосування рестриктивного типу інфузійної терапії в концепції ППВ вірогідно скорочує термін відновлення моторики шлунково-кишкового тракту, зменшуючи частоту гастростазу у пацієнтів після ПДР. Виявилося, що статистично вірогідним фактором впливу на можливість проведення раннього перорального харчування є об’єм інтраопераційної інфузії у пацієнтів після ПДР.
Актуальность. Современные достижения в хирургических и анестезиологических технологиях позволили снизить уровень летальности после панкреатодуоденальной резекции (ПДР) до 3 %, однако послеоперационные осложнения при данной патологии достигают 29,5–70 %. Поэтому вопрос поиска и избежания факторов, вызывающих возникновение осложнений после ПДР, является одним из важнейших в развитии современной хирургической панкреатологии. Материалы и методы. Для оценки эффективности схем периоперационного лечения было проведено проспективно-ретроспективное исследование результатов ПДР 78 больных с доброкачественной и злокачественной патологией билиопанкреатодуоденальной зоны за период с 2003 по 2017 г. С 2015 года при выполнении операции начато применение программы ускоренного восстановления (ПУВ). С целью сравнительного анализа больные были разделены на две группы: в I группу (основная) включено 39 пациентов за период с января 2015 по декабрь 2017 г., периоперационное ведение которых проводили в соответствии с ПУВ, во II группу (группа сравнения) ретроспективно отобраны 39 пациентов за период с января 2003 по октябрь 2014 г., периоперационное лечение которых проводилось по традиционному методу. Изучали объем интраоперационной инфузионной терапии, сроки восстановления моторики желудочно-кишечного тракта (ЖКТ) и частоту развития гастростаза. Результаты. Объем применяемых растворов при интраоперационной инфузионной терапии был значительно ниже в первой группе (2100 мл, 95% CI: [1988; 2300] против 3300 мл, 95% CI: [3100; 3500]; p < 0,001). Пациенты I группы вернулись к обычной диете быстрее, чем пациенты ІІ группы (1,00, 95% CI: [1,00; 1,00] против 6,00, 95% CI: [6,00; 7,00]; p < 0,001). При статистическом анализе по данным ROC-кривой была выявлена взаимосвязь между объемом интраоперационной инфузионной терапии и сроком удаления назогастрального зонда и восстановлением перорального питания в послеоперационном периоде. Выводы. Применение рестриктивного типа инфузионной терапии в концепции ПУВ достоверно сокращает сроки восстановления моторики ЖКТ, уменьшая частоту гастростаза у пациентов после ПДР. Обнаружилось, что статистически достоверным фактором влияния на возможность проведения раннего перорального питания является объем интраоперационной инфузии у пациентов после ПДР.
Background. Modern advances in surgical and anesthetic technologies have reduced mortality rates after pancreaticoduodenectomy (PDE) to 3 %; however, postoperative complications reach 29.5–70 % in this pathology. Therefore, the issue of finding and avoiding the factors that cause complications after PDE is one of the most important ones in modern surgical pancreatology. Materials and methods. To evaluate the efficacy of perioperative treatment regimens, a prospective and retrospective study of PDE outcomes was carried out in 78 patients with benign and malignant pathology of the biliary and pancreatoduodenal zone in 2003–2017. From 2015, we started the use of enhanced recovery program (ERP) in our clinic for patients undergoing PDE. For the purpose of comparative ana-lysis, the patients were divided into two groups: group I included
39 patients who were treated from January 2015 to December 2017 according to ERP; group II consisted of 39 patients who were retrospectively selected for the period from January 2003 to October 2014, their treatment was carried out according to the traditional method. The volume of intraoperative fluid therapy, the реriod of recovery of gastrointestinal motility and the rate of delayed gastric emptying were studied. Results. Intraoperative fluid therapy, in terms of the volume of solutions applied, was significantly lower in group I compared to group II — 2100 ml (95% (confidence interval) CI: 1988–2300) vs 3300 ml (95% CI: 3100–3500), p < 0.001. Patients in group I returned to normal diet faster than patients in group II — 1.00 (95% CI: 1.00–1.00) vs 6.00 (95% CI: 6.00–7.00), p < 0.001. During the statistical analysis, according to the ROC curve, the correlation was revealed between the volume of intraoperative fluid therapy, time of nasogastric tube removal and restoration of oral nutrition in the postoperative period. Conclusions. The use of the restrictive fluid therapy in the concept of ERP significantly reduces the реriod of gastrointestinal motility recovery, the rate of delayed gastric emptying in patients after PDE. The statistically significant factor influencing the possibility of early oral nutrition was the volume of intraoperative fluid in patients after PDE.
мультимодальна програма прискореного відновлення; періопераційна лікувальна тактика; панкреатодуоденальна резекція; рестриктивний тип інфузійної терапії
мультимодальная программа ускоренного восстановления; периоперационное лечение; панкреатодуоденальная резекция; рестриктивный тип инфузионной терапии
multimodal enhanced recovery program; perio-perative treatment; pancreaticoduodenectomy; restrictive fluid therapy
Вступ
Сучасні досягнення в хірургічних та анестезіологічних технологіях дозволили знизити рівень летальності при панкреатодуоденальній резекції (ПДР) до 3 %, але післяопераційні ускладнення досягають 29,5—70 % [1, 2].
Післяопераційні ускладнення, такі як панкреатична фістула, гастростаз тощо, призводять до значного подовження тривалості перебування пацієнтів у стаціонарі, що в середньому становить 14–28 днів у західних спеціалізованих центрах [5]. Тому питання пошуку й уникнення факторів, що спричиняють виникнення ускладнень після панкреатодуоденальної резекції, є одним із найважливіших у розвитку сучасної хірургічної панкреатології [3].
Ініційовано широке впровадження протоколу прискореного відновлення (ERAS — Enhanced Recovery After Surgery) з метою зниження стресової реакції на хірургічну травму у некардіологічних пацієнтів із абдомінальною патоло– гією.
ERAS був розпочатий 1997 року в умовах планової колоректальної хірургії [4, 5] і швидко отримав популярність через значні переваги та безпеку [6]. Одним із компонентів програми прискореного відновлення (ППВ) є рестриктивний тип інфузійної терапії, який може відігравати певну роль у зменшенні набряку анастомозів у післяопераційному періоді [7].
Дані щодо оптимального об’єму періопераційної інфузійної терапії для пацієнтів в абдомінальній хірургії є суперечливими [3].
Матеріали та методи
У дослідження включили 78 пацієнтів із патологією біліопанкреатодуоденальної зони, яким виконали ПДР за період із 2003 по 2017 р. у ДУ «Національний інститут хірургії і трансплантології імені О.О. Шалімова».
З метою порівняльного аналізу ефективності застосування підходів ERAS хворих було розподілено на 2 групи: у I групу (основна) включили 39 пацієнтів (за період із січня 2015 по грудень 2017 р.), періопераційне лікування яким проводилося відповідно до ППВ, у II (група порівняння) — ретроспективно послідовно було відібрано 39 пацієнтів (за період з січня 2003 по грудень 2014 р.), періопераційне лікування яких здійснювали за традиційним методом. У всіх пацієнтів була виконана стандартна ПДР, що включала перетин підшлункової залози в ділянці перешийка, холецистектомію, перетин загальної печінкової протоки, резекцію дистальної частини шлунка і першої петлі тонкої кишки та стандартну лімфаденектомію. Реконструктивний етап полягав у послідовному формуванні панкреатико–, гепатико– і попередуободового гастроентероанастомозу на одній кишковій петлі. Панкреатикоєюноанастомоз формували дворядним швом із ізольованою імплантацією головної протоки підшлункової залози з використанням прецизійного вузлового шва атравматичною ниткою PDS 5/0 і бінокулярного збільшення. Усі операції виконані однією хірургічною бригадою.
У 2015 р. в НІХТ імені О.О. Шалімова НАМН України розроблена та впроваджена в клінічну практику ППВ для передопераційного, інтраопераційного і семидобового післяопераційного періоду. Основними відмінностями даної програми від запропонованих рекомендацій стосовно періопераційного відновлення при ПДР є встановлені терміни, склад і об’єм періопераційної інфузійної терапії, раннього перорального харчування, терміни видалення назогастрального зонда (НГЗ).
Передопераційне ведення хворих згідно з ППВ передбачало такі дії: оцінка нутритивного статусу із виявленням ознак мальнутриції, інформування пацієнта про інтра– та післяопераційний план лікування, рекомендовано відмову від голодування та очищення кишечника перед операцією, прийом вуглеводних сумішей за 3–4 години до оперативного втручання.
Під час оперативних втручань використання інфузійної терапії проводилося в режимі «близьконульового балансу» збалансованими кристалоїдними розчинами із розрахунку 4 мл/кг/год під контролем середнього артеріального тиску, темпу діурезу не менше 0,5 мл/кг/год при задовільному температурному режимі пацієнта (Тcor — 36,2–36,5 °С), при необхідності у випадку гіпотензії застосовувалося введення низьких доз симпатоміметиків (норепінефрин у дозах 0,04–0,05 мкг кг/хв); основними орієнтовними показниками до проведення гемотрансфузії вважали показник гемоглобіну нижче від 80 г/л; установка дренажів у черевну порожнину проводилася залежно від показника ризику утворення панкреатичної фістули за класифікацією ISGPF; для антибіотикопрофілактики були застосовані цефалоспорини ІІ покоління відповідно до керівництва з антибіотикопрофілактики в абдомінальній хірургії [8] за 30–60 хвилин до операції та повторно через 4–6 год. Протягом 24 годин більшість хворих, оцінених як «компенсовані» за основними вітальними показниками (рівень свідомості за шкалою коми Глазго, параметри гемодинаміки, збережена задовільна респіраторна функція, достатній темп діурезу тощо), були переведені із відділення інтенсивної терапії (ВІТ) у хірургічне з метою продовження ранньої активізації. Усім пацієнтам виконувався рентгенологічний контроль пасажу із шлунка та при його наявності видаляли НГЗ. У першу добу післяопераційного періоду об’єм рідкої їжі становив 200–250 мл (у більшості випадків застосовувалася звичайна рідка їжа, а збалансовані суміші для ентерального харчування використовувалися у пацієнтів, які з певних причин не могли отримувати належний об’єм перорального харчування та не досягали 50 % добового калоражу при використанні звичайної їжі або мали граничну величину індексу маси тіла (ІМТ) 18,5), на другу добу — до 500 мл, на третю — до 1 л (за умов відсутності ознак мальнутриції у передопераційному періоді) [9–11]. Прийом твердої їжі пацієнти розпочинали із 4–ї доби післяопераційного періоду. Інфузійну терапію збалансованими кристалоїдами проводили в режимі «близьконульового балансу» та припиняли на 4–ту добу за відсутності додаткових патологічних втрат та за умов нормоволемії. Визначення концентрації амілази у виділеннях із дренажу проводили на 1–шу та 3–тю добу. Дренажі видаляли на 4–6–ту добу за відсутності виділень та підвищення рівня амілази в три рази від норми в крові та відсутності її у виділеннях з дренажу протягом періоду спостереження. Тромбопрофілактика полягала у застосуванні компресії нижніх кінцівок еластичним трикотажем та призначенні препаратів низькомолекулярних гепаринів. Аналоги соматостатину використовували протягом 3 діб тільки при високому ризику утворення панкреатичної фістули ISGPF. Для знеболювання використовували нестероїдні протизапальні препарати та епідуральну анальгезію шляхом безперервного введення у ранньому післяопераційному періоді (48–72 год) із переходом на болюсне «за потребою» пацієнта.
Групи пацієнтів були сформовані за аналогічними демографічними, антропометричними (вік, стать, ІМТ) параметрами. За оцінкою ризику п/о ускладнень та летальністю за шкалою p–POSSUM та за оцінкою ризику виникнення панкреатичної фістули за шкалою ISGPF групи були порівнянними. Однорідність груп за вказаними вище показниками перевірено статистичним критерієм Манна — Уїтні (Mann — Whitney U Test) (p > 0,001). Характеристики коморбідної патології, що включали два основні захворювання, а саме: діабет ІІ типу та серцево–судинну патологію, також були подібними для обох груп (p > 0,001) та характеризували пацієнтів як ASA ІІ–ІІІ. Групи були сформовані когортою пацієнтів, яким виконувалися ПДР за показаннями як доброякісного, так і злоякісного характеру: рак голівки підшлункової залози — у 13 (33,3 %) пацієнтів І групи та 14 (35,9 %) — ІІ, рак великого сосочка дванадцятипалої кишки — у 10 (25,6 %) І групи та 12 (30,8 %) — ІІ, дистальна холангіокарцинома — у 5 (12,8 %) хворих І групи та 5 (12,8 %) — ІІ, нейроендокринна пухлина голівки підшлункової залози — у 4 (10,3 %) хворих І групи та 2 (5,1 %) — ІІ, цистаденома голівки підшлункової залози — у 3 (7,7 %) пацієнтів І та ІІ групи, лімфома дванадцятипалої кишки — у 1 (2,6 %) хворого І групи. Серед факторів, що вивчались, були такі: об’єм інтраопераційної інфузійної терапії, терміни відновлення моторики ШКТ та частота гастростазу.
Статистичний аналіз даних проводили за допомогою спеціалізованого програмного забезпечення Statistica 64 ver.10.0.1011.0 (StatSoft Inc) та додатково з використанням SPSS 21 (SPSS Inc., СШA). Для кількісних показників у виділених групах перевірялася медіана непараметричним критерієм Манна — Уїтні. Групи хворих із ознаками виникнення післяопераційних ускладнень та для вивчення впливу факторів на них, а також їх взаємозв’язок були проаналізовані за допомогою тесту Кокса — Фішера та ROC–
кривої.
Результати
Згідно із запропонованими принципами ППВ об’єм інтраопераційної інфузії збалансованими кристалоїдами був значно меншим в І групі (2100 мл, 95% CI: [1988; 2300] проти 3300 мл, 95% CI: [3100; 3500]; p < 0,001) при порівнянній тривалості оперативних втручань в групах хворих (6 год 50 хв, 95% CІ: [6,25; 6,5] проти 6 год 35 хв, 95% CІ: [6,1; 6,55], p = 0,8) та розрахунковому об’ємі крововтрати (400 мл, 95% CI: [450; 500] проти 450 мл, 95% CI: [400; 600], p = 0,73) (рис. 1).
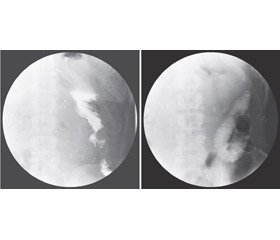
Пацієнти ІІ групи вірогідно довше перебували у ВІТ порівняно із І групою (1,00, 95% CI: [1,00; 1,00] проти 3,00, 95% CI: [3,00; 3,00]; p < 0,001)). Показаннями до видалення НГЗ були рентгенологічне підтвердження евакуації при пасажі контрасту по ШКТ на першу добу після операції та резидуальний об’єм із НГЗ до 200 мл (рис. 2).
НГЗ видаляли вірогідно раніше в І групі, ніж в ІІ (1,00, 95% CI: [1,00; 1,00] проти 6,00, 95% CI: [6,00; 6,00]; p < 0,001)).
Після видалення НГЗ пацієнтам І групи дозволяли вживати рідку їжу з подальшим поступовим поверненням до твердої (у середньому через 2 дні після рідкої дієти, або через 4 доби після оперативного втручання). НГЗ повторно встановили 2 пацієнтам внаслідок розвитку гастростазу. У нашому дослідженні пацієнти І групи повернулися до звичайної дієти швидше, ніж ІІ (1,00, 95% CI: [1,00; 1,00] проти 6,00, 95% CI: [6,00; 7,00]; p < 0,001).
При статистичному аналізі за даними ROC–кривої виявили взаємозв’язок між об’ємом інтраопераційної інфузійної терапії та терміном видалення НГЗ і відновленням перорального харчування в післяопераційному періоді (р = 0,000007) (табл. 1).
Імовірно, рестрикція інтраопераційної інфузії, переведення з ВІТ та активізація пацієнтів, видалення НЗГ з початком перорального харчування з першої доби суттєво вплинули на вірогідне зменшення частоти явищ гастростазу у хворих І групи порівняно з ІІ групою (14 (35,9 %) проти 6 (15,4 %) (за тестом Кокса — Фішера, p = 0,0098).
Обговорення
Згідно з дослідженнями D. Ruess та співавторів, ПДР у високоспеціалізованих центрах залишається єдиним методом лікування раку підшлункової залози з максимальними шансами 5–річного виживання до 30 % [12]. Анатомічне розташування та функціональні особливості підшлункової залози у поєднанні з високими показниками післяопераційних ускладнень роблять панкреатобіліарну хірургію однією із найскладніших. Проте досягнення сучасної хірургії, анестезіології та технологій періопераційної допомоги зробили ПДР набагато безпечнішою операцією порівняно з історичним контролем. У спеціалізованих медичних установах смертність становить 3–5 %, хоча зберігається високий рівень ускладнень (від 25,9 до 70 %) [1, 2]. Виникнення післяопераційних ускладнень є основною причиною тривалого перебування у стаціонарі. Тому актуальність розробки та впровадження періопераційних стратегій, що спрямовані на зменшення післяопераційних ускладнень, не викликають сумнівів. Впровадження протоколу ERAS — це оптимізований підхід до досягнення цієї мети, оскільки він направлений на зниження хірургічної стресової відповіді та прискорення післяопераційного відновлення пацієнтів [19].
Одним із чинників, що впливають на відновлення моторики ШКТ та можливість проведення раннього харчування, є інфузійна терапія як компонент ППВ. Автори в дослідженнях наголошують, що пацієнти при операціях на шлунково–кишковому тракті традиційно отримували великі об’єми періопераційної інфузійної терапії кристалоїдами. У результаті надмірного введення рідини відбувається збільшення ваги на декілька кілограмів, що призводить до тканинного набряку [20] і, ймовірно, є однією із причин післяопераційного парезу та гастростазу. Коли періопераційну інфузію зменшували до кількості, необхідної для підтримки достатнього внутрішньосудинного об’єму, артеріального тиску та темпу сечовиділення, відновлення моторики ШКТ відбувалось раніше, і пацієнти швидше починали пероральне харчування з початком дефекації на кілька днів раніше, ніж ті, які мали більший баланс [21, 22].
Останнім часом спостерігається перегляд підходів до традиційних схем інфузійної терапії в бік обмеження об’єму інфузії в періопераційному періоді. Основою для цього послужили подальші дослідження, які підтвердили, що надлишкове введення в організм сольових розчинів викликає депонування рідини в інтерстиції, що порушує тканинну перфузію й оксигенацію [23]. Але взаємозв’язок інтраопераційної інфузійної терапії та післяопераційних ускладнень все ще достатньо не вивчений [24, 25]. Однак автори у різних дослідженнях прослідкували вплив періопераційних схем інфузії на результати після операцій на підшлунковій залозі. Результати суперечливі: деякі дані демонструють підвищення частоти післяопераційних ускладнень та більш високу летальність [25–27], інші дані не виявили вірогідного взаємозв’язку [28, 29]. B. Kulemann та співавтори у своєму дослідженні визначили кореляцію між кількістю введеної рідини та післяопераційними ускладненнями в когорті з 550 пацієнтів після ПДР [3]. На противагу цьому Ganapathy van Samkar зі співавторами не виявили впливу рестриктивного режиму інфузійної терапії (5 мл/кг/год) порівняно зі стандартним режимом інфузії (10 мл/кг/год) на частоту виникнення гастростазу у пацієнтів після оперативних втручань на підшлунковій залозі [30]. Amit Sastry зі співавторами продемонстрували, що рестриктивна інфузійна терапія перед реконструктивним етапом ПДР зменшила частоту розвитку панкреатичної фістули (23,2 проти 11,1 %, p = 0,05) та гастростазу (48,2 проти 33,3 %, p = 0,200). Наше дослідження підтверджує, що інтраопераційна інфузійна терапія в об’ємі 4 мл/кг/год вірогідно впливає на можливість проведення перорального харчування з першої післяопераційної доби, зменшуючи частоту гастростазу з 35,9 до 15,4 %.
Висновки
1. Статистично вірогідним фактором впливу на можливість проведення раннього перорального харчування виявився об’єм інтраопераційної інфузії у пацієнтів після ПДР. У хворих І групи після ПДР застосування рестриктивного режиму інтраопераційної інфузійної терапії (4 мл/кг/год) порівняно з ліберальним режимом інфузії (6 мл/кг/год), що проводили у хворих ІІ групи, за даними ROC–кривої вірогідно скоротило терміни відновлення моторики шлунково–кишкового тракту з 6–ї до 1–ї післяопераційної доби.
2. Пацієнти основної групи починали пер–оральне харчування з 1–ї п/о доби на відміну від пацієнтів контрольної групи, які починали самостійне харчування не раніше 6–ї доби (1,00, 95% CI: [1,00; 1,00] проти 6,00, 95% CI: [6,00; 7,00]; p < 0,001).
3. Результати проведеного дослідження демонструють вірогідне зменшення частоти явищ гастростазу у хворих І групи порівняно з хворими ІІ групи (14 (35,9 %) проти 6 (15,4 %) (за тестом Кокса — Фішера, p = 0,0098), що свідчить про вплив рестрикції об’єму інтраопераційної інфузійної терапії на розвиток гастростазу в ранньому післяопераційному періоді.
Конфлікт інтересів. Автори заявляють про відсутність конфлікту інтересів при підготовці даної статті.
1. Rebecca L. Siegel, Kimberly D. Miller, Ahmedin Jemal Cancer Statistics, 2018 // CA Cancer J. Clin. 2018; 68:7–30.
2. Pillai S., Palaniappan R., Pichaimuthu A. Feasibility of implementing fast–track surgery in pancreaticoduodenectomy with pancreaticogastrostomy for reconstruction — a prospective cohort study with historical control // Int. J. Surg. 2014; 12(9):1005–9.
3. Kulemann В., Fritz M., Glatz T., Marjanovic G., Sick O., et al. Complications after pancreaticoduodenectomy are associated with higher amounts of intra– and postoperative fluid therapy: A single center retrospective cohort study // Annals of Medicine and Surgery. 2017; (16): 23–29.
4. Kehlet H. Multimodal approach to control postoperative pathophysiology and rehabilitation // Br. J. Anaesth. 1997; 78: 606–617.
5. Lassen K., Coolsen M., van Dam R., van der Wilt A., Slim K., Dejong C. Systematic review and meta–analysis of enhanced recovery after pancreatic surgery with particular emphasis on pancreaticoduodenectomies // World J. Surg. 2012; 37: 1909–
1918.
6. Slim K. Fast–track surgery: the next revolution in surgery care following laparoscopy // Colorectal Dis. 2013:478–480.
7. Miller T., Roche A., Mythen M. Fluid management and goal–directed therapy as an adjunct to Enhanced Reco–very After Surgery (ERAS) // Can. J. Anaesth. 2015 Feb; 62(2):158–68.
8. Bratzler D.W., Dellinger E.P., Olsen K.M., et al. Clinical practice guidelines for antimicrobial prophylaxis in surgery // Am. J. Health–Syst. Pharm. 2013; 70: 195–283.
9. Дронов О., Кучинська І., Арешніков Д., Задорожна К. Особливості проведення нутритивної підтримки у пацієнтів із тяжким гострим некротичним панкреатитом // Медицина неотложных состояний. 2015; 1(64):121–126.
10. Передопераційний скринінг нутритивних порушень у дорослих пацієнтів: використання шкал MUST та MNA–SF // Гострі та невідкладні стани у практиці лікаря. 2018; (2): 49.
11. Weimann A. et al. ESPEN guideline: Clinical nutrition in surgery // Clinical Nutrition. 2017; 36: 623–650.
12. Ruess D., Makowiec F., Chikhladze S., Sick O., Riediger H., Hopt U., Wittel U. The prognostic influence of intrapancreatic tumor location on survival after resection of pancreatic ductal adenocarcinoma // BMC Surg. 2015; 15: 123.
13. Orr R. Outcomes in pancreatic cancer surgery // Surg. Clin. North Am. 2010; 90: 219–234.
14. Kengo A., Zaydfudim V., Truty M., Lombardo K., Kendrick M., Que F., Nagorney D., et al. Management of а delayed post–pancreatoduodenectomy haemorrhage using endovascular techniques // HPB. 2015; 17: 902–908.
15. Robertson N., Gallacher P., Peel N., Garden O., Duxbury M., Lassen K., Parks W. Implementation of an enhanced recovery programme following pancreaticoduodenectomy // HPB. 2012; 14: 700–708.
16. Hallet J., Zih F., Deobald R., Scheer A., Law C., Coburn N., Karanicolas P. The impact of pancreaticojejunostomy versus pancreaticogastrostomy reconstruction on pancreatic fistula after pancreaticoduodenectomy: meta–analysis of randomized controlled trials // HPB. 2015; 17: 113–122.
17. Callery M., Pratt W., Kent T., Chaikof E., Vollmer C. A prospectively validated clinical risk score accurately predicts pancreatic fistula after pancreatoduodenectomy // J. Am. Coll. Surg. 2013; 216: 1–14.
18. Ren L., Zhu D., Wei Y., Pan X., Liang L., Xu J., et al. Enhanced recovery after surgery (ERAS) program attenuates stress and accelerates recovery in patients after radical resection for colorectal cancer: a prospective randomized controlled trial // World J. Surg. 2012; 36: 407–414.
19. Nisanevich V., Felsenstein I., Almogy G., et al. Effect of intraoperative fluid management on outcome after intraabdominal surgery // Anesthesiology. 2005; 103: 25–32.
20. Chowdhury A.H., Lobo D.N. Fluids and gastrointestinal function // Curr. Opin. Clin. Nutr. Metab. Care. 2011; 14: 469–476.
21. Lobo D.N., Bostock K.A., Neal K.R., Perkins A.C., Rowlands B.J., Allison S.P. Effect of salt and water balance on reco–very of gastrointestinal function after elective colonic resection: a randomised controlled trial // Lancet. 2002; 359: 1812–1818.
22. Brandstrup B., Tonnesen H., Beier–Holgersen R., Hjortso E., Ording H., Lindorff–Larsen K., et al. Effects of intravenous fluid restriction on postoperative complications: comparison of two perioperative fluid regimens: a randomized assessor–blinded multicenter trial // Ann. Surg. 2003; 238: 641–648.
23. McClave S.A. The physiologic response and associated clinical benefits from provision of early enteral nutrition / S.A. McClave, D.K. Heyland // Nutr. Clin. Pract. 2009; 24, № 3: 305–315.
24. Wright G., Koehler T., Davis A., Chung M. The drowning whipple: perioperative fluid balance and outcomes follo–wing pancreaticoduodenectomy // J. Surg. Oncol. 2014; 110:
407–411.
25. Weinberg L., Wong D., Karalapillai D., et al. The impact of fluid intervention on complications and length of hospital stay after pancreaticoduodenectomy (Whipple’s procedure) // BMC Anesthesiol. 2014; 14: 14–35.
26. Fischer M., Matsuo K., Gonen M., et al. Relationship between intraoperative fluid administration and perioperative outcome after pancreaticoduodenectomy: results of a prospective randomized trial of acute normovolemic hemodilution compared with standard intraoperative management // Ann. Surg. 2010; 252: 952–958.
27. Lindenblatt N., Park S., Alsfasser G., et al. Intraoperative fluid management in pancreatic resectionsda surgeon’s view // Zentralbl. Chir. 2008; 133: 168–175.
28. Melis M., Marcon F., Masi A., et al. Effect of intra– operative fluid volume on perioperative outcomes after pancreaticoduodenectomy for pancreatic adenocarcinoma // J. Surg. Oncol. 2012; 105: 81–84.
29. Grant F., Protic M., Gonen M., Allen P., Brennan M. Intraoperative fluid management and complications following pancreatectomy // J. Surg. Oncol. 2013; 107: 529–535.
30. van Samkar G., Eshuis W.J., Bennink R.J., van Gulik T.M., Dijkgraaf M.G.W., Preckel B., et al. Intraoperative Fluid Restriction in Pancreatic Surgery: A Double Blinded Randomised Controlled Trial // PLoS One. 2015; 10(10): e0140294.

/112-1.jpg)
/113-1.jpg)
/112-2.jpg)