Журнал «Медицина неотложных состояний» №3(98), 2019
Вернуться к номеру
Зміни функціонального стану ендотелію судин, рівня С-реактивного протеїну та когнітивних функцій у пацієнтів із фібриляцією передсердь та гострим порушенням мозкового кровообігу під впливом лікування
Авторы: Курята О.В.(1), Кушнір Ю.С.(1), Віхрова Т.О.(2)
(1) — ДЗ «Дніпропетровська медична академія МОЗ України», м. Дніпро, Україна
(2) — КЗ «Дніпропетровська обласна клінічна лікарня ім. І.І. Мечникова», м. Дніпро, Україна
Рубрики: Медицина неотложных состояний
Разделы: Клинические исследования
Версия для печати
Фібриляція передсердь залишається основною причиною розвитку гострого порушення мозкового кровообігу (ГПМК), що є однією з основних причин смерті та тяжкої тривалої непрацездатності. Продовжується пошук препаратів, здатних запобігати пошкодженню тканин головного мозку та покращувати відновлення після ГПМК. Метою роботи було визначення зміни функціонального стану ендотелію судин, рівня С-реактивного протеїну та когнітивних функцій у пацієнтів із фібриляцією передсердь та гострим порушенням мозкового кровообігу під впливом лікування цитиколіном. За результатами дослідження в усіх пацієнтів із фібриляцією передсердь та гострим порушенням мозкового кровообігу виявлені порушення ендотеліальної функції та когнітивні розлади, а в 74 % хворих установлено підвищення рівня С-реактивного протеїну. Призначення цитиколіну в дозі 1000 мг на добу сприяло вірогідному поліпшенню функціонального стану ендотелію судин та зниженню рівня С-реактивного протеїну, що є особливо важливим в умовах гострого порушення мозкового кровообігу, бо може допомогти в обмеженні пошкодження тканин на тлі ГПМК та покращити прогноз у даної категорії хворих.
Фибрилляция предсердий остается основной причиной развития острого нарушения мозгового кровообращения (ОНМК), которое является одной из основных причин смерти и тяжелой продолжительной нетрудоспособности. Продолжается поиск препаратов, способных предупредить повреждение тканей головного мозга и улучшить восстановление после ОНМК. Целью работы было определение изменения функционального состояния эндотелия сосудов, уровня С-реактивного протеина и когнитивных функций у пациентов с фибрилляцией предсердий и острым нарушением мозгового кровообращения под влиянием лечения цитиколином. По результатам исследования у всех пациентов с фибрилляцией предсердий и острым нарушением мозгового кровообращения определены нарушение эндотелиальной функции и когнитивные расстройства, а у 74 % больных установлено повышение уровня С-реактивного протеина. Назначение цитиколина в дозе 1000 мг в сутки способствовало достоверному улучшению функционального состояния эндотелия сосудов и снижению уровня С-реактивного протеина, что особенно важно в условиях острого нарушения мозгового кровообращения, поскольку может помочь в ограничении повреджения тканей на фоне ОНМК и улучшить прогноз у данной категории больных.
Atrial fibrillation remains a basic cause of acute stroke (AS) that is a leading reason for death and severe prolonged disability. The agents aimed to prevent brain tissue impairment and improve recovery after AS are being searched. The purpose of the study was to determine the citicoline effects on vascular endothelium functioning, level of C-reactive protein and cognitive status in patients with atrial fibrillation and acute stroke. The results of the study demonstrated that all patients with atrial fibrillation and acute stroke developed endothelial dysfunction and cognitive impairment, 74 % of patients had elevated level of C-reactive protein. Citicoline administration at a dose of 1000 mg a day significantly improves vascular endothelium functioning and decreases the level of C-reactive protein that is of great importance in acute stroke as it helps to restrict tissue impairment in AS and improve prognosis in this cohort of patients.
фібриляція передсердь; гостре порушення мозкового кровообігу; лікування
фибрилляция предсердий; острое нарушение мозгового кровообращения; лечение
atrial fibrillation; acute stroke; treatment
Вступ
Незважаючи на значний прогрес у лікуванні пацієнтів із фібриляцією передсердь (ФП), вона залишається основною причиною смерті, інсульту та серцевої недостатності (СН) [4, 8, 17, 18]. До того ж проблема асимптомного перебігу фібриляції передсердь та її виявлення вперше при госпіталізації хворих уже із судинними ускладненнями продовжує бути актуальною. Найбільш поширеним та соціально значущим ускладненням фібриляції передсердь є гостре порушення мозкового кровообігу [8, 13]. Гостре порушення церебрального кровообігу — це друга основна причина смерті в економічно розвинених країнах і найбільш поширена причина тяжкої тривалої непрацездатності у дорослих [4, 11].
За сучасними уявленнями, гостре порушення мозкового кровообігу може викликати запальну реакцію, що призводить до підвищення рівня С-реактивного протеїну (СРП) [1, 3]. Високі рівні С-реактивного протеїну можуть бути пов’язані з несприятливим прогнозом, оскільки збільшення CРП відображає системну запальну реакцію після ішемічного інсульту та ступінь пошкодження тканин. Крім того, на тваринних моделях вогнищевої ішемії головного мозку показано, що СРП посилює вторинне пошкодження мозку за рахунок активації системи комплементу [1, 5]. CРП протягом 72 годин ішемічного інсульту є незалежним прогностичним фактором несприятливого прогнозу та смерті через 3 місяці [5, 10]. Дослідження, що оцінювали кількісний рівень СРП на ранньому етапі гострого порушення мозкового кровообігу (ГПМК) та його значення як прогностичного фактора, були або рідкісними, або лімітованими щодо критеріїв включення в дослідження. Проте, на нашу думку, визначення рівня СРП із метою оцінки тяжкості стану хворого, динаміки клінічного стану та як можливого маркера прогнозування є досить актуальним: СРП легко вимірюється, процедура доступна в рутинній практиці лікаря. До того ж немає достатніх даних щодо аналізу динаміки рівня С-реактивного протеїну, визначеного в різні періоди гострого інсульту та/або на тлі лікування [10, 12].
Продовжується пошук препаратів, здатних запобігати пошкодженню тканин головного мозку та покращувати відновлення після ГПМК. Наявність такої коморбідної патології, як фібриляція передсердь, несприятливо впливає на ендотеліальну функцію, а також когнітивні зміни, бо, за даними багатьох досліджень, наявність фібриляції протягом чотирьох років спричиняє когнітивні зміни [8, 15, 18]. У дослідженнях, присвячених ГПМК, недостатньо уваги приділяється вивченню когнітивної дисфункції, що можна пояснити тяжкістю стану даної категорії пацієнтів.
Численні експериментальні дослідження на моделях ішемічного інсульту продемонстрували поліпшення результатів і зменшення розмірів зони інфаркту мозку завдяки застосуванню цитиколіну [9].
Цитиколін широко застосовується протягом десятиліть для лікування пацієнтів із різними типами когнітивних порушень [9, 11]. Незважаючи на це, механізм його дії залишається нез’ясованим, але на декількох експериментальних моделях церебральної ішемії продемонстровано здатність препарату відновлювати тканину мозку. У декількох випробуваннях вивчалась ефективність цитиколіну (середньої тривалості й віддалена) при погіршенні пізнавальних функцій унаслідок судинної патології. Результати показали, що цитиколін сприятливо впливає на кілька когнітивних функцій, однак гетерогенність методології цих досліджень ускладнює можливість робити висновки щодо виявлених ефектів [9]. Із метою підтвердження позитивного впливу цитиколіну на когнітивні розлади необхідне проведення більш масштабних досліджень з уніфікованими критеріями включення пацієнтів і стандартизованими шкалами нейропсихологічної оцінки.
У Кокранівському метааналізі (2005), проведеному з метою оцінки ефектів ЦДФ-холіну на когнітивні й поведінкові порушення, асоційовані з хронічними церебральними захворюваннями в осіб похилого віку, зроблено висновок, що препарат позитивно впливає на пам’ять і поведінку (принаймні наявний середньої тривалості та короткочасний ефект) [9]. ЦДФ-холін — єдиний нейропротектор, при вивченні якого отримані позитивні результати в усіх рандомізованих дослідженнях, а також за даними метааналізу з профілем безпеки, аналогічним такому плацебо.
Мета роботи — визначити зміни функціонального стану ендотелію судин, рівня С-реактивного протеїну та когнітивних функцій у пацієнтів із фібриляцією передсердь та гострим порушенням мозкового кровообігу під впливом лікування цитиколіном.
Матеріали та методи
У дослідження залучені 58 хворих (чоловіків — 33, жінок — 25) віком від 55 до 84 років (середній вік — 75 (65; 78) років) із фібриляцією передсердь, яких було госпіталізовано з приводу гострого порушення мозкового кровообігу.
Діагностику фібриляції передсердь проводили згідно з рекомендаціями Української асоціації кардіологів та Європейського товариства кардіологів [6, 13]. Верифікація діагнозу ГПМК проводилась лікарем-неврологом після оцінки неврологічного статусу пацієнта та застосування методів нейровізуалізації (безконтрастна комп’ютерна томографія головного мозку).
Критерії включення у дослідження:
— наявність фібриляції передсердь;
— гостре порушення мозкового кровообігу за ішемічним типом;
— інформована згода пацієнта.
Критерії виключення:
— гостре порушення мозкового кровообігу за геморагічним типом;
— наявність гемодинамічно значущих вад серця;
— гострий коронарний синдром;
— інфаркт міокарда в анамнезі менше 3 місяців тому;
— захворювання крові;
— онкологічні захворювання;
— термінальна СН;
— підвищена чутливість до препарату.
Усі обстежені хворі із ГПМК випадково були розподілені на дві групи. Основна група (n = 33) — пацієнти з ФП та гострим порушенням мозкового кровообігу, які на тлі стандартної терапії додатково отримували цитиколін (препарат Pоноцит, компанія «World Medicine»). Цитиколін додавали в дозі 1000 мг внутрішньовенно краплинно (40–60 крапель на хвилину) протягом 12–14 днів, потім пацієнтам було рекомендовано застосовувати цитиколін у формі розчину для перорального застосування протягом 6–8 тижнів.
Контрольна група (n = 25) — хворі з ФП та гострим порушенням мозкового кровообігу, які отримували стандартну терапію.
Стандартна терапія ФП та ГПМК, яку отримували всі хворі, була порівнянна в обох групах. Клінічна ефективність лікування та динаміка показників оцінювалась через 12–14 днів. Через 6–8 тижнів від початку дослідження всім пацієнтам проводили телефонне інтерв’ю з метою оцінки стану хворого та прихильності до призначеної терапії.
Усім хворим визначали функціональний стан ендотелію судин за допомогою еходопплерографії шляхом вимірювання ендотелійзалежної вазодилатації (ЕЗВД) за результатами проби з реактивною гіперемією за методикою, описаною D. Celermajer [17]. Нормою вважався приріст діаметра артерії на 10 % і більше.
Рівень С-реактивного протеїну визначався за допомогою імунотурбодиметричного методу в сироватці крові, яку брали натщесерце. Референтні інтервали показника знаходились у діапазоні менше від 5 мг/л.
Визначення рівня креатиніну в сироватці крові та обчислення швидкості клубочкової фільтрації усім хворим за формулою CKD-EPI згідно з рекомендаціями Американської національної федерації нирок проводилося з метою клінічної оцінки функції нирок [16, 17].
Наявність атеросклеротичних змін оцінювали за допомогою дуплексного сканування сонних артерій. Усім хворим вимірювали товщину комплексу інтима-медіа, визначали наявність стенозу та його ступінь згідно з North American Symptomatic Carotid Endarterectomy Trial (NASCET) [13].
Оцінка когнітивних порушень проводилась за допомогою Монреальської шкали когнітивних порушень (Montreal cognitive assessment), що оцінює такі когнітивні функції, як увага, концентрація, виконавчі функції, пам’ять, мовленнєві порушення, оптико-просторову діяльність, концептуальне мислення, орієнтованість [14]. Максимальна кількість балів — 30. Результат 26 балів та більше відповідає нормі.
Із метою оцінки тяжкості інсульту лікарем-неврологом використовувалася міжнародна шкала NIHSS (National Institutes of Health Stroke Scale). Інтерпретація тяжкості ішемічного інсульту за шкалою NIHSS: до 5 балів — легкий інсульт; 6–13 балів — інсульт середньої тяжкості; 14–20 балів — тяжкий інсульт; понад 20 балів — дуже тяжкий інсульт [11].
Статистичний аналіз. Для статистичного аналізу даних використовували ліцензійну програму Statistica 6.1. Оцінка типу розподілу даних проводилася за допомогою тесту Шапіро — Уїлка. Оскільки ненормальний розподіл кількісних ознак спостерігався щодо переважної більшості (понад 70,0 %) показників, для опису центральної тенденції даних використовували медіану та інтерквартильний розмах Ме (25%; 75%) [2]. Вірогідність відмінностей кількісних показників між групами визначалася за допомогою тесту Манна – Уїтні. Значущість змін показників у залежних вибірках досліджували за допомогою критерію Вілкоксона. Вірогідність відмінностей якісних показників між групами визначалася за допомогою критерію хі-квадрат Пірсона. Для кореляційного аналізу був застосований коефіцієнт рангової кореляції Спірмена (ρ). Критичне значення рівня значимості (р) приймалося ≤ 0,05.
Результати та обговорення
Усі пацієнти в дослідженні мали гіпертонічну хворобу (ГХ), у більшості пацієнтів (81 %) була діагностована ІІІ стадія ГХ. Частота ішемічної хвороби серця (ІХС) (стабільна стенокардія, постінфарктний кардіосклероз) у пацієнтів у дослідженні була 79,3 %, серцевої недостатності — 75,8 %, інфаркт міокарда в анамнезі мали 13,7 % хворих. Цукровий діабет ІІ типу було виявлено у 22,4 % пацієнтів. Статистично значущої відмінності між групами за згаданими показниками виявлено не було. При порівнянні пацієнтів основної та контрольної груп статистично значущі відмінності було виявлено за віком: середній вік між групами відрізнявся на 9 років (p < 0,05) (табл. 1).
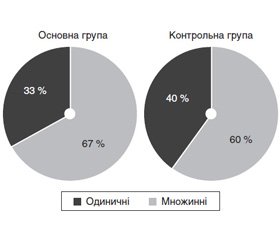
При проведенні дуплексного сканування атеросклеротичні бляшки в сонних артеріях були виявлені в усіх пацієнтів у дослідженні. Суттєвої різниці в кількості каротидних бляшок між групами виявлено не було (рис. 1).
Статистично, але не клінічно значущі розбіжності були виявлені між групами за частотою серцевих скорочень (ЧСС) до лікування та за рівнем діастолічного артеріального тиску (ДАТ) після лікування (табл. 2). В обох групах спостерігалося статистично значуще зниження рівнів систолічного АТ (САТ), ДАТ та ЧСС у відповідь на лікування. Імовірність зниження зазначених показників була вищою для пацієнтів основної групи.
За результатами визначення ЕЗВД зростання показників спостерігалося в обох групах, але в основній групі воно було більш суттєвим (із 5,6 до 6,1 %, p < 0,001) (рис. 2).
На початку лікування рівень С-реактивного протеїну в обох групах був порівнянним: 6,8 (5,8; 7,8) — в основній групі (із цитиколіном) та 7,7 (6,8; 8,5) — в контрольній групі (р > 0,05). Після лікування в обох групах спостерігалась позитивна динаміка, у групі з цитиколіном зміни є вірогідними (рис. 3).
При сумарній бальній оцінці наявності когнітивної дисфункції в пацієнтів із ФП та гострим порушенням мозкового кровообігу встановлено, що жоден хворий не мав показника понад 26 балів, при цьому середній бал був 19,1 в основній групі та 19,8 — в контрольній. Динаміка показників на тлі лікування подана на рис. 4.
На тлі лікування протягом активного періоду спостереження побічних реакцій не відмічалося. Наприкінці активного спостереження рівні печінкових ферментів та білірубіну не зазнали значних змін порівняно з початковими показниками в обох групах (табл. 3).
Висновки
1. У всіх пацієнтів із фібриляцією передсердь та гострим порушенням мозкового кровообігу виявлені порушення ендотеліальної функції та когнітивні розлади, а в 74 % хворих встановлено підвищення рівня С-реактивного протеїну.
2. Призначення цитиколіну в дозі 1000 мг на добу пацієнтам із фібриляцією передсердь сприяє вірогідному поліпшенню функціонального стану ендотелію судин та зниженню С-реактивного протеїну, що є особливо важливим в умовах гострого порушення мозкового кровообігу, бо може свідчити про обмеження пошкодження тканин на тлі ГПМК та покращення прогнозу в даної категорії хворих. Вірогідний позитивний вплив на когнітивні функції у пацієнтів із ФП та ГПМК на тлі додавання цитиколіну до стандартної терапії є перспективним та потребує продовження терміну лікування.
3. Цитиколін (препарат Роноцит) в добовій дозі 1000 мг є безпечним при застосуванні у хворих на ішемічну хворобу серця з фібриляцією передсердь при гострому порушенні мозкового кровообігу.
Конфлікт інтересів. Не заявлений.
1. Cai Z., He W., Zhuang F., Chen Y. The role of high high-sensitivity C-reactive protein levels at admission on poor prognosis after acute ischemic stroke // International Journal of Neuroscience. — 2019. — 129(5). — 423-429. https://doi.org/10.1080/00207454.2018.1538139
2. Cleophas T.J., Zwinderman A.J., Cleophas T.F., Cleophas E.P. Statistics applied to clinical trials. — Springer Science, Business Media B.V., 2009.
3. Den Hertog H., van Rossum V., Van Der Worp H.B., van Gemert [et al.], PAIS investigators. C-reactive protein in the very early phase of acute ischemic stroke: association with poor outcome and death // J. Neurol. — 2009. — 256(12). — 2003-2008. https://doi.org/10.1007/s00415-009-5228-x
4. Durrant J., Lip G.Y., Lane D. Stroke risk stratification scores in atrial fibrillation: current recommendations for clinical practice and future perspectives // Expert. Rev. Cardiovasc. Ther. — 2013. — 11(1). — 77-90.
5. Irimie C., Varcui M., Irimie M., Minea D. C-Reactive Protein and T3: New Prognostic Factors in Acute Ischemic Stroke // J. Stroke Cerebrovasc. Dis. — 2018. — 27(10). — 2731-2737. https://doi.org/10.1016/j.jstrokecerebrovasdis.2018.05.047
6. Kirchhof P., Benussi S., Kotecha D., Ahlsson A. [et al.] 2016 ESC Guidelines for the management of atrial fibrillation developed in collaboration with EACTS // Eur. Heart J. — 2016. — 37(38). — 2893-2962. https://doi.org/10.1093/eurheartj/ehw210
7. Kotecha D., Chudasama R., Lane D.A. Atrial fibrillation and heart failure due to reduced versus preserved ejection fraction: A systematic review and meta-analysis of death and adverse outcomes // Int. J. Cardiol. — 2016. — 203. — 660-666. https://doi.org/10.1016/j.ijcard.2015.10.220
8. Kushnir Y. Risk factors and comorbidity in patients with atrial fibrillation and ischemic heart disease // Eureka: Health Science. — 2018. — 1. — 9-16. https://doi.org/10.21303/2504-5679.2018.00553
9. Milani M. Citicoline as coadiuvant treatment of cognitiveimpairment in chronic degenerative Central Nervous System diseases and in ischemic stroke: a review of available data // Online Journal of Medicine and Medical Science Res. — 2013. — 2(2). — 13-18.
10. Napoli D., Papa F., Bocola V. C-Reactive Protein in Ischemic Stroke An Independent Prognostic Factor // Stroke. — 2001. — 32. — 917-924. https://doi.org/https://doi.org/10.1161/01.STR.32.4.917
11. Sacco R., Kasner S., Broderic J. An Updated Definition of Stroke for the 21st Century. A Statement for Healthcare Professionals From the American Heart Association/American Stroke Association // Stroke. — 2013. — 44(7). — 2064-2089.
12. Schultz N.E.Ø., Hasseldam H. et al. Statin treatment before stroke reduces pro-inflammatory cytokine levels after stroke // Neurological Research. — 2019. — 41(4). — 289-297. https://doi.org/10.1080/01616412.2018.1558000
13. Sychov O., Borodai A., Fedkiv S. Clinical and echocardiographic predictors of silent cerebral infarctions in patients with persistent atrial fibrillation // Sem. Cardiovasc. Medicine. — 2014. — 20. — 10-17.
14. Евтушенко С. Шкалы в общей и детской неврологии. — К., 2015.
15. Курята А., Кушнир Ю. Прямое воздействие на ишемизированный миокард: изученные и новые возможности // Український кардіологічний журнал. — 2016. — № 3. — С. 85-93.
16. Курята О., Кушнір Ю. Маса тіла та рівень альдостерону, лептину у хворих на хронічну серцеву недостатність зі збереженою фракцією викиду // Сучасні медичні технології. — 2014. — № 1. — С. 12-16.
17. Кушнір Ю. Гемодинаміка, функціональний стан ендотелію судин, нирок та тромбоцитів залежно від індексу маси тіла при хронічній серцевій недостатності зі збереженою систолічною функцією // Медичні перспективи. — 2014. — № 19(1). — С. 29-36.
18. Сичов О.С. Серцево-судинні події в пацієнтів з фібриляцією передсердь неклапанного походження та німими інфарктами головного мозку при спостереженні протягом двох років // Український кардіологічний журнал. — 2016. — № 3. — С. 37-43.

/57-1.jpg)
/58-1.jpg)
/58-2.jpg)
/59-1.jpg)
/59-2.jpg)