Архив офтальмологии Украины Том 7, №2, 2019
Вернуться к номеру
Променеві методи у діагностиці патології орбіти
Авторы: Петренко О.В., Бабкіна Т.М., Васильцов І.А.
Національна медична академія післядипломної освіти імені П.Л. Шупика, м. Київ, Україна
Рубрики: Офтальмология
Разделы: Справочник специалиста
Версия для печати
Очна ямка є місцем виникнення великої кількості патологічних процесів різної етіології (запальної, пухлинної, судинної, ендокринної), тому інтерпретація симптомів та клінічних даних має бути пов’язана з візуалізацією патологічного вогнища. Тяжкість верифікації патології очної ямки обумовлена недоступністю для звичних офтальмологічних чи інших методів огляду через неможливість повної візуалізації. Сучасні променеві методи діагностики (комп’ютерна томографія, магнітно-резонансна томографія, однофотонна емісійна комп’ютерна томографія, позитрон-емісійна томографія) необхідні для інтерпретації симптомів і клінічних даних, а також постановки правильного діагнозу на ранньому етапі, що дозволяє уникнути ускладнень для зору та життя пацієнта. В роботі надано огляд променевих методів діагностики патологічних станів орбіти. Означено вибір того чи іншого з них, який ґрунтується на урахуванні переваг та недоліків, показань та протипоказань у кожному окремому випадку, а також світовому досвіді. В комплексі з урахуванням клінічних симптомів, анамнестичних даних та інших методів обстеження використання променевих методів є безумовно необхідним для своєчасної та точної верифікації орбітальної патології, що дозволить визначитися з оптимальною тактикою лікування та уникнути потенційних загроз для здоров’я пацієнта. Водночас із розвитком науки і техніки променева діагностика постійно удосконалюється, і тому подальше дослідження застосування цих методів при орбітальній патології є актуальним та перспективним.
Глазница является местом возникновения большого количества патологических процессов различной этиологии (воспалительной, опухолевой, сосудистой, эндокринной), поэтому интерпретация симптомов и клинических данных должна быть связана с визуализацией патологического очага. Тяжесть верификации патологии обусловлена недоступностью для обычных офтальмологических или иных методов осмотра в связи с невозможностью полной визуализации. Современные лучевые методы диагностики (компьютерная томография, магнитно-резонансная томография, однофотонная эмиссионная компьютерная томография, позитронно-эмиссионная томография) необходимы для интерпретации симптомов и клинических данных, а также постановки правильного диагноза на ранней стадии, что позволяет избежать осложнений для зрения и жизни пациента. В работе представлен обзор лучевых методов диагностики патологических состояний орбиты. Отмечен выбор того или иного из них, обоснованный с учетом преимуществ и недостатков, показаний и противопоказаний в каждом отдельном случае, а также мирового опыта. В комплексе с учетом клинических симптомов, анамнестических данных и других методов обследования использование лучевых методов является безусловно необходимым для своевременной и точной верификации орбитальной патологии, что позволит определиться с оптимальной тактикой лечения и избежать потенциальных угроз для здоровья пациента. В то же время с развитием науки и техники лучевая диагностика постоянно совершенствуется, и поэтому дальнейшее исследование применения этих методов при орбитальной патологии является актуальным и перспективным.
The orbital area is the site of a large number of pathological processes of various origins (inflammatory, tumor, vascular, endocrine); therefore, the interpretation of symptoms and clinical data should include the visualization of pathological focus. The complexity of verifying orbital pathology is associated with inaccessibility for conventional ophthalmic or other methods of examination due to the impossibility of complete visualization. Modern X-ray techniques (computed tomography, magnetic resonance imaging, single photon emission computed tomography, positron emission tomography) are necessary for the interpretation of symptoms and clinical data, as well as for making a correct diagnosis at an early stage, which allows us to avoid complications for the patient’s vision and life. The article presents an overview of X-ray techniques for the diagnosis of pathological conditions of the orbit. The choice of one or other of them is described, which is based on the consideration of advantages and disadvantages, indications and contraindications in each case, as well as international experience. Together with taking into account clinical symptoms, anamnestic data and other methods of examination, the use of X-ray techniques is absolutely necessary for timely and accurate detection of orbital pathology, which will help determine the optimal treatment and avoid potential threats to the patient’s health. At the same time, with the scientific and technological progress, X-ray diagnosis is being improved constantly; therefore, further studies of using these methods in orbital pathology are relevant and promising.
орбіта; діагностика; променеві методи дослідження; огляд
орбита; диагностика; лучевые методы исследования; обзор
orbit; diagnosis; X-ray techniques; review
Орбіта являє собою унікальне і важкодоступне для діагностики та лікування анатомічне утворення людського організму, патологічні стани якого до сьогодні кидають виклик лікарям усього світу та становлять один із найскладніших розділів офтальмології [6, 7, 12].
Очна ямка є місцем виникнення великої кількості патологічних процесів різної етіології (запальної, пухлинної, судинної, ендокринної), тому інтерпретація симптомів та клінічних даних має бути пов’язана з візуалізацією патологічного вогнища. Верифікація захворювань орбіти була значно утруднена до появи сучасних методів променевої діагностики, адже всі патологічні процеси очної ямки найчастіше мають схожу клінічну картину. Як відомо, для ураження орбіти найбільш характерні такі симптоми: екзофтальм, обмеження рухомості ока, зміни розміру очної щілини, набряк навколоочної ділянки та повік, збільшення внутрішньоочного тиску, поява змін на очному дні та зміни рефракції. Будучи замкненим простором, орбіта недоступна для звичайних методів зовнішнього огляду чи будь-яких інших офтальмологічних методів, оскільки вони не дають можливості повної візуалізації. Використання сучасних променевих методів діагностики, таких як комп’ютерна томографія (КТ), магнітно-резонансна томографія (МРТ), однофотонна емісійна комп’ютерна томографія (ОФЕКТ), позитрон-емісійна томографія (ПЕТ), необхідне для своєчасної та точної постановки діагнозу, що дозволить сповільнити або уникнути виникнення потенційно небезпечних наслідків не тільки для зору, а і для життя пацієнта [4, 6, 7, 12, 14, 29, 30].
Детальне знання анатомії орбіти та її вмісту, а також оточуючих структур має важливе значення для діагностики орбітальної патології [29]. Як відомо, очна ямка — це парна кісткова структура, за формою подібна до чотиристоронньої піраміди з верхівкою, що спрямована усередину, назад і дещо догори, а основою — назовні, вперед і дещо донизу. Чотири стінки орбіти (нижня, верхня, зовнішня та внутрішня) утворені за допомогою лобної, виличної, решітчастої, клиноподібної, слізної, піднебінної кісток, верхньої щелепи та покриті окістям. Таким чином, орбіта є кістковим вмістилищем для очного яблука і нараховує велику кількість складних анатомічних структур, що забезпечують захист та функціонування органа зору [14, 40].
Основний вміст орбіти включає очне яблуко, слізну залозу, шість окорухових м’язів, кровоносні судини, черепні (зоровий, окоруховий, блоковий, трійчастий, відвідний), симпатичні, парасимпатичні нерви, циліарний вузол, фасції та жирову клітковину [7].
Анатомічно орбіта межує з придатковими пазухами носа, передньою черепною ямкою, а також за допомогою своїх отворів та щілин має сполучення з крилопіднебінною, скроневою, підскроневою ямками та середньою черепною ямкою і як наслідок — із внутрішньочерепним вмістом. Така близькість розташування може призводити до поширення патологічних процесів із вищезгаданих структур на орбіту і, навпаки, становити небезпеку не тільки для зорового аналізатора, а і для життя при залученні до процесу структур центральної нервової системи [24].
До 1895 року, коли Вільгельм Конрад Рентген представив світовому медичному співтовариству відкрите ним електромагнітне випромінювання, діагностика орбітальних захворювань була головоломкою з двома варіантами відповіді: пухлина або абсцес [17]. У той час як ідея використання рентгенівського випромінювання була схвально сприйнята медиками різних спеціальностей, офтальмологічне співтовариство було більш скептичним. Вперше в офтальмології рентгенівське випромінювання застосували в 1912 році. Тобто лише через 17 років після його запровадження в медичну практику була усвідомлена важливість цього відкриття в діагностиці орбітальної та іншої очної патології [35].
Техніка проведення оглядової рентгенографії очної ямки передбачає виконання двох знімків (у передньому і боковому положеннях), що дозволяють отримати зображення не лише орбіти, а і черепа. За допомогою цього методу променевої візуалізації можна оцінити загальний стан кісткового компоненту орбіти й оточуючих структур, їх травматичні дефекти, окрім того, виявити сторонні тіла не тільки всередині орбіти, а і при проникненні останніх у придаткові пазухи носа чи порожнину черепа. У разі знаходження сторонніх тіл необхідно перейти до більш точної їх локалізації, що дозволить визначитися з тактикою ведення таких пацієнтів. Найбільш поширеними методами рентгенлокалізації є методи Балтіна — Комберга та Абліхіна — Пивоварова, за допомогою яких можна виявити місце розташування стороннього тіла всередині орбіти з точністю до 1–2 мм [8, 11].
Для патології орбіти нетравматичного генезу оглядова рентгенографія є менш інформативним методом через погану візуалізацію м’яких тканин та неможливість вірогідної оцінки поширення патологічного процесу (рис. 1).
Отже, на сьогодні рентгенографія орбіт показана при проникних пораненнях ока для виявлення та уточнення локалізації внутрішньоочних або внутрішньоорбітальних сторонніх тіл, а також для визначення стану кісток орбіти та лицьового черепа при контузії; окрім того, цей метод виправдовує себе широкою доступністю та низькою вартістю [3].
В сучасних умовах провести діагностику патологічних станів орбіти можна за допомогою КТ, МРТ, ОФЕКТ, ПЕТ та комбінації цих методів.
Комп’ютерна томографія — це променевий метод, який використовує пучки рентгенівського випромінювання та детектори, що оточують досліджувану частину тіла або орган. На даний час представлені п’ять різновидів (поколінь) рентгенівських комп’ютерних томографів, найсучаснішим із яких є прилад зі спіральним принципом сканування.
Простіше кажучи, КТ виконує дві основні функції. Перша функція полягає у вимірюванні та реєстрації розбіжності поглинаючої здатності різних тканин, адже пучок рентгенівських променів стає більш слабким залежно від щільності тканини, через яку проходить. Ступінь цієї щільності оцінюється в умовних відносних одиницях — коефіцієнтах абсорбції (КА) за шкалою Хаунсфілда [20, 39]. До сьогодні для всіх тканин та органів в нормі, а також для низки патологічних субстратів розроблені такі коефіцієнти, адже сучасне КТ-обладнання може розрізняти 2000 різних відтінків сірого в кінцевому зображенні [41].
Друга функція — отримання зображення за рахунок швидкого обертання рентгенівської трубки навколо пацієнта на 360 градусів. Таким чином робиться певна кількість рентгенографічних зрізів у різних проекціях, а остаточне зображення може бути відтворене в форматах 2D або 3D залежно від мети, різновиду комп’ютерної томографії й апарату, на якому виконане дослідження. Наприклад, при мультиспіральній КТ за одне обертання рентгенівської трубки можна зробити до 320 рентгенографічних зрізів за рахунок одночасного сканування в декількох проекціях [28, 30].
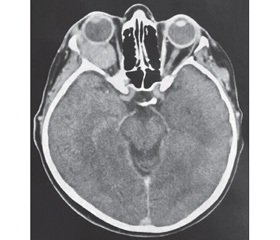
До переваг КТ можна віднести швидкість сканування та обробки інформації, добру візуалізацію кісткового компонента та можливість 3D-реконструкції кісток орбіти, відсутність чутливості до рухів очного яблука, виявлення металевих орбітальних сторонніх тіл, меншу вартість порівняно з МРТ, а до недоліків — променеве навантаження за рахунок використання рентгенівського випромінення та погану візуалізацію м’яких тканин орбіти (рис. 2, 3) [5, 22].
Магнітно-резонансна томографія ґрунтується на використанні фізичного явища ядерного магнітного резонансу, суть якого полягає у властивості поглинати і випромінювати енергію ядрами водню при наявності зовнішнього сталого магнітного поля. Тобто за допомогою МР-томографів визначається насиченість тканин воднем і магнітні властивості їх ядер, пов’язані з перебуванням в оточенні інших атомів та молекул. Загалом сканер МРТ є трубкою, оточеною гігантським круглим магнітом, що створює сильне магнітне поле та вирівнює протони атомів водню. Потім вони зазнають впливу радіохвильових пучків, міняючи свою просторову орієнтацію і виробляючи сигнал, що реєструється сприймаючою частиною МР-сканера з подальшою комп’ютерною обробкою та виведенням зображення. Крім того, в арсеналі сучасних томографів є декілька режимів (Т1, T2, FLAIR, STIR), що дозволяють отримати більш чітке зображення певної тканини, пригнічуючи зображення інших оточуючих тканин [23]. МР-томографія дозволяє оцінити анатомо-топографічний стан тканин орбіти без використання рентгенівського випромінювання, відображаючи ступінь гідратації, і є особливо корисною для диференційної діагностики та верифікації патології м’яких тканин орбіти. В сучасних умовах МРТ є методом вибору і може надати інформацію, що недоступна на КТ, за рахунок кращої візуалізації м’яких тканин (рис. 4) [12]. Головними недоліками цього методу є довготривалість обстеження та чутливість до рухів очного яблука, гірша візуалізація кісткового компонента орбіти та повітроносних порожнин придаткових пазух носа, неможливість виконання МРТ при наявності металевих орбітальних сторонніх тіл та інших феромагнітних компонентів у тілі пацієнта, наприклад протезів, а також вища вартість порівняно з КТ [22].
Окрім того, для підсилення сигналу від патологічних утворень орбіти, що добре кровопостачаються, необхідно застосовувати КТ і МРТ з контрастуванням. Для проведення КТ використовуються рентгенконтрастні речовини, найчастіше — йодовмісні, а для МРТ — речовини, що збільшують час релаксації, підсилюючи магнітний сигнал (наприклад, гадоліній). Контрастування під час КТ і МРТ показане при пі–дозрі на поширення патологічного процесу на структури порожнини черепа або придаткові пазухи носа та уточненні меж пухлин всередині орбіти, для диференційної діагностики гліом зорового нерва від менінгіом його оболонок, при судинній патології орбіти [3, 4, 25].
Постійно зростає значення ядерної медицини у діагностиці патології орбіти, особливо при верифікації злоякісних новоутворень та метастатичних уражень очної ямки на ранніх, доклінічних стадіях захворювання [2, 9, 26].
До сучасних методів радіонуклідної діагностики відносяться ОФЕКТ і ПЕТ, що дозволяють сформувати молекулярне зображення патологічного вогнища за рахунок визначення його метаболічної та біохімічної активності, але без урахування макроскопічної будови та взаєморозташування оточуючих структур. Через низький рівень візуалізації анатомо-топографічних даних як самостійні методи орбітальної діагностики ОФЕКТ і ПЕТ застосовуються рідко, вони є допоміжними у виявленні внутрішньоорбітальних метастазів пухлин інших органів і тканин, а також диференційній діагностиці пухлинних процесів із визначенням ступеня анаплазії [9, 10, 27].
Однофотонна емісійна комп’ютерна томографія — метод, сформований на основі реєстрації випромінювання від радіонуклідів, що при кожному акті розпаду випромінюють один гамма-квант (фотон). Для виконання таких досліджень пацієнту вводяться радіофарм–препарати — субстанції, що належать до різних класів біологічно активних речовин, мічені певним радіоізотопом та беруть участь у метаболізмі тропної тканини. Реєстрація виконується гамма-камерою, що обертається на 180 або 360 градусів і захоплює випромінювання у декількох проекціях, а за допомогою коліматора відбувається визначення точних координат джерела фотонів. За рахунок співставлення проекцій можна отримати 3D-зображення розподілу радіонукліду у досліджуваній тканині [37].
До переваг ОФЕКТ відноситься можливість використання методу для спостереження біохімічних та метаболічних процесів у патологічних вогнищах. Серед недоліків слід зазначити відносно низьку просторову розподільну здатність діагностичних зображень, адже у процесі колімації втрачається певна кількість доступних фотонів, а також обмежені можливості візуалізації анатомічних орієнтирів [9, 10, 36].
На відміну від ОФЕКТ формування зображення при позитрон-емісійній томографії відбувається за рахунок реєстрації двох гамма-квантів, що утворюються при анігіляції позитрона з електроном, а до складу радіофармпрепаратів для цього дослідження входять позитронвипромінюючі радіоізотопи [2].
Перевагами ПЕТ є реєстрація випромінювання в реальному часі без використання процесу фізичної колімації, що дозволяє отримати більш чітке зображення, ніж при ОФЕКТ, а недоліками — вища вартість, яка формується в основному за рахунок складності виготовлення, транспортування та зберігання радіофарм–препаратів, необхідних для ПЕТ (рис. 5) [2, 10].
Наведені радіонуклідні методи є високоінформативними щодо визначення функціонально-метаболічних змін, але в той же час і вузькоспецифічними, без урахування анатомо-топографічних даних. Це може викликати певні труднощі при інтерпретації отриманої діагностичної інформації. В сучасній лікарській практиці доступні гібридні комплекси, що об’єднують різні види променевої діагностики: ОФЕКТ/КТ, ПЕТ/КТ, ОФЕКТ/МРТ, ПЕТ/МРТ, доповнюючи один одного та нівелюючи недоліки [18, 19]. За останні роки отримано повідомлення про успішну діагностику та верифікацію діагнозу гемангіом [1, 15], карцином [31, 42], меланом [21, 34], лімфом орбіти [33, 38] та внутрішньоорбітальних метастазів [13, 16, 31, 32] із застосуванням мультимодальних томографічних даних.
Отже, на сьогодні для діагностики патологічних станів орбіти доступний широкий спектр променевих методів, вибір того чи іншого з яких ґрунтується на врахуванні переваг і недоліків, показань та протипоказань у кожному окремому випадку, а також світовому досвіді. В комплексі з урахуванням клінічних симптомів, анамнестичних даних та інших методів обстеження використання променевих методів є безумовно необхідним для своєчасної та точної верифікації орбітальної патології, що дозволить визначитися з оптимальною тактикою лікування та уникнути потенційних загроз для здоров’я пацієнта. Водночас із розвитком науки і техніки променева діагностика постійно удосконалюється, і тому подальше дослідження застосування цих методів при орбітальній патології є актуальним та перспективним.
Конфлікт інтересів. Автори заявляють про відсутність конфлікту інтересів при підготовці даної статті.
1. Алтынбаева Л.Р., Сережин И.Н., Акчурина Р.А. Дифференциальная диагностика гемангиом и других объемных образований орбиты // Казанский медицинский журнал. — 2015. — № 3. — С. 361-364.
2. Арсвольд Д., Верник М. Эмиссионная томография. Основы ПЭТ и ОФЭКТ/Emission Tomography: The Fundamentals of PET and SPECT. — М.: Техносфера, 2009. — 612 с.
3. Бабий Я.С., Болгова И.М., Удовиченко В.В. Лучевые методы диагностики при заболеваниях глаза и орбиты // Вестник Российского научного центра рентгенорадиологии. — 2004. — № 3. http://vestnik.rncrr.ru/vestnik/v3/papers/bab_v3.htm
4. Бабкина Т.М., Полякова С.И. Возможности магнитно-резонансной и компьютерной томографии в дифференциальной диагностике менингиомы и глиомы зрительного нерва // Офтальмол. журнал. — 2007. — № 6. — С. 34-41.
5. Бабкина Т.М., Терентьева Л.С., Полякова С.И., Легеза С.Г. Спиральная рентгеновская компьютерная томография и рентгеновская компьютерная томография новообразований орбиты с распространением в параназальные синусы и полость черепа // Офтальмологический журнал. — 2001. — № 3. — С. 16-20.
6. Бикбов М.М., Габдрахманова А.Ф., Верзакова И.В. Комплексная диагностика заболеваний орбиты. — Уфа, 2008. — 151 с.
7. Бровкина А.Ф. Болезни орбиты / Бровкина А.Ф. — М.: Медицина. — 1999. — 238 с.
8. Волков В.В., Горбань А.И., Джалиашвили О.А. Клиническое исследование глаза с помощью приборов. — Л., 1971. — 334 с.
9. Габдрахманова А.Ф., Алтынбаева Л.Р. Первый опыт применения радионуклидного исследования с помощью однофотонной эмиссионной компьютерной томографии в диагностике новообразований орбиты // Вестн. офтальмол. — 2008. — Т. 124, № 4. — С. 39-41.
10. Канаев С.В., Новиков С.Н., Гиршович М.М. и др. Значение методов ядерной медицины для определения тактики лучевого лечения у больных со злокачественными новообразованиями различной локализации // Вопросы онкологии. — 2012. — Т. 58, № 3. — С. 189-193.
11. Слободин К.Э. Лучевая диагностика повреждений глаз: Руководство для врачей. — СПб.: СПбМАПО, 2007. — 137 с.
12. Терентьева Л.С. Псевдотумор орбиты воспалительного характера и лучевая диагностика опухолевых и псевдоопухолевых заболеваний орбиты / Л.С. Терентьева, В.Н. Соколов, С.Г. Легеза // Таврический медико-биологический вестник. — 2013. — Т. 16, № 3(2). — С. 140-144.
13. Ahmad S.M., Esmaeli B. Metastatic tumors of the orbit and ocular adnexa // Current opinion in ophthalmology. — 2007. — Vol. 18, № 5. — P. 405-413.
14. Aviv R.I., Casselman J. Orbital imaging: Part 1. Normal anatomy // Clin. Radiol. — 2005. — P. 279-287.
15. Burroni L., Borsari G., Pichierri P. et al. Preoperative diagnosis of orbital cavernous hemangioma: a 99mTc — RBC SPECT study // Clin. Nucl. Med. — 2012. — Vol. 37. — P. 11.
16. Carreras C., Kulkarni H.R., Baum R.P. Rare metastases detected by 68Ga-somatostatin receptor PET/CT in patients with neuroendocrine tumors // Theranostics, Gallium-68, and Other Radionuclides. — Springer Berlin Heidelberg, 2013. — P. 379-384.
17. Casper D.S., Chi T.L., Trokel S.L. Introduction to orbital disease imaging and analysis / Casper D.S., Chi T.L., Trokel S.L., eds. // Orbital disease imaging and analysis. — New York: Thieme, 1993. — P. 9-10.
18. Cherry S.R. Multimodality imaging: beyond PET/CT and SPECT/CT // Semin. Nucl. Med. — 2009. — 39(5). —P. 348-353.
19. Estorch M., Carrio I. Future challenges of multimodality ima–ging. Recent results // Cancer Res. — 2013. — 187. — P. 403-415.
20. Feeman Timothy G. The Mathematics of Medical Imaging: A Beginner’s Guide. Springer Undergraduate Texts in Mathematics and Technology. — Springer, 2010. — 114 р.
21. Finger P.T. et al. Whole body PET/CT for initial staging of choroidal melanoma // British journal of ophthalmology. — 2005. — Vol. 89, № 10. — P. 1270-1274.
22. Goh P.S., Gi M.T., Charlton A., Tan C., Gangadhara Sundar J.K., Amrith S. Review of orbital imaging // Eur. J. Radiol. — 2008. — 66. — P. 387-395.
23. Hallinan James Thomas Patrick Decourcy et al. Eye Globe Abnormalities on MR and CT in Adults: An Anatomical Approach // Korean Journal of Radiology. — 2016. — 17, 5. — P. 664-673.
24. Hande Pradipta C., Inder Talwar. Multimodality imaging of the orbit // Indian Journal of Radiology and Imaging. — 2012. — 22, 3. — P. 227.
25. Henderson I.W. Orbital Tumors. Third Edition. — New York: Raven Press ltd., 1994. — 448 p.
26. Hosokawa C. et al. Usefulness of 99mTc-PMT SPECT and 18F-FDG PET in diagnosing orbital metastasis of hepatocellular carcinoma // Kaku igaku. The Japanese journal of nuclear medicine. — 1994. — Vol. 31, № 10. — P. 1237-1242.
27. José Pablo Martínez Barbero, Inmaculada Rodríquez Jiménez, Teodoro Martin Noguerol, Antonio Luna Alcalá Cancers. Utility of MRI Diffusion Techniques in the Evaluation of Tumors of the Head and Neck // Cancers (Basel). — 2013 Sep. — 5(3). — P. 875-889.
28. Linköping University. Introduction to CT physics. http://bit.ly/O8W4aH.
29. Mafee M.F. Orbit: embryology, anatomy, and pathology / Som P.M., Curtin H.D., eds. // Head and neck imaging. — 4th ed. — St. Louis, Mo: Mosby, 2003. — P. 529-654.
30. Müller-Forell W.S. Imaging of the orbit and visual pathway / Baert K., Sartor K., eds. Medical radiology, diagnostic imaging. — New York: Springer, 2006. — P. 15-7.
31. Muzaffar R., Shousha M.A., Sarajlic L., Osman M.M. Ophthalmologic abnormalities on FDG-PET/CT: a pictorial essay // Cancer. Imaging. — 2013. — 13(1). — P. 100-112.
32. Nguyen B.D., Roarke M.C. Choroidal and extraocular muscle metastases from non-small-cell lung carcinoma: F-18 FDG PET/CT imaging // Clinical nuclear medicine. — 2008. — Vol. 33, № 2. — P. 118-121.
33. Perry C., Herishanu Y., Metzer U., Bairey O., Ruchlemer R., Trejo L., Naparstek E., Sapir E.E., Polliack A. Diagnostic accuracy of PET/CT in patients with extranodal marginal zone MALT lymphoma // European Journal of Haematology. — 2007 Sep. — 79(3). — Р. 205-9.
34. Romero-Aroca P., Montero-Jaime M., Intriago B. et al. 18FDG-PET/CT assessing the absence of cell viability and excluding metastatic disease in a case of necrotic choroidal melanoma // Eur. J. Ophthalmol. — 2012. — Vol. 22, № 2. — P. 288-292.
35. Schiiller A. Roentgen diagnosis of diseases of the head / Translated by F.F. Stocking. — St. Louis: C.V. Mosby, 1918. — P. 8-9.
36. Scuffhama J.W., Wilson M.D., Seller P., Veale M.C., Sel–lin P.J., Jacques S.D.M., Cernik R.J. A CdTe detector for hyperspectral SPECT imaging // Journal of Instrumentation. — 2012. — Vol. 7. https://www.research.manchester.ac.uk/portal/en/publications/a-cdte-detector-for-hyperspectral-spect-imaging(d8cf20cc-a26e-4dca-a449-17656c141da1).html
37. SPECT at the US National Library of Medicine Medical Subject Headings (MeSH). https://www.nlm.nih.gov/cgi/mesh/2011/MB_cgi?mode=&term=SPECT
38. Suga K. et al. F-18 FDG PET/CT findings in a patient with bilateral orbital and gastric mucosa-associated lymphoid tissue lymphomas // Clinical nuclear medicine. — 2009. — Vol. 34, № 9. — P. 589-593.
39. Tawfik Hatem A., Abdelhalim Ahmed, Elkafrawy Mamdouh H. Computed tomography of the orbit, a review and an update // Saudi Journal of Ophthalmology. — 2012. — 26, 4. — P. 409-418.
40. Van Tassel P., Mafee M.F., Atlas S.W., Galetta S.L. Eye, orbit and visual system / Atlas S.W., ed. // Magnetic resonance imaging of the brain and spine. — 4th ed. — Philadelphia: Lippincott Williams & Wilkins, 2009. — Chapter 23, Vol. 2. — P. 1258-1363.
41. Webb A.G. X ray imaging and computed tomography / Webb A.G., ed. // Introduction to biomedical imaging. — New york: Wiley, 2003. — P. 1-56.
42. Wild D. et al. In-line 18 F-fluorodeoxyglucose positron emission tomography with computed tomography (PET/CT) in patients with carcinoma of the sinus/nasal area and orbit // Journal of Cranio-Maxillofacial Surgery. — 2006. — Vol. 34, № 1. — P. 9-16.
43. Case courtesy of Dr Ian Bickle. Radiopaedia.org, rID: 46403
44. Case courtesy of Dr Dalia Ibrahim. Radiopaedia.org, rID: 44049
45. Case courtesy of Dr Ian Bickle. Radiopaedia.org, rID: 52509
46. Ophthalmologic abnormalities on FDG-PET/CT: a pictorial essay. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3607251/figure/F3/?report=objectonly

/62-1.jpg)
/63-1.jpg)
/63-2.jpg)
/64-1.jpg)
/64-2.jpg)