Журнал «Почки» Том 8, №4, 2019
Вернуться к номеру
Менеджмент гіперкаліємії в дітей із хронічною хворобою нирок
Авторы: Кушніренко С.В.
Національна медична академія післядипломної освіти імені П.Л. Шупика, м. Київ, Україна
Рубрики: Нефрология
Разделы: Клинические исследования
Версия для печати
Актуальність. Гіперкаліємія є найбільш поширеним електролітним порушенням, що спостерігається в пацієнтів із захворюванням нирок, особливо з хронічною хворобою нирок (ХХН), цукровим діабетом, серцевою недостатністю або тих, хто знаходиться на лікуванні антагоністами ренін-ангіотензин-альдостеронової системи. Мета дослідження: вивчення поширеності гіперкаліємії в дітей, хворих на ХХН 1–5-ї ст., і впровадження поетапного підходу із застосуванням калієвого біндера полістиренсульфонату натрію (ПСН) для лікування гіперкаліємії. Матеріали та методи. У 300 зразках крові дітей, хворих на ХХН 1–5-ї ст., визначали рівень сироваткового калію (СК). У 23 пацієнтів із ХХН 1–5-ї ст. вивчали ефективність і переносимість ПСН для корекції гіперкаліємії. ПСН призначали перорально з розрахунку 1 г/кг маси тіла на добу, поділяючи розраховану дозу на 3 прийоми. Курс лікування тривав протягом 4 тижнів з наступним переходом на підтримуючу терапію в дозі 0,5 г/кг маси тіла. Результати. Отримані результати продемонстрували, що нормокаліємія (рівень СК 3,5–5,4 ммоль/л) мала місце в 73,3 % дітей із ХХН 1–5-ї ст. Діапазон значень СК 5,0–5,4 ммоль/л визначено в 60 пацієнтів (20,0 %) із ХХН 1–5-ї ст. Легкий ступінь гіперкаліємії (5,5–5,9 ммоль/л) реєструвався в 13,7 % дітей, хворих на ХХН 1–5-ї ст., середній ступінь гіперкаліємії (6,0–6,4 ммоль/л) — у 7 %, і тяжкий ступінь гіперкаліємії (≥ 6,5 ммоль/л) — у 6 % відповідно. Через 4 тижні лікування ПСН рівень СК знизився з 5,9 ± 0,4 ммоль/л до 4,7 ± 0,3 ммоль/л (р < 0,05). Застосування ПСН супроводжувалось незначним підвищенням у сироватці крові рівня натрію (з 138,3 ± 2,4 ммоль/л до 140,7 ± 2,2 ммоль/л), що не виходив за межі нормального діапазону. Терапія ПСН добре переносилась, тільки 1 із 23 пацієнтів припинив прийом ПСН через шлунково-кишкову непереносимість. Висновки. Дисбаланс рівня СК у дітей із ХХН 1–5-ї ст. починається з порогових значень 5,0–5,4 ммоль/л, що потребує ретельного контролю й своєчасного поетапного підходу з метою усунення прогресування гіперкаліємії і мінімізації можливості виникнення небажаних наслідків. ПСН — калієвий біндер — ефективний лікарський засіб, який можна застосовувати для послідовного й безпечного зниження рівня СК у дітей із ХХН із гіперкаліємією в складі комплексної терапії.
Актуальность. Гиперкалиемия является наиболее распространенным электролитным нарушением, наблюдаемым у пациентов с заболеваниями почек, особенно с хронической болезнью почек (ХБП), сахарным диабетом, сердечной недостаточностью или тех, кто находится на лечении антагонистами ренин-ангиотензин-альдостероновой системы. Цель исследования: изучение распространенности гиперкалиемии у детей с ХБП 1–5-й ст. и внедрение поэтапного подхода с использованием калиевого биндера полистиренсульфоната натрия (ПСН) для лечения гиперкалиемии. Материалы и методы. В 300 образцах крови детей с ХБП 1–5-й ст. определяли уровень сывороточного калия (СК). У 23 пациентов с ХБП 1–5-й ст. изучали эффективность и переносимость ПСН для коррекции гиперкалиемии. ПСН назначали перорально из расчета 1 г/кг массы тела в сутки, разделяя рассчитанную дозу на 3 приема. Курс лечения длился 4 недели с последующим переходом на поддерживающую терапию в дозе 0,5 г/кг массы тела. Результаты. Полученные результаты продемонстрировали, что нормокалиемия (уровень СК 3,5–5,4 ммоль/л) имела место у 73,3 % детей с ХБП 1–5-й ст. Диапазон значений СК 5,0–5,4 ммоль/л определен у 60 пациентов (20,0 %) с ХБП 1–5-й ст. Легкая степень гиперкалиемии (5,5–5,9 ммоль/л) регистрировалась у 13,7 % детей с ХБП 1–5-й ст., средняя степень гиперкалиемии (6,0–6,4 ммоль/л) — у 7 %, и тяжелая степень гиперкалиемии (≥ 6,5 ммоль/л) — у 6 % соответственно. Через 4 недели лечения ПСН уровень СК снизился с 5,9 ± 0,4 ммоль/л до 4,7 ± 0,3 ммоль/л (р < 0,05). Использование ПСН сопровождалось незначительным повышением в сыворотке крови уровня натрия (с 138,3 ± 2,4 ммоль/л до 140,7 ± 2,2 ммоль/л), не выходящего за границы нормального диапазона. Терапия ПСН хорошо переносилась, только 1 из 23 пациентов прекратил прием ПСН из-за желудочно-кишечной непереносимости. Выводы. Дисбаланс уровня СК у детей с ХБП 1–5-й ст. начинается с пороговых значений 5,0–5,4 ммоль/л, что требует тщательного контроля и своевременного поэтапного подхода с целью устранения прогрессирования гиперкалиемии и минимизации возможности возникновения нежелательных последствий. ПСН — калиевый биндер — эффективное медикаментозное средство, которое можно использовать для последовательного и безопасного снижения уровня СК у детей с ХБП с гиперкалиемией в составе комплексной терапии.
Background. Hyperkalemia is the most common electrolyte disorder in patients with kidney disease, especially with chronic kidney disease (CKD), diabetes mellitus, heart failure, or in those who are treated with renin-angiotensin-aldosterone system antagonists. Objective: to study the prevalence of hyperkalemia in children with CKD stage 1–5 and introduce a phased approach using potassium binder sodium polystyrene sulfonate (SPS) to treat hyperkalemia. Materials and methods. In 300 blood samples of children with CKD stage 1–5, the level of serum potassium (SP) was determined. In 23 patients with CKD stage 1–5, the efficacy and tolerability of SPS for the correction of hyperkalemia was studied. SPS was administered orally at the rate of 1 g/kg body weight per day in 3 divided doses. The course of treatment lasted 4 weeks with the subsequent transition to maintenance therapy at a dose of 0.5 g/kg body weight. Results. The results showed that 73.3 % of children with CKD stage 1–5 had normokalemia (SP level of 3.5–5.4 mmol/l). The range of SP values of 5.0–5.4 mmol/l was determined in 60 patients (20.0 %) with CKD stage 1–5. Mild hyperkalemia (5.5–5.9 mmol/l) was recorded in 13.7 % of children with CKD stage 1–5, moderate (6.0–6.4 mmol/l) — in 7 % and severe hyperkalemia (≥ 6.5 mmol/l) — in 6 %. After 4 weeks of treatment with SPS, SP level decreased from 5.9 ± 0.4 mmol/l to 4.7 ± 0.3 mmol/l (p < 0.05). The use of SPS was accompanied by a slight increase in serum sodium levels (from 138.3 ± 2.4 mmol/l to 140.7 ± 2.2 mmol/l), which was within the normal range. SPS therapy was well tolerated, only 1 out of 23 patients stopped taking SPS due to gastrointestinal intolerance. Conclusions. Imbalance in the level of SP in children with CKD stage 1–5 begins with threshold values of 5.0–5.4 mmol/l, which requires careful monitoring and timely phased approach in order to control hyperkalemia progression and minimize the occurrence of adverse outcomes. SPS, a potassium binder, is an effective medication that can be used to reduce consistently and safely the level of SP in children with CKD and hyperkalemia as a part of comprehensive therapy.
гіперкаліємія; хронічна хвороба нирок; діти; полістиренсульфонат натрію
гиперкалиемия; хроническая болезнь почек; дети; полистиренсульфонат натрия
hyperkalemia; chronic kidney disease; children; sodium polystyrene sulfonate
Вступ
Гіперкаліємія визначається як вміст калію в сироватці або плазмі крові > 5,5 ммоль/л, проте верхня межа в недоношених і маленьких дітей може сягати 6,5 ммоль/л. Хоча в дітей імовірність розвитку гіперкаліємії менша, ніж у дорослих, вона не є рідкістю [16].
Гомеостатичні механізми регулюють баланс калію для підтримки високих внутрішньоклітинних рівнів, необхідних для забезпечення клітинних функцій (наприклад, метаболізму й росту), і низьких позаклітинних концентрацій для збереження крутого градієнта концентрації через клітинну мембрану, необхідного для збудження нерва й скорочення м’язів. Нормальні концентрації калію в сироватці й плазмі дітей і підлітків аналогічні таким у дорослих. Проте немовлята мають більш високий нормальний рівень калію за рахунок зниження екскреції калію із сечею, що викликається відносно підвищеною нечутливістю до альдостерону й зниженням швидкості клубочкової фільтрації (ШКФ).
Гіперкаліємія є найбільш поширеним електролітним порушенням, що спостерігається в пацієнтів із захворюванням нирок, особливо з хронічною хворобою нирок (ХХН), цукровим діабетом (ЦД), серцевою недостатністю (СН) або тих, які перебувають на лікуванні антагоністами ренін-ангіотензин-альдостеронової системи (РААС) [2, 7, 12, 13].
Справжня частота й поширеність гіперкаліємії невідома, але, за оцінками, вона становить 2–3 % серед населення в цілому і 1–10 % серед госпіталізованих пацієнтів. Особи з ХХН, СН, ЦД і ті, хто приймає антагоністи РААС, а також більше ніж половина пацієнтів із преддіалізними стадіями мають приблизно вдвічі-втричі вищий ризик розвитку гіперкаліємії [22].
Незважаючи на наявність низки публікацій, які демонструють, що гіперкаліємія є менш небезпечним станом при ХХН із кращою переносимістю при гіршій функції нирок (Stockholm CREAtinine Measurements (SCREAM) project), пояснюють це формуванням адаптації/толерантності до затримки калію (K+) і ставлять під сумнів поточне використання єдиного оптимального діапазону K+ для всіх пацієнтів, гіперкаліємія, однак, визнана основним ризиком потенційно небезпечних для життя серцевих аритмічних ускладнень і основним показанням для проведення невідкладної медичної допомоги й звернення до екстракорпоральної замісної терапії [3, 4, 5, 8, 11, 15, 20, 21].
Уперше в Україні аналізується поширеність гіперкаліємії за рівнем ШКФ у дітей, хворих на ХХН 1–5-ї ст. Уперше запропоновано поетапний підхід при гіперкаліємії в дітей, хворих на ХХН, із досвідом застосування калієвого біндера полістиренсульфату натрію (ПСН) для лікування гіперкаліємії в дітей, хворих на ХХН.
Мета даного дослідження полягала у вивченні поширеності гіперкаліємії в дітей, хворих на ХХН 1–5-ї ст., і впровадженні поетапного підходу із застосуванням калієвого біндера ПСН для лікування гіперкаліємії.
Матеріали та методи
У дослідженні брали участь 300 дітей із ХХН 1-5-ї ст. віком від 2 до 17 років, які перебували на стаціонарному лікуванні у відділенні нефрології Київського міського дитячого нефрологічного центру на базі Київської міської дитячої клінічної лікарні № 1. Усі пацієнти підлягали повному обстеженню й лікуванню згідно з Протоколом лікування дітей із хронічною нирковою недостатністю, затвердженим Наказом МОЗ України № 365 від 20.07 2005 «Про затвердження Протоколів лікування дітей за спеціальністю «Дитяча нефрологія».
Пацієнти, залучені в дослідження, і їхні батьки дали інформовану письмову згоду на участь у дослідженні. Дослідження було схвалене комітетом з біоетики Київської міської дитячої клінічної лікарні № 1 і відповідало етичним і морально-правовим вимогам згідно з Наказом МОЗ України № 281 від 01.11.2000.
Усім хворим визначали ШКФ за формулою Шварца (GFR Calculator for children and adolescents 1 to 17 years), що стало підставою для розподілу їх за стадіями безвідносно до діагнозу відповідно до класифікації ХХН.
У 300 зразках крові дітей, хворих на ХХН 1–5-ї ст., після виключення псевдодетермінант гіперкаліємії визначали рівень сироваткового калію (СК). Для інтерпретації результатів використовували таку градацію: СК < 5,0 ммоль/л; СК 5,0–5,4 ммоль/л; СК 5,5–5,9 ммоль/л; СК 6,0–6,4 ммоль/л; СК ≥ 6,5 ммоль/л. Визначення гіперкаліємії варіює. СК > 5,0 ммоль/л вказує на дисбаланс калію. Для визначення ступеня тяжкості застосовуються порогові значення, такі як: легкий (К+ = 5,5–5,9 ммоль/л), середній (К+ = 6,0–6,4 ммоль/л), тяжкий (К+ ≥ 6,5 ммоль/л).
Статистична обробка даних проводилась із застосуванням пакета сучасних прикладних програм для статистичного аналізу і обробки даних Statistica 6.0 із використанням параметричного методу оцінки відмінностей середніх двох вибірок за критерієм Стьюдента, результати наводились у формі таблиць. Для оцінки вірогідності отриманих результатів прийнятий рівень значимості p < 0,05.
Результати та обговорення
Отримані результати продемонстрували, що рівень СК < 5,0 ммоль/л, але вище ніж 3,5 ммоль/л реєструвався в 160 пацієнтів з ХХН 1–5-ї ст. (53,3 %). Дані наведені в табл. 1. Діапазон значень СК 5,0–5,4 ммоль/л визначено в 60 пацієнтів (20,0 %) із ХХН 1–5-ї ст. Отже, нормокаліємія (3,5–5,4 ммоль/л) мала місце в 73,3% досліджуваних пацієнтів із ХХН 1–5-ї ст. Легкий ступінь гіперкаліємії (5,5–5,9 ммоль/л), керуючись Європейськими пороговими значеннями, визначили в 41 дитини (13,7 %) із ХХН 1–5-ї ст. Середній ступінь гіперкаліємії (6,0–6,4 ммоль/л) зареєстровано у 21 пацієнта (7 %) із ХХН 1–5-ї ст., тяжкий ступінь гіперкаліємії (≥ 6,5 ммоль/л) — у 18 пацієнтів (6 %) відповідно.
Детальний аналіз вмісту СК залежно рівня ШКФ продемонстрував, що рівень СК < 5,0 ммоль/л, але вище ніж > 3,5 ммоль/л реєструвався в 76,5 % пацієнтів із ХХН 1-ї ст., 60 % — з ХХН 2-ї ст., 52,6 % — із ХХН 3-ї ст., 26,9 % — з ХХН 4-ї ст. і 14,9 % — із ХХН 5-ї ст. Діапазон значень СК 5,0–5,4 мммоль/л визначався в 14,1 % пацієнтів із ХХН 1-ї ст., 23,5 % — з ХХН 2-ї ст., 22,8 % — із ХХН 3-ї ст., 23,1 % — із ХХН 4-ї ст. і 19,2 % — із ХХН 5-ї ст. Оцінюючи динаміку рівня СК відповідно до європейських порогових значень і значень, прийнятих у США, можна відмітити, що навіть при значеннях СК < 5,0 ммоль/л кількість пацієнтів зменшується зі зниженням рівня ШКФ майже в 5 разів — з 76,5 % при ХХН 1-ї ст. до 14,9 % при ХХН 5-ї ст. У той же час динаміка кількості пацієнтів із рівнем СК 5,0–5,4 ммоль/л, який європейськими пороговими значеннями інтерпретується як нормокаліємія, продемонструвала зовсім іншу тенденцію — до збільшення з 14,1 % пацієнтів із ХХН 1-ї ст. до 23,1 % пацієнтів із ХХН 4-ї ст. Частка хворих із легким ступенем гіперкаліємії (5,5–5,9 ммоль/л) також мала тенденцію до збільшення зі зменшенням ШКФ. Так, серед хворих із ХХН 1-ї ст. кількість пацієнтів з легким ступенем гіперкаліємії дорівнювала 8,2 %, з ХХН 2-ї ст. — 10,6 %, з ХХН 3-ї ст. — 14,0 %, з ХХН 4-ї ст. — 19,2 % і з ХХН 5-ї ст. — 25,5 %. Отже, кількість пацієнтів із легким ступенем гіперкаліємії збільшувалась втричі при зниженні ШКФ з > 90 мл/хв/1,73 м2 до < 15 мл/хв/1,73 м2.
Середній ступінь гіперкаліємії (6,0–6,4 ммоль/л) реєструвався в 1,2 % пацієнтів із ХХН 1-ї ст., 3,5 % пацієнтів з ХХН 2-ї ст., 5,3 % пацієнтів із ХХН 3-ї ст., 7,7 % пацієнтів із ХХН 4-ї ст. і 25,5 % пацієнтів із ХХН 5-ї ст. Аналізуючи приріст пацієнтів із середнім ступенем гіперкаліємії, можна зробити висновок, що найбільша різниця існує між 1, 3 і 5-ю стадією ХХН. Кількість пацієнтів збільшується в 5 разів. А у випадку порівняння ХХН 1-ї ст. і ХХН 5-ї ст. — у 25 разів. Тяжкий ступінь гіперкаліємії визначено у 2,4 % пацієнтів із ХХН 2-ї ст., 5,3 % — із ХХН 3-ї ст., 23,1 % — із ХХН 4-ї ст. і 14,9 % пацієнтів із ХХН 5-ї ст. Поступове збільшення пацієнтів із тяжким ступенем гіперкаліємії від ХХН 1-ї ст. до ХХН 4-ї ст. у 10 разів і зменшення до 14,9 % при ХХН 5-ї ст. пояснювалось тим, що пацієнти з ХХН 5-ї ст. отримували нирково-замісну терапію (гемодіаліз).
Отже, можна констатувати, що дисбаланс рівня СК у пацієнтів з ХХН 1–5-ї ст. починається з порогових значень 5,0–5,4 ммоль/л, що потребує ретельного контролю й своєчасного поетапного підходу із метою усунення прогресування гіперкаліємії і мінімізації виникнення небажаних наслідків.
На сьогодні немає єдиної думки щодо того, скільки тестів, які показують збільшення СК, необхідно для виявлення клінічно значимої гіперкаліємії. Відповідно до принципів KDIGO вимірювання калію рекомендується протягом 1 тижня після початку антиРААС-терапії або титрування дози в пацієнтів зі зниженою нирковою функцією. Аналогічно до принципів KDIGO рекомендується вимірювання СК перед початком антиРААС-терапії, між 1–2 тижнями і в подальшому — після кожного збільшення дози (2008). Тому хоча б одноразове тестування СК може ідентифікувати пацієнтів із ризиком розвитку хронічної гіперкаліємії, особливо з більш розвиненою ХХН і введеними антиРААС-препаратами, тестування щонайменше двічі на рік, мабуть, є розумним підходом до правильного виявлення хронічної гіперкаліємії. Оцінка СК у пацієнтів із ХХН стає необхідною перед початком антиРААС-терапії, через 1–2 тижні після початку й при кожному збільшенні дози.
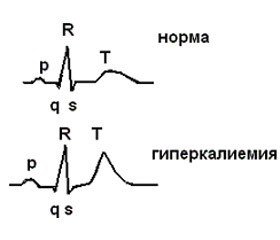
Гіперкаліємія в переважної більшості досліджуваних пацієнтів перебігала безсимптомно, але 23 пацієнти скаржились на такі неспецифічні симптоми, як серцебиття, нудота, біль у м’язах, слабкість або парестезія. Брадикардія під час спостереження за хворими з гіперкаліємією спостерігалась у 5 пацієнтів із ХХН 5-ї ст., ініціюючи проведення позапланового сеансу діалізу. При хронічній гіперкаліємії брадикардія зустрічається рідко через адаптаційні механізми, моніторинг електрокардіограми дозволяє отримати клінічне уявлення про тяжкість відхилень, пов’язаних із калійзалежними змінами серцевого ритму.
Дійсно, хоча ЕКГ вважається основним інструментом для діагностики гіперкаліємії, у нашому дослідженні тільки у 18 пацієнтів (22,5 %) із 80 відповідали критеріям зміни ЕКГ, що відображають гіперкаліємію.
Поетапний практичний підхід менеджменту гіперкаліємії у хворих на ХХН подано в табл. 2 [6, 18]. Лікування є багатогранним, основними його складовими є моніторинг з ретельним переглядом ліків, які потенційно збільшують СК, дієтичне консультування, застосування калієвих біндерів.
У 23 пацієнтів із ХХН 1–5-ї ст. вивчали ефективність і переносимість полістиренсульфонату натрію для корекції гіперкаліємії. ПСН — органічна натрійвмісна смола, що не абсорбується, для перорального й ректального застосування. ПСН застосовується упродовж останніх шести десятиріч (затверджений FDA в 1958 році) для лікування хронічної гіперкаліємії шляхом індукції водянистої діареї із залежною втратою калію [1, 6, 9, 10, 14, 17, 19]. ПСН призначали перорально з розрахунку 1 г/кг маси тіла на добу, поділяючи розраховану дозу на 3 прийоми. Дозу порошку перед застосовуванням змішували з невеликою кількістю рідини — 3–4 мл води на кожен грам порошку. Курс лікування тривав протягом 4 тижнів з наступним переходом на підтримуючу терапію в дозі 0,5 г/кг маси тіла. Терапія припинялась, при досягненні рівня СК нижче за 5 ммоль/ л.
Оцінювали наявність побічних ефектів, потенційно пов’язаних із застосуванням ПСН, аналізували зміни в електролітному складі сироватки крові до і після призначення ПСН-терапії. Через 4 тижні в сироватці крові рівень калію знизився з 5,9 ± 0,4 ммоль/л до 4,7 ± 0,3 ммоль/л (р < 0,05).
Застосування ПСН було пов’язане з невеликим підвищенням у сироватці крові рівня натрію (з 138,3 ± 2,4 ммоль/л до 140,7 ± 2,2 ммоль/л), що не виходив за межі нормального діапазону. Рівень СК залишався ≥ 3,5 ммоль/л у всіх пацієнтів. Найпоширеніші побічні явища реєструвалися у вигляді діареї або запору (13,0 % пацієнтів), що є прийнятним для даної категорії пацієнтів. Терапія ПСН добре переносилась, тільки 1 із 23 пацієнтів припинив прийом ПСН через шлунково-кишкову непереносимість.
Отже, ПСН — калієвий біндер — ефективний лікарський засіб, який можна застосовувати для послідовного й безпечного зниження рівня СК у дітей із ХХН і гіперкаліємією в складі комплексної терапії.
Висновки
Отримані результати продемонстрували, що нормокаліємія (рівень СК 3,5–5,4 ммоль/л) мала місце в 73,3 % дітей із ХХН 1–5-ї ст. Діапазон значень СК 5,0–5,4 ммоль/л визначено в 60 пацієнтів (20,0 %) з ХХН 1–5-ї ст. Легкий ступінь гіперкаліємії (5,5–5,9 ммоль/л) реєструвався в 13,7 % дітей, хворих на ХХН 1–5-ї ст., середній ступінь гіперкаліємії (6,0–6,4 ммоль/л) — у 7 % і тяжкий ступінь гіперкаліємії (≥ 6,5 ммоль/л) — у 6 % відповідно.
Отже, можна констатувати, що дисбаланс рівня СК у пацієнтів із ХХН 1–5-ї ст. починається з порогових значень 5,0–5,4 ммоль/л, що потребує ретельного контролю й своєчасного поетапного підходу з метою усунення прогресування гіперкаліємії і мінімізації виникнення небажаних наслідків.
Поетапний практичний підхід до менеджменту гіперкаліємії є багатогранним, основними його складовими є моніторинг із ретельним переглядом ліків, що потенційно збільшують СК, дієтичне консультування й застосування калієвих біндерів (ПСН).
Конфлікт інтересів. Не заявлений.
Рецензенти: зав. відділом дитячої урології ДУ «Інститут урології НАМНУ», д.м.н. В.Ф. Петербургський; завідувач кафедри педіатрії № 2 НМАПО ім. П.Л. Шупика, д.м.н., професор Т.В. Марушко.
1. Abuelo J.G. Treatment of severe hyperkalemia: confronting 4 fallacies. Kidney Int. Rep. 2017. Vol. 7. № 3(1). P. 47-55.
2. Best Practices in Managing Hyperkalemia in Chronic Kidney Disease. NKF. 2016. URL: www.kidney.org.
3. Bianchi S., Aucella F., De Nicola L. et al. Management of hyperkalemia in patients with kidney disease: a position paper endorsed by the Italian Society of Nephrology. Journal of Nephrology. 2019. Vol. 32(4). P. 499-516.
4. Chang A.R., Sang Y., Leddy J. et al. Antihypertensive medications and the prevalence of hyperkalemia in a large health system. Hypertension. 2016. Vol. 67(6). P. 1181-1188.
5. Collins A.J., Pitt В., Reaven N. et al. Association of serum potassium with all-cause mortality in patients with and without heart failure, chronic kidney disease, and/or diabetes. Am. J. Nephrol. 2017. Vol. 46. P. 213-221.
6. De Nicola L., Di Lullo L., Paoletti Е. et al. Chronic Hyperkalemia in non-dialysis CKD: controversial issues in nephrology practice. Journal of Nephrology. 2018. Vol. 31(5). P. 653-664.
7. Fitch K., Woolley J.M., Engel Т., Blumen Н. The Clinical and economic burden of hyperkalemia on medicare and commercial payers. American Health & Drug Benefits. 2017. Vol. 10(4).
P. 202-209.
8. Gasparini A., Evans M., Barany Р. et al. Plasma potassium ranges associated with mortality across stages of chronic kidney disease: the Stockholm CREAtinine Measurements (SCREAM) project. Nephrol. Dial. Transplant. 2019. Vol. 34(9). P. 1534-1541.
9. Georgianos P.I., Liampas І., Kyriakou А. et al. Evaluation of the tolerability and efficacy of sodium polystyrene sulfonate for long-term management of hyperkalemia in patients with chronic kidney disease. Int. Urol. Nephrol. 2017. Vol. 49(12). P. 2217-2221.
10. Georgianos P.I., Agarwal R. Revisiting RAAS blockade in CKD with newer potassium-binding drugs. Kidney international. 2018. Vol. 93. P. 325-334.
11. Hughes-Austin J.M., Rifkin D.E., Beben T. et al. The relation of serum potassium concentration with cardiovascular events and mortality in community-living individuals. Clin. J. Am. Soc. Nephrol. 2017. Vol. 12. P. 245-252.
12. Kovesdy C.P. Updates in hyperkalemia: Outcomes and therapeutic strategies. Rev. Endocr. Metab. Disord. 2017. Vol. 18(1). P. 41-47.
13. Lazich I., Bakris G.L. Prediction and management of hyperkalemia across the spectrum of chronic kidney disease. Semin. Nephrol. 2014. Vol. 34. P. 333-339.
14. Lepage L., Dufour A.C., Doiron J. et al. Randomized clinical trial of sodium polystyrene sulfonate for the treatment of mild hyperkalemia in CKD. Clin. J. Am. Soc. Nephrol. 2015. Vol. 10(12). P. 2136-2142.
15. Luo J., Brunelli S.M., Jensen D.E., Yang A. Association between serum potassium and outcomes in patients with reduced kidney function. Clin. J. Am. Soc. Nephrol. 2016. Vol. 11. P. 90-100.
16. Masilamani K., van der Voort. The management of acute hyperkalaemia in neonates and children. J. Arch. Dis. Child. 2012. Vol. 97(4). P. 376-380.
17. Mistry M., Shea А., Giguere Р., Nguyen M.L. Evaluation of sodium polystyrene sulfonate dosing strategies in the inpatient management of hyperkalemia. Ann. Pharmacother. 2016. Vol. 50(6). P. 455-462.
18. Montford J.R., Linas S. How dangerous is hyperkalemia. JASN. 2017. Vol. 28(11). P. 3155-3165.
19. Nakamura T., Fujisaki Т., Miyazono М. et al. Risk and benefits of sodium polystyrene sulfonate for hyperkalemia in patients on maintenance hemodialysis. Drugs in R&D. 2018. Vol. 18(3).P. 231-235.
20. Nakhoul G.N., Huang Н., Arrigain S. et al. Serum potassium, end-stage renal disease and mortality in chronic kidney disease. Am. J. Nephrol. 2015. Vol. 41. P. 456-463.
21. Núñez J., Bayés-Genís A., Zannad F. et al. Long-term potassium monitoring and dynamics in heart failure and risk of mortality. Circulation. 2018. Vol. 137(13). P. 1320-1330.
22. Sarafidis P.A., Blacklock R., Wood Е. et al. Prevalence and factors associated with hyperkalemia in predialysis patients followed in a low-clearance clinic. Clin. J. Am. Soc. Nephrol. 2012. Vol. 7. P. 1234-1241.

/20-1.jpg)
/21-1.jpg)