Газета «Новости медицины и фармации» №14 (709), 2019
Вернуться к номеру
Гриндолис в лечении хронических фарингитов: новое решение старой проблемы
Авторы: Татьяна Чистик
Разделы: Справочник специалиста
Версия для печати
Хронический фарингит (ХФ) занимает одно из ведущих мест среди всей патологии лор–органов по распространенности и числу обращений не только к оториноларингологам, но и к врачам общей практики: терапевтам, семейным врачам, педиатрам. Согласно результатам эпидемиологических исследований, проведенных в странах Европы, данной патологией страдает около 7 % взрослого населения [1, 2]; в амбулаторной практике до 70 % обращений к врачу–отоларингологу связаны именно с ХФ [3]. При этом наиболее часто встречающимся поражением при хроническом фарингите является мезофарингит — воспаление слизистой оболочки ротовой полости, несколько реже наблюдаются назофарингит — воспаление носоглотки и гипофарингит — воспаление глотки и гортани [4].
Хронический фарингит — полиэтиологическое заболевание, в большинстве случаев (70 %) вызванное респираторными вирусами: риновирусом, коронавирусом, аденовирусом, респираторным синцитиальным вирусом [5]. В 15–30 % случаев его причиной могут быть бактериальные патогены — β–гемолитический стрептококк группы А, реже — стрептококки групп С и G [6, 12]. Кроме того, немаловажная роль в развитии ХФ отводится рецидивирующим острым воспалительным заболеваниям верхних дыхательных путей, в том числе носа и околоносовых пазух, приводящим к длительному ротовому дыханию, а также общесоматической патологии — заболеваниям желудочно–кишечного тракта, гастрофарингеальному рефлюксу и другим [7–9].
В зависимости от характера развивающихся в слизистой оболочке изменений выделяют катаральный, атрофический и гипертрофический фарингит. Катаральная форма фарингоскопически представляет собой застойную гиперемию, отечность, утолщение слизистой оболочки задней стенки глотки. Патоморфологически отмечаются расширение и стаз вен малого калибра, за счет чего возникает пастозность слизистой оболочки, в периваскулярном пространстве наблюдается периваскулярная клеточная инфильтрация. При данной форме фарингита пациент жалуется на чувство дискомфорта и боль в глотке в виде щекотания и саднения, ощущения инородного тела, стекания слизи по задней стенке глотки, кашель [4, 10].
При осмотре пациентов с гипертрофической формой фарингита можно отметить гиперемию задней стенки глотки, на фоне которой возвышаются гранулы, округлые лимфоидные образования темно–красного цвета или тяжи разной величины, расположенные за задними небными дужками. Для гипертрофического фарингита характерными являются утолщение и уплотнение слизистой оболочки глотки, сопровождающиеся расширением кровеносных и лимфатических сосудов, гиперсекрецией. В периваскулярном пространстве появляются лимфоциты. Жалобы пациентов, страдающих гипертрофическим фарингитом, аналогичны таковым при катаральном фарингите, однако их интенсивность нарастает, может присоединяться заложенность ушей, исчезающая после совершения глотательных движений [7, 8].
При атрофическом фарингите выявляются сухость, истончение слизистой оболочки задней стенки глотки, местами усыпанной инъецированными сосудами, иногда покрытой корками или вязкой слизью. Патоморфологами отмечено уменьшение величины и размеров слизистых желез, а также десквамация эпителиального покрова. Клинически присутствуют жалобы на боль, сухость и першение в горле [7, 8]. Также пациентов с хроническими фарингитами нередко беспокоят частые ОРВИ, заложенность носа, длительный сухой, иногда приступообразный кашель, прерывистый сон, раздражительность, значительно нарушающие качество жизни больного и снижающие его работоспособность [11].
Множественность этиологии хронических фарингитов и разнообразие их форм диктуют необходимость применения различных терапевтических подходов в лечении данной патологии, успех которых во многом определяется своевременным и рациональным подбором лекарственных препаратов. Так, при фарингите, вызванном β–гемолитическим стрептококком, целесообразно назначение антибактериальных средств, действие которых обеспечивает эрадикацию возбудителя. В остальных случах важное место в лечении ХФ занимают лекарственные средства, обладающие противовоспалительным действием. Следует обратить внимание, что противовоспалительные средства снижают содержание простагландинов, т.к. ингибируют циклооксигеназу, при этом сохраняется синтез лейкотриенов, часть которых повышает тонус бронхов и способствует загустению слизи. Поэтому в последнее время возрос интерес к применению препаратов, воздействующих на лейкотриеновые рецепторы, а также противовоспалительных средств, ингибирующих в том числе синтез лейкотриенов. Среди них особый интерес представляет натуральный экстракт растения Grindelia robusta, который стал основой комплексного препарата Гриндолис (Silvestrini, Италия) [13].
Патофизиологические аспекты развития хронического фарингита: роль лейкотриенов в процессах воспаления и ремоделирования
Вирусное инфицирование при ОРВИ часто является первой фазой хронического фарингита, прокладывающей путь для последующего присоединения бактериальной инфекции [24]. В ответ на это развивается воспаление — комплекс защитно–приспособительных реакций организма, влекущий за собой изменения в организме местного и общего характера. Основными компонентами воспаления являются: альтерация, изменение гемодинамики, экссудация с развитием отека, миграция лейкоцитов, фагоцитоз и пролиферация [14]. В ответ на повреждение тканей патогенным агентом и его фагоцитоз происходит синтез медиаторов воспаления — биогенных аминов (гистамин, серотонин), активных полипептидов и белков (кинины, факторы системы комплемента, ферменты, цитокины), производных арахидоновой кислоты (простагландины группы Е, тромбоксаны, лейкотриены, активные формы кислорода) [14]. Простагландины и лейкотриены являются конечными продуктами метаболизма фосфолипидов клеточной мембраны. Гиперфункция простагландинов обусловлена активацией фермента циклооксигеназы (ЦОГ). ЦОГ–1 обладает функциональной активностью структурного фермента, экспрессируется в большинстве клеток, регулирует продукцию простагландинов, участвующих в обеспечении нормальной функциональной активности клеток. ЦОГ–2 в норме отсутствует в большинстве тканей, однако ее экспрессия существенно увеличивается на фоне воспаления [4].
Цистеиниловые лейкотриены (С4, D4 и Е4) — ключевые медиаторы острого и хронического воспаления, состоящие из биологически активных жирных кислот, образующихся из арахидоновой кислоты под воздействием 5–липоксигеназы. Поскольку впервые эти медиаторы были выделены из лейкоцитов и имеют конъюгированную триеновую структуру, они были названы лейкотриенами (ЛТ) [15].
Лейкотриены продуцируются на плазматической мембране воспалительных (эозинофилы, моноциты, макрофаги, тучные клетки, базофилы, лимфоциты, дендритные клетки) и структурных клеток (эпителиальные, гладкомышечные, фибробласты, миобласты) [15] при воздействии патогенных агентов. В результате связывания с рецепторами, прежде всего субтипа 1, на клетках–мишенях ЛТ увеличивают сосудистую проницаемость, усиливают продукцию слизи, уменьшают мукоцилиарный транспорт, увеличивают хемотаксис эозинофилов в дыхательных путях, индуцируют бронхоспазм, вызывают ремоделирование дыхательных путей [16]. Более того, ингибирование циклооксигеназного пути метаболизма арахидоновой кислоты снижает концентрацию простагландинов и одновременно реципрокно увеличивает содержание лейкотриенов. Это, в свою очередь, приводит к отеку слизистой оболочки, загустению секрета, нарушению его оттока, что нередко чревато замедлением процесса выздоровления и развитием осложнений.
Все это послужило стимулом к разработке и созданию препаратов, воздействующих на лейкотриеновый путь и являющихся антагонистами лейкотриеновых рецепторов. Они предотвращают активность лейкотриенов, блокируют активность 5–липоксигеназы, тем самым уменьшая воспаление и ремоделирование дыхательных путей — метаплазию слизистых клеток, утолщение гладкомышечного слоя, субэпителиальное отложение коллагена [16].
Воздействие Гриндолиса на лейкотриеновые рецепторы: фокус на экстракт гринделии (Grindelia robusta)
Гриндолис (Silvestrini, Италия) — комплексный препарат на основе экстракта гринделии (Grindelia robusta) 50 мг; также в его состав входят ацерола (Malpighia punicifolia) 50 мг, прополис 150 мг, экстракт мяты перечной (Mentha piperita) 3,9 мг и эвкалипта (Eucalyptus globulus) 1,95 мг. Все составляющие Гриндолиса дополняют эффекты друг друга, обеспечивают синергизм и усиление его действия. Это способствует более эффективному устранению симптомов воспаления в горле, разжижению мокроты, улучшению ее выведения из дыхательных путей, а также препятствует дальнейшему распространению воспаления по дыхательным путям [17].
Ключевая роль в этом принадлежит экстракту гринделии (Grindelia robusta). Гринделия содержит флавоноиды — метиловые и диметиловые эфиры кверцетина и кемпферола, которые купируют спазм дыхательных путей и улучшают отхождение мокроты. Действие этих соединений связывают со способностью гринделии снижать уровень медиаторов воспаления, в том числе лейкотриенов, и активность провоспалительных цитокинов, что обусловливает их противовоспалительное и спазмолитическое действие [17, 18].
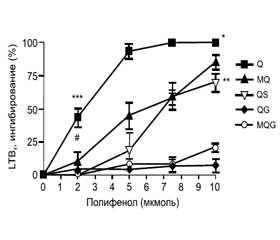
Результаты исследований последних лет подтверждают влияние флавоноидов, содержащихся в экстракте гринделии, на лейкотриеновый путь воспалительной реакции. В работе, проведенной W.M. Loke et al. (2008), была выявлена способность эфиров кверцетина, содержащихся в Grindelia robusta, снижать выработку лейкотриенов моноцитами и нейтрофилами в очаге воспаления (рис. 1, 2) [18]. В исследовании L. Krenna et al. (2009) была продемонстрирована противовоспалительная активность флавоноидных фракций экстракта гринделии, реализуемая за счет ингибирования эластазы нейтрофилов [19].
В исследовании La et al. (2010) показано, что флавоноидная фракция гринделии обладает противовоспалительным эффектом. Это проявлялось статистически достоверным дозозависимым снижением уровня медиаторов воспаления (IL-6, TNF-α, RANTES, MCP–1, PGE2) и металлопротеиназ (MMP–1, –3, –7, –8, –9, –13) [20]. В исследовании Verma et al. (2010) экстракт гринделии на 50 % снижал уровень секреции IL–1β и IL–12.
Оценка клинических эффектов экстракта Grindelia robusta продемонстрировала ее способность содействовать уменьшению симптомов острого фарингита и трахеобронхита, в том числе снижать тяжесть кашля, препятствовать загустеванию мокроты, облегчать ее выведение, что во многом опеределяется антилейко–триеновым действием экстракта [17, 18].
Вышеперечисленные исследования и успешный опыт применения Grindelia robusta позволили внести ее в Европейский формуляр лекарственных растений ESCOP (2009) как антиастматическое и бронхолитическое средство и зафиксировать ее полезные свойства в отчете EMA (Европейское агентство лекарственных средств) в 2012 году [17].
Важные эффекты других компонентов Гриндолиса [13]
Ацерола (Malpighia punicifolia) демонстрирует мощные антиоксидантные свойства благодаря высокому содержанию витамина С, β–каротина и минеральных солей. Прополис способствует репарации тканей, оказывает капилляроукрепляющий, противовоспалительный и антибактериальный эффекты. Мята перечная (Mentha piperita) оказывает противовирусное, антибактериальное и противогрибковое действие, а также обладает противоотечным и противовоспалительным эффектом благодаря содержанию ментола, метилового эфира и прочих производных монотерпенов. Эвкалипт (Eucalyptus globulus) часто применяют в комплексном лечении воспаления верхних и нижних отделов дыхательных путей, фарингитах, синуситах, ОРВИ благодаря антисептическому, антибактериальному, антиоксидантному, анальгезирующему и противовоспалительному действию.
Гриндолис: рекомендации и схема применения
Гриндолис может быть рекомендован при острых и хронических фарингитах, фаринготонзиллитах, бронхитах, ринитах, ОРВИ, гриппе, простудных заболеваниях для облегчения симптомов боли в горле, насморка, улучшения разжижения мокроты и ее выведения из дыхательных путей. Кроме того, Гриндолис применяется как диетическая добавка к рациону питания и дополнительный источник биологически активных веществ природного происхождения [13].
Препарат выпускается в форме пастилок. Взрослым назначается по 1 пастилке 4 раза в день до приема пищи. Пастилку необходимо держать во рту до полного растворения, после чего в течение 15–20 минут следует воздержаться от употребления пищи и напитков.
Выводы
1. Хронические фарингиты — широко распространенная проблема. Согласно результатам эпидемиологических исследований, проведенных в странах Европы, хроническим фарингитом страдает около 7 % взрослого населения; в амбулаторной практике до 70 % обращений к врачу–отоларингологу связаны именно с ХФ.
2. Хронический фарингит — полиэтиологическое заболевание, в большинстве случаев (70 %) вызванное респираторными вирусами: риновирусом, коронавирусом, аденовирусом, респираторным синцитиальным вирусом. В 15–30 % случаев его причиной могут быть бактериальные патогены — β–гемолитический стрептококк группы А, реже — стрептококки групп С и G.
3. При фарингите, вызванном β–гемолитическим стрептококком, целесообразно назначение антибактериальных средств, действие которых обеспечивает эрадикацию возбудителя. В остальных случах важное место в лечении ХФ занимают лекарственные средства, обладающие противовоспалительным действием.
4. На сегодняшний день особый интерес в лечении хронических фарингитов представляют противовоспалительные средства, способные ингибировать синтез лейкотриенов. К ним относится экстракт гринделии (Grindelia robusta), который входит в состав комплексного средства Гриндолис (Silvestrini, Италия).
5. Лейкотриены увеличивают сосудистую проницаемость, усиливают продукцию слизи, уменьшают мукоцилиарный транспорт, увеличивают хемотаксис эозинофилов в дыхательных путях, индуцируют бронхоспазм, вызывают ремоделирование дыхательных путей.
6. Гриндолис, а именно входящий в его состав экстракт гринделии (Grindelia robusta), воздействует на лейкотриеновый путь воспалительной реакции при хроническом фарингите, что клинически проявляется уменьшением боли в горле, тяжести кашля, разжижением мокроты и облегчением ее выведения.
7. Гринделия внесена в Европейский формуляр лекарственных растений ESCOP (2009) как антиастматическое и бронхолитическое средство, а ее полезные свойсва зафиксированы в отчете EMA (Европейское агентство лекарственных средств) в 2012 году [17].
8. Гриндолис может быть рекомендован при острых и хронических фарингитах, фаринготонзиллитах, бронхитах, ринитах, ОРВИ, гриппе, простудных заболеваниях для облегчения симптомов боли в горле, насморка, улучшения разжижения мокроты и ее выведения из дыхательных путей. Кроме того, Гриндолис применяется как диетическая добавка к рациону питания и дополнительный источник биологически активных веществ природного происхождения.
Подготовила Татьяна Чистик
1. Арцимович Н.Г., Корнев А.В., Чугунов B.C. и др. Фарингит как один из ранних симптомов синдрома хронической усталости и иммунной дисфункции. Мат–лы Всероссийского симпозиума «Проблемы иммунологии в оториноларингологии». СПб., 1994. С. 55–56.
2. Адеишвили П.С., Шамшева О.В., Осипов Г.А. Дисбиотические нарушения микробиоценоза слизистых оболочек ротоглотки и их роль в этиопатогенезе инфекционного мононуклеоза. Вестник РГМУ. 2013. 3. С. 44–47.
3. Плужников М.С., Панова Н.В., Левин М.Я.
и др. Фарингит (клинико–морфологические аспекты и криохирургия). СПб.: Диалог, 2006. 120 с.
4. Соболев В.П., Карпова О.Ю., Артамонова П.С. Новые возможности лечения воспалительных заболеваний глотки. Consilium Medicum. 2018. 20 (11). С. 30–32. DOI: 10.26442/20751753.2018.11.000026.
5. Schappert S.M., Rechtsteiner E.A. Ambulatory me–dical care utilization estimates for 2006. Natl. Health Stat. Report. 2008. 8. Р. 1–29.
6. Shulman S.T., Bisno A.L., Clegg H.W. et al. Clinical practice guideline for the diagnosis and management of group A streptococcal pharyngitis: 2012 update by the Infectious Diseases Society of America. Clin. Infect. Dis. 2012. 55 (10). Р. 1279–82.
7. Пальчун В.Т. и др. Оториноларингология: национальное руководство. М.: ГЭОТАР–Медиа, 2008.
8. Пальчун В.Т., Лучихин Л.А., Крюков А.И. Воспалительные заболевания глотки. М.: ГЭОТАР–Медиа, 2007.
9. Морозова С.В. Перспективные направления медикаментозной терапии воспалительных заболеваний носа, околоносовых пазух и глотки. Южно–Российский мед. журн. 2003. 5–6. С. 9–12.
10. Гострый А.В., Симонова А.В., Михайлова Н.А. и др. Хронический фарингит: этиология, патогенез, лечение. Новые подходы в оценке этиопатогенеза. Архивъ внутренней медицины. 2019. № 1.
11. Шпынев К.В., Кречиков В.А. Современные подходы к диагностике стрептококкового фарингита. КМАХ. 2007. 9 (1). С. 20–33.
12. Gwaltney J.M. The common cold. In: Mandell G.L., Bennet J.E., Dolin R. Principles and Practice of Infectious Diseases. 4th ed. NY: ChurchillLivingstone. 1996. 6. 561 р.
13. Инструкция по применению препарата Гриндолис. https://www.medcentre.com.ua/medikamenty/grin–dolis.html
14. Войнов В.А. Атлас по патофизиологии. 2–е изд., перераб. и доп. М.: Медицинское информационное агентство, 2007. С. 52–7.
15. Баранова И.А. Антилейкотриеновые препараты в лечении бронхиальной астмы. Consilium Medicum. 2014. 11. С. 18–22.
16. Henderson W.R. et al. Montelukast inhibits neutrophil pro–inflammatory activity by a cyclic AMP–dependent mechanism. Am. J. Respir. Crit. Care Med. 2006. 173. 718.
17. Гриндолис: природа против боли в горле! Аптека. 2019. № 32 (1203).
18. Ковалев В.Н., Журавель И.А., Ковалева–Загравская И.В. Гринделия растопыренная — перспективное лекарственное растение. Провизор. 2000. № 9.
19. Krenna L., Wollenweberb E., Steyrleuthnera K., Görickc C., Melzigc M.F. Contribution of methylated exudate flavonoids to the anti–inflammatory activity of Grindelia robusta. https://www.sciencedirect.com/science/article/abs/pii/S0367326X09000483
20. La V.D., Lazzarin F., Ricci D., Fraternale D. Active principles of Grindelia robusta exert antiinflammatory properties in a macrophage model. https://onlinelibrary.wiley.com/doi/abs/10.1002/ptr.3195.

/18-1-1.jpg)