Международный эндокринологический журнал Том 15, №7, 2019
Вернуться к номеру
Ефективність і патогенетичне обґрунтування застосування вілдагліптину у хворих на цукровий діабет 2-го типу
Авторы: Паньків В.І.
Український науково-практичний центр ендокринної хірургії, трансплантації ендокринних органів і тканин МОЗ України, м. Київ, Україна
Рубрики: Эндокринология
Разделы: Клинические исследования
Версия для печати
Актуальність. Інгібітори дипептидилпептидази 4-го типу (ДПП-4), маючи інкретинову активність, впливають на основні патогенетичні механізми цукрового діабету (ЦД) 2-го типу. Вілдагліптин є інноваційним препаратом класу інгібіторів ДПП-4 з унікальними характеристиками фармакокінетики, ефективність і безпека якого вивчалися в плацебо-контрольованих дослідженнях. Мета дослідження: вивчення фармакотерапевтичної ефективності, безпеки й переносимості препарату Гліптар виробництва ПАТ «Київмедпрепарат» (Україна) у терапії хворих на ЦД 2-го типу. Матеріали та методи. У дослідження було включено 49 пацієнтів із ЦД 2-го типу. До включення в дослідження хворі отримували монотерапію метформіном у дозі не менше за 1000 мг на добу принаймні упродовж останніх шести місяців. Тривалість перебігу ЦД 2-го типу в середньому становила 6,2 ± 1,8 року. Пацієнти сформували дві групи для подальшого спостереження. 29 пацієнтам, які до цього часу отримували препарати метформіну в дозі до 2000 мг/добу, був додатково призначений препарат Гліптар (вілдагліптин) у дозі 50 мг двічі на добу. Пацієнти другої групи (n = 20) продовжували прийом метформіну двічі на день в дозі 2000 мг/добу. Результати. Через 12 тижнів у хворих першої групи на тлі терапії метформіном у поєднанні з вілдагліптином рівень НbА1с вірогідно знизився до 6,42 ± 0,21 %, глікемія натще — до 6,14 ± 0,22 ммоль/л, глікемія постпрандіальна — до 8,63 ± 0,23 ммоль/л. На тлі комбінованого лікування у хворих на ЦД 2-го типу відзначалися зниження маси тіла на 1,18 кг, а також тенденція до зниження індексу маси тіла з 31,49 ± 1,08 кг/м2 до 29,98 ± 0,76 кг/м2. Рівень імунореактивного інсуліну становив після лікування в першій групі 14,08 ± 1,83 мкОд/мл (при початковому 21,11 ± 2,03 мкОд/мл), індекс HOMA-IR — 3,14 ± 0,21 (проти початкового 6,28 ± 1,42). Вірогідне зниження показників вуглеводного обміну, інсулінорезистентності можна оцінювати як позитивну динаміку завдяки комбінованому лікуванню. Висновки. З огляду на отримані переваги подвійної терапії в лікуванні хворих на ЦД 2-го типу відповідно до загальноприйнятої покрокової терапії на другому етапі пацієнтам, які отримують метформін і не досягли цільового глікемічного контролю, доцільно призначати препарат вілдагліптину. Комбінована терапія вілдагліптином у поєднанні з метформіном забезпечує комплексну дію на чинники ризику серцево-судинних захворювань у вигляді запобігання розвитку гіперінсулінемії та зниження інсулінорезистентності.
Актуальность. Ингибиторы дипептидилпептидазы 4-го типа (ДПП-4), обладая инкретиновой активностью, влияют на основные патогенетические механизмы сахарного диабета (СД) 2-го типа. Вилдаглиптин — инновационный препарат класса ингибиторов ДПП-4 с уникальными характеристиками фармакокинетики, эффективность и безопасность которого изучались в плацебо-контролируемых исследованиях. Цель исследования: изучить фармакотерапевтическую эффективность, безопасность и переносимость препарата Глиптар производства ПАТ «Киевмедпрепарат» (Украина) в терапии больных СД 2-го типа. Материалы и методы. В исследование было включено 49 пациентов с СД 2-го типа. Больные получали монотерапию метформином в дозе не менее 1000 мг в сутки как минимум в течение последних шести месяцев. Длительность течения СД 2-го типа в среднем составила 6,2 ± 1,8 года. Пациенты сформировали две группы для дальнейшего наблюдения. 29 пациентам, которые получали препараты метформина в дозе до 2000 мг/сутки, был дополнительно назначен препарат Глиптар (вилдаглиптин) в дозе 50 мг два раза в сутки. Пациенты второй группы (n = 20) продолжали прием метформина дважды в день в дозе 2000 мг/сут. Результаты. Через 12 недель у больных первой группы на фоне терапии метформином в сочетании с вилдаглиптином уровень НbА1с достоверно снизился до 6,42 ± 0,21 %, гликемия натощак — до 6,14 ± 0,22 ммоль/л, гликемия постпрандиальная — до 8,63 ± 0,23 ммоль/л. На фоне лечения у больных СД 2-го типа отмечались снижение массы тела на 1,18 кг, а также тенденция к снижению индекса массы тела с 31,49 ± 1,08 кг/м2 до 29,98 ± 0,76 кг/м2. Уровень иммунореактивного инсулина составил после лечения в первой группе 14,08 ± 1,83 мкЕд/мл (при начальном 21,11 ± 2,03 мкЕд/мл), индекс HOMA-IR — 3,14 ± 0,21 (против начального 6,28 ± 1,42). Достоверное снижение показателей углеводного обмена, инсулинорезистентности можно оценивать как положительную динамику благодаря комбинированному лечению. Выводы. С учетом полученных преимуществ двойной терапии в лечении больных СД 2-го типа в соответствии с общепринятой пошаговой терапией на втором этапе пациентам, которые получают метформин и не достигли целевого гликемического контроля, целесообразно назначать вилдаглиптин. Комбинированная терапия вилдаглиптином в сочетании с метформином обеспечивает комплексное воздействие на факторы риска сердечно-сосудистых заболеваний в виде предотвращения развития гиперинсулинемии и снижения инсулинорезистентности.
Background. Dipeptidyl peptidase-4 inhibitors, having incretin activity, influence the main pathogenetic mechanisms of type 2 diabetes mellitus (DM). Vildagliptin is an innovative dipeptidyl peptidase-4 inhibitor with unique pharmacokinetic characteristics, the efficacy and safety of which have been studied in placebo-controlled studies. The purpose: to study the pharmacotherapeutic efficacy, safety and tolerability of Gliptar produced by PJSC “Kievmedpreparat” (Ukraine) in the treatment of patients with type 2 DM. Materials and methods. The study included 49 patients with type 2 DM. They received metformin monotherapy at a dose of at least 1,000 mg daily for at least the last six months. Duration of type 2 DM averaged 6.2 ± 1.8 years. The patients formed two groups for follow-up. The first group consisted of 29 patients who were still taking metformin doses up to 2,000 mg/day and additionally received Gliptar (vildagliptin) at a dose of 50 mg twice daily. Patients in the second group (n = 20) continued to receive metformin twice daily at a dose of 2,000 mg/day. Results. After 12 weeks in patients of the first group on the background of metformin therapy combined with vildagliptin, the level of HbA1c decreased significantly to 6.42 ± 0.21 %, fasting glycemia — to 6.14 ± 0.22 mmol/l, postprandial glycemia — to 8.63 ± 0.23 mmol/l. On the background of combined treatment, patients with type 2 DM had a decrease in body weight by 1.18 kg, as well as a tendency to decrease in body mass index from 31.49 ± 1.08 kg/m2 to 29.98 ± 0.76 kg/m2. After treatment, the level of immunoreactive insulin in the first group was 14.08 ± 1.83 µU/ml (baseline 21.11 ± 2.03 µU/ml), HOMA-IR — 3.14 ± 0.21 (baseline 6.28 ± 1.42). A significant decrease in carbohydrate metabolism and insulin resistance can be assessed as a positive trend in combination therapy. Conclusions. Given the benefits of dual therapy in the treatment of patients with type 2 DM, according to conventional step-by-step therapy, in the second stage it is advisable to prescribe vildagliptin to patients who receive metformin and who have not reached the target glycemic control. Combination therapy of vildagliptin and metformin provides a comprehensive effect on cardiovascular risk factors in the form of preventing hyperinsulinemia and reducing insulin resistance.
цукровий діабет 2-го типу; вілдагліптин; глікований гемоглобін; інсулінорезистентність
сахарный диабет 2-го типа; вилдаглиптин; гликированный гемоглобин; инсулинорезистентность
type 2 diabetes mellitus; vildagliptin; glycated hemoglobin; insulin resistance
Вступ
Інгібітори дипептидилпептидази 4-го типу (ДПП-4), маючи інкретинову активність, впливають на основні патогенетичні механізми цукрового діабету (ЦД) 2-го типу. Вілдагліптин — інноваційний препарат класу інгібіторів ДПП-4 з унікальною фармакокінетикою, ефективність і безпека якого вивчена в плацебо-контрольованих дослідженнях у моно- або комбінованій терапії ЦД 2-го типу [1–3]. Препарат стійко знижує рівень глікованого гемоглобіну (HbA1c), не збільшує ризик гіпоглікемії і серцево-судинної патології [4, 5].
Інгібітори дипептидилпептидази 4-го типу (ДПП-4) підвищують рівень ендогенного інсуліну, знижують рівень глюкагону в плазмі крові й пригнічують глюконеогенез у печінці, зменшують інсулінорезистентність, забезпечуючи повноцінний глікемічний контроль [6, 7]. Вілдагліптин (LAF237) — високоселективний інгібітор ДПП-4, який запобігає швидкому руйнуванню дипептидилпептидази-1 (ДПП-1) і глюкозозалежного інсулінотропного поліпептиду (ГІП), у результаті чого фізіологічна дія інкретинових гормонів на клітини острівцевого апарату підшлункової залози подовжується. Тривалість такої дії залежить в основному від того, наскільки повного пригнічення вдається досягнути [6, 8]. З огляду на кристалічну структуру хімічно споріднених піролідинових нітрилів інгібіторів ДПП-4 можна вважати, що вілдагліптин є повільним субстратом для ДПП-4, який блокує інактивацію ДПП-1 і ГІП протягом 24 годин і утворює зворотну ковалентну сполуку з активною сериновою ділянкою ДПП-4. Це сприяє протонуванню сусіднього амінокислотного залишку й призводить до морфологічних змін ділянки зв’язування, що пояснює істотно більш сприятливий добовий профіль ДПП-1 і глюкагону на терапії вілдагліптином [7–9].
Вілдагліптин уповільнює деградацію інкретинів в організмі й подовжує дію ендогенних інкретинів. У результаті стимулюється секреція інсуліну, однак лише за умов, якщо рівень глікемії перевищує норму. При цьому пригнічується секреція глюкагону, стимулюється проліферація бета-клітин і відновлюється певною мірою зменшений при ЦД 2-го типу пул бета-клітин острівців Лангерганса підшлункової залози [10].
Також показано, що на терапії вілдагліптином збільшення рівня концентрації ДПП-1, що спостерігається відразу після прийому їжі, зберігається на високому рівні протягом більш тривалого періоду часу порівняно із ситагліптином [11, 12]. У клінічних дослідженнях з вивчення впливу вілдагліптину на функцію острівцевих клітин підшлункової залози було продемонстровано покращання глюкозозалежної регуляції вуглеводного обміну. Так, у періоди гіперглікемії в результаті покращання чутливості α- і β-клітин до глюкози співвідношення інсуліну й глюкагону збільшується, знижуючи тим самим рівень глікемії, а також швидкість продукування глюкози в печінці. Зниження надмірного рівня глюкагону під час їжі, у свою чергу, викликає зменшення інсулінорезистентності. При наростаючій тенденції до гіпоглікемії співвідношення інсуліну й глюкагону, навпаки, починає знижуватися, і під впливом цього процесу відбувається стимуляція вироблення глюкози печінкою, що дозволяє пацієнтові уникнути тяжкої гіпоглікемії. У той же час у дослідженнях в осіб без ЦД2-го типу вілдагліптин не стимулював секрецію інсуліну, а також не впливав на рівень глюкагону [13], що підтверджує фізіологічність дії даного препарату.
Метою дослідження було вивчення фармакотерапевтичної ефективності, безпеки й переносимості препарату Гліптар виробництва ПАТ «Київмедпрепарат» (Україна) в терапії хворих на цукровий діабет 2-го типу.
Матеріали та методи
У дослідження було включено 49 пацієнтів із ЦД 2-го типу (середній вік — 51,7 ± 1,8 року) з рівнем глікованого гемоглобіну (HbA1c) у межах 7,2–9,0 %. До включення в дослідження хворі отримували монотерапію метформіном у дозі не менше за 1000 мг на добу принаймні упродовж останніх шести місяців. Тривалість перебігу ЦД 2-го типу в середньому становила 6,2 ± 1,8 року. Середній показник маси тіла дорівнював 87,3 ± 6,2 кг, індекс маси тіла (ІМТ) — 31,58 ± 1,28 кг/м2. Артеріальна гіпертензія встановлена в 38 пацієнтів (77,6 %). Рівень артеріального тиску (АТ) у середньому становив: систолічного — 138,4 ± 11,2 мм рт.ст., діастолічного — 86,8 ± 5,7 мм рт.ст. У процесі спостереження додаткова корекція АТ не здійснювалася. Нормальні показники ліпідограми відзначалися лише в 7 хворих (14,3 %), в інших випадках (85,7 %, n = 42) спостерігалися різні порушення ліпідного обміну.
Пацієнти сформували дві групи для подальшого спостереження. 29 пацієнтам, які до цього часу отримували препарати метформіну в дозі до 2000 мг/добу, був додатково призначений препарат Гліптар (вілдагліптин) у дозі 50 мг двічі на добу (перша група). Пацієнти другої групи (n = 20) продовжували прийом метформіну двічі на день у дозі 2000 мг/добу. Пацієнтам проводили обстеження на першому, четвертому, восьмому і дванадцятому тижнях спостереження. Здійснювали періодичний контроль антропометричних параметрів і показників вуглеводного обміну, інші методи додаткового обстеження застосовували на початку й через 12 тижнів терапії.
Стан вуглеводного обміну оцінювали за рівнем глюкози в капілярній крові натще й через 2 години після їжі (постпрандіально) і за рівнем HbA1c. Ступінь інсулінорезистентності оцінювали за допомогою математичної моделі HOMA-IR. Визначення індексу HOMA-IR проводили за формулою: інсулін натще (мкОд/мл) × глюкоза крові натще (ммоль/л)/22,5. Нормальним вважали показник < 2,77. Ліпідний спектр оцінювали за показниками загального холестерину, холестерину ліпопротеїнів високої щільності, холестерину ліпопротеїнів низької щільності (ЛПНЩ), холестерину ліпопротеїнів дуже низької щільності (ЛПДНЩ). Концентрацію холестерину ЛПДНЩ і ЛПНЩ визначали за формулою Фрідвальда. Уміст імунореактивного інсуліну (ІРІ) в сироватці венозної крові визначали радіоімунологічним методом. Згідно з нормативами використаної в роботі методики концентрацію ІРІ натще вважали нормальною, якщо вона не перевищувала 25,0 мкОд/мл. Для оцінки безпеки застосування препарату визначалися такі лабораторні показники: загальний аналіз крові, загальний аналіз сечі, біохімічний аналіз крові (креатинін, сечовина, активність АЛТ, АСТ).
Обробку даних проводили методом варіаційної статистики з визначенням середньої арифметичної (М) і похибки середньої (m), використовуючи персональний комп’ютер з пакетом програм для автоматизації статистичних досліджень Statistica 10. Кількісні результати порівнювали із застосуванням критерію Стьюдента й поправки Бонферроні, точного критерію Фішера. Відмінності вважали статистично вірогідними при р < 0,05.
Протокол клінічного дослідження, інформація для пацієнта й форма інформованої згоди були схвалені комісією з етики при Українському науково-практичному центрі ендокринної хірургії, транс–плантації ендокринних органів і тканин МОЗ України (протокол № 2 від 10.06.2019). Усіма учасниками дослідження підписана форма інформованої згоди.
Результати
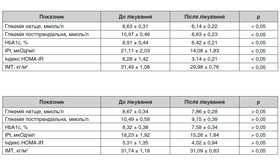
В усіх 29 хворих групи комбінованої терапії на момент початку дослідження відзначалася гіперглікемія, підтверджена лабораторними даними. Так, глікемія натще становила 8,63 ± 0,31 ммоль/л; постпрандіальна — 10,97 ± 0,46 ммоль/л. При цьому HbA1c дорівнював 8,91 ± 0,43 %, індекс HOMA-IR — 5,94 ± 1,42 (табл. 1).
Через 12 тижнів у хворих першої групи на тлі терапії метформіном у поєднанні з вілдагліптином рівень НbА1с вірогідно знизився до 6,42 ± 0,21 %, глікемія натще — до 6,14 ± 0,22 ммоль/л, глікемія постпрандіальна — до 8,63 ± 0,23 ммоль/л. На тлі лікування у хворих на ЦД 2-го типу відзначалося зниження маси тіла на 1,18 кг, а також тенденція до зниження показника ІМТ з 31,49 ± 1,08 кг/м2 до 29,98 ± 0,76 кг/м2. Рівень ІРІ становив після лікування в першій групі 14,08 ± 1,83 мкОд/мл (при початковому 21,11 ± 2,03 мкОд/мл), індекс HOMA-IR — 3,14 ± 0,21 (проти початкового 6,28 ± 1,42). Вірогідне зниження показників вуглеводного обміну, інсулінорезистентності можна оцінювати як позитивну динаміку завдяки комбінованому лікуванню (табл. 1).
Так, у результаті додаткового призначення вілдагліптину в поєднанні з метформіном досягнутий глікемічний контроль із рівнем HbA1c ≤ 7 % у 75,9 % (n = 22) хворих, з рівнем HbA1c 7,1–8 % — у 24,1 % (n = 7) спостережень.
При оцінці взаємозв’язків лабораторних показників, що характеризують вуглеводний обмін та інсулінорезистентність, нами були отримані такі дані: найбільш виражена кореляційна залежність відзначена між показниками ІРІ та HOMA-IR (r = 0,91). Рівень ІРІ натще слабо корелював з глікемією натще (r = 0,083). Виявлений кореляційний зв’язок між рівнем HOMA-IR і глікемією натще (r = 0,36). Отримані дані свідчать про те, що зниження глікемії натще відбувається головним чином за рахунок зменшення інсулінорезистентності.
У хворих другої групи вірогідних змін показників вуглеводного обміну й інсулінорезистентності не спостерігалося (табл. 2).
Порівняння отриманих показників вказує на ефективність вілдагліптину на периферичному рівні й покращання чутливості периферичних тканин до дії власного інсуліну. При вивченні параметрів ліпідного обміну до і після лікування вірогідних відмінностей у групах дослідження не виявлено. Через 12 тижнів терапії метформіном у комбінації з вілдагліптином встановлено зниження значень систолічного й діастолічного АТ порівняно з початковими показниками на 5–10 мм рт.ст., здебільшого в пацієнтів з істотним зниженням маси тіла й покращанням глікемічного контролю. При порівняльній оцінці показників АТ відмінностей між хворими обох груп знайдено не було.
Аналіз безпеки здійснювали за показниками загального аналізу крові, загального аналізу сечі, біохімічного аналізу крові (креатинін, сечовина, активність АЛТ, АСТ). Дослідження креатиніну, сечовини, АСТ і АЛТ показало відсутність токсичного впливу препарату вілдагліптину. Рівень креатиніну у хворих другої групи становив 72,24 ± 11,68 мкмоль/л, у першій групі (прийом вілдагліптину і метформіну) — 71,62 ± 10,57 мкмоль (норма 44–88 мкмоль/л). Уміст сечовини в крові хворих другої групи становив 5,84 ± 1,22 ммоль/л; у хворих першої групи на тлі прийому вілдагліптину і метформіну — 5,72 ± 1,16 ммоль/л (норма 2,5–8,3 ммоль/л). Показник АСТ дорівнював у пацієнтів на монотерапії метформіном 22,84 ± 5,14 МО; на комбінованій терапії метформіном і вілдагліптином — 19,91 ± 4,76 МО (норма 2–25 МО). При цьому показники АЛТ становили відповідно 26,23 ± 5,19 МО і 23,31 ± 4,93 МО (норма 2–25 МО) відповідно. Результати загального аналізу крові й загального аналізу сечі також не виявили відхилень від норми в пацієнтів обох груп.
Побічних реакцій і небажаних явищ упродовж спостереження у хворих першої та другої груп не зареєстровано.
Обговорення
Традиційно і згідно з міжнародними настановами фармакотерапія ЦД 2-го типу таблетованими антигіперглікемічними препаратами ініціюється метформіном. Встановлено, що після трьох років лікування приблизно в 50 % пацієнтів із ЦД можна досягнути цільових рівнів глікемії при монотерапії, однак через 9 років цей показник знижується до 25 % [14]. Отже, стає необхідним застосування комбінованої терапії. Протягом останніх десятиліть поєднання метформіну з похідними сульфонілсечовини найчастіше використовувалося в клінічній практиці.
Потім у терапію ЦД 2-го типу увійшли меглітинід, глітазони й інгібітори альфа-глюкозидази, але всі згадані групи препаратів асоціювалися з різним ступенем небажаних або навіть тяжких серцево-судинних подій. Надалі були синтезовані інгібітори ДПП-4, які успішно застосовуються при лікуванні ЦД 2-го типу, покращуючи функцію ендотелію, знижуючи рівні маркерів запалення й оксидативний стрес. Крім того, повідомлялося про підвищення рівня адипонектину, зниження гіперліпідемії і АТ на тлі лікування вілдагліптином [15].
ЦД 2-го типу — прогресуюче захворювання, і монотерапія не забезпечує належного глікемічного контролю в довгостроковій перспективі. Похідні сульфонілсечовини, що мають тривалу історію застосування, традиційно використовувалися як препарати другої лінії, які додаються до метформіну при погіршенні глікемічного контролю. Однак їх використання пов’язане з небажаними побічними ефектами, у тому числі підвищеним ризиком гіпоглікемії і збільшенням маси тіла [16]. Інгібітори ДПП-4 не поступаються похідним сульфонілсечовини за ефективністю, але не призводять до гіпоглікемічних реакцій або збільшення маси тіла, позбавлені багатьох побічних ефектів і, як показали великі проспективні дослідження, не збільшують серцево-судинні ризики [17].
Фізіологічно обґрунтована комбінація метформіну і вілдагліптину дозволяє впливати на основні патогенетичні механізми розвитку ЦД 2-го типу. До клінічних переваг поєднаного використання вілдагліптину і метформіну належить потенціювання й посилення цукрознижувального ефекту, низький ризик гіпоглікемії, відсутність збільшення маси тіла пацієнта, збереження плейотропних ефектів метформіну, передбачувана здатність зберігати й відновлювати функцію бета-клітин. Тому метформін і вілдагліптин можуть синергічно підсилювати й подовжувати інкретинову активність [18–21].
При виборі цукрознижувальної терапії як важливий критерій розглядається безпечне досягнення контролю глікемії, відсутність тяжких гіпоглікемій і алергічних реакцій [19]. Перевагою застосування в пацієнтів із ЦД 2-го типу комбінації метформіну й вілдагліптину можна вважати добру переносимість препарату, відзначену в клінічних умовах. При цьому не зареєстровано гіпоглікемічних станів, а оцінка суб’єктивної переносимості за результатами опитування пацієнтів була високою.
Отже, переваги комбінованої терапії порівняно з монотерапією метформіном полягають у високій вибірковості дії вілдаліптину, що на тлі багатофокусного впливу метформіну дає безпечний цукро–знижувальний ефект, впливаючи на основні патогенетичні механізми розвитку ЦД 2-го типу.
E. Bekiari із співавт. провели систематичний огляд і метааналіз інформації (69 досліджень, 28 006 пацієнтів), присвячений ефективності й безпеці вілдагліптину в лікуванні ЦД 2-го типу. Порівняно з плацебо рівень НbА1с на терапії вілдагліптином вірогідно знижувався без збільшення ризику гіпоглікемії, не зростала частота виникнення панкреатиту й інших серйозних небажаних явищ або летального кінця [8].
Отже, вілдагліптин успішно застосовується у комбінованій терапії ЦД 2-го типу, має плейотропну дію, забезпечує серцево-судинну безпеку, ефективний при патології печінки і нирок, позитивно впливає на стан при артеріальній гіпертензії та асоціюється з низьким ризиком гіпоглікемій. Це визначає високу прихильність пацієнтів до такого лікування й забезпечує можливість його використання при коморбідній патології.
Висновки
У результаті додаткового призначення вілдагліптину (препарат Гліптар виробництва ПАТ «Київмедпрепарат», Україна) у поєднанні з метформіном досягнутий глікемічний контроль з рівнем HbA1c ≤ 7 % у 75,9 % (n = 22) хворих, у решті спостережень (24,1 %, n = 7) рівень HbA1c становив 7,1–8 %. На тлі лікування вілдагліптином у хворих на ЦД 2-го типу відзначалися зниження маси тіла на 1,18 кг, а також тенденція до зниження показника ІМТ з 31,49 ± 1,08 кг/м2 до 29,98 ± 0,76 кг/м2. Рівень ІРІ становив після лікування в першій групі 14,08 ± 1,83 мкОд/мл (при початковому 21,11 ± 2,03 мкОд/мл), індекс HOMA-IR — 3,14 ± 0,21 (проти початкового 6,284 ± 1,42).
З огляду на отримані переваги подвійної терапії в лікуванні хворих на ЦД 2-го типу відповідно до загальноприйнятої покрокової терапії на другому етапі пацієнтам, які отримують метформін і не досягли цільового глікемічного контролю, серед препаратів доцільно призначати препарат вілдагліптину.
Комбінована терапія вілдагліптином у поєднанні з метформіном забезпечує комплексну дію на чинники ризику серцево-судинних захворювань у вигляді запобігання розвитку гіперінсулінемії та зниження інсулінорезистентності.
Відзначаються добра переносимість і високий ступінь безпеки препарату впродовж періоду спостереження.
Конфлікт інтересів. Не заявлений.

/531-1.jpg)