Журнал «Медицина неотложных состояний» Том 16, №1, 2020
Вернуться к номеру
Порівняння показників гемодинаміки й вентиляції при використанні різних методик анестезіологічного забезпечення лапароскопічної холецистектомії
Авторы: Машин О.М.
ДЗ «Дніпропетровська медична академія МОЗ України», м. Дніпро, Україна
Рубрики: Медицина неотложных состояний
Разделы: Клинические исследования
Версия для печати
Актуальність. Поширюється використання лапароскопічних оперативних втручань, у тому числі в осіб похилого віку з серйозними супутніми захворюваннями. Ретроспективне вивчення ускладнень, що мали місце при проведенні лапароскопічних оперативних втручань, продемонструвало, що абсолютна їх більшість не пов’язана з технікою операції, а обумовлена розвитком серцевих і легеневих порушень. Мета: оцінка ефективності та безпеки різних варіантів анестезіологічного забезпечення лапароскопічної холецистектомії на підставі дослідження динаміки основних гемодинамічних і вентиляційних параметрів гомеостазу у хворих у періопераційному періоді. Матеріали та методи. Обстежено 120 пацієнтів (середній вік — 50 (38–63) років), яким виконувались оперативні втручання з приводу жовчнокам’яної хвороби та гострого холециститу методом лапароскопічної холецистектомії. Хворі були розподілені на 3 групи дослідження. Група TIVA (n = 40) — тотальна внутрішньовенна анестезія (ТВА) на основі пропофолу та фентанілу з інфузією гіпнотика через перфузор. Швидкість інфузії пропофолу за розробленою болюсно-інфузійною схемою 10–8–6; анестезіолог самостійно вибирав достатню, на його думку, швидкість інфузії пропофолу. Група SEVO (n = 40) — інгаляційна анестезія на основі севофлурану методом низького потоку та фентанілу. Група ТСІ (n = 40) — ТВА на основі пропофолу та фентанілу з інфузією гіпнотика за цільовою концентрацією за допомогою перфузора B. Braun perfusor space; анестезіолог не повинен був порушувати нижню (3,5 мкг/мл) і верхню (5,5 мкг/мл) межі цільових концентрацій препарату в ефекторних зонах (математична модель Shnеider). Результати. Показники гемодинаміки в усіх групах мали закономірні коливання під час анестезіологічної підготовки пацієнтів на етапах інсуфляції вуглекислого газу в черевну порожнину та десуфляції. Внутрішньочеревний тиск у пацієнтів усіх груп не перевищував 10 мм рт.ст. Під час індукції в анестезію відмічалося зниження показників системної та центральної гемодинаміки. Так, показники середнього артеріального тиску порівняно з вихідними даними зменшувалися на 17,70 ± 2,33 %, особливо у пацієнтів групи TIVA (p < 0,001). Подібні зміни пов’язані з тим, що препарати, які використовувалися для індукції анестезії, знижували тонус симпатичної нервової системи, перерозподіляли обсяг циркулюючої крові в ємнісну судинну мережу, шо сприяло зменшенню переднавантаження, а також за рахунок периферичної вазодилатації. На етапі інтубації також відзначалася зміна показників гемодинаміки за типом гіпердинамічної реакції, що було обумовлено симпатоадреналовою реакцією на ларингоскопію та інтубацію. Більш виражені зміни відзначалися в групі TIVA. Так, показники середнього артеріального тиску порівняно з попереднім етапом збільшувалися на 22,2 ± 2,9 % (р < 0,001). Співставлення змін показників гемодинаміки залежно від варіанту анестезіологічного забезпечення показало їх статистичну порівнянність (p > 0,05) і менш виражені коливання у групах TCI і SEVO, ніж у групі з тотальною внутрішньовенною анестезією (TIVA). Аналіз показників вентиляції легень та оксигенації (SaO2, EtCO2) в умовах пневмоперитонеуму показав їх стабільність та керованість у пацієнтів усіх груп. Випадків підвищення EtCO2 більше 45 мм рт.ст. не виявлено, всі анестезії проводилися в умовах помірної гіпервентиляції. Водночас показники середнього тиску у дихальних шляхах були вірогідно вищими при застосуванні тотальної внутрішньовенної анестезії з цільовою концентрацією анестетика (група ТСІ) та при застосуванні тотальної внутрішньовенної анестезії (група TIVA), ніж при використанні інгаляційного анестетика. Це обумовлено бронходилатаційним ефектом севофлурану, проведенням низькопоточної інгаляційної анестезії. Висновки. Порівняльні дослідження між групами мають незначні відмінності при використанні севофлурану та пропофолу за методом ТСІ як складової анестезіологічного забезпечення. Найкраща стабільність та передбачуваність змін гемодинаміки в інтраопераційному періоді були виявлені в групах із застосуванням інгаляційної низькопоточної анестезії севофлураном та інфузією пропофолу за цільовою концентрацією (ТСІ). Підвищений внутрішньочеревний тиск до 10 мм вод.ст. за рахунок карбоксіперитонеуму тривалістю до 1 години на умовах використання інгаляційного агента севофлуран методом низького потоку або при внутрішньовенній анестезії пропофолом не викликає суттєвих змін показників вентиляції й оксигенації та легко піддається корекції зміною налаштування параметрів вентиляції.
Актуальность. Все шире используются лапароскопические оперативные вмешательства, в том числе у лиц пожилого возраста с серьезными сопутствующими заболеваниями. Ретроспективное изучение осложнений, которые имели место при проведении лапароскопических оперативных вмешательств, продемонстрировало, что абсолютное их большинство не связано с техникой операции, а обусловлено развитием сердечных и легочных нарушений. Цель: оценка эффективности и безопасности различных вариантов анестезиологического обеспечения лапароскопической холецистэктомии на основании исследования динамики основных гемодинамических и вентиляционных параметров гомеостаза у больных в периоперационном периоде. Материалы и методы. Обследовано 120 пациентов (средний возраст — 50 (38–63) лет), которым выполнялись оперативные вмешательства по поводу желчнокаменной болезни и острого холецистита методом лапароскопической холецистэктомии. Больные были разделены на 3 группы исследования. Группа TIVA (n = 40) — тотальная внутривенная анестезия (ТВА) на основе пропофола и фентанила с инфузией гипнотика через перфузор. Скорость инфузии пропофола осуществлялась по разработанной болюсно-инфузионной схеме 10–8–6; анестезиолог самостоятельно выбирал достаточную, по его мнению, скорость инфузии пропофола. Группа SEVO (n = 40) — ингаляционная анестезия на основе севофлурана методом низкого потока и фентанила. Группа ТСI (n = 40) — ТВА на основе пропофола и фентанила с инфузией гипнотика по целевой концентрации с помощью перфузора B. Braun perfusor space; анестезиолог не должен был нарушать нижнюю (3,5 мкг/мл) и верхнюю (5,5 мкг/мл) границы целевых концентраций препарата в эффекторных зонах (математическая модель Shnеider). Результаты. Показатели гемодинамики во всех группах имели закономерные колебания во время анестезиологической подготовки пациентов на этапах инсуффляции углекислого газа в брюшную полость и десуффляции. Внутрибрюшное давление у пациентов всех групп не превышало 10 мм рт.ст. Во время индукции в анестезию отмечалось снижение показателей системной и центральной гемодинамики. Так, показатели среднего артериального давления по сравнению с исходными данными уменьшались на 17,70 ± 2,33 %, особенно у пациентов группы TIVA (p < 0,001). Подобные изменения связаны с тем, что препараты, которые использовались для индукции анестезии, снижали тонус симпатической нервной системы, перераспределяли объем циркулирующей крови в емкостную сосудистую сеть, что способствовало уменьшению преднагрузки, а также за счет периферической вазодилатации. На этапе интубации также отмечалось изменение показателей гемодинамики по типу гипердинамической реакции, что было обусловлено симпатоадреналовой реакцией на ларингоскопию и интубацию. Более выраженные изменения отмечались в группе TIVA. Так, показатели среднего артериального давления по сравнению с предыдущим этапом увеличивались на 22,2 ± 2,9 % (р < 0,001). Сопоставление изменений показателей гемодинамики в зависимости от варианта анестезиологического обеспечения показало их статистическую сопоставимость (p < 0,05) и менее выраженные колебания в группах TCI и SEVO, чем в группе с тотальной внутривенной анестезией (TIVA). Анализ показателей вентиляции легких и оксигенации (SaO2, EtCO2) в условиях пневмоперитонеума показал их стабильность и управляемость у пациентов всех групп. Случаев повышения EtCO2 более 45 мм рт.ст. не обнаружено, все анестезии проводились в условиях умеренной гипервентиляции. В то же время показатели среднего давления в дыхательных путях были достоверно выше при применении тотальной внутривенной анестезии с целевой концентрацией анестетика (группа ТСI) и при применении тотальной внутривенной анестезии (группа TIVA), чем при использовании ингаляционного анестетика. Это обусловлено бронходилатирующим эффектом севофлурана, проведением низкопоточной ингаляционной анестезии. Выводы. Сравнительные исследования между группами имеют незначительные различия при использовании севофлурана и пропофола по методу ТСІ как составляющей анестезиологического обеспечения. Лучшая стабильность и предсказуемость изменений гемодинамики в интраоперационном периоде были обнаружены в группах с применением ингаляционной низкопоточной анестезии севофлураном и инфузии пропофола по целевой концентрации (ТСI). Повышенное внутрибрюшное давление до 10 мм вод.ст. за счет карбоксиперитонеума продолжительностью до 1 часа при использовании ингаляционного агента севофлуран методом низкого потока или при внутривенной анестезии пропофолом не вызывало существенных изменений показателей вентиляции и оксигенации и легко поддавалось коррекции изменением настройки параметров вентиляции.
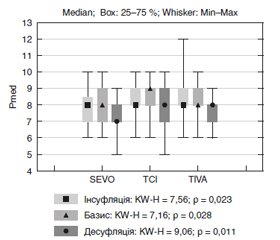
Laparoscopic surgical interventions are increasingly being introduced, including in the elderly with serious concomitant diseases. A retrospective study of the complications that occurred during laparoscopic surgical interventions demonstrated that their absolute majority is not related to the technique of surgery, but is due to the development of cardiac and pulmonary disorders. The study aimed to assess the effectiveness and safety of various approaches to the anesthetic management of laparoscopic cholecystectomy, based on a study of the dynamics of the main hemodynamic and ventilation parameters of homeostasis in patients in the perioperative period. Materials and methods. One hundred and twenty patients (mean age 50 (38–63) years) who underwent surgical interventions for gallstone disease and acute cholecystitis using laparoscopic cholecystectomy were examined. Patients were divided into 3 study groups: TIVA group (n = 40) — total intravenous anesthesia (TIVA) based on propofol and fentanyl with hypnotic infusion through the perfusor. Propofol infusion rate was carried out according to the bolus-infusion scheme 10–8–6 developed. The anesthetist independently chose a sufficient, to his opinion, propofol infusion rate; SEVO group (n = 40) — inhalation anesthesia based on sevoflurane low flow and fentanyl; TCI group (n = 40) — TIVA based on propofol and fentanyl with hypnotic infusion at the target concentration using the B. Braun Perfusor Space; an anesthetist was not supposed to violate the lower (3.5 μg/ml) and upper (5.5 μg/ml) boundaries of the target concentrations in the effector zones (Shneider mathematical model). Results. The hemodynamic parameters in all groups had regular fluctuations during the anesthetic preparation of patients at the stages of carbon dioxide insufflation in the abdominal cavity and desufflation. Intra-abdominal pressure in patients of all groups did not exceed 10 mm Hg. During the induction of anesthesia, a decrease in systemic and central hemodynamics was noted. Thus, the average blood pressure compared with the initial level decreased by 17.7 ± 2.33 %, especially in patients of the TIVA group (p < 0.001). Such changes are due to the fact that the drugs used to induce anesthesia reduced the tone of the sympathetic nervous system, redistributed the volume of circulating blood to the capacitive vasculature, which helped to reduce preload, as well as due to the peripheral vasodilation. At the stage of intubation, there was also a change in hemodynamic parameters in the form of a hyperdynamic type of reaction, which was due to the sympathoadrenal reaction to laryngoscopy and intubation. More pronounced changes were noted in the TIVA group. Thus, the average blood pressure compared with the previous stage increased by 22.2 ± 2.9 % (p < 0.001). Comparison of changes in hemodynamic parameters depending on the variant of anesthetic management showed their statistical comparability (p < 0.05) and less pronounced fluctuations in the TCI and SEVO groups than in the group with total intravenous anesthesia. The analysis of lung ventilation and oxygenation (SaO2, EtCO2) in conditions of pneumoperitoneum showed their stability and controllability in patients of all groups. There were no cases of increased EtCO2 over 45 mm Hg and all anesthesia were performed under moderate hyperventilation. At the same time, the medium airway pressure (Pmed) was significantly higher with total intravenous anesthesia with a target concentration of anesthetic (TCI group) and with total intravenous anesthesia (TIVA group) than with an inhaled anesthetic. This is due to the bronchodilation effect of sevoflurane, low-flow inhalation anesthesia. Conclusions. A comparative study showed insignificant differences when using sevoflurane and propofol according to the TCI. The best stability and predictability of hemodynamic changes in the intraoperative period was found in groups using inhaled low-flow anesthesia with sevoflurane and propofol infusion at the target concentration (TCI). Increased abdominal pressure up to 10 mm H2O due to carboxyperitoneum lasting up to 1 hour when using the sevoflurane inhalation agent by the low-flow method or with intravenous anesthesia with propofol, it did not cause significant changes in ventilation and oxygenation parameters and was easily amenable to correction by changing the ventilation parameter settings.
холецистектомія; лапароскопія; інгаляційна анестезія; esCCO-моніторинг; анестезіологія
холецистэктомия; лапароскопия; ингаляционная анестезия; esCCO-мониторинг; анестезиология
cholecystectomy; laparoscopy; inhalation anesthesia; esCCO-monitoring; anesthesiology
Вступ
Матеріали та методи
Результати та обговорення
/111.jpg)
Висновки
1. Nagy A.G., Poulin E.C., Girotti M.J. History of laparoscopic surgery. Can. J. Surg. 1992. Vol. 35. P. 271-274.
2. Seed R.F., Shakespeare T.F., Muldoon M.J. Carbon dioxide hemostasis during anesthesia for laparoscopy. Anaesth. 1970. Vol. 25(2). P. 223-225
3. Cunningham A.J., Sorin J.B. Laparoscopic cholecystectomy: anesthetic implications. Anesth. Analg. 1993. Vol. 76. P. 1120-1124.
4. Loder W.A., Minnich M., Brotman S. Hemodynamic effects of laparoscopic cholecystectomy. American Surg. 1994. Vol. 60. P. 322-325.
5. Караваев Б.И., Головкин А.С., Стамов В.И. Применение методики транспищеводной эхо- и допплерографии для оценки изменений показателей гемодинамики при лапароскопических операциях. Вестник интенсивной терапии. 2006. № 3. С. 48-51.
6. Лебединский К.М. Мониторинг артериального давления. СПб., 2009.
7. Kelman G., Swapp G. Cardiac output and arterial blood gas tension during laparoscopy. Br. J. Anaesth. 1972. Vol. 44. P. 1155-1158.
8. Richardson J.D., Trincle K. Hemodynamic and respiratory alterations with increased intraabdominal pressure. J. Surg. Res. 1976. Vol. 20. P. 401-403.
9. Nesek-Adam V., Mrsić V., Smiljanić A. Pathophysiologic effects of CO2-pneumoperitoneum in laparoscopic surgery. Acta Med. Croatica. 2007. Vol. 61(2). P. 165-170.
10. Puri J.D., Singh H. Ventilatory effects of laparoscopy under general anesthesia. J. Anesth. 1992. Vol. 68. P. 211-214.
11. Бутров A.B., Рыбина Д.М., Онегин М.А. Анестезия севофлураном при лапароскопических холецистэктомиях. Вестник интенсивной терапии. 2007. № 5. С. 11-12.

/109.jpg)
/110.jpg)