Вступ
Діагноз «гостра печінкова недостатність» часто використовується як узагальнюючий термін опису гострого епізоду дисфункції печінки. Проте в контексті гепатологічної практики гостра печінкова недостатність (ГПН) належить до високоспецифічного синдромокомплексу, що достатньо рідко зустрічається і характеризується різними абнормальними змінами лабораторних показників за умов відсутності в анамнезі хронічних захворювань печінки.
Класично прогресування захворювання супроводжується розвитком коагулопатії печінкового генезу і проявами порушення свідомості з розвитком енцефалопатії. Термін «гостра печінкова недостатність» часто помилково використовується в разі гострого погіршення перебігу хронічних захворювань печінки (acute-on-chronic liver failure — AoCLF) чи прояву печінкової недостатності на фоні інших системних захворювань. Вторинне пошкодження печінки на фоні тривалого прийому алкоголю чи проявів інших форм хронічного ураження печінки часто складно віддиференціювати від гострого стану, що потребує проведення додаткових діагностичних заходів, а отже, й інших підходів до лікування.
Так, наприклад, при розширеній резекції печінки в пацієнтів із попередніми проявами хронічної печінкової недостатності чи без них також можуть виникати синдроми жовтяниці, коагулопатії та печінкової енцефалопатії (ПЕ), прояв яких дуже нагадує картину так званого малого синдромокомплексу, також характерного і для післяопераційного періоду після трансплантації печінки.
У контексті гепатологічної практики ГПН належить до високоспецифічного синдрому, що супроводжується різкими змінами в лабораторних показниках печінкових ферментів без попередніх симптомів хронічних захворювань печінки. Перебіг захворювання характеризується розвитком коагулопатії печінкового генезу, що відрізняється від коагуляційних зрушень при септичних станах, та порушенням рівня свідомості аж до розвитку ПЕ. У разі розвитку печінкової коагулопатії без проявів порушення свідомості такий стан у пацієнтів має назву «гостре ураження печінки» (Acute Liver injury — ALI). Також прояви коагулопатії, зростання рівня трансаміназ, підвищення рівня білірубіну, порушення рівня свідомості можуть виникати в пацієнтів із різними системними захворюваннями. У таких пацієнтів за умови відсутності анамнестичних даних про первинне ураження печінки надання допомоги слід зосередити на лікуванні супутніх захворювань [1].
Рекомендації стосовно діагностики і лікування ГПН, які наведені нижче, класифіковані згідно із системою Grading of Recommendations Assessment Development and Evaluation (GRADE).
Визначення й основні клінічні прояви ГПН
Клінічні прояви ГПН асоціюються з гострим ураженням печінки і характеризуються підвищенням у 2–3 рази рівня трансаміназ (як маркер пошкодження печінки), жовтяницею і коагулопатією. Такі ж зміни підходять і до опису проявів, характерних при застосуванні гепатотоксичних медичних препаратів за умови наявних в анамнезі даних про їх прийом.
Уперше термін «гостра печінкова недостатність» був використаний Trey і Davidson у 1970 році для опису фульмінантної печінкової недостатності як «...потенційно оборотного стану, що виник внаслідок важкої травми печінки, і супроводжувався наростанням ознак печінкової енцефалопатії протягом 8 тижнів без раніше діагностованих захворювань печінки» [2]. У 1993 році визначення терміна було переоцінене і перефразоване з урахуванням етіології, частоти розвитку ускладнень і прогнозу (табл. 2).
/115.jpg)
Гостра печінкова недостатність розвивається, коли в пацієнтів виникають симптоми ПЕ з 8-го по 28-й день із моменту виникнення симптомів жовтяниці. Тривалість захворювання більше 28 тижнів перед виникненням симптомів енцефалопатії належить до категорії хронічного захворювання печінки. За визначенням Міжнародної асоціації з вивчення захворювань печінки (The International Association for the Study of the Liver — IASL) у заяві субкомітету (1999) визначили як надгостру печінкову недостатність терміном менше 10 днів, до фульмінантної форми належить ГПН, що розвивається в межах від 10 до 30 днів, та підгострої, що розвивається протягом 5–24 тижнів [3]. Симптоми надгострої форми ГПН охоплюють гостру коагулопатію, значне зростання сироваткових трансаміназ та помірне початкове підвищення рівня білірубіну. Зі свого боку, перебіг підгострої/субфульмінантної ГПН часто супроводжується помірним зростанням трансаміназ, вираженою жовтяницею і незначними проявами коагулопатії. Слід зазначити, що зростання рівня трансаміназ не слід вважати надійним діагностичним маркером тяжкості перебігу захворювання. У пацієнтів із підгострою ПН часто наявні ознаки спленомегалії, асциту і зменшення розміру печінки. При появі симптомів печінкової енцефалопатії в разі ГПН шанси на одужання в пацієнтів значно знижуються на відміну від підгострої ПН, при якій шанси на спонтанне одужання пацієнтів значно вищі, незважаючи навіть на наявні можливі ознаки недостатності екстрапечінкових органів [4].
Предиктори епізодів печінкової енцефалопатії
— Інфекція.
— Шлунково-кишкова кровотеча.
— Передозування діуретиків.
— Електролітні розлади.
— Запори.
— Прийом психоактивних препаратів.
— Дегідратація.
— Неповноцінне харчування.
Кожний наступний епізод проявів ПЕ пов’язаний зі збільшенням відсотка 1-річної летальності. Найчастіше для клінічної оцінки ступеня проявів печінкової енцефалопатії використовуються критерії West Haven (WHC), наведені в табл. 1. При ПЕ І ступеня в пацієнтів виявляються брак уваги та деякі тонкі зміни особистості, особливо при спілкуванні щодо близьких людей, родичів. При ПЕ ІІ ступеня виявляються прояви дезорієнтації в часовому аспекті в поєднанні з невідповідністю поведінки і сонливістю. При встановленні ступеня ІІІ ПЕ пацієнти мляві, але реагують на зовнішні подразники, дезорієнтовані в місці і просторі. IV ступінь ПЕ відповідає стану коми.
Приклади психометричних та нейропсихологічних тестів на мінімальну і приховану енцефалопатію: тести на синдром портосистемної енцефалопатії (PSE), тест на критичну частоту мигтіння (CFF); тест на безперервний час реакції (CRT); контрольний тест інгібування (ICT); тест STROOP; SCAN тест; електроенцефалографія.
/114.jpg)
Порушення згортальної функції крові для підтвердження ГПН супроводжується пролонгацією міжнародного нормалізованого співвідношення (МНС/INR), зазвичай > 1,5, та подовженням протромбінового часу (ПЧ). Здавалося б, триваліше за часом значення МНС могло б бути відображення тяжкості перебігу ГПН, проте на сьогодні значення МНС не є стандартизованим критерієм у гепатології і використовується здебільшого для моніторингу ефективності проведення варфаринотерапії. Багато клініцистів рекомендують до використання ПЧ як більш точний маркер, одночасно оцінюючи прояви печінкової енцефалопатії та жовтяниці в контексті клінічної маніфестації. Проте в дітей та новонароджених ГПН може розвиватися за відсутності ознак ПЕ, але вимагає вищих значень МНС — > 4 («глибша» коагулопатія), а початкові зміни ментального статусу потребуватимуть детального пошуку й уточнення генезу виникнення. Така ж ситуація стосується і дорослих пацієнтів, коли розроблені складні шкали для виявлення початкових порушень ментального статусу не набули широкого використання, оскільки за своїми вимогами до їх реалізації значно перевищували можливості звичайних районних лікарень [5]. При підгострій печінковій недостатності прояви ПЕ виникають пізніше і доволі часто є проявами маніфестації інфекційного процесу; як тільки з’являються ознаки ПЕ, трансплантологічне вікно для таких пацієнтів значно звужується.
Ще однією важливою умовою підтвердження гостроти процесу захворювання є відсутність в анамнезі фіброзних або циротичних захворювань печінки. Певним виключенням є такі стани, як гострий автоімунний гепатит та синдром Бадда — Кіарі, при яких неможливо діагностувати попередні хронічні прояви захворювань печінки; у такому разі рекомендоване виконання гістологічного підтвердження проявів цирозу. Хвороба Вільсона належить до іншої категорії виключень, коли виражене хронічне захворювання, що супроводжується розвитком спленомегалії, доволі часто попередньо не діагностоване, оскільки здебільшого виникає в підлітків на фоні перенесеної вірусної інфекції або недотримання призначеної терапії. У такої категорії пацієнтів, які мають ГПН, прогноз перебігу захворювання часто невтішний внаслідок значних коагулопатичних зрушень і розвитку ПЕ. Також наявний невеликий відсоток пацієнтів, які не мають ознак фіброзу, але мають інші стани (метаболічний синдром, жирова дистрофія печінки, перенесений вірусний гепатит С тощо), прогресування яких може проявлятися як ГПН [19, 20].
Таким чином, на сьогодні для визначення ступеня печінкової недостатності необхідно визначати рівень коагулопатичних порушень разом з оцінкою змін рівня трансаміназ, білірубіну, альбуміну і ліпідного обміну.
Рекомендації
— Тяжка гостра травма печінки визначає характерний синдром пошкодження за маркерами ураження печінки (підвищені сироваткові трансамінази); порушення функції печінки (жовтяниця та МНС > 1,5), що зазвичай передують клінічним проявам енцефалопатії (ступінь доказовості — ІІ-2, рівень рекомендації — 1).
— Пацієнти з гострим проявом хронічного автоімунного гепатиту, хвороби Вільсона та синдрому Бадда — Кіарі вважаються такими, які мають ГПН, якщо в них розвивається печінкова енцефалопатія, незважаючи на наявність ознак попереднього захворювання печінки в умовах відповідних відхилень в аналізах печінки та профілю згортання крові (ступінь доказовості — ІІ-2, рівень рекомендації — 1).
— Клінічні прояви печінкової енцефалопатії мають вирішальне значення для встановлення діагнозу ГПН, при цьому ранні психічні зміни й інтенсивний скринінг ранніх ознак печінкової енцефалопатії є обов’язковими (ступінь доказовості — ІІ-2, рівень рекомендації — 1).
Міркування стосовно подальших досліджень
1. Виявлення біомаркерів — предикторів прогресування та переходу гострого пошкодження печінки в гостру печінкову недостатність.
2. Розробка та впровадження тестів для виявлення початкових ознак розвитку печінкової енцефалопатії при підгострому перебігу ГПН.
3. Переоцінка показників МНС/протромбіну для підтвердження ГПН як найгострішої, так і підгострої.
Стан проблеми ГПН у європейських країнах
Частота виникнення, особливості перебігу та тривалість захворювання ГПН серед жителів країн Європи не визначені, оскільки, на жаль, відсутня база збору даних стосовно поширеності зазначеної патології. Усі дані базуються переважно на результатах лікування пацієнтів у межах центрів із трансплантації печінки. Відомо, що у 8 % випадків трансплантація печінки була виконана через гостру печінкову недостатність як первинну причину. Проміжний аналіз зазначених 8 % випадків захворювань показав, що серед обстеженої групи пацієнтів 19 % хворих мали вірусний генез захворювання, у 18 % ГПН розвивалася внаслідок токсичної дії медикаментозних препаратів, у 4 % причиною захворювання було вторинне ішемічне ураження печінки, у 3 % випадків — постопераційне посттравматичне ураження печінки, тоді як у 56 % чітка причина розвитку ГПН не була встановлена [6].
Діагностичні заходи у разі ГПН
При надходженні в лікарняний заклад пацієнтам із гострою печінковою недостатністю рекомендовано виконати такі невідкладні заходи ще до контакту з третинним центром надання допомоги і до узгодження переводу пацієнтів у спеціалізований заклад:
1. Провести негайний скринінг на виявлення ознак печінкової енцефалопатії.
2. Виключити наявність цирозу печінки, алкогольного ураження печінки або метастатичного ураження.
3. Виявити показання і протипоказання до виконання трансплантації печінки.
4. Пошук етіологічного фактора з метою надання патофізіологічно обґрунтованого лікування та полегшення прогностичної стратифікації.
5. Раннє переведення пацієнта в спеціалізований заклад за умови МНС > 1,5 та наявності ознак печінкової енцефалопатії.
6. Рання комунікація з трансплантаційним центром, навіть якщо на момент первинного обстеження немає даних про необхідність виконання пересадки печінки.
7. Візуалізація кровотоку судин печінки, наявність тромбозу печінкових та селезінкових судин при проведенні ультразвукової діагностики, магнітно-резонансної томографії.
Виключення наявності цирозу або алкогольіндукованого ураження печінки
Клінічні знахідки та результати інструментальних методів обстеження пацієнтів у разі ГПН, особливо підгострої форми ГПН, можуть імітувати цироз печінки (ступінь доказовості — ІІ-3, рівень рекомендації — 1). Під час виконання ультразвукового обстеження поєднання даних щодо зниження маси печінки, наявність регенераторних вузлів зі сформованими нерівними контурами печінки одночасно зі спленомегалією й асцитом свідчать на користь цирозу. Виконання біопсії печінки рекомендоване з метою підтвердження діагнозу шляхом транс’югулярного доступу або через мінілапаротомію, проте з урахуванням ризику розвитку можливої кровотечі, а також обмеження застосування анестезіологічних препаратів в аспекті наявної енцефалопатії (ступінь доказовості — ІІ-3, рівень рекомендації — 1).
Проте не визначена наявність чіткої кореляції між даними біопсії печінки та неінвазивними тестами діагностики ступеня фіброзу.
Етіологічні фактори
Етіологія розвитку ГПН є важливим індикатором прогнозу необхідності виконання ургентної трансплантації печінки або ж, навпаки, її уникнення (табл. 3).
Причини розвитку ГПН, внаслідок яких не показане негайне виконання трансплантації печінки
Злоякісна інфільтрація печінки. У пацієнтів із підтвердженим онкологічним анамнезом чи наявною гепатомегалією з метою виключення метастатичного ураження печінки рекомендоване виконання МРТ або біопсії (ступінь доказовості — ІІ-3, рівень рекомендації — 1).
Гостре ішемічне ураження печінки. Такий стан більш характерний для пацієнтів похилого віку із супутньою серцевою недостатністю і спостерігається близько в 11 % випадків, переважно у відділенні інтенсивної терапії після перенесених, часто незадокументованих епізодах гіпоксії та гіпотензії. При гіпоксичному гепатиті лабораторні зміни показників крові дуже схожі на такі в разі передозування парацетамолу або N-нітрозодиметиламіну (ступінь доказовості — ІІ-3, рівень рекомендації — 1).
Причини розвитку ГПН, внаслідок яких можливо показана ургентна трансплантація печінки
І. Медикаментозно cпровокована гепатотоксичність.
1. Передозування парацетамолу можливе в разі тривалого його вживання у великих дозах із метою купірування больового синдрому або з метою виконання суїциду при одномоментному застосуванні високої дози препарату. Рекомендована доза парацетамолу становить 4 г (або 75 мг/кг) за 24 години для дорослого пацієнта. Будь-який прийом, що перевищує рекомендовану дозу, розцінюється як передозування. Однак токсичність є вкрай малоймовірною, якщо протягом 24 годин було вжито < 75 мг/кг парацетамолу [6–8]. Одноразовий прийом 4 г парацетамолу вважається гострим передозуванням. The National Poisons Information Service рекомендують для обчислення потенційно токсичних доз враховувати таке:
— Токсична доза парацетамолу для вагітних розраховується на масу тіла, яку мала жінка до вагітності.
— Для пацієнтів вагою > 110 кг токсичну дозу слід розраховувати, використовуючи максимум 110 кг замість фактичної маси пацієнта.
— Ознакою передозування парацетамолу є підвищення рівня аспартатамінотрансферази (АСТ) щонайменше до 1000 МО/л і вище (The Preliminary Clinical Toxicology Database of The Nation Poisons Informational Service, 2019).
— На фоні стрімкого підвищення рівня АСТ значення білірубіну залишаються в межах норми; окрім цього, на ранній стадії захворювання в пацієнтів можуть виявлятися метаболічний ацидоз, гіпоглікемія й ознаки гострої ниркової недостатності. З урахуванням незначної зміни в показниках системи коагуляції для оцінки тяжкості та проявів поліорганної недостатності можливе використання шкали SOFA. Токсикологічний скринінг та визначення циркулюючої концентрації парацетамолу слід виконати при госпіталізації в кожного пацієнта з характерним анамнезом, особливо у випадках із фульмінантною ГПН та значно підвищеним рівнем сироваткових трансаміназ. Пацієнтам із підвищеним рівнем парацетамолу за наявності метаболічного ацидозу, підвищеного рівня лактату рекомендовано негайно розпочати інфузійну терапію, призначити N-ацетилцистеїн, а також прийняти рішення про замісну ниркову терапію з метою корекції ацидозу (ступінь доказовості — ІІ-3, рівень рекомендації — 1).
2. Токсини (токсичне враження іншими медикаментозними засобами).
Близько 10 % пацієнтів із непарацетамоловим токсичним медикаментозно індукованим гострим пошкодженням печінки (non-paracetamol drug induced liver injury — DILI) мають прояви ГПН, рівень летальності при якій становить близько 80 % у разі неможливості виконання ургентної трансплантації печінки. DILI частіше розвивається в пацієнтів старшого віку (> 60 років) у зв’язку з прийомом різних медикаментозних засобів [9–11].
У разі DILI гіперсенситивна реакція розвивається близько в 1/3 пацієнтів і характеризується проявами синдрому DRESS (Drug reaction with eosinophilia and systemic symptoms), що підтверджується еозинофілією, гіпертермією, лімфаденопатією та шкірною висипкою. У такому випадку рекомендоване застосування високих доз стероїдів (ступінь доказовості — ІІ-2, рівень рекомендації — 1).
Групи препаратів, за умови прийому яких найчастіше виникає ГПН:
— протитуберкульозні препарати (ізоніазид);
— антибіотики (нітрофурани, кетоконазол);
— антиепілептичні засоби (фенітоїн, препарати вальпроєвої кислоти);
— нестероїдні протизапальні препарати;
— широка група препаратів, таких як пропілтіоурацил (при дифузному токсичному зобі), дисульфірам (інгібітор ферменту ALDH2, що використовується для лікування хронічної алкогольної залежності) [12, 13].
ІІ. Вірусні гепатити, інші вірусні агенти. Найчастіше ГПН розвивається внаслідок вірусних гепатитів В (HBV), А (НАV) та HЕV. У разі HBV тяжке гостре пошкодження печінки чи ГПН можуть виникати через інфекцію de novo, дельта-суперінфекцію чи реактивацію попередньо перенесеної інфекції. Вакцинація значно зменшує ймовірність зараження HBV. Реактивація інфекції може розвиватися під час лікування імуносупресивними ліками, зокрема ритуксимабом, а також при злоякісних захворюваннях крові.
— Вірус простого герпесу 1 та 2 та Varicella zoster — інші рідкісні вірусні причини, що можуть спровокувати розвиток ГПН, переважно в пацієнтів із вираженою імуносупресією. Відсутність характерних проявів на шкірі не виключає діагноз, додатково рекомендоване проведення скринінгу на цитомегаловірус (CMV) та вірус Епштейна — Барр (ЕBV) (ступінь доказовості — ІІ-2, рівень рекомендації — 1).
ІІІ. Автоімунний гепатит. Наявність інших автоімунних захворювань у пацієнта із симптомами ГПН може наштовхнути на думку про наявність автоімунної природи гострого ураження печінки, основними проявами якої є підвищена глобулінова фракція та позитивні автоантитіла. Може бути ефективним раннє застосування стероїдів, однак відсутність ефекту протягом 7 днів лікування стероїдами свідчить про необхідність виконання трансплантації печінки, оскільки триваліший прийом стероїдів асоційований зі зростанням летальності внаслідок розвитку септичних ускладнень (ступінь доказовості — ІІ-2, рівень рекомендації — 1).
IV. ГПН, асоційована з вагітністю. Під час III триместру вагітності можуть розвиватися 2 критичні сценарії, пов’язані з гострою печінковою недостатністю: гемоліз, підвищення рівня печінкових ферментів та тромбоцитопенія (HELLP-синдром) і гостра жирова дистрофія печінки вагітних (AFLP — acute fatty liver of pregnancy). Диференціальну діагностику HELLP-синдрому слід проводити з атиповим гемолітичним уремічним синдромом і тромботичною тромбоцитопенічною пурпурою (синдром Мошковіца) [14]. AFLP характеризується множинними печінковими стеатозами, абдомінальним болем і вираженою слабкістю, незначно підвищеними трансаміназами, гіпоглікемією, підвищеним рівнем уратів на фоні полідипсії та поліурії. При обох клінічних сценаріях швидке розродження дає добрий результат одужання і дуже рідко необхідна трансплантація печінки в матері. Стійке підвищення лактату за наявності симптомів гострої печінкової недостатності є негативною прогностичною ознакою з високим ризиком летальності [15].
V. Гостра печінкова недостатність після гемігепатектомії. Втрата великої частки паренхіми печінки після резекції може призвести до розвитку гострої печінкової недостатності. Більшість пацієнтів при збереженій функції печінки спонтанно одужують після резекції. Здебільшого повідомлення про розвиток ГПН стосуються пацієнтів після перенесеної трансплантації печінки від живого донора [16].
VI. Гіпертермічна травма печінки після теплового удару. Клінічна картина може виникнути після прийому наркотичних засобів, таких як екстазі, з одночасним впливом високої температури оточуючого середовища або під час фізичного навантаження за умов зовнішньої високої температури [17].
Клінічна діагностика
Важливу роль у встановленні діагнозу відіграють комплексна клінічна оцінка та ретельний збір анамнезу, виявлення етіології, наявності коморбідних станів, а також уточнення часового проміжку між появою жовтяниці і проявами печінкової енцефалопатії.
Основні анамнестичні дані при надходженні пацієнта в стаціонар
Пошук етіологічного фактора:
— Прийом медикаментозних засобів з акцентом на вживання парацетамолу та парацетамолвмісних препаратів, біологічні добавки, трави < 6 місяців.
— Суїцидальні спроби, депресії в анамнезі.
— Шлунково-кишкові розлади після вживання грибів.
Умови, що передували проявам гострої печінкової недостатності:
— Вагітність.
— Подорожі в ендемічні зони вірусних гепатитів В та Е.
— Отримання імуносупресивної та/або хіміотерапії.
— Автоімунні захворювання в анамнезі.
Умови, що впливають на рішення щодо ургентної трансплантації печінки:
— Хронічне захворювання печінки в анамнезі.
— Активне зловживання алкоголем.
— Нещодавно перенесене онкологічне захворювання (необхідна консультація онколога).
— Застійна серцева недостатність чи супутня патологія дихальної системи.
Інтервал між появою жовтяниці і першими симптомами печінкової енцефалопатії.
Лабораторні обстеження під час надходження пацієнта з ГПН
1. З метою визначення тяжкості захворювання: ПЧ, МНС, коагулограма з визначенням фібриногену, печінкові ферменти, включаючи визначення рівня лактатдегідрогенази, фракцій білірубіну, креатинкінази. Оцінка ниркової функції: погодинний діурез; низький рівень сечовини — ранній маркер тяжкої печінкової дисфункції; визначення креатиніну може бути ускладнене при підвищеному рівні білірубіну. Окрім того, рекомендована оцінка газового складу крові й аміаку.
2. Для встановлення етіологічного фактора: токсикологічна панель сечі, визначення рівня парацетамолу в сироватці крові, серологічний скринінг на вірусні гепатити HBsAg, анти-HBc IgM (HBV DNA), delta, якщо позитивний тест на HBV, анти-HAV IgM, анти-HEV IgM, анти-HSV IgM, анти-VZV IgM, CMV, HSV, EBV, парвовірус і VZV PCR. Автоімунні маркери: антинуклеарні антитіла, ASMA, глобуліновий профіль, HLA-типування.
3. Для виявлення ускладнень: ліпаза чи амілаза, КФК, тропонін у пацієнтів із ішемічною хворобою серця, метаболічний синдром [21, 22].
Діагностичні процедури, моніторинг, стандарти надання допомоги при надходженні пацієнтів із ГПН
Основними інструментальними методами обстеження, рекомендованими до виконання, є рентгенографія грудної клітки, базова ехокардіографія, ехографія печінки (структура, розмір печінки, напрям кровотоку в судинах, розмір селезінки), комп’ютерна або магнітно-резонансна томографія (виключення панкреатиту, цирозу). На сьогодні найчастішими причинами смерті при ГПН вважають розвиток поліорганної недостатності і сепсис. Тому одним з основних аспектів лікування пацієнтів із ГПН є раннє виявлення і лікування інфекційних ускладнень. Необхідно чітко моніторувати виникнення ранніх ознак печінкової енцефалопатії та проводити диференціальну діагностику з іншими причинами (алкогольна інтоксикація, метаболічні розлади). Моніторинг неврологічних ознак слід проводити кожні 2 години з відповідним записом в історії хвороби, а при розвитку ПЕ 2-го ступеня слід негайно перевести пацієнта у відділення інтенсивної терапії з усіма необхідними можливостями протезування вітальних функцій (респіраторна підтримка, цілодобовий кардіомоніторинг тощо).
Основні підходи до лікування гострої печінкової недостатності та печінкової енцефалопатії
— N-ацетилцистеїн (N-ацетилхолін): 72-годинна внутрішньовенна інфузія: початкова навантажувальна доза 150 мг/кг на годину протягом однієї години, потім 12,5 мг/кг на годину протягом чотирьох годин, потім безперервні вливання 6,25 мг/кг на годину протягом решти 67 годин (ступінь доказовості — ІІ-3, рівень рекомендації — 1).
— Запобігання розвитку набряку головного мозку при печінковій енцефалопатії
— Рання інтубація та респіраторна підтримка при 3-й або 4-й стадії печінкової енцефалопатії.
— Вентиляція 6–7 мл/кг ідеальної маси тіла, PEEP +5 см вод.ст. Цільове значення CO2 — 35 мм рт.ст.
— Седація пропофолом та фентанілом (тіопентал опційно).
— За потреби застосування нервово-м’язової блокади рекомендоване використання цисатракурію.
— Позиція в ліжку з підйомом головного кінця на 30 градусів, голова в нейтральному положенні.
— Підтримка середнього артеріального тиску > 75 мм рт.ст., для підтримки рекомендоване використання норепінефрину в стартовій дозі 0,05 мкг/кг/хв, за потреби додатково вазопресин у початковій дозі 1–2 Од/год, якщо дози епінефрину перевищують 0,2–0,3 мкг/кг/хв. Окрім того, якщо пацієнт отримує вазопресорну підтримку з дозою 0,2 мкг/кг/хв і вище, рекомендоване проведення інвазивного моніторингу артеріального тиску.
— Підтримка рівня натрію плазми Na 140–150 ммоль/л за допомогою гіпертонічного натрію хлориду (ступінь доказовості — ІІ-2, рівень рекомендації — 1).
— Вірогідно (доказово) не доведена ефективність використання методів еферентної терапії при ГПН (плазмаферез, обмінний плазмаферез, гемокарбоперфузія тощо).
— У разі підвищеного ВЧТ рекомендована короткочасна гіпервентиляція пацієнта з досягненням PaCO2 25–30 мм рт.ст.; підтримка гіпервентиляції лише в період підвищеного ВЧТ, після нормалізації рекомендоване повернення до нормокарбії.
— Внутрішньовенний болюс манітолу 15% 0,5 г/кг. У разі задовільної реакції на манітол (ВЧТ < 20 мм рт.ст. і досягнення церебрального перфузійного тиску > 60 мм рт.ст.) рекомендовано повторити внутрішньовенне введення манітолу для запобігання зростанню ВЧТ. Манітол слід негайно відмінити у разі досягнення осмолярності плазми > 320 мекв/л чи олігоануричної (< 20 мл/год) ниркової недостатності. Якщо реакція на введення манітолу відсутня, рекомендоване призначення гіпертонічного (10%) розчину натрію хлориду в дозі 2 мл/кг через центральний венозний доступ. У разі задовільної реакції на гіпертонічний розчин натрію хлориду (ВЧТ < 20 мм рт.ст. і/або досягнення церебрального перфузійного тиску > 60 мм рт.ст.) рекомендовано повторити болюс гіпертонічного розчину в дозі 1 мл/кг для запобігання зростанню ВЧТ та підтримки рівня натрію плазми 140–150 ммоль/л. Гіпертонічний розчин натрію хлориду слід негайно відмінити за умови виникнення гіпернатріємії (натрій плазми > 160 ммоль/л) чи появи ознак застійної серцевої недостатності. 23,4% розчин хлориду натрію можна використовувати як альтернативу (30 мл інфузії) (ступінь доказовості — ІІ-2, рівень рекомендації — 1).
— За наявності ознак водного перевантаження рекомендоване застосування фуросеміду в дозі 10–40 мг, за умови якщо це не рання стадія гострої ниркової недостатності і немає необхідності застосування нирковозамісної терапії (RRT — renal replacement therapy).
— Вирішення питання про гіпотермічне лікування набряку головного мозку базується на стійкості до осмотичної терапії. Показання до застосування гіпотермії: а) відсутність терапевтичної відповіді на застосування манітолу і гіпертонічних розчинів натрію хлориду; б) зростання ВЧТ й осмолярності плазми при застосуванні гіперосмолярних розчинів; в) підтримка внутрішньої температури тіла 33–34 °С за допомогою охолоджуючих ковдр і інших охолоджуючих пристроїв; г) застосування нейром’язових релаксантів для уникнення тремтіння.
На сьогодні тактика лікування гострої печінкової недостатності та енцефалопатії базується на принципі 4Н-терапії:
1) Mild Hyperventilation — помірна гіпервентиляція. Пацієнти, оцінені за ШКГ ≤ 8 балів і з респіраторним ацидозом чи без нього за умов проявів тяжкої енцефалопатії (енцефалопатія ≥ 3) повинні бути заінтубовані і переведені на респіраторну підтримку для досягнення артеріального парціального тиску СО2 (РаСО2) у межах 32–35 мм рт.ст.
2) High-dose Hemodiafiltration — високооб’ємна гемо–діафільтрація. Її використання в обсязі 40–60 мл/кг/год показане пацієнтам із тяжкою енцефалопатією, олігурією, ацидозом та/чи гіперамоніємією (> 80 ммоль/л) із використанням контурів без гепарину або можливістю системного застосування антиагрегантів із простацикліновою активністю (дипіридамол).
3) Hypothеrmia — гіпотермія. Стан помірної гіпотермії (цільова температура 35 °С) може досягатися шляхом використання екстракорпоральних методів охолодження або зовнішніх охолоджуючих пристроїв.
4) Нypernatremia — помірна гіпернатріємія. Цільове значення концентрації натрію в плазмі рекомендовано підтримувати на рівні 140–150 ммоль/л шляхом внутрішньовенної інфузії гіпертонічних розчинів через центральний венозний доступ. Наявність або відсутність набряку головного мозку слід оцінювати шляхом щоденного неврологічного обстеження на виявлення ознак внутрішньочерепної гіпертензії з допоміжною КТ-оцінкою за клінічними показаннями.
— Додаткове використання внутрішньовенного введення стероїдів (солу-кортеф 100 мг в/в у вигляді короткотривалої болюсної інфузії або в/м введення гідрокортизону ацетату 50 мг чи преднізолону 40 мг/добу) та/чи вазопресину призначається на розсуд лікуючого лікаря.
— Антимікробна профілактика застосовується в разі підозри на наявність бактеріальної інфекції. Стартовими препаратами вибору рекомендовані піперацилін/тазобактам або цефалоспорини 3-го покоління в комбінації з протигрибковими препаратами.
— Ентеральне харчування. Якомога раніше слід розпочати (продовжувати) пероральне харчування. У пацієнтів із прогресуючою ПЕ та/або анорексією у зв’язку з недостатнім калоражем й обмеженим споживанням їжі слід розглянути питання про встановлення назогастрального або інтестинального зонду, зваживши при цьому можливі ризики розвитку ускладнень (кровотеча з носа, мікроаспірація тощо). Вказівки щодо харчових потреб переважно емпіричні, а калорійність та потреба в білках багато в чому відповідають вимогам критично хворих пацієнтів інших етіологій. Рішення про парентеральне харчування приймається відповідно до спроможності підтримки базового харчування та кількості отриманих кілокалорій. Особливу увагу слід приділяти у виборі сумішей з урахуванням амінокислотного співвідношення (коефіцієнта Фішера) не менше 4,0. Рутинно рекомендоване проведення моніторингу глікемії, оскільки гіпоглікемія є частим й одним з основних метаболічних розладів у пацієнтів із ГПН (ступінь доказовості — ІІ-3, рівень рекомендації — 1).
— Препарати крові: свіжозаморожена плазма не рекомендована для рутинного застосування, лише при клінічній ситуації, що того потребує. Показаннями до трансфузії еритроцитарної маси є величина гемоглобіну 70 г/л і нижче (ступінь доказовості — ІІ-2, рівень рекомендації — 1).
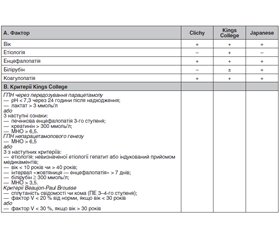
Основні критерії стосовно трансплантації печінки
Найбільш видатним досягненням у лікуванні ГПН протягом останніх 40 років вважають пересадку печінки, що значно впливає на виживаність пацієнтів. Особливе місце посідає питання вибору пацієнтів. Основними клінічними факторами, що впливають на негативний прогноз виживання після трансплантації, вважають енцефалопатію, недостатність екстрагепатичних органів, етіологічні фактори ГПН, тяжкість ураження печінки. Серед великої кількості прогностичних критеріїв щодо селекції пацієнтів для трансплантації основну роль відіграють King’s College Criteria і Clichy Criteria, наведені в табл. 4.
Висновки
Гостра печінкова недостатність — рідкісний синдром, що виникає внаслідок гострого ураження печінки в пацієнтів без попередніх хронічних захворювань печінки. Він характеризується втратою синтетичної функції та розвитком печінкової енцефалопатії разом із проявами синдрому поліорганної недостатності. На фоні різних можливих причин розвитку ГПН найпоширенішими етіологічними факторами в усьому світі є передозування парацетамолу та вірусний гепатит. Вторинні прояви синдрому поліорганної недостатності, що часто супроводжують ГПН, часто є результатом початкової масивної протизапальної відповіді. З урахуванням множинних системних проявів гострої печінкової недостатності рішення про оптимальний тип лікування має прийматися на рівні мультидисциплінарної команди, а пацієнти з ранніми тяжкими проявами ГПН та ПЕ повинні отримувати належну допомогу в спеціалізованих центрах, здатних виконувати ургентну трансплантацію печінки.
Конфлікт інтересів. Автори заявляють про відсутність конфлікту інтересів та власної фінансової зацікавленості при підготовці даної статті.

/115.jpg)
/114.jpg)
/117.jpg)
/120.jpg)