Международный неврологический журнал Том 16, №4, 2020
Вернуться к номеру
Нейристон® — комбинация уридинмонофосфата, витамина В12 и фолиевой кислоты для лечения периферической нейропатической боли
Авторы: А.В. Савустьяненко
Рубрики: Неврология
Разделы: Справочник специалиста
Версия для печати
Низка засобів, традиційно застосовуваних для боротьби з нейропатичним болем (трициклічні антидепресанти, інгібітори зворотного захоплення серотоніну і норадреналіну, габапентиноїди), незважаючи на їх позитивну дію з точки зору усунення симптомів полінейропатії, таких як біль, печіння, парестезії і т.д., можуть викликати побічні ефекти і, на жаль, не впливають на регенерацію нервів. Досить давно з цією метою застосовуються такі групи препаратів, як вітаміни групи В, альфа-ліпоєва кислота і т.д. Протягом останнього десятиліття досить активно в лікарській практиці використовується група так званих нуклеотидів. Накопичуються додаткові відомості про ефекти цієї групи препаратів і відбувається поступова трансформація в тому числі і їх складів. Так, останнім часом увагу дослідників присвячено вивченню ефективності комбінації «уридинмонофосфат + вітамін В12 (ціанокобаламін) + фолієва кислота», для якої характерний досить високий профіль безпеки і хороший регенеративний потенціал. Мета цього короткого огляду зводилася до того, щоб висвітлити механізми дії і результати клінічного застосування даної комбінації. Уридинмонофосфат, ціанокобаламін і фолієва кислота беруть участь у метаболічних процесах, підсилюючи регенерацію нервів. Це веде до розвитку непрямого (вторинного) знеболюючого ефекту. Крім того, дані нових досліджень свідчать про здатність похідних уридинмонофосфату впливати на пуринергічні P2Y-рецептори. Це обумовлює пряму знеболюючу і пряму регенеративну дію. У виконаних роботах була продемонстрована клінічна ефективність комбінації уридинмонофосфату 50 мг, ціанокобаламіну 3 мкг і фолієвої кислоти 400 мкг при основних видах периферичного нейропатичного болю (люмбальна/люмбосакральна радикулопатія, ішіалгія, цервікальна радикулопатія, карпальний тунельний синдром, діабетична нейропатія та ін.). При цьому комбінація не викликала побічних ефектів і добре переносилася. У цих дослідженнях повідомлялося про зменшення загального бала болю, різних параметрів інтенсивності, виду, поширеності, локалізації та іррадіації болю. Було відзначено зменшення або повне скасування прийому супутніх анальгетиків. Підвищилася якість життя пацієнтів. Загальне клінічне враження про успіх терапії у лікарів і пацієнтів відповідало рівню «значне поліпшення». Висновки. Нейристон® (уридинмонофосфат 50 мг + ціанокобаламін 3 мкг + фолієва кислота 400 мкг) у дозі 1 капсула на день може бути досить ефективним доповненням до стандартної терапії периферичного нейропатичного болю різного генезу.
Ряд средств, традиционно применяемых для борьбы с нейропатической болью (трициклические антидепрессанты, ингибиторы обратного захвата серотонина и норадреналина, габапентиноиды), несмотря на их позитивное действие с точки зрения устранения симптомов полинейропатии, таких как боль, жжение, парестезии и т.д., могут вызывать побочные эффекты и, к сожалению, не влияют на регенерацию нервов. Достаточно давно с этой целью применяются такие группы препаратов, как витамины группы В, альфа-липоевая кислота и т.д. На протяжении последнего десятилетия достаточно активно во врачебной практике используется группа так называемых нуклеотидов. Накапливаются дополнительные сведения об эффектах этой группы препаратов и происходит постепенная трансформация в том числе и их составов. Так, в последнее время внимание исследователей посвящено изучению эффективности комбинации «уридинмонофосфат + витамин В12 (цианокобаламин) + фолиевая кислота», для которой характерен достаточно высокий профиль безопасности и хороший регенераторный потенциал. Цель настоящего краткого обзора сводилась к тому, чтобы осветить механизмы действия и результаты клинического применения данной комбинации. Уридинмонофосфат, цианокобаламин и фолиевая кислота участвуют в метаболических процессах, усиливая регенерацию нервов. Это ведет к развитию непрямого (вторичного) обезболивающего эффекта. Кроме того, данные новых исследований свидетельствуют о способности производных уридинмонофосфата воздействовать на пуринергические P2Y-рецепторы. Это обусловливает прямое обезболивающее и прямое регенеративное действие. В выполненных работах была продемонстрирована клиническая эффективность комбинации уридинмонофосфата 50 мг, цианокобаламина 3 мкг и фолиевой кислоты 400 мкг при основных видах периферической нейропатической боли (люмбальная/люмбосакральная радикулопатия, ишиалгия, цервикальная радикулопатия, карпальный туннельный синдром, диабетическая нейропатия и пр.). При этом комбинация не вызывала побочных эффектов и хорошо переносилась. В этих исследованиях сообщалось об уменьшении общего балла боли, различных параметров интенсивности, вида, распространенности, локализации и иррадиации боли. Было отмечено уменьшение или полная отмена приема сопутствующих анальгетиков. Повысилось качество жизни пациентов. Общее клиническое впечатление об успехе терапии у врачей и пациентов соответствовало уровню «значительное улучшение». Выводы. Нейристон® (уридинмонофосфат 50 мг + цианокобаламин 3 мкг + фолиевая кислота 400 мкг) в дозе 1 капсула в день может быть достаточно эффективным дополнением к стандартной терапии периферической нейропатической боли различного генеза.
A number of drugs traditionally used to manage neuropathic pain (tricyclic antidepressants, serotonin and norepinephrine reuptake inhibitors, gabapentinoids) cause side effects and, unfortunately, do not do not affect nerve regeneration despite their positive effect in terms of eliminating the symptoms of polyneuropathy, such as pain, burning, paresthesia, etc. For a long time, groups of drugs such as B vitamins, alpha-lipoic acid and other have been used for this purpose. Over the past decade, a group of so-called nucleotides has been used quite actively in medical practice. Additional information is accumulating on the effects of this group of drugs, and a gradual transformation is taking place, particularly in their compositions. So, recently the researchers’ attention has been devoted to studying the effectiveness of the combination “uridine monophosphate + vitamin B12 (cyanocobalamin) + folic acid”, which has a rather high safety profile and good regenerative potential. The purpose of this brief review was to highlight the mechanisms of action and the results of the clinical application of this combination. Uridine monophosphate, cyanocobalamin and folic acid are involved in metabolic processes, enhancing nerve regeneration. This leads to the development of an indirect (secondary) analgesic effect. In addition, data from new studies indicate the ability of uridine monophosphate derivatives to act on purinergic P2Y receptors. This causes a direct analgesic and a direct regenerative effect. In the performed works it was demonstrated the clinical efficacy of the combination of uridine monophosphate 50 mg, cyanocobalamin 3 μg and folic acid 400 μg for the main types of peripheral neuropathic pain (lumbar/lumbosacral radiculopathy, sciatica, cervical radiculopathy, carpal tunnel syndrome, diabetic neuropathy, etc.). Moreover, the combination did not cause side effects and was well tolerated. In these trials, a decrease in the total pain score and various parameters of the intensity, type, prevalence, localization and irradiation of pain were reported. A decrease or complete withdrawal of concomitant analgesics was noted. The quality of life of patients has improved. The global clinical impression of the success of the therapy among doctors and patients corresponded to “considerable better state”. Conclusions. Neuriston® (uridine monophosphate 50 mg + cyanocobalamin 3 μg + folic acid 400 μg) at a dose of 1 capsule per day can be a rather effective addition to standard therapy for peripheral neuropathic pain of various origins.
уридинмонофосфат; ціанокобаламін; фолієва кислота; периферичний нейропатичний біль
уридинмонофосфат; цианокобаламин; фолиевая кислота; периферическая нейропатическая боль
uridine monophosphate; cyanocobalamin; folic acid; peripheral neuropathic pain
Введение
Общие сведения о нейропатической боли
/82.jpg)
Механизмы действия
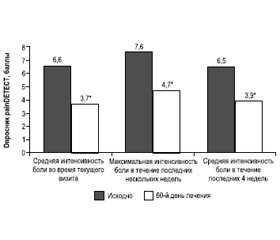
Данные клинических исследований
/83.jpg)
/85_2.jpg)
Выводы
1. Scholz J., Finnerup N.B., Attal N. et al. The IASP classification of chronic pain for ICD-11: chronic neuropathic pain. Pain. 2019. V. 160. № 1. P. 53-59.
2. Szok D., Tajti J., Nyári A., Vécsei L. Behav. Therapeutic Approaches for Peripheral and Central Neuropathic Pain. Neurol. 2019. V. 2019. Article ID 8685954.
3. Negrão L., Almeida P., Alcino S. et al. Effect of the combination of uridine nucleotides, folic acid and vitamin B12 on the clinical expression of peripheral neuropathies. Pain Manag. 2014. V. 4. № 3. P. 191-196.
4. Keltican N. https://www.catalog.md
5. Нуклео Ц.М.Ф. Форте. https://compendium.com.ua
6. Wurtman R.J., Regan M., Ulus I., Yu L. Effect of oral CDP-choline on plasma choline and uridine levels in humans. Biochem. Pharmacol. 2000. V. 60. № 7. P. 989-992.
7. Synoradzki K., Grieb P. Citicoline: A Superior Form of Choline? Nutrients. 2019. V. 11. № 7. Pii: E1569.
8. Cansev M., Wurtman R.J., Sakamoto T., Ulus I.H. Oral administration of circulating precursors for membrane phosphatides can promote the synthesis of new brain synapses. Alzheimers Dement. 2008. V. 4. № 1 (Suppl. 1). P. S153-S168.
9. Wurtman R.J. A nutrient combination that can affect synapse formation. Nutrients. 2014. V. 6. № 4. P. 1701-1710.
10. Negrão L., Nunes P.; Portuguese Group for the Study of Peripheral Neuropathy. Uridine monophosphate, folic acid and vitamin B12 in patients with symptomatic peripheral entrapment neuropathies. Pain Manag. 2016. V. 6. № 1. P. 25-29.
11. Rückert U., Hedding-Eckerich M., Lärm G. Uridine monophosphate after nucleotomy: Investigation of pain reduction and quality of life. Deutscher Wirbelsäulenkongress. Jahrestagung der Deutschen Wirbelsäulengesellschaft. Dezember 2009, München. Eur. Spine J. 2009. V. 18. P. 1713-1826.
12. Nicholson B. Differential diagnosis: nociceptive and neuropathic pain. Am. J. Manag. Care. 2006. V. 12. № 9 (Suppl.). P. S256-S262.
13. Trouvin A.P., Perrot S. New concepts of pain. Best Pract. Res. Clin. Rheumatol. 2019. V. 33. № 3. Article ID 101415.
14. Dresden D. Nociceptive and neuropathic pain: What are they? https://www.medicalnewstoday.com-2017.
15. Freynhagen R., Parada H.A., Calderon-Ospina C.A. et al. Current understanding of the mixed pain concept: a brief narrative review. Curr. Med. Res. Opin. 2019. V. 35. № 6. P. 1011-1018.
16. Jensen T.S., Baron R., Haanpää M. et al. A new definition of neuropathic pain. Pain. 2011. V. 152. № 10. P. 2204-2205.
17. Agamanolis D. Peripheral nerve pathology (Chapter 12). In: Neuropathology course. https://neuropathology-web.org-2011.
18. Shields R.W. Peripheral Neuropathy. https://www.clevelandclinicmeded.com-2010.
19. Pasnoor M., Dimachkie M.M., Kluding P., Barohn R.J. Diabetic neuropathy part 1: overview and symmetric phenotypes. Neurol. Clin. 2013. V. 31. № 2. P. 425-445.
20. Sheki A.A., Hamdan F.B. The role of different neurophysiological tests in the differential diagnosis of diabetic axonal neuropathy and lumbosacral radiculopathy. Neurosciences (Riyadh). 2009. V. 14. № 1. P. 25-30.
21. Manole E., Bastian A., Neagu M. et al. Schwann Cell Plasti-city in Peripheral Nerve Regeneration after Injury. https://www.intechopen.com-2020.
22. Wang L., Albrecht M.A., Wurtman R.J. Dietary supplementation with uridine-5'-monophosphate (UMP), a membrane phosphatide precursor, increases acetylcholine level and release in striatum of aged rat. Brain Res. 2007. V. 1133. № 1. P. 42-48.
23. Urasaki Y., Pizzorno G., Le T.T. Uridine affects liver protein glycosylation, insulin signaling, and heme biosynthesis. PLoS One. 2014. V. 9. № 6. Article ID e99728.
24. Li G., Xie C., Wang Q. et al. Uridine/UMP metabolism and their function on the gut in segregated early weaned piglets. Food Funct. 2019. V. 10. № 7. P. 4081-4089.
25. Spector R. Uridine transport and metabolism in the central nervous system. J. Neurochem. 1985. V. 45. № 5. P. 1411-1418.
26. Dobolyi A., Juhász G., Kovács Z., Kardos J. Uridine function in the central nervous system. Curr. Top. Med. Chem. 2011. V. 11. № 8. P. 1058-1067.
27. Okada M., Nakagawa T., Minami M., Satoh M. Analgesic effects of intrathecal administration of P2Y nucleotide receptor agonists UTP and UDP in normal and neuropathic pain model rats. J. Pharmacol. Exp. Ther. 2002. V. 303. № 1. P. 66-73.
28. Pooler A.M., Guez D.H., Benedictus R., Wurtman R.J. Uridine enhances neurite outgrowth in nerve growth factor-differentiated PC12 [corrected]. Neuroscience. 2005. V. 134. № 1. P. 207-214.
29. Vrbova G., Mehra N., Shanmuganathan H. et al. Chemical communication between regenerating motor axons and Schwann cells in the growth pathway. Eur. J. Neurosci. 2009. V. 30. № 3. P. 366-375.
30. Martiáñez T., Carrascal M., Lamarca A. et al. UTP affects the Schwannoma cell line proteome through P2Y receptors lea-ding to cytoskeletal reorganisation. Proteomics. 2012. V. 12. № 1. P. 145-156.
31. Martianez, Tania M.C. Estudio del fármaco CMP Forte y del nucleótido UTP encélulas de Schwann. http://hdl.handle.net/10803/77766-2011.
32. Shane B. Folate and vitamin B12 metabolism: overview and interaction with riboflavin, vitamin B6, and polymorphisms. Food Nutr. Bull. 2008. V. 29. № 2 (Suppl.). P. S5-S16; discussion S17-S19.
33. Calderón-Ospina C.A., Nava-Mesa M.O. B Vitamins in the nervous system: Current knowledge of the biochemical modes of action and synergies of thiamine, pyridoxine, and cobalamin. CNS Neurosci. Ther. 2020. V. 26. № 1. P. 5-13.
34. Lucock M. Folic acid: nutritional biochemistry, molecular biology, and role in disease processes. Mol. Genet. Metab. 2000. V. 71. № 1–2. P. 121-138.
35. Reynolds E. Vitamin B12, folic acid, and the nervous system. Lancet Neurol. 2006. V. 5. № 11. P. 949-960.
36. Suezawa Y., Jacob H.A. Percutaneous nucleotomy. An alternative to spinal surgery. Arch. Orthop. Trauma Surg. 1986. V. 105. № 5. P. 287-295.
37. Yonezawa T., Onomura T., Kosaka R. et al. The system and procedures of percutaneous intradiscal laser nucleotomy. Spine (Phila. Pa 1976). 1990. V. 15. № 11. P. 1175-1185.

/84.jpg)
/85.jpg)