Вступ
Глаукома є хронічним захворюванням, яке часто супроводжується підвищенням внутрішньоочного тиску, що призводить до загибелі гангліозних клітин сітківки і, як наслідок, дефіциту поля зору. Останнє може прогресувати до сліпоти [1]. Відповідно до статистики, число уражених у всьому світі віком старше 40 років у 2020 р. становитиме 76 млн осіб, а до 2040 р. — 112 млн осіб, що частково може бути пояснено постарінням населення [1, 2].
Спочатку для досягнення успіху в лікуванні ставки були зроблені на зниження внутрішньоочного тиску як основного модифікованого фактора ризику при глаукомі. Однак навіть у пацієнтів із добре контрольованим тиском часто спостерігається прогресування хвороби й поле зору продовжує звужуватися. Стало зрозуміло, що для досягнення цілей лікування необхідне додаткове призначення нейропротекторних засобів, таких як цитиколін [1].
Раніше цитиколін підтвердив свою ефективність при низці неврологічних захворювань, таких як травматичне пошкодження головного мозку, гострий ішемічний інсульт, хронічна цереброваскулярна хвороба, хвороба Альцгеймера, хвороба Паркінсона [3]. Цитиколін ефективний також при низці офтальмологічних хвороб, таких як амбліопія і неартеріїтна ішемічна оптична нейропатія [4]. Усе це вказує на можливий високий терапевтичний потенціал цитиколіну при лікуванні глаукоми.
Дані нових досліджень свідчать про те, що глаукома не обмежується лише периферичними проявами в ділянці ока. Були продемонстровані дегенеративні зміни в латеральному колінчастому ядрі, атрофія внутрішньочерепної частини зорового нерва, стоншення зорової кори великих півкуль [1, 5]. Саме тому роль цитиколіну може бути навіть ще більшою з огляду на його неврологічні ефекти.
Після надходження пероральним або парентеральним шляхом цитиколін (цитидин-5-дифосфохолін) у стінці кишечника й печінці гідролізується до холіну й цитидину. Ці метаболіти надходять у системний кровотік, проникають через гематоенцефалічний бар’єр і беруть участь у низці важливих біохімічних реакцій:
1) холін важливий для синтезу мембранних фосфоліпідів, таких як фосфатидилхолін — один з основних компонентів нейрональних мембран;
2) холін є попередником ацетилхоліну — одного з основних нейромедіаторів;
3) цитидин використовується для побудови РНК і ДНК у нейронах.
Додатково цитиколін підвищує вміст інших мембранних фосфоліпідів (сфінгомієлін, кардіоліпін) та інших нейромедіаторів (допамін, норадреналін, серотонін). Цитиколін підвищує вміст глутатіону — однієї з основних антиоксидантних молекул, і знижує вміст глутамату — однієї з головних речовин, відповідальних за загибель нейронів унаслідок ексайтотоксичності [1, 4, 6–8].
Усі перераховані вище ефекти закладають базу для основних нейроефектів цитиколіну в нервовій тканині: нейропротекції (захист нейронів від пошкоджень, включно із захистом від апоптозу), нейровідновлення (відновлення пошкоджених нейронів), нейрорегенерації (нейрогенез — утворення нових нейронів, нейропластичність — формування нових аксонів, дендритів і синапсів) [7, 8].
Оскільки сітківка може розглядатися як частина центральної нервової системи, передбачається, що глаукома розвивається за тими ж механізмами, що й інші хронічні нейродегенеративні захворювання. Звідси випливає, що й підходи до їх лікування також мають бути однаковими. Усе це знаходить підтвердження в результатах робіт із вивчення цитиколіну [1].
З огляду на значущість теми нами був підготовлений короткий огляд клінічних досліджень цитиколіну як засобу для лікування первинної глаукоми. Виділено основні клінічні ефекти препарату, рекомендовані оптимальна лікарська форма, доза й режим терапії.
Характеристика клінічних ефектів
До сьогодні виконано 10 основних клінічних досліджень, присвячених застосуванню цитиколіну для лікування глаукоми [9–18]. У цих роботах препарат призначався парентерально (внутрішньом’язово), перорально у вигляді таблеток або розчинів і місцево у вигляді очних крапель. При характеризуванні клінічних ефектів ми будемо посилатися на всі ці 10 робіт.
Найважливіші клінічні ефекти цитиколіну при глаукомі за даними клінічних досліджень [9–18] (у дужках вказані методи дослідження, за допомогою яких ці ефекти були виявлені):
— збереження поля зору (периметрія);
— посилення функції сітківки (патерн-електроретинографія (патерн-ЕРГ));
— підтримання морфології сітківки (оптична когерентна томографія (ОКТ));
— покращання провідності по зорових шляхах (викликані зорові потенціали (ВЗП)).
Збереження поля зору
Периметрія дозволяє оцінити стан поля зору в пацієнтів з офтальмологічними захворюваннями. Сьогодні ця процедура багато в чому автоматизована. Пацієнту пред’являють зорові стимули різної інтенсивності, і якщо він їх бачить, то натискає кнопку. У пацієнтів із глаукомою спостерігається пошкодження поля зору, що пов’язано із загибеллю гангліозних клітин сітківки [19–21].
За даними L. Ottobelli і співавт. [15], призначення цитиколіну уповільнює швидкість пошкодження поля зору в пацієнтів із глаукомою приблизно в 7,3 раза. У цей ефект також робить внесок невелике зниження внутрішньоочного тиску — приблизно на 1 мм рт.ст.
У результаті такого впливу на показник швидкості поле зору фактично переставало погіршуватися. У роботі L. Ottobelli і співавт. [15] стабілізація поля зору спостерігалася протягом перших 4 місяців лікування, без прогресування протягом наступних 2 років терапії. У роботі М. Lanza і співавт. [18] стабілізація відбувалася протягом перших 4 місяців лікування, без прогресування упродовж наступних 2 років терапії. У роботі М. Virno і співавт. [11] стабілізація відбувалася протягом 1-го року лікування, без прогресування упродовж наступних 9 років терапії.
Два з цих досліджень будуть детально описані в розділі «Дані клінічних досліджень». Тут ми відзначимо, що в усіх пацієнтів початково внутрішньоочний тиск добре контролювався, а цитиколін весь час призначався на циклічній основі: періоди прийому препарату змінювалися перервами в лікуванні, і навпаки.
Посилення функції сітківки
При виконанні патерн-електроретинографії пацієнту пред’являють зорові стимули, реєструючи викликані ними зміни за допомогою електродів, розташованих на рогівці або найближчій бульбарній кон’юнктиві. Даний метод дозволяє оцінити функцію сітківки (в основному гангліозних клітин сітківки; при цьому зміни на патерн-ЕРГ зазвичай передують гістологічній втраті цих клітин, коли дефектів поля зору ще немає або вони мінімальні) [22–24].
У хворих із глаукомою спостерігається збільшення латентності й зменшення амплітуди патерн-ЕРГ, що вказує на ослаблення функції сітківки [14]. Разом з тим у більшості досліджень було показано, що цитиколін зменшує латентність і збільшує амплітуду патерн-ЕРГ, що свідчить про посилення функції сітківки при призначенні даного засобу [10, 13, 14, 16, 17].
Підтримання морфології сітківки
Оптична когерентна томографія є відносно новим методом дослідження, що серед іншого дозволяє розглядати морфологічну структуру сітківки. ОКТ схожа на ультразвукове дослідження (УЗД) з тією відмінністю, що в ОКТ замість ультразвуку використовують світло. При цьому роздільна здатність ОКТ у 10–100 разів вища, ніж УЗД [25].
У пацієнтів із глаукомою спостерігається стоншення шару нервових волокон сітківки й комплексу гангліозних клітин (комплекс включає 3 шари: внутрішній плексиформний шар, шар гангліозних клітин і шар нервових волокон сітківки). Призначення цитиколіну запобігало стоншенню цих шарів, що свідчить про здатність препарату підтримувати морфологічну цілісність сітківки [18, 26].
Цей ефект цитиколіну обумовлений підтримкою життєздатності гангліозних клітин сітківки [27].
Покращання провідності по зорових шляхах
При оцінці викликаних зорових потенціалів пацієнтові пред’являють зорові стимули, одночасно реєструючи викликані ними зміни на електроенцефалограмі за допомогою електродів, розташованих іззаду голови над зорової корою. Таким чином оцінюється здатність нервових імпульсів проходити від сітківки до зорової кори. У хворих із глаукомою спостерігається збільшення латентності й зменшення амплітуди ВЗП, що вказує на уповільнення нервового проведення по зорових шляхах [12, 14, 28, 29].
У переважній кількості досліджень було продемонстровано, що цитиколін зменшує латентність і збільшує амплітуду ВЗП, що свідчить про покращання нервового проведення по зорових шляхах у хворих із глаукомою [10, 12–14, 16, 17].
Вибір лікарської форми, дози й режиму терапії
Немає необхідності в парентеральному введенні, достатньо перорального прийому
Добре відомо, що ін’єкції не є найкращим способом уведення лікарських засобів офтальмологічним пацієнтам із хронічними хворобами [30]. Тому була протестована клінічна ефективність пероральних форм цитиколіну, у тому числі порівняно з парентеральними формами.
У першій роботі 11 пацієнтам (21 око з відкритокутовою глаукомою) був призначений цитиколін у вигляді таблеток у дозі 1000 мг/день (2 рази на день по 500 мг). Таблетки приймалися протягом 2 тижнів, за якими йшла двотижнева перерва, потім таблетки приймалися ще 2 тижні з подальшою двотижневою перервою. Лікувальна відповідь була відзначена в 62 % очей: спостерігалося високовірогідне зменшення латентності ВЗП і невелике, але вірогідне збільшення амплітуди ВЗП [12].
У другій роботі 60 пацієнтам (70 очей із відкритокутовою глаукомою і помірними дефектами поля зору) був призначений цитиколін у вигляді внутрішньом’язових ін’єкцій у дозі 1000 мг/день або перорально в дозі 1600 мг/день; частка хворих не отримувала лікування цитиколіном (контрольна група). Терапію призначали за такою схемою: 60 днів прийому цитиколіну, 120 днів перерви, потім знову 60 днів прийому цитиколіну, потім знову 120 днів перерви. У результаті цього дослідження було з’ясовано, що незалежно від лікарської форми, яку використовували, ін’єкції або пероральної форми, спостерігалося однакове зменшення латентності патерн-ЕРГ і ВЗП, збільшення амплітуди патерн-ЕРГ і ВЗП після кожного з 60-денних періодів лікування [14].
Отже, у цій роботі було продемонстровано, що пероральні й парентеральні форми цитиколіну здатні викликати однакові клінічні ефекти в пацієнтів із глаукомою.
В експериментах на тваринах було встановлено, що біодоступність пероральних і парентеральних форм цитиколіну перевищує 90 %, що знову підтверджує взаємозамінність обох лікарських форм [1, 31].
Підсумовуючи все вищевикладене, а також з огляду на загальновідомі дані про те, що пероральні форми більш прості в застосуванні й пов’язуються з більшим комплаєнсом [18], перевагу в офтальмології слід віддати пероральним формам цитиколіну порівняно з парентеральними.
Очні краплі з цитиколіном вимагають удосконалення
У низці нових досліджень була продемонстрована ефективність місцевої форми цитиколіну, у вигляді очних крапель, для лікування глаукоми. Однак поява цієї лікарської форми відразу ж викликала дискусію серед наукової спільноти.
Р. Grieb і співавт. в оглядовій роботі 2016 р., опублікованій у журналі Frontiers in Aging Neuroscience [30], перерахували низку причин, за яких очні краплі можуть бути не такими хорошими, як це здалося на початку. Було відзначено, що цитиколін є водорозчинною речовиною і тому погано проникає через рогівку. Крім того, для підвищення проникності цитиколіну в розчин крапель додають високомолекулярну гіалуронову кислоту й бензалконію хлорид, останній з яких може бути небезпечним для ока.
У тому ж 2016 році в журналі Frontiers in Aging Neuroscience був опублікований відповідний коментар V. Parisi і співавт. [32], який опротестовував зауваження P. Grieb і співавт. Автори коментаря посилалися на свій експеримент з очима мишей, у якому за допомогою рідинної хроматографії з мас-спектрометрією (LC-MS/MS) була продемонстрована здатність цитиколіну досягати склоподібного тіла.
Проте на сьогодні досліджуються вже безконсервантні ліпосомні форми топічного цитиколіну, що дозволять покращити проникнення препарату до гангліозних клітин без супутніх ефектів [39].
З огляду на подібні дискусії і продовження досліджень щодо покращання ефективності й безпеки крапель ми вважаємо більш правильним використовувати сьогодні пероральні лікарські форми, безпеку яких добре підтверджено в неврологічних дослідженнях [33, 34].
Існує ще кілька додаткових обставин, що також вказують на перевагу вибору пероральних форм цитиколіну.
У той час як поширеність глаукоми збільшується з віком [35], дослідження очних крапель цитиколіну були виконані в основному на пацієнтах 40–60 років, і подібна когорта, говорячи словами однієї групи авторів, не є «досить старою». Сьогодні невідомо, чи буде лікувальний ефект, виявлений в даному віковому діапазоні, проявлятися в осіб віком понад 60 років, які найчастіше хворіють на глаукому [17].
Не слід також забувати, що для пацієнтів із глаукомою багато лікарських засобів доступні у вигляді очних крапель. З огляду на те, що в основному це люди похилого віку, додавання ще й крапель цитиколіну може ускладнити прийом усієї панелі призначених засобів: пацієнту буде складно пам’ятати про всі препарати, правильно розподіляти їх прийом протягом доби тощо. У зв’язку з цим прийом перорального цитиколіну більш виправданий [18].
До того ж застосування пероральних форм цитиколіну дозволяє лікувати не тільки глаукому, але й супутні неврологічні захворювання, часто наявні в осіб похилого віку. Підвищення когнітивних здібностей, що спостерігається при цьому, може підвищувати прихильність до різних аспектів антиглаукоматозного лікування (включно з належним прийомом очних крапель для зниження внутрішньоочного тиску) [30].
Доза й режим терапії
У ранніх дослідженнях як пероральні, так і ін’єкційні форми застосовували у високих дозах — 1000–1600 мг/день [9–14]. Однак в останніх дослідженнях із цих двох лікарських форм перевага віддається пероральному прийому, причому доза знижена до 500 мг/день [15, 18].
Добову дозу, на наш погляд, слід розподілити на два прийоми для більш рівномірного надходження діючої речовини в організм пацієнта, як це зроблено, наприклад, у дослідженні [12].
Лікувальний ефект цитиколіну при терапії глаукоми відносять до категорії treatment-dependent — він зберігається лише тоді, коли препарат приймається регулярно. Можна скористатися схемою лікування, запропонованою для пероральних форм у дослідженнях [15, 18]. Препарат приймається 4 місяці, потім слід зробити 2-місячну перерву, потім препарат знову приймається 4 місяці, далі знову 2-місячна перерва. У згаданих роботах така схема була апробована протягом 2 років з підтвердженням ефективності й безпеки цитиколіну.
Підсумовуємо вищевикладене: для лікування первинної глаукоми може бути рекомендоване призначення таблеток цитиколіну — вранці 250 мг і ввечері 250 мг у загальній добовій дозі 500 мг. Курс лікування слід проводити циклами: 4 місяці лікування, 2 місяці перерви, що йдуть один за одним.
Дані клінічних досліджень
Для зручності викладу матеріалу ми спочатку зупинимося на деяких периметричних показниках, а потім будемо приводити короткий аналіз клінічних досліджень із подальшим повним їх описом.
Загальні відомості про деякі периметричні показники
Як уже було згадано вище, периметрія дозволяє оцінити стан поля зору в пацієнтів з офтальмологічними захворюваннями. Отримані результати виражають у децибелах (дБ) для кожної з точок поля зору (що характеризує чутливість сітківки) [19, 20].
У пацієнтів із глаукомою спостерігається пошкодження поля зору, що пов’язано із загибеллю гангліозних клітин сітківки. Пілотні дані вказують на те, що пошкодження поля зору на –0,2... –0,4 дБ відповідає загибелі 1 % гангліозних клітин; загибель 20–50 % гангліозних клітин відповідає пошкодженню поля зору на –6 дБ [21, 36].
Для ясності зазначимо [37], що характеризуючи пошкодження поля зору, використовують такий показник, як MD (mean deviation, середнє відхилення). Наприклад, при застосуванні приладу Humphrey field analyzer (24-2 testing algorithm) усе поле зору розбивають на 54 окремих точки, для кожної з яких визначають інтенсивність сигналу, що приймається, у децибелах. Потім для кожної точки визначають, наскільки вона відрізняється від аналогічних показників здорової людини порівнянного віку. 54 різниці усереднюють, щоб отримати одне значення в децибелах. Його й називають середнім відхиленням (MD) для даного ока в даного пацієнта. Вище фігурували цифри –0,2... –0,4 дБ і –6 дБ — усе це приклади MD.
Роблячи регулярні виміри MD у даного пацієнта, можна оцінити швидкість пошкодження поля зору. Якщо протягом трьох років MD становив –7, –8, –9 дБ, то швидкість пошкодження поля зору становить –1 дБ/рік.
Дослідження L. Ottobelli та співавт. [15]
Аналіз дослідження
У роботі L. Ottobelli і співавт. призначення цитиколіну в дозі 500 мг/день призводило до уповільнення швидкості пошкодження поля зору вже з перших 4 місяців лікування. Через 2 роки цей показник становив –0,15 ± 0,3 дБ/рік, хоча до лікування він дорівнював –1,1 ± 0,7 дБ/рік. Якщо поділити вихідне значення на значення після лікування, то уповільнення швидкості пошкодження становило приблизно 7,3 раза.
До цієї роботи були включені пацієнти з добре контрольованим внутрішньоочним тиском, утримуваним нижче за 18 мм рт.ст. Незважаючи на це, протягом 2 років дослідження воно знизилося ще приблизно на 1 мм рт.ст.
Тому в обговоренні статті автори зробили висновок, що уповільнення швидкості пошкодження поля зору в 7,3 раза слід пояснювати як впливом цитиколіну, так і невеликим зниженням внутрішньоочного тиску.
Важливо відзначити, що в цій роботі призначення цитиколіну призводило до стабілізації пошкодження поля зору — воно не зростало. До лікування цей показник становив –9,2 дБ, через 2 роки — –9,5 дБ. Автори пишуть, що відмінність у –0,3 дБ є несуттєвою і нею можна знехтувати. У цей ефект також робить внесок невелике зниження внутрішньоочного тиску.
Опис дослідження
У відкрите багатоцентрове проспективне дослідження L. Ottobelli і співавт. був включений 41 пацієнт із діагнозом прогресуючої первинної глаукоми. Наводимо деякі критерії включення в дослідження:
— вік 18 років або старше;
— швидкість пошкодження поля зору не менше за –1 дБ/рік хоча б протягом 3 років до включення в дослідження, незважаючи на хороший контроль внутрішньоочного тиску;
— внутрішньоочний тиск утримували нижче за 18 мм рт.ст. протягом не менше ніж 3 років до включення в дослідження (медикаментозно, лазер, оперативні втручання).
У 30 з 41 включеного пацієнта з глаукомою були уражені обидва ока, у решти 11 пацієнтів — одне око. У пацієнтів із двобічним ураженням в аналіз було включено «гірше» око. Отже, матеріал статті будувався на даних 41 пацієнта (41 око).
Усім пацієнтам був призначений цитиколін перорально в дозі 500 мг/день протягом 4 місяців, потім йшла 2-місячна перерва, потім повтор, і так упродовж 2 років (за два роки в цілому чотири лікувальних цикли по 4 місяці). Крім цього, хворі отримували базову місцеву гіпотензивну терапію глаукоми.
Після того, як автори переконалися, що 41 пацієнт відповідає критеріям включення в дослідження (див. вище), були розраховані фактичні значення показників у вихідних умовах. Вік пацієнтів становив 72,5 ± 11,6 року; стаж первинної глаукоми — 5 років і більше. Величина внутрішньоочного тиску дорівнювала 15,5 ± 2,6 мм рт.ст. Пошкодження поля зору становило –9,2 ± 6,7 дБ; швидкість пошкодження поля зору — –1,1 ± 0,7 дБ рік, розрахована на інтервалі «2 роки до включення в дослідження».
Призначення цитиколіну призводило до уповільнення швидкості пошкодження поля зору вже з першого 4-місячного циклу лікування. До кінця дослідження (2 роки після включення в дослідження) швидкість пошкодження поля зору становила –0,15 ± 0,3 дБ/рік, що було вірогідно нижче порівняно з її початковим значенням (р = 0,01). До цього ж терміну внутрішньоочний тиск також вірогідно знизився приблизно на 1 мм рт.ст. (Р = 0,02). При цьому пошкодження поля зору не збільшувалося (було практично стабільним) і становило –9,5 дБ.
Під час дослідження лікування цитиколіном не призводило до розвитку побічних ефектів. Препарат добре переносився.
За результатами дослідження автори зробили висновок про те, що лікування цитиколіном може вірогідно сповільнювати прогресування первинної глаукоми й необхідні подальші підтвердження в рандомізованих контрольованих дослідженнях.
Дослідження M. Lanza і співавт. [18]
Аналіз дослідження
У роботі M. Lanza і співавт. цитиколін також призначали в дозі 500 мг/день, також протягом 2 років. На відміну від попереднього дослідження тут була виділена контрольна група, яка не отримувала цитиколін.
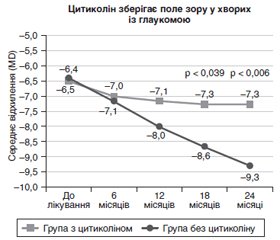
Автори не уточнюють, але, судячи з графіку (рис. 1), стабілізація ушкодження поля зору (MD) у групі з цитиколіном відбувається через 6 місяців. Можна помітити, що MD не наростає — невеликим приростом у –0,3 дБ (з –7,0 дБ у 6 місяців до –7,3 дБ у 24 місяці) можна знехтувати.
Говорячи про стабілізацію через 6 місяців, важливо розуміти, що йдеться фактично про 4 місці лікування цитиколіном (оскільки 6 місяців складалися з 4 місяців лікування цитиколіном і 2 місяців перерви в лікуванні).
Усі пацієнти, включені в роботу М. Lanza і співавт., мали добре контрольований внутрішньоочний тиск, що утримувався нижче 18 мм рт. ст. Протягом 2 років дослідження він не знижувався.
Отже, у цій роботі здатність цитиколіну зберігати поле зору була зафіксована в чистому вигляді, без додаткового внеску зниження внутрішньоочного тиску.
Опис дослідження
У рандомізованому контрольованому проспективному дослідженні M. Lanza і співавт. в аналіз були включені 60 пацієнтів із діагнозом прогресуючої первинної глаукоми. Критерії включення в дослідження в цілому відповідали таким у дослідженні L. Ottobelli і співавт., за винятком того, що внутрішньоочний тиск утримували нижче за 18 мм рт.ст. тільки медикаментозно (не допускалися, наприклад, хірургічні втручання).
Навіть якщо пацієнт мав двосторонню глаукому, у статистичний аналіз було випадковим чином взяте тільки одне око. Отже, матеріал статті був побудований на даних 60 пацієнтів (60 очей).
Усі пацієнти випадковим чином були розподілені на дві групи. У першій (30 пацієнтів) був призначений цитиколін перорально в дозі 500 мг/день за тією ж схемою, як і в попередньому дослідженні, протягом 2 років (за два роки в цілому чотири лікувальних цикли по 4 місяці). У другій групі (30 пацієнтів), що служила контрольною групою, цитиколін не призначали. Хворі обох груп отримували базову місцеву гіпотензивну терапію глаукоми.
Для 60 пацієнтів, які відповідали критеріям включення в дослідження (див. вище) і були взяті в аналіз, були розраховані фактичні значення показників у вихідних умовах. Вік пацієнтів у групі з цитиколіном становив 64,1 ± 5,8 року, у групі без цитиколіну — 62,9 ± 7,2 року. Стаж первинної глаукоми в обох групах становив приблизно 3 роки. Величина внутрішньоочного тиску в групі з цитиколіном дорівнювала 13,83 ± 1,34 мм рт.ст., у групі без цитиколіну — 14,3 ± 1,15 мм рт.ст. Пошкодження поля зору в групі з цитиколіном становило –6,51 ± 2,65 дБ, у групі без цитиколіну — –6,39 ± 2,03 дБ. Швидкість пошкодження полів зору в пацієнтів обох груп була в діапазоні від –1 до –1,5 дБ/рік, розрахована на інтервалі «2 роки до включення в дослідження». Товщина шару нервових волокон сітківки в групі з цитиколіном становила 72,9 ± 7,3 мкм, у групі без цитиколіну — 73,3 ± 4,9 мкм. Товщина комплексу гангліозних клітин в групі з цитиколіном становила 73,8 ± 7,5 мкм, у групі без цитиколіну — 74,6 ± 5,2 мкм. З наведених значень видно, що за вихідними умовами група з цитиколіном і група без цитиколіну (контрольна) вірогідно не розрізнялися між собою.
Через 6 і 12 місяців дослідження пошкодження поля зору в групах із цитиколіном і без цитиколіну вірогідно не відрізнялося (рис. 1). Через 18 місяців дослідження пошкодження поля зору в групі з цитиколіном було менш виражене (–7,25 дБ), ніж у групі без цитиколіну (–8,64 дБ; р = 0,039). При цьому в групі з цитиколіном пошкодження далі не наростало, а в групі без цитиколіну продовжувало наростати, становлячи до 24-го місяця дослідження –9,28 дБ (p < 0,006).
Через 6 місяців дослідження товщина шару нервових волокон сітківки й товщина комплексу гангліозних клітин у групах із цитиколіном і без цитиколіну вірогідно не розрізнялися. Через 12 місяців дослідження товщина шару нервових волокон сітківки й товщина комплексу гангліозних клітин у групі з цитиколіном була вірогідно більша (70,39 і 71,19 мкм відповідно), ніж у групі без цитиколіну (64,91 і 65,60 мкм відповідно; p < 0,01). При цьому в групі з цитиколіном товщина обох структур далі не зменшувалася, а в групі без цитиколіну продовжувала зменшуватися, становлячи до 24-го місяця дослідження ≈ 56 мкм і ≈ 56 мкм відповідно (p < 0,001).
Під час дослідження внутрішньоочний тиск в обох групах не зазнавав вірогідних змін. Лікування цитиколіном не приводило до розвитку побічних ефектів. Препарат добре переносився.
За результатами дослідження автори зробили висновок про те, що лікування цитиколіном здатне уповільнювати прогресування первинної глаукоми. Необхідно проводити надалі більш великі й більш тривалі дослідження, щоб підтвердити результати цієї пілотної роботи.
Висновки
Аналіз 10 основних клінічних досліджень, присвячених застосуванню цитиколіну для лікування первинної глаукоми, свідчить про те, що препарат виявляє чотири важливих клінічних ефекти: зберігає поле зору, посилює функцію сітківки, підтримує морфологію сітківки, покращує провідність по зорових шляхах.
Щодо збереження поля зору необхідно зазначити, що у двох детально розглянутих нами дослідженнях з пероральною формою цитиколіну (Ottobelli L. і співавт. [15], Lanza M. і співавт. [18]) швидкість пошкодження поля зору до лікування становила: у першій роботі — –1,1 дБ/рік, у другій роботі — від –1 до –1,5 дБ/рік. Це досить багато, оскільки зазвичай швидкість пошкодження в осіб, пролікованих із приводу підвищеного внутрішньоочного тиску, становить від –0,3 до –0,6 дБ/рік. І якщо цитиколіну вдавалося стабілізувати поле зору (припинити його погіршення) при високій швидкості ушкодження, то тим більше препарат зробить це при більш низькій швидкості.
Автори другої докладно цитованої нами роботи (Lanza M. і співавт. [18]) відзначили ще одну дуже важливу обставину. У це дослідження були включені пацієнти з різною стадією первинної глаукоми за класифікацією Glaucoma Staging System 2 (Система класифікації глаукоми за стадіями 2). Спостерігалися пацієнти з генералізованим дефектом стадії 1, 2 і 3, зі змішаним дефектом стадії 1, 2 і 3, з локалізованим дефектом стадії 1. У результаті дослідження було з’ясовано, що цитиколін ефективний при всіх стадіях глаукоми.
У всіх дослідженнях, наведених у цьому огляді, препарат не викликав побічних ефектів і добре переносився [9–18].
Подібні ефекти цитиколіну та сприятливий профіль безпеки при лікуванні глаукоми не могли залишитися непоміченими. У Європейському Союзі цитиколін був схвалений як новий харчовий інгредієнт у біодобавках і дієтичних продуктах, призначених для спеціальних медичних цілей (2014/423/EU). Крім того, міністерство охорони здоров’я Італії схвалило цитиколін у вигляді перорального розчину як дієтичний продукт, призначений для спеціальних медичних цілей з терапевтичним показанням для пацієнтів із глаукомою, у яких, незважаючи на фармакологічну стабілізацію, спостерігається прогресивне погіршення поля зору [38].
Відштовхуючись від схеми лікування, запропонованої в роботах L. Ottobelli і співавт. [15], М. Lanza і співавт. [18], для лікування первинної глаукоми можна рекомендувати призначення таблеток цитиколіну вранці 250 мг і ввечері 250 мг, у загальній добовій дозі 500 мг. Курс лікування здійснювати циклами «4 місяці лікування, 2 місяці перерви», що йдуть один за одним.
В Україні з цією метою може бути використаний препарат Аксобрекс, представлений сучасною фармацевтичною компанією «Юніфарм», що спеціалізується на виробництві безрецептурних лікарських засобів і дієтичних добавок для лікування та підтримки балансу здоров’я пацієнтів в усьому світі.
Аксобрекс — це перевірена якість від американської компанії та зручна для пацієнта таблетована форма, що містить по 250 мг цитиколіну в 1 таблетці. Саме таке дозування є додатковою перевагою для кращого розподілення концентрації цитиколіну в організмі. А оскільки лікувальний ефект цитиколіну при терапії глаукоми, як вже згадано вище, відносять до категорії treatment-dependent, саме завдяки препарату Аксобрекс можна забезпечити постійне рівномірне надходження діючої речовини до зорового нерва.
До того ж таблетована форма цитиколіну має низку значних переваг над іншими та довела свою біоеквівалентність ін’єкційній формі, маючи при цьому біодоступність більше 90 % [1, 31].
Саме тому все вищезазначене робить препарат Аксобрекс привабливим для застосування як нейропротектора в лікуванні глаукоми.
Рекомендована схема терапії полягає в тривалому циклічному прийомі препарату Аксобрекс протягом 4 місяців по 250 мг (1 капсула) двічі на добу, за яким слідують 2 місяці перерви.
/45.jpg)