Международный эндокринологический журнал Том 17, №1, 2021
Вернуться к номеру
Чи всі препарати L-тироксину терапевтично еквівалентні?
Авторы: Зінич О.В.
ДУ «Інститут ендокринології та обміну речовин ім. В.П. Комісаренка НАМН України», м. Київ, Україна
Рубрики: Эндокринология
Разделы: Справочник специалиста
Версия для печати
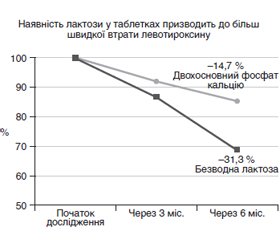
На українському фармацевтичному ринку наявний широкий асортимент препаратів левотироксину як вітчизняного, так і зарубіжного виробництва. Препарати левотироксину різних виробників не завжди є терапевтично еквівалентними, тому що відрізняються за складом допоміжних речовин. Застосування двохосновного фосфату кальцію як допоміжної речовини в L-тироксині не тільки поліпшує біодоступність, а й забезпечує більшу стабільність препарату левотироксину порівняно з використанням лактози.
На украинском фармацевтическом рынке представлен широкий ассортимент препаратов левотироксина как отечественного, так и зарубежного производства. Препараты левотироксина разных производителей не всегда являются терапевтически эквивалентными, так как отличаются по составу вспомогательных веществ. Применение двухосновного фосфата кальция в качестве вспомогательного вещества в L-тироксине не только улучшает биодоступность, но и обеспечивает большую стабильность препарата левотироксина по сравнению с использованием лактозы.
There is a wide range of drugs of levothyroxine of both domestic and foreign manufacture on the Ukrainian pharmaceutical market. The drugs of levothyroxine by different manufactures do not always have the equivalent therapeutic action due to the varying excipients. The use of dibasic calcium phophate as an excipient in L-thyroxine not only improves the bioavailability but also provides greater stability of levothyroxine compared to lactose use.
гіпотиреоз; L-тироксин; терапевтична еквівалентність; стабільність препарату
гипотиреоз; L-тироксин; терапевтическая эквивалентность; стабильность препарата
hypothyroidism; L-thyroxine; therapeutic equivalence; drug stability
/48.jpg)
- Паньків В.І. Синдром гіпотиреозу. Міжнар. ендокринол. журн. 2012. 5. 136-148.
- Mendes D., Alves C., Silverio N. & Batel Marques F. Prevalence of Undiagnosed Hypothyroidism in Europe: A Systematic Review and Meta-Analysis. European Thyroid Journal. 2019. 8. 130-143. doi: 10.1159/000499751.
- Ендокринологія: Підручник для студ. вищих мед. навч. закладів. П.М. Боднар, Ю.І. Комісаренко, Г.П. Михальчишин та ін.; за ред. Ю.І. Комісаренка, Г.П. Михальчишина. Вінниця: Нова Книга, 2020. 536 с.
- Jonklaas J., Bianco A.C., Bauer A.J., Burman K.D., Cappola A.R., Celi F.S. et al. Guidelines for the Treatment of Hypothyroidism: Prepared by the American Thyroid Association Task Force on Thyroid Hormone Replacement. Thyroid. 2014. 24(12). 1670-1751.
- Зинчук С.Ф. Проблемы и перспективы применения фармапрепаратов левотироксина и пути оптимизации их применения. Международный эндокринологический журнал. 2005. 2(2).
- Quality assurance of pharmaceuticals: a compendium of guidelines and related materials. Vol. 2. Good manufacturing practices and inspection. 2nd ed. World Health Organization, 2007. 409 p.
- Van der Merwe J., Steenekamp J., Steyn D., & Hamman J. The Role of Functional Excipients in Solid Oral Dosage Forms to Overcome Poor Drug Dissolution and Bioavailability. Pharmaceutics. 2020. 12(5). 393.
- Платонова Н.М., Бирюкова Е.В. Пациент с гипотиреозом: возможности заместительной терапии. Эффективная фармакотерапия. 2019. Т. 15. № 22. С. 46-52.
- Hebbink G.A., Dickhoff B.H.J. Application of lactose in the pharmaceutical industry. In: Lactose. 2019. 175-229.
- Lactose: Evolutionary Role, Health Effects, and Applications. Ed. by Paques M., Lindner С. Academic Press, 2019. 310 р.
- Muñoz-Torres M., Varsavsky M., Alonso G. Lactose intolerance revealed by severe resistance to treatment with levothyroxine. Thyroid. 2006. 16. 11. 1171-1173.
- Patel H., Stalcup A., Dansereau R., Sakr A. The effect of excipients on the stability of levothyroxine sodium pentahydrate tablets. Int. J. Pharm. 2003. 264. 1–2. 35-43.
- Burman K.D., Emerson Ch.H. The FDA Revises Requirements for Levothyroxine Products. Thyroid. 2008. 18. 5. 487-490.
- Lippa H.-P., Hostalek U. A new formulation of levothyroxine engineered to meet new specification standards. Current medical research and opinion. 2019. 35. 1. 147-150.
- Dong B.J. Bioequivalence of Generic and Brand-name Levothyroxine Products in the Treatment of Hypothyroidism. JAMA. 1997. 277(15). 1205. doi: 10.1001/jama.1997.03540390035032.
- Meredith P. Bioequivalence and other unresolved issues in generic drug substitution. Clinical Therapeutics. 2003. 25(11). 2875-2890. doi: 10.1016/s0149-2918(03)80340-5.
- Fish L.H., Schwatz H.L., Cavanaugh J. et al. Replacement dose, metabolism bioavailabiity of levothyroxine in the treatment of hypothyroidism. N. Engl. J. Med. 1987. 316. 764-770.
- Фадеев В.В., Моргунова Т.Б. Актуальные вопросы заместительной терапии гипотиреоза. Фарматека. 2007. 11.
- McMillan M., Rotenberg K.S., Vora K. et al. Comorbidities, Concomitant Medications, and Diet as Factors Affecting Levothyroxine Therapy: Results of the CONTROL Surveillance Project. Drugs RD. 2016. 16. 53-68. doi: 10.1007/s40268-015-0116-6.
- Benvenga S., Carlé A. Levothyroxine Formulations: Pharmacological and Clinical Implications of Generic Substitution. Advances in Therapy. 2019. 36(Suppl. 2). S59-S71.
- Марушко Ю.В., Іовіца Т.В. Обґрунтування практичних рекомендацій щодо терапевтичних заходів при транзиторній лактазній недостатності у дітей грудного віку. Дитячий лікар. 2016. 4.
- Cellini M., Santaguida M.G., Gatto I. et al. Systematic appraisal of lactose intolerance as cause of increased need for oral thyroxine. J. Clin. Endocrinol. Metab. 2014. May 5.
- Asik M., Gunes F., Binnetoglu E. et al. Decrease in TSH levels after lactose restriction in Hashimoto’s thyroiditis patients with lactose intolerance. Endocrine. 2014. 46. 2. 279-284.
- Sciama Y. France brings back a phased-out drug after patients rebel against its replacement. Science. 2017. Sep. 27.
- Dong B.J., Young V.R., Rapaport B. The nonequivalence of levothyroxine products. Drug Intelligence Clin. Pharmacy. 1986. 20. 77-78.