Вступ
Захворювання щитоподібної залози (ЩЗ) є дуже поширеними серед мешканців усіх країн, а їхня кількість постійно продовжує зростати. У цьому винна не тільки генетична схильність, але й чинники зовнішнього середовища, особливо йодний дефіцит. Загальна хімізація, забруднення навколишнього простору, наслідки аварії на ЧАЕС, паління тютюну значно впливають на стан і захворювання ЩЗ у населення. Сьогодні відомо, що навіть коронавірусна інфекція COVID-19 сприяла збільшенню захворюваності на автоімунні захворювання ЩЗ, в індійських дослідженнях відмічають статистично вірогідне їх зростання на 25–30 %.
За останні 100 років більшість країн світу побороли йодний дефіцит завдяки національним програмам боротьби з ним. На жаль, Україна не стала боротися із цією проблемою, що обумовлює значну поширеність йододефіцитних станів в усіх верствах нашого населення. Нестача йоду не тільки призводить до тиреоїдної патології (вузловий і дифузний зоб, гіпотиреоз і гіпертиреоз), але й впливає і на розумові здібності, тобто на рівень інтелекту, навіть в умовах легкого дефіциту, кількість випадків безпліддя і викиднів, зростання вартості лікування наслідків нестачі йоду, взагалі знижує якість і тривалість життя.
Нещодавні дослідження жінок, які не могли завагітніти, показали, що за наявності ідіопатичного безпліддя [1], яке визначається як відсутність зачаття в пари після одного року регулярного незахищеного сексу за відсутності ідентифікованої причини безпліддя у будь-якого з партнерів, жінки з концентраціями йоду в діапазоні від помірного до тяжкого дефіциту мають значно більший час до вагітності (12 місяців або довше) та зниження загальної репродуктивної здатності [2]. Додавання йоду таким пацієнтам сприяло вагітності в 60 % жінок упродовж найближчих 6–12 місяців.
Адекватне забезпечення йодом протягом років є запорукою надмірного накопичення ЩЗ радіоактивного йоду під час техногенних радіаційних аварій або при застосуванні атомної зброї, при яких викиди завжди, без винятків, містять велику кількість ізотопів йоду. Застосування аварійних блокуючих доз йоду (125–130 мг, що в 1000 разів більше за профілактичні дози) може мати значні ризики для певних категорій осіб, особливо за наявності патології нирок або ЩЗ, серця (аритмій), у алергіків, а також не має проводитися в осіб віком від 40 років. Тому єдиним безпечним шляхом зниження ризиків надмірного накопичення йоду під час радіаційних інцидентів є довгострокове щоденне вживання фізіологічних доз йоду, що ліквідує ефект «голодної» ЩЗ, здатної накопичувати надмірні дози ізотопів. Нормалізація щоденного поглинання йоду призводить до збереження здоров’я тиреоїдної, нервової, статевої та інших систем.
Боротьба з нестачею йоду не є дорогою або складною, але вона повинна проводитись постійно і щодня, тому що йод не може надовго накопичуватись, швидко виводиться, він екскретується майже весь за 3 дні. Саме за цієї причини ВООЗ та інші наукові організації, такі як Американська тиреоїдна асоціація (АТА), не рекомендують використовувати визначення йоду в сечі як індивідуальний маркер йодного дефіциту, який є суто науковим показником для епідеміологічних (групових) досліджень, коли дослідники ставлять за мету визначити вміст йоду в сотнях-тисячах зразків одночасно. Для індивідуальної діагностики йодної нестачі рекомендують використовувати визначення тиреоглобуліну в крові, норма — нижче за 10 нг/мл, що є метою для ефективного поповнення. Маючи підвищений рівень тиреоглобуліну, про що свідчить наявність легкого (10–19 нг/мл), помірного (20–39 нг/мл) або тяжкого (понад 40 нг/мл) йодного дефіциту, необхідно тривалий час (роками) приймати йодовмісні пігулки в рекомендованих ВООЗ дозах (150 мкг/день дорослим, табл. 1) з метою поступового зниження концентрації тиреоглобуліну до нормальних значень, а потім підтримувати її нормальний рівень і періодично проводити контроль (раз на 6–12 місяців).
/32.jpg)
В Україні до регіонів з тяжким дефіцитом йоду і максимальними ризиками розвитку йододефіцитних захворювань традиційно відносять Волинську, Закарпатську, Івано-Франківську, Львівську, Рівненську, Тернопільську й Чернівецьку області. На інших територіях України, включно з Київською, Харківською, Полтавською, Одеською, Дніпровською областю, повсюдно існує легкий або помірний (середній) йодний дефіцит, але це не виключає наявності індивідуальних випадків тяжкого дефіциту. За оцінками ВООЗ, кожний українець вживає близько 90 мкг йоду щоденно протягом року замість 150 мкг, які є рекомендованими. Слід враховувати, що навіть легкий йодний дефіцит призводить до низки тяжких наслідків, у тому числі до вузлового зоба, а таких регіонів значно більше, ніж територій з тяжким дефіцитом.
Профілактика йодного дефіциту однакова для всіх країн і може бути масовою (йодизація продуктів харчування йодованою сіллю, включно з молоком і м’ясом через корми для худоби), груповою (у групах ризику діти, підлітки, вагітні й жінки, які годують груддю, вони всі повинні вживати дозовані препарати йоду) або індивідуальною (за бажанням пацієнта, включно з харчовими домішками, у тому числі рослинного походження). Однак у регіонах, де є йодний дефіцит, до яких належить саме Україна, профілактичне вживання йоду має бути запроваджено за критеріями ВООЗ серед 90 % домогосподарств, що повинне призвести в подальшому до подолання його дефіциту. Тобто кожний розсудливий українець, який хоче зберегти здоров’я, щодня має вживати йодовмісні харчові продукти. Лише 33 % українців щоденно використовують йодовану сіль і близько 10–15 % — йодовмісні пігулки, у тому числі рослинного походження, протягом всього року.
У травні 2021 року Iodine Global Network опубліковані нові зведені дані [5] епідеміологічних досліджень щодо забезпечення йодом населення різних країн світу за йодурією (табл. 2).
Найгіршою забезпеченість виявилася в Україні, Німеччині й Естонії.
Термін «йододефіцитні розлади» (ЙДР) охоплює широкий спектр проблем від субклінічного гіпотиреозу до ендемічного кретинізму, зниження фертильності й порушення розвитку плода, зокрема зниження коефіцієнту інтелекту (IQ), ексцеси, пов’язані з абортами, мертвонародженнями й уродженими аномаліями (табл. 3).
Навіть легкий або помірний (середній) йододефіцит може погіршити когнітивну (пізнавальну) функцію в будь-якому віці, що продовжує впливати на велику популяцію українців і, як показують окремі дослідження, обумовлює зниження бальної оцінки IQ і порушення шкільного й студентського навчання, а також багато інших розладів здоров’я. Йододефіцит залишається основною глобальною загрозою здоров’ю і розвитку, оскільки він є найпоширенішою причиною психічних розладів, яким можна запобігти в усьому світі [6]. Особливо вразливі до нього вагітні жінки й маленькі діти.
Будь-яку патологію ми можемо подолати або контролювати лише за рахунок усунення причини, що призвела до неї. З йодним дефіцитом усе простіше: нестача йоду ліквідується завдяки відновленню надходження йоду до організму. Для цього використовується вже не тільки йодована сіль, але й дозовані препарати йоду в дозах, рекомендованих ВООЗ: 150 мкг на день (можливо використовувати 200 мкг/день), а в США, де побороли йодний дефіцит, дозволено широко використовувати домішки рослинного походження, що містять 350 мкг. Оптимізація споживання йоду населенням є важливою складовою профілактичної медичної допомоги для зниження поширеності захворювань ЩЗ. Йод не можна накопичити, його більша частина виводиться з організму за 3 доби. Це потребує щоденного поповнення. Запровадження йодування солі в щоденному харчуванні є безпечним, може доповнюватись застосуванням дозованих препаратів йоду (пігулок) і похідними рослинного походження, однак, за визначенням АТА, морські водорості не є надійними джерелами йоду. Наводимо безпечні дози сумарного добового вживання протягом року за рекомендаціями ВООЗ, Європи, деяких країн (табл. 4).
/34.jpg)
Йодний дефіцит змінює співвідношення активних лівообертальних форм тироксину й трийодтироніну на біологічно неактивні правообертальні, що є основою розвитку як субклінічного гіпотиреозу, так і пухлинних захворювань ЩЗ (вузлового зоба, фолікулярного раку). Нестача селену й вітаміну-гормону D викликає дисфункцію імунної системи й сприяє активації генетично детермінованої автоімунної патології, наприклад автоімунного тиреоїдиту або тиреотоксикозу, частота яких завжди вища в дефіцитних регіонах. Знаючи ці закономірності, можна впливати на профілактику цих захворювань і на саму патологію, яка вже розвинулась у пацієнтів, для блокування її прогресування.
Питання ось у чому: що робити тим пацієнтам, у яких вже є клінічні ознаки йододефіцитних порушень (табл. 3)? Наприклад, за наявності вузлового зоба або тиреотоксикозу (гіпертиреозу). Чи можемо застосовувати препарати йоду при лікуванні вузлового зоба? Відповідь дає АТА, що у 2016 році опублікувала свою настанову, у якій у рекомендації № 26 визначила [7]: «Пацієнти з доброякісними, твердими або переважно твердими вузлами повинні споживати адекватну кількість йоду. У разі, якщо передбачається або доведено неадекватне надходження цього мікроелементу, рекомендується застосувати добавки, які містять 150 мкг йоду». Ця рекомендація чітко показує, що вузловий (або багатовузловий) зоб пов’язаний з нестачею йоду, навіть у США, де йододефіцит ефективно поборений, а авторитетна американська організація, до складу якої входять багато відомих експертів, радить застосовувати для лікування й контролю захворювання саме препарати йоду. Дійсно, сьогодні накопичені наукові свідчення про значну користь застосування йоду для профілактики й терапії вузлового зоба [8]. Прийом добавок йоду в контексті вузлового зоба давно є досить популярним підходом у таких європейських країнах, як Німеччина, Італія, Швейцарія, та низці інших, тобто там, де спостерігається найгірша ситуація з йодним дефіцитом.
Наявні дані свідчать про те, що дефіцит йоду є фактором ризику раку ЩЗ, зокрема папілярної форми [9], особливо фолікулярного раку ЩЗ і, можливо, анапластичного раку. У недавньому огляді зроблено висновок, що [9]: а) існують узгоджені дані, що свідчать про збільшення частоти раку ЩЗ (переважно фолікулярного) із дефіцитом йоду; б) існує вірогідний механізм (хронічна стимуляція ТТГ, спричинена дефіцитом йоду); в) є узгоджені дані до і після досліджень йодної профілактики, що показують зменшення фолікулярного раку ЩЗ та анапластичного раку; г) існує непрямий зв’язок між змінами споживання йоду і смертністю від раку ЩЗ за десятиліття з 2000 по 2010 рр.; ґ) дослідження при розтині прихованого раку ЩЗ демонструють більш високі показники мікрокарцином при меншому споживанні йоду; д) дослідження «випадок — контроль» свідчать про нижчий ризик розвитку раку ЩЗ при більш високому загальному споживанні йоду [9]. Схоже, що прогноз раку ЩЗ значно покращується після прийому йоду через зсув у бік диференційованих його форм, які діагностуються на більш ранніх стадіях [9]. Загалом виявляється, що корекція йодного дефіциту зменшує ризики й захворюваність на рак ЩЗ. Отже, переваги корекції йододефіциту значно перевищують ризики [9].
Останнім часом з’явилася нова ідея про те, що в різних людей є дозові відмінності потреби в йоді, тобто необхідно запроваджувати індивідуальні підходи до дозування йоду. Такою мірою виміру може виступати саме тиреоглобулін — найбільш поширений білок ЩЗ, рівень якого зростає за наявності йодного дефіциту. Одним особам необхідні менші дози йоду, іншим — великі для досягнення клінічних цілей. Дійсно, у практиці ми бачимо, що призначення стандартної рекомендованої ВООЗ профілактичної дози йоду 150 мкг/день, яка застосовується у хворих на вузловий зоб, спроможна стримати ріст і прогресування тиреоїдних пухлин у значної кількості пацієнтів, у той час як в інших випадках у пацієнтів з високими концентраціями тиреоглобуліну в крові понад 100 нг/мл може спостерігатися подальше зростання розмірів вузлів і концентрацій цього білка. Але в таких випадках можливо розглядати застосування більших лікувальних доз неорганічного йоду — до 350 мкг/добу, дозволених в США, аналогічних американським органічним харчовим рослинним домішкам, що створені на основі морських водоростей. Це майже завжди дозволяє досягти бажаного клінічного ефекту стабілізації вузлів із поступовим (відстроченим) зниженням рівнів тиреоглобуліну. Ми часто успішно використовуємо комбінації препаратів, що містять йод і селен (пігулки 150/75 мкг + 200/30 мкг), рослинні біофлавоноїди у сумарній добовій дозі 150–200–350 мкг йоду, таким чином отримуємо необхідну безпечну дозу, що дозволяється стандартами США для довготривалого застосування.
Отже, збільшення сумарної лікувальної дози препаратів йоду до 350 мкг посилює ефективність лікування йододефіцитних станів, зокрема, надійніше контролює перебіг вузлового (багатовузлового) зоба, особливо тих утворень, що мають великий розмір, і прискорює нормалізацію концентрацій тиреоглобуліну в крові таких пацієнтів. Це є безпечним, потребує звичайного контролю УЗД, лабораторних показників і тиреоглобуліну — не частіше за кожні 4–6 місяців. Збільшення лікувальних доз йоду до 350 мкг/день при вузловому зобі спрямоване на боротьбу з резистентністю до йоду через стимулювання синтезу натрій-йод-симпортера, підвищує ефективність терапії в довгостроковому періоді, а додавання селену 75–100 мкг/день забезпечує безпечність і дієвість такої комбінації.
Наразі на вітчизняному фармацевтичному ринку присутні різні форми випуску й дозування препаратів йоду, серед яких найбільш доцільною можна вважати готову комбінацію йоду й селену, яка може бути рекомендована дорослим (ЙоСен, 1 таблетка якого містить 150 мкг йоду, 75 мкг селену), вагітним (ЙоСен для вагітних і матерів, які годують груддю; в 1 таблетці — 200 мкг йоду, 30 мкг селену), а також дітям (ЙоСен для дітей віком від 3 до 11 років; в 1 таблетці — 90 мкг йоду, 25 мкг селену).
У клінічній практиці часто спостерігається ситуація, коли великий розмір вузлів у ЩЗ або їхніх конгломератів поєднується з надвисокими рівнями тиреоглобуліну, що свідчить про надтяжкий дефіцит йоду і вказує на необхідність застосування більших лікувальних доз, ніж ті, що є профілактичними, рекомендованими ВООЗ, АТА, ЄТА та іншими настановами. У тиреоїдних вузлах великого розміру завжди виникає рефрактерність клітин до дії йоду, тобто нечутливість (резистентність), що нагадує їх автономізацію. У частини пацієнтів відбувається погане засвоювання йоду, є більша потреба в ньому з різних причин. Цьому можна запобігти шляхом призначення більших доз йоду (до 350 мкг/день) на тлі безпечної добової дози за визначенням ВООЗ — до 1000 мкг/добу, яка споживається людиною впродовж усього року від усіх джерел щодня.
Автономія ЩЗ визначається як ТТГ-незалежна функція і проліферація тиреоїдних фолікулів, яка виникає за рахунок генетичних мутації тиреоїдних рецепторів до ТТГ і не пов’язана з йодним дефіцитом. Проте встановлено, що надлишок йоду пригнічує зріст клітин, індукує апоптоз і впливає на морфологію тиреоцитів, а тим самим руйнує аденому (вузол) [10]. Гіпотетично вплив йоду також може пригнічувати проліферацію автономних тиреоцитів, тим самим сповільнюючи автономний ріст, і запобігає в подальшому гіпертиреозу [10]. Нормалізація споживання йоду налагоджує діяльність ЩЗ, що в довгостроковій перспективі зменшує ризики рефрактерності (резистентності) вузлів до дії йоду в тиреоїдній тканині й молочних залозах через стимуляцію синтезу натрій-йод-симпортера.
Що ми отримуємо завдяки додаванню стандартизованого екстракту кореня перстачу білого?
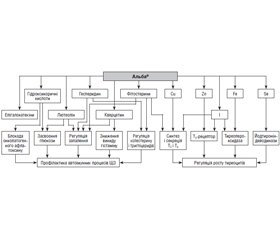
При всіх успіхах, які можемо мати в профілактиці й лікуванні захворювань ЩЗ, ми часто використовуємо нібито всі наявні лікувальні заходи, але не досягаємо бажаної мети в терапії вузлового зоба або порушень функціонального стану ЩЗ. З одного боку, це пов’язано з обмеженням лікарського арсеналу дієвих засобів. Однак народна медицина традиційно використовувала рослинні засоби в ті часи, коли не було очищених препаратів, що мали багатогранні тиреоїдні ефекти. До таких засобів належать перш за все корені перстачу білого (Potentilla аlba), які містять не лише мікроелементи, але й велику кількість біологічно активних компонентів — біофлавоноїдів, поліфенолів (до 33 % від власного складу), альбінін та інші речовини, встановлено присутність сапонінів, флавоноїдів (рутин, кверцетин, лютеолін, апігенін, кофеїнова, хлорогенова й ферулова кислоти), танінів (до 20,5 % від власного складу), більшість з яких мають значні антиоксидантні властивості, що сприяють зниженню рівнів пероксид-радикалів, гідроксильних радикалів і деградації фосфоліпідів, а також демонструють антимутагені, протизапальні та імуномодулюючі властивості [11–14] (рис. 1).
/35.jpg)
Наприклад, катехін перстачу білого дозозалежно гальмує зростання й патологічну трансформацію клітин карциноми ЩЗ (уже в дозах 10–60 ммоль/л) за рахунок регулювання сигнальних шляхів AKT і ERK1/2, а також знижує активність металопротеїнази-9 [16]. При цьому катехін ініціює апоптоз абнормально трансформованих тиреоїдних клітин за рахунок регулювання шляхів виживання EGFR/ERK, цикліну B1/CDK1 і підвищення рівнів каспази-3 [17].
Фітостерини перстачу є природними гіпохолестеринемічними агентами, вони сприяють значному зменшенню холестерину низької щільності й тригліцеридів у плазмі крові.
Отже, досліджені медичні ефекти екстракту перстачу білого мають загальнозміцнюючу, адаптогенну, кровоспинну, протизапальну, бактерицидну, протипухлинну, мембраностабілізуючу, тиреопротективну дії. Також рослина активно накопичує у фізіологічних дозах йод, цинк, селен, магній, калій, кальцій, фосфор, залізо, марганець, які є молекулярними синергістами йоду (табл. 5) [18, 22].
Одна капсула препарату Альба® може містити 76 мкг йоду, а дві капсули здатні покривати середню добову потребу дорослого організму в йоді (150 мкг/добу).
Що ми отримуємо завдяки додаванню стандартизованого екстракту кореня перстачу білого до стандартної схеми лікування тиреоїдної патології? Біологічно активні компоненти, які містяться в перстачі (сапоніни, флавоноїди), пригнічують проліферативні процеси в тиреоїдній тканині, що пояснює ефективність їх застосування за наявності гіпертрофічних і гіперпластичних процесів у ЩЗ та інших тканинах. Додавання стандартизованого екстракту кореня перстачу білого до основної довготривалої терапії призводить до посилення ефективності лікування й швидшого досягнення бажаних результатів, що доведено в Національному дослідженні препарату Альба® (біля півтори тисячі пацієнтів), декількох клінічних дослідженнях у відомих наукових центрах України і експериментальних роботах [18–21]. В усіх дослідженнях отримані майже однакові результати: зменшення об’єму ЩЗ і розмірів вузлів, покращення функціонального стану ЩЗ при гіпотиреозі й гіпертиреозі, скорочення термінів лікування до досягнення мети. Ефективність застосування стандартизованого екстракту кореня перстачу білого при порушеннях стану ЩЗ, за даними експериментальних робіт, переважно пояснюється стабілізуючим впливом компонентів на мембрани тиреоцитів.
/36.jpg)
Отже, у лікарів є можливість застосування рослинних препаратів, що містять не лише йод та інші мікроелементи, але й біологічно активні складові, завдяки яким забезпечується лікувальний ефект. Для прискорення процесів апоптозу в клітинах аденоми нам потрібні додаткові лікувальні засоби. До таких засобів можливо віднести препарат стандартизованого екстракту кореня перстачу білого Альба®. Його застосування в дозі 600 мг/день протягом тривалого часу (понад 6–12 місяців) є безпечним і ефективним у лікуванні тиреоїдної патології. Його можна використовувати одночасно з іншими лікувальними заходами (прийомом препаратів йоду, гормонів, тиреостатиків), досягаючи максимального терапевтичного тиреоїдного ефекту. Така комбінація є найбільш дієвою.
Дуже ефективною комбінацією є застосування стандартизованого екстракту кореня перстачу білого з препаратами йоду, що містять 150–200 мкг/день, і селену — 30–75 мкг/день. Як вже вище пояснювалося, є пацієнти, які мають потреби в більших дозах йоду, крім того, діє принцип «доза — ефект» (збільшення дози препарату призводить до зростання ефективності). Якщо діяти в рамках добової сумарної безпечної дози 500–1000 мкг, ефективність лікування йододефіцитних розладів покращується й прискорюється. Щоденне лікувальне використання препаратів йоду зі стандартизованим екстрактом кореня перстачу білого на тлі профілактичного застосування рекомендованої кількості йодованої солі є ефективним лікувальним і безпечним заходом, не дозволяє перевищити сумарну дозу 500–1000 мкг/добу впродовж року.
АТА у своїх рекомендаціях чітко каже, що водорості не є надійними джерелами йоду, тому їх не рекомендують застосовувати в лікуванні та груповій профілактиці, але ми можемо їх використовувати як варіант в індивідуальній профілактиці. Японці та корейці за рахунок широкого застосування водоростей і морепродуктів мають надлишок йоду в загальній популяції населення, бо немає можливості контролювати кількість йоду в харчових продуктах, вони не є дозованими. Це є значним недоліком рослин.
В Україні є рослинний препарат кореню перстачу білого Альба®, який містить екстракт із стандартизованою кількістю біологічно активних речовин (кверцетин, низка біофлавоноїдів/поліфенолів, йод та інші), тропних до клітин ЩЗ. Завдяки такому складу цей лікарський засіб дозволяє отримати бажані клінічні ефекти в лікуванні спектра тиреоїдних захворювань, таких як вузловий (багатовузловий) і дифузний зоб, гіпертиреоз і гіпотиреоз, а також може бути застосований у їх профілактиці.
В Україні протягом останнього десятиліття було проведено декілька клінічних та експериментальних досліджень з вивчення тиреоїдних лікувальних ефектів стандартизованого екстракту кореня перстачу білого в дозі 300 мг у капсулі — 600 мг на день. Щодо препарату Альба® в Україні накопичено значну доказову базу. Препарат був апробований у низці незалежних клінічних досліджень у ДУ «Інститут ендокринології та обміну речовин ім. В.П. Комісаренка НАМН України» [18], Українському науково-практичному центрі ендокринної хірургії, трансплантації ендокринних органів та тканин МОЗ України [19, 20], ДУ «Національний науковий центр радіаційної медицини НАМН України» [21]. Отримані результати показали, що клінічне застосування рослинного препарату Альба® в тривалому режимі (3–6 місяців) є безпечним, дозволяє в більшої частини хворих з тиреоїдною патологією (дифузним нетоксичним зобом, гіпертиреозом, гіпотиреозом, автоімунним тиреоїдитом) нормалізувати функціональний стан ЩЗ. Додатково зазначено скорочення термінів досягнення цільових рівнів ТТГ приблизно на 20 %, а також загалом тривалості лікування гіпертиреозів у всіх групах дослідження.
Ці дані незалежних дослідників було підтверджено також у Національному багатоцентровому клінічному дослідженні на незвично великій для України вибірці хворих — 1107 осіб [14]. Застосування фітопрепарату Альба® сприяло покращенню функціонального стану ЩЗ, що виявилося у вірогідному зниженні рівня ТТГ до середньопопуляційного в пацієнтів з хронічним автоімунним тиреоїдитом, дифузним нетоксичним зобом і вузловим зобом на тлі зменшення загального обсягу ЩЗ.
Отже, найкращий бажаний клінічний ефект в лікуванні вузлового (багатовузлового) зоба та інших тиреоїдних захворювань може бути отриманий при застосуванні комбінації йоду (150–200 мкг/щоденно), селену (30–100 мкг/щоденно) в поєднанні зі стандартизованим препаратом кореня перстачу білого (600 мг/добу, який містить екстракт із визначеною кількістю біологічно активних речовин).
Конфлікт інтересів. Не заявлений.
Отримано/Received 15.08.2022
Рецензовано/Revised 27.08.2022
Прийнято до друку/Accepted 01.09.2022
/33.jpg)

/32.jpg)
/33_2.jpg)
/34.jpg)
/35.jpg)
/36.jpg)